Resumos
A dosagem de cortisol livre na urina (CLU) é um método útil na triagem de pacientes suspeitos de síndrome de Cushing. Os imunoensaios atuais apresentam limitações que dificultam sua aplicação e a comparação de resultados por diferentes ensaios. No presente método para dosagem de cortisol e cortisona livres urinários, baseado em cromatografia líquida com detecção por espectrômetro de massa em tandem (LC-MS/MS), uma alíquota de urina 24h (200µL) é misturada com solução contendo quantidade conhecida de cortisol deuterado e extraída on-line em fase sólida (C18). O eluato é transferido para uma segunda coluna C18 (Phenomenex Luna, 3µ, de 50 x 2mm), e o eluato obtido em modo isocrático é aplicado diretamente no MS/MS modelo Quattro Micro, operando no modo positivo de ionização química a pressão atmosférica (APCI). Todo o processo é automatizado e a quantificação é feita por diluição isotópica com base nas razões das áreas dos picos dos analitos e do padrão interno deuterado. O estudo de especificidade mostrou que nenhum esteróide testado apresenta reatividade cruzada superior a 1% com cortisol ou cortisona. A sensibilidade funcional é <1µg/L para os dois esteróides, e o CV interensaio <8%. Os estudos de recuperação e de linearidade foram satisfatórios, e a comparação entre os resultados obtidos para cortisol em 98 amostras de rotina, pelo ensaio em estudo e por um RIE, mostraram correlação de r= 0,838, sendo os valores obtidos por LC-MS/MS significativamente mais baixos (medianas de 22,0 e 49,4µg/24h, respectivamente) (P<0,0001). Os valores de referência para cortisol foram definidos entre 11 e 43µg/24h, compatíveis com métodos semelhantes recentemente descritos. A dosagem concomitante de cortisona livre urinária permite o estudo da atividade da enzima 11beta-HSD2 e a pesquisa da síndrome do excesso aparente de mineralocorticóides. O método descrito representa a primeira descrição, em nosso meio, de uma nova geração de métodos para a medida de esteróides hormonais, baseados em processos preparativos automatizados e leitura por espectrometria de massa em tandem.
Cortisol livre urinário; Cortisona livre urinária; Cromatografia líquida; Espectrometria de massa
Free urinary cortisol (UFF) measurement is one of the most useful screening tests for Cushing's syndrome. Immunoassays employed today by most clinical laboratories present limitations, specially concerning specificity. These limitations restrain a widespread application of the method, as well as the comparison of results obtained by the use of different methods. We present the development and characterization of a UFF and cortisone method based on liquid chromatography and tandem mass spectrometry (LC-MS/MS). A 200µL aliquot from a 24h urine sample is mixed with a solution containing a known quantity of deuterated cortisol and on-line extracted in solid phase (C18). The eluate is transferred to a second C18 column (Phenomenex Luna, 3µ, 50x2 mm) and the isocratic mode elution profile is directly applied to a tandem mass spectrometer model Quattro Micro operating in positive mode atmospheric pressure chemical ionization (APCI). All process is automated and the quantification is performed by isotopic dilution, based on the analyte and the deuterated internal standard peak area ratios. The specificity study showed that all the steroids tested presented cross reactivity of <1% for cortisol and cortisone. Functional sensitivity is <1µg/L for both steroids, and the interassay CV <8%. Recovery and linearity studies were satisfactory and comparison of results obtained using a RIA for UFF and the present method in 98 routine samples showed a correlation of r= 0.838, with the results obtained with LC-MS/MS significantly lower (medians of 22.0 vs. 49.4µg/24h for RIA) (P<0.0001). Reference values for cortisol were defined as values between 11 and 43µg/24h, compatible to those recently described for similar methods. The concomitant measurement of UF cortisone allows the study of the activity of the enzyme 11beta-HSD2 and the diagnosis of the apparent mineralocorticoid excess syndrome. The method represents the first steroid assay of a new generation, based on automated preparative methods and tandem mass spectrometry, described in our country.
Free urinary cortisol; Free urinary cortisone; Liquid chromatography; Mass spectrometry
ARTIGO ORIGINAL
Dosagem de cortisol e cortisona livres urinários empregando cromatografia líquida associada a espectrometria de massa em tandem (LC-MS/MS)
Measurement of free urinary cortisol and cortisone using liquid chromatography associated with tandem mass spectrometry method
José Gilberto H. Vieira; Odete H. Nakamura; Valdemir M. Carvalho
Setor de Cromatografia e Laboratório de Esteróides, Laboratório Fleury, São Paulo, SP
Endereço para correspondência Endereço para correspondência José Gilberto H. Vieira Laboratório Fleury Avenida General Waldomiro de Lima 508 04344-070 São Paulo, SP
RESUMO
A dosagem de cortisol livre na urina (CLU) é um método útil na triagem de pacientes suspeitos de síndrome de Cushing. Os imunoensaios atuais apresentam limitações que dificultam sua aplicação e a comparação de resultados por diferentes ensaios. No presente método para dosagem de cortisol e cortisona livres urinários, baseado em cromatografia líquida com detecção por espectrômetro de massa em tandem (LC-MS/MS), uma alíquota de urina 24h (200µL) é misturada com solução contendo quantidade conhecida de cortisol deuterado e extraída on-line em fase sólida (C18). O eluato é transferido para uma segunda coluna C18 (Phenomenex Luna, 3µ, de 50 x 2mm), e o eluato obtido em modo isocrático é aplicado diretamente no MS/MS modelo Quattro Micro, operando no modo positivo de ionização química a pressão atmosférica (APCI). Todo o processo é automatizado e a quantificação é feita por diluição isotópica com base nas razões das áreas dos picos dos analitos e do padrão interno deuterado. O estudo de especificidade mostrou que nenhum esteróide testado apresenta reatividade cruzada superior a 1% com cortisol ou cortisona. A sensibilidade funcional é <1µg/L para os dois esteróides, e o CV interensaio <8%. Os estudos de recuperação e de linearidade foram satisfatórios, e a comparação entre os resultados obtidos para cortisol em 98 amostras de rotina, pelo ensaio em estudo e por um RIE, mostraram correlação de r= 0,838, sendo os valores obtidos por LC-MS/MS significativamente mais baixos (medianas de 22,0 e 49,4µg/24h, respectivamente) (P<0,0001). Os valores de referência para cortisol foram definidos entre 11 e 43µg/24h, compatíveis com métodos semelhantes recentemente descritos. A dosagem concomitante de cortisona livre urinária permite o estudo da atividade da enzima 11b-HSD2 e a pesquisa da síndrome do excesso aparente de mineralocorticóides. O método descrito representa a primeira descrição, em nosso meio, de uma nova geração de métodos para a medida de esteróides hormonais, baseados em processos preparativos automatizados e leitura por espectrometria de massa em tandem.
Descritores: Cortisol livre urinário; Cortisona livre urinária; Cromatografia líquida; Espectrometria de massa
ABSTRACT
Free urinary cortisol (UFF) measurement is one of the most useful screening tests for Cushing's syndrome. Immunoassays employed today by most clinical laboratories present limitations, specially concerning specificity. These limitations restrain a widespread application of the method, as well as the comparison of results obtained by the use of different methods. We present the development and characterization of a UFF and cortisone method based on liquid chromatography and tandem mass spectrometry (LC-MS/MS). A 200µL aliquot from a 24h urine sample is mixed with a solution containing a known quantity of deuterated cortisol and on-line extracted in solid phase (C18). The eluate is transferred to a second C18 column (Phenomenex Luna, 3µ, 50x2 mm) and the isocratic mode elution profile is directly applied to a tandem mass spectrometer model Quattro Micro operating in positive mode atmospheric pressure chemical ionization (APCI). All process is automated and the quantification is performed by isotopic dilution, based on the analyte and the deuterated internal standard peak area ratios. The specificity study showed that all the steroids tested presented cross reactivity of <1% for cortisol and cortisone. Functional sensitivity is <1µg/L for both steroids, and the interassay CV <8%. Recovery and linearity studies were satisfactory and comparison of results obtained using a RIA for UFF and the present method in 98 routine samples showed a correlation of r= 0.838, with the results obtained with LC-MS/MS significantly lower (medians of 22.0 vs. 49.4µg/24h for RIA) (P<0.0001). Reference values for cortisol were defined as values between 11 and 43µg/24h, compatible to those recently described for similar methods. The concomitant measurement of UF cortisone allows the study of the activity of the enzyme 11b-HSD2 and the diagnosis of the apparent mineralocorticoid excess syndrome. The method represents the first steroid assay of a new generation, based on automated preparative methods and tandem mass spectrometry, described in our country.
Keywords: Free urinary cortisol; Free urinary cortisone; Liquid chromatography; Mass spectrometry
A TRIAGEM DE PACIENTES SUSPEITOS de síndrome de Cushing, bem como a tentativa de sua comprovação laboratorial, é um dos maiores desafios da clínica endocrinológica (1,2). Por se tratar de condição relativamente rara, mas com sinais e sintomas comuns a outras condições clínicas muito mais freqüentes, fica clara a necessidade de um método de triagem sensível e específico. Dentre os métodos preconizados, a dosagem de cortisol livre urinário é dos mais utilizados e aceitos, sendo considerado de primeira linha por muitos autores, em conjunto com as medidas de cortisol salivar coletado à meia-noite e o teste de supressão com dose baixa de dexametasona (3,7). A dosagem de cortisol livre na urina de 24 horas apresenta como vantagens teóricas o fato de ser imune a flutuações da proteína carregadora de cortisol (CBG), e de representar a integração da secreção de 24 horas, eliminando a variável do ritmo circadiano. Por outro lado, a dosagem do cortisol livre urinário apresenta uma limitação específica que concerne à coleta da urina, procedimento que exige participação ativa do paciente. No entanto, sua maior limitação sempre foi técnica, de origem metodológica. Desde a descrição inicial do método, baseado em um ensaio de ligação protéica competitiva precedido de detalhado processo preparativo cromatográfico, a definição de valores de referência e a necessidade de processos cromatográficos tem sido muito debatida, em especial por Murphy e cols. (8-11).
Há alguns anos publicamos trabalho relatando o desenvolvimento de um radioimunoensaio para cortisol livre urinário, baseado num anticorpo de boa qualidade, e com um processo preparativo relativamente simples (12). O método foi utilizado em nossa rotina durante mais de cinco anos, mostrando alta reprodutibilidade e robustez. No entanto, encontramos casos isolados onde claramente observamos interferência de glicocorticóides exógenos, observação que se coaduna com o fato de que os valores descritos como normais para o método (até 86µg/24h) serem superiores aos descritos para os métodos de referência (até 50µg/24h), situação freqüentemente relatada na literatura (13). Estas observações são perfeitamente condizentes com a presença de inúmeros metabólitos do cortisol na urina, que se apresentam em quantidades muito superiores ao mesmo, desde que a fração livre constitui menos de 0,1% do total de metabólitos de cortisol presentes (14). O método preparativo empregado em nosso ensaio assumia um compromisso entre a praticidade e a especificidade, condição comum a este tipo de método (15). Em função disto, e levando em consideração as limitações intrínsecas dos imunoensaios, valores reais de cortisol livre urinário só eram possíveis até pouco tempo com o emprego de processos cromatográficos de alta complexidade, associados ou não à leitura por absorção de ultravioleta (16,17).
O controle da ação do cortisol sobre os receptores mineralocorticóides é feito pela sua oxidação local à cortisona, catalisada pela ação da enzima 11b-hidroxiesteróide dehidrogenase tipo 2 (11b-HSD2). Esta metabolização do cortisol, levada a cabo por uma enzima localizada na proximidade dos receptores mineralocorticóides, e que é tecido-específica, previne a ação do esteróide nesse receptor (18). Este fenômeno se baseia no fato de que os receptores mineralocorticóides têm afinidade semelhante por cortisol e aldosterona, mas cortisona não se liga ao receptor, e aldosterona não é substrato para a enzima. Desta maneira, previne-se a ação do cortisol no receptor mineralocorticóide, desde que sua concentração sérica é muito superior à do mineralocorticóide de referência, a aldosterona. A ausência, ou deficiência, da 11b-HSD2 leva a uma ação mineralocorticóide excessiva, com retenção de sódio e água e uma condição de hipertensão com hipocalemia e supressão da atividade da renina plasmática conhecida como síndrome do excesso aparente de mineralocorticóides (Apparent Mineralocorticoid Excess AME) (19). Sendo os rins a principal fonte de cortisona livre urinária, a avaliação da atividade da enzima 11b-HSD2 pode ser feita com o estudo da relação entre cortisol e cortisona livres na urina, o que torna a dosagem concomitante dos dois esteróides de interesse prático (20).
A introdução, na prática diagnóstica, de metodologias para a dosagem de hormônios esteróides baseadas na detecção final por espectrometria de massa vem ocorrendo lentamente ao longo das últimas décadas, em especial graças aos trabalhos de Shackleton e seu grupo (21-24). Em teoria, o espectrômetro de massa, especialmente no arranjo em tandem (MS/MS), tem um potencial de identificação de substâncias inigualável, e sua aplicação mais ampla na prática diagnóstica está na dependência de evoluções técnicas pontuais, disseminação de conhecimento e custos. Com a evolução dos equipamentos e das técnicas de introdução de amostras para leitura, a concretização de todo o potencial dessa metodologia está se tornando realidade. No caso da determinação do cortisol urinário, devido à sua relativa alta concentração, os recursos técnicos já estão disponíveis, e laboratórios de referência nos EUA e Europa têm recentemente publicado metodologias baseadas em cromatografia líquida e espectrometria de massa com este objetivo (25-27). Neste trabalho, apresentamos nossa experiência no desenvolvimento de um método de alta especificidade para a medida de cortisol e cortisona livres na urina, baseado em cromatografia líquida e espectrometria de massa em tandem (LC-MS/MS).
MATERIAL E MÉTODOS
As amostras de urina para a comparação entre métodos de dosagem de cortisol livre urinário provieram de nossa rotina diagnóstica, sendo utilizadas 98 amostras seqüenciais. Os pacientes foram instruídos a desprezar a primeira urina da manhã e coletar todo o volume até a manhã do dia seguinte. Foram fornecidos frascos contendo 10g/L de ácido bórico e solicitado que a amostra fosse mantida em lugar fresco durante o período de coleta. O método comparativo utilizado foi o baseado em extração e cromatografia, seguido por radioimunoensaio, conforme descrito anteriormente (12), e baseado no método preparativo simplificado descrito por Morineau (28). A metodologia estatística empregada para a comparação entre os resultados, e extrapolação de pontos de decisão, baseou-se no programa EP Evaluator, fornecido por David Rhoads Associates Inc., Kennett Square, PA, USA. Adicionalmente, 165 amostras de urina de nossa rotina foram utilizadas para definição da relação entre cortisol e cortisona livres. Para os cálculos estatísticos gerais e execução dos gráficos empregamos o programa Prism 4, fornecido por GraphPad Inc., San Diego, Ca, USA (www.graphpad.com). O cortisol deuterado (cortisol-1a, 2a-d2, 98,5% D código D-2878) utilizado como padrão interno foi adquirido de C/D/N Isotopes (Quebec, Canadá). Os solventes empregados foram todos de qualidade p.a. ou superior, e os sais empregados para a manufatura dos tampões adquiridos de Merck Indústrias Químicas, Rio de Janeiro.
Toda a manipulação de amostras e de eluentes foi feita com a utilização de sistema de manipulação de líquidos Gilson 215, equipado com software Gilson 735 (Gilson, Inc., Middleton, WI, USA). Os seguintes esteróides sintéticos foram utilizados para a avaliação de especificidade do método: corticosterona, desoxicorticosterona, 11-desoxicortisol, 21-desoxicortisol, progesterona, aldosterona, prednisona, prednisolona, 6a-metilprednisolona, betametasona, fludrocortisol, triancinolona, dexametasona, 5a-dihidrocortisol, 5b-dihidrocortisol, 6b-dihidrocortisol, 5a-tetrahidrocortisol, 5a-tetrahidro-11-desoxicortisol, 5b-tetrahidro-11-desoxicortisol, 20a-dihidrocortisol, 20b-dihidrocortisol, 5b-tetrahidrocortisol, cortisol-21-glucoronato e cortisol-21-sulfato, todos eles, bem como os padrões de cortisol e cortisona, obtidos de Steraloids Inc., Newport, RI, USA. Para o estudo de especificidade, os esteróides foram analisados numa concentração de 5.000µg/L, preparada no mesmo tampão utilizado para a diluição do cortisol deuterado (vide abaixo).
Método Analítico
As amostras de urina foram homogeneizadas, e a uma alíquota de 200µL adicionamos 50µL de solução de cortisol-d2 (10mg/L) em tampão fosfato 0,002M, acrescido de 60mmol/L de NaCl, 34,0mmol/L de uréia e 0,9mmol/L de creatinina. Após homogenização, o sistema aspira 200µL da mistura e os injeta em uma linha cromatográfica eluída com uma fase móvel constituída por 14% de acetonitrila em água a um fluxo de 0,7mL/min. A amostra é conduzida a uma válvula de seis portas e duas posições, onde encontra-se instalado um cartucho C18 de 3 x 4mm (Phenomenex Security Guard, Labtron, São Paulo), sendo os esteróides de interesse retidos e parcialmente purificados. Em seguida, a válvula altera o fluxo de solventes fazendo com que o cartucho seja eluído em sentido reverso por uma fase móvel de 40% de formiato de amônio 5mM, pH 3 e 60% de metanol. Nessa condição cromatográfica, os esteróides são eluídos do cartucho e a fração contendo cortisol e cortisona é encaminhada a uma segunda coluna cromatográfica (Phenomenex Luna C18, 3µ, de 50 x 2mm). As duas fases móveis são bombeadas por um sistema de cromatografia líquida de alta eficiência composto de duas bombas LC-10ATvp controladas pelo módulo SCL-10Avp (Shimadzu Corp., Kioto, Japão), com eluição isocrática. O perfil cromatográfico obtido é diretamente aplicado no espectrômetro de massas em tandem (MS/MS) modelo Quattro Micro (Waters/Micromass, Manchester, UK), equipado com sonda de ionização química a pressão atmosférica (APCI), operando em modo positivo. A análise quantitativa foi feita no modo de monitoração de múltiplas reações, onde foram monitoradas as seguintes transições: m/z 363>121 (cortisol), m/z 365>122 (cortisol-d2,) e m/z 361>163 (cortisona). O gás de colisão empregado foi o argônio a uma pressão de 4 x 10-4 kPa. A corrente da agulha de APCI foi 5,0µA e a energia de colisão foi de 24eV. Para as transições 363>121 e 165>122, utilizou-se uma voltagem do cone de 32V, e para a transição 361>163, uma voltagem de 42 V. A quantificação é feita automaticamente com a utilização do módulo QuanLynx do software MassLynx (Micromass), através de diluição isotópica. Nesse método, utilizam-se as razões entre as áreas dos picos referentes aos analitos (cortisol ou cortisona) e as áreas do cortisol deuterado (padrão interno). A razão é interpolada em curva-padrão obtida a partir de quatro níveis de calibradores (cortisol a 10, 50, 100 e 200µg/L, cortisona a 20, 100, 200 e 400µg/L), que é refeita em cada lote de determinações. O tempo de ensaio, desde a colocação da alíquota de urina no amostrador até o resultado final, é inferior a 5 minutos por amostra. Na figura 1 estão representados os perfis obtidos para o cortisol deuterado, cortisol e cortisona, após o processo cromatográfico e a leitura no MS/MS.
RESULTADOS
Características do Método
Para a validação do método, estudamos a precisão através do coeficiente de variação (CV) interensaio obtido pela dosagem de dois pools de urina, um com valor médio de 18,0mg/L e outro de 102,2mg/L. Foram realizadas 20 dosagens em duplicata ao longo de 4 semanas, sendo os CV obtidos 7,9% e 7,4%, respectivamente. O CV intraensaio das duplicatas das dosagens foi de 4,4%. O estudo de linearidade foi feito pela diluição seriada de alíquota de urina contendo 800mg/L até alcançarmos 3mg/L, obtendo-se valores entre 93,9 e 101,3% do esperado. A sensibilidade funcional foi calculada tendo como base 20 dosagens em duplicata, efetuadas ao longo de quatro semanas, de quatro alíquotas com valores de 8,4, 4,2, 1,7 e 0,8mg/L. Com base no CV interensaio de cada uma das amostras, e definindo como 20% o valor máximo aceitável, este valor foi alcançado com a alíquota contendo 0,8mg/L (14,3% de variação interensaio, com limite de confiança entre 10,9 e 20,3%). Pode-se, pois, considerar que a sensibilidade funcional do método descrito está abaixo de 1mg/L.
A recuperação foi avaliada pela adição de quantidade fixa de cortisol (100mg/L) e de cortisona (150mg/L) a 15 amostras de urina com valores basais entre 2,8 e 22,3mg/L, obtendo-se recuperação média (± desvio padrão) de 93,3 ± 2,9% para cortisol e 118,7 ± 9,1% para cortisona. Quanto à especificidade, dos esteróides testados na concentração de 5.000mg/L, reatividade cruzada detectável (acima de 0,2%) foi observada com 6b-dihidrocortisol (0,97%), 20b-dihidrocortisol (0,88%), 21-desoxicortisol (0,27%), prednisolona (0,24%) e cortisol-21-glicuronato (0,24%).
Resultados da Comparação Com o Método Anterior
O resultado das dosagens de cortisol, realizadas em paralelo em 98 amostras de nossa rotina diagnóstica, mostrou correlação (Spearman) de 0,838 (P<0,0001) com os valores obtidos com o RIE e com o método de LC-MS/MS, sendo estes significativamente mais baixos que os obtidos com o RIE, com medianas de 22,0 e 49,4mg/24h, respectivamente. O estudo estatístico (teste de Wilcoxon para determinações pareadas) mostrou alta significância (P<0,0001). Os dados encontram-se representados na figura 2. Com base nestes resultados e utilizando-se o programa EP Evaluator, extrapolamos os valores correspondentes à faixa de normalidade do RIE (27 a 86µg/24h) (12), obtendo os valores de 11 a 43µg/24h.
Resultados de Cortisona Livre Urinária
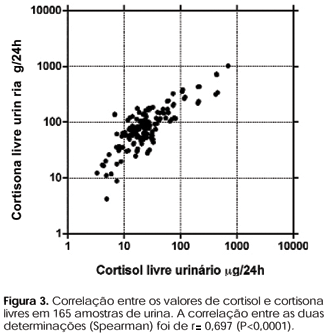
O estudo dos resultados obtidos nas 165 amostras de rotina mostrou uma mediana de 77,5µg/L de cortisona, com intervalo de distribuição entre 4,2 e 1020,0µg/L, e mediana de 22,0µg/L de cortisol, com intervalo de distribuição entre 3,3 e 698,0µg/L. A correlação (Spearman) entre as determinações de cortisol e cortisona mostrou um r= 0,697 (P<0,0001). A relação média entre as dosagens de cortisona/cortisol foi de 2,48. A representação gráfica dos resultados está na figura 3.
DISCUSSÃO
A introdução das técnicas de radioimunoensaio para dosagens hormonais, incluindo esteróides, trouxe uma verdadeira revolução em pesquisa e diagnóstico de patologias endócrinas (29-31). Os métodos em geral incluíam um processo de extração em solvente orgânico seguido, ou não, de cromatografia. Com a evolução dos imunoensaios, novos marcadores não radioativos passaram a ser empregados e, principalmente, novos desenhos de ensaios foram desenvolvidos e aplicados. Dentre estes, destacam-se os ensaios imunométricos, não competitivos e com dupla identificação, que elevaram significantemente o nível de qualidade dos ensaios hormonais (32). No caso da dosagem dos hormônios esteróides, devido ao seu baixo peso molecular, o princípio dos ensaios imunométricos não pode ser aplicado, permanecendo até hoje o desenho de ensaio competitivo, sendo as únicas variáveis aperfeiçoadas o tipo de separação e o traçador (33). O mesmo ocorre com as tironinas, pela mesma razão. No entanto, a partir da década de 80, e principalmente 90, com a disponibilidade de ensaios imunométricos de excelente qualidade para os hormônios peptídicos (ex. TSH, LH, FSH, Prolactina, PTH, insulina etc.), estes métodos foram adaptados a plataformas automatizadas. Colocou-se, então, a necessidade de adaptação das rotinas de esteróides hormonais de alto volume, especificamente estradiol, testosterona, progesterona e cortisol, às mesmas plataformas automatizadas. Pela impossibilidade técnica e prática de serem mantidos os processos preparativos, diversas modificações foram introduzidas visando à "simplificação" das dosagens de esteróides hormonais. Tais modificações foram bem sucedidas, pois atualmente as dosagens dos esteróides de maior interesse são disponíveis na maioria das plataformas automatizadas. No entanto, um alto custo em termos de qualidade de ensaio teve que ser pago, desde que o desenho competitivo dos ensaios foi mantido com todas as suas limitações. Tentativas de desenvolvimento de ensaios não competitivos para moléculas de baixo peso molecular foram, em teoria, bem sucedidos (34), no entanto nunca atingiram o estágio de aplicação prática.
Com a crescente demanda por qualidade dos ensaios disponíveis, estas limitações, impostas aos ensaios de esteróides hormonais, têm se tornado mais evidentes, e impulsionado a pesquisa em novas metodologias (35-37). Dentre estas, a espectrometria de massa é a que apresenta maior potencial, desde que permite, teoricamente, uma especificidade muito maior que aquela proporcionada pelo reconhecimento por anticorpo específico. A demora da aplicação da metodologia na medida de esteróides hormonais, e na de outras substâncias de interesse clínico, tem várias razões, destacando-se aspectos técnicos e econômicos. Do ponto de vista técnico, a maior barreira na popularização da espectrometria de massa era a ausência de ferramentas que possibilitassem a ionização de substâncias poucos voláteis, como é o caso dos esteróides hormonais, assim como outras biomoléculas. O desenvolvimento de técnicas como o electrospray e a ionização química à pressão atmosférica (APCI) ampliaram o universo de substâncias que podem ser analisadas pela espectrometria de massa, permitindo a ionização direta a partir da fase líquida, dispensando as etapas trabalhosas de derivatização química. Além disso, os novos métodos de ionização possibilitaram o acoplamento direto com a cromatografia líquida de alta eficiência, resultando num método de alta sensibilidade e seletividade, excelente desempenho em análises quantitativas e passível de automatização. Do ponto de vista econômico, o custo dos equipamentos sempre foi o maior empecilho, e continua sendo, apesar da queda constante do preço das máquinas nas últimas décadas. Associe-se a este aspecto os custos de instalação, manutenção, e a necessidade de mão de obra especializada para o desenvolvimento e operação.
A introdução na rotina, de maneira pioneira, por vários laboratórios de referência internacional da nova metodologia na dosagem de cortisol livre urinário tem várias razões (25-27). Dentre estas, além da concentração relativamente elevada, a presença de inúmeros interferentes potenciais torna a medida altamente propícia a ganhos em especificidade metodológica. A disseminação da metodologia deverá reposicionar a dosagem de cortisol livre dentre as técnicas utilizadas para o screening de hipercortisolismo endógeno (síndrome de Cushing). Isto por que a alta especificidade analítica permite um diagnóstico mais preciso do que aquele obtido com os imunoensaios mais comuns, tornando a dosagem, já aceita como uma das mais úteis, ao lado de cortisol pós-depressão com dexametasona e cortisol salivar à meia-noite (38-42), ainda mais atrativa. O método aqui descrito apresenta a vantagem adicional de permitir a dosagem concomitante da cortisona livre, e conseqüentemente o estudo da atividade da enzima 11b-HSD2. Apesar de, teoricamente, o interesse ser restrito aos raros casos de excesso aparente de mineralocorticóides (Apparent Mineralocorticoid Excess, AME), a possibilidade de diagnóstico de outras variantes da síndrome pode ser aberta pela maior disponibilidade da dosagem.
Recebido em 15/06/04
Revisado em 30/07/04
Aceito em 17/08/04
- 1. Newell-Price J, Trainer P, Besser M, Grossman A. The diagnosis and differential diagnosis of Cushing's syndrome and pseudo-Cushing's states. Endocr Rev 1998;19:647-72.
- 2. Findling JW, Raff H. Diagnosis and differential diagnosis of Cushing's syndrome. Endocrinol Metab Clin North Am 2001;30:729-47.
- 3. Gorges R, Knappe G, Gerl H, Ventz M, Stahl F. Diagnosis of Cushing's syndrome: re-evaluation of midnight cortisol vs. urinary free cortisol and low-dose dexamethasone suppression test in a large patient group. J Endocrinol Invest 1999;22:241-9.
- 4. Putignano P, Toja P, Dubini A, Giraldi FP, Corsello SM, Cavagnini F. Midnight salivary cortisol versus urinary free and midnight serum cortisol as screening tests for Cushing's syndrome. J Clin Endocrinol Metab 2003;88:4153-7.
- 5. Vieira JGH, Accursio WL, Russo EMK, Maciel RMB, Kater CE, Chacra AR. Estudo do valor do teste rápido de supressão com dexametasona na triagem de pacientes suspeitos de síndrome de Cushing. Rev Ass Med Brasil 1985;31:129-32.
- 6. Raff H, Raff JL, Findling JW. Late-night salivary cortisol as a screening test for Cushing's syndrome. J Clin Endocrinol Metab 1998;83:2681-6.
- 7. Castro M, Elias PC, Quidute AR, Halah FP, Moreira AC. Out-patient screening for Cushing's syndrome: the sensitivity of the combination of circadian rhythm and overnight dexamethasone suppression salivary cortisol tests. J Clin Endocrinol Metab 1999;84:878-82.
- 8. Murphy BEP. Clinical evaluation of urinary cortisol determinations by competitive protein-binding radioassay. J Clin Endocrinol Metab 1968;28:343-8.
- 9. Murphy BEP, Okouneff L, Klein GP, Ngo SC. Lack of specificity of cortisol determinations in human urine. J Clin Endocrinol Metab 1981;53:91-9.
- 10. Murphy BEP. Lack of specificity of urinary free cortisol determinations: why does it continue? J Clin Endocrinol Metab 1999;84:2258-9.
- 11. Murphy BEP. Editorial: how much "UFC" is really cortisol? Clin Chem 2000;46:794.
- 12. Vieira JGH, Noguti KO, Rayol MP, Maciel RMB. Desenvolvimento e caracterização de método para a dosagem de cortisol livre urinário. Arq Bras Endocrinol Metab 2000;44:233-8.
- 13. Kelly CJG, Ogilvie A, Evans JR, Shapiro D, Wallace AM, Davies DL. Raised cortisol excretion rate in urine and contamination by topical steroids. BMJ 2001;322:594.
- 14. White PC, Pescovitz OH, Cutler Jr GB. Synthesis and metabolism of corticosteroids. In: Becker KL, editor. Principles and practice of endocrinology and metabolism Philadelphia:Lippincott; 1995p.647-62.
- 15. Schöneshöfer M, Fenner A, Dulce JK. Interferences in the radioimmunological determination of urinary free cortisol. Clin Chim Acta 1980;101:125-34.
- 16. Schöneshöfer M, Kage A, Weber B, Lenz I, Köttgen E. Determination of urinary free cortisol by "on-line" liquid chromatography. Clin Chem 1985;31:564-8.
- 17. Turpeinen U, Markkanen H, Välimäki M, Stenman U-H. Determination of urinary free cortisol by HPLC. Clin Chem 1997;43:1386-91.
- 18. Edwards CR, Stewart PM, Burt D, Brett L, McIntyre MA, Sutanto WS, et al. Localization of 11b-hydroxysteroid dehydrogenase tissue-specific protector of the mineralocorticoid receptor. Lancet 1988;2:986-9.
- 19. White PC, Mune T, Agarwal AK. 11b-Hydroxysteroid dehydrogenase and the syndrome of apparent mineralocorticoid excess. Endocr Rev 1997;18:135-56.
- 20. Palermo M, Shackleton CH, Mantero F, Stewart PM. Urinary free cortisone and the assessment of 11-beta-hydroxysteroid dehydrogenase activity in man. Clin Endocrinol 1996;45:605-11.
- 21. Shackleton CH, Honour JW. The use of combined gas chromatography-mass spectrometry in the quantitative measurement of urinary tetrahydroaldosterone. Z Klin Chem Klin Biochem 1974;12:259-60.
- 22. Shackleton CH. Mass spectrometry: application to steroid and peptide research. Endocr Rev 1985;6:441-86.
- 23. Shackleton CH, Kletke C, Wudy S, Pratt JH. Dehydroepiandrosterone sulfate quantification in serum using high-performance liquid chromatography/mass spectrometry and deuterated internal standard: a technique suitable for routine use or as a reference method. Steroids 1990;55:472-8.
- 24. Shackleton CH. Mass spectrometry in the diagnosis of steroid-related disorders and in hypertension research. J Steroid Biochem Mol Biol 1993;45:127-40.
- 25. Taylor RL, Machacek D, Singh RJ. Validation of a high-throughput liquid chromatography-tandem mass spectrometry method for urinary cortisol and cortisone. Clin Chem 2002;48:1511-9.
- 26. Kushnir MM, Rockwood AL, Nelson GJ, Terry AH, Meikle AW. Liquid chromatography-mass spectrometry analysis of urinary free cortisol. Clin Chem 2003;49:965-7.
- 27. Turpeinen U, Stenman U-H. Determination of urinary free cortisol by liquid chromatography-tandem mass spectrometry. Scand J Clin Lab Invest 2003;63:143-50.
- 28. Morineau G, Gosling J, Patricot M-C, Soliman H, Boudou P, Halnak AA, et al. Convenient chromatographic prepurification step before measurement of urinary cortisol by radioimmunoassay. Clin Chem 1997;43:786-93.
- 29. Abraham GE. Solid-phase radioimmunoassay of estradiol-17b. J Clin Endocrinol Metab 1969;29:866-70.
- 30. Korth-Schutz S, Virdis R, Saenger P, Chow DM, Levine SL, New MT. Serum androgens as a continuing index of adequacy of treatment of adrenal hyperplasia. J Clin Endocrinol Metab 1978;46:452-8.
- 31. Kater CE, Vieira JGH, Furlanetto RP, Chacra AR, Lima MPH. Determinação do cortisol sérico por radioimunoensaio e sua aplicação no diagnóstico de síndrome de Cushing. Arq Bras Endocrinol Metab 1979;23:155-65.
- 32. Miles LEH, Hales CN. Labelled antibodies and immunological assay systems. Nature 1968;219:186-9.
- 33. Kim JB, Barnard GJ, Collins WP, Kohen F, Lindner HR, Eshhar Z. Measurement of plasma estradiol-17 beta by solid-phase chemiluminescence immunoassay. Clin Chem 1982;28:1120-4.
- 34. Barnard GJ, Kohen F. Idiometric assay: noncompetitive immunoassay for small molecules typified by the measurement of estradiol in serum. Clin Chem 1990;36:1945-50.
- 35. Vieira JGH, Tachibana TT, Noguti KO, Ferrer CM, Maciel RMB. Valores falsamente elevados em ensaios diretos para a medida de hormônios esteróides no soro. J Bras Patol 1999;35:71-4.
- 36. Herold DA, Fitzgerald RL. Immunoassays for testosterone in women: better than a guess? Clin Chem 2003;49:1250-1.
- 37. Taieb J, Mathian B, Millot F, Patricot M-C, Mathieu E, Queyrel N, et al. Testosterone measured by 10 immunoassays and isotope-dilution gas chromatography-mass spectrometry in sera from 116 men, women, and children. Clin Chem 2003;49:1381-95.
- 38. Invitti C, Giraldi FP, Martin M, Cavagnini F. Diagnosis and management of Cushing's syndrome: results of an Italian multicentre study. J Clin Endocrinol Metab 1999;84:440-8.
- 39. Martinelli CE, Sader SL, Oliveira EB, Daneluzzi JC, Moreira AC. Salivary cortisol for screening of Cushing's syndrome in children. Clin Endocrinol (Oxf) 1999;51:67-71.
- 40. Tsigos C, Chrousos GP. Differential diagnosis and management of Cushing's syndrome. Annu Rev Med 1996;47:443-61.
- 41. Gorges R, Knappe G, Gerl H, Ventz M, Stahl F. Diagnosis of Cushing's syndrome: re-evaluation of midnight plasma cortisol vs. urinary free cortisol and low-dose dexamethasone supression test in a large patient group. J Endocrinol Invest 1999;22:241-9.
- 42. Goldfarb DA. Contemporary evaluation and management of Cushing's syndrome. World J Urol 1999;17:22-5.
Datas de Publicação
-
Publicação nesta coleção
12 Set 2005 -
Data do Fascículo
Abr 2005