Resumos
OBJETIVO: O presente estudo visa testar a possibilidade de que indivíduos não diabéticos, com glicemia de jejum < 126 mg/dL e com HbA1c alterada, já apresentem diminuição na filtração glomerular estimada (FGe) e aumento do MCP-1, em comparação com aqueles com HbA1c normal, independente de outras alterações metabólicas. MATERIAIS E MÉTODOS: Este estudo utilizou dados do Estudo CAMELIA (cardiometabólico renal familiar), de julho de 2006 a dezembro de 2007, com visitas aos módulos do Programa Médico de Família (PMF) de Niterói, RJ. RESULTADOS: Verificamos associação independente entre a alteração da HbA1c (≥ 5,7 e < 6,5% versus < 5,7%) e diminuição da taxa de filtração glomerular estimada. A HbA1c mostrou ser um marcador subclínico de alterações metabólicas em pacientes não diabéticos e com glicemia de jejum < 126 mg/dL, em especial na população de mulheres e de indivíduos com a cor da pele preta. CONCLUSÃO: Essas observações indicam a possibilidade de se utilizar a HbA1c no intuito de se triar grupos de risco, visando propor estratégias de intervenção precoce e, assim, promover a prevenção de doenças crônicas, como diabetes e doença renal crônica.
Diabetes melito; hemoglobina glicosilada; MCP-1; filtração glomerular; atenção primária
OBJECTIVE: This study aims investigate if nondiabetic subjects with fasting glucose < 126 mg/dL but altered HbA1c already have lower estimated glomerular filtration (eGFR) and high serum MCP-1 levels in comparison to nondiabetics with normal HbA1c, independent of other metabolic changes. MATERIALS AND METHODS: Data were derived from the database of the CAMELIA (cardio-metabolic-renal family) study, a cross sectional study performed between July 2006 and December 2007, with participants recruited from the Family Doctor Program, Niterói, RJ. RESULTS: An independent association between changes in HbA1c (≥ 5.7 and < 6.5% versus < 5.7%) and decreased eGFR rate was found. The HbA1c was shown to be a marker of metabolic changes in nondiabetic subjects with fasting glucose < 126 mg/dL, particularly in women and blacks. CONCLUSION: These observations support the use of HbA1c levels in strategies for early intervention and prevention of chronic diseases such as diabetes mellitus and chronic kidney disease.
Diabetes mellitus; hemoglobin glycosylated; MCP-1; glomerular filtration; primary attention
ARTIGOS ORIGINAIS
Correlação entre MCP-1, HbA1c e a filtração glomerular em pacientes não diabéticos
Correlation between MCP-1, HbA1c and glomerular filtration in nondiabetic patients
Verônica Alcoforado de MirandaI; Maria Luiza Garcia RosaII; Jocemir Ronaldo LugonIII; Rubens Antunes Cruz FilhoIII; Talita Sposito de OliveiraII; Adriana Neves Ladeira da SilvaII; Hye Chung KangIV; Denizar Vianna AraújoV
IUniversidade Federal do Rio de Janeiro (UFRJ), Macaé, Faculdade de Medicina, Macaé, RJ, Brasil
IIUniversidade Federal Fluminense (UFF), Departamento de Epidemiologia e Bioestatística, Niterói, RJ, Brasil
IIIUFF, Departamento de Medicina Clínica, Niterói, RJ, Brasil
IVUFF, Departamento de Patologia, Niterói, RJ, Brasil
VUniversidade Estadual do Rio de Janeiro (UERJ), Departamento de Medicina Clínica, Rio de Janeiro, RJ, Brasil
Correspondência para Correspondência para: Maria Luiza Garcia Rosa Rua Marquês do Paraná, 303, 3º andar do prédio anexo 24030-21 Niterói, RJ, Brasil mluizagr@gmail.com
RESUMO
OBJETIVO: O presente estudo visa testar a possibilidade de que indivíduos não diabéticos, com glicemia de jejum < 126 mg/dL e com HbA1c alterada, já apresentem diminuição na filtração glomerular estimada (FGe) e aumento do MCP-1, em comparação com aqueles com HbA1c normal, independente de outras alterações metabólicas.
MATERIAIS E MÉTODOS: Este estudo utilizou dados do Estudo CAMELIA (cardiometabólico renal familiar), de julho de 2006 a dezembro de 2007, com visitas aos módulos do Programa Médico de Família (PMF) de Niterói, RJ.
RESULTADOS: Verificamos associação independente entre a alteração da HbA1c (≥ 5,7 e < 6,5% versus < 5,7%) e diminuição da taxa de filtração glomerular estimada. A HbA1c mostrou ser um marcador subclínico de alterações metabólicas em pacientes não diabéticos e com glicemia de jejum < 126 mg/dL, em especial na população de mulheres e de indivíduos com a cor da pele preta.
CONCLUSÃO: Essas observações indicam a possibilidade de se utilizar a HbA1c no intuito de se triar grupos de risco, visando propor estratégias de intervenção precoce e, assim, promover a prevenção de doenças crônicas, como diabetes e doença renal crônica.
Descritores: Diabetes melito; hemoglobina glicosilada; MCP-1; filtração glomerular; atenção primária
ABSTRACT
OBJECTIVE: This study aims investigate if nondiabetic subjects with fasting glucose < 126 mg/dL but altered HbA1c already have lower estimated glomerular filtration (eGFR) and high serum MCP-1 levels in comparison to nondiabetics with normal HbA1c, independent of other metabolic changes.
MATERIALS AND METHODS: Data were derived from the database of the CAMELIA (cardio-metabolic-renal family) study, a cross sectional study performed between July 2006 and December 2007, with participants recruited from the Family Doctor Program, Niterói, RJ.
RESULTS: An independent association between changes in HbA1c (≥ 5.7 and < 6.5% versus < 5.7%) and decreased eGFR rate was found. The HbA1c was shown to be a marker of metabolic changes in nondiabetic subjects with fasting glucose < 126 mg/dL, particularly in women and blacks.
CONCLUSION: These observations support the use of HbA1c levels in strategies for early intervention and prevention of chronic diseases such as diabetes mellitus and chronic kidney disease.
Keywords:Diabetes mellitus; hemoglobin glycosylated; MCP-1; glomerular filtration; primary attention
INTRODUÇÃO
O diabetes é reconhecidamente um dos maiores fatores de risco para doenças cardiovasculares e renais. Seu diagnóstico é estabelecido a partir da identificação da presença de hiperglicemia e, mais recentemente, pelo aumento da hemoglobina glicada (HbA1c) (1). Níveis elevados de HbA1c em indivíduos sem diabetes e com níveis normais de glicemia em jejum têm sido associados a alterações micro e macrovasculares, entre elas alterações da filtração glomerular (2). Diversos marcadores inflamatórios, em especial a MCP-1 (proteína quimiotática de macrófagos-1), estão envolvidos no mecanismo de lesão glomerular descrito em casos de nefropatia diabética (3). Não encontramos estudos que tenham investigado a associação da alteração da HbA1c em não diabéticos com glicemia de jejum < 126 mg/dL, com diminuição da filtração glomerular (FGe) e aumento de marcadores inflamatórios, em especial o MCP-1. O presente estudo visa testar a possibilidade de que indivíduos não diabéticos, com glicemia de jejum < 126 mg/dL e com HbA1c alterada, já apresentem diminuição na filtração glomerular estimada (FGe) e aumento do MCP-1, em comparação àqueles com HbA1c normal, independente de outras alterações metabólicas.
MATERIAIS E MÉTODOS
Este estudo utilizou dados do Estudo CAMELIA (cardiometabólico renal familiar) cujo objetivo foi investigar a existência de agregação familiar de componentes da síndrome metabólica e associação desses com fatores demográficos e sociais, hábitos de vida e marcadores inflamatórios. De julho de 2006 a dezembro de 2007, foram visitados 13 módulos do Programa Médico de Família (PMF), selecionados por conveniência, buscando-se incluir todas as regiões político-administrativas da cidade de Niterói, RJ. Após projeto piloto, pesquisadores treinados investigaram participantes de famílias, selecionadas aleatoriamente, em cada um dos módulos. Os critérios de inclusão foram ser hipertenso, diabético, diabético hipertenso ou não diabético e não hipertenso, ser vinculado ao PMF, com cônjuge e pelo menos um filho natural do casal de 12 a 30 anos, todos concordando em participar da pesquisa. Os critérios de exclusão foram: ser gestante, portador de doenças associadas à baixa imunidade, ou que estivessem em uso de medicamentos que pudessem interferir nos resultados dos exames (como corticoides e citostáticos). Os participantes responderam a questionário padronizado, contendo questões relacionadas a características demográficas, socioeconômicas, comorbidades e estilo de vida. Também foram realizadas consulta médica, mensuração da pressão arterial, coleta de sangue e urina, assim como avaliação antropométrica e nutricional.
Para avaliação da massa corporal (kg), utilizou-se balança digital (Filizola S/A, modelo PL18) com variação de 0,1 kg e capacidade de até 150 kg. Para a medição da estatura, foi utilizado estadiômetro digital (Kirchner & Wilhelm, Medizintechnik, Alemanha) com precisão de 1,0 centímetro (cm). A medição foi realizada uma vez com os participantes descalços e em posição ortostática. Foram realizadas duas medidas da circunferência abdominal e do quadril, com a utilização de fita métrica inelástica de 200 cm e precisão de 0,1 cm, calculando-se a média e admitindo-se variação máxima de 1 cm entre as duas, repetindo-se o procedimento no caso de ultrapassar essa variação. A circunferência abdominal foi aferida após uma expiração, no ponto do menor perímetro na região abdominal. Os indivíduos encontravam-se em posição ereta, sem camisa, com o abdômen relaxado, braços estendidos ao longo do corpo e os pés juntos. A circunferência do quadril foi medida no ponto de maior perímetro, passando pelas nádegas, com os indivíduos mantendo-se em posição ereta, braços ao lado do corpo e pés juntos. Como referência para a classificação das medidas antropométricas, utilizou-se o Guidelines on Overweight and Obesity do National Health Institute (NHI), 1998 (4). A pressão arterial foi medida três vezes, segundo as VI Diretrizes Brasileiras de Hipertensão Arterial (5), com o aparelho oscilométrico Omron validado (6), e foi considerada a média entre a segunda e terceira medidas. Quando havia uma diferença de mais de 5 mmHg entre as medidas, uma nova mensuração era realizada. As dosagens bioquímicas foram feitas no Laboratório Vizela da Fundação Municipal de Saúde e no Hospital Universitário Antonio Pedro (HUAP) da Universidade Federal Fluminense. Amostras de urina e alíquotas de soro foram armazenadas em freezer a -80ºC, no Serviço de Hematologia do HUAP. As dosagens de glicose de jejum, insulina de jejum, colesterol total (CT), HDL-colesterol (HDL-c) e triglicerídeos (TG) foram realizadas no equipamento Selectra da marca Wiener®. A HbA1c foi dosada por imunoturbidimetria no equipamento Labmax 240 da Labtest, método certificado pelo National Glycohemoglobin Standardization Program (NGSP) (posicionamento). Todas as análises foram realizadas no mesmo dia de coleta.
As dosagens de insulina de jejum, MCP-1, inibidor do ativador do plasminogênio 1 (PAI-1), resistina, adiponectina e interleucina-6 (IL-6) foram realizadas no equipamento Luminex®, Luminex Corporation, Austin, Texas, EUA. A dosagem de proteína C reativa (PCR) foi realizada com kits comerciais de ELISA. Foram realizadas a partir de amostras de soro congelado a -80ºC.
A taxa de filtração glomerular estimada (FGe) foi calculada usando-se a equação desenvolvida pelo estudo Modification of Diet in Renal Disease simplificada: FGe = 186 x creatinina sérica-1,154 x idade-0,203 x 0,742 (se mulher), uma fórmula validada para esse fim (7). A ingestão de sódio foi estimada pela determinação da taxa de excreção de sódio ([Na em mEq/L na amostra de urina/creatinina urinária em mg%] x 100) expresso em mEq Na/g de creatinina.
O presente estudo é do tipo transversal e incluiu dados de participantes de ambos os gêneros, com 20 anos ou mais, além de dados completos de exames bioquímicos. Foram excluídos diabéticos (autorrelato de diagnóstico médico) e aqueles com glicemia de jejum ≥ 126 mg/dL.
Para análise univariada, utilizamos a HbA1c em três categorias: < 5,7%, ≥ 5,7% e < 6,5% e ≥ 6,5%. Todas as variáveis associadas com um nível de significância < 0,10 foram incluídas no modelo multivariado.
Foi utilizado o pacote estatístico SPSS versão 17.0. As análises bivariadas foram testadas com o teste do qui-quadrado (números absolutos e percentuais) ou pelo teste de Mann-Whitney, teste não paramétrico (dados contínuos foram apresentados em medianas e intervalo interquartílico IQR). As análises multivariadas foram realizadas por meio do modelo logístico de equações de estimação generalizadas (GEE), adequado para observações não independentes, uma vez que a unidade de inclusão no estudo original foram famílias. Foram calculadas razões de chance de prevalência (OR) ajustadas de alteração de HbA1c (≥ 5,7% e < 6,5% versus < 5,7%). O projeto foi aprovado pelo Comitê de Ética em Pesquisa da Faculdade de Medicina da Universidade Federal Fluminense/Hospital Universitário Antônio Pedro e todos os participantes assinaram um Termo de Consentimento Livre e Esclarecido.
RESULTADOS
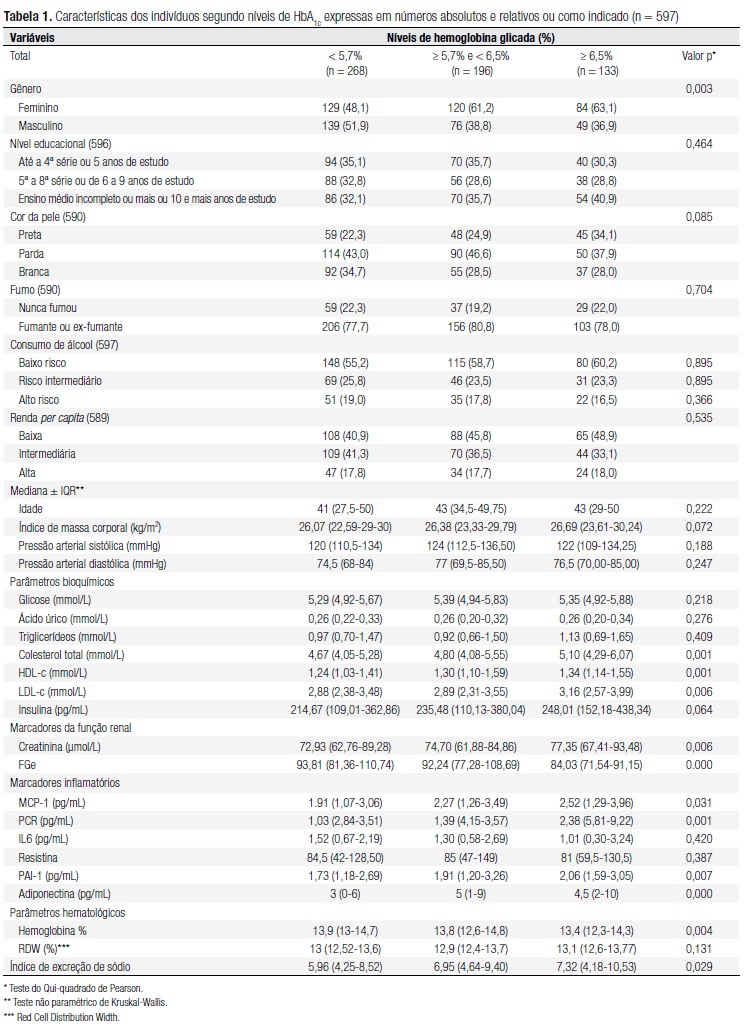
Foram incluídos 597 não diabéticos com glicose em jejum < 126 mg/dL: 268 (44,9%) com HbA1c < 5,7% categoria 1; 196 (32,8%) com HbA1c ≥ 5,7% e < 6,5% categoria 2 e 133 (22,3%) com HbA1c ≥ 6,5% categoria 3, esta excluída da análise multivariada. Mulheres e indivíduos com a cor da pele preta foram maioria nas categorias 2 e 3 e apresentaram maiores medianas de IMC, CT, HDL-c, LDL-c, insulina em jejum, creatinina, FGe, MCP-1, PCR, PAI-1, ingestão de sódio e menor valor percentual de hemoglobina. A mediana da adiponectina foi maior na categoria 2 (Tabela 1). Na análise multivariada, calcularam-se OR ajustados de alteração da HbA1c: categoria 2 (de risco: HbA1c ≥ 5,7% e < 6,5%)/categoria 1 (de referência: HbA1c < 5,7%), sendo examinados 464 indivíduos. Excluiu-se a categoria 3 (maior risco: HbA1c ≥ 6,5%), uma vez que o objetivo era saber se mesmo uma menor alteração na HbA1c já estava associada a uma menor taxa de filtração glomerular estimada.
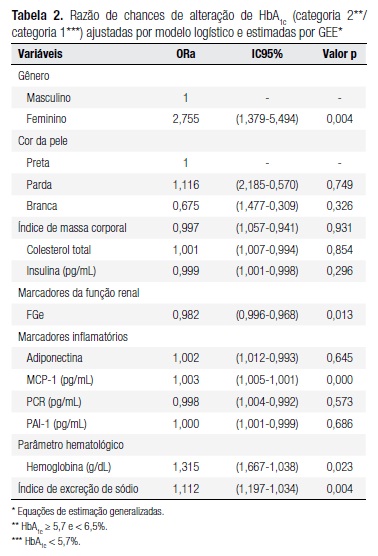
As variáveis incluídas foram gênero, cor da pele, IMC, CT, insulina de jejum, FGe, adiponectina, MCP-1, PCR, PAI-1, hemoglobina e índice de excreção de sódio (Tabela 2). A chance de estar na categoria 2 foi inversamente associada à FGe e positivamente associada ao sexo feminino, MCP-1, hemoglobina e ao índice de excreção de sódio, com p < 0,05.
DISCUSSÃO
Embora a concentração de HbA1c reflita os índices médios de glicose no sangue nos últimos três meses, sendo um sensível marcador do metabolismo da glicose (8) e distúrbios da homeostase da glicose sejam comuns em portadores de doença renal crônica (DRC) (9), no presente estudo, verificamos associação independente entre a alteração da HbA1c (≥ 5,7 e < 6,5% versus < 5,7%) e a diminuição da taxa de filtração glomerular estimada.
Um crescente corpo de evidências sugere uma ligação entre hiperglicemia crônica e o estresse oxidativo, disfunção endotelial e inflamação. A HbA1c é um alvo para a glicoxidação intracelular e as reações de peroxidação que resultam na formação de produtos finais de glicação avançada (AGE) (10,11). Os AGE têm sido implicados na iniciação e progressão da aterosclerose. Hiperglicemia crônica também foi associada ao aumento dos níveis circulantes de LDL-oxidado, uma forma altamente aterogênica do colesterol LDL (12). Em um estudo de base populacional, elevações moderadas nos níveis da glicose foram associadas com anormalidades de mecanismos de antioxidação celular (12).
Na análise univariada (Tabela 1), observou-se, consistentemente com outros estudos, que a HbA1c esteve mais elevada nas mulheres (13), nos indivíduos de cor da pele preta (9,13) e em indivíduos com maior IMC, maior LDL-c (9,13,14), triglicerídeos (13,14) e hemoglobina (14). A associação positiva entre HbA1c, HDL-c e adiponectina, observada no presente estudo, não seria esperada. Os dois marcadores são anti-inflamatórios e logo deveriam estar diminuídos diante do aumento da HbA1c.
Com base nos argumentos que mencionaremos, levantamos a hipótese enunciada a seguir. Em primeiro lugar, correlação positiva entre HDL-c e adiponectina plasmática foi descrita em diversos estudos (15-17). Em segundo, em uma coorte de jovens do sexo masculino não obesos e não hipertensos, houve diminuição tanto da adiponectina quanto do HDL-c plasmáticos com a restrição do sódio da dieta (18). Em terceiro lugar, a paraoxonase, responsável pelo efeito protetor do HDL-c, tem seu metabolismo afetado apenas quando há altos índices glicêmicos, o que leva à redução do HDL-c (19). Finalmente, o aumento da HbA1c em indivíduos sem diabetes e com a glicemia normal em jejum leva à inflamação subclínica (9). No presente estudo, o consumo de sal foi positivamente associado à HbA1c, tanto na análise univariada (Tabela 1) quanto na análise multivariada (Tabela 2), e todos os pacientes estudados não possuíam diabetes e a glicemia de jejum era inferior a 126 mg/dL. Acreditamos que o estado inflamatório dos indivíduos com alteração da HbA1c era ainda insuficiente para alterar o HDL-c e a adiponectina, e o consumo mais elevado de sal poderia explicar o aumento dos dois marcadores. Embora o estudo de Krikken e cols. (18) não tenha testado se o aumento do consumo de sal poderia estar positivamente associado ao aumento da adiponectina e sim o contrário, essa possibilidade nos parece plausível.
O estado inflamatório de baixo grau associou-se à HbA1c alterada, observando-se maiores níveis de PCR e do PAI-1 na análise univariada (Tabela 1) e do MCP-1, mesmo após ajuste (Tabela 2). O MCP-1 está elevado em diabéticos (20) e pacientes com doença renal (21). Não encontramos relatos sobre a associação entre o MCP-1 e a HbA1c. O MCP-1 está presente nas placas ateroscleróticas (22) e sua superexpressão no endotélio leva às lesões iniciais da aterosclerose (23,24) em uma cascata inflamatória, na medida em que as células endoteliais também secretam MCP-1 em resposta às citocinas. Sabe-se que as doenças glomerulares estão associadas à esclerose mesangial e são caracterizadas pela infiltração dos macrófagos nos glomérulos em estágios iniciais da doença, antes da expansão da matriz extracelular e da glomeruloesclerose (25), um dos mecanismos que explica a diminuição do FGe diante do aumento da MCP-1.
Sabanayagam e cols. (26) observaram que há uma relação linear e positiva, sem um ponto de corte definido, entre HbA1c e complicações microvasculares, incluindo doença renal crônica. Selvin e cols. (2) estudaram prospectivamente cerca de 10 mil adultos americanos livres de diabetes e observaram que, após cerca de 14 anos de acompanhamento, os níveis de HbA1c mensurados no início do estudo foram previsores do aparecimento de DRC. Assim como Sabanayagam e cols. (26), Selvin e cols. (2) também não identificaram um ponto de corte significativo para previsão de DRC. No presente estudo, pacientes com HbA1c alterada apresentaram menores níveis de FGe, mesmo depois de ajuste.
Ibrahim e Rashed (27) sugerem que a hiperglicemia está associada ao aumento dos níveis urinários de MCP-1, que está estreitamente relacionada à lesão renal refletida por níveis de proteinúria e filtração glomerular. Esses resultados sugerem que a MCP-1 está envolvida na patogênese da nefropatia diabética nas suas várias fases.
É necessário ressaltar algumas limitações do presente estudo. Trata-se de um estudo transversal e não se pode garantir a antecedência das alterações da HbA1c, impedindo que se cogitem relações causais. Por outro lado, por ser uma hipótese pos-hoc, o tamanho da amostra não conferiu poder estatístico suficiente para se alcançar significância em várias associações, cuja inclusão no modelo poderia, teoricamente, alterar as associações observadas.
No presente estudo, observou-se que a alteração da HbA1c em indivíduos não diabéticos e com glicemia de jejum < 126 mg/dL esteve associada a diminuição da FGe, aumento da MCP-1 e maior índice de excreção de sódio.
A HbA1c mostrou ser um marcador subclínico de alterações metabólicas em pacientes não diabéticos e com glicemia de jejum < 126 mg/dL, em especial na população de mulheres e de indivíduos com a cor da pele preta, estando associada à diminuição da FGe. As alterações nos níveis de adiponectina e HDL-c provavelmente estão ligadas à dieta hipersódica, correlacionada positivamente com a HbA1c.
Essas observações indicam a possibilidade de se utilizar a HbA1c no intuito de se triar grupos de risco, visando propor estratégias de intervenção precoce e, assim, promover a prevenção de doenças crônicas como diabetes e doença renal crônica.
Agradecimentos: o Estudo CAMELIA recebeu financiamento da Fundação de Amparo à Pesquisa do Estado do Rio de Janeiro (Faperj) para compra de kits para os exames bioquímicos, da Fundação Municipal de Saúde para realização de exames de sangue e urina, e foram concedidas bolsas de estudo pela Universidade Federal Fluminense, Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq) e Faperj.
Recebido em 3/Set/2012
Aceito em 5/Mar/2013
Declaração: os autores declaram não haver conflitos de interesse científico neste estudo.
- 1. American Diabetes Association (ADA). Diagnosis and Classification of Diabetes Mellitus. Diabetes Care. 2010;33(Suppl. 1):S67-9.
- 2. Selvin E, Ning Y, Steffes MW, Bash LD, Klein R, Wong TY, et al. Glycated hemoglobin and the risk of kidney disease and retinopathy in adults with and without diabetes. Diabetes. 2011;60(1):298-305.
- 3. Banba N, Nakamura T, Matsumura M, Kuroda H, Hattori Y, Kasai K. Possible relationship of monocyte chemoattractant protein-1 with diabetic nephropathy. Kidney Int. 2000;58(2):684-90.
-
4Clinical Guidelines on the Identification, Evaluation, and Treatment of Overweight and Obesity in Adults. The Evidence Report, National Institutes of Health. 1998;6(Suppl. 2):51S-209S.
- 5. Sociedade Brasileira de Cardiologia/Sociedade Brasileira de Hipertensão/Sociedade Brasileira de Nefrologia. VI Diretrizes Brasileiras de Hipertensão. Arq Bras Cardiol. 2010;95(1 suppl. 1):151.
- 6. O'Brien E, van Montfrans G, Palatini P, Tochikubo O, Staessen J, Shirasaki O, et al. Task. Force I: methodological aspects of blood pressure measurement. Blood Press Monit. 2001;6(6):313-5.
- 7. Levey AS, Greene T, Beck GJ, Caggiula AW, Kusek JW, Hunsicker LG, et al. Dietary protein restriction and the progression of chronic renal disease: what have all of the results of the MDRD study shown Modification of Diet in Renal Disease Study group. J Am Soc Nephrol. 1999;10(11):2426-39.
- 8. Dunn PJ, Cole RA, Soeldner JS, Gleason RE. Reproducibility of hemoglobin AIc and sensitivity to various degrees of glucose intolerance. Ann Intern Med. 1979;91:390-6.
- 9. Menon V, Greene T, Pereira AA, Wang X, Beck GJ, Kusek JW, et al. Glycosylated hemoglobin and mortality in patients with nondiabetic chronic kidney disease. J Am Soc Nephrol. 2005;16(11):3411-7.
- 10. Linden E, Cai W, He JC, Xue C, Li Z, Winston J, et al. Endothelial dysfunction in patients with chronic kidney disease results from advanced glycation end products (AGE)-mediated inhibition of endothelial nitric oxide synthase through RAGE activation. Clin J Am Soc Nephrol. 2008;3(3):691-8.
- 11. Himmelfarb J, Stenvinkel P, Ikizler TA, Hakim RM. The elephant in uremia: oxidant stress as a unifying concept of cardiovascular disease in uremia. Kidney Int. 2002;62:1524-38.
- 12. Menon V, Ram M, Dorn J, Armstrong D, Muti P, Freudenheim JL, et al. Oxidative stress and glucose levels in a population-based sample. Diabet Med. 2004;21:1346-52.
- 13. Selvin E, Ning Y, Steffes MW, Bash LD, Klein R, Wong TY, et al. Glycated hemoglobin and the risk of kidney disease and retinopathy in adults with and without diabetes. Diabetes. 2011;60(1):298-305.
- 14. Yoriko H, Hara S, Arase Y, Saito K, Fujiwara K, Tsuji H, et al. HbA1c 5·7-6·4% and impaired fasting plasma glucose for diagnosis of prediabetes and risk of progression to diabetes in Japan (TOPICS 3): a longitudinal cohort study. Lancet. 2011;378(9786):147-55.
- 15. Zietz B, Herfarth H, Paul G, Ehling A, Müller-Ladner U, Schölmerich J, et al. Adiponectin represents an independent cardiovascular risk factor predicting serum HDL-cholesterol levels in type 2 diabetes. FEBS Lett. 2003;545(2-3):103-4.
- 16. von Eynatten M, Humpert PM, Bluemm A, Lepper PM, Hamann A, Allolio B, et al. High-molecular weight adiponectin is independently associated with the extent of coronary artery disease in men. Atherosclerosis. 2008;199(1):123-8.
- 17. Yamamoto Y, Hirose H, Saito I, Tomita M, Taniyama M, Matsubara K, et al. Correlation of the adipocyte-derived protein adiponectin with insulin resistance index and serum high-density lipoprotein-cholesterol, independent of body mass index, in the Japanese population. Clin Sci (Lond). 2002;103(2):137-42.
- 18. Krikken JA, Dallinga-Thie GM, Navis G, Dullaart RP. Short term dietary sodium restriction decreases HDL cholesterol, apolipoprotein A-I and high molecular weight adiponectin in healthy young men: relationships with renal hemodynamics and RAAS activation. Nutr Metab Cardiovasc Dis. 2012;22(1):35-41.
- 19. Serrato M, Marian AJ. A variant of human paraoxonase/arylesterase (HUMPONA) gene is a risk factor for coronary artery disease. J Clin Invest. 1995;96(6):3005-8.
- 20. Papatheodorou K, Papanas N, Papazoglou D, Gioka T, Antonoglou C, Glaros D, et al. Monocyte chemoattractant protein 1 is correlated with glycemic control and peripheral arterial disease in type 2 diabetic patients with metabolic syndrome. Angiology. 2013;64(3):223-9.
- 21. Papayianni A, Alexopoulos E, Giamalis P, Gionanlis L, Belechri AM, Koukoudis P, et al. Circulating levels of ICAM-1, VCAM-1, and MCP-1 are increased in haemodialysis patients: association with inflammation, dyslipidaemia, and vascular events. Nephrol Dial Transplant. 2002;17(3):435-41.
- 22. Nelken NA, Coughlin SR, Gordon D, Wilcox JN. Monocyte chemoattractant protein-1 in human atheromatous plaques. J Clin Invest. 1991;88:1121-7.
- 23. Grewal IS, Rutledge BJ, Fiorillo JA, Gu L, Gladue RP, Flavell RA, et al. Transgenic monocyte chemoattractant protein-1 (MCP-1) in pancreatic islets produces monocyte-rich insulitis without diabetes. Abrogation by a second transgene expressing systemic MCP-1. J Immunol. 1997;159:401-8.
- 24. Klahr S, Schreiner G, Ichikawa I. The progression of renal disease. N Engl J Med. 1988;318:1657-66.
- 25. Rovin BH, Schreiner GF. Cell-mediated immunity in glomerular disease. Annu Rev Med. 1991;42:25-33.
- 26. Sabanayagam C, Liew G, Tai ES, Shankar A, Lim SC, Subramaniam T, et al. Relationship between glycated haemoglobin and microvascular complications: is there a natural cut-off point for the diagnosis of diabetes. Diabetologia. 2009;52(7):1279-89.
- 27. Ibrahim S, Rashed L. Correlation of urinary monocyte chemo-attractant protein-1 with other parameters of renal injury in type-II diabetes mellitus. Saudi J Kidney Dis Transpl. 2008;19(6):911-7.
Correspondência para:
Datas de Publicação
-
Publicação nesta coleção
25 Jul 2013 -
Data do Fascículo
Jul 2013
Histórico
-
Recebido
03 Set 2012 -
Aceito
05 Mar 2013