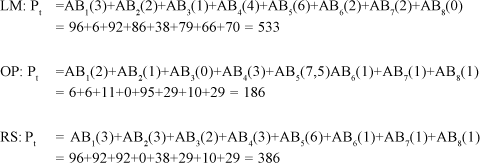Resumos
Em razão da urgência de se decidir por um tratamento clínico ou por uma intervenção cirúrgica imediata, o estudo da colestase neonatal prolongada envolve dois objetivos básicos: o diagnóstico diferencial entre atresia biliar e hepatite neonatal e a pesquisa dos agentes etiológicos associados. Desta maneira, através de estudo prospectivo desenvolvido na década de 1970, foram avaliadas 77 crianças portadoras de colestase neonatal prolongada para estabelecer o diagnóstico diferencial entre atresia biliar e hepatite neonatal e, numa segunda fase, 108 crianças, visando esclarecer a etiopatogenia da colestase neonatal prolongada. Os resultados do diagnóstico diferencial revelaram que, dos 18 atributos avaliados, apenas oito mostraram-se bons indicadores de atresia biliar, em ordem decrescente: ductos proliferados (espaço-porta), fibrose (espaço-porta), colestase (espaço-porta), cor das fezes -- acolia, hepatomegalia, colestase canalicular (lóbulo), infiltrado (espaço-porta), células gigantes (lóbulo). Estes oito atributos foram então compostos, mediante uma ponderação, em um único indicador de grande poder discriminativo, capaz de decidir o diagnóstico diferencial em 99% dos casos. Quanto à etiopatogenia, registrou-se: vírus rubéola 0%, vírus herpes simples 0%, listeriose 0%, citomegalovirose 2,2%, vírus hepatite B 2,4%, toxoplasmose 2,8%, deficiência de alfa-1-antitripsina 13,1%, sífilis 21,1 %, auto-anticorpos hepáticos 58,4%. O trabalho desenvolvido mostra que as 8 variáveis mais decisivas, como indicadoras diferenciais entre atresia biliar e hepatite neonatal, permanecem como índices fundamentais, auxiliando, em conjunto com novos métodos diagnósticos, na composição de uma estratégia multifatorial cada vez menos invasiva e mais precisa. O estudo da etiopatogenia, dependente das condições epidemiológicas locais e da época, com a introdução de novos métodos diagnósticos, torna-se atualmente cada vez mais completo e abrangente, evoluindo para a ideal diminuição progressiva dos processos idiopáticos.
Colestase; Hepatite neonatal; Atresia biliar; Biopsia; Lactente
Due to the urgency in choosing either clinical treatment or immediate surgical intervention, the study of the prolonged neonatal cholestasis involves two basic aims: the differential diagnosis between biliary atresia and neonatal hepatitis and the research into the associated etiological agents. So, in a prospective trial carried out in the 70´s, 77 children with prolonged neonatal cholestasis were studied in order to establish the differential diagnosis between biliary atresia and neonatal hepatitis, followed by the evaluation of 108 children towards a pathogenesis of the prolonged neonatal cholestasis. The results of the differential diagnosis showed that within 18 items examined only 8 proved to be good biliary atresia indicators. They are as follows (in decreasing order): ductular proliferation (portal tracts), fibrosis (portal tracts), cholestasis (portal tracts), stools colour -- acholia, hepatomegaly, canalicular cholestasis (lobule), infiltrate (portal tracts), giant cells (lobule). These eight items were then gathered in a sole indicator of great discriminative power, with a confidence level of 99%. The figures regarding the pathogenesis are: rubella virus 0%, herpes simplex virus 0%, listeriosis 0%, cytomegalovirus 2.2%, hepatitis B virus 2.4%, toxoplasmosis 2.8%, alpha-1-antitrypsin deficiency 13.1%, syphilis 21.1%, autoantibodies against the liver 58.4%. Such work thus revealed that those eight most important factors when differentiating biliary atresia from neonatal hepatitis remain as fundamental indicators and, when employed alongside other diagnostic methods, can help in the assembling of a multifactorial strategy less and less invasive and more precise. The pathogenic study, with its heavy dependency on time and place, has become more complete with the introduction of new diagnostic methods, evolving to the ideal progressive reduction of idiopathic processes.
Cholestasis; Hepatitis; Hepatitis; Biliary atresia; Biopsy; Infant
ARTIGO ORIGINAL / ORIGINAL ARTICLE
COLESTASE NEONATAL PROLONGADA:
estudo prospectivo
Elizabeth Teixeira Mendes Livramento PRADO* * Professora Adjunta do Departamento de Pediatria da Faculdade de Ciências Médicas da Santa Casa de São Paulo - FCMSCSP. , Maria de Fátima ARAUJO** * Professora Adjunta do Departamento de Pediatria da Faculdade de Ciências Médicas da Santa Casa de São Paulo - FCMSCSP. e José Vicente Martins CAMPOS*** * Professora Adjunta do Departamento de Pediatria da Faculdade de Ciências Médicas da Santa Casa de São Paulo - FCMSCSP.
RESUMO ¾ Em razão da urgência de se decidir por um tratamento clínico ou por uma intervenção cirúrgica imediata, o estudo da colestase neonatal prolongada envolve dois objetivos básicos: o diagnóstico diferencial entre atresia biliar e hepatite neonatal e a pesquisa dos agentes etiológicos associados. Desta maneira, através de estudo prospectivo desenvolvido na década de 1970, foram avaliadas 77 crianças portadoras de colestase neonatal prolongada para estabelecer o diagnóstico diferencial entre atresia biliar e hepatite neonatal e, numa segunda fase, 108 crianças, visando esclarecer a etiopatogenia da colestase neonatal prolongada. Os resultados do diagnóstico diferencial revelaram que, dos 18 atributos avaliados, apenas oito mostraram-se bons indicadores de atresia biliar, em ordem decrescente: ductos proliferados (espaço-porta), fibrose (espaço-porta), colestase (espaço-porta), cor das fezes ¾ acolia, hepatomegalia, colestase canalicular (lóbulo), infiltrado (espaço-porta), células gigantes (lóbulo). Estes oito atributos foram então compostos, mediante uma ponderação, em um único indicador de grande poder discriminativo, capaz de decidir o diagnóstico diferencial em 99% dos casos. Quanto à etiopatogenia, registrou-se: vírus rubéola 0%, vírus herpes simples 0%, listeriose 0%, citomegalovirose 2,2%, vírus hepatite B 2,4%, toxoplasmose 2,8%, deficiência de alfa-1-antitripsina 13,1%, sífilis 21,1 %, auto-anticorpos hepáticos 58,4%. O trabalho desenvolvido mostra que as 8 variáveis mais decisivas, como indicadoras diferenciais entre atresia biliar e hepatite neonatal, permanecem como índices fundamentais, auxiliando, em conjunto com novos métodos diagnósticos, na composição de uma estratégia multifatorial cada vez menos invasiva e mais precisa. O estudo da etiopatogenia, dependente das condições epidemiológicas locais e da época, com a introdução de novos métodos diagnósticos, torna-se atualmente cada vez mais completo e abrangente, evoluindo para a ideal diminuição progressiva dos processos idiopáticos.
DESCRITORES ¾ Colestase. Hepatite neonatal, etiologia. Atresia biliar, etiologia. Biopsia. Lactente.
INTRODUÇÃO
A compreensão dos processos que envolvem o desenvolvimento da colestase neonatal prolongada (CNP), composta, principalmente, pela atresia biliar (AB) e hepatite neonatal (HN), constitui ainda um desafio à hepatologia pediátrica. As dificuldades provêm da complexa fisiopatologia hepática infantil, derivada das extensas alterações estruturais e metabólicas que se processam desde a organogênese até a fase pós-natal imediata. Por outro lado, a interação dos inúmeros fatores etiológicos freqüentemente associados torna mais difícil a qualificação e a quantificação do comprometimento funcional e histopatológico das diversas áreas afetadas. Contudo, o principal objetivo do estudo da CNP foi sempre a definição diagnóstica precoce, principalmente em decorrência da necessidade de cirurgia ¾ a portoenterostomia de Kasai(27)¾ antes dos dois meses de idade na AB, antecedendo a instalação da esclerose irreversível dos ductos biliares intra-hepáticos.
De qualquer forma, o diagnóstico diferencial da CNP continua cerceado por inúmeras limitações clínicas e laboratoriais. Tais limitações não devem impedir, contudo, que se façam tentativas diagnósticas cada vez mais precisas, principalmente nas situações em que a prática clínica exija simplificação semiológica, face à escassez de recursos, comum entre nós. Deste ponto de vista, impõe-se a tentativa de selecionar os exames laboratoriais verdadeiramente eficazes. Essa tentativa de sistematização ¾ para maior rendimento prático da semiologia clínica e laboratorial ¾ constituiu a base para o desenvolvimento da avaliação da CNP em nosso meio, conforme estudo prospectivo realizado na década de 1970(42, 43).
Como foi situada, a finalidade da análise realizada envolveu a indagação sobre a validade de certos índices semiológicos e laboratoriais, procurando prioritariamente diferenciar a CNP que requer conduta terapêutica clínica da cirúrgica e, em segundo lugar, estudar a etiopatogenia.
MATERIAL E MÉTODOS
1. Diagnóstico diferencial entre: CNP sem ductos biliares patentes ¾ AB e com ductos biliares patentes ¾ HN (42)
Foram observadas, através de estudo prospectivo na década de 1970, 77 crianças portadoras de CNP na Disciplina de Gastroenterologia Infantil do Departamento de Pediatria da Faculdade de Ciências Médicas da Santa Casa de São Paulo, São Paulo, SP, tendo sido destacados e sistematicamente pesquisados 18 atributos: sexo, peso ao nascer, idade do início da colestase, persistência da acolia fecal (+ 25%, ++ 50%, +++ 75%,++++ 100% do tempo de observação), tamanho do fígado, tamanho do baço, aspartato-aminotransferase, alfa-feto-proteína sérica, histopatologia hepática. A biopsia hepática foi realizada em 21 lactentes com idade inferior a 2 meses, nos restantes em período etário posterior. Foram utilizadas fixação e inclusão de rotina e colorações de HE, tricrômico de Masson, reticulina e PAS. As anormalidades histológicas foram graduadas em ordem crescente de intensidade da lesão, em cinco valores, conforme a seguinte classificação: 0 nula, + leve, ++ moderada, +++ intensa, ++++ muito intensa. Os dados do exame anatomopatológico compuseram 10 atributos: a) espaço-porta (EP): infiltrado, fibrose, colestase, ductos proliferados; b) lóbulo (L): células gigantes, esteatose, necrose, colestase celular, colestase canalicular e c) comparação entre colestase-L e colestase-EP.
Outros dados da observação clínica, laboratorial e de imagem, como bilirrubina total e frações, alanina-aminotransferase, eletroforese de proteínas, color-cintilograma hepático realizado com 131I-Rosa-Bengala, não foram utilizados na análise, assim como os relacionados à etiologia da CNP (foram excluídas as com septicemia ou processos infecciosos de outra localização). O diagnóstico final entre AB e HN baseou-se nas características da evolução clínica, com eventual desaparecimento da icterícia e normalização dos níveis séricos da bilirrubina conjugada, ou foi confirmado através de laparotomia exploradora ou necropsia.
2. Estudo da etiopatogenia da CNP (43)
Foram igualmente observadas 108 crianças portadoras de CNP, através de provas específicas para sífilis, toxoplasmose, listeriose, hepatite B, rubéola, herpes simples, citomegalovirose, e também da determinação da alfa-1-antitripsina sérica e dos auto-anticorpos hepáticos. A histopatologia foi avaliada seguindo os métodos anteriormente descritos.
RESULTADOS
1. Diagnóstico diferencial entre AB e HN (42)
Os atributos estudados compuseram 18 variáveis e a análise estatística efetuada revelou serem oito delas as mais decisivas para indicar AB. Desta maneira, os dados obtidos, em ordem decrescente de importância decisória para indicar AB, são os seguintes:
A variável estatística Ø, onde Ø = (c2/n)1/2, sendo c2 = "qui quadrado" de Pearson e n = tamanho da amostra(45), indica o grau de correlação existente entre os critérios adotados e a ocorrência de AB. Vê-se, então, que o maior indicador de AB é a presença de ductos proliferados (EP) com x ³ +++ que acarretou uma correlação de 85% com AB; em segundo lugar, a presença de fibrose (EP) com x ³ +++ que apresentou uma correlação de 79% com a AB; a presença de colestase (EP), com x ³ + mostrou-se correlacionada em 75% com a AB.
A existência destas altas correlações entre os critérios adotados e a AB pode ser visualizada nos histogramas de 1 a 8 mostrados na Figura 1, onde se observa também o forte poder discriminativo desses critérios para distinguir AB da HN. O quadro abaixo evidencia essa capacidade de separação dos critérios apontados acima, ao mostrar percentualmente a quantidade de portadores de AB que foram apartados dos demais.
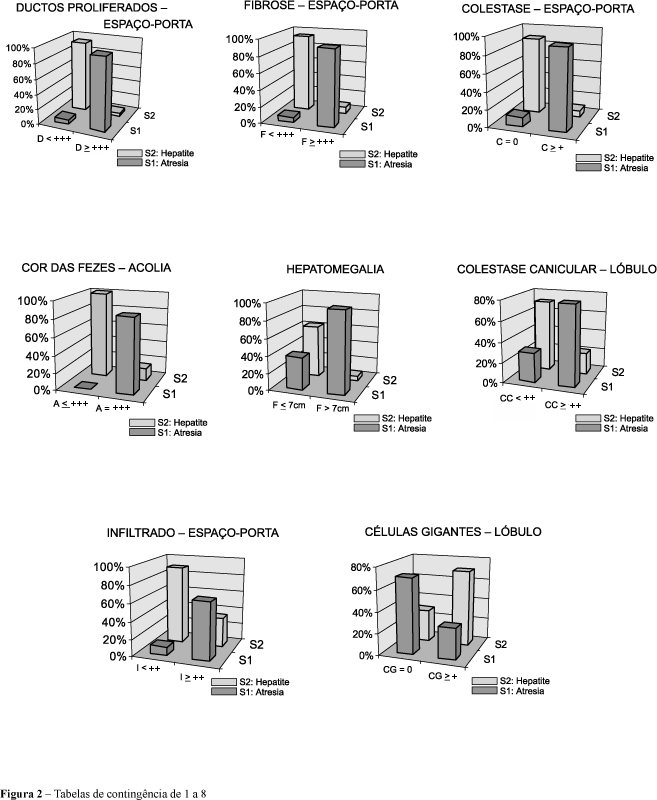
Essas freqüências relativas constantes no quadro acima são indicadoras da probabilidade de realização do evento. O poder de discriminação desses critérios, para distinguir AB da HN, pode ser visualizado através das tabelas de contingência de 1 a 8 da Figura 2.
Vê-se, então, que cada um desses critérios oferece uma indicação, favorável ou desfavorável, de AB. O passo seguinte consiste em buscar um único critério que, englobando os critérios específicos acima apontados, resulte em um indicador altamente confiável.
A avaliação exata da probabilidade do evento ser AB, com base nas oito freqüências relativas do quadro acima, é difícil porque são desconhecidos os vínculos de dependência entre estas variáveis(11, 51). Contudo, uma avaliação aproximada, com precisão satisfatória, pode ser feita atribuindo-se pesos proporcionais às freqüências relativas e considerando-se a soma Pt destes pesos como indicadora de AB. De fato, essa ponderação Pt constitui-se em nova variável aleatória dada por:
Onde:
Exemplo: são apresentadas três crianças hipotéticas, LM, OP e RS, com os seguintes dados clínicos e histopatológicos:
Terão a ponderação total calculada da seguinte maneira:
Essa ponderação total Pt constitui uma variável aleatória cuja distribuição resulta em duas curvas normais: uma para doentes da AB e outra para os de HN.
Pt da AB
Curva normal estimada no nível de confiança de 95% com:
Pt da HN
Curva normal estimada no nível de confiança de 95% com:
Concluiu-se, no trabalho citado(42), que a ponderação total Pt = 360 é o valor crítico que separa a população dos indivíduos com AB daquela dos indivíduos portadores de HN: 99,6% dos indivíduos portadores de AB têm a ponderação total superior ao valor crítico, Pt > 360, e, 99,6% dos indivíduos portadores de HN têm a ponderação total inferior ao valor crítico, Pt < 360.
Estimou-se, então, o intervalo de limites críticos [339, 389] que separa os portadores de AB dos portadores de HN, de tal forma que 99% dos casos de HN apresentam Pt < 339 e 99% dos casos de AB apresentam Pt > 389.
No caso dos exemplos acima citados temos as seguintes indicações:
LM: Pt = 533 como 533 é superior ao limite crítico, 533>389, então a indicação aqui é de AB;
OP: Pt = 186 como 186 é inferior ao limite crítico, 186<339, então a indicação aqui é de HN;
RS: Pt = 386 como 386 cai dentro da região crítica, 339<386<389, a indicação aqui é, por isso, duvidosa, embora o fato de 386 ser superior ao ponto valor crítico VC = 360 sugira tratar-se de AB.
A função densidade de probabilidade desta ponderação total Pt apresenta a forma de duas curvas normais (sinos de Gauss) que se entrecruzam nas caudas, conforme se observa na Figura 3. Neste gráfico estão indicados os limites críticos L1 = 339 e L2 = 389 da região crítica que separa os pacientes, colocando 99% dos portadores de HN no lado esquerdo e 99% dos portadores de AB no lado direito.
2. Etiopatogenia da CNP (43)
A avaliação efetuada revelou:
2.1 Vírus rubéola, em nenhum;
2.2 Vírus herpes simples, em nenhum;
2.3 Listeriose, em nenhum;
2.4 Citomegalovirose, em 2,2%;
2.5 Vírus hepatite B, em 2,4%;
2.6 Toxoplasmose, em 2,8%;
2.7 Deficiência de alfa-1-antitripsina, em 13,1%;
2.8 Sífilis, em 21,1%;
2.9 Auto-anticorpos hepáticos, presentes em 58,4%.
DISCUSSÃO
1. Diagnóstico diferencial entre AB e HN (42)
Em trabalho realizado utilizando metodologia semelhante(22), o estudo da hierarquia dos valores de certos índices revelou, em ordem decrescente: proliferação de ductos biliares, coloração das fezes durante os 10 dias após admissão, peso ao nascer, idade do início da descoloração das fezes, necrose focal dos hepatócitos, trombo biliar no EP, caracteres clínicos do comprometimento hepático, fibrose portal. Diversos autores assinalam hepatomegalia mais acentuada na AB, principalmente se associada ao igualmente progressivo aumento da consistência hepática(2, 35). Em relação aos elementos histopatológicos, é importante considerar a idade da criança na época do exame, pois são alterações que evoluem gradualmente(17). Outro aspecto é o da relativa heterogeneidade histológica da HN, que decorre da sua multiplicidade etiológica, contrastando com quadros mais homogêneos encontrados na AB. Desta maneira, diversos autores(1, 3, 9, 10, 14, 22, 26, 35, 56) descrevem as principais alterações encontradas na HN (células gigantes, degeneração e necrose hepatocelular, desarranjo lobular), contrapondo-se às observadas na AB (proliferação de ductos biliares, colestase intensa com trombos biliares, fibrose, discretas alterações hepatocelulares, raras células gigantes). Coincidiram, em grande parte, com os nossos resultados. O mesmo ocorreu com elaborados estudos posteriores (**** * Professora Adjunta do Departamento de Pediatria da Faculdade de Ciências Médicas da Santa Casa de São Paulo - FCMSCSP. , 31, 47, 59, 60).
Por outro lado, propusemos a utilização de um índice discriminativo global compondo um indicador de grande poder de definição, que pode ser utilizado, desde que as amostras clínicas, colhidas para estudo, admitam as variáveis utilizadas. Contudo, a tendência mais adequada é o progressivo aperfeiçoamento com o acréscimo de novas variáveis.
2. Etiopatogenia da CNP(43)
Diversos autores(15, 32, 33, 38, 50) enfatizam o comprometimento hepático nas infecções congênitas. Contudo, a presença de agente infeccioso relacionado à CNP é variável, às vezes controvertida e dependente das condições epidemiológicas locais (***** * Professora Adjunta do Departamento de Pediatria da Faculdade de Ciências Médicas da Santa Casa de São Paulo - FCMSCSP. , 19, 20, 21, 23, 24, 29, 44, 55, 57, 58). Por outro lado, os estudos sobre a deficiência de alfa-1-antitripsina revelam, algumas vezes, elevada porcentagem de associação(15). Os auto-anticorpos hepáticos, presentes na maioria dos lactentes observados, indicam um envolvimento relevante, podendo ser complexa a interpretação da detecção destes marcadores da atuação e comportamento do sistema imunitário na CNP. Contudo, a recente ampliação das pesquisas relacionadas à genética molecular, organogênese, virologia e imunologia acarreta importante tendência a uma mais precisa definição etiológica da CNP (***** * Professora Adjunta do Departamento de Pediatria da Faculdade de Ciências Médicas da Santa Casa de São Paulo - FCMSCSP. , 4, 5, 6, 8, 12, 16, 18, 25, 30, 36, 40, 41,48, 49, 52, 53, 54).
CONCLUSÕES
Considera-se que o encaminhamento precoce e a investigação rápida da etiologia e do diagnóstico diferencial entre HN e AB são objetivos fundamentais no manejo da CNP, determinando conduta mais adequada e o sucesso evolutivo(****** * Professora Adjunta do Departamento de Pediatria da Faculdade de Ciências Médicas da Santa Casa de São Paulo - FCMSCSP. , 5, 6, 7, 28, 34, 46).
As oito variáveis mais decisivas obtidas como indicadoras diferenciais entre HN e AB, permanecem como índices fundamentais, auxiliando, em conjunto com novos métodos diagnósticos(5, 6, 13, 37, 39), na composição de uma estratégia multifatorial cada vez menos invasiva e mais precisa.
Prado ETML, Araujo M de F, Campos JVM. Prolonged neonatal cholestasis: a prospective study. Arq Gastroenterol, São Paulo, 36(4):185-194, 1999.
ABSTRACT ¾ Due to the urgency in choosing either clinical treatment or immediate surgical intervention, the study of the prolonged neonatal cholestasis involves two basic aims: the differential diagnosis between biliary atresia and neonatal hepatitis and the research into the associated etiological agents. So, in a prospective trial carried out in the 70´s, 77 children with prolonged neonatal cholestasis were studied in order to establish the differential diagnosis between biliary atresia and neonatal hepatitis, followed by the evaluation of 108 children towards a pathogenesis of the prolonged neonatal cholestasis. The results of the differential diagnosis showed that within 18 items examined only 8 proved to be good biliary atresia indicators. They are as follows (in decreasing order): ductular proliferation (portal tracts), fibrosis (portal tracts), cholestasis (portal tracts), stools colour ¾ acholia, hepatomegaly, canalicular cholestasis (lobule), infiltrate (portal tracts), giant cells (lobule). These eight items were then gathered in a sole indicator of great discriminative power, with a confidence level of 99%. The figures regarding the pathogenesis are: rubella virus 0%, herpes simplex virus 0%, listeriosis 0%, cytomegalovirus 2.2%, hepatitis B virus 2.4%, toxoplasmosis 2.8%, alpha-1-antitrypsin deficiency 13.1%, syphilis 21.1%, autoantibodies against the liver 58.4%. Such work thus revealed that those eight most important factors when differentiating biliary atresia from neonatal hepatitis remain as fundamental indicators and, when employed alongside other diagnostic methods, can help in the assembling of a multifactorial strategy less and less invasive and more precise. The pathogenic study, with its heavy dependency on time and place, has become more complete with the introduction of new diagnostic methods, evolving to the ideal progressive reduction of idiopathic processes.
HEADINGS ¾ Cholestasis. Hepatitis, neonatal, etiology. Biliary atresia, etiology. Biopsy. Infant.
** Professora Adjunta do Departamento de Ciências Patológicas da FCMSCSP.
*** Homenagem póstuma ¾ ao valioso apoio e à excelência da orientação nas Teses de Mestrado e de Doutorado. Departamento de Pediatria ¾ FCMSCSP.
Endereço para correspondência: Dra. Elizabeth T.M. Livramento Prado - Rua Herculano de Freitas, 207 - apto.61 - 01308-020 - São Paulo, SP.
**** Patrício FRS. Conferência: "Diagnóstico anatomopatológico da colestase neonatal". 1ª Conferência Internacional de Gastroenterologia, Hepatologia e Nutrição em Pediatria. São Paulo, 19/6/1999.
***** Porta G. Seminário: "Hepatite neonatal", Curso de Pós-Graduação em Medicina, área de concentração em Pediatria, Disciplina Gastroenterologia Pediátrica, FCMSCSP. São Paulo, 23/4/1998.
****** Porta G. Seminário: "Hepatite neonatal", Curso de Pós-Graduação em Medicina, área de concentração em Pediatria, Disciplina Gastroenterologia Pediátrica, FCMSCSP. São Paulo, 23/4/1998.
- 1. Alagille D, Kremp L. Les ictères du nouveau-né en dehors de l'incompatibilité foeto-maternelle: données statistiques. Rev Int Hepatol, 14:539, 1964.
- 2. Alagille D, Odièvre M. Cholestases du nouveau-né et du nourrisson. In: Alagille D, Odièvre M. Maladies du foie et des voies biliaires chez l'enfant. Paris, Flammarion, 1978. p.61-77.
- 3. Alagille D. Cholestasis in the first three months of life. Prog Liv Dis, 6:471, 1979.
- 4. Balistreri WF. Neonatal cholestasis ž medical progress. J Pediatr, 106:171, 1985.
- 5. Balistreri WF, Grand R, Hoofnagle JH, Suchy FJ, Ryckman FC, Perlmutter DH, Sokol RJ. Biliary atresia: current concepts and research directions. Summary of a symposium. Hepatology, 23:23, 1996.
- 6. Bates MD, Bucuvalas JC, Alonso MH, Ryckman FC. Biliary atresia: pathogenesis and treatment. Semin Liver Dis, 18:281,1998.
- 7. Bernard O. Diagnostic précoce des ictères cholestatiques chez le nouveau-né. Arch Pédiatr, 5:1031, 1998.
- 8. Bezerra JA. Liver development: a paradigm for hepatobiliary disease in later life. Semin Liver Dis, 18:203, 1998.
- 9. Brough AJ, Bernstein NJ. Liver biopsy in the diagnosis of infantile obstrutive jaundice. Pediatrics, 43:519, 1969.
- 10. Brough AJ, Bernstein NJ. Conjugated hyperbilirrubinemia in early infancy. A reassessment of liver biopsy. Hum Pathol, 5:507, 1974.
- 11. Campos H. Estatística experimental não-paramétrica Piracicaba, E.S.E. "Luiz de Queiroz", Universidade de São Paulo,1979.
- 12. Costa AM, Pegado CS, Porto, LC. Quantification of the intrahepatic biliary tree during human fetal development. Anat Rec, 251:297, 1998.
- 13. Choi SO, Park WH, Lee HJ. Ultrasonographic "triangular cord": the most definitive findings for noninvasive diagnosis of extrahepatic biliary atresia. Eur J Pediatr Surg, 8:12,1998.
- 14. Craig JM, Landing B. Form of hepatitis in neonatal period simulating biliary atresia. Arch Dis Child, 90:299,1952.
- 15. Danks DM, Campbell IJ, Rogers J, Smith AL. Studies of the aetiology of neonatal hepatitis and biliary atresia. Arch Dis Child, 52:360, 1977.
- 16. Desmet VJ. Cholangiophaties: past, present and future. Semin Liver Dis, 7:67, 1987.
- 17. Desmet VJ, Callea F. Cholestatic syndromes of infancy and childhood. In: Zakim D, Boyer TD, ed. Hepatology: a textbook of liver disease. 3.ed. Philadelphia. W.B. Saunders, 1996. p.1649-98.
- 18. Dillon P, Belchis D, Tracy T, Cilley T, Hafer L, Krummel T. Increased expression of intercelular adhesion molecules in biliary atresia. Am J Pathol, 145:263, 1994.
- 19. Dowle WR, Ferreira W, Salles-Gomes LF, King D, Kourany M, Madalengoitia J, Pearson E, Swanston WH, Tosi HC, Vilches AM. WHO collaborative study on the sero-epidemiology of rubella in Carebbean and Middle and South American populations in 1968. Bull WHO, 42:419, 1970.
- 20. Drut R, Drut RM, Gomez MA, Cueto, RE, Lojo MM. Presence of human papillomavirus in extrahepatic biliary atresia. J Pediatr Gastroenterol Nutr, 27:530,1998.
- 21. Drut R, Gomez MA, Drut RM, Cueto RE, Lojo M. Virus papiloma humano, hepatitis gigantocelular neonatal y atresia de vias biliares. Acta Gastroenterol Latinoam, 28:27, 1998.
- 22. Eliot N, Odièvre M, Hadehouel M, Hill C, Flamant R. Analyse statistique des données cliniques, biologiques et histologiques dans 288 observations de cholestase neonatale. Arch Fr Pédiatr, 34:213, 1977.
- 23. Fischler B, Ehrnst A, Forsgren M, Orvell C, Nemeth A. The viral association of neonatal cholestasis in Sweden: a possible link between cytomegalovirus infection and extrahepatic biliary atresia. J Pediatr Gastroenterol Nutr, 27:57,1998.
- 24. Jevon GP, Dimmick JE. Biliary atresia and cytomegalovirus: a DNA study. AADE Ed J, 2:11, 1999.
- 25. Jurado A, Jara P, Camarena C, Hierro L, Lahoz C, Palomino P. Is extrahepatic biliary atresia an HLA-associated disease? J Pediatr Gastroenterol Nutr, 25:557, 1997.
- 26. Kasai M, Yakovac WC, Koop CE. Liver in congenital biliary atresia and neonatal hepatitis: a histopathologic study. Arch Pathol, 74:152, 1962.
- 27. Kasai M. Treatment of biliary atresia with special reference to hepatic portoenterostomy and its modifications. Prog Pediatr Surg, 6:5, 1974.
- 28. Keffler S, Kelly DA, Powell JE, Green A. Population screening for neonatal liver disease: a feasibility study. J Pediatr Gastroenterol Nutr, 27:306, 1998.
- 29. Kiss MHB. Diagnóstico diferencial das hiperbilirrubinemias diretas nos primeiros quatro meses de vida. São Paulo, 1982. [Tese de Doutoramento ž Faculdade de Medicina da Universidade de São Paulo].
- 30. Lamiraux T, Le Bail B, Boussarie L, Fabre M, Vergnes P, Bernard O, Gautier F, Bioulac-Sage P, Rosenbaum J. Expression of collagens type l e lV, osteonectin and transforming growth factor beta-1 (TGF b1) in biliary atresia and paucity of intrahepatic bile ducts during infancy. J Hepatol, 31:248, 1999.
- 31. Lai MW, Chang MH, Hsu SC, Hsu HC, Su CT, Kau CL, Lee CY. Differential diagnosis of extrahepatic biliary atresia from neonatal hepatitis: a prospective study. J Pediatr Gastroenterol Nutr, 18:121, 1994.
- 32. Löwy G, Meilman I, Serapião CJ, Amoedo A. Sífilis congênita precoce. An Bras Dermatol, 52:257, 1977.
- 33. Marret S, Buffet-Janvresse C, Metayer J, Fessard C. Herpes simplex hepatitis with chronic cholestasis in a newborn. Acta Paediatr, 82:321,1993.
- 34. Miele-Vergani G, Portman B, Howard ER, Mowat AP. Late referral for biliary atresia ž missed opportunities for effective surgery. Lancet, 1:421, 1989.
- 35. Mowat AP, Psacharopoulos HT, Williams R. Extrahepatic biliary atresia versus neonatal hepatitis. Arch Dis Child, 51:763, 1976.
- 36. Park WH, Kim SP, Park KK, Choi SO, Lee HJ, Kwon KY. Eletron microscopic study of the liver with biliary atresia and neonatal hepatitis. J Pediatr Surg, 31:367, 1996.
- 37. Park WH, Choi SO, Lee HJ, Kim SP, Zeon SK, Lee SL. A new diagnostic approach to biliary atresia with emphasis on the ultrasonographic triangular cord sign: comparison of ultrasonography, hepatobiliary scintigraphy, and liver needle biopsy in the evaluation of infantile cholestasis. J Pediatr Surg, 32:1555, 1997.
- 38. Passos AO, Fernandes MIM, Galvão LC, Zucoloto S, Sawamura R, Goldani HAS. Colestase neonatal e infecção por citomegalovirus.: formas de apresentação clínica e histopatológica. J Pediatr, 72:159, 1996.
- 39. Peng SS, Li YW, Chang MH, Ni YH, Su CT. Magnetic resonance cholangiography for evaluation of cholestatic jaundice in neonates and infants. J Formos Med Assoc, 97:698,1998.
- 40. Petersen C, Grashoff S, Luciano L. Diverse morphology of biliary atresia in an animal model. J Hepatol, 28:137,1998.
- 41. Petersen C, Kuske M, Bruns E, Biermanns D, Wussow PV, Mildenberger H. Progress in developing animal models for biliary atresia. Eur J Pediatr Surg, 8:137, 1998.
- 42. Prado ETML. Contribuição ao estudo da colestase prolongada do lactente. São Paulo, 1980. [Dissertação ž Mestrado ž Instituto Brasileiro de Estudos e Pesquisas em Gastroenterologia].
- 43. Prado ETML. Contribuição ao estudo da etiopatogenia da colestase prolongada do lactente. São Paulo, 1982. [Tese ž Doutorado Faculdade de Ciências Médicas da Santa Casa de São Paulo].
- 44. Proença NG, Freitas THP. A sífilis na atualidade no Brasil. Rev Assoc Med Bras, 27:43, l981.
- 45. Rummel RJ. Applied factor analysis Evanston, Northwestern University Press, 1977.
- 46. Santos JL, Silveira TR, Almeida H, Carvalho PA, Cerski CT. Colestase neonatal ž atraso no encaminhamento de crianças para diagnóstico diferencial. J Pediatr, Rio de Janeiro, 73:32, 1997.
- 47. Santos JL, Almeida H, Cerski CTS, Silveira TR. Histopathological diagnosis of intra- and extrahepatic neonatal cholestasis. Braz J Med Biol Res, 31:911, 1998.
- 48. Santos JL, Silveira TR, Cerski CT, Almeida H. Síndrome de polisplenia associada à hepatite neonatal idiopática. J Pediatr, 74:59, 1998.
- 49. Schreiber RA, Kleinman RE. Genetics, immunology, and biliary atresia: an opening or a diversion? J Gastroenterol Nutr, 16:111,1993.
- 50. Seeliger HPR. Listeriosis in man. In: Seeliger HPR. Listeriosis. 2.ed. Basel, S.Karger, 1961. p.112-204.
- 51. Siegel S. Nonparametric statistics for the behavioral sciences New York, McGraw-Hill, 1956.
- 52. Silveira TR, Salzano FM, Howard ER, Mowat AP. Congenital strutural abnormalities in biliary atresia: evidence for etiopathogenic heterogeneity and therapeutic implications. Acta Paediatr Scand, 80:1192, 1991.
- 53. Silveira TR, Salzano FM, Howard ER, Mowat AP. Extrahepatic biliary atresia and twinning. Braz J Med Biol Res, 24:67, 1991.
- 54. Silveira TR, Salzano FM, Donaldson PT, Mieli-Vergani G, Howard ER, Mowat AP. Association between HLA and extrahepatic biliary atresia. J Pediatr Gastroenterol Nutr, 16:114, 1993.
- 55. Steele CM, Marshall CM, Lloyd RE, Randolph VE. Reovirus 3 not detected by reverse transcriptase-mediated polymerase chain reaction analysis of preserved tissue from infants with cholestatic liver disease. Hepatology, 21:697, 1995.
- 56. Stokes JR, Wolman IJ, Blanchard MC, Farquhar JD. Viral hepatitis in the newborn: clinical features, epidemiology and pathology. Am J Dis Child, 82:213, 1951.
- 57. Tyler KL, Sokol RJ, Oberhaus SM, Lee M, Karrer FM, Narkewicz MR, Tyson RW, Murphy JR, Low R, Brown WR. Detection of reovirus RNA in hepatobiliary tissues from patients with extrahepatic biliary atresia and choledochal cysts. Hepatology, 27:1475, 1998.
- 58. Wehba J, Fagundes Neto U, Patricio FR, Machado NL, Nassif MK. Síndrome colestática prolongada do lactente jovem. Estudo de 57 casos. J Pediatr, 54:156, 1983.
- 59. Zerbini MCN. Análise semi-quantitativa e quantitativa das variáveis histopatológicas no diagnóstico diferencial das formas intra e extra-hepáticas da síndrome colestática do recém-nascido. São Paulo,1985. [Tese de Doutorado ž Faculdade de Medicina da Universidade de São Paulo].
- 60. Zerbini MCN, Gallucci SD, Maezono R, Ueno CM, Porta G, Maksoud JG, Gayotto LC. Liver biopsy in neonatal cholestasis: a review on statiscal grounds. Mod Pathol, 10:793, 1997.
Datas de Publicação
-
Publicação nesta coleção
15 Jul 2003 -
Data do Fascículo
Dez 1999