Resumos
Objetivo — Estudar a proliferação celular através das contagens das AgNORs (regiões argirofílicas organizadoras nucleolares) nos tecidos de câncer gástrico e/ou da mucosa normal adjacente e correlacionar com as variáveis clínico-patológicas. Casuística e Método - Foram estudados 34 casos de adenocarcinoma gástrico, 23 do tipo intestinal e 11 do tipo difuso de Lauren. A coloração das AgNORs foi realizada em cortes histológicos e a análise quantitativa foi realizada pela contagem de um total de 100 núcleos de células neoplásicas e 100 de células da mucosa de aspecto normal. Resultados - O número de AgNORs nos núcleos das células normais variou entre 1 e 2 pontos castanho-escuros, enquanto nos núcleos das células neoplásicas estes eram numerosos, pequenos, agregados ou únicos e maiores. A média das contagens das AgNORs nos núcleos das células neoplásicas (3,86) foi significativamente maior do que nos núcleos das células da mucosa gástrica normal (1,25). Esta diferença foi também observada entre tumores do tipo intestinal (4,43) e difuso (2,58). Não foram observadas correlação entre as médias das contagens das AgNORs por núcleo e o sexo ou a idade dos pacientes. Conclusão - A contagem das AgNORs pode ser utilizada como marcador de atividade proliferativa, podendo auxiliar no diagnóstico de câncer.
Região organizadora do nucléolo; Neoplasias gástricas
Objective — To study the proliferative activity of AgNORs (argyropholic nucleolar organizer region) in gastric cancer tissue and in the adjacent normal tissue and correlate with the clinical and pathological parameters. Material and Methods — Thirty four formalin-fixed paraffin-embedded tissues sections of patients with adenocarcinoma of the stomach were analysed retrospectively, being 23 of intestinal and 11 of diffuse type of Lauren. The AgNORs can be detected by a specific silver staining and the number de AgNORs was counted in 100 nucleus of tumoral cells and in 100 nucleus of the adjacent normal tissue. Results - The tumoral cells had numerous, smaller, aggregated or one solitary and bigger AgNORs in the nuclei, while the normal cells had one or two AgNORs by nuclei. A significant difference was found between the mean numbers of AgNORs in the nuclei of tumor (3.86) and the normal tissue (1.25). There was also a significant difference between intestinal (4.43) and diffuse type (2.58) means. No significant correlation was found between mean AgNOR count and sex or age of the patients. Conclusions - The quantification of AgNORs can be used as a marker of proliferative activity, helping on the diagnosis of cancer.
Nucleolus organizer region; Stomach neoplasms
ARTIGO ORIGINAL / ORIGINAL ARTICLE
AgNOR EM CÂNCER GÁSTRICO
Celina Tizuko Fujiyama OSHIMA* * Pesquisadora Assistente. Divisão de Oncologia Clínica e Laboratorial. Fundação Oncocentro de São Paulo. e Nora Manoukian FORONES** ** Professora Adjunta. Disciplina de Gastroenterologia da Universidade Federal de São Paulo - UNIFESP/EPM.
RESUMO Objetivo Estudar a proliferação celular através das contagens das AgNORs (regiões argirofílicas organizadoras nucleolares) nos tecidos de câncer gástrico e/ou da mucosa normal adjacente e correlacionar com as variáveis clínico-patológicas. Casuística e Método - Foram estudados 34 casos de adenocarcinoma gástrico, 23 do tipo intestinal e 11 do tipo difuso de Lauren. A coloração das AgNORs foi realizada em cortes histológicos e a análise quantitativa foi realizada pela contagem de um total de 100 núcleos de células neoplásicas e 100 de células da mucosa de aspecto normal. Resultados - O número de AgNORs nos núcleos das células normais variou entre 1 e 2 pontos castanho-escuros, enquanto nos núcleos das células neoplásicas estes eram numerosos, pequenos, agregados ou únicos e maiores. A média das contagens das AgNORs nos núcleos das células neoplásicas (3,86) foi significativamente maior do que nos núcleos das células da mucosa gástrica normal (1,25). Esta diferença foi também observada entre tumores do tipo intestinal (4,43) e difuso (2,58). Não foram observadas correlação entre as médias das contagens das AgNORs por núcleo e o sexo ou a idade dos pacientes. Conclusão - A contagem das AgNORs pode ser utilizada como marcador de atividade proliferativa, podendo auxiliar no diagnóstico de câncer.
DESCRITORES Região organizadora do nucléolo. Neoplasias gástricas.
INTRODUÇÃO
O câncer gástrico é doença que ocorre mais freqüentemente a partir da quinta década da vida e, segundo trabalho colaborativo da Fundação Oncocentro de São Paulo (FOSP) e Fundação Sistema Estadual de Análise de Dados (SEADE), verificaram-se que no Estado de São Paulo o câncer de estômago é a segunda causa de morte por neoplasia(4).
Histologicamente, os carcinomas gástricos podem ser classificados em dois tipos(11): o intestinal, que é o mais comum em populações de alto risco para o câncer gástrico e está associado a fatores ambientais(12, 17), e o difuso, que não guarda relação com a atrofia da mucosa gástrica e acomete com maior freqüência mulheres e indivíduos mais jovens.
Pesquisas histopatológicas nestes tecidos envolvem, direta ou indiretamente, a avaliação da proliferação celular, diferenciação celular e a regulação destes mecanismos.
No câncer gástrico, como em outros cânceres, têm sido realizados vários tipos de medidas da atividade proliferativa, como a contagem da mitose, índice de marcação com timidina 3H, índice de marcação com bromo deoxiuridina, análise de citometria de fluxo, contagens de AgNORs e a expressão de antígenos relacionados à proliferação celular, como o Ki-67 e o PCNA.
O termo regiões organizadoras nucleolares ou NORs (do inglês, "nucleolar organizer regions") é utilizado para descrever regiões constituídas de fragmentos de cromossomos em torno das quais se formam os nucléolos no final da mitose. Estas regiões correspondem a alças do DNA contendo genes responsáveis pela transcrição do RNA ribossômico, de 18S e 28S, situados no nucléolo da célula(7, 16) e por possuírem reatividade com a prata, foram chamadas de AgNORs.
No homem, estas regiões correspondem a constrições secundárias e se localizam no braço curto dos cromossomos acrocêntricos 13, 14, 15, 21 e 22. Como as NORs estão associadas aos cromossomos acrocêntricos, pensou-se, inicialmente, que estivessem relacionadas a ploidia. Entretanto, estudos correlacionando as NORs com as variáveis histológicas convencionais(20), o estudo do núcleo interfásico através dos métodos citogenéticos(9), a cinética celular(3), a imunoreatividade do Ki-67(6) e a citometria de fluxo(1), sugerem que as AgNORs estejam associadas principalmente à proliferação celular.
PLOTON et al.(18) padronizaram uma versão modificada da técnica de coloração pela prata, realizando a reação em uma só fase, à temperatura ambiente (20 0C) e penumbra. Tal modificação permitiu que estas regiões fossem vistas em cortes de tecido em parafina, fixados em formalina e incluídas em parafina tanto em células em metáfase, como em interfase.
Este estudo teve por objetivo analisar a proliferação celular através das contagens das AgNORs nos tecidos de câncer gástrico e/ou da mucosa normal adjacente e as possíveis relações com as variáveis clínico-patológicas.
CASUÍSTICA E MÉTODOS
Foram analisados, retrospectivamente, 34 casos de câncer gástrico utilizando blocos em parafina obtidos dos arquivos dos serviços de Anatomia Patológica do Hospital São Paulo da Universidade Federal de São Paulo/UNIFESP/EPM, Santa Casa de Misericórdia de São Paulo e Hospital São Judas Tadeu da Fundação Pio XII de Barretos, SP.
Dos 34 adenocarcinomas gástricos analisados, 25 eram de pacientes do sexo masculino e 9 do sexo feminino. Dezenove tumores eram de estádios menos agressivos (I + II), enquanto 10, mais avançados (III + IV). Segundo a classificação de LAUREN(11), 23 tumores (67,65%) eram do tipo intestinal e 11 (32,35%) do tipo difuso. Em relação ao grau histológico dos tumores, 22 (64,70%) eram diferenciados e a localização predominante foi o antro gástrico.
Os tecidos foram fixados em formalina e processados rotineiramente pelo método de inclusão em parafina, para análise histológica, no laboratório de patologia de cada Serviço. Portanto, não foi possível a padronização prévia da fixação do tecido.
A coloração das AgNORs foi realizada em cortes histológicos com 3 mm de espessura. A solução de incubação foi preparada dissolvendo-se 0,2 g de gelatina em 10 mL de água destilada e desionizada a 60 oC, acrescentando-se 100 mL de ácido fórmico à solução fria. Esta solução foi misturada com outra de nitrato de prata 30% (modificado de PLOTON et al.(18)), na proporção de 1:2. A solução resultante foi gotejada sobre o corte histológico e incubado por 30 minutos a 37 oC em câmara escura. Após este tempo, as lâminas foram lavadas em água desionizada, desidratadas e montadas em meio sintético.
Água destilada e desionizada foi utilizada para o preparo das soluções, reações e lavagens, a fim de reduzir-se a coloração de fundo. Os cortes histológicos não foram contracorados e como resultado, obtiveram-se os cortes corados em tom amarelo-acastanhado claro e os AgNORs como pontos negros ou castanho-escuros.
A análise quantitativa das AgNORs foi realizada por microscopia óptica, onde um total de 100 núcleos de células neoplásicas e 100 núcleos de células da mucosa não-neoplásica, de aspecto normal, ao acaso, foram analisadas com aumento de 1.000 vezes em um microscópio Nikon. As células em "anel de sinete" foram excluídas da contagem.
Foram selecionados os núcleos com maior número de pontos corados, não superpostos, sendo realizada busca extensa em grandes áreas e para que não houvesse repetição dos campos observados.
A escala de coloração para visualização dos pontos das AgNORs foi selecionada individualmente, após aumento do contraste, até o momento em que os pontos das AgNORs fossem facilmente identificados como pontos negros ou castanho-escuros dentro do núcleo. Esses pontos podiam se apresentar isolados e arredondados, aglomerados, formando cachos ou dispersos pelo núcleo.
Análise Estatística
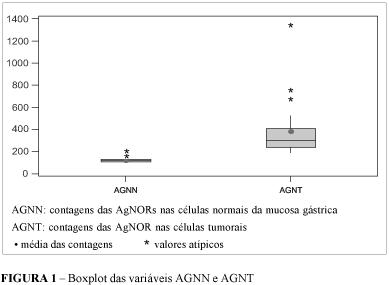
O teste t para duas amostras independentes foi aplicado para verificação da igualdade entre as médias dos dois grupos (AGNN contagens das AgNORs em núcleos das células normais da mucosa gástrica e AGNT contagens das AgNORs em núcleos das células tumorais). Adotou-se um nível de significância de 0,05 (5%). Níveis descritivos (P) inferiores a esse valor foram considerados significativos.
RESULTADOS
A média e a mediana das contagens das AgNORs nas células neoplásicas (385,7) foi significativamente mais alta do que nas células normais (124,68) da mucosa gástrica (P <0,001*) (Tabela 1). Portanto, a média de AgNORs no núcleo neoplásico e normal foi de 3,86 e 1,25, respectivamente.
A Figura 1 representa o "boxplot" das variáveis AGNT e AGNN. A parte inferior da caixa indica o primeiro quartil, onde 25% das contagens estão abaixo do valor de Q1 e a parte superior, o terceiro quartil, onde 75% das contagens estão abaixo do valor de Q3. A linha horizontal interna da caixa representa a mediana. Valores maiores que 1,5 (Q3-Q1), acima ou abaixo da caixa são valores atípicos (ou possíveis "outliers"). As linhas verticais representam o maior e o menor valor observado. As médias (representadas no "boxplot" por um ponto) das contagens das AGNT e AGNN foram estatisticamente diferentes (teste t para duas amostras independentes, P <0,001*).
Observou-se diferença estatística entre a média das contagens nas células tumorais do tipo intestinal (443,1) e difuso (258,3) (P = 0,0075) (Figura 2). Não se observaram diferenças entre as contagens das AgNORs nas células normais e nas células neoplásicas, nos dois sexos, e nas faixas etárias acima ou abaixo de 50 anos. Não se observou, também, diferença entre o número de AgNORs entre os doentes estádios I e II versus IIII e IV (P >0,05).
Observa-se na fotomicrografia da Figura 3, uma glândula gástrica normal, com 1 a 2 AgNORs intranucleares de cor castanho-escuro e nas fotomicrografias das Figuras 4 e 5, glândulas neoplásicas contendo AgNORs intranucleares corados em castanho-escuro, isolados e maiores, pequenos e numerosos ou agrupados.
DISCUSSÃO
O interesse na suplementação dos métodos tradicionais usados para avaliar o prognóstico do câncer tem levado ao desenvolvimento de diferentes tipos de marcadores tumorais. A descoberta destes marcadores permitiria discriminar com maior clareza pacientes que seriam favorecidos com a cirurgia, cirurgia associada à quimioterapia, tratamentos mais agressivos ou protocolos experimentais.
CROCKER et al.(2) sugeriram que a técnica de AgNOR teria utilidade prática em patologia, para demonstração de potencial neoplásico e para avaliação de prognóstico e agressividade de neoplasias malignas. Em vista disso, a quantificação das AgNORs foi introduzida em histopatologia como marcador da atividade celular e nucleolar(14).
A análise da expressão das AgNORs pode ser realizada pela contagem e pelo padrão de distribuição dos pontos negros dentro do núcleo na microscopia óptica e pela medida de sua área por análise de imagem ou pelo cálculo de coeficientes que relacionam esses dois critérios(13).
As AgNORs variam em tamanho e forma, de acordo com a transcrição nucleolar, e estão intimamente relacionadas ao ciclo celular, à proliferação e à ploidia(19).
Observaram-se que as AgNORs se apresentaram como pontos intranucleares castanhos-escuro isolados e grandes, pequenos e numerosos e aglomerados.
Evitou-se a análise em regiões com representações incompletas do núcleo e quando os pontos apareciam sobrepostos, de forma aglomerada, dificultando a visualização.
Núcleos de células, supostamente normais, apresentaram 1 a 2 pontos castanho-escuros, enquanto os núcleos das células neoplásicas apresentaram número variável de pontos com diferentes tamanhos e formas.
Apesar de não terem sido realizadas contagens das AgNORs nos núcleos das células da região de transição entre mucosa normal e neoplásica, aparentemente normais em coloração de hematoxilina-eosina, observaram-se que estes núcleos apresentavam padrões de AgNOR intermediários, aproximando-se na maioria das vezes mais ao padrão neoplásico do que ao normal, semelhante ao observado por IRAZUSTA et al.(8).
Utilizando a contagem dos pontos negros dentro do núcleo, encontrou-se resultado semelhante ao de outros autores(5, 10, 15) que também observaram maior número de AgNORs no tecido tumoral. A média das contagens das AgNORs em núcleos das células neoplásicas (média de 3,85) foi superior a de células normais (média de 1,25). Esta diferença foi estatisticamente significativa (P <0,001).
Segundo TREVISAN(21), se o ciclo celular estiver acelerado, a coloração pela prata vai demonstrar vários pontos negros nos núcleos, indicando, indiretamente, os locais onde os genes do RNA ribossômico estão ativos. As observações deste estudo mostraram que núcleos de células normais, aparentemente em repouso, apresentaram 1 a 2 pontos castanho-escuro, enquanto os núcleos das células neoplásicas, com atividade nuclear aumentada, um número variável de pontos com diferentes tamanhos e formas.
A diferença observada entre as contagens nas células tumorais do tipo intestinal e difuso sugerem que tumores bem diferenciados possuem atividade proliferativa mais intensa. Por outro lado, os núcleos dos tumores do tipo intestinal são maiores, facilitando a contagem de AgNORs.
Apesar de observar-se uma atividade proliferativa intensa, isto não indica o tempo de duplicação das células, podendo as células tumorais do tipo intestinal ter o seu tempo de duplicação superior ao do tipo difuso.
Assim como ÖFNER et al.(14), chama-se a atenção para a qualidade da coloração como fator limitante na reprodução dos resultados da contagem das AgNORs.
Sugere-se após estas observações que estudo mais acurado das áreas de displasias através do uso da técnica de AgNOR possa auxiliar na detecção das lesões malignas precoces e que possa ser utilizada como marcador de atividade proliferativa no diagnóstico do câncer gástrico.
AGRADECIMENTO
Ao Prof. Dr. Kiyoshi Iriya do Departamento de Patologia da Faculdade de Medicina da Universidade de São Paulo, pela cuidadosa revisão quanto à classificação de Lauren, de todas as lâminas escolhidas para este trabalho.
Oshima CTF, Forones NM. AgNOR in cancer of the stomach. Arq Gastroenterol 2001;38(2):89-93.
ABSTRACT Objective To study the proliferative activity of AgNORs (argyropholic nucleolar organizer region) in gastric cancer tissue and in the adjacent normal tissue and correlate with the clinical and pathological parameters. Material and Methods ¾ Thirty four formalin-fixed paraffin-embedded tissues sections of patients with adenocarcinoma of the stomach were analysed retrospectively, being 23 of intestinal and 11 of diffuse type of Lauren. The AgNORs can be detected by a specific silver staining and the number de AgNORs was counted in 100 nucleus of tumoral cells and in 100 nucleus of the adjacent normal tissue. Results - The tumoral cells had numerous, smaller, aggregated or one solitary and bigger AgNORs in the nuclei, while the normal cells had one or two AgNORs by nuclei. A significant difference was found between the mean numbers of AgNORs in the nuclei of tumor (3.86) and the normal tissue (1.25). There was also a significant difference between intestinal (4.43) and diffuse type (2.58) means. No significant correlation was found between mean AgNOR count and sex or age of the patients. Conclusions - The quantification of AgNORs can be used as a marker of proliferative activity, helping on the diagnosis of cancer.
HEADINGS Nucleolus organizer region. Stomach neoplasms.
Recebido em 17/4/2000.
Aprovado em 7/8/2000.
Endereço para correspondência: Dra. Nora Manoukian Forones - Rua Botucatu, 740, 2o andar - 04023-900 - São Paulo, SP. e-mail: nora@gastro.epm.br
- 1. Crocker J, Macartney JC, Smith PJ. Correlation between DNA flow cytometric and nucleolar organizer region data in non-Hodgkin's lymphomas. J Pathol 1988;154:151-6.
- 2. Crocker J, Boldy DAR, Egan MJ. How should we count AgNORs? Proposals for a standardized approach. J Pathol 1989;158:185-8.
- 3. Derenzini M, Pession A, Farabegoli F, Trerè D, Badiali M, Dehan P. Relationship between interphasic nucleolar organizer regions and growth rate in two neuroblastoma cell lines. Am J Pathol 1989;134:925-32.
- 4. Fonseca LAM, Mameri CP. Mortalidade por câncer no Estado de São Paulo. Ed. Prov. São Paulo: Fundação Sistema Estadual de Análise de Dados SEADE/Fundação Oncocentro de São Paulo; 1994.
- 5. Giuffre G, Caruso RA, Barresi G, Tuccani G. Prognostic significance of standardized AgNOR analysis in early and advanced gastric carcinomas. Virchows Arch 1998;433:261-6.
- 6. Hall PA, Crocker J, Watts A, Stansfeld AG. A comparison of nucleolar organizer region staining and Ki-67 immunostaining in non-Hodgkin's lymphoma. Histopathology 1988;12:373-81.
- 7. Hsu TC, Spirito SE, Pardue ML. Distribution of 18+28S ribosomal genes in mammalian genomes. Chromosoma 1975;53:25-36.
- 8. Irazusta SP, Vassallo J, Magna LA, Metze K, Trevisan M. The value of PCNA and AgNOR staining in endoscopic biopsies of gastric mucosa. Pathol Res Pract 1998;194:33-9.
- 9. Jan-Mohamed RM, Armstrong SJ, Crocker J, Leyland MJ, Hulten MA. The relationship between number of interphase NORs and NOR-bearing chromosomes in non-Hodgkin's lymphoma. J Pathol 1989;158:3-7.
- 10. Kakeji Y, Maehara Y, Tomoda M, Kabashima A, Ohmori M, Oda S, Ohno S, Sugimachi I. Long-term survival of patients with stage IV gastric carcinoma. Cancer 1998;82:2307-11.
- 11. Lauren P. The two histological main types of gastric carcinoma: diffuse and so-called intestinal-type carcinoma: an attempt at a histoclinical classification. Acta Pathol Microbiol Scand 1965;64:31-49.
- 12. Muñoz N, Correa P, Cuello C, Duque E. Histologic types of gastric cancer in high and low-risk areas. Int J Cancer 1968;3:809-18.
- 13. Öfner D, Bankfalvi A, Riehemann K, Bier B, Böcker W, Schmid KW. Wet autoclave pretreatment improves the visualization of silver stained nucleolar organizer region associated proteins (AgNORs) in routinely formalin-fixed and paraffin-embedded tissues. Mod Pathol 1994;7:946-50.
- 14. Öfner D, Riedmann B, Maier H, Hittmair A, Rumer A, Tötsch M, Spechtenhauser B, Böcker W, Schmid KW. Standardized staining and analysis of argyrophilic nucleolar organizer region associated proteins (AgNORs) in radically resected colorectal adenocarcinoma - correlation with tumor stage and long-term survival. J Pathol 1995;175:441-8.
- 15. Ozercan IH, Bahcecioglu IH, Ozercan MR, Bozlak N, Dogan C, Yekeler H. Proliferating cell nuclear antigen and nucleolar organizer region for differential diagnosis of dysplasia and adenocarcinoma in gastric biopsies. Indian J Gastroenterol 2000;19:57-60.
- 16. Pardue ML, Gall JG. Molecular hybridization of radioactive DNA to the DNA of cytological preparations. Proc Natl Acad Sci USA 64:600-4, 1969.
- 17. Parsonnet J, Friedman GD, Vandersteen DP, Chang Y, Vogelman JH, Orentreich N, Sibley R. Helicobacter pylori infection and the risk of gastric cancer. N Engl J Med 1991;325:1127-31.
- 18. Ploton D, Menager M, Jeannesson P, Himber G, Pigeon F, Adnet JJ. Improvement in the staining and in the visualisation of the argyrophilic proteins of the nucleolar organizer region at the optical level. Histochem J 1986;18:5-14.
- 19. Ploton D, Thiry M, Menager M, Lepoint A, Adnet JJ, Goessens G. Behaviour of nucleolus during mitosis. Chromosoma 1987;95:95-107.
- 20. Rüschoff J, Bittinger A, Neumann K, Schmitz-Moormann P. Prognostic significance of nucleolar organizing regions (NORs) in carcinomas of the sigmoid colon and rectum. Path Res Pract 1990;186:85-91.
- 21. Trevisan MAS. A técnica Ag-NOR no diagnóstico do câncer da mucosa colo-retal: aplicação em exames citológicos. [tese de livre-docente]. Campinas: Faculdade de Ciências Médicas da UNICAMP; 1995.
Datas de Publicação
-
Publicação nesta coleção
05 Fev 2003 -
Data do Fascículo
Abr 2001
Histórico
-
Aceito
07 Ago 2000 -
Recebido
17 Abr 2000