Resumos
OBJETIVO: Determinar se a fita de DNA de leucócitos mononucleares endógenos é alvo de fototerapia. MÉTODOS: O estudo incluiu 65 recém-nascidos a termo com idades entre 3 e 10 dias que haviam sido expostos a fototerapia intensiva (n = 23) ou convencional (n = 23) por pelo menos 48 horas devido à icterícia neonatal, além de um grupo controle (n = 19). Dano ao DNA foi avaliado por eletroforese alcalina em gel de célula única (ensaio cometa). A capacidade antioxidante total plasmática e os níveis de estado oxidativo total também foram medidos, e a correlação entre danos ao DNA e estresse oxidativo foi investigada. RESULTADOS: Os valores médios de escores de danos ao DNA nos grupos de fototerapia intensiva e convencional foram significativamente maiores do que os do grupo controle (p < 0,001). Os valores médios e desvio padrão foram 32 (9), 28 (9), 21 (7) unidades arbitrárias, respectivamente. Os níveis de estado oxidativo nos grupos de fototerapia intensiva e convencional foram significativamente maiores do que os do grupo controle (p < 0,005). Os valores médios (desvio padrão) foram 18, 1 (4,2), 16.9 (4,4), 13,5 (4,2) µmol H2O2 equivalente/L, respectivamente. De maneira semelhante, os níveis de estresse oxidativo nos grupos de fototerapia intensiva e convencional foram significativamente maiores do que os do grupo controle (p = 0,041). A capacidade antioxidante total plasmática e os níveis de bilirrubina total não diferiram entre os grupos (p > 0,05). Não houve correlações significativas entre escores de danos ao DNA e bilirrubina, estado oxidante total e níveis de estresse oxidativo entre os grupos de fototerapia (p > 0,05). CONCLUSÕES: Tanto a fototerapia intensiva quanto a convencional causam danos ao DNA dos leucócitos mononucleares endógenos em recém-nascidos a termo com icterícia.
Danos ao DNA; ensaio cometa; hiperbilirrubinemia; estresse oxidativo; fototerapia
OBJECTIVE: Our aim was to determine whether endogenous mononuclear leukocyte DNA strand is a target of phototherapy. METHODS: The study included 65 term infants aged between 3-10 days that had been exposed to intensive (n = 23) or conventional (n = 23) phototherapy for at least 48 hours due to neonatal jaundice, and a control group (n = 19). DNA damage was assayed by single-cell alkaline gel electrophoresis (comet assay). Plasma total antioxidant capacity and total oxidant status levels were also measured, and correlation between DNA damage and oxidative stress was investigated. RESULTS: Mean values of DNA damage scores in both the intensive and conventional phototherapy groups were significantly higher than those in the control group (p < 0.001). Mean values and standard deviation were 32 (9), 28 (9), 21 (7) arbitrary unit, respectively. Total oxidant status levels in both the intensive and conventional phototherapy groups were significantly higher than those in the control group (p = 0.005). Mean (standard deviation) values were 18.1 (4.2), 16.9 (4.4), 13.5 (4.2) µmol H2O2 equivalent/L, respectively. Similarly, oxidative stress index levels in both the intensive and conventional phototherapy groups were significantly higher than those in the control group (p = 0.041). Plasma total antioxidant capacity and total bilirubin levels did not differ between the groups (p > 0.05). There were no significant correlations between DNA damage scores and bilirubin, total oxidant status and oxidative stress levels in either phototherapy group (p > 0.05). CONCLUSIONS: Both conventional phototherapy and intensive phototherapy cause endogenous mononuclear leukocyte DNA damage in jaundiced term infants.
DNA damage; comet assay; hyperbilirubinemia; oxidative stress; phototherapy
ARTIGO ORIGINAL
Fototerapia causa danos ao DNA de leucócitos mononucleares periféricos em recém-nascidos a termo
Ali AycicekI; Abdurrahim KocyigitII; Ozcan ErelII; Hakan SenturkIII
IMD. Pediatrics Department, Medical Faculty, Harran University, Sanliurfa, Turkey
IIMD. Clinical Biochemistry Department, Medical Faculty, Harran University, Sanliurfa, Turkey
IIIMD. Pediatrics Department, Sanliurfa Children's Hospital, Sanliurfa, Turkey
Correspondência Correspondência: Ali Aycicek Pediatrics Department, Medical Faculty, Harran University 63300 - Sanlıurfa - Turquia Tel.: +90 (414) 314.8410 Fax: +90 (414) 313.9615 Email: ayciceka@hotmail.com, ali_aycicek@yahoo.com.tr
RESUMO
OBJETIVO: Determinar se a fita de DNA de leucócitos mononucleares endógenos é alvo de fototerapia.
MÉTODOS: O estudo incluiu 65 recém-nascidos a termo com idades entre 3 e 10 dias que haviam sido expostos a fototerapia intensiva (n = 23) ou convencional (n = 23) por pelo menos 48 horas devido à icterícia neonatal, além de um grupo controle (n = 19). Dano ao DNA foi avaliado por eletroforese alcalina em gel de célula única (ensaio cometa). A capacidade antioxidante total plasmática e os níveis de estado oxidativo total também foram medidos, e a correlação entre danos ao DNA e estresse oxidativo foi investigada.
RESULTADOS: Os valores médios de escores de danos ao DNA nos grupos de fototerapia intensiva e convencional foram significativamente maiores do que os do grupo controle (p < 0,001). Os valores médios e desvio padrão foram 32 (9), 28 (9), 21 (7) unidades arbitrárias, respectivamente. Os níveis de estado oxidativo nos grupos de fototerapia intensiva e convencional foram significativamente maiores do que os do grupo controle (p < 0,005). Os valores médios (desvio padrão) foram 18, 1 (4,2), 16.9 (4,4), 13,5 (4,2) µmol H2O2 equivalente/L, respectivamente. De maneira semelhante, os níveis de estresse oxidativo nos grupos de fototerapia intensiva e convencional foram significativamente maiores do que os do grupo controle (p = 0,041). A capacidade antioxidante total plasmática e os níveis de bilirrubina total não diferiram entre os grupos (p > 0,05). Não houve correlações significativas entre escores de danos ao DNA e bilirrubina, estado oxidante total e níveis de estresse oxidativo entre os grupos de fototerapia (p > 0,05).
CONCLUSÕES: Tanto a fototerapia intensiva quanto a convencional causam danos ao DNA dos leucócitos mononucleares endógenos em recém-nascidos a termo com icterícia.
Palavras-chave: Danos ao DNA, ensaio cometa, hiperbilirrubinemia, estresse oxidativo, fototerapia.
Introdução
A fototerapia é a forma mais utilizada de terapia para recém-nascidos (RN) com hiperbilirrubinemia para diminuir a carga corporal de bilirrubina neurotóxica1-3. Uma vasta experiência clínica sugere que efeitos biológicos adversos de longo prazo resultantes de fototerapia são ausentes, mínimos ou não reconhecidos.
Entretanto, todos que estiverem utilizando fototerapia devem permanecer alertas a essas possibilidades e evitar qualquer uso desnecessário, pois efeitos indesejáveis sobre o DNA já foram demonstrados in vitro4.
Peroxidases também podem gerar dióxido de nitrogênio (NO2) cataliticamente usando H2O2 e nitrato como substratos5. Quantidades excessivas de espécies reativas de oxigênio e de nitrogênio (ERO e ERN) podem danificar células hospedeiras e induzir quebras na fita de DNA.
Com o tempo, o acúmulo de danos ao DNA pode levar a modificações genéticas nas células, as quais podem ser mutagênicas ou carcinogênicas6. Até o presente momento, embora existam alguns estudos sobre estado oxidativo em RN tratados com fototerapia7-10, não há relato disponível sobre danos ao DNA desses pacientes. Previamente, relatamos que a fototerapia tem impacto negativo em diversas partes do sistema de defesa oxidante/antioxidante em RN com hiperbilirrubinemia, expondo-os a um potente estresse oxidativo11. Neste estudo, medimos quebras na fita de DNA de leucócitos mononucleares endógenos e investigamos a correlação entre o escore de danos ao DNA e a capacidade antioxidante total (CAT) plasmática, estado oxidante total (EOT) e índice de estresse oxidativo (IEO) em RN com icterícia tratados com fototerapia convencional e intensiva.
Métodos
População
Este estudo incluiu 65 RN (38-41 semanas) com idades entre 3 e 10 dias que tiveram parto vaginal e foram admitidos no Hospital Infantil Sanliurfa devido a hiperbilirrubinemia indireta clinicamente significativa.
Todos os RN estavam sendo amamentados e não apresentavam fator etiológico para hiperbilirrubinemia. Os critérios de exclusão foram: RN com malformação congênita grave; prematuridade ou pós-maturidade; diabete materna; asfixia ao nascimento; sepse ou hiperbilirrubinemia do tipo hemolítico devido a incompatibilidade de grupo sangüíneo (Rh ou ABO); RN que receberam fototerapia convencional ou intensiva antes da coleta de sangue; RN nos quais o nível de bilirrubina plasmática total tinha aumentado em mais de 5 mg/dL por dia ou era maior que 24 mg/dL nas primeiras 24 horas após o nascimento; RN com sinais e sintomas sugestivos de doença grave. Hiperbilirrubinemia indireta clinicamente significativa foi definida como estando presente em RN com concentração de bilirrubina plasmática total de mais de 13 mg/dL12.
Sistemas de fototerapia convencional consistiam de seis lâmpadas fluorescentes brancas (Philips TL 52/20W) posicionadas 40 cm acima do RN. Sistemas de fototerapia intensiva consistiam de 12 lâmpadas fluorescentes azuis (Philips TL03) posicionadas 20 cm acima e abaixo do RN. Os RN foram posicionados nus, com exceção de uma fralda e proteção para os olhos, em uma incubadora, berço ou unidade de fototerapia intensiva (Bilicrystal, Medestime). A energia de luz das unidades de fototerapia foi medida por um fotômetro padrão (Light Meter VF, Minolta, Japão); as unidades de fototerapia convencional foram de 12-16 µW/cm2/nm, e as unidades de fototerapia intensiva, de 30-34 µW/cm2/nm. Para níveis de bilirrubina maiores que 22 mg/dL, aplicou-se fototerapia intensiva; para níveis menores de 22 mg/dL, aplicou-se fototerapia convencional ou intensiva aleatoriamente. Os RN foram expostos a fototerapia convencional e intensiva continuamente por pelo menos 48 horas (máximo de 72 horas; média intensiva = 58 horas, convencional = 61 horas), exceto durante alimentação, limpeza e coletas. O grupo controle foi composto de 19 RN cujas concentrações de bilirrubina plasmática total eram de 12,9-19,1 mg/dL, mas que não receberam fototerapia (antes da fototerapia).
O escore de danos ao DNA e os níveis totais de antioxidantes/oxidantes plasmáticos foram medidos em amostras retiradas de RN com hiperbilirrubinemia após tratamento com fototerapia (grupos convencional ou intensivo) e antes da fototerapia (controles). Amostras sangüíneas de, no máximo, 2,5 mL foram colhidas por RN para todos os parâmetros. Esse tempo foi escolhido para permitir a amostragem simultânea de testes rotineiros de bilirrubina, evitando um procedimento de coleta de sangue unicamente para o propósito deste estudo. Os controles não foram incluídos nos grupos de fototerapia. Todos os RN foram amamentados. O comitê local de ética aprovou este estudo. Os pais forneceram consentimento para a participação dos RN neste estudo.
Preparação da amostra
Foram coletadas amostras de sangue de uma veia periférica em tubos heparinizados, armazenados a 10 ºC no escuro para prevenir danos adicionais ao DNA e processados em 2 horas. O isolamento do leucócito mononuclear para o ensaio cometa foi realizado com Histopaque 1077 (Sigma); 1 mL de sangue total heparinizado foi cuidadosamente colocado sobre 1 mL de Histopaque e centrifugado por 35 minutos a 500 x g e 25 ºC. A faixa de interface contendo leucócitos mononucleares foi lavada com solução salina tamponada com fosfato (PBS) e, a seguir, coletada após 15 minutos de centrifugação a 400 x g. Os pellets resultantes foram suspensos novamente em PBS, e as células foram contadas em uma câmara de Neubauer. A integridade da membrana foi avaliada pelo método de exclusão com azul de tripano. O sangue restante foi centrifugado a 1.500 x g por 10 minutos para obter o plasma. O plasma separado foi dividido em duas partes, uma das quais foi utilizada para medir a bilirrubina total e direta, ao passo que a outra foi armazenada a -80 ºC até análise posterior de CAT e EOT.
Determinação de danos ao DNA por ensaio cometa alcalino
Danos endógenos ao DNA de leucócitos mononucleares periféricos foram analisados por ensaio cometa alcalino, segundo Singh et al.13 com pequenas modificações14. Todos os passos da análise foram conduzidos sob luz vermelha ou sem luz direta para prevenir danos adicionais ao DNA.
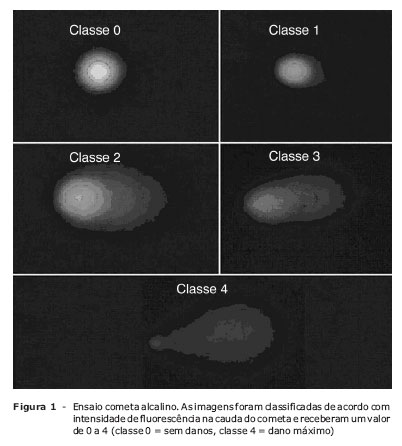
As imagens de 100 núcleos escolhidos aleatoriamente (50 núcleos de cada uma das duas lâminas duplicadas) foram analisadas visualmente para cada indivíduo. Cada imagem foi classificada de acordo com intensidade da fluorescência na cauda do cometa, recebendo um valor de 0, 1, 2, 3, ou 4 (sem danos, classe 0, até dano máximo, classe 4) (Figura 1), para que o escore total de uma lâmina pudesse ser entre 0 e 400 unidades arbitrárias (UA). Fotomicrografias de amostras representativas estão mostradas nas Figuras 2 e 3. A mesma equipe de bioquímica realizou todos os procedimentos, e um único observador, cego quanto ao grupo do indivíduo, determinou o escore de danos ao DNA.
Níveis de CAT e EOT foram medidos pelos métodos de Erel15,16. A porcentagem de nível de EOT em relação a nível de CAT foi considerada como sendo IEO17,18. Para realizar o cálculo, a unidade de resultado de CAT, mmol equivalente de Trolox/L, foi alterada para µmol equivalente de Trolox/L, e o valor do IEO foi calculado da seguinte forma: IEO = [(EOT, µmol/L/(CAT, µmol equivalente de Trolox/L)/100].
Análise estatística
O teste de normalidade de variâncias foi realizado através dos testes estatísticos de Levene. As variâncias neste ensaio foram homogêneas. Os dados foram comparados pela análise de variância one-way com o teste de comparação múltipla de Tukey honestamente significante. A razão entre sexos foi comparada através de um teste do qui-quadrado. Associações bivariadas entre as variáveis foram avaliadas pelo teste de correlação de Pearson. Os dados foram expressos como média + desvio padrão, e as diferenças foram consideradas estaticamente significativas se p < 0,05. A análise estatística foi conduzida com o auxílio do SPSS para Windows, versão 11.5 (SPSS, Chicago, EUA).
Resultados
A média de idade do grupo fototerapia intensiva foi de 7+3 dias, altura média de 50+3,2 cm, média de peso corporal de 3,1+1,6 kg, duração média de fototerapia de 54+6 horas e razão entre sexos de 12/11 (M/F). A média de idade do grupo fototerapia convencional foi de 7+4 dias, altura média de 50+3,6 cm, média de peso corporal de 3,2+1,2 kg, duração média de fototerapia de 61+10 horas e razão sexual de 13/10 (M/F). A média de idade do grupo controle foi de 5+2 dias, altura média de 50+2,9 cm, média de peso corporal de 3+1,1 kg e razão entre sexos de 10/9 (M/F). Não houve diferença significativa entre os três grupos quanto à idade, comprimento, peso, duração da fototerapia (entre intensiva e convencional), idade gestacional (todos os grupos foram de 39+1) ou distribuição masculino/feminino (p > 0,05).
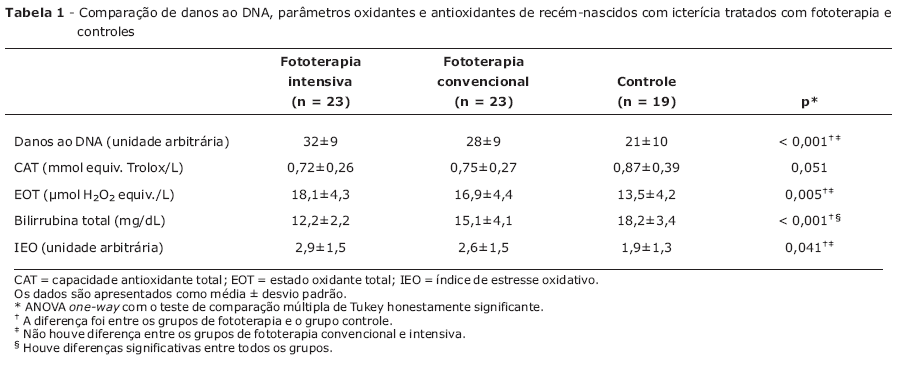
Os escores de danos ao DNA e os níveis de CAT, EOT, IEO e bilirrubina total estão mostrados na Tabela 1. Os escores de danos ao DNA foram de 32+9 no grupo de fototerapia intensiva, 28+9 no grupo de fototerapia convencional e 21+7 no grupo controle (p < 0,001). Os níveis de EOT e IEO foram significativamente maiores nos grupos intensivo e convencional do que no grupo controle (p < 0,05). Os escores de danos ao DNA e os níveis de EOT e IEO não diferiram significativamente entre os grupos de fototerapia convencional e intensiva. A CAT plasmática e os níveis de bilirrubina total não diferiram entre os grupos (p > 0,05). Não houve correlações significativas entre escores de danos ao DNA e níveis de bilirrubina, EOT e IEO nos grupos de fototerapia convencional ou intensiva (p > 0,05).
Discussão
Os principais resultados deste estudo são que as quebras da fita de DNA dos leucócitos mononucleares endógenos, que são um tipo bem conhecido de dano ao DNA, estiveram significativamente aumentadas nos RN tratados com fototerapia convencional e intensiva, quando comparados aos controles. É interessante notar que não houve correlação significativa entre escores de danos ao DNA e níveis de EOT nos grupos de fototerapia convencional ou intensiva. Este é o primeiro relato demonstrando associação entre danos ao DNA de leucócitos mononucleares em RN a termo com icterícia tratados com fototerapia convencional ou intensiva.
Leucócitos mononucleares periféricos humanos vêm sendo amplamente utilizados para monitorar danos genéticos induzidos ambientalmente por uma variedade de métodos, como micronúcleo, aberração cromossômica e ensaios de trocas entre cromátides irmãs19. Entre os vários ensaios para medir danos ao DNA, a eletroforese alcalina em gel de célula única (ensaio cometa) é um método sensível e poderoso para determinação de quebras na fita do DNA20,21. Também já houve relatos de que as quebras na fita ocorrem devido a danos ao DNA gerados por estresse oxidativo14,22. A medição do dano ao DNA com o ensaio cometa na epiderme humana de RN tratados com fototerapia não é possível em razão da dificuldade em obter células únicas viáveis deste tecido em RN. Portanto, utilizamos este método para medir o dano ao DNA em leucócitos mononucleares circulantes. Entretanto, futuras avaliações de oxidação do DNA na epiderme podem lançar luz sobre o papel do estresse oxidativo em RN tratados com fototerapia.
Embora tenhamos demonstrado a presença de danos ao DNA na forma de quebras diretas na fita, não podemos descartar oxidação de bases. O reparo da ligação das quebras de fita (meia-vida de aproximadamente 30 minutos) é um processo muito mais rápido do que o de lesões de base oxidada por reparo de excisão de base (meia-vida de aproximadamente 3 horas)23. Desta forma, os procedimentos de reparo já existiam para fototerapia 48 horas mais tarde. De forma semelhante, a inibição parcial de reparo induzido pelo inibidor de DNA polimerase após a fototerapia pode representar interferência com a recombinação de quebras diretas de fita. Embora a presença de cometas após a fototerapia também possa indicar que as quebras de fita foram induzidas como lesões primárias, as quebras de fita medidas pelo ensaio cometa imediatamente após a fototerapia poderiam representar fendas entre os estágios de incisão e recombinação dos processos de reparo por excisão iniciados durante a irradiação solar24.
As fotorreações podem induzir fotoprodutos mutagênicos ou lesões no DNA entre pirimidinas na forma de reguladores de luz25. Embora o comprimento de onda de 245-290 nm seja absorvido maximamente pelo DNA26, conforme observado neste estudo, comprimentos de onda de 460 nm causam danos ao DNA. Este resultado pode ser causado pelo comprimento de onda maior que penetra uma camada profunda do tecido, principalmente na pele macia e vulnerável do RN27. Parece que, sob fototerapia, a taxa de danos excede a capacidade de reparo. Este estudo mostrou que os danos ao DNA de leucócitos mononucleares são maiores em RN tratados por fototerapia convencional e intensiva do que em RN a termo com icterícia não tratados por fototerapia. No entanto, neste estudo, a principal limitação é não usar os mesmos pacientes como seus próprios controles (antes e durante a fototerapia). O ensaio cometa alcalino é muito complexo, e as amostras em espera não são possíveis14. Além disso, o laboratório somente aceitava amostras sangüíneas para estudo do ensaio cometa em horários especiais da semana. Essas dificuldades causaram perda de casos e a impossibilidade de usar os mesmos pacientes como seus próprios controles (antes e durante a fototerapia). Lidamos com essas dificuldades usando pacientes diferentes tratados com fototerapia por, pelo menos, 48 horas e controles (não expostos a fototerapia). Acreditamos que novos estudos sejam necessários para determinar se há alterações em casos semelhantes.
Radicais livres podem adversamente alterar lipídeos, proteínas e DNA28,29. Reações de bilirrubina envolvendo radicais livres ou produtos de redução de oxigênio tóxico já estão bem documentados: bilirrubina não conjugada absorve oxigênio singlete com alta eficiência, reage com ânions do superóxido e radicais peroxil, além de servir como substrato redutor para peroxidases na presença de peróxido de hidrogênio ou hidroperóxidos orgânicos30,31. Esta deterioração é particularmente evidente na presença de estresse oxidativo, como na fototerapia7. Bohles et al. relataram uma diminuição significativa em antioxidantes durante a fototerapia32. Entretanto, nosso estudo demonstrou que os níveis de CAT não foram significativamente alterados pela fototerapia. O equilíbrio oxidante/antioxidante pendeu significativamente para o lado oxidante, pois outros indicadores de nível de estado oxidante, EOT e IEO tiveram aumento significativo em RN expostos a fototerapia convencional e intensiva. Também verificamos que não houve correlações significativas entre razões de danos ao DNA e níveis de EOT e IEO (p > 0,05). Neste estudo, esses resultados indicam que os danos ao DNA não foram somente causados por estresse oxidativo, mas também por outros fatores, como interação direta da luz da fototerapia com o DNA.
É interessante notar que a fototerapia convencional e intensiva causa níveis semelhantes de danos ao DNA e estresse oxidativo. Pode haver um efeito limiar da fototerapia sobre esses parâmetros.
Considera-se que a natureza não-invasiva da fototerapia, fácil disponibilidade, baixo custo e poucos efeitos colaterais relatados inicialmente quase levaram à suposição de que ela seja inócua33.
Entretanto, todos que estiverem utilizando fototerapia devem permanecer alertas a essas possibilidades e evitar qualquer uso desnecessário, pois efeitos indesejáveis sobre o DNA já foram demonstrados in vitro3,4,11. Nosso estudo demonstrou que a fototerapia, tanto convencional quanto intensiva, causa efeitos indesejáveis no DNA in vivo.
Em conclusão, a fototerapia intensiva e convencional causa danos ao DNA dos leucócitos mononucleares endógenos em RN a termo com icterícia.
Agradecimentos
Agradecemos às enfermeiras do Serviço Neonatal do Hospital Infantil Sanliurfa e ao Departamento de Bioquímica da Faculdade de Medicina da Harran University, por seu auxílio na realização deste estudo.
Artigo submetido em 22.10.07, aceito em 19.12.07.
Não foram declarados conflitos de interesse associados à publicação deste artigo.
- 1. Porter ML, Dennis BL. Hyperbilirubinemia in the term newborn. Am Fam Physician. 2002;65:599-606.
- 2. Tan KL. Phototherapy for neonatal jaundice. Acta Paediatr. 1996;85:277-9.
- 3. Lamola AA, Blumberg WE, McClead R, Fanaroff A. Photoisomerized bilirubin in blood from infants receiving phototherapy. Proc Natl Acad Sci U S A. 1981;78:1882-6.
- 4. Babara JS, Robert MK. Jaundice and hyperbilirubinemia in the newborn. In: Behrman RE, Kliegman RM, Jenson HB, editors. Nelson Textbook of Pediatrics. 17th ed. Philadelphia, PA: Saunders; 2004. p. 592-7.
- 5. Brennan ML, Wu W, Fu X, Shen Z, Song W, Frost H, et al. A tale of two controversies: defining both the role of peroxidases in nitrotyrosine formation in vivo using eosinophil peroxidase and myeloperoxidase-deficient mice, and the nature of peroxidase-generated reactive nitrogen species. J Biol Chem. 2002;277:17415-27.
- 6. Valko M, Izakovic M, Mazur M, Rhodes CJ, Telser J. Role of oxygen radicals in DNA damage and cancer incidence. Mol Cell Biochem. 2004;266:37-56.
- 7. Gathwala G, Sharma S. Oxidative stress, phototherapy and the neonate. Indian J Pediatr. 2000;67:805-8.
- 8. Turgut M, Basaran O, Cekmen M, Karatas F, Kurt A, Aygun AD. Oxidant and antioxidant levels in preterm newborns with idiopathic hyperbilirubinaemia. J Paediatr Child Health. 2004;40:633-7.
- 9. Akisu M, Yilmaz D, Tuzun S, Kultursay N. Antioxidant defense systems in newborns undergoing phototherapy. Indian J Pediatr. 1999;66:651-5.
- 10. McDonagh AF. The role of singlet oxygen in bilirubin photo-oxidation. Biochem Biophys Res Commun. 1971;44:1306-11.
- 11. Aycicek A, Erel O. Total oxidant/antioxidant status in jaundiced newborns before and after phototherapy. J Pediatr (Rio J). 2007;83:319-22.
- 12. Newman TB, Maisels MJ. Evaluation and treatment of jaundice in the term newborn: A kinder, gentler approach. Pediatrics. 1992;89:809-18.
- 13. Singh NP, McCoy MT, Tice RR, Schneider EL. A simple technique for quantitation of low levels of DNA damage in individual cells. Exp Cell Res. 1988;175:184-91.
- 14. Kocyigit A, Keles H, Selek S, Guzel S, Celik H, Erel O. Increased DNA damage and oxidative stress in patients with cutaneous leishmaniasis. Mutat Res. 2005;585:71-8.
- 15. Erel O. A novel automated direct measurement method for total antioxidant capacity using a new generation, more stable ABTS radical cation. Clin Biochem. 2004;37:277-85.
- 16. Erel O. A new automated colorimetric method for measuring total oxidant status. Clin Biochem. 2005;38:1103-11.
- 17. Aycicek A, Erel O, Kocyigit A. Increased oxidative stress in infants exposed to passive smoking. Eur J Pediatr. 2005;164:775-8.
- 18. Harma M, Harma M, Erel O. Oxidative stress in women with preeclampsia. Am J Obstet Gynecol. 2005;192:656-7.
- 19. Cole J, Skopek TR. International Commission for Protection Against Environmental Mutagens and Carcinogens. Working paper no. 3. Somatic mutant frequency, mutation rates and mutational spectra in the human population in vivo. Mutat Res. 1994;304:33-105.
- 20. Moller P, Knudsen LE, Loft S, Wallin H.The comet assay as a rapid test in biomonitoring occupational exposure to DNA-damaging agents and effect of confounding factors. Cancer Epidemiol Biomarkers Prev. 2000;9:1005-15.
- 21. Garcia O, Mandina T, Lamadrid AI, Diaz A, Remigio A, Gonzalez Y, et al. Sensitivity and variability of visual scoring in the comet assay. Results of an inter-laboratory scoring exercise with the use of silver staining. Mutat Res. 2004;556:25-34.
- 22. Rojas E, Lopez MC, Valverde M. Single cell gel electrophoresis assay: methodology and applications. J Chromotogr B Biomed Sci Appl. 1999;722:225-54.
- 23. Sparrow JR, Zhou J, Cai B. DNA is a target of the photodynamic effects elicited in A2E-laden RPE by blue-light illumination. Invest Ophthalmol Vis Sci. 2003;44:2245-51.
- 24. Arlett CF, Lowe JE, Harcourt SA, Waugh AP, Cole J, Roza L, et al. Hypersensitivity of human lymphocytes to UV-B and solar irradiation. Cancer Res. 1993;53:609-14.
- 25. Matsumura Y, Ananthaswamy HN. Toxic effects of ultraviolet radiation on the skin. Toxicol Appl Pharmacol. 2004;195:298-308.
- 26. Tornaletti S, Pfeifer GP. UV damage and repair mechanisms in mammalian cells. Bioessays 1996;18:221-8.
- 27. Meulemans CC, Werner M. Skin penetration depth optical radiation. http://www.solarcsystems.com/pdfs/philips_light_sources_for_phototherapy.pdf Acesso: 19/9/2007.
- 28. Warner BB, Wispe JR Free radical mediated diseases in pediatrics. Semin Perinatol. 1992;16:47-57.
- 29. Halliwell B. Free radicals, antioxidants, and human disease: curiosity, cause, or consequence? Lancet. 1994;344:721-4.
- 30. Stocker R, Ames BN. Potential role of conjugated bilirubin and copper in the metabolism of lipid peroxides in bile. Proc Natl Acad Sci USA. 1987; 84:8130-4.
- 31. Stocker R, Glazer AN, Ames BN. Antioxidant activity of albumin bound bilirubin. Proc Natl Acad Sci USA. 1987;84:5918-22.
- 32. Bohles H, Schnall B. The effect of phototherapy on serum uric acid. Klin Padiatr. 1981;193:308-10.
- 33. Tan KL. Phototherapy for neonatal jaundice. Clin Perinatol. 1991;18:423-39.
Datas de Publicação
-
Publicação nesta coleção
14 Abr 2008 -
Data do Fascículo
Abr 2008
Histórico
-
Aceito
19 Dez 2007 -
Recebido
22 Out 2007