Resumos
OBJETIVO: Avaliar a aplicabilidade de um protocolo de atendimento padronizado para crianças de até 36 meses de idade com febre sem sinais localizatórios (FSSL). MÉTODOS: Estudo de coorte prospectivo em crianças com FSSL atendidas no Pronto-Socorro do Hospital Universitário da Universidade de São Paulo, São Paulo (SP), de junho de 2006 a maio de 2007. O protocolo estratifica o risco de infecção bacteriana grave (IBG) de acordo com a presença ou não de toxemia, idade e valor da temperatura. Conforme avaliação de risco, indicava-se triagem laboratorial: hemograma, hemocultura, sedimento urinário, urocultura e, se necessário, radiografia torácica, liquor e coprocultura. RESULTADOS: Foram estudadas 251 crianças das quais 215 foram acompanhadas até o diagnóstico final. Vinte crianças apresentavam toxemia, e 195 estavam em bom estado geral (30 com idade de até 3 meses, e 165, de 3 a 36 meses). Nas crianças de 3 a 36 meses não toxêmicas, 95 tinham temperatura axilar > 39 ºC. Em 107 crianças (49,8%), houve melhora espontânea do quadro febril; em 88 (40,9%), foi identificada doença benigna autolimitada; e em 20 (9,3%), IBG. Dentre as IBG, identificamos 16 infecções urinárias, três pneumonias e uma bacteremia oculta. Das 215, 129 (60%) não receberam qualquer antibioticoterapia, e 86 receberam antibiótico em algum momento (45, empiricamente). O antibiótico empírico foi mantido por, em média, 72 horas. CONCLUSÃO: O protocolo aplicado mostrou-se adequado para o seguimento destas crianças que fizeram coleta de exames simples e passíveis de serem realizados na maioria dos serviços. A infecção urinária foi a IBG mais frequente nas crianças com FSSL.
Febre sem sinais localizatórios; criança; infecção bacteriana grave
OBJECTIVE: To evaluate the applicability of a standardized guideline for children up to 36 months of age with fever without source (FWS). METHODS: Prospective cohort study involving children with FWS treated at the emergency department of Hospital Universitário, Universidade de São Paulo, São Paulo, Brazil, from June 2006 to May 2007. The guideline classifies the risk of serious bacterial infection (SBI) according to the presence or absence of toxemia, age, and temperature. Laboratory screening was based on risk assessment: complete blood count, blood culture, urinalysis, urine culture, and, if necessary, chest radiography, cerebrospinal fluid, and coproculture. RESULTS: We studied 251 children and, of these, 215 were followed up until the final diagnosis. Toxemia was found in 20 children, and 195 were well-appearing (30 up to 3 months old and 165 from 3 to 36 months old). Among those children from 3 to 36 months without toxemia, 95 had axillary temperature > 39 ºC. In 107 (49.8%) children, there was spontaneous resolution of fever; in 88 (40.9%), benign self-limited disease was identified; and in 20 (9.3%), there was SBI. Among the cases of SBI, we identified 16 urinary tract infections, three cases of pneumonia and one occult bacteremia. Of the 215 children, 129 (60%) received no antibiotics, and 86 received antibiotics at some point (45 empirically). Empirical antibiotic treatment was maintained for an average of 72 hours. CONCLUSION: The guideline was shown to be appropriate to follow up these children using simple laboratory tests that can be carried out at most health facilities. The most frequent SBI in this sample was urinary tract infection.
Fever without source; children; serious bacterial infection
ARTIGO ORIGINAL
Febre sem sinais localizatórios: avaliação de um protocolo de atendimento
Beatriz Marcondes MachadoI; Débora Morais CardosoII; Milena de PaulisI; Ana Maria de Ulhôa EscobarIII; Alfredo Elias GilioIV
IDoutoranda, Departamento de Pediatria, Faculdade de Medicina, Universidade de São Paulo (USP), São Paulo, SP. Médica assistente, Pronto-Socorro de Pediatria, Hospital Universitário, USP, São Paulo, SP
IIMédica assistente, Pronto-Socorro de Pediatria, Hospital Universitário, USP, São Paulo, SP
IIILivre-docente, Departamento de Pediatria, Faculdade de Medicina, USP, São Paulo, SP
IVDoutor, Pediatria, Faculdade de Medicina, USP, São Paulo, SP
Correspondência Correspondência: Beatriz Marcondes Machado Divisão de Pediatria do Hospital Universitário da USP Av. Professor Lineu Prestes, 2.565 CEP 05088-900 - São Paulo, SP Tel.: (11) 3091.9409 Fax: (11) 3091.9460 E-mail: beatriz@hu.usp.br
RESUMO
OBJETIVO: Avaliar a aplicabilidade de um protocolo de atendimento padronizado para crianças de até 36 meses de idade com febre sem sinais localizatórios (FSSL).
MÉTODOS: Estudo de coorte prospectivo em crianças com FSSL atendidas no Pronto-Socorro do Hospital Universitário da Universidade de São Paulo, São Paulo (SP), de junho de 2006 a maio de 2007. O protocolo estratifica o risco de infecção bacteriana grave (IBG) de acordo com a presença ou não de toxemia, idade e valor da temperatura. Conforme avaliação de risco, indicava-se triagem laboratorial: hemograma, hemocultura, sedimento urinário, urocultura e, se necessário, radiografia torácica, liquor e coprocultura.
RESULTADOS: Foram estudadas 251 crianças das quais 215 foram acompanhadas até o diagnóstico final. Vinte crianças apresentavam toxemia, e 195 estavam em bom estado geral (30 com idade de até 3 meses, e 165, de 3 a 36 meses). Nas crianças de 3 a 36 meses não toxêmicas, 95 tinham temperatura axilar > 39 ºC. Em 107 crianças (49,8%), houve melhora espontânea do quadro febril; em 88 (40,9%), foi identificada doença benigna autolimitada; e em 20 (9,3%), IBG. Dentre as IBG, identificamos 16 infecções urinárias, três pneumonias e uma bacteremia oculta. Das 215, 129 (60%) não receberam qualquer antibioticoterapia, e 86 receberam antibiótico em algum momento (45, empiricamente). O antibiótico empírico foi mantido por, em média, 72 horas.
CONCLUSÃO: O protocolo aplicado mostrou-se adequado para o seguimento destas crianças que fizeram coleta de exames simples e passíveis de serem realizados na maioria dos serviços. A infecção urinária foi a IBG mais frequente nas crianças com FSSL.
Palavras-chave: Febre sem sinais localizatórios, criança, infecção bacteriana grave.
Introdução
A presença de febre é uma das queixas mais frequentes na pediatria e corresponde a aproximadamente 25% das consultas de emergência. Geralmente, a origem da febre pode ser identificada na avaliação inicial após anamnese e exame físico cuidadosos1-6.
Entretanto, em aproximadamente 20% dos casos, o pediatra pode se deparar com uma criança febril cujo foco de infecção não é identificado a partir dos dados fornecidos pela história clínica e pelo exame clínico bem conduzido. Esta situação é conhecida como febre sem sinais localizatórios (FSSL)1-5,7,8. A FSSL é a ocorrência de febre com menos de 7 dias de duração numa criança em cujo caso a história e o exame físico cuidadosos não revelam a causa da febre.
A maioria das crianças com FSSL apresenta doença infecciosa aguda autolimitada ou está em fase prodrômica de uma doença infecciosa benigna. Poucas têm infecção bacteriana grave (IBG). As IBG são todas as infecções que, caso ocorra atraso no diagnóstico, acarretam risco de morbidade ou mortalidade1,3,4,6,8,9. São consideradas IBG: bacteremia oculta (BO), pneumonia, infecção urinária (IU), meningite bacteriana, artrite séptica, osteomielite e celulite1,3,4,6-8. O grande desafio dos pediatras reside na diferenciação dos processos febris de uma doença benigna autolimitada, daqueles poucos que podem ter como causa uma IBG.
Durante a década de 70, surgiram os primeiros relatos de que algumas crianças febris, menores de 3 anos, em bom estado geral e pouco ou nenhum achado clínico tinham hemocultura positiva (BO). Isso acarretou uma intensa busca dos fatores de risco para identificação precoce dessas crianças10,11.
Estudos dos anos 80 e 90 constataram que as crianças de até 3 anos com FSSL, contagem de leucócitos > 15.000/mm3 e temperatura > 39 ºC tinham risco de IBG7,12-14. Em 1992, Baraff & Lee12 estimaram em 13% o risco de BO em pacientes com contagem de leucócitos ≥ 15.000/mm3.
O protocolo de Baraff et al.7, publicado em 1993, foi baseado na meta-análise de 85 artigos e opiniões de especialistas. O documento estratifica as crianças por faixa etária e, ainda, pelo risco para IBG (baixo e alto), através de critérios clínicos e laboratoriais. A partir dele, várias estratégias foram elaboradas no intuito de padronizar a abordagem das crianças com FSSL1,2,4,15-17.
No Pronto-Socorro do Hospital Universitário (PSHU) da Universidade de São Paulo (USP), São Paulo (SP), passou-se a utilizar para avaliação e seguimento dessas crianças um protocolo de atendimento que estratifica o risco de IBG de acordo com a presença ou não de toxemia, a idade e o valor da temperatura. Este protocolo, baseado nos protocolos da literatura e na experiência do nosso serviço, foi elaborado e adaptado à nossa realidade.
As divergências na literatura e a ausência de estudos nacionais que avaliem o atendimento e seguimento das crianças com FSSL em hospitais gerais justificam este estudo. O objetivo é avaliar a aplicabilidade do protocolo de atendimento padronizado para crianças de até 36 meses de idade com FSSL atendidas no PSHU-USP.
Métodos
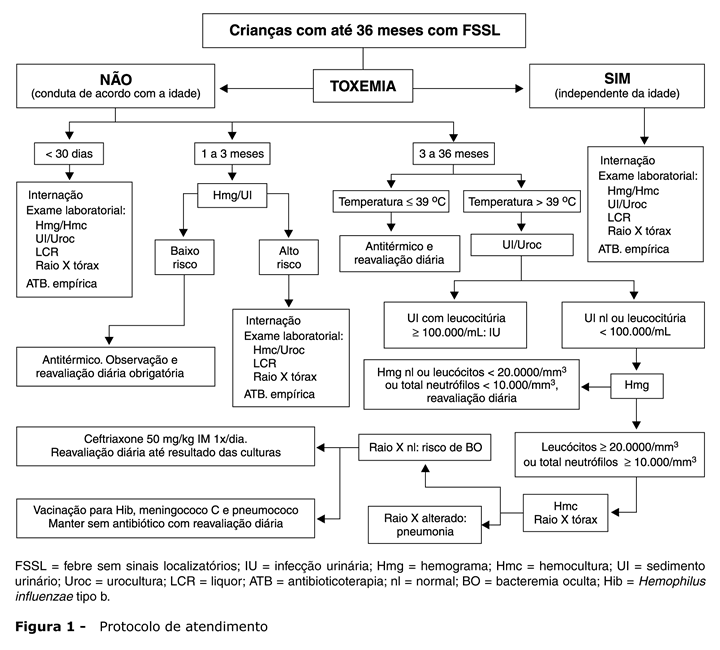
Foi realizado estudo prospectivo em crianças de 0 a 36 meses que procuraram o PSHU-USP com quadro de FSSL durante um período de 12 meses (25/05/06 a 31/05/07). Foram incluídas no estudo as crianças atendidas no PSHU-USP de segundas a sextas-feiras das 7 às 19 horas. As crianças foram atendidas conforme o protocolo de atendimento (Figura 1) e seguidas até resolução do quadro febril, ou identificação do foco, ou resultado final das culturas, quando colhidas.
Para todas as crianças foi obtido o termo de consentimento dos pais após o esclarecimento detalhado dos objetivos da pesquisa.
Os motivos de exclusão foram:
- Presença de doença de base que potencialmente implicasse em alterações na imunidade;
- Utilização de antibioticoterapia na última semana.
Este estudo foi aprovado pelo Comitê de Ética em Pesquisa do HU-USP (protocolo nº 630/05 e registro SISNEP nº 0035.0.198.000-08).
Protocolo de atendimento
Segundo o protocolo, as crianças de até 36 meses com FSSL foram avaliadas inicialmente em relação à presença ou não de toxemia. Esta avaliação foi feita com a criança afebril, pois a própria febre pode deixar o paciente com variados graus de prostração. Foram consideradas crianças toxêmicas aquelas que apresentassem algum grau de inabilidade de interagir com os pais ou responsáveis, irritabilidade, alteração do nível de consciência, hipoatividade, hipotonia, letargia, hiper ou hipoventilação, hipotensão, taquicardia, sinais de má perfusão periférica ou cianose1,2,4,7,8,18. A criança com aparência toxêmica, independentemente da idade, foi avaliada criteriosamente, sendo realizada triagem laboratorial, introdução de antibiótico parenteral de largo espectro e admissão hospitalar. A triagem laboratorial compreendia coleta de hemograma completo, hemocultura, sedimento urinário, urocultura, e, quando indicado, liquor (análise bioquímica, coloração de Gram e cultura), radiografia torácica e coprocultura. Todas as crianças toxêmicas na avaliação inicial permaneceram em observação enquanto aguardavam os resultados dos exames.
As crianças não toxêmicas foram classificadas em três grupos etários distintos para efeitos de avaliação de FSSL: recém-nascidos (≤ 30 dias de vida), lactentes jovens (de 30 a 90 dias) e crianças de 3 a 36 meses de idade.
O recém-nascido febril, pelo maior risco de IBG, foi internado para coleta da triagem laboratorial e introdução de antibiótico empírico (ampicilina e cefotaxima) até identificação do foco ou resultados finais das culturas.
Os lactentes jovens febris foram avaliados inicialmente em relação ao risco de IBG através dos critérios de Rochester (Figura 2)19. Para ser considerada de baixo risco, a criança deve preencher todos os itens previstos por esses critérios. O não preenchimento de apenas um dos itens caracteriza a criança como de alto risco para IBG. O lactente jovem caracterizado como paciente de baixo risco para IBG teve a opção de observação domiciliar quando os pais ou responsáveis tinham condições socioculturais para tal: maturidade, termômetro e telefone em casa, carro disponível, moradia a uma distância do hospital percorrível em no máximo 30 minutos e possibilidade de retorno em até 24 horas. Caso não fosse possível esta alternativa, o paciente ficava em observação por no mínimo 24 horas no serviço. Os pais eram informados sobre os riscos e benefícios de cada alternativa para que participassem da decisão de observar em domicílio ou no hospital. Nestas crianças, a administração do ceftriaxone empírico intramuscular só foi considerada quando realizada, previamente, a coleta de líquor. Quando considerados de alto risco, os pacientes foram internados com antibiótico empírico (ceftriaxone) até o resultado final das culturas ou a identificação, na evolução, do foco de infecção após coleta da triagem laboratorial.
As crianças de 3 a 36 meses de idade e não toxêmicas foram subdivididas em dois grupos de acordo com a temperatura axilar. Os pais das crianças com temperatura ≤ 39 ºC foram orientados, após avaliação clínica cuidadosa e levando-se em consideração as condições socioculturais da família, a retornarem diariamente para reavaliação clínica até resolução da febre ou identificação do foco infeccioso.
A criança com temperatura > 39 ºC iniciava sua avaliação com coleta de amostra de urina por cateterização vesical ou jato médio para realização de análise bioquímica (fita reagente, microscopia e coloração de Gram) e urocultura. O exame de urina com leucocitúria ≥ 100.000/mL indicava tratamento (suspeita IU) até resultado da urocultura. Foi considerada positiva a urocultura com crescimento ≥ 50.000 UFC/mL colhida por cateterização, ou ≥ 100.000 UFC/mL por jato médio20.
Quando se constatava sedimento urinário normal ou leucocitúria ≤ 100.000/mL, era realizada a coleta de hemograma completo. A radiografia torácica foi considerada na criança com contagem de leucócitos > 20.000/mm3 para identificação de pneumonia oculta. Na evidência de radiografia de tórax normal com contagem de leucócitos > 20.000/mm3ou neutrófilos > 10.000/mm3 era obtida a hemocultura e introduzido antibiótico empírico (ceftriaxone em dose única diária de 50 mg/kg intramuscular) devido ao risco de BO.
A reavaliação clínica de todos os pacientes era realizada no mínimo a cada 24 horas. Todas as crianças que não retornaram nas 24 horas seguintes foram contatadas por telefone para entrevista de avaliação.
A coleta de exames de sangue e introdução de antibiótico empírico era opcional nas crianças que receberam duas ou mais doses das vacinas conjugadas para hemófilos, meningococo e pneumococo, pois a taxa BO nesta população passa a ser inferior a 1%17,21,22.
Resultados
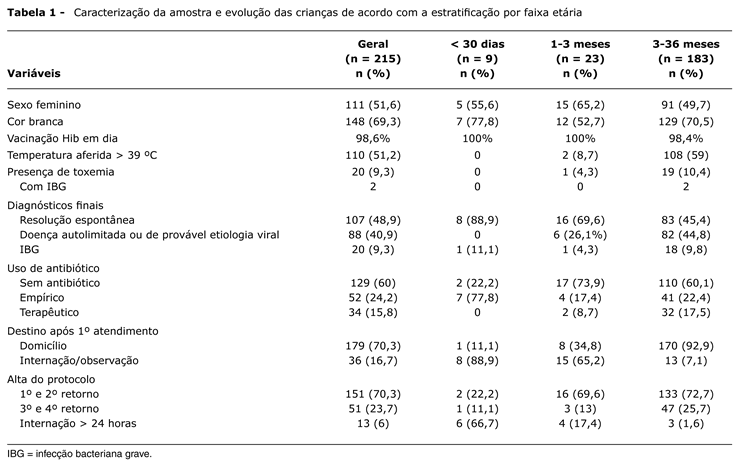
Durante o período de estudo foram incluídos 251 casos. Destes, foram excluídos 36: 27 por perda de contato (sem retorno para avaliação e/ou sem sucesso ao contato telefônico) e nove retirados do estudo (por solicitação dos pais, ou pela não coleta dos exames, ou a não manutenção do antibiótico por decisão dos pais). A caracterização da amostra e a evolução das crianças estão detalhadas na Tabela 1.
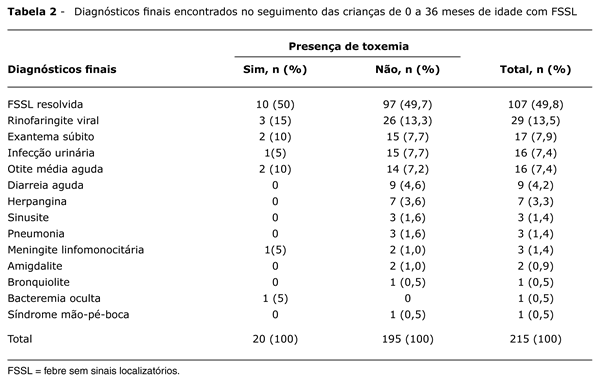
Das 215 crianças incluídas no protocolo, 20 se apresentavam toxemiadas na avaliação inicial. Os diagnósticos finais encontrados neste grupo e no grupo das crianças não toxemiadas estão listados na Tabela 2. Foram identificadas 20 crianças com IBG (9,3%): 16 com IU, três com pneumonia e uma com BO por Streptococcus pneumoniae. Foi colhido, por decisão do médico assistente, liquor em cinco crianças, não sendo identificada meningite bacteriana.
As crianças restantes (195), sem toxemia, apresentavam a seguinte distribuição quanto à idade: oito recém-nascidos, 22 lactentes jovens e 165 crianças de 3 a 36 meses. Os lactentes jovens foram classificados de acordo com os critérios de Rochester19, sendo considerados cinco como pacientes de alto risco para IBG e 17, como de baixo risco.
Das 165 crianças de entre 3 e 36 meses de idade e não toxêmicas, 68 (41,2%) tinham temperatura axilar ≤ 39 ºC e 97 (58,8%) apresentavam temperatura > 39 ºC. Estas últimas foram submetidas à triagem laboratorial.
Colheram sedimento urinário e urocultura 95 crianças e, destas, 10 apresentaram sedimento urinário com presença de mais de 100.000 leucócitos/mL, configurando-se então suspeita de IU e sendo iniciado tratamento. Todas elas apresentaram urocultura positiva. Das 85 que possuíam sedimento urinário normal ou leucocitúria ≤ 100.000/mL foram colhidos hemograma e hemocultura. Destas, 54 apresentavam hemograma com número total de leucócitos ≤ 20.000/mm3 e total de neutrófilos ≤ 10.000/mm3. Foram orientadas a retornar diariamente até resolução da febre e/ou identificação do foco infeccioso e resultado final das culturas colhidas. As 31 crianças restantes possuíam hemograma com contagem de leucócitos > 20.000/mm3 ou total de neutrófilos > 10.000/mm3. Foi realizada radiografia torácica em 23 crianças, sendo evidenciada pneumonia oculta em uma criança.
Das 215 crianças estudadas, 86 receberam antibioticoterapia: 34 (15,81%) de forma terapêutica e 52 (24,2%) empiricamente, sendo que sete crianças receberam antibioticoterapia empírica em desacordo com o protocolo (julgamento clínico). O tempo médio de duração do uso de antibiótico empírico foi de 72 horas. A presença de IBG foi evidenciada em sete (15,56%) das 45 crianças que receberam antibiótico empírico de acordo com o protocolo e não foi identificado qualquer caso de IBG nas crianças sem antibiótico. Dessa forma, das 215 crianças estudadas, 86 receberam antibiótico em algum momento e 129 (60%) não receberam antibioticoterapia.
Discussão
Neste estudo apresentamos um protocolo de atendimento para avaliação e seguimento das crianças de até 36 meses de idade com FSSL.
Desde a publicação do protocolo de Baraff et al.7, várias estratégias foram elaboradas para o atendimento e seguimento das crianças com FSSL1,2,4,15-17. Atualmente, as publicações discutem as mudanças que ocorreram após a introdução da vacina conjugada para pneumococo em 2001. Os artigos comparam a taxa de IBG, principalmente nas doenças invasivas por pneumococo, no que chamam de era pré e pós-introdução da vacina5,17,21-23. Já se observam reduções significativas das infecções invasivas por Streptococcus pneumoniae e, sendo assim, as intervenções nas crianças com FSSL devidamente vacinadas para hemófilos e pneumococo passam a ser observacionais8,15. Entretanto, esta não é a realidade do Brasil. Em nosso país, a vacinação para Hib faz parte do calendário vacinal, mas a vacina para pneumococo ainda não está incluída nos calendários oficiais. Portanto, a abordagem para avaliação e seguimento das crianças de até 36 meses com FSSL deve ser mais minuciosa, e os exames laboratoriais continuam sendo de grande auxílio na tomada de decisão.
A maioria dos estudos não detalha os diagnósticos finais, exceto em casos de IBG e com atenção especial à BO. Fica então difícil comparar nossos resultados gerais com a literatura. Galetto-Lacour et al.24 realizaram estudo com 124 crianças de até 36 meses com FSSL e identificaram 23% de casos de IBG, 10% de infecção bacteriana focal e 67% de provável infecção viral. Gervaix et al.4 relatam um estudo no qual no seguimento de crianças febris de até 2 anos de idade foi constatada a presença de 20,2% de crianças com FSSL; destas, 17,3% tinham IBG. Na nossa casuística, a grande maioria das crianças apresentou melhora espontânea do quadro febril (49,8%). A presença de doença benigna autolimitada ou de provável etiologia viral foi observada em 40,9%. A IBG foi identificada em 9,3% das crianças.
A IU é a infecção bacteriana mais comum nas crianças com FSSL, principalmente nas meninas. A prevalência geral de IU é de 2 a 5% em crianças febris menores de 2 anos de idade20. Nesta faixa etária, a febre é frequentemente a única manifestação de IU8,9,15,20. Na nossa casuística, a IU foi a IBG mais encontrada.
Nos menores de 3 meses de idade, vários aspectos fisiopatológicos, epidemiológicos e etiológicos são diferentes daqueles das crianças acima dessa faixa etária1,2,9,25. As IBG são mais comuns nesta faixa etária, principalmente nos recém-nascidos. Alguns estudos mostram a ocorrência de IBG em aproximadamente 10% dos lactentes febris de 1 a 2 meses de idade e em até 13% dos recém-nascidos9,25. Portanto, este grupo etário continua sendo abordado de maneira mais agressiva no intuito de se identificar o mais precocemente possível as IBG. A nossa casuística é pequena para esta faixa etária (nove recém-nascidos e 23 lactentes jovens).
Mukai et al.26 realizaram estudo prospectivo com 82 lactentes febris menores de 2 meses de idade atendidos no PSHU-USP. As crianças permaneceram em observação no pronto-socorro por pelo menos 24 horas para avaliação, triagem laboratorial e início de terapêutica. Após este período, 65 crianças foram liberadas para o domicílio, e, destas, três tiveram que ser internadas. Chegou-se à conclusão de que o período de 24 horas de observação associado à triagem laboratorial era suficiente para a avaliação e indicação de seguimento ambulatorial destes lactentes. No nosso estudo, para os lactentes jovens considerados de baixo risco para IBG foi assegurada a avaliação ambulatorial com retornos diários em nosso pronto-socorro após observação clínica por 12 a 24 horas.
As crianças de 3 a 36 meses não toxêmicas são o grupo de maior controvérsia no que se refere à abordagem. Segundo Baraff15 e o American College of Emergency Physicians Clinical Policy Committee8, as crianças com FSSL de 3 a 36 meses de idade que não têm IU e que não receberam vacinas conjugadas para pneumococo, ou que possuem imunização incompleta (duas doses ou menos), devem seguir a seguinte orientação: coleta de hemograma nas crianças com temperatura > 39 ºC com introdução de antibioticoterapia empírica quando o número total de leucócitos for > 15.000/mm3 e radiografia torácica quando o número de leucócitos for > 20.000/mm3. Na nossa casuística, apenas duas crianças estavam vacinadas para pneumococo.
No nosso estudo, foi utilizado como ponto de corte para tomada de decisão sobre antibioticoterapia empírica o número total de leucócitos > 20.000/mm3 ou o número total de neutrófilos > 10.000/mm318,27. Esta escolha teve o objetivo de aumentar a especificidade para o reconhecimento da IBG e reduzir a utilização de antibioticoterapia empírica. Em contrapartida, o seguimento clínico teve que ser assegurado. A antibioticoterapia empírica é outro ponto de grande controvérsia nestas estratégias. A introdução de antibiótico empírico pode reduzir as IBG e suas complicações12,13,28-30. Entretanto, o uso exagerado de antibióticos pode ter um impacto no aumento das taxas de resistência bacteriana.
Uma das limitações do nosso estudo foi a perda do seguimento de 36 crianças (14,34%). Na maioria dos casos (27), isto ocorreu pela perda de contato, o que é justificável nos estudos com este tipo de população. As restantes nove crianças foram excluídas da casuísta por decisão dos familiares ou por não aderirem ao protocolo. Estas foram acompanhadas até o final com resolução espontânea do quadro febril, mas os resultados não foram computados na nossa casuística.
Conclusões
Após 15 anos da publicação da estratégia proposta por Baraff et al.7, inúmeros desdobramentos no conhecimento da BO e da IBG acarretaram mudanças de atitude frente a uma criança com FSSL. O diagnóstico e seguimento destas crianças continuam sendo objetos de intensa discussão e evoluem constantemente com o resultado de inúmeras pesquisas, otimização das técnicas de laboratório, utilização de novos marcadores de IBG, estudos para identificação rápida de vírus e controle de doenças virais, assim como com o advento de novas vacinas.
Todavia, nenhuma combinação de exames laboratoriais e avaliação clínica identificam, na avaliação inicial, todos os pacientes que têm IBG. Nenhuma estratégia tem a sensibilidade e especificidade desejada pelos médicos. A reavaliação e a instrução dos responsáveis para que frente a qualquer deterioração da condição da criança retornem para avaliação médica são pontos fundamentais. Qualquer protocolo de atendimento da criança febril deve servir como um suplemento, e não como um substituto, para a avaliação clínica. Entretanto, estes protocolos continuarão sendo úteis.
Independentemente dos progressos alcançados, o segredo da avaliação das crianças com FSSL repousa na habilidade clínica da equipe médica para identificação e seguimento das crianças de risco para IBG associada à interação com a família.
Por fim, o protocolo elaborado mostrou-se adequado para o seguimento das crianças com FSSL de até 36 meses de idade que fizeram coleta de exames simples e passíveis de serem realizados na maioria dos serviços. Todas as crianças que apresentaram IBG foram identificadas, se não no início da avaliação, durante seu seguimento.
Agradecimentos
Agradecemos a toda a equipe do PSHU-USP pelo apoio para a realização deste estudo, em especial aos médicos assistentes Denise M. Lellis Garcia, Eloisa C. Souza, Rodrigo P. P. Locatelli, João Paulo B. Lotufo, Maki Hirose, Fabíola Stollar, Renato C. Calheiros, Álvaro R. Bueno, Sergio M. Horita, Juliana Mendes, Heloisa M. Sabino e Matheus D. Leme.
Artigo submetido em 02.03.09, aceito em 03.06.09.
Este trabalho foi realizado na Divisão de Clínica Pediátrica, Hospital Universitário, Universidade de São Paulo (USP), São Paulo, SP, e no Departamento de Pediatria, Faculdade de Medicina, USP, São Paulo, SP.
Não foram declarados conflitos de interesse associados à publicação deste artigo.
Como citar este artigo: Machado BM, Cardoso DM, de Paulis M, Escobar AM, Gilio AE. Fever without source: evaluation of a guideline. J Pediatr (Rio J). 2009;85(5):426-432.
- 1. Trotta EA, Gilio AE. Febre aguda sem sinais de localização em crianças menores de 36 meses de idade. J Pediatr (Rio J). 1999;75:s214-s22.
- 2. Baraff LJ. Management of fever without source in infants and children. Ann Emerg Med. 2000;36:602-14.
- 3. Singer JI, Vest J, Prints A. Occult bacteremia and septicemia in the febrile child younger than two years. Emerg Med Clin North Am. 1995;13:381-416.
- 4. Gervaix A, Caflisch M, Suter S. Pediatrie au Quotidien: Prise en charge des enfants fébriles sans signes localisateurs d'un foyer infectieux. Arch Pédiatr. 2001;8:324-30.
- 5. Akintemi OB, Roberts KB. Evaluation and management of the febrile child in the conjugated vaccine era. Adv Pediatr. 2006;53:255-78.
- 6. Mahajan P, Stanley R. Fever in the toddler-aged child: old concerns replaced with new ones. Clin Pediatr Emerg Med. 2008;9:221-7.
- 7. Baraff LJ, Bass JW, Fleisher GR, Klein JO, McCracken GH, Powell KR, et al. Practice guideline for the management of infants and children with fever without source 0-36 months of age. Pediatrics. 1993;92:1-12.
- 8. American College of Emergency Physicians Clinical Policies Committee; American College of Emergency Physicians Clinical Policies Subcommittee on Pediatric Fever. Clinical policy for children younger than three years presenting to the emergency department with fever. Ann Emerg Med. 2003;42:530-45.
- 9. Avner JR, Baker D. Management of fever in infants children. Emerg Med Clin North Am. 2002;20:49-67.
- 10. McGowan JE Jr, Bratton L, Klein JO, Finland M. Bacteremia in febrile children seen in a "walk-in" pediatric clinic. N Engl J Med. 1973;288:1309-12.
- 11. Teele DW, Pelton SI, Grant MJ, Herskowitz J, Rosen DJ, Allen CE, et al. Bacteremia in febrile children under 2 years of age: results of cultures of blood of 600 consecutive febrile children seen in a "walk-in" pediatric clinic. J Pediatr. 1975;87:227-30.
- 12. Baraff LJ, Lee SI. Fever without source: management of children 3 to 36 months of age. Pediatr Infect Dis J. 1992;11:146-51.
- 13. Bass JW, Steele RW, Wittler RR, Weisse ME, Bell V, Heisser AH, et al. Antimicrobial treatment of occult bacteremia: a multicenter cooperative study. Pediatr Infect Dis J. 1993;12:466-73.
- 14. Fleisher GR, Rosenberg N, Vinci R, Steinberg J, Powell K, Christy C, et al. Intramuscular versus oral antibiotic therapy for the prevention of meningitis and other bacterial sequelae in young, febrile children at risk for occult bacteremia. J Pediatr. 1994;24:504-12.
- 15. Baraff LJ. Editorial: Clinical policy for children younger than three years presenting to the emergency department with fever. Ann Emerg Med. 2003;42:546-9.
- 16. Belfer RA, Gittelman MA, Muniz AE. Management of febrile infants and children by pediatric emergency medicine and emergency medicine: comparison with practice guidelines. Pediatr Emerg Care. 2001;17:837.
- 17. Klein JO. Management of the febrile child without a focus in the era of universal pneumococcal immunization. Pediatr Infect Dis J. 2002;21:584-8.
- 18. Kuppermann N. Occult bacteremia in young febrile children. Pediatr Clin North Am. 1999;46:1073-109.
- 19. Dagan R, Powell KR, Hall CB, Menegus MA. Identification of infants unlikely to have serious bacterial infection although hospitalized for suspected sepsis. J Pediatr. 1985;107:855-60.
- 20. Practice parameter: the diagnosis, treatment, and evaluation of the initial urinary tract infection in febrile infants and young children. American Academy of Pediatrics. Committee on Quality Improvement. Subcommittee on Urinary Tract Infection. Pediatrics. 1999;103:843-52.
- 21. Lee GM, Fleisher GR, Harper MB. Management of febrile children in the age of the conjugate pneumococcal vaccine: a cost-effectiveness analysis. Pediatrics. 2001;108:835-44.
- 22. Herz AM, Greenhow TL, Alcantara J, Hansen J, Baxter RP, Black SB, et al. Changing epidemiology of outpatient bacteremia in 3- to 36-month-old children after the introduction of the heptavalent-conjugated pneumococcal vaccine. Pediatr Infect Dis J. 2006;25:293-300.
- 23. Kuppermann N. The evaluation of young febrile children for occult bacteremia: time to reevaluate our approach? Arch Pediatr Adolesc Med. 2002;156:855-7.
- 24. Lacour AG, Gervaix A, Zamora SA, Vadas L, Lombard PR, Dayer JM, et al. Procalcitonin, IL-6, IL-8, IL-1 receptor antagonist and C-reactive protein as identificators of serious bacterial infections in children with fever without localising signs. Eur J Pediatr. 2001;160:95-100.
- 25. Baker MD, Avner JR. The febrile infant: What's new? Clin Pediatr Emerg Med. 2008;9:213-20.
- 26. Mukai LS, Ejzenberg B, Lotufo JP, Barbante LF, Yamashita CA, Vieira SE, et al. Febre no lactente jovem atendido em serviço de emergência: Aspectos diagnósticos e terapêuticos. J Pediatr (Rio J). 1995;71:322-30.
- 27. Kuppermann N, Fleisher GR, Jaffe DM. Predictors of occult pneumococcal bacteremia in young febrile children. Ann Emerg Med. 1998;31:67987.
- 28. Baraff LJ, Oslund S, Prather M. Effect of antibiotic therapy and etiologic microorganism on the risk of bacterial meningitis in children with occult bacteremia. Pediatrics. 1993;92:140-3.
- 29. Harper MB, Bachur R, Fleisher GR. Effect of antibiotic therapy on the outcome of outpatients with unsuspected bacteremia. Pediatr Infect Dis J. 1995;14:760-7.
- 30. Bulloch B, Craig WR, Klassen TP. The use of antibiotics to prevent serious sequelae in children at risk for occult bacteremia: a meta-analysis. Acad Emerg Med. 1997;4:67983.
Correspondência:
Datas de Publicação
-
Publicação nesta coleção
28 Out 2009 -
Data do Fascículo
Out 2009
Histórico
-
Aceito
03 Jun 2009 -
Recebido
02 Mar 2009