Resumos
JUSTIFICATIVA E OBJETIVOS: O desenvolvimento de sistemas de liberação controlada tem sido alvo de pesquisas há pelo menos quatro décadas. Desde que foi sugerida sua aplicação na indústria farmacêutica, muitos resultados foram obtidos, especialmente na manipulação molecular de carreadores e no estudo de suas interações com as drogas encapsuladas. Esses novos carreadores têm a vantagem de contornar propriedades físico-químicas limitantes (como a solubilidade aquosa ou em membranas) das drogas encapsuladas, melhorando assim a farmacodinâmica (potencialização do efeito terapêutico), farmacocinética (controle da absorção e distribuição tecidual) e os efeitos toxicológicos (redução da toxicidade local e sistêmica) das mesmas. Entre os principais carreadores, destacam-se os lipossomas e as ciclodextrinas, que vêm trazendo inúmeras vantagens no desenvolvimento de formulações para liberação controlada de anestésicos locais. Este trabalho de revisão objetiva descrever a interação de anestésicos locais com lipossomas ou ciclodextrinas, o desenvolvimento das pesquisas básica e clínica nessa área, além da aplicabilidade terapêutica dessas formulações. CONTEÚDO: Lipossomas têm a capacidade de veicular drogas em órgãos-alvo, disponibilizando apenas uma fração - liberação controlada - para o sítio de ação. Já as ciclodextrinas alteram a intensidade e a duração do efeitos das drogas através da baixa absorção sistêmica do complexo. Pesquisas básicas e clínicas apontam como vantagens do uso de anestésicos locais encapsulados em lipossomas ou complexados com ciclodextrinas a liberação lenta da droga que prolonga a duração da anestesia e reduz a toxicidade para os sistemas cardiovascular e nervoso central. CONCLUSÕES: Embora várias pesquisas ainda estejam em andamento, os sistemas de liberação controlada de anestésicos locais indicam uma nova direção no desenvolvimento de formulações anestésicas mais eficazes e seguras.
ANESTÉSICOS
JUSTIFICATIVA Y OBJETIVOS: El desenvolvimiento de sistemas de liberación controlada ha sido motivo de pesquisas desde cuatro décadas por lo menos. Desde que fue sugerida su aplicación en la industria farmacéutica, fueron obtenidos muchos resultados, especialmente en la manipulación molecular de carreadores y en el estudio de sus interacciones con las drogas encapsuladas. Esos nuevos carreadores tienen la ventaja de contornar propiedades físico-químicas limitantes (como la solubilidad acuosa o en membranas) de las drogas encapsuladas, mejorando asi la farmacodinámica (potencialización del efecto terapéutico), farmacocinética (control de la absorción y distribución de tejidos) y los efectos toxicológicos (reducción de la toxicidad local y sistémica) de las mismas. Entre los principales carreadores, se destacan los liposomas y las ciclodextrinas, que están trayendo innúmeras ventajas en el desarrollo de formulaciones para liberación controlada de anestésicos locales. Este trabajo de revisión, objetiva describir la interacción de anestésicos locales con liposomas o ciclodextrinas, el desarrollo de las pesquisas básica y clínica en esa área, además de la aplicabilidad terapéutica de esas formulaciones. CONTENIDO: Liposomas tienen la capacidad de transportar drogas en órganos-clave, disponibilizando apenas una fracción - liberación controlada - para el sitio de acción. Ya las ciclodextrinas alteran la intensidad y la duración de efectos de las drogas a través de la baja absorción sistémica del complejo. Pesquisas básicas y clínicas, apuntan como ventajas del uso de anestésicos locales encapsulados en liposomas o complejos con ciclodextrinas la liberación lenta de la droga que prolonga la duración de la anestesia, y reduce la toxicidad para los sistemas cardiovascular y nervioso central. CONCLUSIONES: No obstante varias pesquisas están aún en andamiento, los sistemas de liberación controlada de anestésicos locales indican una nueva dirección en el desarrollo de formulaciones anestésicas más eficaces y seguras.
BACKGROUND AND OBJECTIVES: Many researchers in the last four decades have been devoted to the development of drug-delivery systems. Since its first application in the pharmaceutical industry, many results have been obtained especially in the molecular manipulation of carriers and their interaction with encapsulated drugs. These new carriers have the advantage of bypassing encapsulated drugs restraining physicochemical properties (such as water or membrane solubility), thus improving pharmacodynamics (therapeutic effect potentiation), pharmacokinetics (control of tissue absorption and distribution) and toxic effects (lower local and systemic toxicity). Liposomes and cyclodextrins are among the most important carriers which have shown to be quite advantageous in the development of drug-delivery systems for local anesthetics. This study aimed at reviewing the interaction of local anesthetics with liposomes and cyclodextrins, the development of basic and applied research on the field, in addition to therapeutic applicability of these formulations. CONTENTS: Liposomes have the ability to control drug delivery to target tissues, fractionating drug release in its site of action. Cyclodextrins, on the other hand, change intensity and duration of effects due to low systemic drug absorption. Basic and clinical studies have pointed out that the administration of local anesthetics in liposome or cyclodextrin formulations induces slow release of the drugs, prolonging the anesthetic action and decreasing cardiac and nervous systems toxicity. CONCLUSIONS: Although studies are still in progress, drug-delivery systems are flagging a new direction for the development of safer and more effective local anesthetic formulations.
ANESTHETICS
ARTIGO DIVERSO
Formulações de anestésicos locais de liberação controlada: aplicações terapêuticas* * Recebido do Departamento de Bioquímica, Instituto de Biologia da Universidade Estadual de Campinas, UNICAMP
Drug-delivery systems for local anesthetics: therapeutic applications
Formulaciones de anestésicos locales de liberación controlada: aplicaciones terapéuticas
Daniele Ribeiro de AraújoI; Luciana de Matos Alves PintoII; Angélica de Fátima de Assunção Braga, TSAIII; Eneida de PaulaIV
IDoutoranda em Biologia Funcional e Molecular, Bioquímica, Universidade Estadual de Campinas, UNICAMP
IIDoutora em Biologia Funcional e Molecular, Bioquímica, Universidade Estadual de Campinas, UNICAMP
IIIProfessora Doutora do Departamento de Anestesiologia da Faculdade de Ciências Médicas da Universidade de Campinas, UNICAMP
IVProfessora Associada (MS5) do Departamento de Bioquímica, Instituto de Biologia da Universidade Estadual de Campinas, UNICAMP
Endereço para Correspondência Endereço para Correspondência Dra. Daniele Ribeiro de Araújo Deptº de Bioquímica, Instituto de Biologia UNICAMP Caixa Postal, 6109 13083-970 Campinas, SP E-mail: daraujo@unicamp.br
RESUMO
JUSTIFICATIVA E OBJETIVOS: O desenvolvimento de sistemas de liberação controlada tem sido alvo de pesquisas há pelo menos quatro décadas. Desde que foi sugerida sua aplicação na indústria farmacêutica, muitos resultados foram obtidos, especialmente na manipulação molecular de carreadores e no estudo de suas interações com as drogas encapsuladas. Esses novos carreadores têm a vantagem de contornar propriedades físico-químicas limitantes (como a solubilidade aquosa ou em membranas) das drogas encapsuladas, melhorando assim a farmacodinâmica (potencialização do efeito terapêutico), farmacocinética (controle da absorção e distribuição tecidual) e os efeitos toxicológicos (redução da toxicidade local e sistêmica) das mesmas. Entre os principais carreadores, destacam-se os lipossomas e as ciclodextrinas, que vêm trazendo inúmeras vantagens no desenvolvimento de formulações para liberação controlada de anestésicos locais. Este trabalho de revisão objetiva descrever a interação de anestésicos locais com lipossomas ou ciclodextrinas, o desenvolvimento das pesquisas básica e clínica nessa área, além da aplicabilidade terapêutica dessas formulações.
CONTEÚDO: Lipossomas têm a capacidade de veicular drogas em órgãos-alvo, disponibilizando apenas uma fração - liberação controlada - para o sítio de ação. Já as ciclodextrinas alteram a intensidade e a duração do efeitos das drogas através da baixa absorção sistêmica do complexo. Pesquisas básicas e clínicas apontam como vantagens do uso de anestésicos locais encapsulados em lipossomas ou complexados com ciclodextrinas a liberação lenta da droga que prolonga a duração da anestesia e reduz a toxicidade para os sistemas cardiovascular e nervoso central.
CONCLUSÕES: Embora várias pesquisas ainda estejam em andamento, os sistemas de liberação controlada de anestésicos locais indicam uma nova direção no desenvolvimento de formulações anestésicas mais eficazes e seguras.
Unitermos: ANESTÉSICOS: Local
SUMMARY
BACKGROUND AND OBJECTIVES: Many researchers in the last four decades have been devoted to the development of drug-delivery systems. Since its first application in the pharmaceutical industry, many results have been obtained especially in the molecular manipulation of carriers and their interaction with encapsulated drugs. These new carriers have the advantage of bypassing encapsulated drugs restraining physicochemical properties (such as water or membrane solubility), thus improving pharmacodynamics (therapeutic effect potentiation), pharmacokinetics (control of tissue absorption and distribution) and toxic effects (lower local and systemic toxicity). Liposomes and cyclodextrins are among the most important carriers which have shown to be quite advantageous in the development of drug-delivery systems for local anesthetics. This study aimed at reviewing the interaction of local anesthetics with liposomes and cyclodextrins, the development of basic and applied research on the field, in addition to therapeutic applicability of these formulations.
CONTENTS: Liposomes have the ability to control drug delivery to target tissues, fractionating drug release in its site of action. Cyclodextrins, on the other hand, change intensity and duration of effects due to low systemic drug absorption. Basic and clinical studies have pointed out that the administration of local anesthetics in liposome or cyclodextrin formulations induces slow release of the drugs, prolonging the anesthetic action and decreasing cardiac and nervous systems toxicity.
CONCLUSIONS: Although studies are still in progress, drug-delivery systems are flagging a new direction for the development of safer and more effective local anesthetic formulations.
Key Words: ANESTHETICS: Local
RESUMEN
JUSTIFICATIVA Y OBJETIVOS: El desenvolvimiento de sistemas de liberación controlada ha sido motivo de pesquisas desde cuatro décadas por lo menos. Desde que fue sugerida su aplicación en la industria farmacéutica, fueron obtenidos muchos resultados, especialmente en la manipulación molecular de carreadores y en el estudio de sus interacciones con las drogas encapsuladas. Esos nuevos carreadores tienen la ventaja de contornar propiedades físico-químicas limitantes (como la solubilidad acuosa o en membranas) de las drogas encapsuladas, mejorando asi la farmacodinámica (potencialización del efecto terapéutico), farmacocinética (control de la absorción y distribución de tejidos) y los efectos toxicológicos (reducción de la toxicidad local y sistémica) de las mismas. Entre los principales carreadores, se destacan los liposomas y las ciclodextrinas, que están trayendo innúmeras ventajas en el desarrollo de formulaciones para liberación controlada de anestésicos locales. Este trabajo de revisión, objetiva describir la interacción de anestésicos locales con liposomas o ciclodextrinas, el desarrollo de las pesquisas básica y clínica en esa área, además de la aplicabilidad terapéutica de esas formulaciones.
CONTENIDO: Liposomas tienen la capacidad de transportar drogas en órganos-clave, disponibilizando apenas una fracción - liberación controlada - para el sitio de acción. Ya las ciclodextrinas alteran la intensidad y la duración de efectos de las drogas a través de la baja absorción sistémica del complejo. Pesquisas básicas y clínicas, apuntan como ventajas del uso de anestésicos locales encapsulados en liposomas o complejos con ciclodextrinas la liberación lenta de la droga que prolonga la duración de la anestesia, y reduce la toxicidad para los sistemas cardiovascular y nervioso central.
CONCLUSIONES: No obstante varias pesquisas están aún en andamiento, los sistemas de liberación controlada de anestésicos locales indican una nueva dirección en el desarrollo de formulaciones anestésicas más eficaces y seguras.
INTRODUÇÃO
Há muito existe a preocupação em compreender o fenômeno da dor e, conseqüentemente, conceituá-lo. Segundo a Associação Internacional para o Estudo da Dor, esse fenômeno é caracterizado por uma experiência sensitiva e emocional desagradável, em que há percepção de um estímulo nocivo associado à lesão tecidual real ou potencial. De acordo com a duração da lesão tecidual pode-se classificar a dor em aguda ou de curta duração, que persiste apenas enquanto durar o dano representando uma reação fisiológica normal; e a dor crônica ou lenta, associada às lesões mais profundas, evidenciando-se quando cessa a função dos mecanismos normais de cicatrização e estados patológicos que podem persistir por um longo período, como câncer, artrite reumatóide e pinçamentos nervosos 1.
Apesar de incômoda, a dor desempenha uma função biológica essencial. É a resposta do organismo a um determinado ou potencial trauma. Porém, em algumas situações, o sofrimento doloroso perde sua função biológica e começa a representar uma conseqüência insuportável às desordens refratárias ao tratamento. Por isso, a capacidade de instituir novos métodos de tratamento com o objetivo de produzir analgesia, isto é, aliviar ou eliminar a dor, é um desafio atual.
Os avanços nas pesquisas básica e clínica têm expandido as opções na farmacoterapia da dor. Para pacientes com câncer ou dor neuropática, por exemplo, a farmacoterapia é a principal ou senão a única saída para mantê-la sob controle. Muitos fármacos têm sido utilizados (anticonvulsivantes, agonistas GABAérgicos, neurolépticos), inclusive, a combinação de anestésicos locais e analgésicos opióides (bupivacaína - morfina) tem sido sugerida tanto para tratamento da dor pós-operatória quanto para a dor neuropática em pacientes que não respondem ao tratamento somente com opióides, pois a liberação subaracnóidea da combinação resulta em um ritmo mais lento no aparecimento da tolerância aos opióides. Porém, pesquisas ainda são necessárias para a determinação dos limites de toxicidade dessa associação 2,3.
A dor também pode ser controlada pelo uso de anestésicos locais para o bloqueio de nervos periféricos específicos, embora esses fármacos apresentem limitações devido a sua duração de ação relativamente curta (2 a 4 horas). Nas últimas décadas, alguns anestésicos locais como lidocaína, bupivacaína e, mais recentemente, levobupivacaína e ropivacaína, têm sido introduzidos na terapia da dor aguda e crônica na tentativa de melhorar a ação dos fármacos já utilizados 4.
As características desejáveis para uma molécula anestésica são: a longa duração de ação, diminuição da toxicidade local e/ou sistêmica e aumento da seletividade para o bloqueio sensorial, em relação ao bloqueio motor 5. Com a alteração de propriedades físicas e químicas na molécula dos anestésicos locais (síntese direcionada por estudos de correlação estrutura-função), alguns desses objetivos têm sido atingidos. Mas uma alternativa, que atualmente vem promovendo os efeitos desejáveis, é a liberação controlada desses fármacos através da encapsulação em lipossomas e/ou outros veículos, como complexos com ciclodextrinas 6.
LIPOSSOMAS
Os lipossomas, descobertos em 1963, consistem de esferas microscópicas de tamanhos variados (em escalas de nm e µm) com uma ou mais bicamadas lipídicas concêntricas separadas por compartimentos aquosos, onde as caudas hidrofóbicas dos lipídios estão voltadas para o interior e as cabeças polares para o exterior da bicamada (Figura 1), mantendo contato com a fase aquosa 7.
Revista Brasileira de Anestesiologia, 2003; 53: 5: 663 - 671
Formulações de Anestésicos Locais de Liberação Controlada: Aplicações Terapêuticas
Daniele Ribeiro de Araújo; Luciana de Matos Alves Pinto; Angélica de Fátima de Assunção Braga; Eneida de Paula
A natureza da interação entre os lipídios, a composição dos mesmos e o método de preparação determinam o padrão, o tamanho e o número de bicamadas formadas, sendo os lipossomas (quanto ao número de bicamadas) classificados em vesículas multi (MLV) ou unilamelares (LUV) (Figura 1 e Figura 2), influenciando diretamente na absorção, distribuição, metabolismo, eliminação e no perfil de toxicidade das drogas encapsuladas 8. O tamanho do lipossoma afeta a biodistribuição, pois, após administração subcutânea, lipossomas menores que 120 nm atravessam rapidamente os capilares, enquanto que lipossomas maiores (com cerca de 200 nm ou mais) tendem a permanecer no local de injeção 9.
Revista Brasileira de Anestesiologia, 2003; 53: 5: 663 - 671
Formulações de Anestésicos Locais de Liberação Controlada: Aplicações Terapêuticas
Daniele Ribeiro de Araújo; Luciana de Matos Alves Pinto; Angélica de Fátima de Assunção Braga; Eneida de Paula
Já a encapsulação de drogas é orientada pela hidro ou lipofilicidade das mesmas. Drogas hidrofílicas têm tendência a permanecer no compartimento central aquoso e drogas hidrofóbicas encontram-se dispersas na bicamada lipídica (Figura 2). Além disso, drogas lipofílicas permanecem mais tempo encapsuladas devido ao alto particionamento na fase membranar 10.
A função dos lipossomas como veículos é liberar determinadas concentrações de drogas em alvos específicos, evitando a toxicidade sistêmica, já que somente uma fração da droga está disponível para o local de ação 9.
A similaridade dos monômeros lipídicos constituintes dos lipossomas (fosfatidilcolina derivada de ovo, soja ou sintéticas e colesterol, em geral) com as membranas biológicas elimina o risco de antigenicidade ou lesões histológicas após a administração desses veículos 11.
Lipossomas têm sido utilizados em imunoensaios 12 e como sistemas de liberação controlada para várias drogas incluindo antivirais 13, antifúngicos 14 , no desenvolvimento de vacinas 15 e de medicamentos anti-câncer 16 e também para melhorar as propriedades terapêuticas de anestésicos locais.
Trabalhos realizados em animais de laboratório e em humanos, utilizando bupivacaína em lipossomas multilamelares, apresentaram resultados satisfatórios no tratamento da dor crônica e pós-operatória com relação ao aumento na duração da anestesia, do bloqueio nervoso diferencial (potencialização da analgesia sem bloqueio motor), além de permitir o controle dos níveis sistêmicos da droga 11, 17-23.
Uma interessante revisão sobre o uso de anestésicos locais e opióides encapsulados em lipossomas foi feita por Simonetti e col. 24 e publicada nesta revista. De maneira geral, pode-se dizer que o uso de anestésicos locais encapsulados em lipossomas tem como vantagens a liberação lenta da droga, prolongando a duração da anestesia e a redução da toxicidade para os sistemas cardiovascular e nervoso central 25,26.
CICLODEXTRINAS
A hidrólise enzimática do amido usualmente resulta na formação de glicose, maltose e em uma longa classe de dextrinas lineares e ramificadas. No entanto, alguns microorganismos e plantas (que produzem enzimas denominadas ciclodextrina glicosiltransferases) são capazes de degradar o amido em produtos cíclicos chamados ciclodextrinas 27,28.
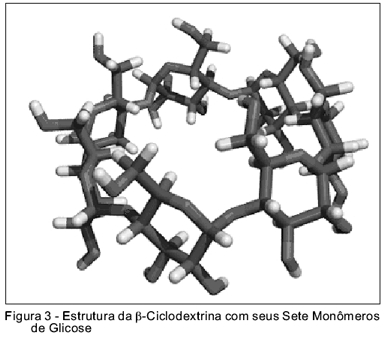
As três ciclodextrinas naturais são a alfa (a-ciclodextrina), beta (b-ciclodextrina) (Figura 3)e gama (g-ciclodextrina) compostas de seis, sete e oito unidades de D-(+)-glicopiranose, respectivamente. Esses agentes têm em sua estrutura grupos hidroxil primários e secundários orientados para o exterior. Portanto, possuem um exterior hidrofílico e uma cavidade interna relativamente hidrofóbica que, por sua vez, permite as ciclodextrinas complexarem-se com moléculas que apresentam dimensões compatíveis com a sua cavidade. A complexação altera propriedades físico-químicas, como a solubilidade em água, estabilidade e biodisponibilidade de drogas complexadas 29.
Revista Brasileira de Anestesiologia, 2003; 53: 5: 663 - 671
Formulações de Anestésicos Locais de Liberação Controlada: Aplicações Terapêuticas
Daniele Ribeiro de Araújo; Luciana de Matos Alves Pinto; Angélica de Fátima de Assunção Braga; Eneida de Paula
A habilidade das ciclodextrinas de formarem complexos de inclusão depende essencialmente da compatibilidade estérica e da polaridade com a droga. Além disso, as forças que dirigem a complexação têm sido atribuídas à alta energia de repulsão da água na cavidade das ciclodextrinas, às interações de van der Waals, pontes de hidrogênio e interações hidrofóbicas 30, já que a cavidade interna tem diâmetros de 5 a 8Å 28, sendo grande o bastante para acomodar um hexanel aromático, no caso da b-ciclodextrina 31.
As moléculas complexadas permanecem, normalmente, orientadas em posição onde há o máximo contato entre sua porção hidrofóbica e a cavidade apolar (Figura 4), estando sua porção hidrofílica em contato com os grupos hidroxil da ciclodextrina 32.
Revista Brasileira de Anestesiologia, 2003; 53: 5: 663 - 671
Formulações de Anestésicos Locais de Liberação Controlada: Aplicações Terapêuticas
Daniele Ribeiro de Araújo; Luciana de Matos Alves Pinto; Angélica de Fátima de Assunção Braga; Eneida de Paula
As b-ciclodextrinassão as dextrinas cíclicas mais largamente utilizadas para a complexação com várias classes de drogas, como: agentes antitumorais (doxorubicina) 33, antidiabéticos (tolbutamida) 34 e antiinflamatórios (piroxicam) 35, que podem ser administrados por diversas vias como subaracnóidea, venosa, muscular, peridural, oral, nasal e dérmica 27, 33-36.
As ciclodextrinas naturais, em particular a b-ciclodextrina, têm solubilidade aquosa limitada (16,4 mM ou 18,6 mg/ml) e a formação de complexos com compostos lipofílicos geralmente resulta em precipitação dos complexos sólidos, se o limite de solubilidade for atingido. Assim, numerosas modificações na estrutura química das b-ciclodextrinas têm sido feitas, originando derivados mais solúveis como 2,6-dimetil-b-ciclodextrina (DM-b-ciclodextrina), 2-hidroxipropil-b-ciclodextrina (HP-b-ciclodextrina) e ciclodextrinas sulfatadas como sulfobutiléter-b-ciclodextrina (SBE-b-ciclodextrina) 37.
Além da estabilização, a modificação da farmacocinética e das propriedades biofarmacêuticas das drogas são os efeitos mais significantes da complexação com ciclodextrinas. Esses efeitos são observados especialmente na solubilidade e na liberação da droga complexada. Como conseqüência disso, a administração de fármacos complexados com b-ciclodextrina altera a intensidade e a duração de seus efeitos através da baixa absorção sistêmica das drogas 32.
Essa propriedade das ciclodextrinas torna bastante promissor seu uso para a complexação com anestésicos locais. Além disso, estudos indicam que a utilização de b-ciclodextrina e alguns de seus derivados (dimetil e hidroxipropil b-ciclodextrina) aumentam a solubilidade de anestésicos locais - como etidocaína, lidocaína, prilocaína, mepivacaína e, especialmente, bupivacaína - bem como melhoram os índices terapêuticos das drogas complexadas 38-42.
CONCLUSÕES
O benefício terapêutico das várias drogas administradas na forma tradicional é, algumas vezes, limitado pelas propriedades físico-químicas (solubilidade) e toxicológicas das mesmas ou até por barreiras fisiológicas. Através do desenvolvimento de sistemas de liberação controlada é possível manipular algumas dessas propriedades além de melhorar os efeitos terapêuticos das drogas, favorecendo sua utilização clínica. As pesquisas com formulações de anestésicos locais de liberação controlada têm mostrado resultados promissores.
Estudos em pacientes demonstraram a aplicabilidade e eficácia da encapsulação de bupivacaína (0,5 %) em lipossomas por administração peridural e infiltração no plexo braquial, no tratamento da dor pós-cirúrgica e dor crônica oncológica. Foi observada uma maior duração da analgesia, quando comparada àquela obtida após administração do anestésico local livre, além da potencialização do bloqueio nervoso diferencial. Esses resultados podem ser atribuídos à manutenção de altos níveis da droga no local de injeção 22,23. Apesar dos grandes avanços no desenvolvimento dessas formulações, estudos ainda são necessários para a determinação da razão de liberação dos anestésicos em lipossomas e estabilidade das preparações, bem como para o controle de alguns efeitos como indução de bloqueio simpático. Por isso, modificações nos métodos de preparação e/ou variações na composição dos lipossomas têm sido utilizadas com o objetivo de aumentar a eficiência e a encapsulação de anestésicos locais 43-46.
Com relação à complexação de anestésicos locais com ciclodextrinas, a utilização de derivados (menos tóxicos e mais solúveis) das b-ciclodextrinas com bupivacaína têm demonstrado um aumento no efeito anestésico aliado ao controle da absorção sistêmica da droga após administração epidural e infiltração intramuscular em animais de laboratório, promovendo a formulação como um sistema de liberação controlada potencialmente eficaz na farmacoterapia da dor 40-42. Porém, essas formulações ainda necessitam ser submetidas a ensaios para avaliação da neurotoxicidade local de forma a garantir sua utilização segura em clínica.
Embora as pesquisas ainda estejam em andamento, é importante ressaltar que anestésicos locais encapsulados em lipossomas ou complexados com ciclodextrinas apontam uma nova direção no desenvolvimento de formulações mais eficazes e seguras. Pacientes submetidos a cirurgias (no alívio da dor pós-operatória) ou com dor crônica (que freqüentemente necessitam de administrações repetidas de anestésicos locais, seja para bloqueio de nervos periféricos, centrais ou autonômicos) seriam os principais beneficiados pelo desenvolvimento dessas formulações, denominadas de longa duração ou de liberação controlada, possibilitando aumento na duração da anestesia, diminuindo a freqüência de administrações diárias e reduzindo a toxicidade sistêmica inerente aos anestésicos locais atualmente disponíveis.
Apresentado em 04 de outubro de 2002
Aceito publicação em 31 de janeiro de 2003
- 01. Siddall PJ, Cousins MJ - Pain mechanisms and management: an update. Clin Exp Pharmacol Physiol, 1995;22:679-688.
- 02. Bennett G, Deer T, Stuart DP et al - Future directions in the management of pain by intraspinal drug delivery. J Pain Symp Manag, 2000;20:44-50.
- 03. Åkerman B, Arweström E, Post C - Local anesthetics potentiate spinal morphine antinociception. Anesth Analg, 1988;67:943-948.
- 04. Whiteside JB, Wildsmith JAW - Developments in local anesthetics drugs. Br J Anaesth, 2001;87:27-35.
- 05. de Jong RH - Local Anesthetics, 1st Ed, USA, Mosby-Year Book, 1994;87-88.
- 06. Kuzma PJ, Kline MD, Calkins MD et al - Progress in the development of ultra-long-acting local anesthetics. Reg Anesth, 1997;22:543-551.
- 07. Ranade VV - Drug delivery systems. 1. Site-specific drug delivery using liposomes as carriers. J Clin Pharmacol, 1989;29:685-694.
- 08. Lichtenberg D, Barenholz Y - Liposomes - Preparation, characterization and preservation. Method Biochem Anal, 1988;33:337-462.
- 09. Grant GJ, Bansinath M - Liposomal delivery systems for local anesthetics. Reg Anesth Pain Med, 2001;26:61-63.
- 10. Sharata HH, Katz KH - Liposomes. Int J Dermatol, 1996;35:761-769.
- 11. Malinovsky J-M, Benhamou D, Alafandy M et al - Neurotoxicological assessment after intracisternal injection of liposomal bupivacaine in rabbits. Anesth Analg, 1997b;85:1331-1336.
- 12. Rongen HAH, Bult A, van Bennekom WP - Liposomes and immunoassays. J Immunol Meth, 1997;204:105-133.
- 13. Law SL, Huang KJ, Chiang CH - Acyclovir-containing liposomes for potential ocular delivery corneal penetration and absorption. J Control Release, 2000;63:135-140.
- 14. Kotwani RN, Gokhale PC, Bodhe PV et al - A comparative study of plasma concentrations of liposomal amphotericin B (L-AMP-LRC-1) in adults, children and neonates. Int J Pharm, 2002;238:11-15.
- 15. Erridge C, Stewart J, Bennet-Guerrero et al - The biological activity of a liposomal complete core lipopolysacharide vaccine. J Endotoxin Res 2002;8:39-46.
- 16. Stuart DD, Kao GY, Allen T - A novel long-circulating and functional liposomal formulation of antisense oligonucleotides targeted against MDR1. Cancer Gene Therapy, 2000;7:466-475.
- 17. Boogaerts J, Declercq A, Lafont N et al - Toxicity of bupivacaine encapsulated into liposomes and injected intravenously: comparision with plain solutions. Anesth Analg, 1993a;76:553-555.
- 18. Boogaerts JG, Lafont ND, Luo HC et al - Plasma concentrations of bupivacaine after brachial plexus administration of liposome-associated and plain solutions to rabbits. Can J Anaesth, 1993b;40:1201-1204.
- 19. Yu H-Y, Sun P, Hou W-Y - Prolonged local anesthetic effect of bupivacaine liposomes in rats. Int J Pharm, 1998;176:133-136.
- 20. Malinovsky JM, Bernard JM, Baudriment M et al - A chronic model for experimental investigation of epidural anesthesia in the rabbit. Reg Anesth, 1997a;22:80-85.
- 21. Malinovsky JM, Le Corre P, Meunier JF et al - A dose-response study of liposomal bupivacaine in rabbits. J Contr Rel, 1999;60:111-119.
- 22. Boogaerts JG, Lafont ND, Declerq AG et al - Epidural administration of liposome-associated bupivacaine for the management of postsurgical pain:a first study. J Clin Anesth, 1994;6:315-320.
- 23. Lafont ND, Legros FJ, Boogaerts JG - Use of liposome-associated bupivacaine in a cancer pain syndrome. Anaesthesia, 1996;51:578-579.
- 24. Simonetti MPB, Andrade MP - Anestésicos locais e opióides encapsulados em lipossomas: um avanço farmacológico em progresso. Rev. Bras. Anestesiol. 1996;46:35-42.
- 25. Langerman L, Grant GJ, Zakowski M et al - Prolongation of epidural anesthesia using a lipid carrier with procaine, lidocaine and tetracaine. Anesth Analg, 1992;75:900-905.
- 26. Mowat JJ, Mok MJ, MacLeod BA et al - Liposomal bupivacaine. Anesthesiol, 1996;85:635-643.
- 27. Loftsson T, Masson M - Cyclodextrins in topical drug formulations: theory and practice. Int J Pharm, 2001;225:15-30.
- 28. Matioli G - Ciclodextrinas e suas aplicações em alimentos, fármacos, agricultura, biotecnologia, química analítica e produtos gerais. 1ª Ed, Maringá, Eduem, 2000;3-5.
- 29. McCormack B, Gregoriadis G - Drugs-in-cyclodextrins-in-liposomes: an approach to controlling the fate of water insoluble drugs in vivo Int J Pharmac, 1998;162:59-69.
- 30. Bibby D, Davies NM, Tucker IG - Mechanisms by wich cyclodextrins modify drug release from polymeric drug delivery systems. Int J Pharmac, 2000;197:1-11.
- 31. Kalinkova GN - Studies of beneficial interactions between active medicaments and excipients in pharmaceutical formulations. Int J Pharm, 1999;187:1-15.
- 32. Frömming K-H, Szejtli J - Topics in Inclusion Science - Cyclodextrins in Pharmacy, 1st Ed, Hungria, Kluwer Academic Publishers, 1994;50-51.
- 33. Kirchmeier MJ, Ishida T, Chevrette J et al - Correlations between the rate of intracellular release of endocytosed liposomal doxorubicin and cytotoxicity as determined by a new assay. J Liposome Res, 2001;11:15-29.
- 34. Veiga F, Fernandes C, Teixeira F - Oral availability and hypoglycaemic activity of tolbutamide/cyclodextrin inclusion complexes. Int J Pharm, 2000;202:165-171.
- 35. Dalmora ME, Dalmora SL, Oliveira AG - Inclusion complex of piroxicam with b-cyclodextrin and incorporation in cationic microemulsion. In vitro drug release and in vivo topical anti-inflammatory effect. Int J Pharm, 2001;222:45-55.
- 36. Irie T, Uekama K - Pharmaceutical applications of ciclodextrins. III. Toxicological issues and safety evaluation. J Pharm Sci, 1997;86:147-162.
- 37. Rajewski RA, Stella VJ - Pharmaceutical applications of cyclodextrins. 2. In vivo Drug delivery. J Pharm Sci 1996;85:1142-1169.
- 38. Dollo G, Le Corre P, Chevanne F - Inclusion complexation of amide-type local anesthetics with b-cyclodextrin and derivates. I. Physicochemical characterization. Int J Pharmac, 1996a;131:219-228.
- 39. Dollo G, Le Corre P, Chevanne F - Inclusion complexation of amide-type local anesthetics with b-cyclodextrin and derivates. II. Evaluation of affinity constants and in vitro transfer rate constants. Int J Pharmac, 1996b;136:165-174.
- 40. Fréville JC, Dollo G, Le Corre P et al - Controlled systemic absorption and increased anesthetic effect of bupivacaine following epidural administration of bupivacaine-hydroxypropyl-beta-cyclodextrin complex. Pharm Res, 1996;13:1576-1580.
- 41. Dollo G, Thompson DO, Le Corre P et al - Inclusion complexation of amide-type local anesthetics with b-cyclodextrin and derivates. III. Biopharmaceutics of bupivacaine-SBE7-b-ciclodextrina complex following percutaneous sciatic nerve administration in rabbits. Int J Pharmac, 1998;164:11-19.
- 42. Dollo G, Le Corre P, Freville JC et al - Biopharmaceutics of local anesthetic cyclodextrin complexes following loco-regional administration. Ann Pharm Fr, 2000;58:425-432.
- 43. Fletcher D, Le Corre P, Guilbaud G et al - Antinociceptive effect of bupivacaine encapsulated in poly(D,L)-lactide-co-glycolide microspheres in the acute inflammatory pain model of carrageenin-injected rats. Anesth Analg, 1997;84:90-94.
- 44. Garry MG, Jackson DL, Geier HE et al - Evaluation of the efficacy of a bupivacaine polymer system on nociception and inflammatory mediator release. Pain, 1999;82:49-55.
- 45. Kohane DS, Lipp M, Kinney RC et al - Sciatic nerve blockade with lipid-protein-sugar particles containing bupivacaine. Pharm Res, 2000;17:1243-1249.
- 46. Grant GJ, Barenholz Y, Piskoun B et al - DRV liposomal bupivacaine: preparation, characterization and in vivo evaluation in mice. Pharm Res, 2001;18:336-343.
Datas de Publicação
-
Publicação nesta coleção
12 Nov 2003 -
Data do Fascículo
Set 2003
Histórico
-
Aceito
31 Jan 2003 -
Recebido
04 Out 2002