Resumos
JUSTIFICATIVA E OBJETIVOS: O mecanismo de ação dos anestésicos locais (AL) na junção neuromuscular motivou a realização de vários estudos. Em baixas doses eles não interferem na transmissão neuromuscular, mas em altas doses podem comprometer a transmissão neuromuscular e potencializar os efeitos de bloqueadores neuromusculares. O objetivo do estudo foi avaliar, em diafragma de rato, a interação da lidocaína com o rocurônio através da influência no grau de bloqueio neuromuscular. MÉTODO: Foram utilizados ratos, com peso entre 250 e 300 g. A preparação foi feita de acordo com a técnica descrita por Bulbring. Formaram-se grupos (n = 5) de acordo com a droga em estudo: lidocaína - 20 µg.mL-1 (Grupo I); rocurônio - 4 µg.mL-1 (Grupo II) e rocurônio - 4 µg.mL-1 com lidocaína - 20 µg.mL-1 (Grupo III). Foram avaliadas: 1) a amplitude das respostas do músculo diafragma à estimulação indireta, antes e 60 minutos após a adição da lidocaína e do bloqueador neuromuscular; 2) os potenciais de membrana (PM) e potenciais de placa terminal em miniatura (PPTM); 3) a eficácia da neostigmina e 4-aminopiridina na reversão do bloqueio neuromuscular. RESULTADOS: A lidocaína isoladamente não alterou a amplitude das respostas musculares. Com o uso prévio de lidocaína o bloqueio neuromuscular do rocurônio foi de 82,8% ± 1,91%, com diferença significativa (p = 0,0079) em relação ao grupo com rocurônio isolado (57,8% ± 1,9%). O bloqueio foi parcial e totalmente revertido pela neostigmina e 4-aminopiridina, respectivamente. A lidocaína não alterou o potencial de membrana e ocasionou aumento inicial na freqüência dos PPTM, seguido de bloqueio. CONCLUSÕES: A lidocaína potencializou o bloqueio neuromuscular produzido pelo rocurônio. As alterações do PPTM identificam ação pré-sináptica. O antagonismo completo da 4-aminopiridina sugere componente pré-sináptico, idéia que é suportada pelo antagonismo parcial pela neostigmina.
ANESTÉSICOS, Local; ANIMAIS; BLOQUEADORES NEUROMUSCULARES, Não-despolarizantes
JUSTIFICATIVA Y OBJETIVOS: El mecanismo de acción de los anestésicos locales (AL) en la junción neuromuscular motivó la realización de varios estudios. Con dosis bajas, los mismos no interfieren en la transmisión neuromuscular, altas dosis pueden comprometer la transmisión neuromuscular y potenciar los efectos de bloqueadores neuromusculares. El objetivo del estudio fue evaluar en diafragma de ratón, la interacción entre la lidocaína y el rocuronio a través de la influencia en el grado del bloqueo neuromuscular. MÉTODO: Fueron utilizados ratones, con peso entre 250 y 300 g. La preparación fue montada de acuerdo con la técnica descripta por Bulbring. Se formaron grupos (n = 5) de acuerdo con la droga en estudio: lidocaína - 20 µg.mL-1 (Grupo I); rocuronio - 4 µg.mL-1 (Grupo II) y rocuronio - 4 µg.mL-1 con lidocaína - 20 µg.mL-1 (Grupo III). Fueron evaluados: 1) la amplitud de las respuestas del músculo diafragma a la estimulación indirecta, antes y 60 minutos después de la adición de la lidocaína y del bloqueador neuromuscular; 2) los potenciales de membrana (PM) y potenciales de placa terminal en miniatura (PPTM); 3) la eficacia de la neostigmina y 4) aminopiridina en la reversión del bloqueo neuromuscular. RESULTADOS: La lidocaína aisladamente no cambió la amplitud de las respuestas musculares. Con el uso previo de lidocaína, el bloqueo neuromuscular del rocuronio fue del 82,8% ± 1,91%, con diferencia significativa (p = 0,0079) con relación al grupo con rocuronio aislado (57,8% ± 1,9%). El bloqueo fue parcial y totalmente revertido por la neostigmina y la 4-aminopiridina, respectivamente. La lidocaína no cambió el potencial de membrana y causó un aumento inicial en la frecuencia de los PPTM, seguido de bloqueo. CONCLUSIONES: La lidocaína potenció el bloqueo neuromuscular que el rocuronio produjo. Los cambios del PPTM identifican una acción presináptica. El antagonismo completo de la 4-aminopiridina sugiere un componente presináptico, idea apoyada por el antagonismo parcial de neostigmina.
BACKGROUND AND OBJECTIVES: The action mechanism of local anesthetics (LA) on neuromuscular junction motivated several studies. When administered at low doses, they do not interfere on neuromuscular transmission. But high doses may compromise neuromuscular transmission and increase the effects of neuromuscular blockers. The objective of this study was to evaluate lidocaine interaction with rocuronium on rat diaphragm through its influence on neuromuscular block degree. METHODS: Rats, weighing between 250 and 300 g, were used. Preparation was set according to the technique described by Bulbring. Groups were formed (n = 5) according to the drug being studied: lidocaine - 20 µg.mL-1 (Group I); rocuronium - 4 µg.mL-1 (Group II), and rocuronium - 4 µg.mL-1 with lidocaine - 20 µg.mL-1 (Group III). The following items were assessed: 1) the extent of diaphragm muscle responses to indirect stimulation, both before and 60 minutes after adding lidocaine and a neuromuscular blocker; 2) membrane potentials (MP) and miniature end-plate potentials (MEPP); 3) the effectiveness of neostigmine, and 4) aminopyridine on neuromuscular blockage reversal. RESULTS: When administered separately, lidocaine did not alter the extent of muscular responses. With the previous use of lidocaine, rocuronium neuromuscular blockage was 82.8% ± 1.91%, with a significant difference (p = 0.0079) when compared to the group with isolated rocuronium (57.8% ± 1.9%). Blockage was both partially and fully reverted by neostigmine and 4-aminopyridine, respectively. Lidocaine did not alter membrane potential and caused an initial increase on MEPP, followed by a blockage. CONCLUSIONS: Lidocaine increases the neuromuscular blocking produced by rocuronium. MEPP modifications identify a presynaptic action. The complete antagonism of 4-aminopyridine indicates a presynaptic component. This idea is supported by the partial antagonism through neostigmine.
ANESTHETICS, Local; ANIMALS; NEUROMUSCULAR BLOCKERS, Nondepolarizing
ARTIGO CIENTÍFICO
Influência da lidocaína no bloqueio neuromuscular produzido pelo rocurônio. Estudo em preparação nervo frênico-diafragma de rato* * Recebido do Departamento de Farmacologia da Faculdade de Ciências Médicas da Universidade de Campinas (UNICAMP), Campinas, SP
Influencia de la lidocaína en el bloqueo neuromuscular producido por el rocuronio. Estudio en preparación nervio frénico-diafragma de ratón
Yolanda Christina S. LoyolaI; Angélica de Fátima de Assunção Braga, TSAII; Glória Maria Braga Potério, TSAII; Silmara Rodrigues de SousaI; Samanta Cristina Antoniassi FernandesI; Franklin S. da Silva BragaIII
IAluna do Curso de Pós-Graduação do Departamento de Farmacologia da FCM da UNICAMP
IIProfª Associada do Departamento de Anestesiologia da FCM da UNICAMP
IIIProf. Dr. do Departamento de Anestesiologia da FCM da UNICAMP
Endereço para correspondência Endereço para correspondência: Dra. Angélica de Fátima de Assunção Braga Rua Luciano Venere Decourt, 245 Cidade Universitária 13084-040 Campinas, SP E-mail: franklinbraga@terra.com.br
RESUMO
JUSTIFICATIVA E OBJETIVOS: O mecanismo de ação dos anestésicos locais (AL) na junção neuromuscular motivou a realização de vários estudos. Em baixas doses eles não interferem na transmissão neuromuscular, mas em altas doses podem comprometer a transmissão neuromuscular e potencializar os efeitos de bloqueadores neuromusculares. O objetivo do estudo foi avaliar, em diafragma de rato, a interação da lidocaína com o rocurônio através da influência no grau de bloqueio neuromuscular.
MÉTODO: Foram utilizados ratos, com peso entre 250 e 300 g. A preparação foi feita de acordo com a técnica descrita por Bulbring. Formaram-se grupos (n = 5) de acordo com a droga em estudo: lidocaína 20 µg.mL-1 (Grupo I); rocurônio 4 µg.mL-1 (Grupo II) e rocurônio 4 µg.mL-1 com lidocaína 20 µg.mL-1 (Grupo III). Foram avaliadas: 1) a amplitude das respostas do músculo diafragma à estimulação indireta, antes e 60 minutos após a adição da lidocaína e do bloqueador neuromuscular; 2) os potenciais de membrana (PM) e potenciais de placa terminal em miniatura (PPTM); 3) a eficácia da neostigmina e 4-aminopiridina na reversão do bloqueio neuromuscular.
RESULTADOS: A lidocaína isoladamente não alterou a amplitude das respostas musculares. Com o uso prévio de lidocaína o bloqueio neuromuscular do rocurônio foi de 82,8% ± 1,91%, com diferença significativa (p = 0,0079) em relação ao grupo com rocurônio isolado (57,8% ± 1,9%). O bloqueio foi parcial e totalmente revertido pela neostigmina e 4-aminopiridina, respectivamente. A lidocaína não alterou o potencial de membrana e ocasionou aumento inicial na freqüência dos PPTM, seguido de bloqueio.
CONCLUSÕES: A lidocaína potencializou o bloqueio neuromuscular produzido pelo rocurônio. As alterações do PPTM identificam ação pré-sináptica. O antagonismo completo da 4-aminopiridina sugere componente pré-sináptico, idéia que é suportada pelo antagonismo parcial pela neostigmina.
Unitermos: ANESTÉSICOS, Local: lidocaína; ANIMAIS: ratos BLOQUEADORES NEUROMUSCULARES, Não-despolarizantes: rocurônio.
RESUMEN
JUSTIFICATIVA Y OBJETIVOS: El mecanismo de acción de los anestésicos locales (AL) en la junción neuromuscular motivó la realización de varios estudios. Con dosis bajas, los mismos no interfieren en la transmisión neuromuscular, altas dosis pueden comprometer la transmisión neuromuscular y potenciar los efectos de bloqueadores neuromusculares. El objetivo del estudio fue evaluar en diafragma de ratón, la interacción entre la lidocaína y el rocuronio a través de la influencia en el grado del bloqueo neuromuscular.
MÉTODO: Fueron utilizados ratones, con peso entre 250 y 300 g. La preparación fue montada de acuerdo con la técnica descripta por Bulbring. Se formaron grupos (n = 5) de acuerdo con la droga en estudio: lidocaína 20 µg.mL-1 (Grupo I); rocuronio 4 µg.mL-1 (Grupo II) y rocuronio 4 µg.mL-1 con lidocaína 20 µg.mL-1 (Grupo III). Fueron evaluados: 1) la amplitud de las respuestas del músculo diafragma a la estimulación indirecta, antes y 60 minutos después de la adición de la lidocaína y del bloqueador neuromuscular; 2) los potenciales de membrana (PM) y potenciales de placa terminal en miniatura (PPTM); 3) la eficacia de la neostigmina y 4) aminopiridina en la reversión del bloqueo neuromuscular.
RESULTADOS: La lidocaína aisladamente no cambió la amplitud de las respuestas musculares. Con el uso previo de lidocaína, el bloqueo neuromuscular del rocuronio fue del 82,8% ± 1,91%, con diferencia significativa (p = 0,0079) con relación al grupo con rocuronio aislado (57,8% ± 1,9%). El bloqueo fue parcial y totalmente revertido por la neostigmina y la 4-aminopiridina, respectivamente. La lidocaína no cambió el potencial de membrana y causó un aumento inicial en la frecuencia de los PPTM, seguido de bloqueo.
CONCLUSIONES: La lidocaína potenció el bloqueo neuromuscular que el rocuronio produjo. Los cambios del PPTM identifican una acción presináptica. El antagonismo completo de la 4-aminopiridina sugiere un componente presináptico, idea apoyada por el antagonismo parcial de neostigmina.
INTRODUÇÃO
As propriedades farmacológicas dos bloqueadores neuromusculares (BNM), tais como início de ação, grau de bloqueio neuromuscular e duração de ação dependem de vários fatores. Estes incluem o débito cardíaco, o tempo circulatório para o músculo, o fluxo sanguíneo muscular, a afinidade pelo local de ação, a potência e a dose administrada 1. Também existem evidências de que altas doses de anestésicos locais empregadas isoladamente podem comprometer a transmissão neuromuscular, e potencializar o bloqueio neuromuscular produzido por baixas doses de bloqueadores neuromusculares não-despolarizantes e despolarizantes 2.
Os anestésicos locais, particularmente as amino-amidas, tais como a lidocaína e a bupivacaína, são fármacos comumente empregados na prática clínica em anestesia peridural associada à anestesia geral. Por via venosa, a lidocaína é usada durante a indução anestésica para atenuar as respostas reflexas desencadeadas pelas manobras de laringoscopia e intubação traqueal e como droga auxiliar no tratamento de disritmias cardíacas no intra-operatório 2-7. O rocurônio é um bloqueador neuromuscular não-despolarizante, aminoesteróide, de duração de ação intermediária, com início rápido de ação, característica que o diferencia dos demais bloqueadores não-despolarizantes e o torna um agente alternativo para a succinilcolina em situações de indução de seqüência rápida 7-9.
São admitidos vários mecanismos para explicar a interação entre os anestésicos locais e os bloqueadores neuromusculares, tais como ação pré-sináptica, inibindo a liberação da acetilcolina e ação pós-sináptica, através da estabilização da membrana pós-juncional, além de interferência com o mecanismo de excitação-contração da fibra muscular 10-14.
Trabalhos apontam para possível interação lidocaína - bloqueadores neuromusculares, potencializando os efeitos dos bloqueadores neuromusculares 4,10. Embora somente em altas doses os anestésicos locais possam produzir bloqueio neuromuscular, a interação com os bloqueadores neuromusculares, particularmente os não-despolarizantes, torna-se clinicamente relevante, necessitando-se de observação cuidadosa quando do emprego simultâneo desses agentes, ou em situações em que a margem de segurança da transmissão neuromuscular estiver reduzida 2,15.
O objetivo deste estudo foi avaliar, em modelo experimental, o efeito da lidocaína na transmissão neuromuscular e a sua influência no bloqueio neuromuscular produzido pelo rocurônio.
MÉTODO
Foi realizado estudo experimental obedecendo aos princípios éticos do Colégio Brasileiro de Experimentação Animal (COBEA) que foram aprovados pela Comissão de Ética em Experimentação Animal do Instituto de Biologia da Universidade Estadual de Campinas (UNICAMP).
Foram utilizados ratos machos da linhagem Wistar, com peso entre 250 e 300 g, sacrificados sob anestesia com hidrato de cloral a 10% (250 mg.kg-1), por via intraperitonial, e sangria por secção dos vasos do pescoço. A preparação foi feita de acordo com a técnica descrita por Bulbring 16. Os hemidiafragmas com os nervos frênicos correspondentes foram retirados e fixados em cuba contendo 40 mL de solução nutritiva de Tyrode com a seguinte composição em mM: NaCl 137; KCl 2,7; CaCl2 1,8; NaHCO3 11,9; MgCl2 0,25; NaH2PO4 0,3 e glicose 11. A solução foi aerada constantemente com carbogênio (95% O2 + 5% CO2) e mantida a 37º C. O nervo foi colocado sobre eletrodos de platina ligados a um estimulador Grass S48. O diafragma foi mantido por sua porção tendinosa sob tensão constante (5,0 g), através de fio ligado a transdutor isométrico Load Cell BG50 GMS, e submetido à estimulação indireta de 0,1 Hz de freqüência e duração de 0,2 mseg, sendo que as variações de tensão produzidas pelas contrações do diafragma foram registradas em fisiógrafo Gould RS 3400. Formaram-se grupos (n = 5), de acordo com o fármaco adicionado à preparação: Grupo I - lidocaína (20 µg.mL-1); Grupo II - rocurônio (4 µg.mL-1); Grupo III - rocurônio (4 µg.mL-1) em preparação previamente exposta à lidocaína (20 µg.mL-1). No Grupo III (lidocaína-rocurônio), o rocurônio foi adicionado à preparação 30 minutos após a adição da lidocaína. As respostas musculares à estimulação indireta foram registradas durante 60 minutos após a adição dos fármacos. Para a reversão do bloqueio neuromuscular ocasionado pela associação lidocaína-rocurônio, empregaram-se neostigmina (2 µg.mL-1) e a 4-aminopiridina (4AP) (20 µg.mL-1), adicionadas à preparação 60 minutos após o BNM. Utilizou-se também a preparação nervo frênico-diafragma para a o estudo dos efeitos da lidocaína nos potenciais de placa terminal em miniatura e nos potenciais de membrana. Foram avaliados: 1) a amplitude das respostas do músculo diafragma à estimulação indireta, antes e 60 minutos após a adição de lidocaína; 2) a amplitude das respostas do músculo diafragma à estimulação indireta, antes e 60 minutos após a adição do bloqueador neuromuscular; 3) os potenciais de membrana (PM) e potenciais de placa terminal em miniatura (PPTM); 4) a eficácia da neostigmina e da 4-aminopiridina na reversão do bloqueio neuromuscular.
Os resultados foram expressos em média e desvios-padrão. Para análise estatística foram utilizados os testes de Mann-Whitney e de Wilcoxon para amostras pareadas. Assumiu-se nível significativo de 5% (a = 5%). O poder do teste foi calculado e obteve-se b > 20% (poder > 80%).
RESULTADOS
A lidocaína na concentração estudada e empregada isoladamente em preparação nervo frênico-diafragma de rato não causou redução na amplitude das respostas musculares à estimulação elétrica indireta (Figura 1).
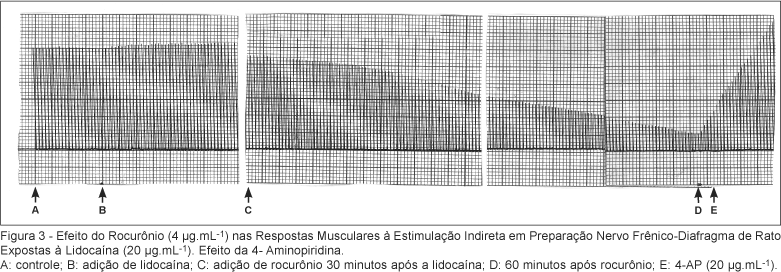
Nas preparações expostas previamente à lidocaína o bloqueio produzido pelo rocurônio foi de 82,8% ± 1,91%, com diferença significativa (p = 0,0079) em relação ao produzido pelo rocurônio empregado isoladamente (57,8% ± 11,9%), figuras 2 e 3, respectivamente.
O bloqueio neuromuscular causado pelo rocurônio, nas preparações expostas à lidocaína, foi revertido parcial e totalmente pela neostigmina (Figura 4) e pela 4-aminopiridina (Figura 3), respectivamente.
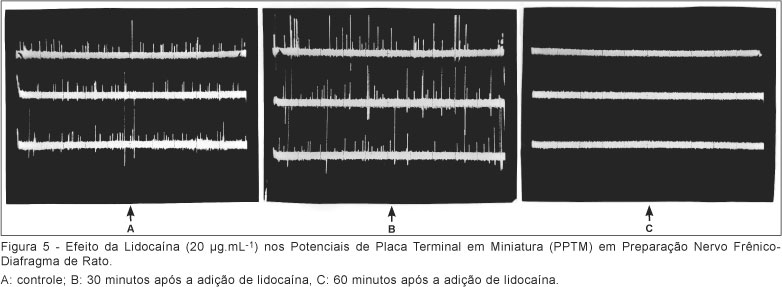
Não se observou efeito com diferença estatística significativa da lidocaína sobre os potenciais de membrana. Os efeitos sobre os potenciais de placa terminal em miniatura caracterizaram-se inicialmente por aumento na freqüência, observado 30 minutos após a adição da droga, seguido de bloqueio aos 60 minutos (Figura 5).
DISCUSSÃO
Os efeitos dos anestésicos locais na junção neuromuscular e sua influência no bloqueio produzido por bloqueadores neuromusculares não-despolarizantes é ainda alvo de pouca investigação, no entanto esta interação tem sido observada na prática clínica 2,4-6.
Esses resultados clínicos foram confirmados em trabalhos experimentais, que têm como maior vantagem, em relação às pesquisas clínicas, a possibilidade de eliminar a grande variabilidade individual de sensibilidade aos bloqueadores neuromusculares 10,17-19.
O presente estudo, realizado em preparação nervo frênico-diafragma de rato, mostrou que na concentração estudada a lidocaína empregada isoladamente não exerceu efeitos na junção neuromuscular, no entanto potencializou o bloqueio produzido pelo rocurônio. Estes resultados assemelham-se aos de outros autores que também relataram ausência de efeito dos anestésicos locais na transmissão neuromuscular, mas observaram potencialização de diferentes bloqueadores neuromusculares, quando do emprego de anestésicos locais por diferentes vias de administração 4-6,10,17,19.
Na década de 1950, Ellis e col. 17, em experimentos realizados em gatos, observaram que a procaína, embora não exercendo efeito na transmissão neuromuscular, intensificou o bloqueio produzido pela d-tubocurarina e succinilcolina, resultados confirmados em outros trabalhos que também relataram ser verdadeira essa interação para outros anestésicos locais e bloqueadores neuromusculares 10,19. Matsuo e col. 10 avaliaram em preparação nervo frênico-diafragma de rato, a ação da associação da d-tubocurarina a diferentes anestésicos locais como procaína, lidocaína e etidocaína. Observaram que mesmo em concentrações consideradas ineficazes, os anestésicos locais diminuíram de modo significativo a ED50 dos agentes bloqueadores neuromusculares e que estes, em concentrações eficazes para causar bloqueio neuromuscular, também causaram similar diminuição da ED50 dos anestésicos locais. Assim, os autores concluíram que a interação bloqueadores neuromusculares-anestésicos locais pode ser conseqüente à potencialização verdadeira, causada pela ação dos dois tipos de drogas, em diferentes locais da junção neuromuscular.
Em experimentos realizados em gatos, o bloqueio neuromuscular produzido pela associação lidocaína-pancurônio foi 20% maior, com diferença estatística significativa em relação ao observado quando do emprego do pancurônio isoladamente 18. Similarmente, a lidocaína na dose de 5 mg.kg-1 administrada por via venosa, também aumentou em 25% o bloqueio neuromuscular produzido pela d-tubocurarina 19. No homem, os efeitos do vecurônio e do atracúrio foram prolongados pela bupivacaína administrada no espaço peridural, e o rocurônio teve sua duração farmacológica aumentada pela lidocaína administrada por via venosa 4-6.
A interação entre os anestésicos locais e os bloqueadores neuromusculares não está completamente elucidada, e vários mecanismos podem ser responsáveis pela potencialização observada. Teoricamente esses agentes podem interferir em alguma etapa envolvida na transmissão neuromuscular. Por ação pré-sináptica, os anestésicos locais deprimem seletivamente a condução nas fibras motoras e diminuem a liberação de acetilcolina durante a estimulação nervosa 12,20,21. Por ação pós-sináptica podem se ligar a diferentes locais específicos de acetilcolina, resultando em dessensibilização desses receptores, além de poderem ocluir temporariamente os canais dos receptores nicotínicos 13,14,22,23.
A lidocaína pode bloquear completamente a condução nervosa e também deprimir a condução do impulso pré e pós-juncional 24. Em estudo que correlaciona a estrutura molecular de vários derivados da lidocaína com as suas respectivas propriedades inibitórias da transmissão neuromuscular e com a sua potência anestésica local, foi demonstrado que as propriedades moleculares desses derivados, relacionadas com o comprometimento da transmissão neuromuscular, são similares àquelas envolvidas na ativação de receptores de acetilcolina, e não com as associadas à sua potência anestésica local. Esses resultados sugerem que a lidocaína produz bloqueio neuromuscular por mecanismos distintos do seu mecanismo de ação como anestésico local 24.
O bloqueio neuromuscular ocasionado pela associação lidocaína-rocurônio foi revertido pela neostigmina e pela 4-aminopiridina. A neostigmina foi menos eficaz do que a 4-aminopiridina na reversão do bloqueio. Com esta última, a amplitude das respostas musculares à estimulação do nervo frênico, ultrapassou a das respostas consideradas como controle. A neostigmina, ao inibir a acetilcolinesterase, aumenta a concentração do neurotransmissor na fenda sináptica sendo capaz de deslocar competitivamente os agentes causadores do bloqueio. A 4-aminopiridina, além do efeito inibidor de dessensibilização de receptores nicotínicos da placa terminal, provoca grande aumento dos quanta de acetilcolina. Esse aumento é resultante de duas ações distintas na membrana das terminações nervosas, a inibição dos canais de potássio, que produz aumento na duração do potencial de ação, e o maior influxo de íons cálcio para as terminações nervosas motoras durante a despolarização da membrana 25-30. Embora o mecanismo subsináptico pelo qual a 4-aminopiridina aumenta a liberação do transmissor ainda não esteja completamente elucidado, a eficácia da droga como antagonista do bloqueio neuromuscular pré e pós-sináptico tem sido evidenciada em testes experimentais 10,25-31. No entanto, seu uso na clínica não é preconizado, pois atravessa facilmente a barreira hematoencefálica com estimulação do sistema nervoso central, podendo causar convulsões 30.
Na avaliação dos potenciais bioelétricos, observou-se que a lidocaína na concentração empregada não alterou o potencial de membrana das fibras musculares, demonstrando-se, portanto, que não possui ação despolarizante sobre a fibra muscular esquelética. Embora a lidocaína não tenha apresentado efeito sobre a fibra muscular, os estudos dos potenciais bioelétricos evidenciaram que este fármaco na concentração empregada interferiu nos potenciais de placa terminal em miniatura (PPTM). Inicialmente verificou-se aumento na freqüência dos PPTM, o que pode ser atribuído à ação pré-sináptica, aumentando a liberação do neurotransmissor, com redução na amplitude, provavelmente devido à ação pós-sináptica.
Os resultados mostraram que a lidocaína na concentração estudada e empregada isoladamente não comprometeu a transmissão neuromuscular, mas potencializou o bloqueio neuromuscular produzido pelo rocurônio. As alterações do potencial de placa terminal em miniatura indicaram ação pré-sináptica, modificando a liberação quantal de acetilcolina; a ausência de alterações no potencial de membrana demonstrou que nesta concentração a lidocaína não possuiu ação despolarizante sobre a fibra muscular e que o provável local de ação é na junção neuromuscular, particularmente na placa motora terminal. O antagonismo completo obtido com a 4-aminopiridina sugeriu que a interação da lidocaína com o rocurônio tem componente pré-sináptico, relacionado à diminuição da liberação de acetilcolina. O antagonismo parcial pela neostigmina suporta essa idéia, uma vez que os anticolinesterásicos são eficazes apenas na reversão do bloqueio pós-sináptico.
É provável que a potência dos anestésicos locais na junção neuromuscular possa diferir entre as diferentes espécies e, embora a extrapolação desses resultados para o homem não seja quantitativamente semelhante, as implicações clínicas dessa interação evidenciaram a necessidade de monitorização do bloqueio neuromuscular e de redução da dose de bloqueadores neuromusculares, quando do uso simultâneo desses agentes.
Apresentado em 18 de agosto de 2005
Aceito para publicação em 19 de dezembro de 2005
- 01. Donati F - Onset of action of relaxants. Can J Anesth, 1988;35:S52-S58.
- 02. Telivuo L, Katz RL - The effects of modern intravenous local analgesics on respiration during partial neuromuscular block in man. Anesthesia, 1970;25:30-35.
- 03. Hamaya Y, Dohi S - Differences in cardiovascular response to air-way stimulation at different sites and blockade of the response by lidocaine. Anesthesiology, 2000;93:95-103.
- 04. Cardoso LSM, Martins CR, Tardelli MA - Efeitos da lidocaína por via venosa sobre a farmacodinâmica do rocurônio. Rev Bras Anestesiol, 2005;55:371-380.
- 05. Toft P, Kirkegaard Nielsen H, Severinsen I et al - Effect of epidurally administered bupivacaine on atracurium-induced neuromuscular blockade. Acta Anesthesiol Scand, 1990;34:649-652.
- 06. Taivainen T, Meretoja OA, Rosenberg PH - The effect of epidural bupivacaine on vecuronium-induced neuromuscular blockade in children. Acta Anesthesiol Scand, 1994;38:453-456.
- 07. Yorukoglu D, Asik Y, Okten F - Rocuronium combined with iv lidocaine for rapid tracheal intubation. Acta Anesthesiol Scand, 2003;47:583-587.
- 08. Engbaek J, Viby-Mogensen J - Can rocuronium replace succinylcholine in a rapid-sequence induction of anesthesia? Acta Anesthesiol Scand, 1999;43:1-3.
- 09. Andrews JI, Kumar N, van den Brom RH et al - A large simple randomized trial of rocuronium versus succinylcholine in rapid-sequence induction of anesthesia along with propofol. Acta Anesthesiol Scand, 1999; 43:4-8.
- 10. Matsuo S, Rao DB, Chaudry I et al - Interaction of muscle relaxants and local anesthetics at the neuromuscular junction. Anesth Analg, 1978;57:580-587.
- 11. Usubiaga JE, Wikinski JA, Morales RL et al - Interaction of intravenously administered procaine, lidocaine and succinylcholine in anesthetized subjects. Anesth Analg, 1967;46:39-45.
- 12. Straughan DW - The action of procaine at the neuromuscular junction. J Pharm Pharmacol, 1971;41: 94-104.
- 13. Sine SM, Taylor P - Local anesthetics and histrionicotoxin are allosteric inhibitors of the acetylcholine receptor. J Biol Chem, 1982;257:8106-8114.
- 14. Neher E, Steinbach JH - Local anesthetics transiently block currents through single acetylcholine-receptor channels. J Physiol, 1978; 277:153-176.
- 15. Pederneiras SG - Interação de drogas com relaxantes musculares. Rev Bras Anestesiol, 1988; 38:63-73.
- 16. Bulbring E - Observation on the isolated phrenic nerve diaphragm preparation of the rat. Br J Pharmacol, 1946;1:38-61.
- 17. Ellis CH, Wnuck AL, De Beer EJ et al - Modifying actions of procaine on the myoneural blocking actions of succinylcholine, decamethonium and d-tubocurarine in dogs and cats. Am J Physiol, 1953; 174:277-282.
- 18. Carpenter RL, Mulroy MF - Edrophonium antagonize combined lidocaine-pacuronium and verapamil-pancuronium neuromuscular blockade in cats. Anesthesiology, 1986;65:506-510.
- 19. Harrah MD, Way WL, Katzung BG - The interaction of d-tubocurarine with antiarrhythmic drugs. Anesthesiology, 1970;33:406-410.
- 20. Matthews EK, Quilliam JP - Effects of central depressant drugs upon acetylcholine release. Br J Pharmacol Chemother, 1964;22:415-440.
- 21. Usubiaga JE, Standaert F - The effects of local anesthetics on motor nerve terminals. J Pharmacol Exp Ther, 1968;159:353-361.
- 22. Ruff RL - The kinetics of local anesthetic blockade of end-plate channels. Biophys J, 1982;37:625-631.
- 23. Cohen JB, Boyd ND, Shera NS - Interactions of Anesthetics with Nicotinic Postsynaptic Membranes Isolated from Torpedo Electric Tissue. em: Fink BR - Molecular Mechanisms of Anesthesia. Progress in Anesthesiology. New York: Raven Press, 1980: 165-174.
- 24. Steinbach AB - Alteration of xylocaine (lidocaine) and its derivatives of the time course of the end plate potencial. J Gen Physiol, 1968;52:144-161.
- 25. Yeh JZ, Oxford GS, Wu CH et al - Interactions of aminopyridines with potassium channels of squid axon membranes. Biophys J, 1976;16:77-81.
- 26. Ulbricht W, Wagner HH - Block of potassium channels of the nodal membrane by 4-aminopyridine and its partial removal on depolarization. Pflugers Arch, 1976;367:77-87.
- 27. Brazil OV, Fontana MD, Pavani NJ - . Effect of 4-aminopyridine on the postsynaptic action of polymyxin B. Eur J Pharmacol, 1989;159:47-51.
- 28. Vital Brazil O, Fontana MD, Pavani NJ - Effect of 4-aminopyridine on end-plate receptor desensitization caused by carbachol. Eur J Pharmacol, 1982;86:199-205.
- 29. Harvey AL, Marshall IG - The facilitatory actions of aminopyridines and tetraethylammonium on neuromuscular transmission and muscle contractility in avian muscle. Naunyn Schmiedebergs Arch Pharmacol, 1977;299:53-60.
- 30. Harvey AL, Marshall IG - The actions of three diaminopyridines on the chick biventer cervicis muscle. Eur J Pharmacol, 1977;44:303-309.
- 31. Bowman WC, Harvey AL, Marshall IG - The actions of aminopyridines on avian muscle. Naunyn Schmiedebergs Arch Pharmacol, 1977;297:99-103.
Datas de Publicação
-
Publicação nesta coleção
11 Maio 2006 -
Data do Fascículo
Abr 2006
Histórico
-
Aceito
19 Dez 2005 -
Recebido
18 Ago 2005