Resumos
JUSTIFICATIVA E OBJETIVOS: A toxina botulínica (TxB), uma das mais potentes toxinas bacterianas conhecidas, tem reconhecidamente ação terapêutica eficaz no tratamento de algumas síndromes dolorosas. Entretanto, algumas de suas indicações ainda estão em fase de comprovação com relação a sua eficácia. O objetivo deste estudo foi revisar o histórico, propriedades farmacológicas e aplicações clinicas da TxB, quando empregada no tratamento de dores de diferentes origens. CONTEÚDO: A TxB é o produto da fermentação do Clostridium Botulinum, uma bactéria anaeróbia Gram-positiva. Comercialmente, as TxB existem nas formas A e B, agentes biológicos obtidos laboratorialmente. A TxB, uma neurotoxina que possui alta afinidade pelas sinapses colinérgicas, ocasiona bloqueio na liberação de acetilcolina pelo terminal nervoso, sem alterar a condução neural de sinais elétricos ou síntese e armazenamento de acetilcolina. Comprovadamente, a TxB pode enfraquecer seletivamente a musculatura dolorosa, interrompendo o ciclo espasmo-dor. Com relação à dor, varias publicações têm demonstrado a eficácia e segurança da TxB-A no tratamento da cefaleia tipo tensão, migrânea, dor lombar crônica e dor miofascial. CONCLUSÕES: A TxB-A é segura e bem tolerada em desordens dolorosas crônicas, onde regimes de farmacoterapia podem sabidamente provocar efeitos colaterais. Outra vantagem é a redução do uso de analgésicos e o tempo de ação de 3 a 4 meses por dose. Entretanto pesquisas futuras serão necessárias para se estabelecer a eficácia da TxB-A em desordens dolorosas crônicas e seu exato mecanismo no alivio da dor, bem como seu potencial em tratamentos multifatoriais.
DOR, Crônica; DROGAS
JUSTIFICATIVA Y OBJETIVOS: La toxina botulínica (TxB), una de las más potentes toxinas bacterianas de que se tiene conocimiento, posee una reconocida acción terapéutica eficaz en el tratamiento de algunos síndromes dolorosos. Sin embargo, algunas de sus indicaciones, todavía están en fase de comprobación con relación a su eficacia. El objetivo de este estudio fue revisar el historial, las propiedades farmacológicas y las aplicaciones clinicas de la TxB, cuando se usa en el tratamiento de dolores de diferentes etiologías. CONTENIDO: La TxB es el producto de la fermentación del Clostridium Botulinum, una bacteria anaerobia Gram-positiva. Comercialmente, las TxB existen bajo las formas A y B, agentes biológicos obtenidos laboratorialmente. La TxB, una neurotoxina que posee una alta afinidad por las sinapsis colinérgicas, ocasiona un bloqueo en la liberación de acetilcolina por el terminal nervioso, sin alterar la conducción neural de las señales eléctricas o la síntesis y el almacenaje de acetilcolina. Se ha comprobado que la TxB puede debilitar selectivamente la musculatura dolorosa, interrumpiendo el ciclo espasmo-dolor. Con relación a él, varias publicaciones han demostrado la eficacia y la seguridad de la TxB-A en el tratamiento de la cefalea tipo tensión, migraña, dolor lumbar crónico y dolor miofacial. CONCLUSIONES: La TxB-A es segura y se tolera muy bien en los desórdenes dolorosos crónicos, donde los regímenes de farmacoterapia pueden de hecho provocar efectos colaterales. Otra ventaja es la reducción del uso de analgésicos y el tiempo de acción de 3 a 4 meses por dosis. Sin embargo, investigaciones futuras serán necesarias para establecer la eficacia de la TxB-A en los desórdenes dolorosos crónicos y su exacto mecanismo en el alivio del dolor, como también su potencial en tratamientos multifactoriales.
BACKGROOUND AND OBJECTIVES: Botulinum toxin (BTX) is one of the most potent bacterial toxins known and its effectiveness in the treatment of some pain syndromes is well known. However, the efficacy of some of its indications is still in the process of being confirmed. The objective of this study was to review the history, pharmacological properties, and clinical applications of BTX in the treatment of pain of different origins. CONTENTS: Botulinum toxin is produced by fermentation of Clostridium botulinum, a Gram-positive, anaerobic bacterium. Commercially, BTX comes in two presentations, types A and B. Botulinum toxin, a neurotoxin with high affinity for cholinergic synapses, blocks the release of acetylcholine by nerve endings without interfering with neuronal conduction of electrical signals or synthesis and storage of acetylcholine. It has been proven that BTX can selectively weaken painful muscles, interrupting the spasm-pain cycle. Several studies have demonstrated the efficacy and safety of BTX-A in the treatment of tension headaches, migraines, chronic lumbar pain, and myofascial pain. CONCLUSIONS: Botulinum toxin type A is well tolerated in the treatment of chronic pain disorders in which pharmacotherapy regimens can cause side effects. The reduction in the consumption of analgesics and length of action of 3 to 4 months per dose represent other advantages of its use. However, further studies are necessary to establish the efficacy of BTX-A in chronic pain disorders and its exact mechanism of action, as well as its potential in multifactorial treatments.
DRUGS; PAIN, chronic
ARTIGO DE REVISÃO
Toxina botulínica no tratamento da dor* * Recebido da Santa Casa de Maringá, PR
Toxina botulínica en el tratamiento del dolor
Orlando Carlos Gomes ColhadoI; Marcelo BoeingII; Luciano Bornia OrtegaIII
IDoutorando em Ciências Médicas pela USP de Ribeirão Preto; Professor Auxiliar da Faculdade de Medicina da Universidade Estadual de Maringá (UEM); Corresponsável pela residência médica em anestesiologia do Hospital Universitário da UEM
IIAnestesiologista da Santa Casa de Maringá
IIIMédico Residente da Santa Casa de Maringá
Endereço para correspondência Endereço para correspondência: Dr. Orlando C. G. Colhado Rua Marechal Deodoro 682/61 87030-020 Maringá Paraná E-mail: esperanssoli@uol.com.br
RESUMO
JUSTIFICATIVA E OBJETIVOS: A toxina botulínica (TxB), uma das mais potentes toxinas bacterianas conhecidas, tem reconhecidamente ação terapêutica eficaz no tratamento de algumas síndromes dolorosas. Entretanto, algumas de suas indicações ainda estão em fase de comprovação com relação a sua eficácia. O objetivo deste estudo foi revisar o histórico, propriedades farmacológicas e aplicações clinicas da TxB, quando empregada no tratamento de dores de diferentes origens.
CONTEÚDO: A TxB é o produto da fermentação do Clostridium Botulinum, uma bactéria anaeróbia Gram-positiva. Comercialmente, as TxB existem nas formas A e B, agentes biológicos obtidos laboratorialmente. A TxB, uma neurotoxina que possui alta afinidade pelas sinapses colinérgicas, ocasiona bloqueio na liberação de acetilcolina pelo terminal nervoso, sem alterar a condução neural de sinais elétricos ou síntese e armazenamento de acetilcolina. Comprovadamente, a TxB pode enfraquecer seletivamente a musculatura dolorosa, interrompendo o ciclo espasmo-dor. Com relação à dor, varias publicações têm demonstrado a eficácia e segurança da TxB-A no tratamento da cefaleia tipo tensão, migrânea, dor lombar crônica e dor miofascial.
CONCLUSÕES: A TxB-A é segura e bem tolerada em desordens dolorosas crônicas, onde regimes de farmacoterapia podem sabidamente provocar efeitos colaterais. Outra vantagem é a redução do uso de analgésicos e o tempo de ação de 3 a 4 meses por dose. Entretanto pesquisas futuras serão necessárias para se estabelecer a eficácia da TxB-A em desordens dolorosas crônicas e seu exato mecanismo no alivio da dor, bem como seu potencial em tratamentos multifatoriais.
Unitermos:DOR, Crônica; DROGAS: toxina botulínica tipo A.
RESUMEN
JUSTIFICATIVA Y OBJETIVOS: La toxina botulínica (TxB), una de las más potentes toxinas bacterianas de que se tiene conocimiento, posee una reconocida acción terapéutica eficaz en el tratamiento de algunos síndromes dolorosos. Sin embargo, algunas de sus indicaciones, todavía están en fase de comprobación con relación a su eficacia. El objetivo de este estudio fue revisar el historial, las propiedades farmacológicas y las aplicaciones clinicas de la TxB, cuando se usa en el tratamiento de dolores de diferentes etiologías.
CONTENIDO: La TxB es el producto de la fermentación del Clostridium Botulinum, una bacteria anaerobia Gram-positiva. Comercialmente, las TxB existen bajo las formas A y B, agentes biológicos obtenidos laboratorialmente. La TxB, una neurotoxina que posee una alta afinidad por las sinapsis colinérgicas, ocasiona un bloqueo en la liberación de acetilcolina por el terminal nervioso, sin alterar la conducción neural de las señales eléctricas o la síntesis y el almacenaje de acetilcolina. Se ha comprobado que la TxB puede debilitar selectivamente la musculatura dolorosa, interrumpiendo el ciclo espasmo-dolor. Con relación a él, varias publicaciones han demostrado la eficacia y la seguridad de la TxB-A en el tratamiento de la cefalea tipo tensión, migraña, dolor lumbar crónico y dolor miofacial.
CONCLUSIONES: La TxB-A es segura y se tolera muy bien en los desórdenes dolorosos crónicos, donde los regímenes de farmacoterapia pueden de hecho provocar efectos colaterales. Otra ventaja es la reducción del uso de analgésicos y el tiempo de acción de 3 a 4 meses por dosis. Sin embargo, investigaciones futuras serán necesarias para establecer la eficacia de la TxB-A en los desórdenes dolorosos crónicos y su exacto mecanismo en el alivio del dolor, como también su potencial en tratamientos multifactoriales.
INTRODUÇÃO
A história da toxina botulínica (TxB) tem origem quando em 1817 foi publicada primeira descrição do botulismo (ou seja, envenenamento pela TxB). O autor, Justinus Kerner, associou mortes resultantes de intoxicação com um veneno encontrado em salsichas defumadas (do latim botulus que significa salsicha). Ele concluiu que tal veneno interferia com a excitabilidade do sistema nervoso motor e autonômico. Isto permitiu a publicação de duas monografias descrevendo as características clínicas do botulismo 1. Kerner propôs uma variedade de potenciais usos da TxB na Medicina, principalmente em desordens de origem no sistema nervoso central que, atualmente, através de novas pesquisas vêm sendo comprovadas 2,3.
Somente em 1895 que o agente bacteriano, bem como o mecanismo de ação responsável pela toxicidade do botulismo foram descobertos, feitos estes atribuídos ao professor Emile Van Ermengen, cuja publicação data de 1897 2.
A TxB, uma das mais potentes toxinas bacterianas conhecidas, é o produto da fermentação do Clostridium botulinum, uma bactéria anaeróbia Gram-positiva em forma de esporo encontrada comumente no solo e em ambientes marinhos no mundo todo 3. Oito sorotipos imunologicamente distintos têm sido identificados. Destes, sete sorotipos: A, B, C1, D, E, F e G são neurotoxinas (outra TxB, a C2, é também produzida pelo C. botulinum, mas não é neurotoxina) 4.
Embora todos os sorotipos inibam a liberação de acetilcolina na terminação nervosa, suas proteínas intracelulares, seus mecanismos de ação e suas potências variam substancialmente. O sorotipo mais amplamente estudado para o propósito terapêutico é o A, entretanto, os estudos sobre os efeitos dos demais sorotipos estão em crescimento.
Em 1978, Alan Scott conduziu os primeiros testes com a TxB-A injetada em seres humanos para o tratamento de estrabismo 2. Posteriormente sua indicação se estendeu para as distonias segmentares, tremores e outros movimentos anormais.
O uso da TxB no tratamento da espasticidade foi feito pela primeira vez em 1989, onde foi publicado o resultado de sua aplicação em músculos intensamente espásticos de seis pacientes adultos com hemiplegia secundária ao infarto cerebral. Os neurologistas perceberam a potencial utilidade da TxB em desordens neurológicas envolvendo excessiva contração ou tônus muscular 5.
Utiliza-se a unidade internacional (UI) para definir a potência biológica de todas as preparações de TxB, sendo uma UI a quantidade de TxB capaz de matar (em experimentos) a metade de uma população de ratos (DL50) 6.
MECANISMOS DE AÇÃO
O princípio ativo da TxB é um complexo proteico derivado do Clostridium botulinum. Este complexo proteico consiste em uma neurotoxina com 150.000 Daltons e proteínas acessórias não tóxicas associadas de forma não covalente que estabilizam e protegem o componente farmacologicamente ativo, resultando em um peso molecular final que varia de 300.000 a 900.000 Daltons 1,3,4. A composição e o peso molecular total do complexo de macromoléculas dependem do sorotipo e da espécie de Clostridium botulinum que o produz, variando também segundo os métodos de purificação e análise. Comercialmente as TxB dos tipos A e B são agentes biológicos obtidos laboratorialmente, sendo substâncias cristalinas e estáveis, liofilizadas, associadas à albumina humana e utilizadas, após diluição, em solução de NaCl a 0,9% 7.
Em condições fisiológicas espera-se que o complexo sofra dissociação e libere a neurotoxina pura, pois esses complexos multiméricos são estáveis somente em pH ácido4.
A TxB é composta por uma cadeia proteica leve e uma pesada, ligadas entre si por uma ponte dissulfeto. A cadeia pesada é responsável pela internalização da TxB nos terminais colinérgicos pré-sinápticos. Por outro lado, a cadeia leve é uma zinco-endopeptidase, responsável pelos seus efeitos tóxicos.
Trabalhos bioquímicos engenhosos e de paciência têm mostrado que essas toxinas são proteases altamente específicas que clivam proteínas SNARE (Soluble NSF Attachment protein Receptors) pré-sinápticas envolvidas com o processo de exocitose das vesículas sinápticas nos terminais nervosos. A destruição destas proteínas pré-sinápticas é a base para a ação destas toxinas sobre a liberação de neurotransmissores 8.
AÇÃO SOBRE A LIBERAÇÃO DA ACETILCOLINA
A TxB é uma neurotoxina que possui alta afinidade pelas sinapses colinérgicas, ocasionando um bloqueio na liberação de acetilcolina desses terminais nervosos sem, contudo, alterar a condução neural de sinais elétricos e/ou a síntese e armazenamento de acetilcolina 7. A injeção muscular de TxB, em dose e localização apropriadas, provoca desnervação química parcial e diminuição da contratura, sem ocasionar paralisia completa. Quando esse tecido é glandular tem-se o bloqueio da secreção.
A aplicação local intramuscular de uma diluição selecionada de TxB é seguida de difusão rápida no espaço intersticial, depositando-se, especificamente, nas terminações nervosas motoras dos músculos esqueléticos (placa neuromuscular).
A inibição da liberação de acetilcolina pela TxB ocorre em processo de múltiplas etapas. Inicialmente, a TxB liga-se aos receptores de membrana pré-sináptica do terminal nervoso motor de maneira irreversível. Essa especificidade ao local de ligação garante à TxB alta seletividade para sinapses colinérgicas. Esses receptores pré-sinápticos são responsáveis pela endocitose da neurotoxina para o terminal nervoso motor 7.
Após a interiorização da molécula, a mesma é separada em duas cadeias polipeptídicas por proteases presentes no terminal nervoso motor. Essa clivagem da TxB é considerada o passo decisivo para sua ativação, uma vez que, enquanto cadeia única de 150.000 Daltons, a TxB apresenta pouca atividade farmacológica. Com a clivagem, têm-se dois fragmentos de polipeptídeos: uma cadeia pesada com 100.000 Daltons e uma leve com 50.000 Daltons. A percentagem da clivagem varia de acordo com o sorotipo. O sorotipo A é o que tem maior percentagem de clivagem, frequentemente de 90 a 95%, enquanto o sorotipo B apresenta-se clivada em menor percentagem (aproximadamente 70%) 3,4.
Após a clivagem, a cadeia leve é translocada através da membrana da vesícula endocítica para dentro do citosol e se liga com alta especificidade ao complexo proteico SNARE. O alvo proteico também varia conforme o sorotipo de TxB. Atuando como enzimas, as cadeias leves de cada um dos sete sorotipos clivam uma ligação peptídica distinta em um ou mais pontos das proteínas SNARE, de tal forma que nenhum dos sorotipos atua exatamente no mesmo local, o que faz com que suas características de ação e suas potências variem substancialmente, embora todos os sorotipos apresentem o mesmo efeito final: inibição da liberação de acetilcolina na terminação nervosa 4.
Os sorotipos A e E clivam a SNAP-25 (Synaptosomal-Associated Protein of 25 kDa), o sorotipo C age como protease na sintaxina, ambas proteínas SNARE da membrana pré-sináptica. As TxB dos tipos B, D, F, e G clivam especificamente a VAMP (Vesicle-Associated Membrane Protein), mais conhecida com sinaptobrevina II, proteína localizada na vesícula sináptica 1,9.
A clivagem proteolítica do complexo SNARE realizada pela cadeia leve da TxB previne a ancoragem da vesícula sináptica na superfície interna da membrana celular, resultando assim no bloqueio da fusão vesicular, efeito este que impede a liberação de acetilcolina, induzindo paralisia flácida nas fibras musculares atingidas (desnervação química).
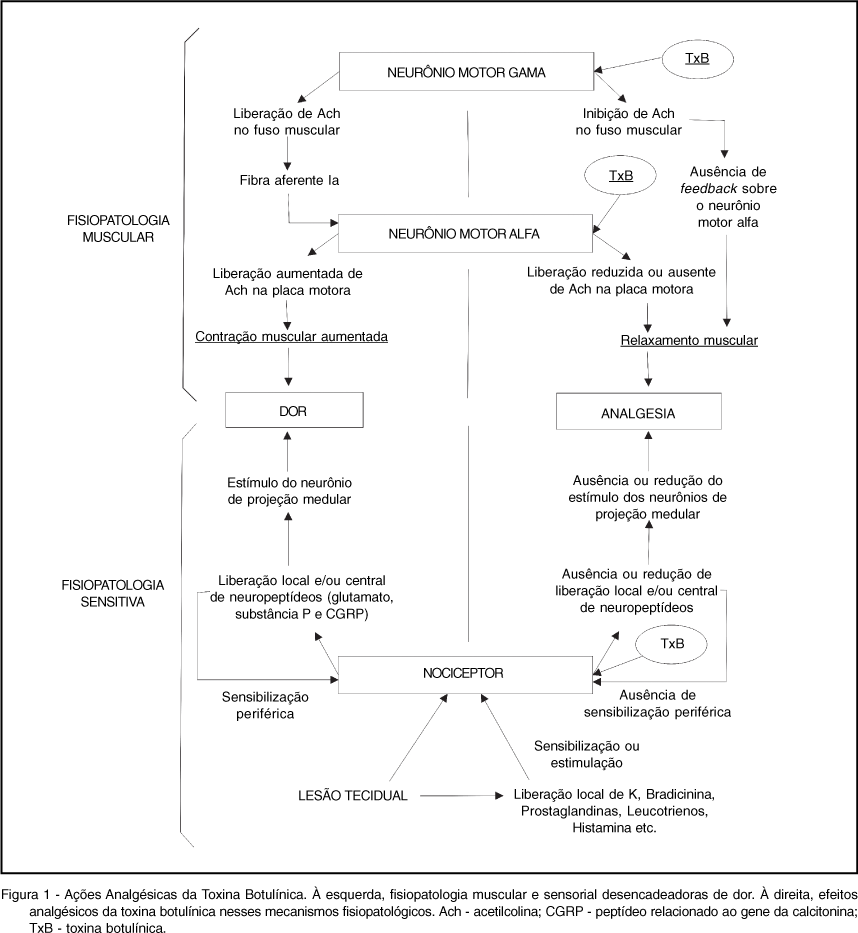
A ação clínica evidente é a fraqueza ou paralisia dose-dependente no músculo esquelético nas terminações nervosas motoras. O primeiro efeito na musculatura é sobre a função do neurônio motor alfa, responsável pela estimulação das fibras musculares propriamente ditas, mas a TxB pode afetar também os neurônios motores gama que inervam o fuso muscular. A inibição destes últimos resulta em diminuição do tônus muscular, devido a consequente diminuição do feedback aferente sobre o neurônio motor alfa, proveniente do fuso muscular 1,10,11 (Figura 1).
DURAÇÃO DA AÇÃO E RESTAURAÇÃO DA FISIOLOGIA NORMAL
A ação da TxB no músculo estriado esquelético tem seu início em alguns dias (2 a 5 dias) se estendendo, em alguns casos, em até duas semanas. Uma vez instalado, o efeito perdura por seis semanas a seis meses (em média de três a quatro meses). Durante o período de efeito mais intenso, por meio de exame histológico, observa-se atrofia muscular e alteração das fibras 7,12. Após dois a três meses, gradualmente começa a diminuir sua ação marginalmente.
A reversão da paralisia local ocorre por dois mecanismos: 1) Pelo "brotamento neural", onde se tem a formação de brotos axonais, reinervação e formação de novas placas terminais menores com a reinervação muscular temporária (receptores de acetilcolina extrajuncionais) e 2) Pela regeneração das proteínas de acoplamento das vesículas de acetilcolina (complexo SNARE) 14, cuja função é restabelecida entre um e quatro meses 10.
A via metabólica da TxB não está devidamente documentada, porém pode ser explicada pela presença de proteases que ocasionam a degradação de suas cadeias polipeptídicas.
IMUNOGENICIDADE DA TXB-A E PARTICULARIDADES DO SOROTIPO B
Por se tratar de compostos proteicos estranhos ao organismo, o complexo polipeptídico da TxB tem como uma de suas características potencial de ativação do sistema imunológico do paciente.
Apesar do uso clínico da TxB ser através da administração local, sua presença na corrente sanguínea tem sido documentada. Pode-se considerar como prova da presença sistêmica da TxB a dosagem de anticorpos resultantes a partir de sua aplicação, demonstrada por técnicas de ELISA (enzyme-linked immunoabsorbent assay) ou RIA (radioimmunoassay).
Altas doses, aplicações frequentes (intervalos curtos) e alta carga proteica associada à TxB nas formas comercialmente disponíveis do produto aumentam o risco de desenvolvimento de anticorpos neutralizantes.
Tem sido observado que o desenvolvimento de anticorpos neutralizantes contra a TxB para tratamentos de distonias tem prevalência similar em crianças e adultos, ocorrendo normalmente entre o primeiro e quarto ano do início do tratamento, reduzindo esta probabilidade após esse período (com baixa imunogenicidade depois de 18 anos de uso) 13.
Quando anticorpos contra a TxB são formados, a duração da ação e a duração máxima dos efeitos terapêuticos são usualmente reduzidas após poucas aplicações de TxB (falha terapêutica parcial).
Apesar de dados de TxB-A relatarem que em 10% ou mais dos pacientes tratados com injeções repetidas houve perda da resposta (não-respondedores secundários) 16, trabalhos com o uso de TxB-A em distonia cervical constataram que as preparações convencionais podem induzir a formação de anticorpos em até 5% dos pacientes 1. Outras casuísticas com uso de TxB-A em distonias dosaram anticorpos neutralizantes em aproximadamente 1% dos pacientes (0 a 2%) 15,16.
Estudos têm demonstrado que anticorpos contra a TxB-A não atuam sobre a TxB-B e que a TxB-B se liga à proteína de uma cadeia transportadora em local diferente da TxB-A, o que aponta estratégia para o manuseio de pacientes imunologicamente reativos, ou seja, tratá-los com outros sorotipos de TxB 12.
Cabe ressaltar que mais estudos clínicos bem fundamentados são necessários para observar a aplicação de TxB-B, visto que a mesma, por ser menos potente que o sorotipo A (já que sua clivagem e consequente ativação ocorre em menor proporção) exige maior dose (em UI), o que acarreta maior carga de proteínas e consequente maior potencial imunogênico. Os estudos indicam que nos paciente com distonia cervical se faz necessária uma dose entre 7.500 e 10.000 UI de TxB-B para produzir um efeito terapêutico razoável. Efeitos terapêuticos similares se conseguem com doses aproximadas de 150 a 200 UI de TxB-A (BOTOX®) ou com 500 a 700 UI de TxB-A (DYSPORT®). Isto indica um fator de conversão para BOTOX® da TxB-B na ordem de 40 a 70 e para DYSPORT® na ordem de 10 a 20 vezes. Sem os dados exatos de conversão é difícil comparar a efetividade, efeitos adversos e custos comparando-se as TxB-A e TxB-B 12.
Pacientes com distonia cervical tratados com TxB-B apresentaram, substancialmente, mais secura de boca e distúrbios visuais (incidência de 30%) que o tratamento feito com TxB-A. É um efeito colateral indesejável, mas também um fenômeno interessante que evidencia maior afinidade desse sorotipo por fibras autonômicas 14.
NOVO HORIZONTE TERAPÊUTICO DA TXB: DOR
Comprovadamente, a TxB pode enfraquecer seletivamente a musculatura dolorosa e interromper o ciclo espasmo-dor, permitindo o alívio sustentado da dor, possibilitando ao paciente a realização de exercícios físicos, os quais são vitais para a recuperação em longo prazo 17.
Como já salientado, a TxB foi inicialmente usada para tratamento de condições motoras como as distonias, sendo que investigações posteriores notaram significantes benefícios na dor, o que com frequência excedia os resultados da melhora da contração muscular e não correspondia estritamente à região dos efeitos neuromusculares. Isto sugeria que essa substância poderia ter efeitos diretos sobre os mecanismos da dor, independentemente das ações neuromusculares.
Em humanos, o efeito analgésico da TxB-A foi primeiramente demonstrado após a observação do alívio significante da dor na distonia cervical. Embora os efeitos antidistônicos e antiespasmódicos da TxB-A são frequentemente atribuídos ao bloqueio da liberação de acetilcolina das vesículas pré-sinápticas, estudos recentes em animais sugerem outros mecanismos analgésicos para a neurotoxina.
Até o presente momento, as evidências sugerem que as propriedades analgésicas observadas fazem parte de um mecanismo de analgesia mais complexo, que vai além de simples relaxamento muscular. Os estudos levantam a possibilidade de interação complexa da TxB com tecidos periféricos e eventuais influências indiretas nos mecanismos centrais da dor 10,11.
POSSIBILIDADES DO PAPEL DA TXB NA REDUÇÃO DA DOR
Conforme já relatado, a aparente especificidade da TxB para nervos colinérgicos in vivo é devida à presença de receptores ou aceptores específicos na membrana do terminal nervoso motor. Alternativamente, tem sido observado através de modelos experimentais em que é feita a internalização da TxB no terminal nervoso, que ela é capaz de inibir prontamente a exocitose de outros neurotransmissores, como é o caso da norepinefrina, sendo o seu mecanismo de ação idêntico ao observado nas sinapses colinérgicas, ou seja, clivagem do complexo SNARE. Entretanto, sob condições in vivo, muitas células nervosas são desprovidas dos receptores/aceptores extracelulares, responsáveis pela internalização da TxB, o que a torna pouco eficiente, já que a única via de entrada alternativa que resta no terminal nervoso é através do caminho pinocitótico não específico. Neste contexto, é possível afirmar que a alta afinidade da TxB nas sinapses colinérgicas é, em parte, o que a faz tão útil em alterações neuromusculares.
Por outro lado, diversas exceções a essa especificidade têm sido observadas em laboratório. TxB-A foi associada à inibição da liberação de substância P em cultura de neurônios de gânglios da raiz dorsal de embriões de ratos, bem como à redução da liberação estimulada (mas não a basal) do peptídeo relacionado ao gene da calcitonina (CGRP) em culturas de neurônios do gânglio trigeminal. Adicionalmente, a administração prévia (subcutânea) de TxB-A na pata de ratos atenuou significativamente a resposta à dor inflamatória induzida pela aplicação subcutânea do agente algésico formalina, além de induzir redução na liberação de glutamato pelo axônio periférico do nociceptor. Atividade reduzida nos neurônios do corno dorsal da medula espinhal foi também constatada. Analisados em conjunto, estes resultados apontam para ação inibitória direta da TxB-A sobre o nociceptor, promovida pela inibição da liberação dos neuropeptídeos (glutamato, CGRP e substância P) responsáveis pela neurotransmissão e/ou sensibilização periférica e central da via de dor (Figura 1). Assim, além de potente inibidor da liberação de acetilcolina, a TxB teria uma ação inibitória em outros neurotransmissores e neuropeptídeos, o que explicaria sua ação antiinflamatória e analgésica 9,18,19.
Estudos são ainda necessários para elucidar os mecanismos envolvidos nessa ação inibitória da TxB sobre o nociceptor, mas acredita-se atualmente que a TxB tenha quatro possíveis modos de atuar na interrupção dos sinais dolorosos:
1) Normalização da hiperatividade muscular;
2) Normalização da excessiva atividade do fuso muscular;
3) Fluxo neuronal retrógrado para o SNC;
4) Inibição da liberação dos neuropeptídeos pelo nociceptor, tanto no tecido periférico, como no sistema nervoso central 9,20.
APLICAÇÕES CLÍNICAS
Em 1990, o NIH (National Institutes of Health) emitiu um consenso considerando o uso clínico da TxB:
- A TxB é segura e efetiva no tratamento de estrabismo* e no tratamento sintomático do blefaroespasmo essencial*, espasmo hemifacial, disfonia espasmódica do adutor, bruxismo, apertamento dentário, distonia mandibular e distonia cervical* (*indicações atuais aprovadas pelo Food and Drug Administration); todas as outras são usadas ainda sem regulamentação definitiva pelo FDA.
- A TxB é promissora para o tratamento de outras condições, entretanto estudos adicionais são necessários como nas seguintes desordens: distonia focal e segmentar, incluindo distonia das mãos e membros, hipercontratilidade do esfíncter interno anal, dissinergia do detrussor (usualmente consequência de lesão da medula espinhal), espasticidades, disfonia espasmódica do abdutor, tremor vocal e gagueira.
- Estudos clínicos adicionais são encorajados para elucidar muitas questões sem resposta sobre a TxB e seus usos terapêuticos 2.
Estudos com a TxB-A formaram a base para tal referência. Rapidamente depois, a TxB-B foi introduzida nos estudos clínicos para distonia cervical e foi provada sua efetividade e segurança. O uso da TxB para distonia focal tornou-se difundido. Relatos da eficácia em espasticidade e outras condições neurológicas seguiram-se. A segurança da terapia com TxB tem permitido seu uso em estética, hiperidrose, sialorreia, dor tensional, entre outras. A eficácia em cada uma dessas aplicações pode ser prontamente explicada através do efeito da TxB na neurotransmissão colinérgica 21.
O sorotipo F tem sido avaliado clinicamente e encontrou-se curta duração de seus efeitos. Atualmente, benefícios terapêuticos com o sorotipo C têm sido relatados em somente três pacientes, um com blefaroespasmo e dois com hemiespasmo facial idiopático 11.
Somente dois sorotipos são comercialmente disponíveis. A primeira formulação da TxB-A foi comercializada nos EUA em 1989 pela Allergan como Toxina Botulínica (Botox®). Em 1991, formulação diferente foi comercializada fora dos EUA pela Ipsen como Toxina Botulínica (Disport®). A TxB-B foi aprovada pela FDA em 2000 e comercializada pela Élan Pharmaceuticals nos EUA como Toxina Botulínica (Mioblock®) (é conhecida como Neurobloc® na Europa). Em 2002, a TxB-A foi comercializada como Toxina Botulínica (Botox Cosmetic®) pela Allergan para usos cosméticos (Botox® e Botox cosmetic® tem a mesma formulação).
No mercado brasileiro, o laboratório Cristália disponibilizou recentemente a Toxina Botulínica (Prosigne®), com apresentação de 50 e 100UI.
Atualmente TxB-A tem sido usado para tratar mais de um milhão de pacientes em todo mundo e seu uso clínico foi aprovado em 73 paises. Essas aprovações incluem o tratamento da paralisia cerebral juvenil em 52 paises e espasticidade adulta em 36 paises, embora essas indicações não estejam regulamentadas nos EUA. Outros usos sem regulamentação do TxB-A nos EUA incluem cefaleias primárias como a migrânea, dor miofacial, acalásia, desordens de sudorese excessiva e sialorreia associada a condições como paralisia cerebral e doença de Parkinson 2.
Há 20 anos, a TxB-A tem sido usada para o tratamento de uma variedade de desordens caracterizadas pelo aumento patológico da contração (tônus) muscular. Correntes de pesquisa se esforçam em focar novas áreas para aplicação da TxB em terapias dolorosas específicas, particularmente em cefaleias primárias e síndrome dolorosa miofacial cervical, da cintura escapular e dorso. Estes estudos embasam novas opções para pacientes com síndromes dolorosas resistentes a tratamentos atualmente disponíveis.
O tratamento adjuvante com fisioterapia é importante para maximizar os benefícios da TxB. Alongamento passivo tem benefício particular imediatamente após as injeções de toxina botulínica, assim como o relaxamento muscular por massagem profunda e aumento da amplitude de movimento dos músculos, tendões e ligamentos. Uma vez que a dor se torna tolerável, exercícios ativos de alongamento podem ser iniciados. O objetivo destes exercícios é alcançar reeducação neuromuscular, quebrando o ciclo espasmo-dor, amplificado por sensibilização central. Então, a postura e a mecânica articular devem melhorar e reflexos tendinosos normais podem ser restabelecidos 19.
As primeiras publicações de estudos clínicos com TxB-A foram em dor miofascial (Aquadro e Borodic, 1994; Cheshire e col., 1994), desordens na região da articulação temporomandibular (Moore e Wood, 1994), dor facial (Girdler, 1994) e cefaleia tipo tensão (Zwart e col., 1994). O número de casos era pequeno e os resultados contraditórios. O aumento da evidência de eficácia foi recentemente obtido com estudos placebo-controlado, duplamente encobertos e com distribuição aleatória dos pacientes e com grande número de casos.
Baseado nas propriedades relaxantes musculares, a TxB-A tem sido usada para tratar uma variedade de condições musculares incluindo desordens do trato digestivo superior, cosmético, desordens geniturinárias, espasticidade, distonia cervical e blefaroespasmo 22.
Mais especificamente com relação à dor, várias publicações tem demonstrado a eficácia e segurança da TxB-A no tratamento da cefaleia tipo tensão, migrânea, dor lombar crônica e dor miofascial 23.
TXB-A NO TRATAMENTO DA SÍNDROME DOLOROSA MIOFASCIAL
Tratamentos convencionais da síndrome dolorosa miofascial são frequentemente insatisfatórios, com episódios persistindo por pelo menos um ano; ou seja, analgésicos usados para o alívio da dor crônica são caros e podem levar ao aumento significativo de nefropatias. Já com a TxB, em uma simples injeção pode se obter benefícios por um a três meses quando acompanhada de adequada fisioterapia sem o efeito colateral de comprometimento da função renal 24.
Em estudo comparativo entre agulhamento seco, anestésico local (lidocaína) em injeção local e baixas doses de TxB no tratamento de pontos gatilho (trigger points) na síndrome dolorosa miofascial, observou-se aumento da amplitude de movimentos na musculatura cervical nos três grupos. Já variáveis como dor, fadiga e inabilidade para o trabalho, medidos pela escala analógica visual (VAS), mostrou importante decréscimo no grupo da injeção com lidocaína e a TxB, não se observando o mesmo resultado positivo com o agulhamento seco. Entretanto a lidocaína demonstrou ser mais eficaz que a TxB quando comparada com agulhamento seco.
Sensações como fadiga, dor muscular e cefaleia podem ser referidas após injeção de TxB-A. Entretanto estes efeitos colaterais duram poucos dias 25.
Também na DTM (disfunção temporomandibular), causada por dor miofascial crônica, a TxB-A tem aplicação clínica. Aqui, a dor miofascial resulta frequentemente de hiperatividade da musculatura mastigatória (apertamento e bruxismo) e hipermobilidade do côndilo e pode se irradiar para região do músculo afetado, durante o sono ou após exercício intenso da musculatura mastigatória.
Como regra, os músculos que fecham a mandíbula (masseter, temporal e pterigoideo medial) e os que protraem a mandíbula (pterigoideo lateral) são afetados.
Em trabalho prospectivo, placebo-controlado, 90 pacientes apresentando DTM, foram previamente tratados com tratamento conservador (placa miorrelaxante e fisioterapia com técnicas relaxantes e massagem) por no mínimo três e no maximo 34 meses. Sessenta destes pacientes, receberam TxB-A 35UI e 30 receberam solução de NaCl (solução fisiológica a 0,9%) em músculos masseter, temporal e pterigoideo lateral pela via intra oral (77%); alguns músculos foram abordados pela via extra oral como temporal e masseter (23%). As injeções foram administradas nas regiões mais doloridas do músculo. A diluição da TxB-A foi feita com 0,7 mL de solução fisiológica a 0,9%. Tanto a solução fisiológica (placebo) quanto a solução de TxB-A foram injetadas nos músculos de forma bilateral. Foi solicitado aos pacientes a suspensão de outros tratamentos para sua dor sete dias antes da primeira injeção.
Os resultados demonstraram melhora em 55 pacientes (91%) no grupo da TxB-A com decréscimo de 3.2 pontos na escala visual analógica (VAS). No grupo placebo, a melhora da dor local foi de apenas 0.4 pontos na VAS. Os pacientes com dor mais intensa (VAS maior que 6.5) apresentaram melhora significativa 26.
TXB-A NO TRATAMENTO DA DOR LOMBAR CRÔNICA
Na dor lombar crônica os principais critérios de inclusão para uso da toxina botulínica são: 1) Dor há no mínimo seis meses; 2) Idade mínima de 18 anos; 3) Falha no tratamento medicamentoso preconizado ou em tratamento cirúrgico. Os critérios de exclusão são: 1) Ressonância eletromagnética lombo-sacra anormal, com indicação de intervenção cirúrgica de urgência ou atenção médica; 2) Gravidez ou o seu planejamento em curso; 3) Desordens na transmissão neuromuscular; 4) Alergia conhecida ou toxicidade à toxina botulínica tipo A; 5) Litígio em curso, como apresentado no quadro I.
A aplicação na dor lombar pode ser unilateral ou bilateral, com base no padrão predominante de distribuição da dor. O primeiro local de injeção é selecionado no nível da vértebra de dor mais intensa (definido pelo paciente e pelo médico através de palpação digital muscular profunda). Injeções subsequentes são aplicadas pelo menos um e frequentemente dois níveis acima e abaixo da localização da dor. Além disto, os pacientes podem receber injeção em cinco pontos da musculatura paraespinhal entre os níveis L1 e S1. Quando a dor se estende lateralmente, a mesma dose é administrada mais lateralmente ao nível do músculo paraespinhal. A dose por injeção (por ponto) é feita com 40 UI para pacientes magros e 50UI para pacientes com peso normal ou acima. A dose total por sessão pode variar de 200 a 500 unidades dependendo de presença de dor unilateral ou bilateral 27.
Anestésicos locais podem ser usados como veículos para TxB-A, sem alterar seus efeitos clinicos 28.
O término da analgesia após a sua aplicação no uso em lombalgia ocorre em três a quatro meses.
TXB-A NO TRATAMENTO DAS CEFALEIAS
Até o ano 2000 apenas cinco estudos haviam sido publicados a respeito da TxB-A no tratamento da migrânea. Interessante notar que todos os estudos mostraram evidência de boa e consistente eficácia da TxB-A . Menção especial deve ser feita aos estudos controlados conduzidos por Brin e col. (2000) e por Silberstein e col. (2000), ambos com delineamento duplamente encoberto, placebo-controlado e com padronização dos pontos de injeção. Estes estudos observaram significante decréscimo na intensidade dos episódios e da frequência de migrânea, cefaleia tipo tensão e outros tipos de cefaleia. A dose utilizada de TxB-A era relativamente baixa, particularmente no estudo de Silberstein e col com 25 UI de TxB-A. A variação de resultados nos estudos clínicos com TxB-A, poderia ter varias origens, tais como, seleção de pacientes, protocolo de injeções administradas e a variação de doses usadas, uso concomitante de medicação profilática para cefaleia. Efeitos adversos mais frequentes, possíveis de ocorrerem são fraqueza muscular, rigidez cervical, dor cervical, sendo que esta ocorrência é de aproximadamente 3%. Os resultados positivos no tratamento das cefaleias podem aparecer de forma plena, somente 90 dias após aplicação 29.
A TxB-A é efetiva na profilaxia de vários tipos de cefaleias, incluindo a migrânea. Cefaleias com desordens musculares respondem ao tratamento com a TxB-A incluindo a cefaleia cervicogênica e a cefaleia crônica associada com lesão cervical tipo chicote (whiplash).
Na migrânea, acredita-se, porém sem conclusão definitiva, que o mecanismo de ação da TxB-A seja pelo relaxamento da musculatura infiltrada pela TxB-A e também em consequência, diminuição da pressão sobre as raízes do nervo trigêmeo. Esta teoria se sustenta pelo fato de pacientes com migrânea apresentarem considerável hipertrofia do músculo corrugador, comprimindo ramos trigeminais e também em região das têmporas 30.
No quadro II são apresentados os critérios de inclusão e exclusão na seleção de pacientes para o tratamento das cefaleias com TxB-A.
TXB-A NO TRATAMENTO DA DOR NEUROPÁTICA
A nocicepção pode ser aumentada pela liberação de agentes pró-inflamatórios como citocinas, adenosina, bradicinina, serotonina e prostaglandinas, que podem alterar ou sensibilizar a transmissão neuronal e criar estado temporário de dor neuropática. Diferentemente, a dor neuropática crônica resulta da lesão do sistema nervoso periférico ou central e representa anormalidade na transmissão nervosa que se desenvolveu em decorrência da lesão.
Pacientes com síndrome complexa de dor regional tipo I (SCDR I), frequentemente sofrem de dor miofascial em músculos próximos do membro afetado mostrando que diferentes tipos de dor podem coexistir no mesmo paciente 31.
Pacientes com síndrome dolorosa miofascial podem apresentar sensações características da dor neuropática, como hiperestesia, parestesia, queimação, fisgada e alodínea. Disfunção autonômica também tem sido observada nos pontos gatilhos e distalmente a eles.
Em pacientes com síndrome complexa de dor regional tipo I, que concomitantemente apresente síndrome dolorosa miofascial, está demonstrada a importância do uso da TxB-A em músculos do mesmo lado da lesão como em regiões paracervical, suboccipital e periescapular, com doses de 300 UI de TxB-A, injetados nos músculos esternocleidomastoideo, trapézio, esplênio da cabeça (splenio captis), esplênio do pescoço (splenio cervicis), supra e infraespinhal e romboide. A seleção dos músculos para receber a TxB-A é baseada no relato do paciente de dor máxima e na identificação de pontos gatilho no exame físico. Um total de 25 a 50 UI de TxB-A pode ser injetado em cada músculo dependendo do seu tamanho 32.
Em trabalho apresentado em 2002, um estudo sobre a efetividade da TxB-A no tratamento de dor segmentar em queimação originada da medula espinhal, dois pacientes com lesão medular em região cervical, que desenvolveram alodínea, hiperestesia e dor espontânea em queimação com distribuição segmentar, foram tratados com injeções subcutâneas múltiplas (16 a 20) de 5 UI de TxB-A (com dose total de 100 U), repetidas a cada dois a três meses por 3 anos. O autor concluiu que injeções subcutâneas de TxB-A podem reduzir os sintomas da dor neuropática por alterar os mecanismos periféricos da transmissão da dor, tendo como consequência a redução da sensibilização central 33.
CONCLUSÃO
A terapia com TxB-A é segura e bem tolerada em desordens dolorosas crônicas, onde regimes de farmacoterapia podem sabidamente provocar efeitos colaterais. O tratamento com TxB-A, inicialmente de alto custo, deveria ser considerado devido a baixa incidência de efeitos colaterais e, quando necessária, internação hospitalar de curto período. Outra vantagem é a redução de medicamentos adjuvantes e tempo de ação, com duração de três a quatro meses por dose, diferentemente do uso contínuo de outras medicações.
Pesquisas futuras serão necessárias para se estabelecer a eficácia da TxB-A em desordens dolorosas crônicas e seu exato mecanismo de ação no alívio da dor, bem como seu potencial em tratamentos multifatoriais 34.
Apresentado em 12 de maio de 2008
Aceito para publicação em 9 de fevereiro de 2009
- 01. Dressler D, Saberi FA, Barbosa ER - Botulinum toxin: mechanisms of action. Arq Neuropsiquiatr 2005;63:180-185.
- 02. Lang A - History and uses of BOTOX (botulinum toxin type A). Lippincott's Case Manag 2004;9:109-112.
- 03. Wenzel RG - Pharmacology of botulinum neurotoxin serotype A. Am J Heath-Syst Pharm 2004;61(suppl 6):s5-10.
- 04. Setler PE - Therapeutic use of botulinum toxins: background and history. Clin J Pain 2002;18(6 suppl):s119-124.
- 05. Aguilar-Rebolledo F, Hernandez-Sanchez J, Rayo-Mares D et al. - Toxina botulínica como tratamiento de la espasticidad y distonia en la parálisis cerebral infantil. Gac Méd Mex 2001;137:403-411.
- 06. Wohlfarth K, Kampe K, Bigalke H - Pharmacokinetic properties of different formulations of botulinum neurotoxin type A. Mov Disord 2004;19:s65-67.
- 07. Unno Ek, Sakato RK, Issy AM - Estudo comparativo entre toxina botulínica e bupivacaína para infiltração de pontos-gatilho em síndrome dolorosa miofascial crônica. Rev Bras Anestesiol 2005; 55:250-255.
- 08. Purves D, Augustine GJ, Fitzpatrick D et al. - Neuroscience. 3 Ed. Massachusetts, Sinauer 2004;110-116.
- 09. Aoki KR - Review of a proposed mechanism for the antinociceptive action of botulinum toxin type A. Neurotoxicology 2005; 26:785-793.
- 10. Freund B; Schwartz M - Temporal relationship of muscle weakness and pain reduction in subjects treated with botulinum toxin A. J Pain 2003;4:159-165.
- 11. Aoki KR - Pharmacology and immunology of botulinum toxin serotypes. J Neurol 2001;248(suppl 1):3-10.
- 12. Dressler D, Chaná Cuevas P - La toxina botulínica tipo B: Dónde estamos? Rev Chil Neuro-psiquiatr 2002;40:6-8.
- 13. Mejia NI, Vuong KD, Jankovic J - Long-term botulinum toxin efficacy, safety and immunogenicity. Mov Disord 2005;20:592-597.
- 14. Cardoso F - Toxina botulínica tipo B no manejo de distonia não-responsiva à toxina botulínica tipo A. Arq Neuropsiquiatr 2003;61: 607-610.
- 15. Yablon S - Toxin neutralizing antibody formation with botulinum toxin type A (BoNTA) treatment in neuromuscular disorders. Neurology 2005;64:1153.
- 16. Comella CL - Interim results of an observation study of neutralizing antibody formation with the current preparation of botulinum toxin type A treatment for cervical dystonia. Neurology 2004;62:6141.
- 17. Graboski CL, Gray DS, Burnham RS - Botulinum toxin A versus bupivacaine trigger point injections for the treatment of myofascial pain syndrome: A randomised double blind crossover study. Pain 2005;118:170-175.
- 18. Sycha T, Samal D, Chizh B et al. - A lack of antinociceptive or antiinflammatory effect of botulinum toxin A in an inflammatory human pain model. Anesth Analg 2006;102:509-516.
- 19. Sheeran G - Botulinum toxin for the treatment of musculoskeletal pain and spasm. Curr Pain Headache Rep 2002;6:460-469.
- 20. Göbel H, Heinze A, Heinze-Kuhn K et al. - Botulinun toxin A in the treatment of headache syndromes and pericranial pain syndromes. Pain 2001;91:195-199.
- 21. Lew MF - Review of the FDA-approved uses of botulinum toxins, including data suggesting efficacy in pain reduction. Clin J Pain 2002;18(6 suppl):s142-146.
- 22. Porta M - A comparative trial of botulinum toxin type A and methilprednisolone for the treatment of myofascial pain syndrome and pain for chronic muscle spasm. Pain 2000; 85:101-105.
- 23. Klein AW - The therapeutic potential of botulinum toxin. Dermatol Surg 2004;30:452-455.
- 24. Porta M, Perreti A, Gamba M et al. - The rationale and results of treating muscle spasm and myofascial syndromes with botulinum toxin type A. Pain Digest 1998;8:346-352
- 25. Kamanli A, Kaya A, Ardicoglu O et al. - Comparison of lidocaine injection, botulinum toxin injection, and dry needling to trigger points in myofascial pain syndrome. Rheumatol Int 2005;25:604-611.
- 26. von Lindern JJ, Niederhagen B, Bergé S et al. - Type A botulinum toxin in the treatment of chronic facial pain associated with masticatory hyperactivity. J Oral Maxillofac Surg 2003;61:774-778
- 27. Jabbari B, Ney J, Sichani A et al. -Treatment of refractory, chronic low back pain with botulinum neurotoxin A: an open-label, pilot study. Pain Med 2006;7:260-264.
- 28. Gassner HG, Sherris DA - Addition of an anesthetic agent to enhance the predictability of the effects of botulinum toxin type A injections: a randomized controlled study. Mayo Clin Proc 2000; 75:701-704
- 29. Silberstein SD, Gobel H, Jensen R et al. - Botulinum toxin type A in the prophylactic treatment of chronic tension-type headache: a multicentre, double-blind, randomized, placebo-controlled, parallel-group study. Cephalalgia 2006;26:790-800
- 30. Smuts JA, Schultz D, Barnard A - Mechanism of action of botulinum toxin type A in migraine prevention: a pilot study. Headache 2004;44: 801-805.
- 31. Allen G, Galer BS, Schwartz L - Epidemiology of complex regional pain syndrome: a retrospective chart review of 134 patients. Pain 1999;80:539-544
- 32. Argoff CE - Botulinum toxin type A treatment of myofascial pain with CRPS type I (reflex sympathetic dystrophy): a pilot study, em: World Pain Congress (IASP), Vienna, Austria, august 1999 - Poster presentation.
- 33. Jabbari B, Maher N - Effectiveness of botulinum toxin A against the segmental burning pain of spinal cord origin. In: International Conference 2002: Basic and Therapeutic Aspects of Botulinum and Tetanus Toxins, Hannover, Germany, 8-12, 2002 - Poster presentation.
- 34. Lang AM - Botulinum toxin type A therapy in chronic pain disorders. Arch Phys Med Rehabil 2003;(3/suppl 1)84:s69-73.
Datas de Publicação
-
Publicação nesta coleção
26 Maio 2009 -
Data do Fascículo
Jun 2009
Histórico
-
Aceito
09 Fev 2009 -
Recebido
12 Maio 2008