Resumos
Justificativa e objetivo:
Em crianças submetidas à cirurgia cardíaca congênita, os níveis plasmáticos de peptídeo natriurético cerebral (PNC) podem ter um papel no desenvolvimento da síndrome de baixo débito cardíaco (SBDC), definida como uma combinação de achados clínicos e intervenções para aumentar o débito cardíaco em crianças com hipertensão pulmonar.
Métodos:
Em um estudo prospectivo observacional, foram inscritas 51 crianças submetidas à cirurgia cardíaca congênita, com avaliação ecocardiográfica pré-operatória que mostrava hipertensão pulmonar. Os níveis plasmáticos de PNC foram avaliados antes e 12, 24 e 48 h após a operação. Os pacientes incluídos no estudo foram divididos em dois grupos em função de: (1) desenvolvimento de SBDC; (2) determinação dos valores de corte de PNC no pré-operatório pela análise da curva de funcionamento do receptor para SBDC. Os desfechos secundários foram: (1) duração da ventilação mecânica ≥ 72 h, (2) permanência em unidade de terapia intensiva > 7 dias e (3) mortalidade.
Resultados:
Os níveis de PNC nos períodos pré- e pós-operatório dos pacientes com ou sem SBDC (n = 35, n = 16, respectivamente) apresentaram diferenças significantes nos tempos de mensuração repetidos (p = 0,0001). O valor de corte de PNC de 125,5 pg mL−1 no pré-operatório obteve a maior sensibilidade de 88,9% e especificidade de 96,9% para prever a SBDC em pacientes com hipertensão pulmonar. Uma boa correlação foi descoberta entre o nível plasmático de PNC no pré-operatório e duração a ventilação mecânica (r = 0,67, p = 0,0001).
Conclusões:
Em pacientes com hipertensão pulmonar submetidos à cirurgia cardíaca congênita, 91% com níveis plasmáticos de PNC acima de 125,5 pg mL−1 no período pré-operatório estão em risco de desenvolver a SBDC, que é um desfecho importante no pós-operatório.
Pediatria; Cardiopatias congênitas; Circulação extracorpórea; Peptídeo natriurético tipo-B; Desfecho; Pós-operatório
Background and objectives:
In children undergoing congenital heart surgery, plasma brain natriuretic peptide levels may have a role in development of low cardiac output syndrome that is defined as a combination of clinical findings and interventions to augment cardiac output in children with pulmonary hypertension.
Methods:
In a prospective observational study, fifty-one children undergoing congenital heart surgery with preoperative echocardiographic study showing pulmonary hypertension were enrolled. The plasma brain natriuretic peptide levels were collected before operation, 12, 24 and 48 h after operation. The patients enrolled into the study were divided into two groups depending on: (1) Development of LCOS which is defined as a combination of clinical findings or interventions to augment cardiac output postoperatively; (2) Determination of preoperative brain natriuretic peptide cut-off value by receiver operating curve analysis for low cardiac output syndrome. The secondary end points were: (1) duration of mechanical ventilation ≥72 h, (2) intensive care unit stay >7days, and (3) mortality.
Results:
The differences in preoperative and postoperative brain natriuretic peptide levels of patients with or without low cardiac output syndrome (n = 35, n = 16, respectively) showed significant differences in repeated measurement time points (p = 0.0001). The preoperative brain natriuretic peptide cut-off value of 125.5 pg mL−1 was found to have the highest sensitivity of 88.9% and specificity of 96.9% in predicting low cardiac output syndrome in patients with pulmonary hypertension. A good correlation was found between preoperative plasma brain natriuretic peptide level and duration of mechanical ventilation (r = 0.67, p = 0.0001).
Conclusions:
In patients with pulmonary hypertension undergoing congenital heart surgery, 91% of patients with preoperative plasma brain natriuretic peptide levels above 125.5 pg mL−1 are at risk of developing low cardiac output syndrome which is an important postoperative outcome.
Pediatrics; Congenital heart defects; Cardiopulmonary bypass; B-type natriuretic peptide; Outcome; Postoperative
Justificación y objetivo:
En niños sometidos a cirugía de cardiopatía congénita, los niveles plasmáticos de péptido natriurético cerebral pueden tener un papel en el desarrollo del síndrome de bajo gasto cardíaco, definido como una combinación de hallazgos clínicos e intervenciones para aumentar el gasto cardíaco en niños con hipertensión pulmonar.
Métodos:
En un estudio prospectivo observacional, se inscribieron 51 niños sometidos a cirugía de cardiopatía congénita, y cuya evaluación ecocardiográfica preoperatoria mostró hipertensión pulmonar. Los niveles plasmáticos de péptido natriurético cerebral fueron evaluados antes de la operación, y 12, 24 y 48 h después de la operación. Los pacientes incluidos en el estudio fueron divididos en 2 grupos en función de: (1) desarrollo de síndrome de bajo gasto cardíaco, definido como una combinación de hallazgos clínicos o de intervenciones para aumentar el gasto cardíaco en el postoperatorio; (2) determinación de los valores de corte de péptido natriurético cerebral en el preoperatorio por el análisis de la curva de funcionamiento del receptor para el síndrome de bajo gasto cardíaco. Los resultados secundarios fueron: (1) duración de la ventilación mecánica ≥ 72 h, (2) permanencia en unidad de cuidados intensivos (UCI) > 7 días, y (3) mortalidad.
Resultados:
Los niveles de péptido natriurético cerebral en los períodos pre y postoperatorio de los pacientes con o sin síndrome de bajo gasto cardíaco (n = 35 y n = 16, respectivamente) tuvieron diferencias significativas en los tiempos de medida repetidos (p = 0,0001). El valor de corte de péptido natriurético cerebral de 125,5 pg/mL−1 en el preoperatorio obtuvo la mayor sensibilidad de un 88,9% y una especificidad del 96,9% para prever el síndrome de bajo gasto cardíaco en pacientes con hipertensión pulmonar. Hubo una buena correlación entre el nivel plasmático de péptido natriurético cerebral en el preoperatorio y la duración de la ventilación mecánica (r = 0,67; p = 0,0001).
Conclusiones:
En pacientes con hipertensión pulmonar sometidos a cirugía de cardiopatía congénita, el 91% de los pacientes con niveles plasmáticos de péptido natriurético > 125,5 pg/mL−1 en el período preoperatorio están en riesgo de desarrollar síndrome de bajo gasto cardíaco que es un resultado importante en el postoperatorio.
Pediatría; Cardiopatías congénitas; Circulación extracorporeal; Péptido natriurético tipo B; Resultado; Postoperatorio
Introdução
Peptídeo natriurético cerebral (PNC) é um neuro-hormônio secretado principalmente pelos ventrículos em resposta ao aumento das pressões dos ventrículos direito ou esquerdo, bem como à sobrecarga do volume. Esse neurohormônio tem propriedades natriuréticas, diuréticas e vasodilatadoras.11. Haddad F, Doyle R, Murphy DJ, et al. Right ventricular function in cardiovascular disease, part II: pathophysiology, clinical importance, and management of right ventricular failure. Circulation. 2008;117:1717-31.,22. Ohuchi H, Takasugi H, Ohashi H, et al. Stratification of pediatric heart failure on the basis of neurohormonal and cardiac autonomic nervous activities in patients with congenital heart disease. Circulation. 2003;108:2368-76. A disfunção do ventrículo direito (VD) refere-se a anormalidades do enchimento ou da contração sem referência a sinais ou sintomas de insuficiência cardíaca. A hipertensão pulmonar (HP) é definida como um achado ecocardiográfico de pressão arterial pulmonar média ≥ 25 mm Hg em repouso e a insuficiência cardíaca (IC) é definida como disfunção ventricular esquerda, o que causa dilatação, afinamento das paredes e má contratilidade do coração, causas importantes de disfunção do VD.11. Haddad F, Doyle R, Murphy DJ, et al. Right ventricular function in cardiovascular disease, part II: pathophysiology, clinical importance, and management of right ventricular failure. Circulation. 2008;117:1717-31.,33. Law YM, Keller BB, Feingold BM, et al. Usefulness of plasma B-type natriuretic peptide to identify ventricular dysfunction in pediatric and adult patients with congenital heart disease. Am J Cardiol. 2005;95:474-8. O uso de PNC como um indicador de disfunção do VD em crianças com HP submetidas a cirurgias de cardiopatias congênitas permanece em grande parte desconhecido.
Estudos anteriores relataram um aumento dos níveis de PNC nos períodos pré- e pós-operatório em pacientes com defeito do septo ventricular ou disfunção ventricular.33. Law YM, Keller BB, Feingold BM, et al. Usefulness of plasma B-type natriuretic peptide to identify ventricular dysfunction in pediatric and adult patients with congenital heart disease. Am J Cardiol. 2005;95:474-8.–66. Paul MA, Backer CL, Binns HJ, et al. B-type natriuretic peptide and heart failure in patients with ventricular septal defect: a pilot study. Pediatr Cardiol. 2009;30:1094-7. Em estudos recentes, o objetivo foi investigar se os níveis de PNC podem ser usados como uma ferramenta para determinar o diagnóstico e prognóstico de crianças.66. Paul MA, Backer CL, Binns HJ, et al. B-type natriuretic peptide and heart failure in patients with ventricular septal defect: a pilot study. Pediatr Cardiol. 2009;30:1094-7.–99. Gessler P, Knirsch W, Schmitt B, et al. Prognostic value of plasma N-terminal pro-brain natriuretic peptide in children with congenital heart defects and open-heart surgery. J Pediatr. 2006;148:372-6. Relatou-se que os níveis plasmáticos de PNC aumentaram imediatamente após as cirurgias cardíacas congênitas, a despeito da descarga hemodinâmica, e também uma correlação entre o nível de pico de PNC e o tempo de circulação extracorpórea (CEC).1010. Koch A, Kitzsteiner T, Zink S, et al. Impact of cardiac surgery on plasma levels of B-type natriuretic peptide in children with congenital heart disease. Int J Cardiol. 2007;114:339-44. O desenvolvimento da SBDC tem sido usado recentemente como uma medida do resultado no pós-operatório em pacientes submetidos à cirurgia cardíaca congênita.1111. Hsu JH, Oishi PE, Keller RL, et al. Perioperative B-type natriuretic peptide levels predict outcome after bidirectional cavopulmonary anastamosis and total cavopulmonary connection. J Thorac Cardiovasc Surg. 2008;135:746-53.,1212. Shih CY, Sapru A, Oishi P, et al. Alterations in plasma B-type natriuretic peptide levels after repair of congenital heart defects: a potential perioperative marker. J Thorac Cardiovasc Surg. 2006;131:632-8. SBDC é definida como taquicardia, má perfusão periférica, oligúria, parada cardíaca, necessidade de um aumento de 100% em suporte farmacológico ou administração de um novo agente inotrópico, acidose metabólica com aumento do déficit basal.1313. Hoffman TM, Wernovsky G, Atz AM, et al. Efficacy and safety of milrinone in preventing low cardiac output syndrome in infants and children after corrective surgery for congenital heart disease. Circulation. 2003;107:996-1002.,1414. Vogt W, Läer S. Prevention for pediatric low cardiac output syndrome: results from the European survey EuLoCOS-Paed. Paediatr Anaesth. 2011;21:1176-84. Existem apenas alguns estudos que relatam que os níveis plasmáticos de PNB podem ajudar a identificar crianças com HP que causa disfunção do VD.66. Paul MA, Backer CL, Binns HJ, et al. B-type natriuretic peptide and heart failure in patients with ventricular septal defect: a pilot study. Pediatr Cardiol. 2009;30:1094-7.,1111. Hsu JH, Oishi PE, Keller RL, et al. Perioperative B-type natriuretic peptide levels predict outcome after bidirectional cavopulmonary anastamosis and total cavopulmonary connection. J Thorac Cardiovasc Surg. 2008;135:746-53.,1212. Shih CY, Sapru A, Oishi P, et al. Alterations in plasma B-type natriuretic peptide levels after repair of congenital heart defects: a potential perioperative marker. J Thorac Cardiovasc Surg. 2006;131:632-8. Além disso, demonstrou-se que em crianças com insuficiência cardíaca sintomática moderada, um nível de PNC maior ou igual a 140 pg mL−1 e idade superior a 2 anos estão independentemente associados a resultados mais modestos.1515. Auerbach SR, Richmond ME, Lamour JM, et al. BNP levels predict outcome in pediatric heart failure patients: post hoc analysis of the Pediatric Carvedilol Trial. Circ Heart Fail. 2010;3:606-11.
Nosso objetivo foi investigar a relação entre os níveis plasmáticos de PNC e os resultados clínicos no pós-operatório, tais como SBDC, tempo de ventilação mecânica, permanência em unidade de terapia intensiva e mortalidade em 30 dias de pós-operatório, em pacientes submetidos a cirurgias de cardiopatias congênitas com CEC. Além disso, comparamos os níveis plasmáticos de PNC prée pós-cirurgia em pacientes com ou sem SBDC.
Métodos
Pacientes
Foram incluídos neste estudo prospectivo observacional 51 pacientes com diagnóstico de HP e doença cardíaca congênita. O estudo foi conduzido após a aprovação do Comitê de Ética local, de julho de 2008 e setembro de 2009. Obtivemos o consentimento informado assinado pelos pais ou responsáveis dos pacientes antes da inscrição no estudo. Em todos os pacientes, a presença de HP e disfunção do VD foi identificada em estudo ecocardiográfico antes da operação. HP é definida como pressões arteriais sistólica e sistêmica de pelo menos 35 mm Hg ou superiores a 50% da pressão arterial média (PAM).1212. Shih CY, Sapru A, Oishi P, et al. Alterations in plasma B-type natriuretic peptide levels after repair of congenital heart defects: a potential perioperative marker. J Thorac Cardiovasc Surg. 2006;131:632-8.,1515. Auerbach SR, Richmond ME, Lamour JM, et al. BNP levels predict outcome in pediatric heart failure patients: post hoc analysis of the Pediatric Carvedilol Trial. Circ Heart Fail. 2010;3:606-11.,1616. Toyono M, Harada K, Tamura M, et al. Paradoxical relationship between B-type natriuretic peptide and pulmonary vascular resistance in patients with ventricular septal defect and concomitant severe pulmonary hypertension. Pediatr Cardiol. 2008;29:65-9. A detecção de HP é baseada na pressão arterial sistólica pulmonar (PAp), calculada a partir das velocidades de regurgitações das válvulas tricúspide ou pulmonar com o uso de ecocardiograma com Doppler.1616. Toyono M, Harada K, Tamura M, et al. Paradoxical relationship between B-type natriuretic peptide and pulmonary vascular resistance in patients with ventricular septal defect and concomitant severe pulmonary hypertension. Pediatr Cardiol. 2008;29:65-9.,1717. Koestenberger M, Nagel B, Avian A, et al. Systolic right ventricular function in children and young adults with pulmonary artery hypertension secondary to congenital heart disease and tetralogy of Fallot: tricuspid annular plane systolic excursion (TAPSE) and magnetic resonance imaging data. Congenit Heart Dis. 2012;7:250-8. Durante a mensuração, os seguintes critérios de diagnóstico foram usados neste estudo: (1) razão estimada entre as pressões pulmonar e sistêmica (Pp/Ps), com uso de ecocardiograma com Doppler > 0,5; (2) PAp medida pela análise com Doppler do fluxo e velocidade de regurgitação tricúspide e, de acordo com estudos anteriores com crianças, as relações entre PAp sistólica e diastólica e PAp média foram avaliadas;1717. Koestenberger M, Nagel B, Avian A, et al. Systolic right ventricular function in children and young adults with pulmonary artery hypertension secondary to congenital heart disease and tetralogy of Fallot: tricuspid annular plane systolic excursion (TAPSE) and magnetic resonance imaging data. Congenit Heart Dis. 2012;7:250-8. (3) regurgitação tricúspide significante; (4) VD aumentado ou hipertrófico, sem evidência de estenose pulmonar; (5) achatamento do septo intraventricular. A disfunção do VD é diagnosticada com base em dados ecocardiográficos e o parâmetro mais importante para o diagnóstico inclui o valor da excursão sistólica no plano anular da valva tricúspide (Espat), que é baseado na idade do paciente para avaliar a função sistólica do VD.1616. Toyono M, Harada K, Tamura M, et al. Paradoxical relationship between B-type natriuretic peptide and pulmonary vascular resistance in patients with ventricular septal defect and concomitant severe pulmonary hypertension. Pediatr Cardiol. 2008;29:65-9.,1717. Koestenberger M, Nagel B, Avian A, et al. Systolic right ventricular function in children and young adults with pulmonary artery hypertension secondary to congenital heart disease and tetralogy of Fallot: tricuspid annular plane systolic excursion (TAPSE) and magnetic resonance imaging data. Congenit Heart Dis. 2012;7:250-8. Os estudos ecocardiográficos foram feitos pelo mesmo cardiologista pediátrico nos períodos pré- e pós-operatório a cada 12 h e se houvesse sinais clínicos de crise de HP.
Todos os pacientes eram portadores de uma das cardiopatias congênitas com alto risco de desenvolver hipertensão pulmonar no pós-operatório e essas incluem: (1) defeito do septo ventricular (DSV) isolado; (2) DSV e conexão anômala total das veias pulmonares (CATVP); (3) DSV e conexão anômala parcial das veias pulmonares (CAPVP); (4) DSV com ou sem defeito do septo atrial (DSA) e/ou CAPVP e (5) defeito do septo atrioventricular (DSAV).1818. Landzberg MJ. Congenital heart disease associated pulmonary arterial hypertension. Clin Chest Med. 2007;28:243-53. Os pacientes com patologia ventricular única foram incluídos no estudo. Os pacientes com cardiomiopatias, transposição das grandes artérias, truncus arteriosus e síndrome de hipoplasia do coração esquerdo foram excluídos. No grupo de estudo, todos os pacientes apresentaram valores sistólicos de PAp entre 40 e 70 mm Hg, com valores sistêmicos de PAM entre 50-60%. Os pacientes com valores sistólicos de PAp acima de 70 mm H e sistêmicos de PAM acima de 60% foram excluídos do estudo.
Todos os pacientes foram submetidos à cirurgia de reparação cardíaca congênita com CEC. Em nosso estudo, a mesma equipe médica esteve envolvida em todos os procedimentos cirúrgicos. Os pacientes foram divididos em dois grupos em função de: (1) desenvolvimento de SBDC no pós-operatório e (2) valor de corte para PNC no pré-operatório, determinado pela análise da curva característica de operação do receptor (ROC) para SBDC.1111. Hsu JH, Oishi PE, Keller RL, et al. Perioperative B-type natriuretic peptide levels predict outcome after bidirectional cavopulmonary anastamosis and total cavopulmonary connection. J Thorac Cardiovasc Surg. 2008;135:746-53.,1313. Hoffman TM, Wernovsky G, Atz AM, et al. Efficacy and safety of milrinone in preventing low cardiac output syndrome in infants and children after corrective surgery for congenital heart disease. Circulation. 2003;107:996-1002.,1414. Vogt W, Läer S. Prevention for pediatric low cardiac output syndrome: results from the European survey EuLoCOS-Paed. Paediatr Anaesth. 2011;21:1176-84. Oligúria foi definida como um débito urinário inferior a 1 mL kg−1 h−1 em lactentes, inferior a 0,5 mL kg−1 h−1 em crianças.1919. Cerda J. Oliguria: an earlier and accurate biomarker of acute kidney injury? Kidney Int. 2011;80:699-701. Em crianças, os valores de referência normais para frequência cardíaca (FC) e pressão arterial média sistêmica foram relatados em diretrizes anteriores.2020. McEwan A. In: Coté CJ, Lerman J, Todres D, editors. Anesthesia techniques for cardiac surgical procedures. A practice of anesthesia for infants and children. 4th ed. Philadelphia: Saunders Elsevier; 2009. p. 331-59.,2121. Falkner B, Daniels SR. Summary of the fourth report on the diagnosis evaluation, and treatment of high blood pressure in children and adolescents. Hypertension. 2004;44:387-8.
Desfechos primários e secundários
O desfecho primário foi o desenvolvimento de SBDC no prazo de 30 dias da cirurgia, o que é uma evolução pós-operatória adversa. Os desfechos secundários incluíram o desenvolvimento de outros resultados adversos dentro de 30 dias da cirurgia, a saber: (1) duração da ventilação mecânica por mais de 72 h no pós-operatório; (2) permanência em unidade de terapia intensiva por mais de sete dias; (3) mortalidade durante o período pós-operatório de 30 dias e (4) desenvolvimento de outras complicações, como déficit neurológico, pneumonia, insuficiência renal, arritmias ventriculares e atriais, bloqueio atrioventricular total.
Conduta anestésica intraoperatória
Os protocolos de conduta para manejo de anestesia no pré-operatório, estratégia cirúrgica no intraoperatório e tratamento intensivo pediátrico foram explicados em detalhes previamente.2020. McEwan A. In: Coté CJ, Lerman J, Todres D, editors. Anesthesia techniques for cardiac surgical procedures. A practice of anesthesia for infants and children. 4th ed. Philadelphia: Saunders Elsevier; 2009. p. 331-59. O monitoramento anestésico padrão inclui: eletrocardiograma (5 derivações), oxímetro de pulso, sonda de temperatura retal, dióxido de carbono expiratório, cateter arterial e cateter venoso central. O uso de ecocardiografia transesofágica foi apenas ocasional no período intraoperatório. No fim da CEC, as pressões sistólica e diastólica do VD foram medidas por meio de um cateter arterial de tamanho adequado inserido no ventrículo direito. O cateter foi removido durante o fechamento do esterno. A pressão média do VD foi medida no fim da CEC. Ecocardiografia transesofágica ou transtorácica foi feita nas crianças com instabilidade hemodinâmica internadas em UTI; contudo, a avaliação ecocardiográfica não estava disponível durante a operação. Durante a cirurgia, anestesia geral foi induzida com midazolam (200 μg kg−1), sulfato de fentanil (25 μg kg−1) e brometo de pancurônio (0,1 mg kg−1). Os pacientes receberam doses repetidas de fentanil (5 μg kg−1) e midazolam (50 μg kg−1) a cada meia hora durante a cirurgia e anestesia inalatória com concentração alveolar mínima (CAM) de sevoflurano (1,0-2,0) também foi administrada, a depender da PAM sistêmica. Os recém-nascidos e lactentes foram entubados com sondas endotraqueais sem balão e a ventilação nos períodos intra e pós-operatório foi mantida com ventilação controlada por pressão ou volume. A profilaxia antibiótica no perioperatório incluiu cefazolina. Metilprednisolona foi administrada em todos os pacientes por via intravenosa, em duas doses igualmente divididas de 10 mg kg−1 cada, antes do início da CEC.
Protocolo de conduta para circulação extracorpórea
O circuito de CEC incluiu uma bomba de roletes, um oxigenador de membrana descartável e um filtro arterial. A CEC foi estabelecida com o uso de uma cânula arterial e cânulas venosas bicaval ou única de duas fases. Refrigeração e reaquecimento foram feitos com um permutador de calor. A solução preparatória consistiu em solução cristaloide isotônica de cloreto de sódio e manitol (3 mL kg−1). Concentrados de hemácias foram usados para obter um valor de hematócritos de 25% antes de iniciar a CEC. Heparinização foi feita com sulfato de heparina. Durante a CEC, um índice de perfusão de 2,4-2,6 L min−1 m−1 foi usado. Hipotermia moderada foi feita a 28 °C. Após o pinçamento, cardioplegia sanguínea com adição de cloreto de potássio, bicarbonato de sódio e sulfato de magnésio foi administrada em dose de 30 mL kg−1. Cardioplegia sanguínea anterógrada, intermitente e fria a 4 °C foi usada para proteger o miocárdio. Heparina foi neutralizada com sulfato de protamina em uma proporção de 1:1,5. Administração intravenosa de vasodilatadores e inotrópicos foi usada, caso necessário, para desmamar os pacientes da CEC. A substituição do volume foi feita com plasma fresco congelado ou albumina humana a 5%.
Tratamento nos períodos perioperatório e pós-operatório
Os parâmetros avaliados durante a cirurgia e em 24 h de pós-operatório incluem: dados demográficos, CEC, tempo de pinçamento aórtico, FC, PAM sistêmica, pressão média do VD, pressão venosa central (PVC), saturação de oxigênio no sangue arterial, débito de urina, balanço de líquidos, agentes inotrópicos e doses. Os parâmetros foram registrados a cada 30 min durante todo o procedimento operatório e a cada 30 min em unidade de terapia intensiva após a operação. Os desfechos adversos relacionados aos parâmetros no pós-operatório, incluindo tempo de ventilação mecânica, permanência em terapia intensiva (UTI) e tempo de internação e mortalidade em 30 dias, foram registrados. Ventilação mecânica prolongada é descrita como uma ventilação mecânica (VM) ≥ 72 h após a cirurgia.2222. Shi S, Zhao Z, Liu X, et al. Perioperative risk factors for prolonged mechanical ventilation following cardiac surgery in neonates and young infants. Chest. 2008;134:768-74. Permanência prolongada em UTI > 7 dias é considerada como um evento adverso.2323. Pagowska-Klimek I, Pychynska-Pokorska M, Krajewski W, et al. Predictors of long intensive care unit stay following cardiac surgery in children. Eur J Cardiothorac Surg. 2011;40: 179-84.Os pacientes foram avaliados para eventos adversos no pós-operatório a cada 12 h pela equipe de pesquisa, incluindo um médico e um residente.
Crise de HP no pós-operatório foi definida como um aumento da PAp sistólica no nível ou maior do que a PAM sistêmica, acompanhada por uma queda da PAM sistêmica, queda da saturação de oxigênio no sangue arterial e/ou venoso. A definição também associa à hipoxemia desenvolvimento de acidose e/ou hipovolemia metabólica. Em todas as nossas crianças, PAp sistólica e PAps média e diastólica correlacionadas1717. Koestenberger M, Nagel B, Avian A, et al. Systolic right ventricular function in children and young adults with pulmonary artery hypertension secondary to congenital heart disease and tetralogy of Fallot: tricuspid annular plane systolic excursion (TAPSE) and magnetic resonance imaging data. Congenit Heart Dis. 2012;7:250-8.foram calculadas com o uso de cardiografia com Doppler em UTI, como descrito na seção "Pacientes". A detecção de HP no pós-operatório foi baseada em sinais clínicos e estudos ecocardiográficos em UTI.1616. Toyono M, Harada K, Tamura M, et al. Paradoxical relationship between B-type natriuretic peptide and pulmonary vascular resistance in patients with ventricular septal defect and concomitant severe pulmonary hypertension. Pediatr Cardiol. 2008;29:65-9.,1717. Koestenberger M, Nagel B, Avian A, et al. Systolic right ventricular function in children and young adults with pulmonary artery hypertension secondary to congenital heart disease and tetralogy of Fallot: tricuspid annular plane systolic excursion (TAPSE) and magnetic resonance imaging data. Congenit Heart Dis. 2012;7:250-8. As medidas de tratamento importantes para evitar um aumento de PAps nos períodos intra- e pós-operatório em UTI incluem: (1) assegurar a oxigenação com FiO2 de 0,6-1,0; (2) fornecer hiperventilação moderada (para manter o nível de PaCO2 entre 30 e 35 mm Hg); (3) evitar o desenvolvimento de acidose metabólica (manter o pH acima de 7,4); (4) aplicar manobra de recrutamento para evitar incompatibilidade de ventilação/perfusão; (5) fornecer ventilação com baixo volume corrente para evitar a pressão excessiva dos alvéolos (para manter o volume corrente entre 6 e 8 mL kg−1 de peso corporal ideal); (6) providenciar o controle da temperatura para manter uma temperatura corporal de 36-37 °C no fim da CEC e (7) fornecer terapia de líquidos e volume "alvodirecionada"e monitoramento eficaz dos parâmetros hemodinâmicos necessários, incluindo FC, PAM sistêmica, pressão do VD, pressão venosa central (PVC), saturação de oxigênio, débito urinário e balanço de líquidos.2424. Lindberg L, Olsson AK, Jögi P, et al. How common is severe pulmonary hypertension after pediatric cardiac surgery? J Thorac Cardiovasc Surg. 2002;123:1155-63.,2525. Bando K, Turrentine MW, Sharp TG, et al. Pulmonary hypertension after operations for congenital heart disease: analysis of risk factors and management. Thorac Cardiovasc Surg. 1996;112:1600-7.
As crianças com risco de desenvolver HP ou com sinais de HP no pós-operatório foram sedadas, receberam suporte ventilatório mecânico e, geralmente, receberam suporte inotrópico (dobutamina e/ou dopamina, inotrópicos adicionais de adrenalina e/ou noradrenalina). Nitroglicerina intradovenosa em dose de 0,5-3 μg kg−1 min−1 foi administrada aos pacientes com acompanhamento adequado dos parâmetros hemodinâmicos. Esses agentes são administrados através de um cateter venoso central na tentativa de manter a PAps inferior a 40% da PAM sistêmica. A administração de nitroglicerina é recomendada para vasodilatação intravenosa. Como o efeito dessa medicação não é limitado à circulação pulmonar e, portanto, também induz vasodilatação sistêmica, sua administração muitas vezes provoca uma queda considerável da PAM sistêmica e envolve o risco de a pressão de perfusão ventricular direita cair abaixo do limite crítico.1616. Toyono M, Harada K, Tamura M, et al. Paradoxical relationship between B-type natriuretic peptide and pulmonary vascular resistance in patients with ventricular septal defect and concomitant severe pulmonary hypertension. Pediatr Cardiol. 2008;29:65-9.,2424. Lindberg L, Olsson AK, Jögi P, et al. How common is severe pulmonary hypertension after pediatric cardiac surgery? J Thorac Cardiovasc Surg. 2002;123:1155-63.,2525. Bando K, Turrentine MW, Sharp TG, et al. Pulmonary hypertension after operations for congenital heart disease: analysis of risk factors and management. Thorac Cardiovasc Surg. 1996;112:1600-7. Na HP agudamente descompensada, óxido nítrico, epoprostenol inalatório ou intravenoso, iloprost e suporte inotrópico são os agentes mais úteis.1818. Landzberg MJ. Congenital heart disease associated pulmonary arterial hypertension. Clin Chest Med. 2007;28:243-53. Contudo, em nosso estudo, o uso rotineiro desses agentes não estava disponível.
Os eventos relacionados à HP foram tratados com hiperventilação manual com oxigênio a 100% e uso intravenoso de opiáceos, fentanil em dose de 5-10 μg kg−1. Nos pacientes com HP, a ventilação mecânica foi mantida até os estudos ecocardiográficos mostrarem valores bem controlados de PAps, bem como melhoria do estado clínico, o que indica que a função miocárdica havia se recuperado. Após a extubação, e quando já não havia necessidade de monitoramento invasivo ou drogas vasoativas, a criança foi transferida para a enfermaria.1616. Toyono M, Harada K, Tamura M, et al. Paradoxical relationship between B-type natriuretic peptide and pulmonary vascular resistance in patients with ventricular septal defect and concomitant severe pulmonary hypertension. Pediatr Cardiol. 2008;29:65-9.,2424. Lindberg L, Olsson AK, Jögi P, et al. How common is severe pulmonary hypertension after pediatric cardiac surgery? J Thorac Cardiovasc Surg. 2002;123:1155-63.,2525. Bando K, Turrentine MW, Sharp TG, et al. Pulmonary hypertension after operations for congenital heart disease: analysis of risk factors and management. Thorac Cardiovasc Surg. 1996;112:1600-7.
Mensurações no perioperatório
Os níveis plasmáticos de PNC e gasometria arterial foram avaliados no pré-operatório, 12, 24 e 48 h de pós-operatório, a partir de amostras de sangue de um cateter arterial, que foi inserido no início da cirurgia, antes da indução anestésica. As equipes médicas e cirúrgicas envolvidas no manejo dos pacientes do estudo desconheciam os valores plasmáticos de PNC. Os níveis plasmáticos de PNC foram medidos com o uso de um imunoensaio de fluorescência comercialmente disponível (Triage, Beckman Coulter, Inc., San Diego, California, EUA). A variação mensurável de PNC nesse dispositivo vai de 5 e 5.000 pg mL−1.
Análise estatística
As análises estatísticas foram feitas com o programa SPSS 17.0.1 para Windows (SPSS Software, Chicago, IL, EUA). No estudo conduzido por Hsu et al., uma amostra de 32 pacientes, com 16 em cada grupo com ou sem SBDC, foi necessária para determinar uma diferença de permanência prolongada em unidade de terapia intensiva de um dia (desvio padrão = 1), com o teste de significância bicaudal, um poder (1 - ß) de 80% e um erro α = 0,05.1111. Hsu JH, Oishi PE, Keller RL, et al. Perioperative B-type natriuretic peptide levels predict outcome after bidirectional cavopulmonary anastamosis and total cavopulmonary connection. J Thorac Cardiovasc Surg. 2008;135:746-53. Todas as variáveis foram testadas para a distribuição normal com o teste de Kolmogorov-Smirnov. As diferenças das variáveis categóricas foram analisadas com o teste do qui-quadrado. As diferenças das variáveis contínuas que não são normalmente distribuídas foram analisadas com o teste de Mann-Whitney. As alterações dos níveis plasmáticos de PNC foram comparadas com a análise de variância (Anova) de medidas repetidas. A utilidade do PNC no pré-operatório como um indicador prognóstico do resultado no pós-operatório foi avaliada com o uso das curvas características de operação do receptor (ROC) e as áreas sob as curvas (ASC), bem como a sensibilidade e especificidade, foram calculadas. As diferenças com um valor-p inferior a 0,05 foram consideradas estatisticamente significantes.
Resultados
Dados dos pacientes
Foram incluídos no grupo de estudo 51 pacientes. Idade, peso, gênero e os tipos de lesões cardíacas estão apresentados na tabela 1. A média de idade do grupo de estudo foi de 1,10 ano (variação de 0,3-3,0). O peso médio foi de 7,00 kg (variação 4,00-26,00). Nesse grupo, havia 23 pacientes (45,1%) do sexo masculino e 28 (54,9%) do feminino. Em todo o grupo havia cinco (9,8%) pacientes com DSV isolado, dois (3,9%) com DSV e CATVP, 13 (25,5%) com DSV e CAPVP (com/sem ASD), 15 (29,4%) com DSV e ASD e 16 (31,4%) com DSAV. Seis apresentaram trissomia 21. Em todo o grupo, 37 (72,5%) pacientes apresentaram um ou mais dos sinais de HF, incluindo déficit de crescimento, dificuldade respiratória ou hepatomegalia, e todos tomavam um ou mais dos seguintes medicamentos: digitalis, diuréticos e inibidor da enzima de conversão da angiotensina.
Distribuição das características basais dos pacientes após a determinação do valor de corte de PNC no pré-operatório pela curva característica de operação do receptor (ROC) para SBDC
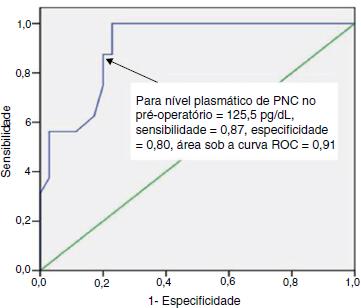
A distribuição das características basais dos pacientes após se determinarem os valores de corte de PNC no préoperatório pela análise da curva característica de operação do receptor (ROC) para SBDC é apresentada na tabela 1. Com o uso de um corte no valor de 125,5 pg mL−1 para PNC no pré-operatório descobriu-se a maior sensibilidade de 88,9% e especificidade de 96,9% na previsão de SBDC em pacientes com HP e uma área sob a curva (ASC) de 91% (fig. 1). Essa constatação mostra que 91% dos pacientes com um nível plasmático de PNC acima de 125,5 pg mL−1 no pré-operatório têm um risco muito elevado de desenvolver SBDC. Os níveis de PNC nos períodos perioperatórios de ambos os grupos são apresentados na tabela 2. Houve diferenças significantes na comparação dos níveis plasmáticos de PNC dos pacientes com ou sem SBDC nos tempos mensurados, (p = 0,0001).
Comparação das alterações nos níveis plasmáticos de PNC nos períodos pré-operatório e pós-operatório
Curva característica de operação do receptor (ROC) para valores plasmáticos de PNC no pré-operatório. Um corte no valor de 125,5 pg mL−1 tem uma sensibilidade de 88,9%, especificidade de 96,9% e área sob a curva (ASC) de 91% para prever a síndrome de baixo débito cardíaco (SBDC).
Cinco crianças com HP foram a óbito dentro de 30 dias após a operação (n = 5/51, 9,8%). Dois desses óbitos ocorreram dentro de dois dias após a correção. As duas crianças, uma menina de 30 meses, 11 kg, com história de síndrome de Down e DSAV, e um menino de 14 meses, 9 kg, com DSV e CATVP, apresentaram aumento da pressão média do VD e desvio grave da direita para a esquerda com saturação transcutânea de oxigênio (45-84%) durante a cirurgia. No fim da correção, ambas as crianças precisaram de suporte inotrópico de dopamina, dobutamina, adrenalina e noradrenalina, além de terapia vasodilatadora com iloprost e nitroglicerina; contudo, a parada cardíaca foi inevitável dentro de 36-48 h após a cirurgia. Em ambos os casos, HP e insuficiência tricúspide foram observadas por estudos ecocardiográficos feitos dentro de 12 h após a cirurgia. O terceiro paciente era um menino de 12 meses, 8 kg, com diagnóstico de DSV e CAPVP, que sobreviveu cinco dias em UTI antes de sofrer parada cardíaca secundária a uma crise de HP diagnosticada com achados clínicos. Os outros dois pacientes apresentaram tanto DSA quanto DSV, bem como HP grave antes da cirurgia. Um deles era um menino de quatro meses, 5 kg, e o outro uma menina de três meses, 4 kg, com diagnóstico de síndrome de Down. O paciente do sexo masculino sobreviveu por apenas três dias em UTI antes de sofrer parada cardíaca secundária à crise de HP e a paciente apresentou sintomas de SBDC dentro de 12 h após a cirurgia e precisou de diálise peritoneal e suporte inotrópico. A despeito de terapia adequada, a paciente sobreviveu 13 dias em UTI antes de sofrer parada cardíaca secundária à SBDC. Óxido nítrico inalatório foi fornecido a apenas seis pacientes com sinais de HP grave em UTI.
Desfechos
Não houve óbito no grupo SBDC (-) que apresentou melhorresultado no período pós-operatório de 30 dias, enquantono grupo SBDC (+) cinco dos 16 pacientes (31,25%) foram aóbito no pós-operatório imediato. Quatro pacientes forama a óbito no período de sete dias e um sobreviveu por 12 dias no pós-operatório. Os dados da evolução dos pacientes, bem como da mortalidade em 30 dias, são apresentados na tabela 3.
As diferenças entre as PAMs sistêmicas, VDs e VCs durante e 12 h após a cirurgia são apresentadas na tabela 4. As PAMs sistêmicas não apresentaram diferenças significantes entre os grupos SBDC (–) e SBDC (+) no fim da CEC. Contudo, nesse período, os pacientes com SBDC apresentaram pressões mais elevadas do VD (43,50 ± 5,96 mm Hg), em comparação com os outros pacientes que apresentam um valor de 38,89 ± 5,03 mm Hg (p = 0,005). As comparações de saturação de oxigênio e PVC não apresentaram diferenças significantes entre os grupos (98,04 ± 2,56% vs. 96,01 ± 9,24, p = 0,191, e 10,26 ± 2,15 mm Hg vs. 10,19 ± 2,29 mm Hg, p = 0,385, respectivamente). Em 12 h de pós-operatório, enquanto não houve diferença entre os pacientes SBDC (–) e SBDC (+) em relação às PAMs sistêmicas, os pacientes com SBDC apresentaram PVC mais alta e saturação de oxigênio arterial mais baixa em comparação com os pacientes sem SBDC (95,75 ± 3,80% vs. 86,06 ± 7,57%, p = 0,0001, e 10,14 ± 2,43 mm Hg vs. 16,19 ± 3,26 mm Hg, p = 0,0001, respectivamente) (tabela 4).
Divisão das características dos pacientes nos períodos intraoperatório e pós-operatório, de acordo com a síndrome de baixo débito cardíaco
Uma boa correlação foi descoberta entre o nível plasmático de PNC no pré-operatório e o tempo de ventilação mecânica (r = 0,67, p = 0,0001); no entanto, correlações fracas estavam presentes entre o nível plasmático de PNC no pré-operatório e o tempo de pinçamento aórtico (rho = 0,431, p = 0,002), permanência em UTI (r = 0,42, p = 0,002) e mortalidade (r = 0,47, p = 0,001).
Discussão
Os principais achados deste estudo são: (1) em comparação com os níveis plasmáticos de PNC no pré-operatório, os valores no pós-operatório apresentaram aumento significante nos tempos mensurados de 12, 24 e 48 h após a cirurgia em pacientes com ou sem desenvolvimento de SBDC no período pós-operatório; (2) nos pacientes com HP submetidos à cirurgia cardíaca congênita, 91% dos pacientes com níveis plasmáticos de PNC no pré-operatória acima de 125,5 pg mL−1têm alto risco de desenvolver SBDC, o que é um fator de risco importante para determinar precocemente o resultado em 30 dias de pós-operatório; (3) o nível plasmático de PNC no pré-operatório prevê com precisão a SBDC no pós-operatório em crianças com HP e esses achados não foram relatados anteriormente em estudos que investigaram hipertensão pulmonar em crianças;1616. Toyono M, Harada K, Tamura M, et al. Paradoxical relationship between B-type natriuretic peptide and pulmonary vascular resistance in patients with ventricular septal defect and concomitant severe pulmonary hypertension. Pediatr Cardiol. 2008;29:65-9.,2424. Lindberg L, Olsson AK, Jögi P, et al. How common is severe pulmonary hypertension after pediatric cardiac surgery? J Thorac Cardiovasc Surg. 2002;123:1155-63.–2727. Malik S, Cleves MA, Zhao W, et al. National Birth Defects Prevention Study Association between congenital heart defects and small for gestational age. Pediatrics. 2007;119:e976-82. (4) os desfechos secundários avaliados no período pós-operatório imediato mostraram tempos prolongados de ventilação mecânica e permanência em UTI para os pacientes com SBDC em comparação com os pacientes sem SBDC (p = 0,0001, p = 0,008, respectivamente).
No estudo de Hoffmann et al., 238 pacientes foram divididos em três grupos – placebo, milrinona em dose baixa e milrinona em dose alta – e as incidências de SBDC foram 25,9%, 17,5% e 11,7%, respectivamente, nas primeiras 36 h após cirurgias de cardiopatias congênitas. Os pacientes com SBDC apresentaram tempos significativamente mais longos de ventilação mecânica (3,1 vs. 1,4 dias, p = 0,001) e internação hospitalar (11,3 vs. 8,9 dias, p = 0,016) em comparação com os pacientes sem SBDC.1313. Hoffman TM, Wernovsky G, Atz AM, et al. Efficacy and safety of milrinone in preventing low cardiac output syndrome in infants and children after corrective surgery for congenital heart disease. Circulation. 2003;107:996-1002.
Em crianças com cardiopatias congênitas que se apresentam com HP relevante e desvio predominante da esquerda para a direita, uma razão de resistência pulmonar:sistêmica ≤ 2/3 é usada como um limiar associado a melhores desfechos cirúrgicos.1818. Landzberg MJ. Congenital heart disease associated pulmonary arterial hypertension. Clin Chest Med. 2007;28:243-53. Nessas crianças, as causas dos sinais de desenvolvimento de insuficiência do VD podem estar relacionadas a: (1) diferentes estados do volume inicial; (2) volumes diastólicos finais variados na fase basal ou (3) graus variados de carga e lesão isquêmicas. Para tratamento desses achados fisiopatológicos, um desafio inicial com líquidos que usem soro fisiológico normal seguido de diurese é necessário.1717. Koestenberger M, Nagel B, Avian A, et al. Systolic right ventricular function in children and young adults with pulmonary artery hypertension secondary to congenital heart disease and tetralogy of Fallot: tricuspid annular plane systolic excursion (TAPSE) and magnetic resonance imaging data. Congenit Heart Dis. 2012;7:250-8.,2424. Lindberg L, Olsson AK, Jögi P, et al. How common is severe pulmonary hypertension after pediatric cardiac surgery? J Thorac Cardiovasc Surg. 2002;123:1155-63. Em estudo conduzido por Bando et al., crianças com DSAV, truncus arteriosus, CATVP, transposição das grandes artérias, síndrome de hipoplasia do coração esquerdo e DSV foram determinadas como de alto risco para o desenvolvimento de eventos de hipertensão pulmonar no pós-operatório.2525. Bando K, Turrentine MW, Sharp TG, et al. Pulmonary hypertension after operations for congenital heart disease: analysis of risk factors and management. Thorac Cardiovasc Surg. 1996;112:1600-7. Nesse estudo, 880 pacientes com alto risco de desenvolver eventos pulmonares no pós-operatório foram avaliados e o número de eventos de hipertensão pulmonar foi registrado e a taxa de mortalidade nessa população de pacientes foi de 75 (8,5%). Os dados mostram que a taxa de mortalidade em crianças com diagnóstico de HP submetidas à cirurgia de reparação de cardiopatia congênita é significativamente maior do que em pacientes sem HP. Além disso, o número de óbitos prematuros associados a eventos de HP foi de 31 (22,5%) em 138 pacientes. Em relação aos pacientes com crise grave de HP, o estudo de Bando et al. relatou uma taxa de mortalidade de 35,5% (n = 11/31) de 1990 a 1994, enquanto estudos recentes também relatam que uma única complicação junto com a simples correção da cardiopatia congênita está associada a uma taxa de mortalidade de até 9,0%.2626. Pasquali SK, Li JS, Burstein DS, et al. Association of center volume with mortality and complications in pediatric heart surgery. Pediatrics. 2012;129:e370-6. Lindberg et al. relataram uma taxa de mortalidade de 7,4% (n = 2/27).2424. Lindberg L, Olsson AK, Jögi P, et al. How common is severe pulmonary hypertension after pediatric cardiac surgery? J Thorac Cardiovasc Surg. 2002;123:1155-63. A taxa de mortalidade em nosso grupo de estudo foi de 9,8% e esse desfecho primário é compatível com relatos anteriores.2424. Lindberg L, Olsson AK, Jögi P, et al. How common is severe pulmonary hypertension after pediatric cardiac surgery? J Thorac Cardiovasc Surg. 2002;123:1155-63.,2727. Malik S, Cleves MA, Zhao W, et al. National Birth Defects Prevention Study Association between congenital heart defects and small for gestational age. Pediatrics. 2007;119:e976-82.
Nossos pacientes deram entrada tardiamente na clínica, com estados de saúde complicados em comparação com a série de casos relatados na literatura. Em nosso grupo de estudo, a mediana de idade de 12 meses foi maior do que a mediana (4,2-8,6 meses) dos estudos relatados, o que mostrou que o diagnóstico e o tratamento precoces nem sempre foram possíveis em nosso grupo de pacientes.2424. Lindberg L, Olsson AK, Jögi P, et al. How common is severe pulmonary hypertension after pediatric cardiac surgery? J Thorac Cardiovasc Surg. 2002;123:1155-63.,2727. Malik S, Cleves MA, Zhao W, et al. National Birth Defects Prevention Study Association between congenital heart defects and small for gestational age. Pediatrics. 2007;119:e976-82. Em nosso estudo, a média de peso corporal dos pacientes com SBDC foi menor e a incidência de história de parto prematuro nesse grupo foi de nove em 16 pacientes (56,3%), enquanto a média de peso corporal dos pacientes sem SBDC foi maior, com incidência de história de parto prematuro de quatro em 35 (11,4%) (tabela 2). Nossos resultados estão de acordo com os dados da literatura quando relatam que o déficit de crescimento é um fator significante em cardiopatias congênitas com HP.33. Law YM, Keller BB, Feingold BM, et al. Usefulness of plasma B-type natriuretic peptide to identify ventricular dysfunction in pediatric and adult patients with congenital heart disease. Am J Cardiol. 2005;95:474-8. Notavelmente, os resultados de crianças prematuras com cardiopatias foram significativamente piores do que os de crianças nascidas a termo.2727. Malik S, Cleves MA, Zhao W, et al. National Birth Defects Prevention Study Association between congenital heart defects and small for gestational age. Pediatrics. 2007;119:e976-82.
Um aumento das conexões anômalas TVP e PVP e insuficiência do VD podem ter desempenhado um papel importante na causa da morte de nossos pacientes. Para prevenir uma crise de HP no período pós-operatório imediato, óxido nítrico inalatório, epoprostenol inalatório ou intravenoso, iloprost e suporte inotrópico são os agentes mais úteis e os métodos mais recentes incluem: oxigenação por membrana extracorpórea e monitoramento contínuo da saturação venosa mista (SvO2) via cateter de artéria pulmonar. Não foi possível fazer a cateterização de artéria pulmonar em todos os nossos pacientes e a inclusão dos dados dessas mensurações em nosso estudo, embora nossas observações confirmem que o cateterismo da artéria pulmonar é benéfico para detectar eventos de hipertensão pulmonar no período inicial. Há relatos de que PAp e PVC aumentam gradualmente e que a SvO2 diminui antes da ocorrência de crises graves de hipertensão pulmonar.2424. Lindberg L, Olsson AK, Jögi P, et al. How common is severe pulmonary hypertension after pediatric cardiac surgery? J Thorac Cardiovasc Surg. 2002;123:1155-63.,2525. Bando K, Turrentine MW, Sharp TG, et al. Pulmonary hypertension after operations for congenital heart disease: analysis of risk factors and management. Thorac Cardiovasc Surg. 1996;112:1600-7.,2828. Zhu W-H, Zhu X-K, Shu Q. Postoperative hemodynamics of children with severe pulmonary hypertension caused by congenital heart disease. World J Pediatr. 2006;1:45-8. Hipoxemia, hipercapnia, acidose metabólica, agitação e aspiração traqueal podem aumentar a vasorreatividade pulmonar e, assim, desenca-dear eventos de hipertensão pulmonar no pós-operatório. Para a prevenção desses eventos, hiperventilação moderada, com uma fração inspirada de oxigênio alta, sedação e paralisia foram usadas em nosso estudo. Óxido nítrico inalatório estava disponível em apenas seis pacientes que apresentaram crise grave de HP em UTI.
A decisão por um valor de corte para os níveis de PNC não pode ser estabelecida mesmo para lesões sem complexidade. Em um estudo conduzido por Koch e colaboradores, 65 pacientes foram avaliados como grupo único de pacientes submetidos à cirurgia de cardiopatia cardíaca congênita e, posteriormente, uma divisão em dois grupos foi feita em função da complexidade das lesões cardíacas. A diferença entre os valores de PNC nos períodos pré- e pós-operatório no primeiro dia foi significativamente maior nos pacientes com defeitos cardíacos complexos do que nos pacientes com defeitos mais simples (mediana de 213 pg mL−1 vs. 453 pg mL−1, p = 0,03). Nesse estudo, os níveis de PNC no pós-operatório foram significativamente maiores nos pacientes com corações univentriculares (mediana de 1.300 pg mL−1).1010. Koch A, Kitzsteiner T, Zink S, et al. Impact of cardiac surgery on plasma levels of B-type natriuretic peptide in children with congenital heart disease. Int J Cardiol. 2007;114:339-44. Oosterhof et al. relataram que, em morfologias univentriculares com disfunção ventricular direita, níveis de PNC no pré-operatório superiores a 45 pg mL−1 detectam insuficiência ventricular direita, com sensibilidade de 78% e especificidade de 84%.2929. Oosterhof T, Tulevski II, Vliegen HW, et al. Effects of volume and/or pressure overload secondary to congenital heart disease (tetralogy of fallot or pulmonary stenosis) on right ventricular function using cardiovascular magnetic resonance and B-type natriuretic peptide levels. Am J Cardiol. 2006;97:1051-5. Esses dois estudos, em particular, fornecem dados que indicam a necessidade de uma investigação mais profunda dos níveis plasmáticos de PNC no pré-operatório de crianças com hipertensão pulmonar submetidas à cirurgia de cardiopatia congênita. Nosso estudo fornece dados valiosos que indicam que um nível plasmático de PNC no pré-operatório superior a 125,5 pg mL−1 detecta SBDC é um importante fator de risco prognóstico no período pós-operatório imediato de 30 dias, com sensibilidade de 88,9% e especificidade de 96,9%. SBDC tem sido usada como uma ferramenta para determinar o desfecho após cirurgias de cardiopatias congênitas.1111. Hsu JH, Oishi PE, Keller RL, et al. Perioperative B-type natriuretic peptide levels predict outcome after bidirectional cavopulmonary anastamosis and total cavopulmonary connection. J Thorac Cardiovasc Surg. 2008;135:746-53.,2929. Oosterhof T, Tulevski II, Vliegen HW, et al. Effects of volume and/or pressure overload secondary to congenital heart disease (tetralogy of fallot or pulmonary stenosis) on right ventricular function using cardiovascular magnetic resonance and B-type natriuretic peptide levels. Am J Cardiol. 2006;97:1051-5. Um achado importante é que os pacientes com SBDC submetidos à cirurgia de cardiopatias congênita com CEC apresentaram valores significativamente mais elevados de PNC no pré-operatório. Nossa observação é semelhante à de um estudo recente conduzido por Hsu et al. que relata: (1) SBDC está associada a um mau prognóstico no pós-operatório; (2) SBDC realmente se desenvolve antes de 48 h após a cirurgia; (3) os níveis de PNC no pós-operatório não prevêem SBDC, porém esses valores estão associados à SBDC.1111. Hsu JH, Oishi PE, Keller RL, et al. Perioperative B-type natriuretic peptide levels predict outcome after bidirectional cavopulmonary anastamosis and total cavopulmonary connection. J Thorac Cardiovasc Surg. 2008;135:746-53.Um valor de PNC no pré-operatório ou valores de PNC em 2, 4, 12 ou 24 h de pós-operatório foram relatados como biomarcadores independentes de fatores de risco relacionados ao prognóstico no pós-operatório, como internação em UTI ou ventilação mecânica prolongada.2424. Lindberg L, Olsson AK, Jögi P, et al. How common is severe pulmonary hypertension after pediatric cardiac surgery? J Thorac Cardiovasc Surg. 2002;123:1155-63.,2727. Malik S, Cleves MA, Zhao W, et al. National Birth Defects Prevention Study Association between congenital heart defects and small for gestational age. Pediatrics. 2007;119:e976-82.–3030. Tissières P, da Cruz E, Habre W, et al. Value of brain natriuretic peptide in the perioperative follow-up of children with valvular disease. Intensive Care Med. 2008;34:1109-13.
Uma correlação entre os níveis plasmáticos de PNC e a duração da ventilação mecânica foi demonstrada em estudos anteriores por Hsu e Shih et al.1212. Shih CY, Sapru A, Oishi P, et al. Alterations in plasma B-type natriuretic peptide levels after repair of congenital heart defects: a potential perioperative marker. J Thorac Cardiovasc Surg. 2006;131:632-8.,3131. Hsu JH, Keller RL, Chikovani O, et al. B-type natriuretic peptide levels predict outcome after neonatal cardiac surgery. J Thorac Cardiovasc Surg. 2007;134:939-45. O estudo de Hsu et al. foi principalmente com recém-nascidos submetidos à operação de Norwood ou correção da dupla via de saída de ventrículo e confirma o valioso papel do PNC na previsão de mau prognóstico após cirurgia de cardiopatia congênita com CEC, especialmente no período pós-operatório de 24 h.3131. Hsu JH, Keller RL, Chikovani O, et al. B-type natriuretic peptide levels predict outcome after neonatal cardiac surgery. J Thorac Cardiovasc Surg. 2007;134:939-45. Em estudo recente, Shih et al. relataram que os níveis do peptídeo natriurético tipo-B em 12 horas foram associados à duração da ventilação mecânica e presença de SBDC após a intervenção cirúrgica. Nesse estudo, o valor de corte do nível de peptídeo natriurético tipo-B em 12 h superior a 540 pg mL−1 previu ventilação mecânica por mais de 48 h, com sensibilidade de 88,9% e especificidade de 82,5%.1212. Shih CY, Sapru A, Oishi P, et al. Alterations in plasma B-type natriuretic peptide levels after repair of congenital heart defects: a potential perioperative marker. J Thorac Cardiovasc Surg. 2006;131:632-8. Em nossa população de pacientes, descobrimos uma boa correlação entre o nível plasmático de PNC no préoperatório e o tempo de ventilação mecânica (r = 0,67, p = 0,0001), similar aos achados de Shih et al. Concordamos que o estudo precisa ser conduzido com um grupo maior de pacientes para demonstrar a importância dos valores plasmáticos de PNC em pacientes com diagnóstico de HP submetidos a cirurgias de cardiopatias congênitas.
Existem várias limitações no presente estudo. Uma importante foi a seleção de pacientes para o grupo de estudo. Usamos critérios diagnósticos ecocardiográficos gerais para medir as PAps em vez de cateterismo cardíaco. Contudo, pensamos que todo o grupo de pacientes representa um único grupo, pois avaliamos as PAps sistólicas com PAMs sistêmicas. Nossos pacientes se apresentaram em idade mais avançada, após um período de tratamento médico inadequado, que causou a deterioração do estado clínico. Em nosso grupo de estudo, 11 pacientes (11/51, 21,6%) tinham história de nascimento prematuro e há relato de que os bebês prematuros apresentam maus prognósticos no pós-operatório.33. Law YM, Keller BB, Feingold BM, et al. Usefulness of plasma B-type natriuretic peptide to identify ventricular dysfunction in pediatric and adult patients with congenital heart disease. Am J Cardiol. 2005;95:474-8.,2727. Malik S, Cleves MA, Zhao W, et al. National Birth Defects Prevention Study Association between congenital heart defects and small for gestational age. Pediatrics. 2007;119:e976-82. Não tínhamos um ecocardiógrafo transtorácico em nossa clínica e o cateterismo da artéria pulmonar não foi feito nessas crianças mais enfermas. Durante a conclusão deste estudo, óxido nítrico inalatório não estava disponível para todos os pacientes e outros agentes mais recentes, como epoprostenol e iloprost inalatório ou intravenoso, não foram usados para evitar uma crise de HP durante ou após a cirurgia.
Em conclusão, o nível plasmático de PNC no préoperatório prediz com precisão a SBDC no pós-operatório. Esse é um importante fator de risco prognóstico imediato no período pós-operatório de 30 dias e 91% dos pacientes com níveis plasmáticos de PNC acima de 125,5 pg mL−1 no pré-operatório têm alto risco de desenvolver SBDC, especialmente crianças submetidas à cirurgia cardíaca congênita com CEC.
-
FinanciamentoEste estudo foi financiado exclusivamente pelo Dr. Kartal Kosuyolu Training and Research Hospital, Kartal, Istambul, Turquia.
-
AutoriaAyse Baysal contribuiu para a coleta de dados, o projeto do estudo, a estatística e a elaboração de manuscrito. Ahmet Şaşmazel contribuiu para a coleta de dados, o projeto do estudo e a estatística. Ayse Yildirim contribuiu para a coleta de dados ecocardiográficos. Buket Ozyaprak contribuiu para a coleta de dados durante a cirurgia. Narin Gundogus contribuiu com a coleta de dados em unidade de terapia intensiva e Tuncer Kocak contribuiu para o projeto do estudo.
References
-
1Haddad F, Doyle R, Murphy DJ, et al. Right ventricular function in cardiovascular disease, part II: pathophysiology, clinical importance, and management of right ventricular failure. Circulation. 2008;117:1717-31.
-
2Ohuchi H, Takasugi H, Ohashi H, et al. Stratification of pediatric heart failure on the basis of neurohormonal and cardiac autonomic nervous activities in patients with congenital heart disease. Circulation. 2003;108:2368-76.
-
3Law YM, Keller BB, Feingold BM, et al. Usefulness of plasma B-type natriuretic peptide to identify ventricular dysfunction in pediatric and adult patients with congenital heart disease. Am J Cardiol. 2005;95:474-8.
-
4Westerlind A, Wåhlander H, Lindstedt G, et al. Clinical signs of heart failure are associated with increased levels of natriuretic peptide types B and A in children with congenital heart defects or cardiomyopathy. Acta Paediatr. 2004;93:340-5.
-
5Suda K, Matsumura M, Matsumoto M. Clinical implication of plasma natriuretic peptides in children with ventricular septal defect. Pediatr Int. 2003;45:249-54.
-
6Paul MA, Backer CL, Binns HJ, et al. B-type natriuretic peptide and heart failure in patients with ventricular septal defect: a pilot study. Pediatr Cardiol. 2009;30:1094-7.
-
7Mir TS, Falkenberg J, Friedrich B, et al. Levels of brain natriuretic peptide in children with right ventricular overload due to congenital heart disease. Cardiol Young. 2005;15:396-401.
-
8Mir TS, Haun C, Lilje C, et al. Utility of N-terminal brain natriuretic peptide plasma concentrations in comparison to lactate and troponin in children with congenital heart disease following open-heart surgery. Pediatr Cardiol. 2006;27:209-16.
-
9Gessler P, Knirsch W, Schmitt B, et al. Prognostic value of plasma N-terminal pro-brain natriuretic peptide in children with congenital heart defects and open-heart surgery. J Pediatr. 2006;148:372-6.
-
10Koch A, Kitzsteiner T, Zink S, et al. Impact of cardiac surgery on plasma levels of B-type natriuretic peptide in children with congenital heart disease. Int J Cardiol. 2007;114:339-44.
-
11Hsu JH, Oishi PE, Keller RL, et al. Perioperative B-type natriuretic peptide levels predict outcome after bidirectional cavopulmonary anastamosis and total cavopulmonary connection. J Thorac Cardiovasc Surg. 2008;135:746-53.
-
12Shih CY, Sapru A, Oishi P, et al. Alterations in plasma B-type natriuretic peptide levels after repair of congenital heart defects: a potential perioperative marker. J Thorac Cardiovasc Surg. 2006;131:632-8.
-
13Hoffman TM, Wernovsky G, Atz AM, et al. Efficacy and safety of milrinone in preventing low cardiac output syndrome in infants and children after corrective surgery for congenital heart disease. Circulation. 2003;107:996-1002.
-
14Vogt W, Läer S. Prevention for pediatric low cardiac output syndrome: results from the European survey EuLoCOS-Paed. Paediatr Anaesth. 2011;21:1176-84.
-
15Auerbach SR, Richmond ME, Lamour JM, et al. BNP levels predict outcome in pediatric heart failure patients: post hoc analysis of the Pediatric Carvedilol Trial. Circ Heart Fail. 2010;3:606-11.
-
16Toyono M, Harada K, Tamura M, et al. Paradoxical relationship between B-type natriuretic peptide and pulmonary vascular resistance in patients with ventricular septal defect and concomitant severe pulmonary hypertension. Pediatr Cardiol. 2008;29:65-9.
-
17Koestenberger M, Nagel B, Avian A, et al. Systolic right ventricular function in children and young adults with pulmonary artery hypertension secondary to congenital heart disease and tetralogy of Fallot: tricuspid annular plane systolic excursion (TAPSE) and magnetic resonance imaging data. Congenit Heart Dis. 2012;7:250-8.
-
18Landzberg MJ. Congenital heart disease associated pulmonary arterial hypertension. Clin Chest Med. 2007;28:243-53.
-
19Cerda J. Oliguria: an earlier and accurate biomarker of acute kidney injury? Kidney Int. 2011;80:699-701.
-
20McEwan A. In: Coté CJ, Lerman J, Todres D, editors. Anesthesia techniques for cardiac surgical procedures. A practice of anesthesia for infants and children. 4th ed. Philadelphia: Saunders Elsevier; 2009. p. 331-59.
-
21Falkner B, Daniels SR. Summary of the fourth report on the diagnosis evaluation, and treatment of high blood pressure in children and adolescents. Hypertension. 2004;44:387-8.
-
22Shi S, Zhao Z, Liu X, et al. Perioperative risk factors for prolonged mechanical ventilation following cardiac surgery in neonates and young infants. Chest. 2008;134:768-74.
-
23Pagowska-Klimek I, Pychynska-Pokorska M, Krajewski W, et al. Predictors of long intensive care unit stay following cardiac surgery in children. Eur J Cardiothorac Surg. 2011;40: 179-84.
-
24Lindberg L, Olsson AK, Jögi P, et al. How common is severe pulmonary hypertension after pediatric cardiac surgery? J Thorac Cardiovasc Surg. 2002;123:1155-63.
-
25Bando K, Turrentine MW, Sharp TG, et al. Pulmonary hypertension after operations for congenital heart disease: analysis of risk factors and management. Thorac Cardiovasc Surg. 1996;112:1600-7.
-
26Pasquali SK, Li JS, Burstein DS, et al. Association of center volume with mortality and complications in pediatric heart surgery. Pediatrics. 2012;129:e370-6.
-
27Malik S, Cleves MA, Zhao W, et al. National Birth Defects Prevention Study Association between congenital heart defects and small for gestational age. Pediatrics. 2007;119:e976-82.
-
28Zhu W-H, Zhu X-K, Shu Q. Postoperative hemodynamics of children with severe pulmonary hypertension caused by congenital heart disease. World J Pediatr. 2006;1:45-8.
-
29Oosterhof T, Tulevski II, Vliegen HW, et al. Effects of volume and/or pressure overload secondary to congenital heart disease (tetralogy of fallot or pulmonary stenosis) on right ventricular function using cardiovascular magnetic resonance and B-type natriuretic peptide levels. Am J Cardiol. 2006;97:1051-5.
-
30Tissières P, da Cruz E, Habre W, et al. Value of brain natriuretic peptide in the perioperative follow-up of children with valvular disease. Intensive Care Med. 2008;34:1109-13.
-
31Hsu JH, Keller RL, Chikovani O, et al. B-type natriuretic peptide levels predict outcome after neonatal cardiac surgery. J Thorac Cardiovasc Surg. 2007;134:939-45.
Datas de Publicação
-
Publicação nesta coleção
Sep-Oct 2014
Histórico
-
Recebido
26 Ago 2013 -
Aceito
17 Out 2013