Resumos
Através da amniocentese em 90 gestações de alto risco, foi feito estudo crítico da citologia do líquido amniótico pelo Sulfato de Azul do Nilo em comparação com a creatinina e o Rx simples de abdomen e sua relação com a idade do RN (calculados pelas tabelas de Lubchenco e Capurro). Concluiu-se que a técnica do Sulfato de Azul do Nilo apresenta real valor, nas nossas condições econômicas, com menor percentagem de falhas com os demais métodos, sendo melhor para a avaliação de maturidade fetal o emprego simultâneo de todos os métodos, aliados à clínica.
Maturidade fetal; Amniocentese; Assistência pré-natal; Risco gravídico
Through amniocentesis carried ou in 90 high-risk pregnant women a critical study of the citology of the amniotic fluid by the Nile-blue sulphate method was undertaken. The results were compared with those obtained by using creatinine and simple X-rays of the abdomen as well as their relationship with the foetal-age of the babies when born (calculated by the Lubchenco and Capurro tables). The Nile-blue sulphate method is of considerable value due to conditions in Brazil and presents a lower percentage of errors than others. For evaluation of foetal maturity, however, one should use all methods simultaneously, along with clinical assessment.
Foetal maturity; Amniocentesis; Pregnancy; Pre-natal care
ARTIGO ORIGINAL
Estudo crítico da avaliação da maturidade fetal pela citologia do líquido âmnico: comparação com outros métodos
A critical study of the evaluation of foetal maturity through citology of the amniotic fluid. Comparison with other methods
Pedro Augusto Marcondes de Almeida; Ana Maria Bertini de Oliveira; Antonio Guilherme Moreira Porto; Domingos Delascio; Neusa Maria Vigorito; Prescilla Chow; Abes Mohamed Amed; Ari Dalla; Krikor Boyacyan; Adelheid Baugartner
Da Disciplina de Obstetrícia do Departamento de Tocoginecologia da Escola Paulista de Medicina
RESUMO
Através da amniocentese em 90 gestações de alto risco, foi feito estudo crítico da citologia do líquido amniótico pelo Sulfato de Azul do Nilo em comparação com a creatinina e o Rx simples de abdomen e sua relação com a idade do RN (calculados pelas tabelas de Lubchenco e Capurro). Concluiu-se que a técnica do Sulfato de Azul do Nilo apresenta real valor, nas nossas condições econômicas, com menor percentagem de falhas com os demais métodos, sendo melhor para a avaliação de maturidade fetal o emprego simultâneo de todos os métodos, aliados à clínica.
Unitermos: Maturidade fetal, avaliação. Amniocentese. Assistência pré-natal. Risco gravídico.
SUMMARY
Through amniocentesis carried ou in 90 high-risk pregnant women a critical study of the citology of the amniotic fluid by the Nile-blue sulphate method was undertaken. The results were compared with those obtained by using creatinine and simple X-rays of the abdomen as well as their relationship with the foetal-age of the babies when born (calculated by the Lubchenco and Capurro tables). The Nile-blue sulphate method is of considerable value due to conditions in Brazil and presents a lower percentage of errors than others. For evaluation of foetal maturity, however, one should use all methods simultaneously, along with clinical assessment.
Uniterms: Foetal maturity. Amniocentesis. Pregnancy, risk. Pre-natal care.
INTRODUÇÃO
O obstetra, com freqüência, necessita saber, o mais exatamente possível a duração da gestação e concomitante maturidade fetal. Com o desenvolvimento do conceito de gestação de alto risco, e do conhecimento de inúmeros fatores que determinam este tipo de gravidez, um dos problemas primordiais constitui a avaliação da maturidade fetal pois, em múltiplas ocasiões é indispensável a sua determinação a mais correta possível, para podermos indicar a antecipação do parto. Não há necessidade de insistirmos sobre os riscos de extraírmos fetos imaturos.
Delascio e Almeida 14 em 1974 estabeleceram um esquema de propedêutica de gestação de alto risco e neste encontramos vários métodos para a avaliação da maturidade fetal. Sem dúvida nenhuma, a avaliação clínica, através de exame obstétrico detalhado é o método inicial e de melhor avaliação.
Os outros métodos propedêuticos são solicitados sempre baseados no exame obstétrico quando existe dúvida efetiva. Assim, na propedêutica bioquímica do líquido âmnico, encontramos, de início, a dosagem de creatinina que é crescente com o evolver da gestação41. Pitkin e Zwirek 32 observaram em 94% das gestações normais o teor de creatinina superior a 2,0 mg% na 37.a semana.
Outros autores 2,5,15, 16,27,33 reconheceram que a concentração de creatinina, produto metabólico fetal, serve como indicador de maturidade fetal e pode ser usada na prática clínica com razoáveis resultados.
Trouchat e col.37 observaram que, em gestantes com isoimunização Rh, toxemia e diabetes, este método foi efetivo em 74% dos casos.
Teoh e col.36, por sua vez, encontraram teores acima de 2,0 mg% relacionados com recém-nascidos imaturos, revelando, portanto, 5% de casos falsos positivos. Jakobovits e col. 22 revelam que níveis de 2,0 mg% ou mais estão freqüentemente relacionados com peso fetal de 3.000 g ou mais.
Ainda na bioquímica do líquido âmnico, vários autores tentaram estabelecer a maturidade fetal através dos teores de ácido úrico e uréia, porém sabe-se que não refletem com exatidão a idade gestacional 4,15,21,33 não podendo ser utilizados isoladamente.
Mandelbaum e col. 28, determinando os níveis de bilirrubina no líquido âmnico, principalmente através de estudo espectrofotométrico a 450 mu de comprimento de onda, afirmam ser útil para valorizar a maturidade fetal, pois, os índices de bilirrubina diminuem gradualmente com o evolver da gestação.
Kittrich23, em 1963, foi um dos primeiros a chamar a atenção para o fato de que a rotura de bolsa amniótica poderia ser detectada pela presença de células originárias do líquido amniótico na vagina, que se coram em alaranjado na presença da solução a 0,1% de Sulfato de Azul do Nilo.
Brosens e Gordon8, em 1966, notaram que a proporção destas células aumenta gradualmente com a evolução da gestação e que o seu número mostra correlação com a maturidade do feto. Outros autores 3,6,12,17,19,34,35,40 confirmam estas observações e desenvolveram métodos que possibilitam a identificação da idade fetal através da quantificação das células orangiófilas no líquido âmnico.
Anderson e Griffiths1, Votta e col. 39 e Caspi e Lederhaendler 11 são unânimes em afirmar que é o método de determinação da maturidade fetal que menos falha, dando mais resultados falso-negativos que falso-positivos, evitando, portanto, prematuridade iatrogênica.
Outros autores 4,15,18,22,31,36 propõem sempre a utilização de vários métodos em conjunto para a avaliação da idade fetal intra-útero, aspecto este com o qual estamos de total acordo.
Assim, Brosens e col.9 sugerem que a fetografia, com injeção intra-amniótica de contraste liposolúvel, associada a contagem de células orangiófilas é um método combinado que pode fornecer bons resultados.
Sem dúvida, existe ainda uma série de métodos para a avaliação da maturidade fetal, assim a identificação dos pontos de ossificação através de radiografia simples; a amniografia ou fetografia; a determinação da relação lecitina-esfingomielina através de teste de Gluck 20 ou teste de Clements e col.13; as dosagens do ácido palmítico no líquido âmnico; a ultrasonogragia (A-Scope ou B-Scope) proposta inicialmente por Ian Donald; a osmolaridade do líquido âmnico; as dosagens de glicose ou de proteína fetal a no mesmo líquido. Todos estes métodos são sem dúvida importantes, porém, alguns são falhos, necessitando de especialistas qualificados para sua avaliação, outros dependem de aparelhagem e de técnica extremamente complicada e ainda inexequível em nosso meio.
Assim, propusemo-nos a estudar, em um grupo de gestantes de alto risco, a determinação da maturidade fetal, através da técnica do Sulfato de Azul do Nilo comparando-a com os teores de creatinina e avaliação com a radiografia simples.
A avaliação da idade intra-útero, foi posteriormente comparada com a idade gestacional, determinada pelo exame do recém-nascido pela técnica de Lubchenco 26 e de Capurro 10.
O método por nós utilizado é importante, por ser simples e de fácil realização por qualquer obstetra na sala de parto, em comparação com outros métodos que implicam equipamentos onerosos e pessoal altamente especializado o que, praticamente, os invalida devido à baixa condição econômica da quase totalidade de nossas maternidades.
MATERIAL E MÉTODO
Foram utilizadas 90 amostras de líquido amniótico, coletados por amniocentese transabdominal de um grupo de gestantes de alto risco, internadas na Clínica Obstétrica do Departamento de Tocoginecologia da Escola Paulista de Medicina.
Estas gestantes apresentavam intercorrências, identificadas na Tabela 1, que indicaram o estudo do líquido âmnico.
O método utilizado foi o proposto por Brosens e Gordon 8, que consiste em se colocar uma gota de líquido âmnico em lâmina e uma gota de solução aquosa de Sulfato de Azul do Nilo a 0,1%. Após mistura de ambos colocamos a lamínula e a preparação é examinada ao microscópio, após 2 a 3 min. As células do líquido âmnico podem se corar em alaranjado ou azul. A estimação da maturidade fetal depende da porcentagem das células orangiófilas, contando-se em cada caso 500 células.
Brosens e Gordon 8 dão as seguintes percentagens em relação à maturidade fetal:
Utilizamos como métodos de comparação para avaliação a dosagem dos teores de creatinina no líquido âmnico segundo Pitkin e Zwirek 32 e a realização da radiografia simples de abdomen da grávida, nas posições frente e perfil, para observação dos núcleos de ossificação fetal, especificamente da epífise distal do femur e proximal da tíbia.
Os recém-nascidos foram avaliados quanto à sua idade gestacional pela técnica de Lubchenco 26 e de Capurro 10, utilizando a tabela de Lubchenco que indica:
pré-termo gestação com menos de 38 semanas
termo 48.a a 40.a semana
pós-termo mais de 42 semanas
RESULTADOS E DISCUSSÃO
A contagem das células orangiófilas do líquido amniótico e determinação da respectiva percentagem revelou-nos, nas 90 gestantes estudadas, 11 resultados falhos (12,22%) em relação ao exame posterior do recém-nascido. Estes casos discordantes da percentagem das células orangiófilas em relação à idade do RN foram sempre falso-negativos. Nestes 11 resultados falhos encontramos a percentagem de células menores que a correspondente idade gestacional.
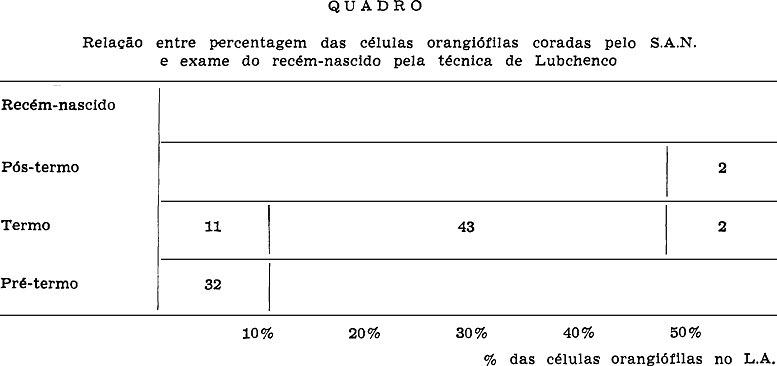
Brosens e Gordon 7,8, Anderson e Griffiths 1, Votta e col. 39 e Caspi e Lederhaendler 11 também concluem que é um método de determinação de maturidade fetal que quando falha, dá mais resultado falso-negativos que falso-positivos. Em nosso trabalho não houve perigo de um pré-termo oferecer uma elevada percentagem de células, sendo indicada a antecipação do parto, o que iria acarretar prematuridade iatrogênica (Quadro).
Nos 11 casos em que ocorreram falhas da percentagem de células orangiófilas em relação ao exame do recém-nascido, observamos a seguinte relação entre as percentagens obtidas através do Sulfato de Azul do Nilo e os pesos dos fetos (Tabela 2).
Por outro lado, relacionando os recém-nascidos de baixo peso e as respectivas percentagens de células orangiófilas, observamos o que se encontra representado na Tabela 3, isto é, níveis elevados de células orangiófilas e peso baixo do RN, porém, todos identificados como de termo.
A percentagem de células orangiófilas guarda relação com a idade fetal e não com o peso fetal. Este aspecto também foi observado por Brosens7, Brosens e Gordon 8, Gordon e Brosens 19, Anderson e Griffiths1, Morrison e col.29,30, Doran e col.15 e Jakobovits e col. 22.
Em relação às dosagens de creatinina por nós realizadas, observamos que considerando como limite para o termo um teor de 2,0 mg% e relacionando com o exame do recém-nascido pela técnica de Lubchenco 26, os valores de creatinina revelaram-nos, em 66 dosagens, 13 casos de falso-positivos (19,69%) e 8 de falso-negativos (12,12%) e um total de falha de 21 em 66 casos (31,81%).
Teoh e col. 36 observaram 5% de resultados falso-positivos. Trouchat e col.37 informam que em gestações patológicas o método é efetivo em 74% dos casos. Por outro lado, existe estreita correlação entre variações de volume do líquido âmnico e a concentração de creatinina, sendo esta variação de volume a causa da menor validade do método em algumas patologias associadas a gestações. Gauthier18 comparou os teores de creatinina com o índice citolipídico, concluindo que a creatinina poderia ser melhor indicador de maturidade antes da 38.a semana, enquanto, a partir desta época, o ideal seria a contagem das células lipídicas coradas pelo Sulfato de Azul do Nilo.
Em 27 gestantes foi realizado também o Rx do abdomen, para identificação dos pontos de ossificação fetal e concomitante identificação da idade do feto, e o mesmo revelou 9 falhas, todas falso-negativas (33,33%).
Infelizmente, a margem de variação biológica para todos os sinais de maturidade através da radiologia é grande, podendo ser utilizado como método acessório, juntamente com outros, mas não isoladamente.
Neste trabalho, ao associarmos os métodos empregados e relacionarmos à avaliação da idade gestacional do recém-nascido, pela técnica de Lubchenco 26 e de Capurro10, observamos uma falha de 2 casos nos 90 estudados. Estes 2 casos apresentaram recém-nascidos caracterizados como de pré-termo e pelo exame conjunto (células orangiófilas, creatinina e Rx) foram identificados como de termo, revelando, portanto, na associação dos 3 métodos, 2,22% de resultados falso-positivos. Esta cifra é, efetivamente, baixa em se considerando o grande número de graves intercorrências como já foi evidenciado na Tabela 1.
Relacionando os 3 exames realizados para determinação da maturidade fetal observamos o que está representado na Tabela 4.
O clínico não dispõe de nenhum método isolado, absolutamente exato para valorizar a idade fetal intra-útero. Considerando-se a disponibilidade técnica, de equipamentos e de pessoal especializado, sem dúvida a combinação de vários métodos para a identificação da maturidade fetal, seria a ideal.
Ao lado disto, Kopelman e col.25, estudando a tabela de Capurro10 e comparando-a com a de outros, Lubchenco26, Usher38 e Koenigsberger 24 consideram que devem ser aplicadas por pessoal especializado e criteriosamente avaliadas.
Devido às deficiências de nossos centros obstétricos, ainda mal aparelhados, a técnica de Sulfato de Azul do Nilo, quando realizada corretamente, e associada com a dosagem dos teores de creatinina no líquido âmnico, sempre baseados em detalhados critérios clínicos de avaliação de maturidade e correta indicação da amniocentese, é um método que deve pertencer ao arsenal propedêutico de qualquer maternidade.
CONCLUSÕES
1 O emprego simultâneo de vários métodos para avaliação da maturidade fetal: clínico, citologia do líquido âmnico com Sulfato de Azul do Nilo, dosagem dos teores de creatinina no líquido âmnico e a radiografia simples do abdomen diminuem, sensivelmente, a percentagem de falhas para a avaliação da idade fetal (2/90 = 2,22%).
2 A técnica do Sulfato de Azul do Nilo apresenta, percentualmente, falhas menores que as da creatinina e da radiografia simples do abdomen.
3 As falhas do Sulfato de Azul do Nilo foram em número de 11 (12,22%) em 90 casos, sempre falsos-negaticos, o que valoriza o método, pois impede a prematuridade iatrogênica.
4 A percentagem de células orangiófilas guarda relação com a idade fetal e não com o peso fetal, podendo ser utilizada em casos de insuficiência placentária que determina, freqüentemente, fetos pequenos para a idade gestacional.
5 Pela facilidade do método, a técnica do Sulfato de Azul do Nilo apresenta real valor nas nossas condições econômicas, devido à simplicidade de nossos centros obstétricos.
Recebido para publicação em 06-06-75
Aprovado para publicação em 30-06-75
Trabalho apresentado no XI Congresso Brasileiro de Ginecologia e Obstetrícia, realizado de 31 de agosto a 6 de setembro de 1975, Rio de Janeiro
- 1. ANDERSON, A. B. M. & GRIFFITHS, A. D. Estimation of duration of gestacion by amniotic fluid cytology. J. Obstet. Gynaec. Brit. Cwlth., 75:300-1, 1968.
- 2. ANDREWS, B. F. Amnotic fluid studies to determine maturity. Pediat. Clin. N. Amer., 17:49-67, 1970.
- 3. BARNETT, H. R. & NEVIN, M. The value of the Nile blue test in estimating fetal maturity in normal and complicated pregnancies. J. Obstet. Gynaec. Brit. Cwlth., 77: 151-5, 1970.
- 4. BATSTONE, G. F. et al. Pediatria pré-natal. Barcelona, Editorial Pediatria, 1972.
- 5. BEGNEAUD Jr., W. P. et al. Amniotic fluid creatinine for prediction of fetal maturity. Obstet. Gynec. 34: 7-13, 1969.
- 6. BISHOP, E. H. & POLLOCK, T. Fetal exfoliative cytology. Obstet. Gynec. 35:909-11, 1970.
- 7. BROSENS, I. A. Cytological study of amniotic fluid with Nile blue sulphate staining. Acta Cytol., Philadelphia, 10:159-60, 1966.
- 8. BROSENS, I. A. & GORDON, H. The estimation of maturity by cytological examination of the liquor amnii. J. Obstet. Gynaec. Brit. Cwlth., 73: 88-90, 1966.
- 9. BROSENS, I. A. et al. Prediction of fetal maturity with combined cytological and radiological methods. J. Obstet. Gynaec. Brit. Cwlth., 76: 20-6, 1969.
- 10. CAPURRO apud KOPELMAN, B. I. et al. Avaliação da idade gestacional pela tabela de Capurro. J. Pediat., Rio de Janeiro, 39:244-6, 1974.
- 11. CASPI, E. & SELIGSON-LEDERHANDLER, E. Determination of maturity by amniotic fluid cytology. Harefuadh, 78:337-42, 1970.
- 12. CHAN, W. H. et al. The value of the Nile blue sulphate stain in the cytology of the liquor amnii. J. Obstet. Gynaec. Brit. Cwlth., 76:193-5, 1969.
- 13. CLEMENTS, J. et al. Assessment of the risk of the respiratory distress syndrome by a rapid test for surfactant in amniotic fluid. New Engl. J. Med., 286:1077-81, 1972.
- 14. DELASCIO, D. & ALMEIDA, P. A. M. de Propedêutica da gestação de alto risco. São Paulo, Editora Manole, 1974.
- 15. DORAN, T. A. et al. Creatinine, uric acid and electrolytes in amniotic fluid. Amer. J. Obstet. Gynec., 106: 325-31, 1970.
- 16. DROEGEMUELLER, W. et al. Amniotic fluid examination as an aid in the assessment of gestational age. Amer. J. Obstet. Gynec., 104:424-8, 1969.
- 17. FENNEFROHN, B. Bedeutung zytologischer und spektrophotometrischer Fruchtwaasseranalysen fur die Feststellung des kindlichen reifegrades. Zbl. Gynaek., 92:1257-63, 1970.
- 18. GAUTHIER Jr., C. et al. Fetal maturity. Amniotic fluid analysis correlated with neonatal assessment. Amer. J. Obstet. Gynec., 112:344-50, 1972.
- 19. GORDON, H. & BROSENS, I. Citology of amniotic fluid: a new test for fetal maturity. Obstet. and Gynec., 30:652-9, 1967.
- 20. GLUCK, L. et al. Diagnosis of the respiratory distress syndrome by amnio-centesis. Amer. J. Obstet. Gynecol., 109:440-5, 1971.
- 21. HARRISON, R. F. Amniotic fluid uric acid levels in the maturing fetus. J. Obstet. Gynaec. Brit. Cwlth., 79: 708-9, 1972.
- 22. JAKOBOVITS, A. et al. Cytologic patterns and creatinine concentration of the amniotic fluid. Acta Cytol., Philadelphia, 16:381-5, 1972.
- 23. KITTRICH, M. Zytodiagnostik des Fruchtwasserabflusses mit Hilfe von Niblau. Geburtsh. u. Frauenheilk., 23:156-63, 1963.
- 24. KOENIGSBERGER, M. R. Judgmen of fetal age. 1. Neurologic evaluation. Pediat. Clin. N. Amer., 13:823-33, 1966.
- 25. KOPELMAN, B. I. et al. Avaliação da idade gestacional pela tabela de Capurro. J. Pediat., Rio de Janeiro, 39:244-6, 1974.
- 26. LUBCHENCO, L. O. Assessment or gestational age and development at birth. Pediat. Clin. N. Amer., 17: 125-45, 1970.
- 27. MANDELBAUM, B. et al. Determination of fetal maturity by spectrophotometric analysis of amniotic fluid. Obstet. and Gynec., 29:471-4, 1967.
- 28. MANDELBAUM, B. & EVANS, T. N. Life in the amniotic fluid. Amer. J. Obst. Gynec., 104:365-77, 1969.
- 29. MORRISON, J. C. et al. Nile Blue Staining of Cells in Amniotic Fluid for Fetal Maturity. Part 1. A Reappraisal. Obstet. and Gynec., 44: 355-61, 1974.
- 30. MORRISON, J. C. et al. Nile blue staining of cells in amniotic fluid for fetal maturity. Part II. In Complicated obstetric cases. Obstet. and Gynec., 44:362-7, 1974.
- 31. O'LEARY, J. A. & BEZJIAN, A. A. Amniotic fluid fetal maturity score. Obstet. and Ginec., 38:375-8, 1971.
- 32. PITKIN, R. M. & ZWIREK, S. J. Amniotic fluid creatinine. Amer. J. Obstet. Gynec., 98:1135-8, 1967.
- 33. ROOPNARINESINGH, S. Amniotic fluid creatinine in normal and abnormal pregnancies. J. Obstet. Gynaec. Brit. Cwlth., 77:785-90, 1970.
- 34. ROSBORG, J. et al. Estimation of fetal maturity by amniotic fluid cytology. Acta Obstet. Gynec. scand., 49:285-7, 1970.
- 35. SHARMA, S. D. & TRUSSEL, R. R. The value of amniotic fluid examination in the assessment of fetal maturity. J. Obstet. Gynaec. Brit. Cwlth., 77:215-20, 1970.
- 36. TEOH, E. S. et al. Amniotic fluid creatinine, uric acid and urea as indices of gestacional age. Acta Obstet. Gynec. scand., 52:323-6, 1973.
- 37. TROUCHAT, H. et al. Significado de la concentracion de creatinina en el embarazo normal y patológico. Obstet. Ginec. lat.-amer., 30:425-30, 1972.
- 38. USHER, V. et al. Judment of fetal age. II. Clinical significance of gestational age and an objetive method for its assessment. Pediat. Clin. N. Amer., 13:835-48, 1966.
- 39. VOTTA, R. A. et al. Cytologic study of amniotic fluid in pregnancy. Amer. J. Obst. Gynec., 102:571-7, 1968.
- 40. WATTEVILLE, H. et al. L'examen cytologique du liquide amniotique. Bull. Soc. roy. beige Gynéc. Obstét., 38:325-42, 1968.
- 41. WOYTON, J. Die Beurteilung des Reifegrades der Frucht auf Grund der Fruchtwasseruntersuchung. II. Teil. Bestimmung des Kreatinin und Fettgehaltes sowie der Fruchtwassertrubung. Zbl. Gynaek., 85:552-60, 1963.
Datas de Publicação
-
Publicação nesta coleção
17 Jul 2006 -
Data do Fascículo
Set 1975
Histórico
-
Recebido
06 Jun 1975 -
Aceito
30 Jun 1975