Resumos
OBJETIVO: Analisar a história de rastreamento citológico anterior em mulheres que apresentaram alterações citológicas e confirmação histológica para câncer cervical. MÉTODOS: Estudo transversal com 5.485 mulheres (15-65 anos) que se submeteram a rastreamento para o câncer cervical entre fevereiro de 2002 a março de 2003, em São Paulo e Campinas, SP. Aplicou-se questionário comportamental e foi feita a coleta da citologia oncológica convencional ou em base líquida. Para as participantes com alterações citológicas indicou-se colposcopia e, nos casos anormais, procedeu-se à biópsia cervical. Para investigar a associação entre as variáveis qualitativas e o resultado da citologia, utilizou-se o teste de qui-quadrado de Pearson com nível de significância de 5%. RESULTADOS: Dentre os resultados citológicos, 354 (6,4%) foram anormais, detectando-se 41 lesões intra-epitelial escamosa de alto grau e três carcinomas; em 92,6% revelaram-se normais. De 289 colposcopias realizadas, 145 (50,2%) apresentaram alterações. Dentre as biópsias cervicais foram encontrados 14 casos de neoplasia intra-epitelial cervical grau 3 e quatro carcinomas. Referiram ter realizado exame citológico prévio: 100% das mulheres com citologia compatível com carcinoma, 97,6% das que apresentaram lesões intra-epiteliais de alto grau, 100% daquelas com confirmação histológica de carcinoma cervical, e 92,9% das mulheres com neoplasia intra-epitelial cervical grau 3. A realização de citologia anterior em período inferior a três anos foi referida, respectivamente, por 86,5% e 92,8% dessas participantes com alterações citológicas e histológicas. CONCLUSÕES: Entre as mulheres que apresentaram confirmação histológica de neoplasia intra-epitelial cervical grau 3 ou carcinoma e aquelas que não apresentaram alterações histológicas não houve diferença estatisticamente significante do número de exames citológicos realizados, bem como o tempo do último exame citológico anterior.
Neoplasias do Colo do Útero; Diagnóstico Precoce; Sobrevida; Programas de Rastreamento; Esfregaço Vaginal; Estudos Transversais
OBJECTIVE: To examine previous Pap smear history in women screened for cervical cancer with cytological or histological abnormalities. METHODS: Cross-sectional study in a sample of 5,485 women (15-65 years old) who self-referred to cervical cancer screening in Sao Paulo and Campinas, Southeastern Brazil, between February 2002 and March 2003. A behavioral questionnaire was applied and cervical specimens were obtained for testing by Pap smears or liquid-based cytology. Women who had abnormal cytology were referred for colposcopic examination and, if abnormal, for cervical punch biopsy. To explore factors associated to cervical abnormalities Pearson's chi-was conduted square test at a 5% significance level. RESULTS: Cytological abnormalities were found in 354 women (6.4%) and included 41 high-grade squamous intra-epithelial lesions and 3 carcinomas; 92.7% were normal results. Colposcopy was performed in 289 women, and 145 (50.2%) showed abnormal results. Punch biopsies showed 14 cervical intraepithelial neoplasias grade 3 and 4 carcinomas. Previous Pap smears were reported in all women who had cytology suspected of carcinoma, 97.6% of those with high-grade squamous intra-epithelial lesions, all women with histological diagnosis of carcinoma and 92.9% of those who had cervical intraepithelial neoplasias grade 3 histologically. Previous Pap smear in the last tree years was reported by 86.5% and 92.8% of women with abnormal cytology and biopsy, respectively. CONCLUSIONS: There was no statistically significant difference regarding the number of Pap tests and time since their last test between women with histologically diagnosed carcinoma and cervical intraepithelial neoplasia grade 3 compared with those with normal cytology.
Uterine Cervical Neoplasms; Early Diagnosis; Mass Screening; Survivorship (Public Health); Vaginal Smears; Cross-Sectional Studies
ARTIGOS ORIGINAIS ORIGINAL ARTICLES
Rastreamento anterior para câncer de colo uterino em mulheres com alterações citológicas ou histológicas
Previous screening for cervical cancer among women with cytological and histological abnormalities
C RamaI; C RoteliMartinsI; S DerchainII; A LongattoFilhoIII; R GontijoII; L SarianII; K SyrjanenIV; T ChingV; J AldrighiVI
IHospital Leonor Mendes de Barros. São Paulo, SP, Brasil
IIUniversidade Estadual de Campinas. Campinas, SP, Brasil
IIIUniversidade de Minho. Braga, Portugal
IVDepartment of Oncology and Radiotherapy. Turku University Hospital. Turku, Finland
VFaculdade de Ciências Médicas. Santa Casa de São Paulo. São Paulo, SP, Brasil
VIFaculdade de Saúde Pública. Universidade de São Paulo (USP). São Paulo, SP, Brasil
Correspondência | Correspondence Correspondência | Correspondence: Cristina Helena Rama Hospital Leonor Mendes de Barros Av. Celso Garcia, 2477 03015000 São PauloSP Email: crisrama@usp.br
RESUMO
OBJETIVO: Analisar a história de rastreamento citológico anterior em mulheres que apresentaram alterações citológicas e confirmação histológica para câncer cervical.
MÉTODOS: Estudo transversal com 5.485 mulheres (1565 anos) que se submeteram a rastreamento para o câncer cervical entre fevereiro de 2002 a março de 2003, em São Paulo e Campinas, SP. Aplicouse questionário comportamental e foi feita a coleta da citologia oncológica convencional ou em base líquida. Para as participantes com alterações citológicas indicouse colposcopia e, nos casos anormais, procedeuse à biópsia cervical. Para investigar a associação entre as variáveis qualitativas e o resultado da citologia, utilizouse o teste de quiquadrado de Pearson com nível de significância de 5%.
RESULTADOS: Dentre os resultados citológicos, 354 (6,4%) foram anormais, detectandose 41 lesões intraepitelial escamosa de alto grau e três carcinomas; em 92,6% revelaramse normais. De 289 colposcopias realizadas, 145 (50,2%) apresentaram alterações. Dentre as biópsias cervicais foram encontrados 14 casos de neoplasia intraepitelial cervical grau 3 e quatro carcinomas. Referiram ter realizado exame citológico prévio: 100% das mulheres com citologia compatível com carcinoma, 97,6% das que apresentaram lesões intraepiteliais de alto grau, 100% daquelas com confirmação histológica de carcinoma cervical, e 92,9% das mulheres com neoplasia intraepitelial cervical grau 3. A realização de citologia anterior em período inferior a três anos foi referida, respectivamente, por 86,5% e 92,8% dessas participantes com alterações citológicas e histológicas.
CONCLUSÕES: Entre as mulheres que apresentaram confirmação histológica de neoplasia intraepitelial cervical grau 3 ou carcinoma e aquelas que não apresentaram alterações histológicas não houve diferença estatisticamente significante do número de exames citológicos realizados, bem como o tempo do último exame citológico anterior.
Descritores: Neoplasias do Colo do Útero, diagnóstico. Diagnóstico Precoce. Sobrevida. Programas de Rastreamento. Esfregaço Vaginal. Estudos Transversais.
ABSTRACT
OBJECTIVE: To examine previous Pap smear history in women screened for cervical cancer with cytological or histological abnormalities.
METHODS: Crosssectional study in a sample of 5,485 women (1565 years old) who selfreferred to cervical cancer screening in Sao Paulo and Campinas, Southeastern Brazil, between February 2002 and March 2003. A behavioral questionnaire was applied and cervical specimens were obtained for testing by Pap smears or liquidbased cytology. Women who had abnormal cytology were referred for colposcopic examination and, if abnormal, for cervical punch biopsy. To explore factors associated to cervical abnormalities Pearson's chiwas conduted square test at a 5% significance level.
RESULTS: Cytological abnormalities were found in 354 women (6.4%) and included 41 highgrade squamous intraepithelial lesions and 3 carcinomas; 92.7% were normal results. Colposcopy was performed in 289 women, and 145 (50.2%) showed abnormal results. Punch biopsies showed 14 cervical intraepithelial neoplasias grade 3 and 4 carcinomas. Previous Pap smears were reported in all women who had cytology suspected of carcinoma, 97.6% of those with highgrade squamous intraepithelial lesions, all women with histological diagnosis of carcinoma and 92.9% of those who had cervical intraepithelial neoplasias grade 3 histologically. Previous Pap smear in the last tree years was reported by 86.5% and 92.8% of women with abnormal cytology and biopsy, respectively.
CONCLUSIONS: There was no statistically significant difference regarding the number of Pap tests and time since their last test between women with histologically diagnosed carcinoma and cervical intraepithelial neoplasia grade 3 compared with those with normal cytology.
Descriptors: Uterine Cervical Neoplasms, diagnosis. Early Diagnosis. Mass Screening. Survivorship (Public Health). Vaginal Smears. CrossSectional Studies.
INTRODUÇÃO
Apesar de existirem estratégias eficazes para sua prevenção, o câncer do colo do útero continua sendo importante problema de saúde pública, especialmente nos países em desenvolvimento, onde ocorrem 78% dos casos desta neoplasia. Aproximadamente 371.200 novos casos são registrados a cada ano em todo o mundo, fazendo com que o câncer cervical seja a terceira neoplasia mais comum entre as mulheres.15
As mais altas taxas de incidência ocorrem na América Central (44,44/100.000), em algumas partes da Ásia (43,40/100.000) e no sul da África (40,44/100.000). Na América Latina, a incidência também é alta, variando de 31,79/100.000 no norte, e 27,69/100.000 no sul do continente.14,15 No Brasil, o câncer cervical é o terceiro mais freqüente entre as mulheres; em 2006, estimouse 19.260 casos novos ou 20 casos a cada 100.000 mulheres.* * Instituto Nacional de Câncer. Coordenação de Prevenção e Vigilância. Estimativa 2006: Incidência de câncer no Brasil. Rio de Janeiro; 2005. http://www.inca.gov.br/estimativa/2006/index.asp?link=conteudo_view.asp&ID=5
A prevenção do câncer cervical é possível, pois sua evolução em geral ocorre de forma lenta, com fases préclínicas detectáveis, exibindo expressivo potencial de cura dentre todos os tipos de câncer. Entretanto, no Brasil, uma grande parcela das mulheres já se encontra em fase avançada da doença na ocasião do diagnóstico, limitando a possibilidade de cura.** ** Ministério da Saúde. Secretaria Executiva. Programa Nacional Controle do Câncer do Colo Uterino. Controle do câncer do colo do útero. Brasília; 2001. Disponível em: http://bvsms.saude.gov.br/bvs/publicacoes/cancer_utero.pdf
Este problema pode, em parte, ser explicado pela cobertura irregular dos exames em países sem programas de rastreamento organizados. Enquanto um segmento da população feminina se submete várias vezes ao rastreamento, outros nunca foram rastreados.12 No Brasil, parece estar ocorrendo tendência de aumento temporal no percentual de mulheres submetidas à pelo menos um exame de Papanicolaou. Estudos realizados nos anos 80 mostravam cobertura entre 53,1% e 68,9%.9 Já um inquérito domiciliar realizado em 2003 evidenciou cobertura de 92,9%,3 *** Instituto Nacional de Câncer. Coordenação de Prevenção e Vigilância. Inquérito domiciliar sobre comportamento de risco e morbidade referida de doenças e agravos não transmissíveis. Síntese da situação da cidade de São Paulo em relação às demais capitais. Rio de Janeiro; 2004. Disponível em: http://ww2.prefeitura.sp.gov.br//arquivos/secretarias/saude/morbidade/0001/InCA_2002_2003_alterada.pdf embora ainda se observem desigualdades regionais.
O câncer cervical habitualmente iniciase como neoplasia intraepitelial cervical (NIC), uma condição préinvasiva limitada ao epitélio cervical, conforme a classificação histológica, ou como lesão intraepitelial escamosa, de acordo com o diagnóstico citológico. O exame histológico, normalmente realizado em biópsia cervical obtida na colposcopia, é aceito como o "padrãoouro" para o diagnóstico do câncer cervical, pois podem ocorrer discordâncias entre ele e a citologia.3
Historicamente, o rastreamento para o câncer cervical é baseado no exame citológico do esfregaço cervical (Papanicolaou), utilizado há mais de 50 anos. Nos países onde há eficientes programas de screening é possível comparar as taxas de cobertura às curvas de sobrevida para o câncer cervical, pois a identificação de lesões prémalignas reduz a incidência e previne o câncer em estadios mais agressivos.6
Apesar do sucesso na prevenção do câncer cervical, a citologia apresenta limitações, como os resultados falsosnegativos, que apresentam implicações médicas e legais e em saúde pública.7
Má qualidade das amostras e os erros de interpretação das lâminas são responsáveis pelas limitações na sensibilidade da citologia, cerca de 30% dos diagnósticos histológicos de neoplasia intraepitelial cervical grau 2 e 3 são negativos nos esfregaços citológicos.5 Cerca de 10% das lesões histologicamente classificadas como neoplasia intraepitelial cervical grau 1 (NIC1) podem evoluir para NIC2 ou 3; estimase que 22% dos casos não tratados de NIC2, por sua vez, possam evoluir para NIC3. As mulheres com NIC3, que inclui o carcinoma in situ, apresentam risco substancial para o câncer cervical invasivo. O objetivo dos programas de rastreamento do câncer cervical é identificar estas lesões pré neoplásicas e acompanhálas ou, quando indicado, tratálas.13
Observase que o câncer cervical ocorre com mais freqüência em mulheres que nunca se submeteram ao rastreamento para esta neoplasia, entretanto, um estudo realizado no Reino Unido, detectou que 47% dos casos de câncer cervical invasivo (superior ou igual ao estadio Ib) ocorreu em mulheres que apresentaram resultados negativos em citologias recentes e com uma história de screening aparentemente adequada.18
O presente estudo teve por objetivo analisar a história de realização de exame de citologia cervical prévia em mulheres que se submeteram a rastreamento para o câncer cervical e que apresentaram lesões cervicais citológica e/ou histologicamente confirmadas.
MÉTODOS
Estudo descritivo transversal, parte do Latin American Screening Study (LAMS). O estudo LAMS foi realizado em três centros brasileiros (São Paulo, Campinas e Porto Alegre) e em um centro na Argentina. Os dados do presente estudo são parciais, do período entre fevereiro de 2002 a março de 2003, oriundos de dois centros localizados nos municípios de São Paulo e de Campinas.
Foram incluídas 5.485 mulheres entre 15 e 65 anos de idade, com útero presente, que procuraram prevenção do câncer do colo uterino. Excluíramse as gestantes, mulheres com história de condição suspeita ou confirmada de imunossupressão, que estavam em tratamento de condiloma, com diagnóstico atual ou em tratamento de neoplasia intraepitelial cervical ou com diagnóstico de afecção maligna do trato genital inferior e as portadoras de deficiências que as impediam de compreender o estudo ou responder ao questionário.
Aplicouse questionário padronizado sobre informações sociodemográficas, comportamentais e reprodutivas. Todas as participantes foram submetidas a exame pélvico que incluiu coleta de células cervicais para realização de citologia oncológica convencional ou de base líquida.
As amostras coletadas foram examinadas pelo Laboratório da Divisão de Patologia do Instituto Adolfo Lutz de São Paulo e pelo Laboratório de Patologia do Hospital da Faculdade de Ciências Médicas da Universidade Estadual de Campinas. As amostras foram periodicamente submetidas a controle de qualidade em dois laboratórios europeus (Itália e Eslovênia).
A citologia cervical foi testada por duas formas: convencional ou citologia em base líquida. Cada participante foi submetida a apenas uma dessas técnicas. A citologia em base líquida foi realizada somente no centro de São Paulo, em 1.628 mulheres (do total das 3.000 recrutadas nesse centro).
O esfregaço citológico convencional foi constituído de duas amostras, raspado ectocervical e endocervical, colhidos com espátula de Ayre e escova endocervical. O material foi imediatamente fixado após a coleta com polietilenoglicol e corado pelo método de Papanicolaou.
A citologia em baselíquida foi realizada por DNACitoliq (Digene do Brasil), a amostra foi coletada com escova endocervical e imersa em tubo com o meio conservante UCM (Universal Collecting Medium, Digene do Brasil) e processada conforme instruções do fabricante.8 As lâminas foram coradas pelo método de Papanicolaou. Os resultados foram classificados de acordo com a classificação de Bethesda 2001.21
A colposcopia foi indicada sistematicamente para todas as mulheres com alterações na citologia oncológica, onde se considerou: células escamosas atípicas de significado indeterminado, incluindo lesões possivelmente não neoplásicas e aquelas onde não se pode afastar lesão intraepitelial escamosa de alto grau (ASCUS), atipias glandulares de origem indeterminada (AGUS), lesão intraepitelial de baixo grau, lesão intraepitelial de alto grau, e carcinoma. Todos os exames foram realizados por colposcopistas certificados e experientes. Foi realizado cuidadoso exame da cervix e da junção escamocolunar um minuto após aplicação de ácido acético a 5%. Quando a colposcopia apresentou resultado anormal, foram realizadas biopsias utilizandose pinças de sacabocado, sendo retiradas amostras das regiões alteradas.22 A descrição colposcópica foi consoante à terminologia da International Federation of Cervical Pathology and Colposcopy (IFCPC).22 Os resultados das biópsias foram classificados de acordo com os critérios definidos pela Classificação Internacional de Tumores/Organização Mundial de Saúde.20
As participantes com alteração dos exames citológicos foram encaminhadas para seguimento ou tratamento apropriado para cada caso. As informações originalmente quantitativas em estudo foram transformadas em variáveis qualitativas e são descritas em valores percentuais.
Para investigar a associação entre as variáveis qualitativas e o resultado da citologia, utilizouse o teste de quiquadrado de Pearson com nível de significância de 5%. As variáveis que apresentaram p<0,20 no estudo de associação com o resultado da citologia no teste de quiquadrado foram incluídas na análise multivariada. No ajuste do modelo de regressão logística utilizouse o método forward com o critério de máxima verossimilhança para seleção das variáveis. As odds ratios das variáveis selecionadas e seus respectivos intervalos de confiança de 95% são apresentados. O pacote estatístico SPSS for v13.0 foi utilizado para as análises dos dados.
O estudo foi aprovado pelos Comitês de Ética em Pesquisa do Hospital Leonor Mendes de Barros e da Faculdade de Ciências Médicas da Universidade Estadual de Campinas, pela Comissão Nacional de Ética em Pesquisa e pelo Comitê de Ética em Pesquisa da Faculdade de Saúde Pública da Universidade de São Paulo.
RESULTADOS
A presente análise incluiu 5.485 mulheres, a média etária foi de 36,5 (±10,8) anos, sendo os principais grupos etários de 35 a 44 anos e 25 a 34 anos.
A caracterização da amostra estudada segundo características sociodemográficas, sexuais e reprodutivas encontrase na Tabela 1. Predominaram mulheres da raça branca, que viviam com o parceiro sexual, escolaridade entre cinco e oito anos, e 92,1% das participantes referiram ter realizado citologia oncológica em algum momento da vida.
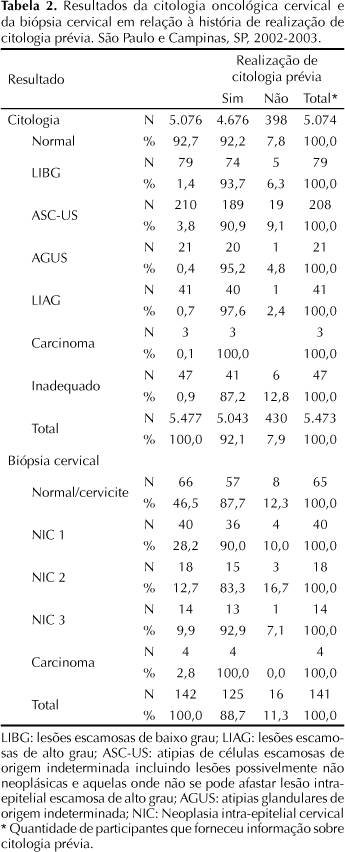
Foram perdidas 8 (0,1%) amostras de esfregaços, ficando disponíveis 5.477 exames e destes, 47 (0,9%) foram considerados inadequados. Os resultados citológicos revelaramse normais em 92,7% das amostras coletadas. Entre as alterações citológicas a mais freqüente foi ASCUS (3,8%), seguida de lesões intraepiteliais escamosas de baixo grau (LIBG 1,4%), lesões intraepiteliais escamosas de alto grau (LIAG 0,7%), 0,4% AGUS e três carcinomas (0,1%), conforme Tabela 2.
A realização de exame citológico anterior foi referida por 92,2% das mulheres que apresentaram resultados normais da citologia e por 92,6% das participantes que apresentaram algum tipo de alteração citológica (ASCUS, AGUS, LIBG, LIAG ou carcinoma). Não houve associação estatisticamente significante entre a história prévia de realização de citologia e o resultado da citologia no presente estudo (p=0,9). Todas as mulheres com citologia compatível com carcinoma e 97,6% das que apresentaram lesões intraepiteliais de alto grau referiram ter realizado citologia prévia (Tabela 2).
Para as participantes que referiram citologia anterior, avaliouse a associação entre o tempo da realização do último exame citológico, o número de exames anteriores e o resultado de exame citológico. Para isto, as anormalidades citológicas foram agrupadas em 3 grupos: LIBG, atipias de origem indeterminada (ASCUS e AGUS), LIAG e carcinomas. Não se observou associação estatisticamente significante nem entre o tempo do último exame citológico referido (p=0,395), tampouco com o número de exames anteriormente realizados (p=0,052) e os resultados da citologia (Tabela 3).
Das 354 colposcopias indicadas por alteração da citologia 289 (81,6%) foram realizadas. Dentre todas as colposcopias realizadas, 144 resultaram normais e, portanto, não se realizou biópsia e 145 (50,2%) colposcopias apresentaram alterações, sendo realizada a biópsia dirigida.
Do total das biópsias realizadas foram disponíveis 141 resultados, com a seguinte distribuição: 65 biópsias normais/colpite e 76 com as seguintes alterações: 40 NIC1; 18 NIC2, 14 NIC3 e 4 carcinomas. Observase que 93% das participantes com resultados histológicos compatíveis com NIC3 (13 casos) e 100% dos carcinomas (4 casos) referiram ter realizado exame citológico anterior (Tabela 2).
Dentre as participantes que apresentaram resultado de biópsia compatível com NIC3 ou carcinoma, 71,4% e 21,4% referiram, respectivamente, ter realizado citologia prévia no ano anterior e entre um a três anos (Tabela 4). Não houve associação estatisticamente significante entre tempo de realização do último exame citológico e o resultado da biópsia (p=0,73), tampouco, entre o número de exames anteriormente realizados (p= 0,55) com resultado de biópsia (Tabela 4).
NIC3 e carcinoma foram agrupados em uma única categoria pela relevância clínica desses dois resultados e pelo pequeno número de casos de carcinoma. Pelo mesmo motivo, os casos de carcinoma não foram classificados separadamente conforme o estadiamento ou tipo histológico.
Encontrouse associação estatisticamente significante no teste de quiquadrado entre resultado da citologia (agrupados em duas categorias: normal e com alterações) e as seguintes variáveis: faixa etária, raça, viver com parceiro, idade da primeira relação sexual, número de parceiros, história de doença sexualmente transmissível anterior e tabagismo. Não apresentaram associação com o resultado da citologia: escolaridade, uso de contracepção, uso de contracepção hormonal, número de partos e realização de citologia anterior.
As variáveis selecionadas na análise multivariada estão apresentadas na Tabela 5. As seguintes variáveis estiveram significativamente associadas com o resultado da citologia: a raça negra mostrou chance 1,5 vez maior que as mulheres da raça branca; mulheres com história de doença sexualmente transmissível apresentaram chance 1,6 vez maior que as que negaram esta condição; e as tabagistas apresentaram chance 1,4 vez maior comparada às mulheres que referiram nunca ter fumado.
Viver com companheiro relacionouse negativamente com resultados citológicos anormais, bem como iniciar vida sexual em idade superior ou igual aos 18 anos em relação às mulheres que referiram início anterior aos 16 anos (Tabela 5).
DISCUSSÃO
Considerase elevado o número de mulheres do presente estudo (92,2%) que referiu ter realizado exame citológico anterior, uma vez que os dois centros atendem principalmente população dependente do Sistema Único de Saúde (SUS). Em recente estimativa da cobertura do exame citológico no País, observaramse valores entre 74% a 93%, entretanto, o percentual de realização desse exame no SUS oscilou entre 33% a 64%.*** *** Instituto Nacional de Câncer. Coordenação de Prevenção e Vigilância. Inquérito domiciliar sobre comportamento de risco e morbidade referida de doenças e agravos não transmissíveis. Síntese da situação da cidade de São Paulo em relação às demais capitais. Rio de Janeiro; 2004. Disponível em: http://ww2.prefeitura.sp.gov.br//arquivos/secretarias/saude/morbidade/0001/InCA_2002_2003_alterada.pdf Outro estudo, realizado na cidade de São Paulo, encontrou cobertura de 68,9%.12 Entretanto, esses dois estudos foram inquéritos domiciliares, cabendo citar a primeira limitação da presente análise, onde as participantes espontaneamente buscaram o rastreamento para o câncer cervical. Portanto, a amostra do presente estudo pode não ser representativa para o restante da população que não teve acesso aos hospitais, limitando a possibilidade de generalização dos resultados.
Na análise multivariada, tanto as variáveis associadas positivamente às alterações citológicas (raça negra, doença sexualmente transmissível anterior e tabagismo), quanto os fatores de proteção (viver com companheiro e ter iniciado vida sexual após os 18 anos) têm sido exaustivamente descritas como fatores respectivamente de risco e de proteção para a infecção por HPV.13,7
Quanto ao tempo de realização do último exame citológico anterior a inclusão no estudo, a maioria das participantes com alterações citológicas referiu exame prévio em período de até três anos. A recomendação de screening no Brasil** ** Ministério da Saúde. Secretaria Executiva. Programa Nacional Controle do Câncer do Colo Uterino. Controle do câncer do colo do útero. Brasília; 2001. Disponível em: http://bvsms.saude.gov.br/bvs/publicacoes/cancer_utero.pdf e em países como o Canadá3 é de intervalos de três anos, após dois exames anuais consecutivos negativos.
Para serem incluídas no presente estudo, as participantes não poderiam apresentar diagnóstico atual ou estarem em acompanhamento ou tratamento de neoplasia intraepitelial cervical ou com diagnóstico de afecção maligna do trato genital inferior. Portanto, esses resultados poderiam refletir três situações: (1) ocorrência de resultados falsonegativos nas citologias prévias; (2) falha dos mecanismos de seguimento ou tratamento inadequado dessas mulheres com lesões cervicais, caso as alterações já houvessem sido anteriormente detectadas; ou ainda (3) a participante poderia ter omitido diagnóstico de patologia cervical anterior por desconhecimento ou outra razão. Uma das limitações do presente estudo foi o fato de que se dispôs somente de informação fornecida pela participante, sem acesso aos registros de prontuário dessas mulheres para verificar a realização de exame colposcópico ou tratamentos anteriores, que auxiliaria confirmar ou refutar a segunda e terceira hipóteses.
O número de exames citológicos prévios referido pelas participantes pode estar sujeito a vieses, como a não distinção entre a coleta do exame citológico e simplesmente a realização de exame ginecológico. Ou ainda, a possibilidade de a mulher superestimar a realização de exames citológicos por ser esta uma prática preventiva em saúde esperada pela sociedade.12
Metade das participantes com citologia alterada referiram realização de mais de três exames citológicos durante a vida. A hipótese de possível resultado falsonegativo em citologia prévia ou de seguimento inadequado de alterações cervicais anteriores deve ser aventada.
O resultado falsonegativo em um teste de rastreamento é mais preocupante que o falsopositivo, já que as mulheres falsonegativas poderão ser perdidas e permanecerão com risco de desenvolver câncer.2 Apesar da alta especificidade da citologia cervical para lesões de alto grau ou câncer, resultados de duas metaanálises mostraram grande variação na sua sensibilidade, com valores médios de 47% e de 58%.4,11
Algumas alternativas têm sido propostas no rastreamento do câncer cervical, como a citologia em baselíquida para ganho da sensibilidade do exame citológico. Nessa técnica, todo o material celular coletado é acondicionado em meio líquido, resultando em menor perda do material e preservação das estruturas morfológicas celulares.8 Recente metanálise mostrou que as taxas médias de espécimes inadequados encontradas, que levam a convocação da mulher para a repetição do exame, foram de 0,8% para a citologia em baselíquida e 7,5 para a citologia convencional.18
Outra alternativa para rastreamento é a utilização dos testes moleculares para identificação do HPV. No entanto, seu alto custo e a elevada prevalência desta infecção nas mulheres em idade reprodutiva são limitações que tornariam impraticável o seguimento de todos os casos positivos. Além disso, 80% das infecções serão transitórias, principalmente nas jovens, representando investimento desnecessário.2,7
Em função disso, a captura de híbridos II (CHII), um ensaio de hibridização molecular para identificação viral, tem seu uso proposto no rastreamento de mulheres com 30 anos ou mais, adjunto à citologia e realizado a cada três anos. Nos casos de positividade da CHII, fazse necessário um seguimento mais intenso.19 Por outro lado, o valor preditivo negativo é alto para lesões de alto grau, quando se realiza um único teste; na vigência de dois testes negativos os intervalos para rastreamento podem ser seguramente realizados com maior intervalo de tempo.7
Para que haja efetiva redução na incidência do câncer cervical os programas de rastreamento devem ser de alta qualidade, organizados e com ampla cobertura da população. O rastreamento citológico organizado compreende agendamento e convocação das mulheres, sistema para pronto tratamento ou seguimento adequado dos casos com alterações, educação contínua da equipe que realiza a coleta e da que faz a leitura dos esfregaços e publicação regular de manuais de procedimentos técnicos para orientação das equipes.3,16,17
Entretanto, o custo de programas de rastreamento que contemplem esses itens para sua real efetividade pode ser impeditivo para os países em desenvolvimento, onde os recursos aplicados em saúde pública competem com outras questões também prioritárias. Mesmo países desenvolvidos que dispõem de sistema de rastreamento adequado ainda não conseguiram erradicar totalmente o câncer cervical, que persiste em minorias economicamente desfavorecidas da população.10
A avaliação de programas de rastreamento citológico para o câncer cervical, que se iniciaram na década de 1970 em oito países da América Latina, inclusive o Brasil, mostrou queda da mortalidade após 20 anos apenas no Chile e em Porto Rico.16
A presente análise mostrou não haver diferença estatisticamente significante entre as mulheres que apresentaram confirmação histológica (NIC3 ou carcinoma) e aquelas que não apresentaram alterações histológicas, tanto entre número de exames citológicos realizados, bem como no tempo de realização do último exame. Isso reforça a necessidade de real prática de controle de qualidade nos programas de rastreamento para o câncer cervical já existentes, além de efetivo seguimento e tratamento dos casos detectados com alterações.
Tendo em vista que os programas de rastreamento para o câncer cervical devem prevenir o câncer e não apenas reduzir a mortalidade, os casos diagnosticados em estádio dois ou mais deveriam ser considerados falha do programa de rastreamento, tendose que realizar auditoria do rastreamento anterior dessas mulheres.17
Em conclusão, os resultados da presente análise evidenciam a necessidade de estudos especialmente desenhados para avaliação da qualidade dos programas de rastreamento para o câncer cervical no País.
Recebido: 30/8/2007
Aprovado: 3/1/2008
Financiado pelo European Commission, Projeto Latin América Study (LAMS DEV Contract #ICA4CT200110013).
Artigo baseado na dissertação de mestrado de C Rama, apresentada à Faculdade de Saúde Pública da Universidade São Paulo, em 2006.
Dados parciais foram apresentados em pôster no XVIII International Federation of Gynecology World Congress of Gynecology & Obstetrics, em Kuala Lumpur, Malásia, novembro, 2006.
- 1. Baseman JG, Koutsky LA. The epidemiology of human papillomavirus infections. J Clin Virol. 2005;32(Supl 1):S1624.
- 2. Bosch FX, Lorincz A, Muñoz N, Meijer CJ, Shah KV. The causal relation between human papillomavirus and cervical cancer. J Clin Pathol 2002;55(4):24465.
- 3. DuarteFranco E, Franco EL. Cancer of the uterine cervix. BMC Women's Health. 2004;4(Supl 1):S13.
- 4. Fahey MT, Irwig L, Macaskill P. Metaanalysis of Pap test accuracy. Am J Epidemiol1995;141(7):6809.
- 5. Ferreccio C, Bratti MC, Sherman ME , Herrero R, Wacholder S, Hildesheim A, et al. A comparison of single and combined visual, cytologic and virologic tests and screening strategies in a region at high risk of cervical cancer. Cancer Epidemol Biomarkers Prev. 2003;12(9):81523.
- 6. Forbes C, Jepson R, MartinHirsch P. Interventions target at women to encourage the uptake of cervical screening. Cochrane Database Syst Rev. 2002;(3):CD002834.
- 7. Franco EL, DuarteFranco E, Ferenczy A. Cervical cancer: epidemiology, prevention and the role of human papillomavirus infection. CMAJ. 2001;164(7): 101725.
- 8. Longatto Filho A, Utagawa ML, Pereira SMM, Pittoli JE, Aguiari LS, Maeda MYS, et al. Low and highrisk HPV types detected with Hybrid Capture II (HC2) in LiquidBased Cytology (DNA CITOLIQ®) System: Experience from the LAMS (Latin American Screening) study. J Bras Doencas Sex Transm. 2004;16(1):1720.
- 9. Martins LFL, Thuler LCS, Valente JG. Cobertura do exame de Papanicolaou no Brasil e seus fatores determinantes: uma revisão sistemática da literatura. Rev Bras Ginecol Obstet 2005;27(8):485492.
- 10. McGoogan E. Liquidbased cytology. In: Monsonego J, editor. Emerging Issues on HPV Infections: From Science to Practice. Basel: Karger; 2006.
- 11. Nanda K, McCrory DC, Myers ER, Bastian LA, Hasselblad V, Hickey JD, et al. Accuracy of the Papanicolaou test in screening for and followup of cervical cytologic abnormalities: a systematic review. Ann Intern Med. 2000;132(10):8109.
- 12. Nascimento CM, ElufNeto J, Rego RA. Pap test coverage in São Paulo municipality and characteristics of the women tested. Bull Pan Am Health Organ. 1996;30(4):30212.
- 13. Pagliusi SR, Teresa Aguado M. Efficacy and other milestones for human papillomavirus vaccine introduction. Vaccine. 2004;23(5):56978.
-
14Pan American Health Organization. Cervical cancer in Latin America and the Caribbean: fact sheet 2001. Washington; 2001[acesso em: 22/02/05]. Disponível em: http://www.ops–oms.org/English/AD/DPC/NC/ccbriefsnapshot.pdf
- 15. Parkin DM, Pisani P, Ferlay J. Global Cancer Statistics. Cancer J Clin. 1999; 49(1):3364.
- 16. Sankaranarayanan R, Budukh AM, Rajkumar R. Effective screening programmes for cervical cancer in low and middleincome developing countries. Bull World Health Organ. 2001;79(10):95462.
- 17. Sasieni PD, Cuzick J, LynchFarmery E. Estimating the efficacy of screening by auditing smear histories of women with and without cervical cancer. The National Coordinating Network for Cervical Screening Working Group. Br J Cancer. 1996;73(8):10015.
- 18. Sasieni P, Fielder H, Rose B. Liquidbased versus conventional cervical cytology. Lancet 2006;367(9521):14813.
- 19. Saslow D, Runowicz C, Solomon D, Moscicki AB, Smith RA, Eyre HJ, et al. American Cancer Society guideline for the early detection of cervical neoplasia and cancer. Cancer J Clin. 2002;52(6):34262.
- 20. Scully RE, Bonfiguio TA, Kurman RJ, Silverberg SG, Wilkins EJ. Histologycal typing of female genital tract tumors. 2. ed. Berlin: Spring Verlag; 1994.
- 21. Solomon D, Davey D, Kurman R, Moriarty A, O'Connor D, Prey M, et al. The 2001 Bethesda System: terminology for reporting results of cervical cytology. JAMA. 2002;287(16):21149.
- 22. Walker P, Dexeus S, De Palo G, Barrasso R, Campion M, Girardi F, et al. Nomenclature Committee of the International Federation for Cervical Pathology and Colposcopy. International terminology of colposcopy: an updated report from the International Federation for Cervical Pathology and Colposcopy. Obstet Gynecol. 2003;101(1):1757.
Datas de Publicação
-
Publicação nesta coleção
09 Maio 2008 -
Data do Fascículo
Jun 2008
Histórico
-
Aceito
03 Jan 2008 -
Recebido
30 Ago 2007