Resúmenes
El examen coproparasitológico (técnica de Kato-Katz) de un total de 113.254 personas, pertenecientes a 100 municipios de Venezuela, permitió establecer las siguientes prevalencias a nivel nacional: Ascaris lumbricoides: 26,9%, Trichuris trichiura: 32,6% y Anquilostomideos: 5,6%. Además se determinaron los valores de la prevalencia para los mencionados geohelmintos en los 100 municipios considerados observándose una gran variabilidad. Para T. trichiura los valores máximos se obtuvieron en los municipios Arévalo González (54,6%), en el Estado Miranda, Urama (76,9%) en el Estado Carabobo y Punta de Piedra (78,4%) en el Estado Sucre. Para A. lumbricoides, en los municipios Punta de Piedra (63%) y Tunapuy (61,9%), en el Estado Sucre y Arévalo González (62,7%) en el Estado Miranda. Mientras que para los Anquilostomideos las prevalencias máximas se detectaron en los municipios El Amparo (39,5%) y San Camilo (35,9%) en el Estado Apure. En cuanto a la edad las prevalencias más altas se determinaron en niños de edad pre-escolar y escolar, para A. lumbricoides y T. trichiura y en adolescentes y adultos para anquilostomideos.
Prevalencia; Geohelmintos; Ascaris lumbricoides; Trichuris trichiura; Anquilostomideos; Venezuela
A total of 113254 individuals from 100 venezuelan municipalities were studied by mean of Kato-Katz coprological examination and the geohelminth prevalences were established. The national prevalences of T. trichiura, A. lumbricoides and Anquilostomideos were 32.6%, 26.9% and 5.6% respectivelly. For T. trichiura the highest values were obtained for the following municipalities: Arévalo González (54.6%) in Miranda state, Urama (76.9%) in Carabobo state and Punta de Piedra (78.4%) in Sucre state. For A. lumbricoides the highest values were determined in Punta de Piedra (63%), Tunapuy (61.9%) in Sucre state and Arévalo González (62,7%) in Miranda state. For hookworm the highest values were detected in El Amparo (39.5%) and San Camilo (35.9%) in the state of Apure. In relation to the age, the highest prevalence of Ascariosis and Trichuriosis were determined in pre-school and school children and for hookworm in adolescents and adults. A high variability between the municipalities belonging to the same state for the three geohelminths was observed.
Prevalence; Geohelminth; Ascaris lumbricoides; Trichuris trichiura; Hookworm; Venezuela
ARTIGO
Prevalencias de las geohelmintiasis intestinales en 100 municipios de Venezuela (1989-1992)
Intestinal nematode prevalences in 100 municipalities from Venezuela
Gustavo A. Morales C., Luz Pino de Morales, César Arteaga, Liboria Matinella y Hermes Rojas
Resumen El examen coproparasitológico (técnica de Kato-Katz) de un total de 113.254 personas, pertenecientes a 100 municipios de Venezuela, permitió establecer las siguientes prevalencias a nivel nacional: Ascaris lumbricoides: 26,9%, Trichuris trichiura: 32,6% y Anquilostomideos: 5,6%. Además se determinaron los valores de la prevalencia para los mencionados geohelmintos en los 100 municipios considerados observándose una gran variabilidad. Para T. trichiura los valores máximos se obtuvieron en los municipios Arévalo González (54,6%), en el Estado Miranda, Urama (76,9%) en el Estado Carabobo y Punta de Piedra (78,4%) en el Estado Sucre. Para A. lumbricoides, en los municipios Punta de Piedra (63%) y Tunapuy (61,9%), en el Estado Sucre y Arévalo González (62,7%) en el Estado Miranda. Mientras que para los Anquilostomideos las prevalencias máximas se detectaron en los municipios El Amparo (39,5%) y San Camilo (35,9%) en el Estado Apure. En cuanto a la edad las prevalencias más altas se determinaron en niños de edad pre-escolar y escolar, para A. lumbricoides y T. trichiura y en adolescentes y adultos para anquilostomideos.
Palabras-claves: Prevalencia. Geohelmintos. Ascaris lumbricoides. Trichuris trichiura. Anquilostomideos. Venezuela.
Abstract A total of 113254 individuals from 100 venezuelan municipalities were studied by mean of Kato-Katz coprological examination and the geohelminth prevalences were established. The national prevalences of T. trichiura, A. lumbricoides and Anquilostomideos were 32.6%, 26.9% and 5.6% respectivelly. For T. trichiura the highest values were obtained for the following municipalities: Arévalo González (54.6%) in Miranda state, Urama (76.9%) in Carabobo state and Punta de Piedra (78.4%) in Sucre state. For A. lumbricoides the highest values were determined in Punta de Piedra (63%), Tunapuy (61.9%) in Sucre state and Arévalo González (62,7%) in Miranda state. For hookworm the highest values were detected in El Amparo (39.5%) and San Camilo (35.9%) in the state of Apure. In relation to the age, the highest prevalence of Ascariosis and Trichuriosis were determined in pre-school and school children and for hookworm in adolescents and adults. A high variability between the municipalities belonging to the same state for the three geohelminths was observed.
Key-words: Prevalence. Geohelminth. Ascaris lumbricoides. Trichuris trichiura. Hookworm. Venezuela.
Existe una clara interelación entre las condiciones socioeconómicas y el medio ambiente como elementos favorecedores de la transmisión de las geohelmintiasis5 de ahí que sea conocido el hecho de que estas parasitosis son mas frecuentes en regiones húmedas y pobres que en las ciudades económicamente desarrolladas27, tal como lo reportaron Kilpatrick et al17 en el Perú, quienes encontraron las tasas mas elevadas de infección en los sectores mas pobres de la población.
Según Stephenson et al32 las infecciones por Ascaris lumbricoides, Trichuris trichiura y anquilostomideos (Necator americanus y Ancylostoma duodenale) son muy frecuentes en los países en vías de desarrollo y constituyen un importante problema de salud debido a su alto carácter endémico, repercusión negativa en el progreso socioeconómico y efectos negativos sobre la población infantil5. Sin embargo, dichas parasitosis ocupan un lugar poco importante en la lista de prioridades, en los programas de Salud Pública3.
En el año 1989, la División de Endemias Rurales del Ministerio de Sanidad y Asistencia Social21, acordó reactualizar los índices parasitarios en el país, tomando como referencia los mismos 100 municipios que habían sido evaluados en 1976.
El objetivo del presente trabajo consiste en reportar la prevalencia de las geohelmintiasis en las entidades federales de Venezuela y al interior de cada una de ellas, considerando los municipios encuestados. Se realiza además, la comparación de las prevalencias de cada una de las geohelmintiasis en relación con la edad de las personas.
MATERIALES Y MÉTODOS
La División de Endemias Rurales del Ministerio de Sanidad y Asistencia Social (MSAS) realizó un muestreo coproparasitológico a un total de 113254 personas, empleando la técnica de Kato-Katz27. La información cuantitativa, expresada en número de huevos por gramo de heces, se estableció para aproximadamente el 26% de la población examinada, pero no fue utilizada en el presente trabajo, el cual está referido únicamente a la prevalencia.
Se consideraron 5 grupos de edad, cuya distribución es presentada en la Tabla 1.
Técnica de muestreo. Se aplicó la metodología del Programa de lucha contra la Anquilostomiasis y otras Parasitosis Intestinales del MSAS, cuyo objetivo es unificar critérios para la toma de muestras significativas de la población, que permitan la estimación confiable de la prevalencia de las geohelmintiasis. Para el estimado del tamaño de la muestra tanto en personas como en viviendas se requiere del conocimiento prévio del número de habitantes de la comunidad a encuestar. Se consideran a razón de 4 personas por vivienda, además se debe disponer de un croquis de la zona y de la numeración corrida de todas las viviendas. El número de personas y el número viviendas a encuestar, puede ser estimado mediante las siguientes ecuaciones predictivas (G. Morales et al: datos no publicados):
1) N° de personas = 815 + 0,32 x n° de habitantes de la localidad
2) N° de viviendas = 2,04 + 0,32 x n° de viviendas de la localidad
Análisis de los datos. La comparación de la frecuencia de casos de la presencia de los geohelmintos considerados, en las distintas entidades federales se realizó mediante la Prueba de Ji-cuadrado23.
La comparación entre los porcentajes de infectados por los nemátodos, arriba mencionados, en relación a los grupos de edad de los individuos, así como la de los porcentajes de infectados entre los municipios de una misma entidad federal, se realizó mediante el análisis de varianza28 31. En los casos en los cuales se evidenció la existencia de diferencias estadísticamente significativas, se procedió al contraste entre las medias correspondientes, mediante la prueba de Tukey19 28.
Como paso prévio a la realización del análisis de varianza, se procedió a la normalización de los datos mediante la transformación arc sen (check)p, por tratarse de porcentajes19. En aquellas entidades federales, en las cuales se encuestaron dos municipios, se empleó la técnica de comparación de porcentajes para muestras grandes23. Los valores presentados en las tablas están sin transformar.
RESULTADOS
Del total de las 113.254 personas examinadas coproscópicamente, el 26,9% presentó huevos de A. lumbricoides, el 32,6% resultó positivo a Trichuris trichiura y sólo el 5,6% presentó en sus heces huevos de Anquilostomideos (Tabla 2).
La frecuencia de casos de cada uno de los geohelmintos mencionados resultó con diferencias estadísticamente significativas entre las entidades federales de Venezuela (Tabla 2), correspondiéndole a A. lumbricoides, la prevalencia mas elevada en los estados Sucre (52,9%) y Amazonas (43,3%), en el caso de T. trichiura, la mayor prevalencia recayó en los estados Sucre (58,5%), Carabobo (49,8%), Yaracuy (45,5%) y Monagas (42,6%). Para los anquilostomideos, la mayor prevalencia se observó en los estados Apure (28,5%), Barinas (19,6%) y Bolívar (19,2%).
Al interior de cada estado, se observó una gran variabilidad en las prevalencias de las geohelmintiasis, revelando en la mayoría de los casos diferencias estadísticamente significativas entre los municipios. En efecto, hubo casos como el del Estado Aragua, en el cual la prevalencia de algunos de los municipios, como el Mario Briceño Iragorri, superaron a la prevalencia nacional, mientras que en otro municipio del mismo estado, como el Santos Michelena, la prevalencia resultó inferior a dicho valor (Tabla 2).
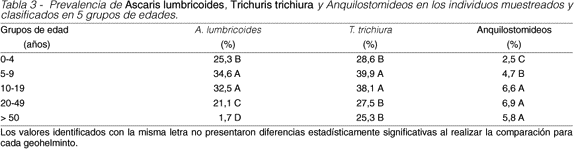
El análisis de la prevalencia, considerando los grupos de edad independientemente de la entidad federal o municipal de procedencia, evidenció que la mayor prevalencia de A. lumbricoides y T. trichiura le correspondió a los grupos comprendidos entre 5 y 9 años y entre 10 y 19 años, entre los cuales no se detectaron diferencias estadísticamente significativas. En el caso de los anquilostomideos, recayó en los grupos de edades superiores a los 10 años, los cuales no arrojaron diferencias estadísticamente significativas (Tabla 3).
DISCUSIÓN
El empleo de técnicas de diagnóstico sensibles y confiables como la de Kato y su variante Kato Katz13 18 27 que garantizan la idoneidad de los resultados29, permite el uso de la prevalencia como estadística epidemiológica para la planificación y evaluación de programas de control, así como, para describir los niveles de endemicidad y patrones de morbilidad de las parasitosis15. Por lo tanto, estas ténicas proveen una información confiable, de gran utilidad para los entes planificadores de salud, justificándose su uso en encuestas oficiales.
La presencia de A. lumbricoides, T. trichiura y Anquilostomideos, en todas las entidades federales de Venezuela, se ve justificada en vista de que en la transmisión de los mismos juegan un papel fundamental las condiciones socioeconómicas y el medio ambiente7 8 y que su difusión está vinculada con la contaminación fecal de la tierra y el inadecuado saneamiento ambiental6 8 14. Estos aspectos están además relacionados con el hecho de que para el año 1990, unas 540.640 viviendas, el 13,5% del total del país, carecía de dispositivos para la eliminación adecuada de las excretas y que prácticamente en todo el territorio nacional se reunen las condiciones ecológicas para el desarrollo y la persistencia de los geohelmintos21.
Los resultados obtenidos evidenciaron las prevalencias más elevadas para A. lumbricoides y T. trichiura, ambas especies con contaminación oral-fecal y vinculadas a factores de riesgo similares5 8. Mientras que los anquilostomideos presentaron los más bajos valores, sin que exista ninguna relación de magnitud con los geohelmintos ya mencionados, lo cual concuerda con lo señalado por Booth y Bundy5. Además la presencia de los anquilostomideos, está fuertemente limitada por las condiciones ambientales extremas, como las de las zonas xerófilas y en aquellas ubicadas por encima de los 2.500m.s.n.m.1 16. A lo que podemos agregar que la presencia de estos parásitos puede ser subestimada debido a que en casos de infecciones leves, es frecuente que se den diagnósticos de falsos negativos4.
En muchos casos, los resultados nacionales no reflejaron la situación crítica de algunos estados y municipios, como lo demuestra el hecho frecuente de encontar diferencias estadísticamente significativas entre las prevalencias de los geohelmintos entre los municipios de un mismo estado, lo cual reafirma el hallazgo de Bundy y Cooper10 de que en zonas de baja prevalencia pueden aparecer focos hiperendémicos como consecuencia de condiciones sanitarias deficientes y alta densidad poblacional.
Al considerar a los grupos de edad, el hecho de haber encontrado positivos a los geohelmintos considerados a niños entre 0 y 4 años, refleja la importancia de la vivienda como sitio de transmisión, cuya importancia fué señalada por Gabaldón en 196714.
En el caso específico de la infección por A. lumbricoides, el haber detectado prevalencias mas elevadas en los niños de edades entre 5 y 9 y entre 10 y 12 años y que en términos de valores absolutos le correspondan los más elevados, al primero de los mencionados, coincide con lo reportado en la bibliografía para otros países latinoamericanos3 33. Además, dicho grupo etáreo ha sido recientemente señalado como de gran importancia en el mantenimiento endémico de la ascariasis, debido a que presenta mayor prevalencia, mayor intensidad de la infección por dicho parásito y mayor riesgo relativo para infectarse, lo cual le confiere interés para el monitoreo de programas de control de dicha parasitosis (G. Morales et al: datos no publicados).
En el caso de Trichuris trichiura, Bundy9 y Bundy et al11 reportaron en comunidades caribeñas un aumento de la prevalencia con el incremento de la edad de las personas y su mantenimiento relativamente constante en los adultos. Sin embargo, los resultados de la presente encuesta revelaron una mayor prevalencia de dicha parasitosis en niños (5 a 9 años) y en adolescentes (10 a 19 años), en ambos casos próxima al 40% y más elevada que en adultos, en los cuales no llegó al 30%.
Para el año 1981, la OMS26 planteaba que la trichocefalosis en las zonas cálidas y húmedas de los países tropicales podía superar el 90%, aunque es frecuente que dicha prevalencia oscile entre el 30 y el 60%. Los resultados de un 32,6% de prevalencia de T. trichiura a nivel nacional, comprendidos en la franja antes mencionada, nos indican que al menos para el momento de la realización del presente estudio, esta parasitosis constiuía un problema aún no resuelto y sin considerar las diferencias del punto de vista estadístico, podemos decir que todos los grupos de edad tienen importancia como contaminadores ambientales, debido a que en todos los grupos etáreos la prevalencia fue superior al 25%.
En el caso de la anquilostomiasis, el haber obtenido una mayor prevalencia en jóvenes y adultos, es coincidente con lo reportado por Anderson et al3 y por Ye, Wu y Sun34, quienes reportaron también una mayor prevalencia e intensidad de la infección por anquilostomideos en los mismos grupos de edad, lo cual podría estar vinculado con el mecanismo de la infección y con las actividades ocupacionales de los afectados7 26 27. Sin embargo, la heterogeneidad de la infección al interior de los grupos de edad12 20 22 30 indica que las estrategias de control deben basarse en los tratamientos selectivos de aquellos individuos más susceptibles por ser ellos los responsables de la mayor contribución a la contaminación ambiental con los huevos de los parásitos2 24 25, además de presentar los mayores riesgos para desarrollar la enfermedad2.
Para finalizar, retomaremos el planteamiento realizado por Botero6, al señalar que en América Latina se han ensayado diversas medidas de control de las parasitosis, que incluyen desde información sobre higiene personal y su relación con la transmisión de los parásitos e instalación de letrinas, hasta tratamientos masivos; sin embargo, los resultados obtenidos han sido insatisfactorios producto de lo esporádico de las medidas, su extensión limitada y ausencia de los cambios necesarios en el modo de vida de las comunidades.
Laboratório de Parasitologia, Instituto de Investigaciones Veterinarias, CENIAP-FONAIAP y División de Endemias Rurales, Ministério de Sanidad y Asistencia Social, Maracay, Edo. Araqua, Venezuela.
Dirección para correspondencia: Dr. Gustavo A. Morales C. Lab. de Parasitologia/Inst. Invest. Veterinarias/CENIAP-FONAIAP. Av. Las Delicias, Maracay, Edo. Aragua, Venezuela.
Fax: 00 58 4 341-9490.
Recebido para publicação em 21/5/98.
- 1. Aguilar C , Dávila I, Pacheco M, Incani R. Parasitología. Servicio de publicaciones de la Facultad de Ciencias de la Salud. Universidad de Carabobo, Valencia Venezuela, 1994.
- 2. Anderson R, May R. Population dynamics of human helminth infections: control by chemotherapic. Nature 297:557-563, 1982.
- 3. Anderson T, Sizza C, Leche G, Scott M, Salomons N. The distribution of intestinal helminth infections in a rural village in Guatemala. Memórias do Instituto Oswaldo Cruz 88:53-65, 1993.
- 4. Booth M, Bundy D. Comparative prevalence of Ascaris lumbricoides, Trichuris trichiura and hookworms infection and the prospect for combined control. Parasitology 105:151-157, 1992.
- 5. Booth M, Bundy D. Estimating the number of multiple species geohelminth infections in human communities. Parasitology 111:645-653, 1995.
- 6. Botero D. Persistencia de parasitosis intestinales endémicas en América latina. Boletín de la Oficina Sanitaria Panamericana 90:39-47, 1981.
- 7. Botero D. Parasitosis de importancia en Colombia. Parasitología al Día 11:27-35, 1987.
- 8. Botero D, Restrepo M. Parasitosis humanas. Corporación para investigaciones biológicas, Medellín, 1992.
- 9. Bundy D. Epidemiological aspects of Trichuris and trichuriasis in Caribean communities. Transactions of the Royal Society of Tropical Medicine and Hygiene 80:706-718, 1986.
- 10. Bundy D, Cooper E. Trichuris and trichiuriasis in humans. Advances in Parasitology 28:107-173, 1989.
- 11. Bundy D, Cooper E, Thompson P, Anderson R, Didier J. Age related prevalence and intensity of Trichuris trichiura infection in a St. Lucian community. Transactions of the Royal Society of Topical Medicine and Hygiene 81:84-115, 1987
- 12. Chourio G. Ecoepidemiología de Ascaris lumbricoides y otros parásitos entéricos en una zona endémica del estado Zulia, Venezuela. Universidad del Zulia, Eac. Exp. de Ciencias, Tésis de Magister Science, 1993.
- 13. Díaz I, Morales G, Pino LA, Chourio G, Calchi M. Eficacia comparada de técnicas coproscópicas empleadas en la determinación de la intensidad geohelmíntica. Kasmera 21:125-151, 1995.
- 14. Gabaldón A. Papel del pediatra en un programa nacional de control de la ascariasis. Archivos venezolanos de puericultura y pediatría 30:215-253, 1967.
- 15. Guyatt H, Bundy D. Estimation of intestinal nematode prevalence: influence of parasite matting patterns. Parasitology 107:99-106, 1993.
- 16. Hómez J, Soto R, de Soto S, Méndez H, Mármol P. Parasitología. Editorial Univeridad del Zulia, Maracaibo, 1989.
- 17. Kilpatrick M, Escamilla J, Barzotti A, Gutierrez W, Paulette E, Bonilla L. Parasitosis intestinales identificadas mediante exámen de heces en tres grupos de población del Perú. Boletín de la Oficina Sanitaria Panamericana 4:412-416, 1986.
- 18. Leger N, Notteghem M, Pesson B. Guide de parasitologie pratique. CDU-Sedes, Paris, 1981.
- 19. Lellouch J, Lazar P. Méthodes statistiques en expérimentation biologique. Flammarion Medecine Sciences, Paris, 1974.
- 20. Loaiza L. Eco-epidemiologia da ascaridíase e sua relaçao com os grupos sanguíneos e tipo de hemoglobina em uma comunidade rural do Estado de Cojedes, Venezuela, Tese Mestre em Medicina. Instituto Oswaldo Cruz, Rio de Janeiro, 1997.
- 21. Ministerio de Sanidad y Asistencia Social. Memoria y Cuenta 1993, Caracas, p. 240-244, 1994.
- 22. Morales G, Pino L. Estrategia de Ascaris lumbricoides y Trichuris trichiura para la contaminación del medio ambiente en una zona endémica. Memórias do Instituto Oswaldo Cruz 83:229-232, 1988.
- 23. Morales G, Pino LA. Parasitometría. Ediciones Universidad de Carabobo, Valencia, Venezuela, 1995.
- 24. Morales G, Pino LA, Chourio G. Epidemiología de Ascaris lumbricoides y su relación con los grupos sanguíneos. Acta Científica Venezolana 45:287-291, 1994.
- 25. Morales G, Pino LA, Chourio G. Contaminación del suelo con huevos de geohelmintos su relación con el sexo y el grupo sanguíneo de los hospedadores. Boletín de la Dirección de Malariología y Saneamiento Ambiental 35:19-24, 1995.
- 26. Organización Mundial de la Salud. Infecciones intestinales por protozoos y helmintos. Serie de Informes técnicos nş 666, Ginebra, 1981.
- 27. Pessoa S, Martins A. Parasitologia Médica. Guanabara Koogan, Rio de Janeiro, 1982.
- 28. Pimentel F. Curso de Estadística experimental. Editorial Hemisferio Sur, Buenos Aires, 1978.
- 30. Pino LA, Morales G, Chourio G, Torres A, Díaz I, Calchi M. Nuevo enfoque para la interpretación de la coproscopía cuantitativa en humanos. Acta Científica venezolana 45:292-295, 1994.
- 31. Ruíz A, Ocampo G, Soto A, José M. El grado de agregación de Ascaris lumbricoides según grupos de edad, después de una intervención antihelmíntica de masas. Salud Pública Mexicana 38:249-256, 1996.
- 31. Ryan B, Joyner B, Ryan T. Minitab. PWS-Kent, Boston, 1985.
- 32. Stepheson L, Latham M, Kinoti S, Kurz K, Brigham H. Improvements in physical fitness of kenyan schoolboys infected with hookworm, Trichuris trichiura and Ascaris lumbricoides following a single dose of albendazole. Transactions of the Royal Society of Tropical Medicine and Hygiene 84:277-282, 1990.
- 33. Torres P, Franjola R, Pérez J, Auad S, Hermosilla C, Flores L, Riquelme J, Salazar S, Miranda J, Montefusco A. Geohelmintosis intestinales en el hombre y animales domésticos de sectores ribereńos de la cuenca del río Valdivia, Chile. Boletin Chileno de Parasitología 50:57-66, 1995.
- 34. Ye X, Wu Z, Sun F. The population biology and control of Necator americanus in a village community in South Eastern China. Annals of Tropical Medicine and Parasitology 88:635-643, 1994.
Fechas de Publicación
-
Publicación en esta colección
13 Jun 2000 -
Fecha del número
Jun 1999
Histórico
-
Recibido
21 Mayo 1998