Resumos
Na Amazônia, as taxas de desmatamento crescem desde 1991 e as previsões não são otimistas quanto à desaceleração desse processo. A devastação da floresta é acompanhada de uma expansão de florestas secundárias (FS) que se estabelecem nas áreas abandonadas. A tendência é um aumento de florestas secundárias, resultando num mosaico de floresta contínua e fragmentos separados por uma matriz de FS. Nesse cenário, autores acreditam que a Amazônia pode passar por um processo massivo de extinção de espécies. Por outro lado, a previsão de um processo massivo de extinção pode ser equivocada, pois muitas espécies florestais poderiam sobreviver nas florestas secundárias. Para avaliar o valor das florestas secundárias para espécies florestais amostramos por oito meses com redes de neblina uma capoeira (FS) em regeneração e uma floresta primária (FP) de uma paisagem fragmentada. Algumas espécies não foram capturadas na capoeira e aparentemente evitam esse tipo de hábitat. No entanto, a maioria das espécies do grupo focal não apresentou diferença na sobrevivência aparente entre os ambientes, o que nos indica que estão habitando a capoeira e a floresta primária da mesma forma. Na realidade amazônica, onde grande parte da matriz é composta por floresta secundária, a matriz tem valor para conservação e deve ser analisada como um elemento dinâmico que não apenas permite a movimentação de indivíduos, mas também serve de hábitat para muitas espécies de floresta primária. Mas ressaltamos que é fundamental a preservação de áreas de floresta primária que servirão de fonte às florestas secundárias adjacentes.
capoeiras; aves; conservação; sobrevivência aparente
Rates of deforestation in the Brazilian Amazon have increased since 1991 and forecasts are not optimistic about the slowing of this process. Some authors believe that the Amazon may be experiencing a massive process of species extinction. However, the deforestation is accompanied by the expansion of secondary forests that are established in the abandoned areas. The trend is an increase in secondary forests cover, resulting in a mosaic of primary forest (FP) and fragments separated by an array of secondary forests (FS). In this scenario, the prediction of a massive extinction could be wrong if many species could survive in the secondary forests. To assess the importance of FS for the understory birds we sampled areas in regeneration and a continuous forest of a fragmented landscape. We conducted mist netting (24 nets/day) for six consecutive days/month, for 8 months (May-November) in 2009. Some forest species as do not seem to be adapted to the secondary forest environment and their occurrences are restricted to continuous forest environments. But most focal species showed no significant difference in apparent survival rates between the enviroments, suggesting that these species inhabit the secondary forest and the primary forest similarly. Because most of the matrix in fragmented landscapes are composed by secondary forests, such results highlights the conservation value that these habitats present in the long term. Thus, FS should be regarded as dynamic matrix that not only allows the movement of individuals but also function as habitat for many species typical of FP.
Secondary forest; apparent survive; avian conservation
ECOLOGIA ANIMAL
Uso de florestas secundárias por aves de sub-bosque em uma paisagem fragmentada na Amazônia central
Use of secondary forests by understory birds in a fragmented landscape in central Amazonia
João Vitor Campos e SilvaI; Beatriz Souza da ConceiçãoII; Marina AnciãesIII
I Projeto Dinâmica Biológica de Fragmentos Florestais (PDBFF), Instituto Nacional de Pesquisas da Amazônia (INPA) e Smithsonian Tropical Research Institute (STRI), Caixa Postal 478, Manaus, AM - 69011-970, Brasil. jvpiedade@gmail.com,
IIProjeto Dinâmica Biológica de Fragmentos Florestais (PDBFF), Instituto Nacional de Pesquisas da Amazônia (INPA) e Smithsonian Tropical Research Institute (STRI), Caixa Postal 478, Manaus, AM - 69011-970, Brasil. eleojeny@yahoo.com.br
IIIInstituto Nacional de Pesquisas da Amazônia (INPA), Av. André Araújo, 2936, Aleixo, CEP 69060-001, Manaus - AM. marina.anciaes@gmail.com
RESUMO
Na Amazônia, as taxas de desmatamento crescem desde 1991 e as previsões não são otimistas quanto à desaceleração desse processo. A devastação da floresta é acompanhada de uma expansão de florestas secundárias (FS) que se estabelecem nas áreas abandonadas. A tendência é um aumento de florestas secundárias, resultando num mosaico de floresta contínua e fragmentos separados por uma matriz de FS. Nesse cenário, autores acreditam que a Amazônia pode passar por um processo massivo de extinção de espécies. Por outro lado, a previsão de um processo massivo de extinção pode ser equivocada, pois muitas espécies florestais poderiam sobreviver nas florestas secundárias. Para avaliar o valor das florestas secundárias para espécies florestais amostramos por oito meses com redes de neblina uma capoeira (FS) em regeneração e uma floresta primária (FP) de uma paisagem fragmentada. Algumas espécies não foram capturadas na capoeira e aparentemente evitam esse tipo de hábitat. No entanto, a maioria das espécies do grupo focal não apresentou diferença na sobrevivência aparente entre os ambientes, o que nos indica que estão habitando a capoeira e a floresta primária da mesma forma. Na realidade amazônica, onde grande parte da matriz é composta por floresta secundária, a matriz tem valor para conservação e deve ser analisada como um elemento dinâmico que não apenas permite a movimentação de indivíduos, mas também serve de hábitat para muitas espécies de floresta primária. Mas ressaltamos que é fundamental a preservação de áreas de floresta primária que servirão de fonte às florestas secundárias adjacentes.
Palavras-chave: capoeiras, aves, conservação, sobrevivência aparente
ABSTRACT
Rates of deforestation in the Brazilian Amazon have increased since 1991 and forecasts are not optimistic about the slowing of this process. Some authors believe that the Amazon may be experiencing a massive process of species extinction. However, the deforestation is accompanied by the expansion of secondary forests that are established in the abandoned areas. The trend is an increase in secondary forests cover, resulting in a mosaic of primary forest (FP) and fragments separated by an array of secondary forests (FS). In this scenario, the prediction of a massive extinction could be wrong if many species could survive in the secondary forests. To assess the importance of FS for the understory birds we sampled areas in regeneration and a continuous forest of a fragmented landscape. We conducted mist netting (24 nets/day) for six consecutive days/month, for 8 months (May-November) in 2009. Some forest species as do not seem to be adapted to the secondary forest environment and their occurrences are restricted to continuous forest environments. But most focal species showed no significant difference in apparent survival rates between the enviroments, suggesting that these species inhabit the secondary forest and the primary forest similarly. Because most of the matrix in fragmented landscapes are composed by secondary forests, such results highlights the conservation value that these habitats present in the long term. Thus, FS should be regarded as dynamic matrix that not only allows the movement of individuals but also function as habitat for many species typical of FP.
Keywords: Secondary forest, apparent survive, avian conservation
INTRODUÇÃO
Na Amazônia brasileira a fragmentação florestal em grande escala se iniciou a partir da década de 70 principalmente, com atividades como queimadas, corte seletivo de madeira, assentamentos e principalmente a agropecuária. O desmatamento vem crescendo consideravelmente desde 1991 e é muito provável que continue aumentando devido à expansão agrícola, rodoviária e pecuária na região (Fearnside 2006). Se o cenário atual de destruição das florestas tropicais for mantido, um processo de extinção em massa é previsto por alguns pesquisadores (Pim e Brooks 2000; Sohdi et al. 2004).
Por outro lado, a devastação das florestas tropicais é acompanhada de uma expansão de florestas secundárias (FS ou capoeiras) que se estabelecem nas áreas abandonadas (Perz e Skole 2003). Segundo algumas previsões, a tendência é um grande aumento da extensão de FS em ambientes tropicais resultando em um grande mosaico de florestas contínuas e fragmentadas separadas por uma matriz de FS (Laurance et al. 2001; Laurance 2006; Wright 2005).
Esse crescente estabelecimento de florestas secundárias em áreas degradadas fez Wright e Muller-Landau (2006a) propor um modelo onde a previsão de uma extinção em massa para os trópicos poderia estar equivocada. Os autores argumentam que a pressão antrópica sobre as florestas tropicais irá diminuir e que as florestas secundárias podem abrigar muitas espécies de floresta primária, atenuando o processo de perda de espécies. A problemática sobre o valor das capoeiras para espécies florestais gerou controvérsias (Brook et al. 2006; Wright e Muller-Landau 2006 a; 2006 b), no entanto, faltam dados empíricos que corroborem com uma argumentação mais conclusiva (Gardner et al. 2007).
Sabe-se que muitas espécies de florestas primárias (FP) ocorrem nas florestas em regeneração, mas a composição de espécies pode demorar muito tempo para ficar equivalente entre os dois ambientes. Além disso, grupos de espécies respondem diferentemente à substituição de uma mata primária por uma capoeira (Dunn 2004; Bowen et al. 2007). Na Amazônia central, nas áreas onde o presente estudo foi conduzido, Borges e Stouffer (1999) capturaram nas florestas secundárias, espécies anilhadas em fragmentos florestais. Cohn-Haft et al (1997) sugere que algumas dessas espécies, características de floresta primária, poderiam estar se locomovendo pelas FS mas não utilizando-as como hábitat Stouffer et al. (2006) verificou que a idade e o histórico da capoeira que circundava os fragmentos florestais foi uma variável importante para a abundância e riqueza de espécies capturadas nos fragmentos. Sberze et al. (2009) não encontrou diferença na riqueza de espécies de aves noturnas entre floresta primária e floresta secundária, os autores mostraram que as florestas secundárias são importantes para corujas, urutaus e bacuraus. Portanto, é evidente que espécies florestais ocorrem nas florestas secundárias. Mas elas estão permanentemente nas FS ou apenas se locomovendo entre manchas de floresta primária?
Com o presente estudo pretendemos contribuir com a problemática do valor das florestas secundárias para espécies florestais de aves de sub-bosque. Amostramos um sítio em floresta primária e outra em uma floresta secundária durante oito meses e verificamos se um grupo de aves de sub-bosque, característico de floresta primária, está realmente habitando a capoeira ou se estão ali apenas de passagem para suprir alguma demanda por recurso, ou para se deslocar entre manchas de hábitat primário. Para testar a hipótese de que as espécies estão apenas se locomovendo pela capoeira estimamos a sobrevivência aparente (1-(mortalidade+emigração)) das espécies, pois na escala temporal deste trabalho uma baixa sobrevivência aparente pode indicar uma baixa fidelidade ao habitat (Parker et al. 2006). Assumindo que a floresta primária é um ambiente de maior qualidade (i.e. alimentos, território), é esperado uma sobrevivência aparente maior quando comparada a um ambiente de baixa qualidade.
Testamos também algumas hipóteses referentes à qualidade de hábitat; Brook et al. (2006) acredita que as florestas secundárias são depauperadas, dominadas por espécies generalistas, já Wright e Muller-Landau (2006a, 2006b) argumentam que as florestas primárias e secundárias podem possuir qualidades semelhantes uma vez que capoeiras, dependendo de sua idade, podem apresentar riqueza e composição de espécies equivalentes às florestas primárias. No caso das aves, a qualidade do hábitat a ser ocupado se relaciona com a idade e classe social dos indivíduos.; machos reprodutivos, por exemplo, tenderiam a se estabelecer em ambientes de maior qualidade, já os jovens podem ser forçados a ocupar ambientes sub-ótimos onde a probabilidade de atração de fêmeas é reduzida (Holmes et al. 1996). Adicionalmente, a sociabilidade e dominância entre indivíduos poderiam levar a manutenção de territórios fixos nos habitat originais (Prum 1994; Durães et al. 2007). Portanto esperamos obter uma sobrevivência aparente de indivíduos jovens mais alta do que a de adultos na floresta secundária.
MATERIAL E MÉTODOS
Área de estudo
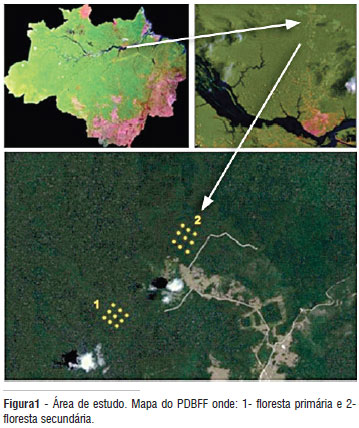
As amostragens foram realizadas nas áreas do Projeto Dinâmica Biológica de Fragmentos Florestais (PDBFF), localizado a 80 km ao norte da cidade de Manaus - AM (lat. 2°30´S, long. 60°W) (Figura 1). O clima da região é do tipo Af de Koppen (Af = Tropical rain forest), com temperatura média de 26 ºC (máxima = 35-39 ºC, mínima = 19-21 ºC) e precipitação anual de 1.900-2.300 mm (estação chuvosa de dezembro a maio; estação seca de junho a novembro). A topografia é ondulada, com latossolos arenosos ou argilosos, pobres em nutrientes(PDBFF, 2010).
O PDBFF foi criado na década de 70 com o objetivo de pesquisar o processo da fragmentação de habitat sobre espécies animais e vegetais (Lovejoy 1986). Há dois históricos diferentes para as florestas secundárias presentes na paisagem; áreas que sofreram apenas o corte originando uma floresta secundária inicialmente dominada por Cecrópia sciadophylla. e áreas que, além do corte, foram submetidas ao fogo, gerando uma floresta dominada inicialmente por Vismia sp. Atualmente, essa dominância não é muito evidente, mas as áreas submetidas somente ao corte possuem uma maior riqueza de espécies devido à baixa alteração no banco de sementes, plântulas remanescentes e rebrotos de espécies. (Mesquita et al. 2001). As grades de amostragem foram preparadas na floresta primária (FP) e em uma floresta secundária (FC) que foi submetida apenas ao corte (Figura 1). Trata-se de uma capoeira com idade estimada em 24 - 28 anos. Possui um dossel mais baixo do que o observado na floresta primária e um sub-bosque mais iluminado. As plantas pioneiras oferecem grande quantidade de recursos alimentares praticamente ao longo do ano todo (Bentos et al. 2008).
Grupo focal
Selecionamos um grupo de espécies de aves que são comprovadamente fáceis de capturar com redes de neblina e que possuem um tamanho de território compatível com o desenho amostral podendo, assim, gerar respostas para as perguntas presentes em nossos objetivos (Tabela 1). São espécies consideradas por Cohn-Haft et al. (1997) características de floresta primária mas que ocorrem nas capoeiras segundo Borges e Stouffer (1999). Algumas espécies presentes nesse grupo não tiveram números de capturas satisfatórios e foram excluídas das análises, outras espécies, que não estavam inicialmente no grupo mas que tiveram alto número de capturas, foram incluídas nas análises.
Desenho amostral
Amostramos duas grades de 400 x 400 m (Figura 2). Uma na floresta primaria e outra na floresta secundária. As amostragens ocorreram de maio a dezembro de 2009; foram oito campanhas, cada campanha tinha duração de seis dias, três dias de amostragem na floresta primária e três dias na floresta secundária. As grades foram montadas a uma distância mínima de 400 m da borda da floresta para evitar possíveis efeitos dessa variável.
Cada grade de amostragem continha 17 pontos amostrais. Em cada ponto era armada uma linha de quatro redes do tipo "mist nets" (36mm de malhas, 12 x 2 m), totalizando 68 redes por campanha. Os 17 pontos amostrais de cada grade eram amostrados em três dias. Em cada campanha os pontos amostrais eram aleatorizados, quando possível, evitando que em cada campanha os pontos fossem amostrados na mesma seqüência.
As redes eram abertas às 06h00 min e fechadas às 14h00 min e eram checadas a cada meia hora. As aves capturadas foram marcadas com anilhas de metal fornecidas pelo Centro Nacional de Pesquisa e Conservação de aves (CEMAVE); a faixa etária foi anotada quando possível e houve coleta de sangue para sexagem de espécies que não apresentam dimorfismo sexual (essa etapa foi realizada em laboratório molecular por equipe de colaboração).
Análises
A sobrevivência aparente dos indivíduos foi estimada no programa MARK 4.3 (White e Burnham 1999). A formulação dos modelos estima os parâmetros p (probabilidade de captura dos animais marcados e não marcados, vivos na ocasião i) e Фi (probabilidade de sobrevivência dos animais marcados e não marcados entre a ocasião i e i+1) (Jolly 1965). Assim, os modelos testados possuem parâmetros p e Ф, cujos valores podem variar ou serem constantes de uma ocasião amostral para outra, ou entre grupos amostrais. O parâmetro Ф é o produto entre a probabilidade de o animal sobreviver entre o intervalo de amostragem, pela fidelidade do animal ao hábitat. A sobrevivência aparente para cada espécie foi considerada significativamente diferente entre os ambientes de FP e FS quando os parâmetros (Ф e p) obtidos para cada ambiente ± seu desvio padrão não foram sobrepostos entre si. Consideramos o modelo nulo como um modelo onde não há efeito dos grupos (hábitat, idade e sexo), ou seja, um modelo onde p e Ф são constantes. Modelamos o efeito do sexo na sobrevivência aparente (Ф) a parte, pois não foram todos os indivíduos que puderam ser sexados, o que gerou um banco de dados diferente.
Os modelos foram comparados através do Critério de Informação de Akaike (AIC) (Williams et al. 2002). O AIC compara os diferentes modelos e através de uma combinação por máxima verossimilhança determina qual modelo melhor explica os dados observados. Quanto menor o AIC mais plausível é o ajuste do modelo aos dados.
O parâmetro Ф também foi modelado como uma função logit do ambiente (FP e FS), Logit (Фi) = α + β(FP), onde α = intercepto da função e β = efeito da FP sobre Ф. Com o valor de β podemos verificar o efeito da floresta primária sobre Ф. O efeito do ambiente FP na sobrevivência aparente (β), foi considerado significativamente positivo ou negativo se os valores obtidos ± seus desvios padrão ficassem respectivamente inteiramente acima ou inteiramente abaixo do limiar zero.
RESULTADOS E DISCUSSÃO
Foram capturadas 76 espécies de aves nos dois hábitat amostrados: 45 espécies na floresta secundária e 65 na floresta primária em um esforço amostral de 10.214,4 horas/redes. As respostas sobre a utilização das florestas secundárias são diferentes para cada grupo de espécie. Algumas aves insetívoras são bastante sensíveis às alterações ambientais e evitam ambientes de floresta secundárias (Stouffer e Bierregaard 1995; Borges e Stouffer 1999; Antongiovani e Metzger 2005). No presente estudo, Cyphorhinus arada, Sclerurus rufigulares, Sclerurus mexicanus, Certhiasomus stictolaemus, Hylexetastes perrotii, Schiffornis turdina, Myrmotherula menetriesii e Myrmotherula longipennis não foram capturadas na floresta secundária. Aparentemente essas espécies evitam as capoeiras ou podem utilizá-la apenas para locomoção entre manchas de hábitat como sugeriu Cohn-Haft et al. (1997).
Embora, para muitas espécies, a taxa de captura seja diferente entre os dois ambientes (Borges e Stouffer 1999), a sobrevivência aparente não apresentou diferença entre os habitat para a maioria das espécies do grupo focal e os modelos mais parcimoniosos foram os nulos (onde p e Ф são constantes). Esse resultado nos indica que essas espécies estão permanecendo na capoeira da mesma forma que na floresta primária. A Tabela 2 mostra os modelos mais parcimoniosos para cada espécie e a Tabela 3 as taxas de captura de cada espécie na Floresta Primária e na Capoeira.
Os bandos mistos se desintegram após a fragmentação, visto que necessitam de grandes áreas para forrageamento (Bierregaard e Lovejoy, 1989); embora sejam sensíveis à alteração do hábitat, os bandos mistos estão presentes nas capoeiras (Borges e Stouffer,1999). No presente estudo, espécies como Xiphorhynchus pardalotus, Thamnomanes ardesiacus e, Thamnomanes caesius, (integrantes do bando misto) foram capturados na capoeira, mas não apresentaram diferença significativa na sobrevivência aparente. Na paisagem em que esse estudo foi conduzido, essas espécies habitam a capoeira da mesma forma que a floresta primária. No entanto, Antongiovani e Metzger (2005) constataram que Thamnomanes ardesiacus forrageava apenas em áreas próximas à floresta primária; os autores atentam que essa espécie pode ser inapta a estabelecer territórios em florestas secundárias distantes da floresta primária. Além disso, a idade das capoeiras, bem como o histórico do uso da terra antes do início da regeneração vegetal também podem ser fatores cruciais para a ocupação e permanência dessas espécies nesses ambientes (Borges e Stouffer 1999; Stouffer et al. 2006).
Para as duas espécies seguidoras de formigas de correição estudadas não encontramos diferença significativa na sobrevivência aparente entre os hábitat. Para Gymnopithys rufigula tanto o hábitat quanto a idade estiverem presentes nos modelos mais plausíveis, já para Pithys albifrons, o tempo foi uma co-variável importante na estimativa da probabilidade de captura (p). Os seguidores de formiga também são espécies consideradas bastante sensíveis à alteração ambiental, sendo as primeiras espécies a desaparecerem dos fragmentos após a fragmentação (Bierregaard e Lovejoy 1989; Canaday 1995; Stouffer e Bierregaard 1995). Essas espécies possuem o hábito de forragear seguindo as formigas de correição e precisam seguir várias colônias de formigas para suprir suas necessidades (Harper 1987); tais formigas possuem período de sedentarismo e períodos migratórios para atender as necessidades fisiológicas da colônia (Schneirla 1971). A biologia das formigas pode explicar o comportamento das aves que as seguem. A ocupação de um determinado hábitat pela ave, bem como sua permanência no local, pode estar fortemente associada com a presença de correições no ambiente e a fase comportamental que a colônia se encontra. As formigas estabelecem colônias em florestas secundárias e em florestas primárias de formas diferentes já que são sensíveis a alteração ambiental (Bierregaard et al. 1992; Roberts et al. 2000). Vieira (2004) observou que as formigas de correição estão presentes em capoeiras velhas (> 20 anos), mas em menor número de colônias quando comparadas a mata primária, e assim diferenças no padrão de uso do hábitat (espacial e temporalmente) por parte das formigas poderiam influenciar diretamente a probabilidade de captura das espécies destas aves em cada ambiente.
A sobrevivência aparente de indivíduos machos e fêmeas nos dois ambientes foi modelada com um subgrupo amostral separado, para o qual havia informação sobre o sexo dos indivíduos obtida através de sexagem molecular. Embora a covarável sexo esteja presente nos modelos mais parcimoniosos de algumas espécies,como Pithys albifrons, Gymnopithys rufigula, Glyphorynchus spirurus e Dixiphia pipra não houve diferença entre a sobrevivência aparente de machos e fêmeas (Figura 3). No cenário estudado machos e fêmeas usam o hábitat da mesma forma. Os modelos mais parcimoniosos estão na Tabela 4.
De uma forma geral, analisando o efeito da floresta primária (β) na sobrevivência aparente, observa-se que para a maioria das espécies não há um efeito significativo, ainda que para algumas espécies exista uma tendência a efeito positivo e para outras uma tendência negativa (Figura 4). Isso indica que cada grupo de espécies responde diferentemente à utilização das florestas secundárias, conforme proposto por Dunn (2004) e Bowen et al. (2007). Existem diferenças estruturais marcantes entre a floresta primária e a floresta secundária (Guariguata e Ostertaga 2001), porém, tais diferenças podem não ser substanciais a ponto de não permitir a ocupação de capoeiras por aves de floresta primária. Com o massivo processo de destruição das florestas tropicais acompanhados do estabelecimento de floresta secundárias nas áreas abandonadas (Wright 2005), as capoeiras podem se tornar elementos fundamentais para a conservação ao fornecer hábitat para espécies de floresta primária.
Em uma paisagem fragmentada, a matriz pode ser um elemento heterogêneo, onde diferentes tipos de habitat se combinam para compor sua qualidade total (Jules e Shahani 2003). Na maioria dos estudos a matriz é considerada um componente estático que pode permitir ou não a movimentação da fauna; uma alusão bastante utilizada é a de que ela teria a função semelhante à de uma membrana semipermeável que permite ou impede o movimento da fauna (Gascon et al. 1999). Todavia, no caso da Amazônia, onde grande parte da matriz é composta por floresta secundária, podemos analisá-la sobre outra perspectiva. Nesse cenário a matriz torna-se um elemento dinâmico, que não apenas permite o deslocamento de organismos, mas que, por servir de hábitat, como verificado em alguns estudos, pode aumentar a distribuição local de algumas espécies características de floresta primária (Borges e Stouffer 1999; Blake e Loiselle 2001; Dunn 2004; Borges 2007; Bowen et al. 2007; Sberze et al. 2009; Dent e Wrigth 2009).
Além disso, a distribuição de uma espécie em um determinado hábitat é uma resposta a uma série de fatores como a estrutura da vegetação, recursos alimentares, locais para nidificação, presença de outras espécies e condições microclimáticas. É comum ocorrer variações nessa gama de fatores, ocasionando uma flutuação nos padrões de ocupação da espécie no hábitat como um todo (Wiens 1989). As florestas secundárias, por possuírem espécies vegetais que frutificam anualmente (Bentos et al. 2008), podem ser bastante importantes para suprir a demanda de recursos alimentares de alguns frugívoros, por exemplo, em épocas que esse recurso for escasso nas manchas de floresta primária. Destacamos que o contexto onde esse estudo foi conduzido é bastante peculiar, pois a grande extensão de floresta contínua presente na paisagem pode servir como fonte de indivíduos para as áreas de capoeira existentes. Numa paisagem onde não há essa fonte de floresta contínua os resultados poderiam ser absolutamente diferentes para algumas espécies. Portanto, é de fundamental importância a existência de áreas de floresta primária na paisagem, para que sirvam de fonte de novos indivíduos para as florestas secundárias.
AGRADECIMENTOS
Agradecemos à equipe do Laboratório de Biologia Evolutiva e comportamental de aves (LABECA), INPA, PDBFF e Rede DB de Hipermercados pelo apoio logístico e financeiro concedido. Ao Gonçalo Ferraz pela grande contribuição em todas as etapas do manuscrito, Mario Cohn-Haft, Erik Johnson, Philip Stouffer, Jared Wolfe, Magalli Henriques e José Luís Camargo pelas sugestões na elaboração do trabalho. Agradecemos também, os amigos que nos ajudaram na coleta de dados: Seu Jairo, Sandra de Freitas, Mariana Tolentino, Gabriela Bochio, Edson Vargas, Ana Carlena, Maria Laura, Izabela Romon, Artur e Nádia Kaster e Ana Andrade. Essa é a publicação de número 572 da série técnica do PDBFF.
BIBLIOGRAFIA CITADA
Recebido em 30/11/2010
Aceito em 24/03/2011
- Antongiovanni, M.; Metzger, J.P. 2005. Influence of matrix habitats on the occurrence of insectivorous bird species in Amazonian forest fragments. Biological Conservation, 122: 441-451.
- Bentos, T.V.; Mesquita, R.C.G.; Williamson, G.B. 2008. Reproductive Phenlogy of Central Amazon Pioneer Trees. Tropical Conservation Science, 1: 186-203.
- Blake, J.G.; Loiselle, B.A. 2001. Variation in Resource Abundance Affects Capture Rates of Birds in Three Lowland Habitats in Costa Rica. The Auk, 108: 114-130.
- Bierregaard, R.O.; Loveojoy, T.E. 1989. Effects of fragmentation on amazonian understory bird communities. Acta Amazônica, 19: 215- 241.
- Bierregaard, R.O.Jr.; Lovejoy, T.E.; Kapos. V.; dos Santos, A.A.; Hutchings, R.W. 1992. The biological dynamics of tropical rainforest fragments. BioScience, 42: 859-866.
- Borges, S.H.; Stouffer, P.C. 1999. Bird communities in two types of anthropogenic successional vegetation in Central Amazônia. Condor, 101: 529-536.
- Borges, S.H. 2007. Bird assemblages in secondary forests developing after slash-and-burn agriculture in the brazilian amazon. Journal of Tropical Ecology, 23: 469-477.
- Bowen, M.E.; Mcalpine, C.A.; House, A.P.N.; Smith, G.C. 2007. Regrowth forests on abandoned agricultural land: A review of their habitat values for recovering forest fauna. Biological Conservation, 140: 273-296.
- Brook, B.W.; Bradshaw, C.J.A.; Koh, L.P.; Sodhi, N.S. 2006. Momentum drives the crash: mass extinction in the tropics. Biotropica, 38: 302-305.
- Canaday, C. 1995. Loss of insectivorous birds along a gradient of human impact in Amazonia. Biological Conservation, 77: 63-77.
- Cohn-Haft, M; Whittaker, A.; Stouffer, P.C. 1997. A new look at the "species-poor" central Amazon: the avifauna North of Manaus, Brazil. Ornithological Monographs. 48: 205-236.
- Dent, D.H.; Wright, J.S. 2009. The future of tropical species in secondary forests: A quantitative review. Biological Conservation, doi:10.1016/j.biocon.05.035.
- Dunn, R. R. 2004. Recovery of faunal communities during tropical forest regeneration. Conservation Biology, 18: 302-309.
- Durães R.; Loiselle, B.A. ; Blake, J.G. 2007. Intersexual spatial relationships in a lekking species: blue-crowned manakins and female hot spots. Behavioral Ecology, 18:1029-1039.
- Fearnside, P.M. 2006. Deforestation in Amazon: Dynamics, impacts and control. Acta Amazonica, 36(3): 395-400.(In Portuguese, with abstract in English).
- Gardner, T.A.; Barlow, J.; Parry, L.W.; Peres, C.A. 2007. Predicting the uncertain future of tropical Forest species in a data vacuum. Biotropica, 39: 25-30.
- Gascon, C.; Lovejoy, T.E.; Bierregaard, R.O.; Malcom, J.R.; Stouffer, P.C; Vasconcelos, H.L.; Laurence, W.F.; Zimmerman, B.; Tocher, M.; Borges, S. 1999. Matrix habitat and species richness in tropical forest remnants. Biological Conservation, 91: 223-230.
- Guariguata. M.R.; Ostertaga, R. 2001. Neotropical secondary forest succession: Changes in structural e functional characteristics. Forest Ecology and Management. 148: 185-206.
- Harper, L.H. 1987. The conservation of ant-fllowing birds is small Amazonian forest Fragments. Acta Amazonica.19:249-243
- Holmes, R.T.; Marra, P.P.; Sherry, T.W. 1996. Habitat-specific demography of breeding Blackthroated Blue Warblers (Dendroica caerulescens): Implications for population dynamics. Journal of Animal Ecology, 65: 183-195.
- Jolly G.M. 1965. Explicit estimates from capture-recapture data with both death and immigration - stochastic model. Biometrika, 52: 225-247.
- Jules, E. S.; Shahani P. 2003. A broader ecological context to habitat fragmentation: Why matrix habitat is more important than we thought. Journal of Vegetative Science 14: 459-464.
- Laurance, W.F.; Cochrane, M.A.; Bergen, S.; Fearnside, P.M.; Delamônica, P.; Barber, C.; D'Angelo, S.; Fernades, T. 2001. The future of the Brazilian Amazon. Science, 291: 438-439.
- Laurance, W. F. 2006. Have we overstated the tropical biodiversity crisis? Trends in Ecology and Evolution, 22(2): 65-70.
- Lovejoy, T.E. 1986. Edge and other effects of isolation on Amazon forest fragments. in M. E. Soul´e, editor. Conservation biology: the science of scarcity and diversity Sinauer, Sunderland, Massachusetts.p 257-285.
- Mesquita, R.C.G.; Ickes, K.; Ganade, G.; Williamson, G.B. 2001. Alternative successional pathways in the amazon basin. Journal of Ecololgy, 89: 528-537.
- Parker, T.H.; Becker, C.D.; Sandercock, B.K.; Agreda, A.E. 2006. Apparente Survival Estimates for Five Species of Tropical birds in an Endangered Forest Habitat in Western Ecuador. Biotropica, 38(6): 764-769.
- PDBFF, 21010. Área de estudo, (http://www.inpa.gov.br/pdbff/). Acesso em 20/08/2009.
- Perz, S. G., Skole, D. L. 2003. Secondary Forest Expansion in the Brazilian Amazon and the Refinement of Forest Transition Theory. Society and Natural Resources, 16: 277-294.
- Pimm, S.L.; Brooks, T.M. 2000. The Sixth Extinction: How large, how soon, and where? In: Raven, P. (Ed). Nature and Human Society: the quest for a sustainable world. National Academy Press, Washington, DC. p 46-62.
- Prum, R.O.1994. Phylogenetic analysis of the evolution of alternative social behavior in the Manakins (Aves: Pipridae). Evolution, 48(5): 1657-1675.
- Roberts, D.L.; Cooper, R.J.; Petit, L.J. 2000. Use of premontane moist forest and shade coffee agroecosystems by army ants in western Panama. Conservation Biology, 14: 192-199.
- Sberze, M. R.; Cohn-haft, M.; Ferraz, G. 2009. Old-growth and secondary-forest site occupancy by nocturnal birds in a Neotropical landscape. Animal Conservation, 13(1):3-11.
- Schneirla, T. C. 1971. Army Ants: A study in social organization. W.H. Freeman and company, San Francisco, CA, USA. 349pp.
- Sohdi, N.S.; Koh, L.P.; Brook, B.W.; Ng, P.K.L. 2004. Southeast Asia biodiversity: an impending disaster. Trends in Ecology and Evolution, 19: 654-660.
- Stouffer, P.C.; Bierregaard Jr; R.O. 1995. Use of Amazonian Forest fragments by Understory Insectivorous Birds. Ecology, 76 (8) 2429-2445.
- Stouffer, P.C.; Bierregaard Jr; R.O.; Strong, C.; Lovejoy, T. E. 2006. Long-Term Landscape Change and Bird Abundance in Amazonian Rainforest Fragments. Conservation Biology, 20: 1212-1223.
- Vieira, R. S. 2004. Effect of Forest Fragmentation on butterflies (Lepidoptera, Hesperiidae) associated with army ants Eciton burchelli (Hymenoptera, Formicidae, Ecitoninae) Tese de doutorado, Universidade Federal de São Carlos, São Carlos, São Paulo. 166 pp. (In Portuguese)
- White G.C.; Burnham K.P. 1999. Program Mark: survival estimations from population of marked individuals. Bird Study, 46: 120-138.
- Wiens, J.A. 1989. The ecology of birds communities:foundations and patterns. Cambridge University Press, Cambridge, 539 pp.
- Williams, B.K.; Nichols, J.D.; Conroy, M.J. 2002. Analysis and management of Animal populations, Academic press. San Diego. 817pp.
- Wright, S.J. 2005. Tropical forests in a changing environment. Trends in Ecology and Evolution, 20: 553-560.
- Wright, S.J.; Muller-Landau, H.C. 2006a. The future of tropical Forest species. Biotropica, 38: 287-301.
- Wright, S.J.; Muller-Landau, H.C. 2006b. The uncertain future of tropical Forest species, Biotropica, 38: 443-445.
Datas de Publicação
-
Publicação nesta coleção
09 Jan 2012 -
Data do Fascículo
Mar 2012
Histórico
-
Recebido
30 Nov 2010 -
Aceito
24 Mar 2011