Resumos
FUNDAMENTO: Estudos prévios demonstraram que a leucocitose e a hiperglicemia verificadas à admissão de pacientes com IAM (infarto agudo do miocárdio), estão correlacionadas com a mortalidade intra-hospitalar. Entretanto, pouco é sabido sobre o impacto desses marcadores a longo prazo. OBJETIVO: Avaliar a curto e longo prazos, a influência dos níveis de glicose e leucócitos no prognóstico de pacientes com IAM. MÉTODOS: Foram analisados, retrospectivamente, 809 pacientes (idade média 63,2 ± 12,87 anos) com IAM, incluídos de forma prospectiva e consecutiva em banco de dados específico. RESULTADOS: a) Na fase intra-hospitalar os valores médios aferidos foram comparados entre pacientes que morreram ou sobreviveram: Leucocitose 12156±5977 vs 10337±3528 (p=0.004, 95% IC= 976-2663); Glicose 176±105 mg/dl vs 140±72 mg/dl (p<0.001, 95% IC= 19.4 - 52.6), respectivamente. b) No modo ajustado, o mesmo padrão foi verificado [valores de p: 0.002 (t-ratio 3.05), 0.04 (t-ratio 2.06), respectivamente]. c) Seguimento a longo prazo: a análise univariada revelou valores de P de 0.001 (t-ratio 3.3), <0.001 (t-ratio 4.16), respectivamente. Pela análise multivariada; P=0.001 (t-ratio 3,35), 0.08 (t-ratio 1,75), respectivamente. d) Após exclusão das mortes intra-hospitalares, os níveis leucocitários (P=0.989) e a glicemia (P=0.144) não permaneceram correlacionadas significativamente com mortalidade. O mesmo resultado foi verificado na análise multivariada. CONCLUSÃO: Níveis de leucócitos e glicemia à admissão de pacientes com IAM são excelentes preditores de mortalidade intra-hospitalar, e pobres preditores de óbitos a longo prazo.
Leucocitose; glucose; infarto do miocárdio
FUNDAMENTO: Estudios previos demostraron que tanto la leucocitosis como la hiperglucemia verificadas cuando de la admisión de pacientes con infarto agudo de miocardio (IAM), están correlacionadas con la mortalidad intrahospitalaria. Sin embargo, poco se sabe acerca del impacto de esos marcadores a largo plazo. OBJETIVO: Evaluar, a corto y largo plazos, la influencia de los niveles de glucosa y leucocitos en el pronóstico de pacientes con IAM. MÉTODOS: Se analizaron, retrospectivamente, a 809 pacientes (edad promedio 63,2 ± 12,87 años) con IAM, incluidos de forma prospectiva y consecutiva en banco de datos específico. RESULTADOS: a) En la fase intrahospitalaria se compararon los valores promedio obtenidos entre pacientes que murieron o supervivieron: leucocitosis 12.156±5.977 vs 10.337±3.528 (p=0.004, 95% IC= 976-2663); glucosa 176±105 mg/dl vs 140±72 mg/dl (p<0.001, 95% IC= 19.4 - 52.6), respectivamente. b) En el modo ajustado, se verificó el mismo estándar [valores de p: 0.002 (t-ratio 3.05), 0.04 (t-ratio 2.06), respectivamente]. c) Seguimiento a largo plazo: el análisis univariado reveló valores de P de 0.001 (t-ratio 3.3), <0.001 (t-ratio 4.16), respectivamente. Ya el análisis multivariado: P=0.001 (t-ratio 3,35), 0.08 (t-ratio 1,75), respectivamente. d) Tras la exclusión de las muertes intrahospitalarias, los niveles leucocitarios (P=0.989) y la glucemia (P=0.144) no permanecieron correlacionadas significativamente con la mortalidad. Igual resultado se verificó en el análisis multivariado. CONCLUSIÓN: Los niveles de leucocitos y glucemia al ingreso de pacientes con IAM resultan excelentes predictores de mortalidad intrahospitalaria, y pobres predictores de óbitos a largo plazo.
Leucocitosis; glucosa; infarto de miocardio
BACKGROUND: Previous studies have demonstrated that leukocytosis and hyperglycemia verified at the admission of patients with acute myocardial infarction (AMI) are associated with intrahospital mortality. However, little is known on the long-term impact of these markers. OBJECTIVE: To evaluate the short-and long-term influence of the levels of glucose and leukocytes on the prognosis of patients with AMI. METHODS: A total of 809 patients with AMI were retrospectively assessed (mean age: 63.2 ± 12.87 yrs) and prospectively and consecutively included in a specific database. RESULTS: a) At the intrahospital phase, the mean values were compared between patients that died and those who survived: Leukocytosis: 12156±5977 vs 10337±3528 (p=0.004, 95%CI = 976-2663); Glucose 176±105 mg/dl vs 140±72 mg/dl (p<0.001, 95%CI = 19.4 - 52.6), respectively. b) With the adjusted mode, the same pattern was observed [p values: 0.002 (t-ratio 3.05), 0.04 (t-ratio 2.06), respectively]. c) Long-term follow-up: the univariate analysis showed P values of 0.001 (t-ratio 3.3), <0.001 (t-ratio 4.16), respectively. The multivariate analysis showed P=0.001 (t-ratio 3.35), 0.08 (t-ratio 1.75), respectively. (d) After the exclusion of the intrahospital deaths, the leukocyte (P=0.989) and glucose levels (P=0.144) did not remain significantly correlated with mortality. The same result was observed at the multivariate analysis. CONCLUSION: The levels of glucose and leukocytes at the hospital admission of patients with AMI are excellent predictors of intrahospital mortality and poor predictors of long-term death.
Leukocytosis; glucose; myocardial infarction
ARTIGO ORIGINAL
CORONARIOPATIA AGUDA
Influência de leucócitos e glicemia no prognóstico de pacientes com infarto agudo do miocárdio
Antonio Eduardo P. Pesaro; Jose Carlos Nicolau; Carlos V. Serrano Jr.; Rodrigo Truffa; Marcus Vinicius B. Gaz; Ralf Karbstein; Roberto R. Giraldez; Roberto Kalil Filho; José A. Ramires
Instituto do Coração, Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo (HCFMUSP), São Paulo, SP - Brasil
Correspondência Correspondência: Antonio Eduardo Pereira Pesaro Rua Carlos Millan, 22 / 141, J Paulistano 01456-030 - São Paulo, SP - Brasil E-mail: eduardopesaro@hotmail.com
RESUMO
FUNDAMENTO: Estudos prévios demonstraram que a leucocitose e a hiperglicemia verificadas à admissão de pacientes com IAM (infarto agudo do miocárdio), estão correlacionadas com a mortalidade intra-hospitalar. Entretanto, pouco é sabido sobre o impacto desses marcadores a longo prazo.
OBJETIVO: Avaliar a curto e longo prazos, a influência dos níveis de glicose e leucócitos no prognóstico de pacientes com IAM.
MÉTODOS: Foram analisados, retrospectivamente, 809 pacientes (idade média 63,2 ± 12,87 anos) com IAM, incluídos de forma prospectiva e consecutiva em banco de dados específico.
RESULTADOS: a) Na fase intra-hospitalar os valores médios aferidos foram comparados entre pacientes que morreram ou sobreviveram: Leucocitose 12156±5977 vs 10337±3528 (p=0.004, 95% IC= 976-2663); Glicose 176±105 mg/dl vs 140±72 mg/dl (p<0.001, 95% IC= 19.4 - 52.6), respectivamente. b) No modo ajustado, o mesmo padrão foi verificado [valores de p: 0.002 (t-ratio 3.05), 0.04 (t-ratio 2.06), respectivamente]. c) Seguimento a longo prazo: a análise univariada revelou valores de P de 0.001 (t-ratio 3.3), <0.001 (t-ratio 4.16), respectivamente. Pela análise multivariada; P=0.001 (t-ratio 3,35), 0.08 (t-ratio 1,75), respectivamente. d) Após exclusão das mortes intra-hospitalares, os níveis leucocitários (P=0.989) e a glicemia (P=0.144) não permaneceram correlacionadas significativamente com mortalidade. O mesmo resultado foi verificado na análise multivariada.
CONCLUSÃO: Níveis de leucócitos e glicemia à admissão de pacientes com IAM são excelentes preditores de mortalidade intra-hospitalar, e pobres preditores de óbitos a longo prazo.
Palavras-chave: Leucocitose, glucose, infarto do miocárdio.
Introdução
Pacientes com síndromes isquêmicas miocárdicas instáveis (SIMI) devem ser rotineiramente submetidos a estratificação de risco quando da chegada ao hospital. A função dessa estratificação precoce é determinar o risco e o prognóstico desses pacientes, o que permite orientar mais adequadamente a terapêutica e o seguimento clínico dos mesmos. Nesse sentido, a classificação de Braunwald1 e os escores de risco publicados pelo grupo TIMI (Thrombolysis In Myocardial Infarction)2,3, tanto para SIMI sem supradesnível do segmento ST (no ECG) quanto para infarto agudo do miocárdio com supradesnível de ST vêm sendo amplamente utilizados para estratificação precoce. No entanto, outros marcadores de risco têm sido investigados na tentativa de tornar essa avaliação prognóstica mais precisa a curto e longo prazos. Estudos prévios demonstraram que a leucocitose e a hiperglicemia verificadas à admissão de pacientes com IAM, estão correlacionadas com a mortalidade intra-hospitalar4-7. Entretanto, pouco é sabido sobre o impacto desses marcadores a longo prazo.
Assim, o propósito principal deste estudo foi avaliar a influência dos níveis de glicose e leucócitos no prognóstico a curto e longo prazos de pacientes com IAM, e comparar o impacto desses "novos" marcadores em relação a marcadores "tradicionais", como fração de ejeção ventricular esquerda e idade.
Métodos
Trata-se de um estudo unicêntrico, onde todos os pacientes foram selecionados em uma unidade coronária de terapia intensiva. Foram analisados, retrospectivamente, 809 pacientes (idade média 63,2 ± 12,87 anos) com IAM, incluídos de forma prospectiva e consecutiva em banco de dados específico entre fevereiro de 1998 e julho de 2005. Os critérios utilizados para o diagnóstico de IAM foram: Curva de troponina ou creatinoquinase fração MB - CK-MB associado a ao menos um dos seguintes: sintomas isquêmicos, desenvolvimento de ondas Q patológicas no eletrocardiograma (ECG), alterações eletrocardiográficas indicativas de isquemia (elevação ou depressão de ST) ou pós intervenção coronária.
Os pacientes foram seguidos por até 6,4 anos (tempo médio de sobrevida 5,15 anos), com avaliações prospectivas anuais em relação à mortalidade. O seguimento da população foi realizado anualmente por telefone ou entrevista pessoal. Os pacientes (ou familiares) eram contatados por telefone, visitas ao consultório, ou busca ativa pessoal (procura pessoal em locais de trabalho, residência, vizinhos, etc).
Foram analisados os valores das primeiras dosagens de leucócitos e glicemia, em relação ao prognóstico intra-hospitalar e a longo prazo. A coleta de sangue para dosagem de glicemia e leucocitose foi efetuada no momento da chegada do paciente ao hospital.
Nos modelos ajustados, as seguintes variáveis foram consideradas: História de angioplastia, cirurgia de revascularização do miocárdio, infarto do miocárdio, diabetes, tabagismo, antecedente de insuficiência cardíaca (IC), idade, sexo, freqüência cardíaca, pressão arterial sistólica, supradesnível do segmento ST, glicemia, leucócitos, fração de ejeção (primeiro ecocardiograma; método de Simpson), presença de fibrinólise e angioplastia primária. Para a fase intra-hospitalar, o teste t de student ou teste de Kruskal-Wallis (análises univariadas) e regressão logística (análise multivariada) foram aplicados. Nas análises de longo prazo foi aplicado o teste de Cox ("Cox proportional hazards estimation"). O método step wise8 (com 0,10 de entrada e 0,10 de saída), foi utilizado para a análise de regressão logística.
Resultados
A. População do estudo
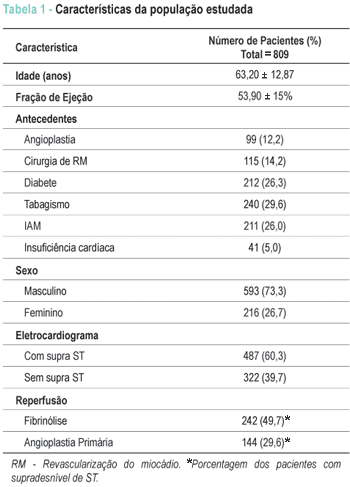
Os dados em relação à população estudada estão na tabela 1.
B. Fase intra-hospitalar
Na fase intra-hospitalar, 92 pacientes (11,37%) faleceram. O tempo médio para o óbito foi de 94 horas (95% IC; 60,90-127,0). Os valores médios aferidos para as variáveis foram comparados entre pacientes que faleceram ou sobreviveram: Leucocitose 12156±5977 vs 10337±3528 (p=0.004, 95% IC= 976-2663); Glicose 176±105 mg/dl vs 140±72 mg/dl (p<0.001, 95% IC= 19.40 - 52.60), respectivamente. Como se pode notar, as duas variáveis analisadas se correlacionaram de forma significativa com o pior prognóstico.
A tabela 2 demonstra os resultados do modelo multivariado. Após análise de regressão logística de 16 variáveis, através do modelo step wise (com 0,10 de entrada e 0,10 de saída), observou-se que apenas 5 variáveis se correlacionaram de forma significativa e independente com mortalidade intra-hospitalar: glicemia, leucócitos, idade, fração de ejeção e pressão arterial sistólica.
C. Seguimento tardio
C.1. População global
Na fase extra-hospitalar houve 94 mortes adicionais. A probabilidade de sobrevivência global foi de 77% (Kaplan-Mayer). Em relação ao seguimento a longo prazo, levando-se em conta a totalidade dos pacientes, demonstra-se correlações significativas entre glicemia e leucócitos, com a mortalidade como se nota na Tabela 3.
Na Tabela 4 demonstra-se que, no modelo multivariado, seis variáveis analisadas permanecem como fatores prognósticos na evolução a longo prazo na população global. Entretanto a glicemia apresentou apenas uma tendência de correlação com mortalidade.
C.2. Pacientes sobreviventes à fase intra-hospitalar
Como se nota na Tabela 5, ao excluírem-se os óbitos hospitalares, leucócitos e glicemia deixam de se correlacionar com evolução a longo prazo. Em outras palavras, o valor prognóstico dos valores de leucócitos e glicemia se restringe à fase intra-hospitalar, não apresentando qualquer impacto após a alta hospitalar. Tal comportamento não se modifica nos modelos ajustados, como se nota na Tabela 6, onde apenas história de IC, idade e fração de ejeção correlacionam-se com a mortalidade.
Discussão
Nas últimas três décadas, o tratamento do IAM avançou significativamente, o que resultou na redução da morbi-mortalidade relacionada à doença9. Isso ocorreu principalmente em virtude de novas estratégias de reperfusão primária farmacológica e mecânica, anti-agregação múltipla, além da ampla utilização da estratificação invasiva e da possibilidade de revascularização com angioplastia e stents10. Entretanto, pacientes com SIMI têm características diferentes, o que determina que seu risco e prognóstico sejam variáveis. Alguns desses pacientes beneficiam-se de medidas terapêuticas agressivas, como por exemplo abordagem invasiva percutânea e controle rígido da glicemia11,12.
Nesse sentido, identificar pacientes de maior risco tem sido uma preocupação constante na literatura. Além dos estudos para validação de escores de risco e de variáveis tradicionalmente associadas a mau prognóstico como idade e disfunção ventricular esquerda, investigadores atuaram recentemente na identificação de novas variáveis prognósticas, como marcadores inflamatórios, peptídeo natriurético, leucocitose e hiperglicemia, entre outros12-15.
Os diabéticos são reconhecidos como pacientes de risco elevado e pior prognóstico a curto e longo prazo após IAM. No registro MONICA, a mortalidade para infartados diabéticos ou não diabéticos, aos 28 dias de evolução, foi, respectivamente, 12.6% e 7.3%16. Dessa maneira, justifica-se a inclusão do diabetes mellitus na estratificação precoce de risco.
Entretanto, a presença de hiperglicemia foi identificada como fator de mau prognóstico também em infartados não diabéticos17-19. Recentemente, demonstrou-se que a hiperglicemia continua sendo um fator de mau prognóstico também em pacientes submetidos a intervenção coronária percutânea, independentemente da presença de diabetes20. Também se verificou nesse e em outros estudos21,22, que há associação entre hiperglicemia, fenômeno de no-reflow e remodelamento ventricular, reconhecidos fatores de gravidade e pior prognóstico na evolução de pacientes com IAM23.
Da mesma forma, outro estudo demonstrou que a hiperglicemia, mas não o diabetes, foi fator de mau prognóstico intra-hospitalar24. Em relação ao seguimento a longo prazo, estudos prévios demonstraram que a hiperglicemia, independente da presença de diabetes, também foi um fator de risco para mortalidade em pacientes com IAM25-27.
Em nosso estudo, encontramos dados semelhantes àqueles encontrados por outros autores em relação à influência da glicemia na mortalidade. A glicemia na admissão hospitalar foi significativamente maior nos pacientes que faleceram durante a internação. Durante o seguimento de mais de seis anos, a hiperglicemia persistiu como fator de mau prognóstico, apesar de haver, no modelo ajustado, apenas uma tendência a pior mortalidade. Entretanto, após exclusão dos óbitos intra-hospitalares, as variáveis idade, fração de ejeção (FE) e história de IC permaneceram correlacionadas significativamente com mortalidade, mas não os níveis leucocitários ou a glicemia. Este dado pode ser relacionado à hipótese de que a hiperglicemia não seja apenas um marcador prognóstico, mas um agressor direto do sistema cardiovascular na fase aguda do IAM.
Estudos experimentais demonstraram que a hiperglicemia é capaz de promover trombose plaquetária, incrementar a circulação de moléculas de adesão leucocitária e reduzir a vasodilatação dependente de endotélio, a disponibilidade de óxido nítrico e o fluxo de circulação coronariana colateral28-31. A redução de óxido nítrico e prostaciclina, ou mesmo a elevação de vasoconstrictores como a endotelina, são favorecidos pela hiperglicemia por meio da ativação da proteína quinase C, da elevação de hexosamina e da ativação do fator nuclear pro-inflamatório Kappa B com formação conseqüente de radicais superóxidos32. Um estudo que induziu diabete em suínos demonstrou elevação de IL-6, fator de necrose tumoral (TNF), proteínas quimiotáticas de macrófagos e de moléculas de adesão em fibroblastos da adventícia coronariana33.
Em relação à leucocitose, alguns estudos exploraram seu valor prognóstico no IAM34. Um dos mais relevantes incluiu a leucocitose como parte de um escore de risco para pacientes com infarto34. Nesse estudo, homens com leucócitos acima 9.000/microL apresentaram risco relativo de morte de 1,66 (1,35 - 2,05) no seguimento de quatro anos. Recentemente, a leucocitose em pacientes com IAM foi associada diretamente com o tamanho da área de infarto, presença de choque e morte em seis meses34. Em outro estudo, pacientes com leucócitos acima de 10,000/microL durante IAM apresentaram maior incidência de fluxo TIMI 0-1, eventos cardiovasculares adversos intra-hospitalares e também ao longo de cinco anos, em comparação com pacientes com leucócitos abaixo dessa faixa35. A elevação de neutrófilos também foi associada tanto ao tratamento tardio, à presença de artéria ocluída, quanto à reduzida reperfusão em pacientes com IAM36. Quando comparado com outros marcadores inflamatórios, a elevação dos níveis de leucócitos foi um preditor de eventos adversos semelhante à proteína C reativa e melhor do que o amiloide sérico A, fibrinogênio e interleucina-6, ao longo de cinco anos após IAM37.
Em nosso estudo a leucocitose foi associada a pior prognóstico intra-hospitalar, mesmo em modelos ajustados. Porém, assim como ocorreu com a hiperglicemia, no seguimento a longo prazo quando excluídos óbitos intra-hospitalares, a leucocitose deixou de ser marcador de mau prognóstico a longo prazo. O maior impacto desse marcador na fase aguda do IAM, pode ser justificado pela associação da leucocitose com estados inflamatórios agudos mais acentuados, presença de isquemia mais importante e dificuldade de reperfusão, como referido anteriormente36,37.
Finalmente, salienta-se que, apesar de haver evidências de que o controle adequado da glicemia na fase aguda do IAM é benéfico11,38, em muitas instituições o controle cuidadoso da hiperglicemia é negligenciado. Por outro lado, tentativas de controle do processo inflamatório têm sido reportadas com resultados conflitantes na literatura39. Apesar de um pequeno estudo apontar inicialmente para um possível benefício do uso de anti-inflamatórios nas SIMI40, o excesso de eventos cardiovasculares associados ao uso de anti-inflamatórios não hormonais em diversos estudos randomizados desfavoreceu a utilização dessa terapêutica41. O controle da inflamação também foi investigado a partir da utilização das estatinas nas SIMI. Nos últimos anos, os efeitos pleiotrópicos desses fármacos foram extensamente investigados, com destaque para a ação anti-inflamatória. Neste sentido, um estudo recente demonstrou a eficiência da redução de proteína C reativa e LDL colesterol em pacientes com SIMI, com a utilização de altas doses de atorvastatina. Além disso, houve um benefício cardiovascular adicional no grupo de pacientes com maior redução inflamatória42-44.
Em conclusão, níveis de leucócitos e glicemia à admissão de pacientes com IAM são excelentes preditores de mortalidade intra-hospitalar, e pobres preditores de óbitos a longo prazo. História prévia de IC foi preditor indepentente de mortalidade apenas a longo prazo. Por outro lado, idade e FE são preditores independentes de mortalidade a curto e longo prazos.
Potencial Conflito de Interesses
Declaro não haver conflito de interesses pertinentes.
Fontes de Financiamento
O presente estudo não teve fontes de financiamento externas.
Vinculação Acadêmica
Não há vinculação deste estudo a programas de pós-graduação.
Artigo recebido em 23/10/07; revisado recebido em 14/04/08; aceito em 09/06/08.
- 1. Braunwald E, Antman EM, Beasley JW, Califf RW, Cheitlin MD, Hochman JS, et al. American College of Cardiology/American Heart Association task force on practice guidelines. ACC/AHA 2002 guideline update for the management of patients with unstable angina and non-ST-segment elevation myocardial infarction-summary article: a report of the J Am Coll Cardiol. 2002; 40: 1366-74.
- 2. Antman EM, Cohen M, Bernink PJ, McCabe CH, Horacek T, Papuchis G, et al. The TIMI risk score for unstable angina/non ST elevation MI: a method for prognostication and therapeutic decision making. JAMA. 2000; 284: 835-42.
- 3. Morrow DA, Antman EM, Charlesworth A, Cairns R, Murphy SA, de Lemos JA, et al. TIMI risk score for ST-elevation myocardial infarction: a convenient, bedside, clinical score for risk assessment at presentation: an intravenous nPA for treatment of infarcting myocardium early II trial substudy. Circulation. 2000; 102: 2031-7.
- 4. Bellodi G, Manicardi V, Malavasi V, Veneri L, Bernini G, Bossini P, et al. Hyperglycemia and prognosis of acute myocardial infarction in patients without diabetes mellitus. Am J Cardiol. 1989; 64: 885-8.
- 5. O'Sullivan JJ, Conroy RM, Robinson K, Hickey N, Mulcahy R. In-hospital prognosis of patients with fasting hyperglycemia after first myocardial infarction. Diabetes Care. 1991; 14: 758-60.
- 6. Afiune Neto A, Mansur AP, Avakian SD, Gomes EP, Ramires JA. Monocytosis is an independent risk marker for coronary artery disease. Arq Bras Cardiol. 2006; 86: 240-4.
- 7. Goyal A, Mahaffey KW, Garg J, Nicolau JC, Hochman JS, Weaver WD, et al. Prognostic significance of the change in glucose level in the first 24 h after acute myocardial infarction: results from the CARDINAL study. Eur Heart J. 2006; 27: 1289-97.
- 8. Bendel RB, Afifi AA. Comparison of stopping rules in forward "stepwise" regression. J Am Stat Assoc. 1977; 72: 46-53.
- 9. Hasdai D, Behar S, Wallentin L, Danchin N, Gitt AK, Boersma E, et al. A prospective survey of the characteristics, treatments and outcomes of patients with acute coronary syndromes in Europe and the Mediterranean basin. The Euro Heart Survey of Acute Coronary Syndromes (Euro Heart Survey ACS). Eur Heart J. 2002; 15: 1190-201.
- 10. Van de Werf F, Ardissino D, Betriu A, Cokkinos DV, Falk E, Fox KA, et al. Management of acute myocardial infarction in patients presenting with ST-segment elevation. ESC task-force report. Eur Heart J. 2003; 24: 28-66.
- 11. Cannon CP, Weintraub WS, Demopoulos LA, Vicari R, Frey MJ, Lakkis N, et al. TACTICS (Treat Angina with Agrastat and Determine Cost of Therapy with an Invasive or Conservative Strategy)-Thrombolysis in myocardial infarction 18 investigators. Comparison of early invasive and conservative strategies in patients with unstable coronary syndromes treated with the glycoprotein IIb/IIIa inhibitor tirofiban. N Engl J Med. 2001; 344: 1879-87.
- 12. Malmberg K, Ryden L, Efendic S, Herlitz J, Nicol P, Waldenstrom A, et al. Randomized trial of insulin-glucose infusion followed by subcutaneous insulin treatment in diabetic patients with acute myocardial infarction (DIGAMI study): effects on mortality at 1 year. J Am Coll Cardiol. 1995; 26: 57-65.
- 13. Ridker PM, Rifai N, Pfeffer M, Sacks F, Lepage S, Braunwald E. Elevation of tumor factor-alpha and increased risk of recurrent coronary events after myocardial infarction. Circulation. 2000; 101: 2149-53.
- 14. Lindmark E, Diderholm E, Wallentin L, Siegbahn A. Relationship between IL-6 and mortality in patients with unstable coronary artery desease: effects of an early invasive or noninvasive strategy. JAMA. 2001; 286: 2107-13.
- 15. Biasucci LM, Liuzzo G, Fantuzzi G, Caligiuri G, Rebuzzi AG, Ginnetti F, et al. Increasing levels of interleucin-1 and IL-6 during the first two days of hospitalization in unstable angina are associated with increased risk of in-hospital coronary events. Circulation. 1999; 99: 2079-84.
- 16. Richards AM, Nicholls MG, Yandle TG, Frampton C, Espiner EA, Turner JG, et al. Plasma n-terminal pro-brain natriuretic peptide and adrenomedullin: new neurohormonal predictors of left ventricular function and prognosis after myocardial infarction. Am Heart J. 1998; 135: 21-8.
- 17. Lowel H, Koenig W, Engel S, Hormann A, Keil U. The impact of diabetes mellitus on survival after myocardial infarction: can it be modified by drug treatment? Results of a population-based myocardial infarction register follow-up study. Diabetalogia. 2000; 43: 218-26.
- 18. Norhammar AM, Ryden L, Malmberg K. Admission plasma glucose: independent risk factor for long-term prognosis after myocardial infarction even in non-diabetic patients. Diabetes Care. 1999; 22: 1827-31.
- 19. Oswald GA, Smith CC, Betteridge DJ, Yudkin JS. Determinants and importance of stress hyperglycemia in non-diabetic patients with myocardial infarction. Br Med J. 1986; 293: 917-22.
- 20. Bolk J, van der Ploeg TJ, Cornel JH, Arnold AE, Sepers J, Umans VA, et al. Impaired glucose metabolism predicts mortality after a myocardial infarction. Intern J Card. 2001; 79: 207-14.
- 21. Ishihara M, Kojima S, Sakamoto T, Asada Y, Tei C, Ogawa H. Japanese acute coronary syndrome study investigators. Acute hyperglycemia is associated with adverse outcome after acute myocardial infarction in the coronary intervention era. Am Heart J. 2005; 150: 814-20.
- 22. Iwakura K, Ito H, Ikushima M, Kawano S, Okamura A, Asano K, et al. Association between hyperglycemia and the no-reflow phenomenon in patients with acute myocardial infarction. J Am Coll Cardiol. 2003; 41: 1-7.
- 23. Nicolau JC, Maia LN, Vitola JV, Mahaffey KW, Machado MN, Ramires JAF. Baseline glucose and left ventricular remodeling after acute myocardial infarction. J Diabetes Complications. 2007; 21 (5): 294-9.
- 24. Caldas MA, Tsutsui JM, Kowatsch I, Andrade JL, Nicolau JC, Ramires JF, et al. Value of myocardial contrast echocardiography for predicting left ventricular remodeling and segmental functional recovery after anterior wall acute myocardial infarction. J Am Soc Echocardiogr. 2004; 17: 923-32.
- 25. Kosuge M, Kimura K, Kojima S, Sakamoto T, Matsui K, Ogawa H. Japanese Acute Coronary Syndrome Study (JACSS) Investigators. Effects of glucose abnormalities on in-hospital outcome after coronary intervention for acute myocardial infarction. Circulation. 2005; 69: 375-9.
- 26. Macin SM, Perna ER, Augier N, Cialzeta J, Farias EF, Fontana M, et al. Clinical characteristics and long-term outcome in patients with heart failure complicating acute myocardial infarction. Rev Esp Cardiol. 2005; 58: 789-96.
- 27. Timmer JR, van der Horst IC, Ottervanger JP, Henriques JP, Hoorntje JC, de Boer MJ, et al. Myocardial Infarction Study Group. Prognostic value of admission glucose in non-diabetic patients with myocardial infarction. Am Heart J. 2004; 148: 399-404.
- 28. Bolk J, van der Ploeg T, Cornel JH, Arnold AE, Sepers J, Umans VA. Impaired glucose metabolism predicts mortality after a myocardial infarction. Int J Cardiol. 2001; 79: 207-14.
- 29. Title LM, Cummings PM, Giddens K, Nassar BA. Oral glucose loading acutely attenuates endothelium-dependent vasodilation in healthy adults without diabetes: an effect prevented by vitamins C and E. J Am Coll Cardiol. 2000; 36: 2185-91.
- 30. Scechter M, Merz NB, Paul-Labrador MJ, Kaul S. Blood glucose and platelet-dependent thrombosis in patients with coronary artery disease. J Am Coll Cardiol. 2000; 35: 300-7.
- 31. Marfella R, Esposito K, Giunta R, Coppola G, De Angelis L, Farzati B, et al. Circulating adhesion molecules in humans: role of hyperglycemia and hyperinsulinemia. Circulation. 2000; 101: 2247-51.
- 32. Kersten JR, Toller WG, Tessmer JP, Pagel PS, Warltier DC. Hyperglycemia reduces coronary blood flow through a nitric oxidemediated mechanism. Am J Physiol Heart Circ Physiol. 2001; 281: H2097-104.
- 33. Moreno PR, Fuster V. New aspects in the pathogenesis of diabetic atherothrombosis. J Am Coll Cardiol. 2004; 44: 2293-30.
- 34. Zhang L, Zalewski A, Liu Y, Mazurek T, Cowan S, Martin JL. Diabetes-induced oxidative stress and low-grade inflammation in porcine coronary arteries. Circulation. 2003; 108: 472-8.
- 35. Patel MR, Mahaffey KW, Armstrong PW, Weaver WD, Tasissa G, Nicolau JC, et al. Prognostic usefulness of white blood cell count and temperature in acute myocardial infarction (from the CARDINAL Trial). Am J Cardiol. 2005; 95: 614-8.
- 36. Marchioli R, Avanzini F, Barzi F, Chieffo C, Di Castelnuovo A, Valagussa F. GISSI-Prevenzione Investigators. Assessment of absolute risk of death after myocardial infarction by use of multiple-risk-factor assessment equations: GISSI-Prevenzione mortality risk chart. Eur Heart J. 2001; 22: 2085-103.
- 37. Comparan-Nunez A, Palacios JM, Jerjes-Sanchez CD. Leucocytosis associated with higher incidence of adverse cardiovascular events in myocardial infarcts. Arch Cardiol Mex. 2005; 75 (Suppl 3): S3-61-8.
- 38. Kirtane AJ, Bui A, Murphy SA, Barron HV, Gibson CM. Association of peripheral neutrophilia with adverse angiographic outcomes in ST-elevation myocardial infarction. Am J Cardiol. 2004; 93: 532-6.
- 39. Zairis MN, Adamopoulou EN, Manousakis SJ, Lyras AG, Bibis GP, Ampartzidou OS, et al. The impact of hs C-reactive protein and other inflammatory biomarkers on long-term cardiovascular mortality in patients with acute coronary syndromes. Atherosclerosis. 2007; 194 (2): 397-402.
- 40. Diaz R, Paolasso EA, Piegas LS, Tajer CD, Moreno MG, Corvalan R, et al. On behalf of the ECLA Collaborative Group. Metabolic modulation of acute myocardial infarction: the ECLA glucoseinsulinpotassium pilot trial. Circulation. 1998; 98: 2227-34.
- 41. Altman R, Scazziota A. Papel de los antiinflamatorios en el tratamiento de los síndromes coronarios agudos: de la ateroinflamación a la aterotrombosis. Rev Esp Cardiol. 2003; 56: 9-15.
- 42. Altman R, Luciardi HL, Muntaner J, Del Río F, Berman SG, López R, et al. Efficacy assessment of meloxicam, a preferential cyclooxygenase-2 inhibitor, in acute coronary syndromes without ST-segment elevation: the Nonsteroidal Anti-Inflammatory Drugs in Unstable Angina Treatment-2 (NUT-2) pilot study. Circulation. 2002; 106: 191-5.
- 43. Mc Gettigan P, Henry D. Cardiovascular risk and inhibition of cyclooxygenase: a systematic review of the observational studies of selective and nonselective inhibitors of cyclooxygenase 2. JAMA. 2006; 296: 1633-44.
- 44. Ridker PM, Cannon CP, Morrow D, Rifai N, Rose LM, McCabe CH, et al. Pravastatin or Atorvastatin Evaluation and Infection Therapy-Thrombolysis in Myocardial Infarction 22 (PROVE IT-TIMI 22) Investigators. C-reactive protein levels and outcomes after statin therapy. N Engl J Med. 2005; 352: 20-8.
Datas de Publicação
-
Publicação nesta coleção
06 Abr 2009 -
Data do Fascículo
Fev 2009
Histórico
-
Recebido
23 Out 2007 -
Revisado
14 Abr 2008 -
Aceito
09 Jun 2008