Resumos
FUNDAMENTO: O exercício físico promove estresse hemodinâmico. OBJETIVO: Testar se programas de treinamento com corridas voluntária e forçada induzem níveis distintos de expressão de Hsp72 no miocárdio de ratas Wistar. MÉTODOS: Ratas Wistar foram alocadas em três grupos (n = 6, cada): treinadas com corrida voluntária (TCV), treinadas com corrida forçada (TCF) e grupo controle (C). Os animais do TCV tiveram livre acesso à roda de corrida voluntária, enquanto os do TCF foram submetidos à corrida forçada em esteira (18 m/min, 0% inclinação, 60 m/min, 5 dias/sem) durante oito semanas. Fragmentos dos ventrículos esquerdo (VE) e direito (VD) foram coletados para análise dos níveis de Hsp72. RESULTADOS: As ratas do grupo TCV correram, em média, 4,87 km, e as do TCF, 4,88 km por semana. Os animais dos grupos TCV e TCF ganharam menos peso (p < 0,05) que os do grupo C (81,67 ± 11,95 g vs 81,17 ± 10,18 g vs 111,50 ± 2,26 g, respectivamente). O peso relativo do coração não foi diferente (p > 0,05) entre os grupos TCV, TCF e C (4,54 ± 0,79 mg/g vs 4,94 ± 0,89 mg/g vs 4,34 ± 0,87 mg/g, respectivamente). Ratas treinadas com corrida forçada apresentaram níveis de Hsp72 maiores (p < 0,05) que as que correram voluntariamente, no VE (287,45 ± 35,86% vs 135,59 ± 5,10%, respectivamente) e no VD (241,31 ± 25,83% vs 137,91 ± 45,20%, respectivamente). CONCLUSÃO: Os programas de treinamento com corrida voluntária e forçada induziram níveis distintos de expressão de Hsp72 no miocárdio de ratas Wistar.
Atividade física; corrida; ratos; estresse; miocárdio
FUNDAMENTO: El ejercicio físico promueve estrés hemodinámico. OBJETIVO: Probar si programas de entrenamiento con carreras voluntaria y forzada inducen niveles distintos de expresión de Hsp72 en el miocardio de ratas hembra Wistar. MÉTODOS: Ratas hembra Wistar fueron distribuidas en tres grupos (n = 6, cada uno): entrenadas con carrera voluntaria (ECV), entrenadas con carrera forzada (ECF) y grupo control (C). Los animales del ECV tuvieron libre acceso a la rueda de carrera voluntaria, mientras que los del ECF fueron sometidos a carrera forzada en cinta sin fin (18 m/min, 0% inclinación, 60 m/min, 5 días/sem) durante ocho semanas. Fragmentos de los ventrículos izquierdo (VI) y derecho (VD) se recolectaron para análisis de los niveles de Hsp72. RESULTADOS: Las ratas del grupo ECV corrieron, en promedio 4,87 km, y las del ECF, 4,88 km por semana. Los animales de los grupos ECV y ECF ganaron menos peso (p<0,05) que los del grupo C (81,67 ± 11,95 g vs. 81,17 ± 10,18 g vs. 111,50 ± 2,26 g, respectivamente). El peso relativo del corazón no fue diferente (p>0,05) entre los grupos ECV, ECF y C (4,54 ± 0,79 mg/g vs. 4,94 ± 0,89 mg/g vs. 4,34 ± 0,87 mg/g, respectivamente). Las ratas entrenadas con carrera presentaron niveles de Hsp72 mayores (p<0,05) que las que corrieron voluntariamente, en el VI (287,45 ± 35,86% vs. 135,59 ± 5,10%, respectivamente) y en el VD (241,31 ± 25,83% vs. 137,91 ± 45,20%, respectivamente). CONCLUSIÓN: Los programas de entrenamiento con carreras voluntaria y forzada inducen niveles distintos de expresión de Hsp72 en el miocardio de ratas Wistar.
Actividad física; carrera; ratones; estrés; miocardio
BACKGROUND: Physical exercise induces hemodynamic stress. OBJECTIVE: To evaluate if voluntary running and forced running induced different levels of stress protein (Hsp72) in the myocardium of female Wistar rats. METHODS: Female rats were randomly assigned to the following groups: forced treadmill running group (FR; n= 6), voluntary running group (VR; n=6) and control group (C; n=6). VR group animals had free access to running wheels, and those from FR group underwent a running program on a treadmill (18 m/min, 60 min/day, 5 days/wk) for 8 weeks. Left ventricle (LV) and right ventricle (RV) fragments were collected at sacrifice, and the relative immunoblot contents of stress protein (Hsp72) were determined. RESULTS: VR animals ran on average 4.87 km/wk, and FR rats ran 4.88 km/wk. Animals from VR and FR groups had less body weight gain (p<0.05) than those from C group (81.67 ± 11.95g vs 81.17 ± 10.18g vs 111.50 ± 2.26g, respectively). Heart weight/body weight ratio was not significantly different (p>0.05) among VR, FR and C groups (4.54 ± 0.79 mg/g vs 4.94 ± 0.89 mg/g vs 4.34 ± 0.87 mg/g, respectively). FR group animals had levels of Hsp72 (p<0.05) higher than those from VR, both in LV (287.45 ± 35.86 % vs 135.59 ± 5.10 %, respectively) and RV (241.31 ± 25.83 % vs 137.91 ± 45.20 %, respectively). CONCLUSION: Voluntary running and forced running induced different levels of Hsp72 in the myocardium of female Wistar rats.
Physical activity; running; rats; stress; myocardium
ARTIGO ORIGINAL
BIOLOGIA MOLECULAR
Níveis distintos de Hsp72 no miocárdio de ratas em resposta aos exercícios voluntário e forçado
Stéphano Freitas Soares Melo; Wellington Lunz; Elizabeth Pacheco Batista Fontes; Cristina Maria Ganns Chaves Dias; Miguel Araujo Carneiro Júnior; Anselmo Gomes de Moura; Ricardo Junqueira Del Carlo; Antonio Jose Natali
Universidade Federal de Viçosa (UFV), Viçosa, MG - Brasil
Correspondência Correspondência: Antonio Jose Natali Avenida PH Rolfs s/n Departamento de Educação Física Campus Universitário Universidade Federal de Viçosa UFV Viçosa/MG 36570-000 Brasil E-mail: anatali@ufv.br
RESUMO
FUNDAMENTO: O exercício físico promove estresse hemodinâmico.
OBJETIVO: Testar se programas de treinamento com corridas voluntária e forçada induzem níveis distintos de expressão de Hsp72 no miocárdio de ratas Wistar.
MÉTODOS: Ratas Wistar foram alocadas em três grupos (n = 6, cada): treinadas com corrida voluntária (TCV), treinadas com corrida forçada (TCF) e grupo controle (C). Os animais do TCV tiveram livre acesso à roda de corrida voluntária, enquanto os do TCF foram submetidos à corrida forçada em esteira (18 m/min, 0% inclinação, 60 m/min, 5 dias/sem) durante oito semanas. Fragmentos dos ventrículos esquerdo (VE) e direito (VD) foram coletados para análise dos níveis de Hsp72.
RESULTADOS: As ratas do grupo TCV correram, em média, 4,87 km, e as do TCF, 4,88 km por semana. Os animais dos grupos TCV e TCF ganharam menos peso (p < 0,05) que os do grupo C (81,67 ± 11,95 g vs 81,17 ± 10,18 g vs 111,50 ± 2,26 g, respectivamente). O peso relativo do coração não foi diferente (p > 0,05) entre os grupos TCV, TCF e C (4,54 ± 0,79 mg/g vs 4,94 ± 0,89 mg/g vs 4,34 ± 0,87 mg/g, respectivamente). Ratas treinadas com corrida forçada apresentaram níveis de Hsp72 maiores (p < 0,05) que as que correram voluntariamente, no VE (287,45 ± 35,86% vs 135,59 ± 5,10%, respectivamente) e no VD (241,31 ± 25,83% vs 137,91 ± 45,20%, respectivamente).
CONCLUSÃO: Os programas de treinamento com corrida voluntária e forçada induziram níveis distintos de expressão de Hsp72 no miocárdio de ratas Wistar.
Palavras-chave: Atividade física, corrida, ratos, estresse, miocárdio.
Introdução
A exposição de células a diferentes situações de estresse induz a expressão de proteínas de choque térmico (HSP), também conhecidas como proteínas de estresse. Tais proteínas conferem às células tolerância a vários agentes estressores, exercem proteção ao organismo contra a desnaturação protéica e auxiliam na eliminação de proteínas danificadas1,2.
O exercício físico, tanto agudo quanto crônico, é um desses agentes estressores que podem induzir a expressão de Hsp72, forma induzível da família das Hsp de peso molecular 70kDa (Hsp70), em vários tecidos, entre os quais os músculos esquelético e cardíaco3-10. Há evidências de que a expressão de Hsp72 no miocárdio, induzida por exercício, está associada à proteção cardíaca contra eventos de estresse cardiovascular7,11-14, apesar de alguns resultados em contrário15. Todavia, a indução da expressão de Hsp72 em resposta ao exercício parece ser dependente do gênero do animal16-18 e da intensidade do exercício6.
Considerando-se que os modelos de exercício forçado para animais provocam alterações nas respostas neuroendócrinas e imunológicas comumente associadas ao estresse19-21, a indução da expressão de Hsp72 pelo exercício forçado pode sofrer interferência de fatores estressantes adversos ao exercício. Ao contrário, a corrida voluntária, modelo em que os animais têm livre acesso ao equipamento a partir da gaiola e correm voluntariamente22, provoca níveis mais baixos de estresse aos animais, em comparação à corrida forçada e à natação4,23.
Assim, este estudo teve como objetivo testar se programas de treinamento com corrida voluntária e forçada induzem níveis distintos de expressão de Hsp72 no miocárdio de ratas Wistar.
Métodos
Animais de experimentação e tratamento
Dezoito ratas Wistar jovens (sete semanas de idade) foram usadas. Formaram-se três grupos em tempos diferentes, a saber: treinadas com corrida voluntária (TCV, n = 6); treinadas com corrida forçada (TCF, n = 6) e grupo controle (C, n = 6). Todos os animais foram manejados identicamente, porém o grupo C não executou exercício. Os animais foram alojados em gaiolas individuais de aço inox (25 x 20 x 18 cm), receberam água e ração própria ad libitum, foram mantidos em ambiente com temperatura média de 22o C e submetidos a um regime de luminosidade de 12 horas de escuridão por 12 horas de claridade durante o período do experimento.
Os animais foram fornecidos pelo Biotério Central do Centro de Ciências Biológicas e da Saúde, da Universidade Federal de Viçosa, e foram seguidas as normas estabelecidas no Guide for the Care and Use of Laboratory Animals (Institute of Laboratory Animal Resources, National Academy of Sciences, Washington, D.C., 1996) e nos “Princípios éticos na experimentação animal”, do Colégio Brasileiro de Experimentação Animal (COBEA).
Programa de treinamento com corrida voluntária
O primeiro grupo a exercitar-se foi o TCV, cujas ratas tiveram livre acesso à roda de corrida voluntária, acoplada às suas respectivas gaiolas de aço inox (25 x 20 x 18 cm), por oito semanas.
Essa roda de corrida voluntária tem uma circunferência interna de 1,53 m, e o número de voltas foi registrado por um contador de voltas mecânico. Dessa forma, a distância percorrida pelos animais foi calculada pelo número de voltas realizadas.
Observa-se que os roedores são animais de hábitos noturnos e, portanto, exercitam-se normalmente durante a fase de escuridão do ciclo de luminosidade.
Programa de treinamento com corrida forçada
Conhecidas as metragens médias semanais e totais percorridas pelas ratas do grupo TCV, elaborou-se o protocolo de treinamento para o outro grupo de ratas (TCF), de forma que as metragens não fossem diferentes entre os dois grupos.
Assim, as ratas do grupo TCF foram submetidas a um regime de corrida forçada em esteira rolante motorizada (Insight Instrumentos Científicos, Ribeirão Preto, SP, Brasil) por oito semanas (adaptado de Samelman)5. Os animais iniciaram o programa de exercício correndo à velocidade de 15 m/min, 0% inclinação, por 15 minutos no primeiro dia, cinco dias por semana. Essa duração foi aumentada em cinco minutos por dia, de maneira que, no último dia da segunda semana, os animais correram durante 60 minutos. A partir do primeiro dia da terceira semana, a velocidade passou para 17 m/min. Da quarta à oitava semana, a sessão de exercício foi mantida com a duração de 60 minutos por dia, 18 m/min, 0 % de inclinação, cinco dias por semana.
Esse programa de corrida em esteira foi aplicado durante a fase de escuridão do ciclo de luminosidade para não diferir do grupo TCV. Os animais foram motivados a correr com leves toques no dorso. Observa-se que esses animais foram alojados em gaiolas individuais de aço inox (25 x 20 x 18 cm), da mesma forma que os animais dos grupos TCV e C. Assim, considera-se que a movimentação (voluntária) dos animais nessas gaiolas, fora do período de treinamento, não é suficiente para provocar adaptações que possam confundir aquelas provocadas pelas corridas voluntária e forçada.
Portanto, em nenhum dos três grupos é necessário contabilizar a movimentação dos animais nas suas respectivas gaiolas, por considerar-se que é semelhante para todos os animais.
Coleta das amostras
Para evitar a resposta aguda do exercício e preservar a resposta crônica, a eutanásia dos animais foi realizada 48 horas após a última sessão de exercício. Coletaram-se fragmentos dos ventrículos esquerdo e direito, que foram envolvidos em papel alumínio, identificados, imediatamente congelados em nitrogênio líquido e armazenados a -80º C para análise posterior.
Extração das proteínas
Fragmentos das amostras foram retirados do freezer e, depois de pesados, foram macerados para obtenção de um extrato tecidual, ao qual foi adicionado o respectivo tampão (composição 15 mM Tris HCL; 600 mM de NaCl; 1 mM PMSF, pH 7,5). A 60 mg de extrato, foram adicionados 1200 µl de tampão de extração (proporção de 1:20). Em seguida, colocaram-se as amostras em eppendorfs, os quais foram identificados e mantidos em gelo por, aproximadamente, cinco minutos.
Após esse período de incubação, os restos celulares foram descartados por centrifugação a 14.000 g, a 4º C, durante 20 minutos, e o sobrenadante foi armazenado a - 20º C. Os extratos de proteínas totais foram quantificados de acordo com o método de Bradford24, utilizando-se as três réplicas preconizadas.
Eletroforese SDS-PAGE
Eletroforese em géis de poliacrilamida (PAGE) com detergente dodecil sulfato sódio (SDS) foi realizada, essencialmente, como descrita por Laemmli25. O extrato de proteína foi incubado por cinco minutos, a 100º C, em tampão da amostra [glicerol 10% (v/v), SDS 2,3%, azul-de-bromofenol 0,25%, 2-mercaptoetanol 5% (v/v) e Tris-HCl 0,0625 mol/L, pH 6,8], antes de ser aplicado no gel. A eletroforese foi conduzida por, aproximadamente, 16 horas, a 48 V, no tampão de corrida [Tris-HCl 0,025 mol/L, glicina 0,2 mol/L, EDTA 1 mmol/L e SDS 3,5 mmol/L].
Esse procedimento foi realizado para obtenção de três géis. Um desses foi corado com solução corante [metanol 40% (v/v), CH3COOH 7,5% (v/v) e coomassie brilhant blue R-250 0,01%] por, aproximadamente, 12 horas e descorado em solução descorante [metanol 10% (v/v) e ácido acético 7,5% (v/v)]. Os outros dois géis foram submetidos à técnica de imunoblotting, para verificar se o anticorpo Monoclonal Anti-Heat Shock Protein 70 contra Hsp72 de animais era capaz de reconhecer a proteína de interesse.
Imunoblotting
As proteínas foram transferidas para a membrana de nitrocelulose, usando-se o sistema de transferência da Biorad (EUA), de acordo com as instruções do fabricante. Após a transferência (em aproximadamente uma hora, a 0,70 Amperes constantes), a membrana de nitrocelulose foi imersa em solução de bloqueio (caseína Non-fat Dry Milk, BIORAD) por uma hora.
Em seguida, foram realizadas quatro lavagens, por 15 minutos cada, à temperatura ambiente, com TBS-T [Tris-HCl 0,01 mol/L, NaCl 1,5 mmol/L, Tween-20 0,1% (v/v), pH 7,6]. A membrana foi incubada com o anticorpo Monoclonal Anti-Heat Shock Protein 70 (SIGMA), em uma diluição de 1:5.000 por três horas sob agitação.
Após o período de incubação, a membrana foi lavada com TBS-T quatro vezes, por 15 minutos cada, e, em seguida, foi incubada com o anticorpo Anti-Mouse IgG [fosfatase alcalina SIGMA], em uma diluição de 1:10.000 por, aproximadamente, duas horas. A membrana foi lavada extensivamente com TBS-T, novamente por quatro vezes, de 15 minutos cada. Subsequentemente, foi incubada com tampão da enzima [Tris-HCl 0,1 mol/L, pH 9,8, NaCl 0,1 mol/L, MgCl2 0,5 mol/L] por dez minutos.
A atividade da fosfatase alcalina foi detectada, usando-se os substratos NBT [azul-nitro-tetrazolium, GIBCO/BRL] e BCIP [5-bromo-4-cloro-3-indolil-fosfato, GIBCO/BRL]. As bandas dos imunoblottings foram quantificadas por meio de densitometria computadorizada, utilizando-se o personal densitometer, equipado com o programa Image Quant, versão 5.2 (Molecular Dinamics EUA).
Tratamento estatístico
As comparações das médias do peso corporal, ganho de peso e do peso relativo do coração foram feitas utilizando-se ANOVA one-way, seguida do teste post hoc de Tukey. As comparações dos níveis de Hsp72 foram realizadas com o teste de Mann-Whitney, pois os dados não apresentaram distribuição normal (Kolmogorov-Smirnov, p < 0,05). As análises foram feitas no programa Sigma Stat (versão 3.0 Richmond CA), e utilizou-se o nível de significância de até 5%.
Este trabalho foi financiado pela Fundação de Amparo à Pesquisa do Estado de Minas Gerais (FAPEMIG CDS nº 947/2002).
Resultados
Os animais do grupo TCV percorreram, voluntariamente, distâncias distintas, de acordo com a capacidade individual, enquanto no grupo TCF todos os animais foram forçados a percorrer a mesma distância. Dessa forma, a distância percorrida pelos animais do grupo TCV será apresentada como média (média ± EPM), e a dos animais do grupo TCF, como valor absoluto para o grupo.
Os animais do grupo TCV percorreram 4,87 ± 0,55 km/semana e um total de 38,96 ± 3,55 km, enquanto os do grupo TCF percorreram, no mesmo período, 4,88 km/semana e um total de 39,03 km. Não houve, portanto, diferença entre as distâncias percorridas nos dois modelos.
Ao final das oito semanas de treinamento, os animais dos grupos TCV e TCF exibiram um ganho de peso significativamente menor que os animais do grupo controle (tabela 1). O peso relativo do coração, índice usado para indicar hipertrofia cardíaca, não apresentou diferença estatística significativa entre os grupos (tabela 1).
A figura 1 é uma representação do acúmulo de Hsp72 e Hsp73 no VE de duas ratas Wistar de cada um dos grupos experimentais. A expressão de Hsp73, um membro constitutivo da família das Hsp70, foi similar nos três grupos (p > 0,05), não sendo afetada pelos programas de exercício usados.
Observou-se, porém, que houve indução da expressão de Hsp72 em resposta aos programas de exercícios voluntário e forçado, mas em níveis distintos. O VE e o VD dos animais do grupo controle mostraram expressão de pequena quantidade de Hsp72, apresentada como unidade arbitrária (282,19 ± 20,02 vs. 287 ± 32,05, respectivamente), provavelmente em função de algum estresse ambiental.
Esses valores foram usados como baseline para comparação dos efeitos dos dois protocolos de exercício, em percentuais. As ratas submetidas à corrida forçada em esteira rolante apresentaram níveis de Hsp72 maiores (p < 0,05) do que as que correram voluntariamente, no VE (287,45 ± 35,86 % vs. 135,59 ± 5,10 %, respectivamente) e no VD (241,31 ± 25,83 % vs. 137,91 ± 45,20 %, respectivamente). Todavia, não houve diferença significativa na expressão de Hsp72 entre o VE e o VD (fig. 1B).
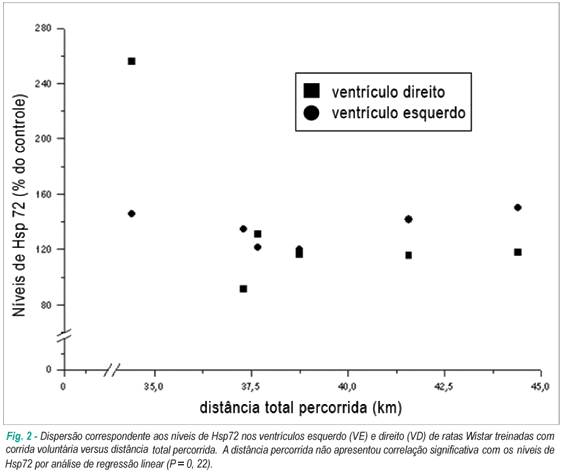
Observou-se que as ratas apresentaram uma variação interindividual na distância total percorrida de, aproximadamente, 3,5 km, mas não houve correlação significativa (p = 0,22) entre a distância total percorrida e a indução da expressão de Hsp72 (fig. 2).
Discussão
Investigamos se programas de treinamento com corridas voluntária e forçada induzem níveis distintos de expressão de Hsp72 no miocárdio de ratas Wistar. Os dados demonstraram que os protocolos de exercício usados foram capazes de induzir a expressão de Hsp72 no miocárdio das ratas de forma distinta, tanto no VE quanto no VD, sendo maior na corrida forçada em esteira do que na corrida voluntária.
Os animais dos grupos exercitados, TCV e TCF, percorreram distâncias similares. Entretanto, deve salientar-se que a forma de execução da corrida é diferente entre os dois modelos. A corrida na esteira é realizada pelos animais de forma contínua, pois a velocidade da esteira permanece constante durante a sessão de treino. Porém, na roda de corrida voluntária, os animais exercitam de forma intermitente, pois correm períodos curtos (60 a 90 s), por, aproximadamente, cinco minutos, com períodos intercalados de descanso26. Assim, é possível calcular o trabalho realizado pelas ratas apenas na corrida forçada, pois esse é dado pela relação da massa corporal do animal com o tempo de execução da corrida, a velocidade da corrida e a inclinação da esteira27.
Embora o peso corporal, as distâncias percorridas e a inclinação tenham sido similares nos dois modelos, a velocidade e o tempo de execução da corrida foram diferentes. Consideramos essa falta de precisão na equivalência do trabalho realizado entre os animais dos grupos TCV e TCF uma limitação do presente estudo. Todavia, os programas de exercício utilizados reduziram o ganho de peso dos animais, comparado ao dos animais sedentários do grupo controle.
Isso indica uma interferência dos programas de corrida no organismo das ratas, pois a redução de peso corporal pode refletir o aumento da taxa de metabolismo ou do gasto energético28. Fisiologicamente, sabe-se que peso corporal similar não significa, necessariamente, composição corporal e metabolismo energético equivalentes. Entretanto, estudos prévios demonstram que treinamentos com exercício aeróbico de diferentes intensidades resultaram em diferentes alterações no peso corporal de ratos29, mas também que diferentes modelos de exercício provocaram reduções similares no ganho de peso de ratos, em comparação aos sedentários (corrida em esteira vs. natação30, corrida em esteira vs. corrida voluntária)4,31. Portanto, é razoável especular que nossos protocolos de corridas voluntária e forçada resultaram em taxas metabólicas similares, o que nos possibilita fazer comparações entre os dois grupos.
O peso relativo do coração não foi diferente entre os três grupos experimentais. Isso sugere que os protocolos de exercício usados no presente estudo não foram suficientes para promover hipertrofia cardíaca. Entretanto, adaptações do músculo cardíaco ao exercício crônico, inclusive a indução da expressão de Hsp72, foram observadas em animais com e sem hipertrofia cardíaca12,31.
O principal achado do presente estudo diz respeito aos protocolos de exercício usados, que foram capazes de induzir a expressão de Hsp72 no miocárdio das ratas de forma distinta, no VE e no VD, sendo significativamente maior na corrida forçada em esteira do que na corrida voluntária. Esses níveis de Hsp72 aumentados refletem o maior nível de estresse intracelular gerado pelo programa de corrida forçada, em comparação ao de corrida voluntária.
Apesar de nossos dados não permitirem especificar os mecanismos responsáveis pelo aumento da expressão de Hsp72 observado, durante o exercício, vários eventos fisiológicos e metabólicos ocorrem em nível celular (por exemplo, aumento da temperatura, hipoxia, estresse oxidativo, aumento da concentração de cálcio e redução do pH) e podem, isoladamente ou em conjunto, induzir a expressão de Hsp7210,32.
Alguns estudos têm creditado altos níveis de expressão de Hsp72, em resposta à corrida na esteira, à intensidade do exercício31. De fato, Milne e Noble6 demonstraram que a indução da expressão de Hsp72 em músculos esquelético e cardíaco é dependente da intensidade do exercício, apresentando as velocidades acima de 24 m/min como as mais eficientes na indução da expressão de Hsp72.
Entretanto, sabendo-se que, no presente estudo, a velocidade durante a corrida em esteira foi 18 m/min, que a distância percorrida nos dois protocolos foi similar e que os animais podem correr a velocidades superiores a 40 m/min33 na corrida voluntária, a maior expressão de Hsp72 observada nos animais do grupo TCF parece ter sido provocada por outros fatores além da carga de exercício.
Um desses fatores poderia ser o nível de estresse proporcionado ao animal pelo modelo de exercício. Existem evidências de que, na corrida voluntária, o nível de estresse sofrido pelo animal é menor se comparado ao da corrida em esteira4,23. No presente estudo, não usamos choque elétrico para forçar os animais a correr na esteira, o que aumenta a expressão de Hsp7234, mas os animais foram estimulados com toques no dorso.
Além disso, o exercício forçado crônico pode causar estresse mental ao animal35 e outras adaptações negativas indicativas de estresse crônico (por exemplo, redução de globulinas ligantes de corticosteróides séricas, hipertrofia adrenal, involução do timo, supressão da proliferação de linfócitos e de IgM antígeno-específico)20. Na corrida voluntária, ao contrário, os animais não foram forçados a correr. Há relatos de que o treinamento com corrida voluntária reduziu os níveis de danos oxidativos ao DNA4 e reduziu a depressão comportamental induzida por estresse em ratos36.
Adicionalmente, observamos que as ratas apresentaram uma variação interindividual de, aproximadamente, 3,5 km na distância total percorrida. Todavia, a distância percorrida não apresentou correlação significativa com a indução da expressão de Hsp72 (fig. 2). Isso pode ser um indicativo de que, no modelo de corrida voluntária, a intensidade do exercício expõe os animais a menor estresse.
De fato, tem sido reportado que a corrida voluntária pode neutralizar a supressão da função imune induzida por estresse, assim como os impactos negativos do estresse no comportamento e na função imune adquirida de ratos36,37. Recentemente, Hill e cols.38 demonstraram que a corrida voluntária crônica foi capaz de aumentar a capacidade de síntese de GABA no cérebro de ratos, o que pode implicar alterações na sensibilidade ao estresse durante o exercício.
Observamos que não houve distinção regional significativa (VE vs. VD) na indução da expressão de Hsp72. Essa observação confirma resultados reportados em estudos prévios5,31. Apesar de as adaptações do músculo cardíaco ao exercício serem mais pronunciadas no ventrículo esquerdo, refletindo o estresse intracelular distinto imposto pela carga mecânica sob a qual as fibras trabalham durante o exercício, todas as fibras do miocárdio são recrutadas a cada batimento, e o trabalho do coração cresce linearmente em função do aumento da contratilidade e da frequência cardíaca em ambos os ventrículos.
Nossos resultados evidenciam que ratas também respondem ao estresse provocado pelo exercício, aumentando a indução da expressão de Hsp72 no miocárdio. Tem sido observado que a indução da expressão de Hsp72 em resposta ao exercício é maior em ratos, o que sugere que a presença de estrogênio nas ratas é suficiente para inibir a expressão de Hsp7216-18. Entretanto, o miocárdio de ratas Sprague-Dawley exibiu duas vezes mais Hsp72 do que o de ratos39, e o músculo cardíaco de ratos não demonstrou dimorfismo sexual na expressão de Hsp72 em resposta ao choque elétrico35.
Por fim, a despeito de não termos avaliado os efeitos dos protocolos de exercício na proteção cardíaca, o aumento da expressão de Hsp72 observado aqui pode ter impactos fisiologicamente importantes na proteção do miocárdio contra eventos de estresse (por exemplo, isquemia ou reperfusão). Apesar de estudos16,18 terem reportado que a resposta da Hsp70 ao exercício físico agudo e crônico (corrida em esteira), mediada por hormônios sexo-específicos, resultou em cardioproteção, preferencialmente em ratos, Chicco e cols.40 demonstraram que ratas que correram voluntariamente por oito semanas apresentaram níveis elevados de Hsp72, os quais estavam associados a uma melhora da disfunção cardíaca induzida pela doxorubicina.
Conclusão
Concluímos que os programas de treinamento com corridas voluntária e forçada adotados no presente estudo induziram níveis distintos de expressão de Hsp72 no miocárdio de ratas Wistar.
Potencial Conflito de Interesses
Declaro não haver conflito de interesses pertinentes.
Fontes de Financiamento
O presente estudo foi financiado por FAPEMIG.
Vinculação Acadêmica
Não há vinculação deste estudo a programas de pós-graduação.
Artigo recebido em 26/09/08; revisado recebido em 03/11/08; aceito em 02/12/08.
- 1. Li GC, Li LG, Liu YK, Mak JY, Chen LL, Lee WM. Thermal response of rat fibroblasts stably transfected with the human 70-kDa heat shock protein-encoding gene. Proc Natl Acad Sci USA. 1991; 88 (5): 1681-5.
- 2. Welch WJ. Mammalian stress response: cell physiology, structure/function of stress proteins, and implications for medicine and disease. Physiol Rev. 1992; 72 (4): 1063-81.
- 3. Locke M, Noble EG, Atkinson BG. Exercising mammals synthesize stress proteins. Am J Physiol. 1990; 258 (4 Pt 1): C723-9.
- 4. Asami S, Hirano T, Yamaguchi R, Tsurudome Y, Itoh H, Kasai H. Effects of forced and spontaneous exercise on 8-hydroxydeoxyguanosine levels in rat organs. Biochem Biophys Res Commun. 1998; 243 (3): 678-82.
- 5. Samelman TR. Heat shock protein expression is increased in cardiac and skeletal muscles of Fischer 344 rats after endurance training. Exp Physiol. 2000; 85 (1): 92-102.
- 6. Milne KJ, Noble EG. Exercise-induced elevation of HSP70 is intensity dependent. J Appl Physiol. 2002; 93 (2): 561-8.
- 7. Campisi J, Leem TH, Greenwood BN, Hansen MK, Moraska A, Higgins K, et al. Habitual physical activity facilitates stress-induced HSP72 induction in brain, peripheral, and immune tissues. Am J Physiol Regul Integr Comp Physiol. 2003; 284 (2): R520-30.
- 8. Atalay M, Oksala NK, Laaksonen DE, Khanna S, Nakao C, Lappalainen J, et al. Exercise training modulates heat shock protein response in diabetic rats. J Appl Physiol. 2004; 97 (2): 605-11.
- 9. Lunz W, Oliveira EC, Neves MT, Fontes EP, Dias CM, Natali AJ. Anabolic steroid- and exercise-induced cardiac stress protein (HSP72) in the rat. Braz J Med Biol Res. 2006; 39 (7): 889-93.
- 10. Whitham M, Fortes MB. Heat shock protein 72: release and biological significance during exercise. Front Biosci. 2008; 13: 1328-39.
- 11. Locke M, Tanguay RM, Klabunde RE, Ianuzzo CD. Enhanced postischemic myocardial recovery following exercise induction of HSP 72. Am J Physiol. 1995; 269 (1 Pt 2): H320-5.
- 12. Powers SK, Demirel HA, Vincent HK, Coombes JS, Naito H, Hamilton KL, et al. Exercise training improves myocardial tolerance to in vivo ischemia-reperfusion in the rat. Am J Physiol. 1998; 275 (5 Pt 2): R1468-77.
- 13. Demirel HA, Powers SK, Zergeroglu MA, Shanely RA, Hamilton K, Coombes J, et al. Short-term exercise improves myocardial tolerance to in vivo ischemia-reperfusion in the rat. J Appl Physiol. 2001; 91 (5): 2205-12.
- 14. Melling CW, Thorp DB, Milne KJ, Krause MP, Noble EG. Exercise-mediated regulation of Hsp70 expression following aerobic exercise training. Am J Physiol Heart Circ Physiol. 2007; 293(6):H3692-8.
- 15. Taylor RP, Harris MB, Starnes JW. Acute exercise can improve cardioprotection without increasing heat shock protein content. Am J Physiol. 1999; 276(3 Pt 2):H1098-102.
- 16. Paroo Z, Haist JV, Karmazyn M, Noble EG. Exercise improves postischemic cardiac function in males but not females: consequences of a novel sex-specific heat shock protein 70 response. Circ Res. 2002; 90(8):911-7.
- 17. Brown DA, Johnson MS, Armstrong CJ, Lynch JM, Caruso NM, Ehlers LB, et al. Short-term treadmill running in the rat: what kind of stressor is it? J Appl Physiol. 2007; 103(6):1979-85.
- 18. Thorp DB, Haist JV, Leppard J, Milne KJ, Karmazyn M, Noble EG. Exercise training improves myocardial tolerance to ischemia in male but not in female rats. Am J Physiol Regul Integr Comp Physiol. 2007; 293(1):R363-71.
- 19 Harri M, Kuusela P. Is swimming exercise or cold exposure for rats? Acta Physiol Scand. 1986; 126(2):189-97.
- 20. Moraska A, Deak T, Spencer RL, Roth D, Fleshner M. Treadmill running produces both positive and negative physiological adaptations in Sprague-Dawley rats. Am J Physiol Regul Integr Comp Physiol. 2000; 279(4):R1321-9.
- 21. Linthorst AC, Penalva RG, Flachskamm C, Holsboer F, Reul JM. Forced swim stress activates rat hippocampal serotonergic neurotransmission involving a corticotropin-releasing hormone receptor-dependent mechanism. Eur J Neurosci. 2002; 16(12):2441-52.
- 22. Shyu BC, Andersson SA, Thoren P. Spontaneous running in wheels: a microprocessor assisted method for measuring physiological parameters during exercise in rodents. Acta Physiol Scand. 1984; 121(2):103-9.
- 23. Rupp H. Differential effect of physical exercise routines on ventricular myosin and peripheral catecholamine stores in normotensive and spontaneously hypertensive rats. Circ Res. 1989; 65(2):370-7.
- 24. Bradford MM. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding. Anal Biochem. 1976; 72:248-54.
- 25. Laemmli UK. Cleavage of structural proteins during the assembly of the head of bacteriophage T4. Nature. 1970; 227: 680-5.
- 26. Eikelboom R, Mills R. A microanalysis of wheel running in male and female rats. Physiol Behav. 1988; 43(5):625-30.
- 27. Brooks GA, White TP. Determination of metabolic and heart rate responses of rats to treadmill exercise. J Appl Physiol. 1978; 45(6):1009-15.
- 28. Brooks GA, Fahey TD. Exercise physiology: human bioenergetics and its applications. New York: Macmillan; 1984.
- 29 Chang FL, Huang TH, Hsieh SS, Yang RS, Lin CC. The effects of different endurance training intensity on systematic and peripheral citrate synthase activity. Med Sci Sports Exerc. 2001; S33:295.
- 30 Huang TH, Lin SC, Chang FL, Hsieh SS, Liu SH, Yang RS. Effects of different exercise modes on mineralization, structure, and biomechanical properties of growing bone. J Appl Physiol. 2003; 95(1):300-7.
- 31. Noble EG, Moraska A, Mazzeo RS, Roth DA, Olsson MC, Moore RL, et al. Differential expression of stress proteins in rat myocardium after free wheel or treadmill run training. J Appl Physiol. 1999; 86(5):1696-701.
- 32. Noble EG. Heat shock proteins and their induction with exercise. In: Locke M, Noble EG, editors. Exercise and stress response: the role of stress proteins. Barcelona: Boca Raton; 2002. p. 43-78.
- 33. Rodnick KJ, Reaven GM, Haskell WL, Sims CR, Mondon CE. Variations in running activity and enzymatic adaptations in voluntary running rats. J Appl Physiol. 1989; 66(3):1250-7.
- 34. Nickerson M, Kennedy SL, Johnson JD, Fleshner M. Sexual dimorphism of the intracellular heat shock protein 72 response. J Appl Physiol. 2006; 101(2):566-75.
- 35. Maier SF. Learned helplessness and animal models of depression. Prog Neuropsychopharmacol Biol Psychiatry. 1984; 8(3):435-46.
- 36. Moraska A, Fleshner M. Voluntary physical activity prevents stress-induced behavioral depression and anti-KLH antibody suppression. Am J Physiol Regul Integr Comp Physiol. 2001; 281(2):R484-9.
- 37. Dishman RK, Warren JM, Youngstedt SD, Yoo H, Bunnell BN, Mougey EH, et al. Activity-wheel running attenuates suppression of natural killer cell activity after footshock. J Appl Physiol. 1995; 78(4):1547-54.
- 38. Hill LE, Droste SK, Nutt DJ, Linthorst AC, Reul JM. Voluntary exercise alters GABAA receptor subunit and glutamic acid decarboxylase-67 gene expression in the rat forebrain. J Psychopharmacol. 2008; 00(00):1-12
- 39. Voss MR, Stallone JN, Li M, Cornelussen RN, Knuefermann P, Knowlton AA. Gender differences in the expression of heat shock proteins: the effect of estrogen. Am J Physiol Heart Circ Physiol. 2003; 285(2):H687-92.
- 40. Chicco AJ, Schneider CM, Hayward R. Voluntary exercise protects against acute doxorubicin cardiotoxicity in the isolated perfused rat heart. Am J Physiol Regul Integr Comp Physiol. 2005; 289(2):R424-R31.
Datas de Publicação
-
Publicação nesta coleção
06 Jan 2010 -
Data do Fascículo
Nov 2009
Histórico
-
Aceito
02 Dez 2008 -
Recebido
26 Set 2008 -
Revisado
03 Nov 2008