DIRETRIZES
I Diretriz brasileira de cardio-oncologia pediátrica da Sociedade Brasileira de Cardiologia
Adriana SeberI,II; Adriana Siviero MiachonII; Ana Cristina Sayuri TanakaIV; Ângela Maria Spínola e CastroII; Antônio Carlos CarvalhoIII; Antônio Sergio PetrilliII; Carla Renata Donato Pacheco MacedoI,II; Clarissa Carvalho Fongaro NarsII; Claudia Naufel TerzianII; Claudio Galvão de Castro JuniorI,V; Cleusa Cavalcanti Lapa SantosVI; Cristina Chaves dos Santos GuerraVII; Dafne Cardoso Bourguignon da SilvaII; Débora Ugayama BassiI; Estela AzekaIV; Fabiana Aragão FeitosaVIII; Fernando HamamotoII; Gilberto SzarfII; Henrique Manoel LedermanII; Humberto João Rigon JuniorIX; Ieda Biscegli JateneX,XI; Isabele Coelho Fonseca da MotaXII; Jeferson Adriano PerrudII; José Soares JuniorIV; Julián Arango GutierrezXIII; Juliana Pepe Marinho PerinII; Juliana dos Santos SoaresII; Liane Hulle CataniXIV; Liliana Yu TsaiII; Livia Cristina ViannaII; Marcelo Goulart PaivaXV; Marcelo José SantosIV; Marcia Marcelino de Souza IshigaiXVI; Maria Suely Bezerra DiógenesIII; Maria Teresa de Seixas AlvesII,XVI; Maria Tereza Castro PiedadeII; Mariana ParreirasXVII; Mônica CyprianoII; Nilce da Silva NegriniIII; Orlando Campos FilhoIII; Paula Andrade FigueiredoII; Paulo Eduardo NovaesII; Paulo Roberto CamargoIV; Priscila dos Santos MaiaII; Renata PetrilliII; Rodrigo Genaro ArduiniII; Roseane Vasconcelos GouveiaII; Suzana Barbosa Miranda TeruyaII; Valdir Ambrosio MoisésIII; Vera Lúcia Lins de MoraisVIII
ISociedade Brasileira de Oncologia Pediátrica - SOBOPE
IIInstituto de Oncologia Pediátrica da Universidade Federal de São Paulo - GRAACC
IIIDisciplina de Cardiologia da Universidade Federal de São Paulo - UNIFESP
IVInstituto do Coração do Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo
VHospital de Clínicas de Porto Alegre - Universidade Federal do Rio Grande do Sul
VIInstituto Materno-Infantil de Pernambuco - IMIP
VIIHospital de Base de Brasília - DF
VIIIHospital Universitário Oswaldo Cruz - Universidade de Pernambuco - UPE
IXHospital A.C. Camargo - São Paulo - SP
XHospital do Coração - São Paulo - SP
XIDepartamento de Cardiopatias Congênitas e Cardiologia Pediátrica da Sociedade Brasileira de Cardiologia
XIIInstituto Nacional de Câncer - INCA - Rio de Janeiro - RJ
XIIIHospital Pequeno Príncipe - Curitiba - PR
XIVSanta Casa de Misericórdia de São Paulo - SP
XVInstituto do Câncer do Estado de São Paulo - ICESP
XVIDepartamento de Patologia da Universidade Federal de São Paulo
XVIIHospital Infantil Joana de Gusmão - Florianópolis - SC
Correspondência Correspondência: Maria Verônica Câmara Santos Instituto de Oncologia Pediátrica - Universidade Federal de São Paulo - IOP/ GRAACC Rua Botucatu, 743, Vila Clementino São Paulo-SP, CEP 04.023-062 E-mail: veronicasantos@graacc.org.br
Clique para ampliar

1. Objetivos da Diretriz
A cardio-oncologia tem sido considerada assunto de interesse para oncologistas e cardiologistas no mundo, com crescente atenção sobre a população pediátrica.
Sabemos que o diagnóstico precoce das neoplasias na infância e adolescência tem proporcionado maiores possibilidades de tratamento em tempo hábil, contribuindo com o sucesso terapêutico.
Contudo, o emprego de alguns quimioterápicos, ou de sua associação com a radioterapia, frequentemente utilizados como instrumentos terapêuticos eficazes, podem deixar sequelas cardiovasculares de diversas grandezas, muitas vezes irreversíveis.
As complicações cardiovasculares são as principais causas de morbidade e mortalidade entre sobreviventes ao câncer infanto-juvenil, depois da recidiva da doença, malignidades secundárias e infecções. Esses indivíduos apresentam cerca de oito vezes mais chances de desfecho fatal quando comparados à população geral.
Tendo em vista as peculiaridades da condução cardiológica do paciente oncológico pediátrico, as Sociedades Brasileiras de Oncologia Pediátrica (SOBOPE) e de Cardiologia, através do Departamento de Cardiopatias Congênitas e Cardiologia Pediátrica (SBC/DCC/CP), reconheceram a necessidade da elaboração de consenso específico.
Um dos principais desafios no desenvolvimento de diretrizes para a prática clínica é manter a uniformidade de opiniões e abertura para novas informações baseadas em evidências. Nesses moldes, essa Diretriz foi elaborada com a colaboração de experientes profissionais nas áreas da oncologia pediátrica e da cardiologia pediátrica em geral, ligados a serviços de referência nacional vinculados à SOBOPE.
Tentamos apresentar o passo a passo real da criança ou do adolescente e dos profissionais envolvidos nas várias etapas do processo, desde o diagnóstico oncológico, passando pelo tratamento quimioterápico, radioterápico e cuidados perioperatórios, abordando as diversas complicações cardiovasculares durante todo esse trajeto, até o seguimento tardio dos sobreviventes.
Estudos específicos relacionados à população pediátrica vêm sendo elaborados. Preocupamo-nos em expor textos com profundo senso prático e realístico, além de revisão da literatura com significativo impacto e embasamento científico.
Nessa primeira Diretriz nacional sobre repercussões cardiovasculares do tratamento do câncer na infância e adolescência, tivemos como objetivos:
Despertar o interesse de todos os profissionais que lidam direta ou indiretamente com o paciente oncológico infanto-juvenil por assunto de tamanha importância;
Disponibilizar importantes fontes bibliográficas para revisão da literatura mais aprofundada em cada tópico abordado;
Estimular os serviços nacionais quanto aos registros científicos retrospectivos e estudos prospectivos sobre os efeitos cardiovasculares do tratamento em questão, avaliando seus resultados de intervenções diagnósticas e terapêuticas;
Permitir a análise de novas evidências que deverão influenciar na aplicação de estratégias que exerçam significativo impacto no prognóstico, sobrevida e qualidade de vida desses pacientes.
2. Introdução
Conceitualmente, o câncer é definido por um grupo de doenças caracterizadas por alterações genéticas que levam à proliferação celular desordenada. Existem mais de 100 tipos da doença, sendo que 5 a 10% dos casos de origem hereditária (cânceres familiais, síndromes genéticas) e 90 a 95% dos casos com aparecimento esporádico1.
A incidência do câncer infanto-juvenil (abaixo de 19 anos) não é diferente nas várias áreas do mundo, apesar dos diferentes estágios de desenvolvimento socioeconômico. É considerado raro, quando comparado com os tumores do adulto, correspondendo entre 1 e 3% de todos os tumores malignos que ocorrem na maioria das populações. Atualmente, cerca de 80% das crianças e adolescentes sobrevivem ao câncer. Nas últimas décadas, as taxas de cura aumentaram significativamente. O objetivo além da cura é o de promover uma boa qualidade de vida e adequadas possibilidades de reintegração social1.
No Brasil, uma estimativa realizada pelo Instituto Nacional de Câncer (INCA) e pelo Ministério da Saúde em 2010, aponta uma incidência de 11000 casos novos de câncer em crianças e adolescentes até 18 anos de idade1 (segundo o último censo populacional do IBGE em 2010, 33,1% da população brasileira encontra-se na faixa etária abaixo de 19 anos)2.
Nos Estados Unidos, segundo a SEER 2009, entre 2004 e 2008 ocorreram cerca de 16,9 casos novos de câncer / 100.000 habitantes / ano3.
Em países desenvolvidos, o câncer infanto-juvenil é a segunda causa de óbito entre 0 e 14 anos, atrás apenas das causas externas (acidentes, violência). Tal fato deve-se, principalmente, às políticas de prevenção de outras doenças. A situação brasileira é semelhante, também ocupando o segundo lugar em causas de óbito na mesma faixa etária.
A probabilidade de um recém-nascido desenvolver câncer antes dos 20 anos é de 0,32%, e essa incidência aumenta 30% na raça branca quando comparada à negra, quando nos referimos, por exemplo, aos casos de leucemia linfoide aguda.
A proporção de sobreviventes ao câncer infanto-juvenil vem aumentando. Há estimativa de que, na população adulta, 1 em cada 1.000 pacientes abaixo de 45 anos seja sobrevivente ao câncer ocorrido em idade pediátrica4,5.
No Brasil, desde 1981, com a criação da Sociedade Brasileira de Oncologia Pediátrica (SOBOPE), a reunião de serviços especializados vem proporcionando o compartilhamento de experiências e dados entre as instituições, além do processo de educação continuada, preparando profissionais nos grandes centros, permitindo atuação dos mesmos em diferentes partes do país, divulgando o problema, principalmente alertando quanto ao diagnóstico precoce, utilização de protocolos terapêuticos reconhecidos internacionalmente, dando margem a levantamentos estatísticos importantes e conhecimento do alto grau de qualidade no tratamento e seguimento do câncer infanto-juvenil em nosso meio.
O câncer infanto-juvenil deve ser estudado separadamente do câncer do adulto por apresentar peculiaridades específicas no que diz respeito aos locais primários de acometimento, diferentes origens histológicas e diferentes comportamentos clínicos.
O câncer do adulto recebe influência significativa de fatores ambientais e comportamentais (tabagismo, alcoolismo, alimentação, exposição ao sol, dentre outros), além do próprio processo de senescência. Os tumores infanto-juvenis tendem a apresentar menores períodos de latência, costumam crescer rapidamente e tornarem-se bastante invasivos, porém respondem melhor à quimioterapia e apresentam melhor prognóstico2,4.
A maioria dos tumores infanto-juvenis apresenta achados histológicos que se assemelham a tecidos fetais nos diferentes estágios do desenvolvimento, sendo considerados embrionários. Essa semelhança a estruturas embrionárias gera grande diversidade morfológica resultante das constantes transformações celulares, podendo haver graus variados de diferenciação celular1.
Na adolescência, os tipos histológicos se assemelham mais aos tipos que ocorrem na criança do que os que ocorrem no adulto; porém com algumas particularidades, merecendo atenção especial, principalmente no que diz respeito aos protocolos utilizados pelos profissionais da área pediátrica, com influência marcante na sobrevida dessa faixa etária5.
A atuação crescente da genética no reconhecimento do comportamento biomolecular dos diferentes tipos de câncer traz expectativas promissoras na tentativa de individualização terapêutica e reconhecimento precoce das predisposições aos variados efeitos adversos5.
Quando consideramos a mortalidade por câncer, devemos incluir não somente os óbitos relacionados ao câncer propriamente dito, mas também os óbitos decorrentes do tratamento. Atribui-se como causa de óbito precoce (primeiro mês) mais a toxicidade da quimioterapia do que a progressão da doença. Os óbitos relacionados à sepse em pacientes com neutropenia, durante o tratamento, consistem na causa mais frequente de mortalidade. Ao longo dos anos, observamos uma queda gradual nas taxas de mortalidade por câncer. Segundo dados da SEER 9, a taxa de incidência do câncer em pacientes menores de 20 anos ao longo dos últimos 28 anos aumentou de 13,5 para 16,4/100.000 habitantes, enquanto que a taxa de mortalidade decresceu em aproximadamente 28% no mesmo período. Segundo a mesma fonte, a taxa de mortalidade apresentada em 2009 (2004 a 2008) foi de 2,6/100.000 habitantes3.
Diversos fatores podem interferir na probabilidade de sobrevida ao câncer infanto-juvenil, e um deles é o atraso no diagnóstico. Na população pediátrica, tanto a prevenção quanto o diagnóstico precoce são extremamente difíceis, com sinais e sintomas muitas vezes inespecíficos, confundindo-se com outras doenças sistêmicas comuns à infância, tornando-se um contínuo desafio ao pediatra. A sobrevida melhorou sensivelmente nos últimos anos, sobretudo graças às melhorias e à centralização do tratamento em instituições especilizadas4. Esses resultados também se devem, principalmente, ao treinamento de mais profissionais especializados, divulgação da importância do diagnóstico precoce, melhoria da sensibilidade dos métodos diagnósticos, utilização de protocolos terapêuticos poli-quimioterápicos mais eficazes, aplicabilidade da radioterapia pediátrica e avanços no suporte terapêutico no manuseio dos efeitos adversos precoces e tardios6,7. E nesse contexto a oncologia pediátrica brasileira tem ocupado posição de destaque no cenário internacional, tendendo a resultados promissores semelhantes aos países desenvolvidos.
Dentre os efeitos adversos decorrentes do tratamento do câncer, as complicações cardiovasculares ocupam lugar de destaque, só perdendo em frequência para as complicações infecciosas e recidiva da própria doença; são mais prevalentes em crianças menores de 5 anos, sexo feminino, negros e mestiços.
A terapêutica com antracíclicos ou por radioterapia (mediastinal ou da região cervical) são as causas mais comuns de complicações cardiovasculares. Além desses, outros agentes quimioterápicos também exercem potencial cardiotóxico5-8.
A incidência de insuficiência cardíaca congestiva, evidenciada clinicamente, tem sido reportada entre 2,8 a 10,0% e tem sido tema de crescente atenção por parte das sociedades de cardiologia e oncologia. Porém, outras formas de manifestação cardiovascular são reportadas, como veremos no decorrer dessa diretriz. Aproximadamente 2 em cada 3 crianças apresentarão alguma complicação cardíaca e cerca de 40% poderá desenvolver alguma consequência 30 anos ou mais após o término do tratamento, podendo evoluir ao óbito por causa da progressão dessa sequela9.
A importância do reconhecimento precoce e intervenção em tempo hábil nos diversos estágios das alterações cardiovasculares influencia diretamente na possibilidade de condução mais segura dos protocolos terapêuticos oncológicos, dando chances ao adequado seguimento desses pacientes, refletindo nas taxas de sobrevida de um novo e crescente grupo de pacientes que sobreviveu a alguma neoplasia na infância e que poderá apresentar sequelas importantes, limitando-os ativamente a médio ou longo prazo8.
É nosso papel transformar o paradigma da atenção ao câncer infanto-juvenil no país, considerando-o como um problema de saúde pública. Apesar da complexidade, a constante participação dos meios científicos na busca pela ampliação da visibilidade, o entendimento e a inclusão do controle do câncer na pauta cotidiana da sociedade refletirão no esforço conjunto pela construção de uma rede de atenção ao câncer com amplitude e consistência suficientes com o objetivo de garantir melhor qualidade de vida e, quando possível, a cura da doença.
3. Cardiotoxicidade
3.1. Conceito
A cardiotoxicidade é definida pela situação na qual agentes externos (químicos ou físicos) interferem negativamente no coração, determinando alterações estruturais, elétricas e funcionais no miocárdio. É considerada como o efeito colateral mais grave decorrente do tratamento com quimioterápicos, principalmente relacionada à doxorrubicina. Dados consistentes indicam que a morte do cardiomiócito ocorre principalmente por apoptose e necrose. Grande estresse oxidativo, danos ao DNA nuclear, modificações na bomba de cálcio e contratilidade celular, supressão da transcrição de fatores que regulam a sobrevivência da célula e a síntese de proteínas, bem como a perda da estabilidade do sarcômero e estímulo à autofagia também são fatores identificados como importantes nos mecanismos de morte do cardiomiócito.
Crianças e adolescentes são particularmente mais susceptíveis aos efeitos cardiotóxicos dos quimioterápicos, especialmente aos antracíclicos, uma vez que a perda de miócitos prejudica o crescimento cardíaco, resultando em inadequada massa ventricular esquerda residual e consequente cardiomiopatia no decorrer dos anos. Também contribuem para a disfunção cardíaca a atrofia e desarranjo das miofibrilas observadas após a quimioterapia10.
Em corações jovens, a repressão da proteína reguladora de genes que agem como fator de crescimento e morfogênese do miocárdio (CARP - cardiac ankyrin repeat protein) pela doxorrubicina também contribui com a maior injúria. Nos corações idosos, a farmacocinética da doxorrubicina é alterada pela lentificação no clearance da droga, causado pelo menor aporte de fluxo sanguíneo regional10. Além do mais, os mecanismos naturais de senescência também contribuem na diferença dessa faixa etária com a pediátrica.
Outra diferença da cardiotoxicidade entre jovens e adultos encontra-se na expressão de moléculas de sinalização para apoptose. A via de apoptose intrínseca é mais atuante em corações jovens e imaturos, podendo-se explicar o porquê da alta sensibilidade do grupo pediátrico aos danos provocados pela doxorrubicina10.
Atualmente, sabemos que mecanismos independentes relacionados à susceptibilidade individual, estudados pela farmacogenômica, podem sinalizar a apoptose celular por meio da inibição da expressão seletiva de genes específicos ao cardiomiócito.
Não existe um conceito padronizado de cardiotoxicidade que englobe achados clínicos e de exames complementares. De forma geral, conceitua-se cardiotoxicidade secundária ao tratamento do câncer como achado de sinais e sintomas clínicos de insuficiência cardíaca não atribuída a outras conhecidas causas como sepsis, insuficiência renal ou disfunção cardíaca prévia ao tratamento, documentada por exames complementares11.
Como manifestações de cardiotoxicidade, podemos encontrar discretas variações da pressão arterial, alterações eletrocardiográficas sutis até arritmias, pericardite, miocardite levando à cardiomiopatia com falência funcional do ventrículo esquerdo e insuficiência cardíaca congestiva, eventos tromboembólicos e até mesmo isquemia miocárdica e infarto agudo do miocárdio.
Podem ocorrer no início ou durante o tratamento, dias a semanas após o tratamento ou não ser aparente por meses ou até anos.
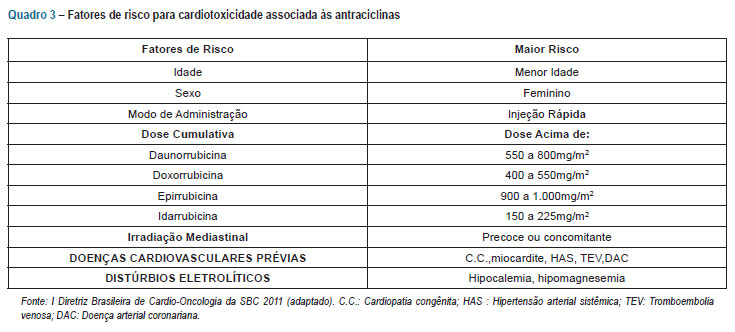
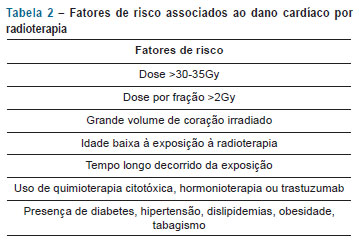
Existem fatores de risco, bem documentados, que predispõem à cardiotoxicidade e são considerados indicadores independentes para disfunção ventricular. Estes incluem dose cumulativa (antraciclinas, mitomicina), dose total administrada em um dia ou ciclo (ciclofosfamida, isofosfamida, carmustina, fluorouracil, cytarabina), esquema de administração em bolus ou lentamente (antraciclina), radiação mediastinal, idade, gênero feminino, administração concomitante de outros agentes cardiotóxicos, doença cardíaca preexistente, distúrbios eletrolíticos (principalmente hipocalemia e hipomagnesemia) (vide Quadro 3):
Além dos achados clínicos no diagnóstico da cardiotoxicidade, a ecocardiografia é aliada importante nessa definição. A porcentagem de encurtamento sistólico do ventrículo esquerdo é recomendada como índice para monitorização da função sistólica de pacientes em tratamento ou tratados com antraciclinas pelo Comitê de Cardiologia do Grupo de Estudos de Crianças com Câncer dos Estados Unidos8,12. Diferentes estudos utilizaram como base a fração de encurtamento e/ou a fração de ejeção para avaliar a função sistólica do ventrículo esquerdo13. Entretanto, sabe-se que estes índices apresentam algumas limitações na avaliação da função cardíaca, principalmente por sofrerem interferência das modificações na pré e pós-carga o que, particularmente, pode ocorrer durante a fase de quimioterapia, na presença de anemia, febre, infusão de grandes volumes e falência renal14. A disfunção ventricular associada às drogas quimioterápicas desenvolve-se por dois mecanismos: diminuição na contratilidade e/ou aumento na pós-carga15,16.
De maneira mais específica, a maioria dos estudos relaciona o conceito de cardiotoxicidade diretamente às medidas de função sistólica ventricular esquerda, principalmente avaliadas ao ecocardiograma, considerando como toxicidade cardíaca11-13:
Fração de encurtamento do ventrículo esquerdo <28% ou uma diminuição, em valor absoluto, >a 10 unidades em relação ao valor basal pré-quimioterapia;
Fração de ejeção ventricular esquerda:
Grau I: redução assintomática da FEVE em 10 a 20% do exame basal
Grau II: redução da FEVE mais que 20% do exame basal ou redução abaixo dos limites normais
Grau III: Insuficiência cardíaca clinicamente sintomática
Fração de ejeção menor que 50% contraindica o uso do antracíclico.
A cardiotoxicidade pode ser detectada por meio de análise criteriosa dos fatores de risco, monitorização dos sinais e sintomas durante e após a quimioterapia e contínua avaliação por exames complementares proporcionando identificação precoce e intervenção clínica em tempo hábil. Todos os pacientes devem ser orientados, antes do início do tratamento, quanto aos riscos de cardiotoxicidade, da necessidade de acompanhamento a longo prazo e da importância da manutenção de um estilo de vida saudável para prevenção ou melhor prognóstico de doenças cardiovasculares e metabólicas13-15.
3.2. Classificação
A cardiotoxicidade pode apresentar-se de forma aguda, subaguda ou crônica, na dependência da época de aparecimento das manifestações clínicas e achados aos exames complementares.
Cardiotoxicidade Aguda: forma rara de cardiotoxicidade que ocorre imediatamente após uma única dose de quimioterápico, ou no curso da terapia, onde as manifestações clínicas se apresentam dentro da primeira semana de tratamento.
Cardiotoxicidade Subaguda: semanas ou meses após o início do tratamento e geralmente de forma insidiosa.
Tanto a forma aguda quanto a subaguda podem se apresentar como alterações transitórias ao eletrocardiograma (ECG), síndrome miopericárdica ou falência aguda do ventrículo esquerdo. Ao ECG, pode-se encontrar alterações inespecíficas da repolarização, diminuição da voltagem dos complexos QRS, prolongamento do intervalo QT. A taquicardia sinusal é a alteração do ritmo mais frequente. Alterações ao ECG são encontradas em cerca de 20 a 30% dos pacientes. Arritmias incluem taquicardias supraventriculares, ventriculares e juncionais (0,5-3%). Arritmias mais graves como flutter ou fibrilação atrial são raras.
Cardiotoxicidade Crônica: pode ser dividida em dois tipos:
crônica precoce (dentro do primeiro ano pós-tratamento)
crônica tardia (depois do primeiro ano e até vários anos após o término da terapia).
Geralmente, a cardiotoxicidade crônica apresenta-se como disfunção ventricular sistólica ou diastólica. Enquanto a cardiomiopatia dilatada (disfunção sistólica do ventrículo esquerdo) pode ocorrer imediatamente após altas doses de quimioterápicos ou no decorrer de meses ou anos, a cardiomiopatia restritiva é de ocorrência sempre crônica. A cardiomiopatia restritiva (disfunção diastólica do ventrículo esquerdo), que ocorre mais frequentemente pós-radioterapia, desenvolve-se em muitos sobreviventes ao longo do tempo, podendo levar à insuficiência cardíaca com função sistólica normal.
3.3. Aspectos anatomopatológicos
A ação adversa de drogas pode ser desencadeada por hipersensibilidade, toxicidade direta, interação medicamentosa etc. O efeito cardiotóxico, diferente da reação de hipersensibilidade, é, em geral, dose dependente e cumulativo, podendo levar, em longo prazo, à doença cardiovascular, importante causa de morte no seguimento tardio de pacientes com câncer, especialmente o grupo pediátrico16.
Os mecanismos de injúria miocárdica, como já referidos, são complexos9 e estão intimamente relacionados ao tipo de tratamento antitumoral, ao tipo de neoplasia e às alterações anatomopatológicas que se apresentam no coração. No caso das antraciclinas, por exemplo, a formação de radicais livres ou espécies reativas de oxigênio são a principal via de agressão com dano direto ao miócito9. Por sua vez, agentes alquilantes e antimetabólicos tais como cisplatina e 5-fluouracil lesam o miocárdio por isquemia secundária a vasoespasmo e trombose17.
A ação cardiotóxica da droga ou de seus metabólitos no miocárdio é ampla atingindo miócitos, células endoteliais e interstício18. Porém, o efeito tóxico direto não é o único responsável pelas manifestações clínicas e anatomopatológicas. Uma série de comorbidades pode desencadear ou contribuir para disfunção cardíaca tais como miocardites, distúrbios metabólicos e renais capazes de gerar arritmias etc. Além disso, a inespecificidade das alterações histopatológicas frente à multiplicidade de agentes agressores nem sempre permite o diagnóstico morfológico de cardiotoxicidade, especialmente na fase crônica da lesão16,19,20. Isso talvez explique a discrepância entre manifestações clínicas e anatomopatológicas16,21,22. Em trabalho de autópsia, quase um terço dos pacientes com sinais de cardiotoxicidade por antraciclina não apresentou alterações morfológicas no coração22. Ao mesmo tempo, boa parte dos pacientes sem manifestações clínicas de cardiotoxicidade exibiu anormalidades cardíacas ao exame anatomopatológico, o que sugere o efeito tóxico prolongado e silencioso da droga sobre o coração.
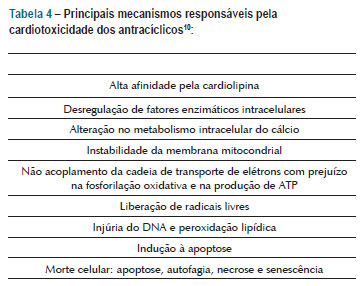
Do ponto de vista anatomopatológico, as alterações cardíacas são quase sempre inespecíficas, sejam elas induzidas por quimioterápicos ou por radiação22, e resultam do somatório dos diversos fatores de risco para lesão cardiovascular como previamente mencionado9. O Quadro 4 relaciona as principais alterações morfológicas encontradas.
Poucos trabalhos estão voltados inteiramente para o estudo histopatológico da cardiotoxicidade por anticancerígenos23. Tanto em humanos quanto em modelos animais, descrevem-se alterações agudas e crônicas, especialmente ao uso de antracíclicos18. A cardiotoxicidade aguda é rara e está associada a tratamentos agressivos. Histologicamente se expressa por necrose isquêmica, alterações inflamatórias pericárdicas e miocárdicas22,23 e degeneração miocelular caracterizada por redução de miofibrilas com vacuolização citoplasmática24. A toxicidade crônica por sua vez é dominada por lesões fibrosantes, sendo a forma mais frequente e de maior repercussão clínica.
De um modo geral, tanto o pericárdio quanto o miocárdio e endocárdio podem estar comprometidos de forma isolada ou global, sendo o padrão das lesões dependente do esquema terapêutico empregado. A toxicidade por antraciclina, por exemplo, acomete geralmente o miocárdio enquanto o efeito radioterápico se estende a todos os componentes do coração. Miopericardites, fibrose pericárdica e lesões de valvas e artérias coronárias são comuns após radiação, mas podem ocorrer após exposição a diversos tipos de agentes antitumorais17,20,22. Na radioterapia, o pericárdio é o principal alvo de injúria usualmente iniciada por pericardite fibrinosa e derrame pericárdico, seguidos por espessamento fibroso preferencialmente no pericárdio parietal e ventrículo direito20,22, podendo estender-se ao mediastino. O comprometimento valvar é menos frequente e, ao contrário do que ocorre no pericárdio, atinge mais o lado esquerdo do coração. Os folhetos tornam-se espessados, podem calcificar e levar a insuficiência e estenose principalmente das valvas mitral e aórtica.
No miocárdio, dependendo do agente e do tempo de agressão, é possível encontrar focos de degeneração e hipertrofia miocíticas, apoptose, necrose, inflamação e fibrose com intensidade e distribuição variáveis. Em geral, o infiltrado inflamatório miocárdico não é expressivo. Quando presente é mononuclear e menos frequentemente misto24, e deve ser diferenciado do infiltrado inflamatório de origem isquêmica ou de origem infecciosa. Na cardiotoxicidade por antraciclina, a inflamação usualmente é discreta ou ausente. Apoptose não é habitualmente encontrada ao exame histológico e parece ter papel insignificante ao menos na fase aguda de toxicidade por antracíclicos25. Um aspecto morfológico característico e bem evidente ao exame ultraestrutural é a vacuolização citoplasmática dos miócitos por ação da adriamicina (adria cells). A presença expressiva de eosinófilos no miocárdio sugere reação de hipersensibilidade e foi descrita após tratamento com interleucina-2. Vasculites são incomuns na miocardite por quimioterápicos. Por outro lado, dano endotelial representado por vasoespasmo e trombose da microcirculação se acompanham de isquemia miocárdica e são comuns a certos agentes17,20. A ciclofosfamida é exemplo no qual a lesão vascular desenvolve padrão hemorrágico de necrose isquêmica representada por extensas bandas de contração miocítica, miocitólise e inclusões eletrodensas intramitocondriais18,24,26. Focos de necrose isquêmica, não relacionados à distribuição anatômica coronariana, são também observados no miocárdio exposto à radiação22.
Na fase crônica de cardiotoxicidade, o exame anatomopatológico pode evidenciar alterações consistentes com cardiomiopatia, frequentemente do tipo dilatada. O coração apresenta aumento de peso, dilatação e adelgaçamento da parede ventricular. Ao exame histológico, evidencia-se atrofia de miofibras e fibrose endomiocárdica associada ou não à trombose mural. A fibrose pode ser perivascular ou de padrão cicatricial, na qual faixas de colágeno isolam grupos de miócitos. A hipertrofia pode ser inconspícua23. De permeio, encontram-se miócitos com alterações degenerativas e mínima reação inflamatória. Esse quadro morfológico, comum na cardiotoxicidade por antraciclina, é indistinguível da cardiomiopatia dilatada de outras causas. Cardiomiopatias hipertrófica e restritiva também são descritas no espectro das lesões induzidas por antracíclicos.
Na radioterapia, o padrão restritivo é o mais observado17,20. Além das lesões pericárdicas e valvares, a radiação leva à fibrose miocárdica difusa, especialmente da parede anterior do ventrículo esquerdo, relacionada à área irradiada. Dano endotelial favorece aterogênese precoce com desenvolvimento de placas ateroscleróticas complicadas por hemorragia e inflamação com riscos de ruptura e trombose22.
A biópsia endomiocárdica, apesar de não ser realizada de rotina, pode ser útil para estabelecer o diagnóstico morfológico de miocardite, e evidenciar alterações miocelulares19 que se correlacionam com o aumento sérico de troponina. Estudos demonstram que as alterações histológicas podem estar presentes mesmo com uso de baixas doses de antraciclina e antes de mudanças bioquímicas mensuráveis20 e de eventos clínicos21, sendo uma fonte para estudo comparativo quando da necessidade de introdução de novos agentes antineoplásicos.
4. Tumores cardíacos
As neoplasias cardíacas são raras, com prevalência de 0,001% a 0,3% em séries de autópsias27-29. Os tumores secundários são mais frequentes que os primários, mas raramente relatados nas séries clínicas27,28. No grupo fetal e neonatal, ocorre predomínio de tumores primários benignos, principalmente rabdomioma30. De maneira geral, no grupo das neoplasias primárias, há predomínio absoluto dos tumores benignos sobre os malignos, sendo os tipos histológicos e as apresentações clínicas dependentes da faixa etária. Somente 25% dos tumores primários são malignos, sendo os sarcomas os tipos mais prevalentes neste grupo31. A melhoria das técnicas de imagem tem aumentado o número de casos diagnosticados em vida28 com sobrevida global29,30, entretanto, os dados de autópsia são ainda fundamentais naqueles clinicamente silentes.
Existem associações com síndromes genéticas tais como Carney, neurofibromatose, esclerose tuberosa, Síndrome de Gorlin-Goltz e Beckwith-Wiedemann sendo, por vezes, a detecção do tumor cardíaco o primeiro sinal da doença genética subjacente30.
O quadro clínico encontra-se na dependência da localização, tamanho da lesão, relação com estruturas adjacentes, fração de ejeção e dimensões da câmara afetada, bem como da faixa etária. Aproximadamente 12% dos casos são assintomáticos32. As principais manifestações incluem insuficiência cardíaca, tromboembolia e arritmias28,33. Nos tumores malignos há infiltração de estruturas adjacentes e derrames pericárdicos que podem ocasionar tamponamento e óbito32. Dos tumores benignos os mais comuns são: rabdomioma, teratoma, fibroma, mixoma e tumores vasculares.
O rabdomioma cardíaco acomete preferencialmente o grupo pediátrico, correspondendo a mais de 60% dos tumores cardíacos neste grupo etário27,29,30. É excepcionalmente raro na população adulta com poucos relatos na literatura27. Aproximadamente 75% dos casos são diagnosticados no primeiro ano de vida, sendo 1/3 abaixo do primeiro mês30. Nas séries de autópsias, a incidência varia de 0,002 a 0,25%, sendo 0,02% a 0,08% nos nascidos vivos e 0,12% nos estudos de imagem pré-natal fetal30. Constitui-se, portanto, na neoplasia primária cardíaca mais comum em crianças. A sintomatologia clínica relaciona-se à presença da massa tumoral com obstrução do fluxo sanguíneo, comprometimento miocárdico e arritmias30,32,34. Pode-se observar sopro, geralmente sistólico na borda esternal direita ou esquerda e insuficiência cardíaca30. A detecção de arritmia no período antenatal torna mandatória a realização de ecocardiografia fetal. As arritmias podem ser de difícil controle, com achados eletrocardiográficos pós-natais bastante variados30. Há forte associação entre a presença de rabdomiomas cardíacos e esclerose tuberosa27,34, sendo observado em até 50% das crianças com esta doença genética30. Quando múltiplos, podem ser a primeira manifestação da esclerose tuberosa, levando-se em conta a alta porcentagem de mutações espontâneas em famílias sem histórico da doença30. No período antenatal, o ultrassom de rotina e a ecocardiografia fetal são ferramentas diagnósticas importantes, detectando mais da metade dos casos, haja vista a grande quantidade de tumores assintomáticos neste período. No período pós-natal, a radiografia do tórax pode mostrar cardiomegalia com trama vascular normal ou aumentada30. A esclerose tuberosa é doença autossômica dominante, causada por mutações nos genes supressores de tumor TSC1 (localizado no cromossomo 9q34) ou TSC2 (localizado no cromossomo 16p13.3), que codificam respectivamente as proteínas hamartina e tuberina, caracterizada pela tríade clássica de retardo mental, epilepsia e angiofibromas faciais30. Pode haver ainda gliomas corticais e subependimários, bem como cistos renais; já os angiolipomas são somente observados na vida adulta30. Pode, numa menor proporção, ser esporádico e associar-se a malformações cardíacas variadas27, como por exemplo: Ebstein, CIA, tetralogia de Fallot, síndrome do ventrículo esquerdo hipoplásico, piorando o tratamento e a sobrevida; o mesmo ocorrendo quando cursa com hidropsia fetal não imunológica30. O prognóstico é bom com altos índices de sobrevida30,34,35. Os rabdomiomas apresentam padrão de crescimento bifásico, com aumento progressivo até a idade gestacional de 32 semanas, com regressões completas ou parciais até o primeiro ano de vida30. Por esta razão, a conduta nesta faixa etária tende a ser conservadora, a menos que o paciente esteja apresentando sinais de disfunção cardíaca, o que piora o prognóstico30,32. Macroscopicamente observam-se um ou mais nódulos sólidos, de consistência elástica, castanho-amarelados, tendo por localização preferencial os ventrículos, principalmente na região septal, muitas vezes ocasionando obstrução ao fluxo sanguíneo27,30. São tumores não infiltrativos, não metastatizantes, sem atipias ou mitoses30. Microscopicamente as células tumorais são grandes, o citoplasma é vacuolizado, rico em glicogênio e se cora pelo PAS sem diastase. O núcleo é redondo e central e conecta-se à parede celular através de delicados filetes onde se detectam estriações transversais periféricas conferindo à célula o clássico aspecto de aranha (spiders cells)27,30. Imuno-histoquimicamente expressam vimentina e os marcadores musculares desmina e actina, além de ubiquitina27. Esta proteína estaria relacionada à degradação dos miofilamentos, levando à apoptose. Nos adultos com lesões celulares pode haver expressão do Ki67, que em geral é negativo nos casos pediátricos27.
Apesar de raros, mais de 2/3 dos teratomas são diagnosticados na população pediátrica, sendo a segunda neoplasia no grupo fetal30. Localizam-se principalmente no pericárdio próximo aos vasos da base sendo, nesta localização, o derrame pericárdico a principal sintomatologia. Mais raramente afetam o miocárdio com poucos casos descritos na literatura, podendo ocasionar óbito intraútero ou morte súbita. Cianose, insuficiência cardíaca congestiva e desconforto respiratório também são relatados30. Os teratomas são macro e histologicamente idênticos àqueles em outras localizações do corpo. São em geral massas sólido-císticas, com elementos maduros e imaturos, principalmente neuroepiteliais, cuja presença não está relacionada ao prognóstico.
Os fibromas constituem-se na segunda ou terceira neoplasia no grupo pediátrico, dependendo da faixa etária do estudo30. Em geral são nodulares e únicos, sem tendência à regressão, podendo associar-se à Síndrome de Gorlin27. Localizam-se preferencialmente no septo ou na parede livre ventricular30. Macroscopicamente firmes, nodulares, não encapsulados, bem ou mal delimitados, com ou sem calcificações27. Histologicamente são compostos por fibroblastos, por vezes estelares, imersos em abundante matriz colágena que expressa vimentina e actina. A celularidade vai gradativamente diminuindo e aumentando o colágeno nas lesões mais antigas30. Podem ser observadas células inflamatórias tais como linfócitos e mastócitos, além de fibras elásticas detectadas pelo Verhoeff27. As células expressam vimentina e actina antimúsculo liso, fenótipo de fibroblastos/miofibroblastos. O tratamento curativo é a excisão completa da lesão32, o que nem sempre é possível pelo tamanho e aspecto infiltrativo. Nestas situações, pode-se considerar a possibilidade de ressecções parciais ou transplante cardíaco27.
O mixoma cardíaco é a neoplasia cardíaca primária benigna mais comum em adultos, compreendendo 50% de todos os tumores neste grupo com incidência aumentando a partir da terceira à sexta década de vida, afetando preferencialmente mulheres numa proporção de 2:132. Na população pediátrica ocorre principalmente em crianças mais velhas, sendo muito raro em fetos e neonatos, havendo relatos desta neoplasia em natimortos30. Mais comumente, encontra-se sob a forma esporádica, sendo denominados sindrômicos aqueles geralmente múltiplos e associados clinicamente à presença de manchas pigmentadas na pele, tumores da bainha do nervo periférico e endocrinopatias. A "síndrome do mixoma" corresponde a doenças genéticas diversas que incluem: síndrome LAMB (lentigenes, atrial myxomas and blue nevi), NAME (nevi, atrial myxomas, myxoid neurofibroma and ephelides) e Carney (mixomas atriais, cutâneos e fibroadenoma mixoide mamário, lentigo, nevo azul, doenças endócrinas tais como hiperplasia adrenal e gigantismo e tumor de células de Sertoli testicular)30. Geralmente estes quadros sindrômicos não são completamente expressos até a segunda ou terceira década de vida30. Nos pacientes diagnosticados com mixoma cardíaco abaixo de 40 anos deve-se pensar nessa possibilidade e realizar nos parentes de primeiro grau screening diagnóstico da doença32. A maior parte dos mixomas cardíacos localiza-se no átrio esquerdo, aderidos ao septo atrial ou adjacentes à fossa oval27,32; contrariamente, na casuística de Isaacs31, de tumores fetais e neonatais, a maioria acometeu o átrio direito. Pode se originar ainda na parede ventricular e nas valvas. As manifestações clínicas dependem, portanto, da localização tumoral e da existência de cardiopatias congênitas. Os originados no átrio, podem projetar-se por intermédio da valva atrioventricular para a câmara ventricular correspondente. Os que acometem o lado esquerdo podem apresentar quadros embólicos sistêmicos (cerebral ou periférico) e insuficiência cardíaca por obstrução mitral. Os que ocorrem no lado direito, além do comprometimento das valvas tricúspide e pulmonar, podem apresentar também distúrbios da condução. Sintomas constitucionais com manifestações inflamatórias e autoimunes, causadas pela secreção tumoral de citocinas, principalmente interleucina-6, foram relatados, tais como: anemia, febre, perda de peso, leucocitose, aumento do VHS e de imunoglobulinas27. No grupo pediátrico, cianose, sopro e insuficiência cardíaca congestiva foram os sinais mais comuns da doença, podendo haver também embolia paradoxal. O diagnóstico de mixoma cardíaco requer intervenção cirúrgica imediata pelo alto risco de morbimortalidade, sendo a principal delas a embolização (observada em até 1/3 dos pacientes), além da morte súbita32. No grupo infantil e neonatal, a maior parte das vezes tem curso fatal30. Macroscopicamente são polipoides com base de adesão ampla, amolecidos e gelatinosos30. Os sólidos são lobulados e lisos. Quando papilíferos e friáveis, têm maior tendência embólica e geralmente exibem trombos organizados em sua constituição. Outros achados macroscópicos incluem: áreas císticas, necróticas, hemorrágicas e focos de calcificação27. Microscopicamente, apresentam células estelares ou poligonais, com citoplasma eosinofílico com bordas indistintas e núcleos ovoides, com nucléolos variando de inconspícuos a grandes, imersas em abundante estroma mixoide frouxo com alto teor de mucopolissacarídeos. Arranjam-se em cordões curtos, sincícios e em múltiplas camadas de anéis ao redor de vasos27. Células endoteliais recobrem externamente a neoplasia e invaginam-se para o interior tumoral. A matriz contêm fibras elásticas e colágeno além de focos de hematopoiese extramedular, calcificações distróficas, às vezes com formações de corpúsculos de Gamna-Gandy, ossificação metaplásica, hemácias extravasadas e hemorragia antiga com pigmento de hemossiderina27. Acredita-se que a neoplasia origine-se de células mesenquimais primitivas multipotentes, morfologicamente similares às células embrionárias do coxim endocárdico30, que podem diferenciar-se para miofibroblastos, fibroblastos, músculo liso e células endoteliais, diferenciação esta documentada estrutural e imuno-histoquimicamente pela expressão de vimentina, CD34 e marcadores musculares. Aproximadamente 75% das células tumorais expressam calretinina, o que auxilia muito o diagnóstico além dos achados morfológicos26. São descritos raramente elementos heterólogos intratumorais tais como epitélio colunar glanduliforme e restos tímicos27,29. O principal diagnóstico diferencial é feito com trombos organizados27. A possibilidade de malignização é controversa na literatura. Muitos autores denominam mixossarcomas tumores que apresentem necrose, hiper-celularidade, atipia e caráter francamente invasivo, refutando a ideia de que estes achados histológicos adversos representem transformação maligna de mixomas preexistentes27.
Os hemangiomas cardíacos são raros, podendo ocorrer em qualquer localização no coração e no pericárdio. A presença de derrame pericárdico é o achado principal e, quando diagnosticado intraútero, pericardiocenteses podem evitar a hidropsia e o tamponamento cardíaco. No período fetal e neonatal são em geral cavernosos, capilares ou mistos. O hemangioendotelioma Kaposiforme da infância e o hemangioma em tufos que acometem o coração associam-se à síndrome de Kassabach-Merrit, com coagulopatia de consumo e diátese hemorrágica30.
O fibroelastoma papilífero constitui-se em lesão mais comum na sexta década de vida, sendo raros os casos pediátricos27. Na casuística de Sun e cols.36, de 162 pacientes, há relato de um caso ocorrendo no período neonatal, e na de Gowda e cols.37, de 725 casos de fibroelastoma papilífero, somente 10 ocorreram em crianças abaixo dos 10 anos. A maior parte dos casos é assintomática, sendo diagnosticados durante exames cardiológicos de rotina ou na autópsia, entretanto, podem ocorrer embolia, insuficiência cardíaca ou morte súbita. Macroscopicamente, são de aspecto vegetativo, papilífero, localizados principalmente na superfície valvar onde são detectados aproximadamente 70% dos casos27,36. A maioria compromete o lado esquerdo, principalmente a valva aórtica36. Histologicamente, observam-se nas papilas, eixo conjuntivo com porção central avascular de aspecto fibroso, tecido mixomatoso periférico e revestimento por células endoteliais hiperplásicas que imunoexpressam CD34 e Fator VIII. Diferem dos mixomas, pois no estroma não se identificam células com expressão de actina36. A histogênese da lesão permanece desconhecida27,35,36.
As neoplasias cardíacas malignas primárias e metastáticas têm prognóstico ruim, exigindo abordagem multidisciplinar29. Os tumores primários malignos são excepcionalmente raros, sendo os sarcomas os mais prevalentes. Há, entretanto, relatos de neoplasias germinativas malignas, tumor rabdoide, linfomas etc. No grupo dos sarcomas primários cardíacos, o rabdomiossarcoma é o prevalente na população pediátrica, sendo o subtipo embrionário o mais comum30. A Organização Mundial da Saúde define o rabdomiossarcoma como "neoplasia mesenquimal maligna com forte tendência à miogênese". Acresce-se a esta definição o fato de ser esta a única linha de diferenciação tumoral, sendo imprescindível identificar esta miogênese seja pela coloração de HE, por métodos imuno-histoquímicos ou, menos raramente, através da microscopia eletrônica. Macroscopicamente, observam-se massas branco-acinzentadas, amolecidas, gelatinosas, com ou sem necrose e hemorragia. A neoplasia é altamente celular e proliferativa, composta por células fusiformes ou redondas, com citoplasma eosinofílico onde se pode eventualmente identificar estriações transversais. À imuno-histoquímica, as células neoplásicas expressam: vimentina, mioglobina, pan-actina, actina sarcomérica, desmina, MyoD1 e miogenina30. Não é raro a doença apresentar-se já disseminada ao diagnóstico32, lembrando-se que, ao contrário da maioria dos sarcomas, a disseminação linfática para linfonodos mediastinais pode ser observada, além dos pulmões, timo por contiguidade, osso e medula óssea. Na população pediátrica os fibrossarcomas cardíacos mais prevalentes são de tipo infantil ou congênito30, com o clássico padrão histológico em "espinha de peixe", ocasionado pelo fato de as células tumorais arranjarem-se em fascículos, em geral longos, que se entrecruzam na porção central30. A neoplasia é infiltrativa e, portanto, com prognóstico reservado. Há relatos de casos de vários outros tipos de sarcomas, como por exemplo o sarcoma sinovial, que compreende 5% dos sarcomas cardíacos e 1% de todos os tumores primários37,38.
Quando nos referenciamos às metástases cardíacas, de maneira geral, independentemente da faixa etária, a incidência em pacientes com neoplasias malignas é de aproximadamente 10% em séries de autópsias29. As metástases cardíacas podem ser das mais variadas e os tipos histológicos diferem significativamente entre adultos e crianças, refletindo a incidência variada dos tumores primários nestas faixas etárias. Pode haver comprometimento cardíaco por contiguidade; em geral, o lado direito do coração é o mais acometido27. O nefroblastoma (tumor de Wilms)39, principal neoplasia maligna renal na infância, apresenta tendência a infiltrar a veia renal e veia cava inferior, havendo extensão atrial em até 0,7% dos casos38,39. Com a quimioterapia é possível aumentar o número de metástases cardíacas necróticas ressecáveis, como nos casos de osteossarcoma descritos por Montpréville30 e Santos40,41. Porém o prognóstico é bastante reservado neste grupo de pacientes.
5. Avaliação cardiovascular inicial da criança oncológica
Sabendo-se que o tratamento oncológico pode exercer potencial repercussão cardiovascular, especialmente na população em fase de desenvolvimento físico (crianças e adolescentes), o devido conhecimento cardiovascular prévio desses candidatos ao tratamento quimioterápico, radioterápico ou cirúrgico, proporciona maior segurança à equipe oncopediátrica na condução de protocolos específicos com menor risco de eventos adversos42.
A avaliação cardiológica deve ser realizada antes de qualquer procedimento terapêutico. A partir do momento em que o cardio-oncologista pediátrico identifica algum fator de risco prévio que possa comprometer o andamento do tratamento, a equipe oncopediátrica deverá ser comunicada para adequar o plano terapêutico à situação física identificada.
A avaliação cardiológica inicial deverá ser constituída por:
Anamnese: aspectos gerais da anamnese pediátrica; antecedentes patológicos remotos e recentes; presença de cardiopatia congênita; antecedentes familiares, principalmente os relacionados aos fatores de risco cardiovascular (hipertensão arterial sistêmica, diabetes mellitus, dislipidemias, doença arterial coronariana; tabagismo passivo ou ativo; drogas); informações sobre medicamentos de uso rotineiro e reações alérgicas;
Exame físico: aspectos gerais, dados antropométricos; sinais vitais; semiologia cardiovascular clássica (inspeção geral; palpação dos pulsos periféricos, precórdio, abdome, membros; ausculta cardíaca);
Eletrocardiografia: avaliação das 12 derivações com os devidos cálculos de intervalos de tempo dos eventos elétricos e cálculo do QT corrigido;
Radiografia do tórax PA e perfil esquerdo: avaliação do arcabouço ósseo; relação das vias aéreas; vasculatura e parênquima pulmonar; situs, área cardíaca e silhueta das estruturas;
Dosagem de biomarcadores (TroponinaT, NTpró-BNP): conhecimento dos níveis basais para consequente comparação evolutiva durante e após a infusão de quimioterápicos sabidamente cardiotóxicos, principalmente doxorrubicina.
Ecocardiografia: avaliação da anatomia cardíaca; dopplerfluxometria espectral com mapeamento de fluxo em cores; avaliação da função diastólica; avaliação da função sistólica por meio da observação da contratilidade global e segmentar, além da quantificação da fração de encurtamento e da fração de ejeção pelos métodos de Teichholz e Simpson e, se possível, avaliação da deformidade miocárdica pelo método do speckle tracking; estimativa da pressão sistólica arterial pulmonar e débito cardíaco.
Avaliações cardiológicas subsequentes são recomendadas antes dos ciclos quimioterápicos, radioterápicos ou pré-operatórios, ou sempre que sinais ou sintomas forem suspeitos. Desse modo, métodos adicionais de investigação cardiológica deverão ser considerados (vide próximas sessões).
6. Agentes quimioterápicos e cardiotoxicidade
Agentes quimioterápicos são há muito conhecidos pelos seus efeitos adversos. Nos princípios gerais da quimioterapia, sabe-se que a maioria das drogas anticâncer tem mecanismos de ação não seletivos para células neoplásicas e células normais, e que a maioria delas produz seu efeito citotóxico interferindo com a síntese ou função dos ácidos nucleicos RNA e DNA.
Alguns desses efeitos, como a toxicidade medular (mielossupressão), náuseas e vômitos, alopécia, mucosite oral e intestinal, anormalidades de função hepática e renal, reações alérgicas sistêmica ou cutânea, são consequências inevitáveis do mecanismo de ação dos agentes citostáticos e/ou citotóxicos em células que se dividem rapidamente. Tais efeitos podem ser revertidos espontaneamente, ser tratados com medicação apropriada ou mudança no esquema de administração da droga e, via de regra, deixam poucas sequelas.
Outros efeitos são mais insidiosos e tendem a surgir em tecidos normais, como o coração, composto por células com uma capacidade regenerativa limitada. Na última década, a comunidade científica assistiu a uma acelerada aprovação de novas drogas que claramente melhoraram a sobrevida dos pacientes com câncer. Infelizmente, entretanto, o tão sonhado objetivo de combinar melhor atividade antineoplásica com redução da toxicidade não foi totalmente obtido por esses novos medicamentos, nem mesmo com a chamada terapia-alvo. A colaboração próxima entre cardiologistas e oncologistas demonstrou que a cardiotoxidade permanece um problema, particularmente quando as velhas drogas são combinadas com as novas terapias, na tentativa de se obter melhores taxas de cura43.
6.1. Antraciclinas
As antraciclinas fazem parte do grupo dos antibióticos antitumorais, ou seja, são produtos naturais do metabolismo microbiano e foram inicialmente isolados da fermentação de espécies de Streptomyces.As antraciclinas estão entre os quimioterápicos de uso mais frequente em oncologia pediátrica, com eficácia comprovada em vários tumores sólidos e hematológicos. Fazem parte deste grupo a doxorrubicina, daunorrobicina, idarrubicina, epirrubicina e mitoxantrona.
As antraciclinas são os quimioterápicos mais comumente associados à toxicidade cardíaca e, embora não existam estudos epidemiológicos conclusivos quanto à sua incidência, há consenso a respeito da associação entre risco de cardiotoxicidade e dose cumulativa, tipo de antraciclina utilizada, doença cardíaca preexistente, radioterapia mediastinal e uso de antraciclinas em combinação com outras drogas.
As evidências sugerem que as antraciclinas lesam os miócitos por meio da geração de radicais livres e incorporação de ferro44. Os miócitos são mais susceptíveis à lesão por radicais livres por causa de seu alto metabolismo oxidativo e relativa falta de defesas antioxidantes. Além disso, as antraciclinas têm alta afinidade por cardiolipina, um fosfolípide da membrana mitocondrial, resultando em um acúmulo de antracíclicos nas células cardíacas45. Histologicamente, nota-se perda de miofibrilas e vacuolização citoplasmática secundária à dilatação do retículo sarcoplasmático das células miocárdicas.
Três formas distintas de cardiotoxicidade induzida por antraciclinas têm sido descritas: aguda, subaguda e crônica (precoce e tardia)46. A toxicidade aguda ocorre imediatamente após a administração dos antracíclicos e pode se manifestar como arritmia transitória (taquicardia supraventricular, ectopia ventricular), pericardite, miocardite ou falência ventricular esquerda. Tais manifestações raramente ocorrem com as terapias atuais e são geralmente reversíveis. A forma subaguda acontece semanas ou meses do início do tratamento, com manifestações clínicas similares à forma aguda. A cardiomiopatia crônica frequentemente ocorre dentro do primeiro ano após o tratamento com antracíclicos. A cardiotoxicidade de início tardio desenvolve-se anos ou décadas após o término do tratamento e manifesta-se como disfunção ventricular e/ou arritmia em indivíduos previamente assintomáticos. Pode ocorrer espontaneamente ou coincidir com exercício, gravidez, procedimento anestésico ou terapia com hormônio de crescimento.
Tanto a cardiotoxicidade crônica quanto a de início tardio são dose-dependentes. Em um estudo em adultos, a incidência de insuficiência cardíaca congestiva (ICC) e cardiomiopatia aumentou de 4% com dose cumulativa de doxorrubicina de 500-550 mg/m2 para 18% com doses de 551-600mg/m2, até chegar aos 36% com doses cumulativas acima de 600mg/m247. Em crianças, doses menores de antracíclicos foram associadas com risco de cardiotoxicidade crônica48, havendo um aumento de 11 vezes no risco de ICC com dose cumulativas >300 mg/m2 quando comparado com doses <300 mg/m2. Outros fatores associados com o aumento do risco de cardiomiopatia secundária às antraciclinas são: idade menor que 5 anos, sexo feminino, raça negra, terapia combinada com outras drogas (ciclofosfamida, por exemplo), radioterapia mediastinal, doença cardíaca preexistente (coronariana, valvar ou miocárdica), hipertensão arterial, hipertermia e hepatopatia48. Embora estudos antigos em adultos tenham sugerido uma redução na prevalência de cardiotoxicidade com a infusão contínua de antracíclicos quando comparada com a administração em bolus48, relatos recentes em pacientes pediátricos demonstraram que a infusão contínua não confere cardioproteção49,50.
O diagnóstico de cardiomiopatia após uso de antraciclinas pode ser feito em bases clínicas e laboratoriais. Além disso, vários exames complementares podem ser utilizados para identificar lesão miocárdica subclínica, incluindo exames de imagem, medicina nuclear, dosagem de marcadores de lesão tecidual e biópsia endomiocárdica. Tais métodos serão discutidos nos próximos capítulos desta diretriz. O tratamento das diferentes manifestações cardíacas associadas às antraciclinas também serão abordados separadamente.
A prevenção da cardiomiopatia induzida pelas antraciclinas representa um importante foco de pesquisa (vide Capítulo 9). Os protocolos contemporâneos para crianças com neoplasias de baixo risco que rotineiramente limitam a dose de antraciclinas e reduzem a dose e o volume de radioterapia, provavelmente diminuirão a incidência de cardiopatia. Entretanto, as antraciclinas continuarão sendo drogas importantes no arsenal terapêutico de várias neoplasias, especialmente sarcomas e leucemias de alto risco51.
6.2. Agentes alquilantes
Exercem efeito citotóxico por intermédio de uma ligação covalente de um grupo alquil a macromoléculas celulares importantes resultando em dano ao DNA. Apresentam ciclo celular não específico. A curva de dose/resposta tem comportamento linear (ideal para regimes de altas doses). Porém, podem ser carcinogênicos, mutagênicos e teratogênicos.
6.2.1. Derivados da mostarda nitrogenada
6.2.1.1. Ciclofosfamida (Oxazafosforina)
É um agente não ciclo celular específico ativo como antineoplásico e imunossupressor utilizado em combinação no tratamento de linfoma não Hodgkin, leucemia, doença de Hodgkin, linfoma de Burkitt, mieloma múltiplo, dentre outros52. Altas doses de ciclofosfamida podem causar cardiotoxicidade aguda dentro de 10 dias da administração, apresentando-se clinicamente como insuficiência cardíaca congestiva ou miocardite, ou ambos, arritmias e miocardiopatia hemorrágica - complicações potencialmente fatais52,53. A nefrotoxicidade por efeito cumulativo de dose e maior susceptibilidade das crianças menores pode causar síndrome de Fanconi, redução da filtração glomerular e acidose tubular renal interferindo indiretamente no sistema cardiovascular.
A incidência de cardiotoxicidade por ciclofosfamida em pacientes pediátricos é menor que em adultos, por causa do fator intrínseco de resistência relacionado à idade e também às doses relativamente mais baixas recebidas por esses pacientes52. A miocardite causada por altas doses de ciclofosfamida (acima de 150mg/kg) pode chegar a 5% das crianças52. Ainda não se identificou nenhum fator de risco definitivo para o desenvolvimento de cardiotoxicidade induzida por ciclofosfamida, com possíveis relações à quimioterapia prévia com antracíclicos e/ou radioterapia53. O mecanismo exato do desenvolvimento desta cardiotoxicidade é desconhecido, apesar de hipótese relacionando lesão endotelial por transudação de metabólitos tóxicos resultando em dano ao miócito, hemorragia intersticial e edema52.
6.2.1.2. Ifosfamida
Estruturalmente similar à ciclofosfamida, apresenta atividade contra sarcomas de partes moles, dentre outros, como agente isolado ou em combinação em doses de até 6g/m252-54. Por ser um agente antineoplásico nefrotóxico, pode reduzir a taxa de filtração glomerular produzindo acidose tubular renal. Sua cardiotoxicidade pode estar relacionada à eliminação retardada de seus metabólitos cardiotóxicos52. Pode ocorrer arritmia cardíaca aguda durante o tratamento com alteração ocasional no segmento ST e onda T. Estas alterações são reversíveis após descontinuação do tratamento, podendo ser necessário o uso de antiarrítmicos. A re-exposição à ifosfamida pode levar à arritmia refratária e irreversível55.
6.2.1.3. Melfalano
É um agente alquilante utilizado como agente isolado ou em combinação em regimes de condicionamento mieloablativo para transplante de medula óssea (TMO)55,56. A associação do melfalano com a fludarabina tem sido usada nos condicionamentos para TMO alogênico, com relato de desenvolvimento de insuficiência grave do ventrículo esquerdo em pacientes tratados com esta combinação56.
A cardiotoxicidade é raramente reportada como complicação ao uso isolado do melfalano. Dentre as complicações mais importantes, podemos citar síndrome de secreção inapropriada do hormônio antidiurético like, hipotensão, dor precordial e até parada cardíaca. As lesões cutâneas decorrentes podem afetar o processo de monitorização cardíaca por causa da necessidade da retirada dos curativos e eletrodos até 24 horas após a infusão. A infusão deverá ser imediata após o preparo em no mínimo 30 minutos e no máximo 40 minutos (a velocidade de infusão aumenta o risco de parada cardíaca). Deixar o carrinho de parada cardíaca pronto.
6.2.2. Nitrosureias
6.2.2.1. Carmustina (BCNU):
É um derivado sintético da nitrosureia. É um agente alquilante utilizado no tratamento de doença de Hodgkin refratária, linfoma não Hodgkin e mieloma múltiplo. Também utilizado em altas doses (600 mg/m2) em combinação com outros agentes no regime preparatório para transplante de medula óssea autólogo para neuroblastoma, gliomas, sarcomas, dentre outros.
A cardiotoxicidade induzida por BCNU é rara, podendo ser relacionada à isquemia miocárdica, possivelmente relacionada ao aumento da demanda de oxigênio, espasmo coronariano ou alterações na distribuição do fluxo sanguíneo regional52. As manifestações podem se dar por dor no peito, hipotensão e taquicardia sinusal, especialmente quando utilizada em altas doses52,53.
6.2.3. Bussulfano
É um agente alquilante com atividade antitumoral limitada. Em dose padrão, é utilizado no tratamento de leucemia mieloide crônica. Em altas doses, em combinação com ciclofosfamida, é utilizado no regime preparatório de transplante de medula óssea para leucemia, linfomas e tumores sólidos pediátricos52. A associação entre o uso de bussulfano e eventos adversos cardíacos (taquicardia, edema) tem sido relatada em pequeno número de pacientes com talassemia, especialmente nos sob regime de condicionamento para transplante de medula óssea quando associado à ciclofosfamida52. Fibrose do endocárdio e tamponamento cardíaco associados ao bussulfano são raros. Fibrose pulmonar pode ocorrer de 4 meses até 10 anos após o início da terapia, necessitando de especial atenção quanto à repercussão cardíaca direita em longo prazo.
6.2.4. Derivados da platina
6.2.4.1. Cisplatina
Agente alquilante com grande espectro de atividade antineoplásica em tumores cerebrais pediátricos e osteossarcoma, dentre outros.
Cardiotoxicidade é uma complicação relativamente incomum no tratamento quimioterápico com cisplatina e os eventos relatados incluem fibrilação atrial, taquicardia supraventricular, bloqueio de ramo esquerdo e infarto do miocárdio. Tais eventos, no entanto, não parecem relacionados à dose e podem ocorrer a qualquer momento, desde horas após a primeira infusão de cisplatina até 18 meses após o término do tratamento. Pacientes podem se queixar de palpitações, dor subesternal ou dor no peito irradiada para o lado esquerdo, náusea, vômito, dispneia e hipotensão. Pode haver alteração de enzimas cardíacas, especialmente CK-MB52.
6.2.4.2. Carboplatina:
É um derivado de platina de segunda geração, utilizado clinicamente contra vários tipos de câncer. É mais hidrossolúvel e produz menos reações adversas que seu análogo cisplatina, mas sua atividade de dano ao DNA é equivalente em doses tóxicas similares. Reações adversas da carboplatina sobre o coração, apesar de reportadas, são geralmente desconhecidas. Sua toxicidade cardíaca pode, muitas vezes, ser subestimada, uma vez que normalmente é utilizada em combinação com outros agentes. Alguns resultados mostram que a carboplatina pode induzir cardiotoxicidade in vivo em culturas de células, relacionada à produção de espécies reativas de oxigênio56. A nefrotoxicidade por perda de função tubular (túbulo proximal, distal e ducto coletor) e os distúrbios hidroeletrolíticos podem exercer riscos ao sistema cardiovascular.
6.3. Antimetabólicos
Os antimetabólicos são uma classe de quimioterápicos muito utilizados em oncologia pediátrica tanto no tratamento dos tumores sólidos quanto leucemias do tipo linfoide e mieloide.
6.3.1. Metotrexato: é um antagonista de folato usado no tratamento de muitas neoplasias hematológicas e tumores sólidos como, por exemplo, osteossarcoma. Não foi identificada nenhuma cardiotoxicidade definitiva com seu uso. Entretanto, relatos de caso de síncope, miocardite e arritmias supraventriculares e ventriculares já foram reportados57.
6.3.2. Citarabina (Ara-C): é um antagonista de pirimidina usado frequentemente no tratamento de leucemias, especialmente da leucemia mieloide aguda. Múltiplos casos de pericardite com derrame pericárdico e tamponamento já foram relatados, especialmente com uso de altas doses (>3 g/m2) de citarabina. Algumas evidências sugerem que corticoterapia pode ser benéfica no tratamento de pericardite secundária à citarabina52,57.
6.3.3. Fludarabina: é um antagonista da purina utilizado no tratamento de linfoma não Hodgkin e recaídas de leucemia. Hipotensão e dor torácica já foram relatados. Uma publicação em transplante de medula óssea no qual se utilizou fludarabina e melfalano no regime de condicionamento relatou um caso de cardiotoxicidade fatal58. O mesmo estudo reportou seis pacientes adicionais que sofreram toxicidade cardíaca grave recebendo o mesmo regime de condicionamento. Curiosamente, tanto a fludarabina quanto o melfalano usados em doses altas isoladamente, raramente estão associados à toxicidade cardíaca52,57.
6.3.4. Fluorouracil (5-FU): age inibindo a timidilato sintase, levando à depleção do nucleosídeo timidina. Em oncologia pediátrica, é utilizado geralmente no tratamento de hepatoblastoma, carcinoma de rinofaringe e tumores de células germinativas.
Em adultos, a manifestação mais comum associada ao 5-fluorouracil é a isquemia miocárdica, com incidência variada, podendo ocorrer em aproximadamente 5 a 10% dos pacientes. Doença coronariana preexistente, presente em muitos desses pacientes, provavelmente exacerba o potencial isquêmico do 5-FU. Além disso, eventos isquêmicos são mais comuns quando este agente é administrado em combinação com a cisplatina57. O sintoma mais frequente em adultos é a dor anginosa, mas há relatos de arritmias, infarto agudo do miocárdio, insuficiência cardíaca e choque cardiogênico. Os eventos cardiovasculares tendem a ocorrer dentro de dois a cinco dias do início da terapia, com duração de aproximadamente 48 horas59. Alterações isquêmicas eletrocardiográficas foram notadas em até 68% dos pacientes recebendo infusão contínua60. Estima-se que a mortalidade relacionada à cardiotoxicidade desse fármaco seja em torno de 2,2 a 13%. Fatores de risco descritos são: altas doses (>800 mg/m2), infusão contínua do fármaco, irradiação mediastinal prévia, doença arterial coronariana prévia e o uso concomitante de quimioterapia cardiotóxica59. A patogênese da cardiotoxicidade associada ao 5-FU é desconhecida. Os mecanismos propostos são trombose coronariana, arterite, vasoespasmo, toxicidade direta por ativação endotelial, ativação da coagulação, depleção dos fosfatos de alta energia e apoptose dos miócitos e das células endoteliais61. A isquemia geralmente é reversível após a suspensão do fármaco e a introdução de terapia anti-isquêmica. Em situações de reintrodução do 5-FU, geralmente há recorrência dos sintomas. O uso profilático de bloqueadores de canais de cálcio pode ser benéfico na prevenção da isquemia cardíaca. Não há dados conclusivos na literatura sobre os efeitos do 5-FU em crianças, merecendo atenção subclínica e prospectiva61.
6.4. Alcaloides da vinca
Os alcaloides da vinca são compostos naturais ou semissintéticos derivados da pervinca Catharantus roseus, presentes no tratamento de várias doenças hematológicas e tumores sólidos.
Dentre os medicamentos que compõem esta classe estão: vincristina (LLA, linfomas, tumor de Wilms, sarcoma de Ewing, neuroblastoma e rabdomiossarcoma), vimblastina (utilizada em combinação na terapia de tumor de células germinativas, linfoma de Hodgkin avançado, dentre outros52) e Vinorelbine52(utilizada no tratamento de crianças com glioma de baixo grau62. Hipertensão, isquemia do miocárdio, infarto do miocárdio e outras complicações veno-oclusivas têm sido relatadas com o uso destes medicamentos. Os sinais e sintomas de cardiotoxicidade são: dor precordial irradiando para as costas, ombros ou pescoço, edema pulmonar, taquipneia, ritmo de galope e estertores pulmonares52. A cardiotoxicidade tem sido descrita mais frequentemente com vimblastina, mas também existem relatos de casos com vincristina e vinorelbine52.
6.5. Inibidores de topoisomerase e epipodofilotoxinas
Análogos da camptotecina têm como alvo a enzima intranuclear topoisomerase I e representam uma promissora classe de agentes quimioterápicos para o tratamento do câncer infantil62.
6.5.1. Irinotecano (CPT-11): é um derivado semissintético da camptotecina. É metabolizado pela enzima carboxilesterase no composto ativo SN-38, responsável pela ação citotóxica do CPT-1163. Estudos avaliam sua eficácia em tumores infantis de mal prognóstico, tais como meduloblastoma/PNET(primitive neuroectodermal tumors), rabdomiossarcoma e neuroblastoma63. As toxicidades dose-limitantes são leucopenia e diarreia. Acredita-se que toxicidade cardiovascular ocorra raramente e pode estar relacionada aos seus efeitos colinérgicos63,64.
6.5.2. Topotecano: topotecano e outros derivados da camptotecina estabilizam o complexo covalente topoisomerase I, no qual a enzima se liga ao DNA. Na prática pediátrica é utilizado em combinação com ciclofosfamida para o tratamento de rabdomiossarcoma, neuroblastoma e sarcoma de Ewing. Estudos de fase I sugerem que a única toxicidade relevante seja no sistema hematopoiético65.
6.5.3. Etoposido: é um derivado semissintético da podofilotoxina, comumente utilizado no tratamento tanto de doenças hematológicas quanto em tumores sólidos57. É um dos quimioterápicos mais utilizados na prática pediátrica. A toxicidade dose-limitante do etoposido é a mielossupressão. No entanto, algumas evidências apontam para toxicidade cardíaca, na forma de infarto do miocárdio e angina, cujos mecanismos propostos para tais ocorrências são espasmo de artéria coronária, dano direto à parede do miocárdio ou indução de resposta imune52,66. O espasmo de artéria coronária pode ocorrer por causa da liberação de substâncias vasoativas após a administração de etoposido, ou pela ação direta da droga nos vasos sanguíneos52,66.
6.5.4. Teniposido: é um derivado semissintético da podofilotoxina semelhante ao etoposido. Eventos cardíacos associados à administração de teniposido incluem hipotensão e arritmias. A hipotensão é transitória e relacionada à taxa de infusão. A administração rápida de teniposido pode causar hipotensão em 2% dos pacientes pediátricos. É rara a ocorrência de arritmias, mas pode resultar em morte súbita52.
6.6. Terapia alvo
6.6.1. Anticorpos monoclonais
6.6.1.1. Rituximabe: é um anticorpo monoclonal quimérico contra o antígeno CD20 em linfócitos B utilizado para tratar diversas doenças hematológicas benignas e malignas, com raros relatos de toxicidade cardíaca por causa de sua administração. Tem-se reportado arritmias e angina durante menos de 1% das infusões. Adicionalmente, mortes relacionadas a reações infusionais agudas têm sido documentadas em 0,04 a 0,07% dos casos. Estas mortes parecem estar relacionadas à infusão e compreendem hipóxia, infiltrado pulmonar, infarto do miocárdio, fibrilação ventricular e choque cardiogênico67.
6.6.1.2. Alemtuzumabe: é um anticorpo monoclonal humanizado cujo alvo é o antígeno CD52 presente na membrana celular da maioria dos linfócitos T e B. A droga foi inicialmente aprovada para o tratamento de LLC refratária à fludarabina e tem se mostrado promissora no tratamento de outras doenças mieloproliferativas, como a síndrome de Sezary. Os efeitos colaterais mais comuns são: febre, náusea, vômito e rash. Apesar de menos frequentes, eventos pulmonares (broncoespasmo, edema) e cardíacos (hipotensão, arritmias, isquemia ou infarto do miocardio) podem ocorrer, e em alguns casos é necessário descontinuar o tratamento66 por causa do risco potencial de parada cardíaca. O mecanismo desta toxicidade é desconhecido e os relatos mostram que os pacientes obtiveram total ou parcial resolução dos sintomas após a descontinuação do tratamento67.
6.6.2. Inibidores de tirosina-quinase
Imatinibe, dasatinibe e nilotinibe são pequenas moléculas inibidoras de ABL quinase desenvolvidas principalmente para tratamento de LMC onde as células leucêmicas expressam a proteína BCR-ABL, também conhecida como cromossomo Filadélfia68. É importante salientar que, salvo raras exceções, as taxas de cardiotoxicidade associadas ao uso de inibidores de tirosina quinase não são conhecidas pelos estudos clínicos não incluírem avaliação da função cardíaca (função do ventrículo esquerdo) antes e durante o tratamento69,70.
6.6.2.1. Imatinibe:mesilato de imatinibe é uma molécula pequena que inibe potencialmente a atividade de quinase do BCR-ABL, e tem mostrado eficácia em pacientes com LMC (>70% dos pacientes tratados apresentaram remissão citogenética completa). Alguns ensaios clínicos reportam a incidência relativamente alta de edema periférico (63-66%), com alguns casos classificados como graves (4-5%), além de dispneia encontrada em 12-16% dos pacientes tratados. Estudos sugerem a cardiotoxidade do imatinibe relacionada à grave disfunção do ventrículo esquerdo e insuficiência cardíaca69.
6.6.2.2. Nilotinibe: indicado em casos de LMC refratária à imatinibe. Seu uso tem sido associado ao prolongamento do intervalo QT e morte súbita.
6.6.2.3. Dasatinibe: apesar de não haver relação causal bem estabelecida, têm sido associados sintomas como dor no peito, derrame pericárdico, disfunção ventricular e insuficiência cardíaca com o uso de dasatinibe, além de prolongamento do intervalo QT69.
6.7. Agentes biológicos
Os modificadores de resposta biológica são agentes que estimulam a imunidade do paciente ou alteram as interações da célula tumoral induzindo à regressão tumoral. A toxicidade desta classe de agentes deve-se, geralmente, não ao efeito citotóxico direto da droga, mas às alterações na fisiologia celular.
6.7.1. Interferons: é uma família de glicoproteína que exibe um amplo espectro de atividade biológica. Três principais classes de interferon foram identificadas: interferon-alfa, derivado de leucócitos; interferon-beta, derivado de fibroblastos; e interferon-gama, derivado de linfócitos T. A toxicidade associada aos interferons parece ser um efeito de classe, sendo o interferon-alfa o mais amplamente estudado em estudos clínicos de fase I e II71.
Os efeitos adversos dos interferons no sistema cardiovascular incluem: isquemia e infarto do miocárdio, arritmias e cardiomiopatia. As alterações isquêmicas estão relacionadas à história prévia de doença coronariana e podem ser consequência de sintomas gripais (flu-like) causados pelo interferon, levando a um aumento do consumo de oxigênio pelo miocárdio. Estudos clínicos em adultos relatam uma incidência de arritmia de até 20%, incluindo taquicardia e fibrilação ventricular, flutter e fibrilação atrial, bloqueio átrio-ventricular e ectopias atriais ou ventriculares57,70. A administração prolongada de interferon tem sido associada com cardiomiopatia, incluindo diminuição da fração de ejeção e insuficiência cardíaca. A cardiomiopatia foi reversível com a suspensão da infusão da droga. A patogênese da cardiomiopatia induzida pelo interferon ainda é desconhecida71.
6.7.2. Interleucina-2 (IL-2): é uma glicoproteína produzida pelo linfócito T helper com múltiplos efeitos imunomoduladores. Virtualmente, todos os pacientes que recebem IL-2 podem desenvolver a síndrome de extravasamento vascular (capillary leak syndrome), caracterizada por um aumento da permeabilidade vascular e hipotensão. A hipotensão inicialmente responde bem à infusão de volume, porém, normalmente, requer o uso de vasopressores. Consequentemente, há um aumento da frequência cardíaca e do débito cardíaco com diminuição da resistência vascular periférica. A IL-2 causa uma constelação de sintomas semelhantes ao choque séptico. O pico destes sintomas ocorre 4 horas após cada dose e piora com tratamentos subsequentes.
Dose em "bolus", que produz uma elevação transitória dos níveis de IL-2, está associada a efeitos mais graves que à infusão contínua. A queda na resistência vascular periférica pode não normalizar por até seis dias após a suspensão da IL-2.
A IL-2 também tem sido associada à toxicidade miocárdica direta em pacientes com doença coronariana preexistente, isquemia, infarto do miocárdio e arritmias, quando óbitos têm sido reportados57.
6.8. Miscelânea
6.8.1. Bleomicina: é uma glicoproteína que foi inicialmente isolada do fungo Streptomycesverticillus.É muito utilizada no tratamento do linfoma de Hodgkin, inserida no complexo ABVD (adriamicina, bleomicina, vimblastina e dacarbazina), tumores de células germinativas e carcinomas. Pericardite é um efeito adverso incomum, com dor torácica aguda na região subesternal ocorrendo em menos de 3% dos pacientes. Quando presente, pode ser potencialmente grave. Estes eventos não causam sequela cardíaca em longo prazo, e geralmente não é necessária a suspensão da bleomicina. Os sintomas não reaparecem com novas infusões da droga. Outras manifestações cardíacas já publicadas durante e após o uso de bleomicina em pacientes jovens incluem a doença coronariana (isquemia miocárdica e infarto)57.
6.8.2. Ácido trans-retinoico (ATRA): é um agente de diferenciação utilizado no tratamento da leucemia promielocítica aguda (LMA-M3). Aproximadamente 10 a 15% dos pacientes expostos desenvolvem a síndrome de ácido retinoico que se manifesta por febre, dispneia, derrame pleural e/ou pericárdico com potencial para tamponamento cardíaco, infiltrado pulmonar, edema periférico e isquemia miocárdica ou infarto. As manifestações são geralmente mais graves durante as duas primeiras semanas de tratamento e os sintomas são amenizados com o uso de dexametasona57.
6.8.3. Trióxido de arsênio: é um agente de diferenciação atualmente aprovado para o tratamento das recaídas de leucemia promielocítica aguda (LMA-M3). De forma semelhante aos pacientes tratados com ATRA, os indivíduos tratados com trióxido de arsênio também podem apresentar a síndrome do ácido retinoico. Adicionalmente, múltiplos estudos têm demonstrado um prolongamento do intervalo QT em até 63% dos pacientes e Torsades de Pointes, arritmia ventricular de difícil tratamento e potencialmente fatal. Sendo assim, os oncologistas devem evitar o uso concomitante de trióxido de arsênio com outros fármacos que também prolonguem o intervalo QT. Por causa da natureza refratária dessa arritmia ventricular, são recomendados eletrocardiogramas seriados e monitorização eletrolítica cuidadosa.
7. Radioterapia e cardiotoxicidade
A radioterapia é um dos pilares do tratamento oncológico multidisciplinar em pediatria.
Estima-se que cerca de 40% das crianças, adolescentes e adultos jovens utilizem radioterapia em alguma etapa do tratamento da doença.
Com o desenvolvimento dos protocolos terapêuticos multidisciplinares e a melhoria das condições de suporte clínico, cerca de 70% dos cânceres que ocorrem na faixa pediátrica são curados e estes pacientes deverão ter uma vida adulta ativa e normal, como sobreviventes do câncer na infância.
Observa-se que cerca de 2/3 dos sobreviventes de câncer na infância e adolescência apresentam pelo menos uma alteração tardia decorrente da terapêutica recebida e em 1/4 deles esta alteração é severa, comprometendo a sobrevida e impactando a qualidade de vida72,73.
Efeitos cardiovasculares são vistos frequentemente em sobreviventes de câncer e a importância clínica da doença cardíaca induzida por radiação é reconhecida há vários anos.
Dentre os sobreviventes de linfoma de Hodgkin que receberam radioterapia, a enfermidade cardiovascular é uma das causas de morte mais comum72. Estudos têm demonstrado maior risco de doença coronariana, alterações valvares, insuficiência cardíaca congestiva, doença pericárdica e morte súbita nestes sobreviventes, particularmente se tratados antes dos 30 anos. O risco de morte por infarto do miocárdio aumenta de 1,5 a 3 vezes em pacientes que receberam irradiação mediastinal e também é maior a ocorrência de isquemia miocárdica e doença coronariana72,73.
Graças à melhora da técnica em radioterapia, o risco tem declinado com o tempo, em particular nas duas últimas décadas, mas em pacientes tratados nos anos 1970 e 80, o risco de insuficiência cardíaca congestiva e disfunção valvular permanece elevado74,75.
O dano da radioterapia ao coração pode envolver cada uma das estruturas cardíacas, isoladamente ou em associação, constituindo um espectro de alterações, conforme pode ser visto na Tabela 1.
As complicações cardíacas após a radioterapia são atribuídas à inflamação e à fibrose das estruturas individuais. A doença pode ser assintomática, com a possibilidade de que sinais e sintomas se tornem clinicamente evidentes depois de 5 a 15 anos do término do tratamento, mas caracteristicamente é sempre progressiva.
A incidência e a severidade são diretamente proporcionais à dose e ao volume irradiado e inversamente proporcionais à idade. A ocorrência também aumenta com o tempo decorrido da radioterapia, o uso de agentes cardiotóxicos, em particular as antraciclinas, e a eventual existência de doença cardíaca prévia. Exposição a 250 mg/m2 ou mais de antraciclinas e dose de radiação superior a 12Gy ao coração aumentam o risco relativo de insuficiência cardíaca congestiva de 2 a 6 vezes, quando comparado a sobreviventes não irradiados76,77.
Dentro de uma perspectiva clinica, a única maneira corrente de reduzir a doença cardíaca radiação-induzida é o investimento em recursos de planejamento, que minimizem a dose e o volume de coração irradiado, pois outros métodos não são ainda viáveis78.
Os sobreviventes atuais usaram técnicas e doses hoje consideradas inadequadas, dentro da realidade do progresso tecnológico e dos protocolos terapêuticos.
No passado, toda a programação de dose e definição dos campos de irradiação tinham como base referências anatômicas e radiológicas, caracterizando a radioterapia em duas dimensões (2D), típica do século XX. As técnicas eram simples e as margens dos campos amplas. Não era possível determinar com precisão a dose recebida pelos órgãos normais e estruturas vizinhas à área tumoral.
O advento dos sistemas de planejamento em três dimensões conferiu uma nova realidade à radioterapia torácica, e em especial à radioterapia pediátrica do século XXI, pois tornou possível a identificação e o delineamento das várias estruturas envolvidas no tratamento, com o conhecimento do volume dos órgãos incluídos nos campos de irradiação. A geração e análise dos histogramas dose-volume levam à adoção de medidas de ajustes de dose, modificação de campos, escolha de outras técnicas que minimizem o impacto da radiação sobre os órgãos normais de risco.
Na infância e adolescência o coração pode estar incluído nos campos de radioterapia dos tumores da parede costal, do mediastino (em particular o linfoma de Hodgkin), nas irradiações torácicas por tumores de Wilms ou sarcoma de Ewing metastático aos pulmões, na radioterapia do neuroeixo em tumores cerebrais e nas lesões que envolvam a coluna torácica e os tecidos paraespinais dorsais.
O conhecimento do volume cardíaco irradiado e da dose recebida por cada uma das estruturas só é possível com o planejamento em 3D, razão pela qual a radioterapia conformada tridimensionalmente é considerada a técnica preferencial de radioterapia em pediatria. O mesmo se passa com adultos jovens que apresentem tumores de bom prognóstico e tenham grandes chances de cura. A informação gerada pelos atuais sistemas de planejamento deve sempre ser conhecida, permitindo a adoção de medidas que previnam o aparecimento de sequelas e façam parte do acompanhamento em longo prazo do paciente irradiado, notadamente quando da combinação de radioterapia e agentes cardiotóxicos.
Os fatores de risco associados ao dano cardíaco por radioterapia podem ser vistos na Tabela 2.
7.1. Recomendações para reduzir a toxicidade cardíaca relacionada à radioterapia
Há evidências de que as técnicas modernas de administração de radiação possam reduzir o risco de dano da radioterapia ao coração, porém maior tempo de seguimento é necessário para confirmar este fato. As doses liberadas na radioterapia contemporânea são muito menores que as liberadas em décadas passadas.
Técnicas conformadas tridimensionais com múltiplos campos ou radioterapia de intensidade modulada (IMRT) são desejáveis e preferenciais para a irradiação do tórax. Também o emprego de elétrons de alta energia pode ser de extrema valia em algumas situações.
Atualmente, o planejamento terapêutico computadorizado tridimensional possibilita que a dose liberada a todo o órgão e a cada estrutura cardíaca, em particular, seja estimada precisamente.
O delineamento de regiões clinicamente relevantes do coração ainda é um desafio porque a sua definição estrutural por intermédio dos sistemas de planejamento é imprecisa. Nenhuma modalidade de imagem mostra claramente estas estruturas. A borda cardíaca inferior pode ser difícil de diferenciar do fígado ou diafragma e a segmentação da borda superior com os grandes vasos pode ser ainda mais desafiadora. Além disso, o coração se move com os ciclos respiratórios e cardíacos e a anatomia da interseção dos grandes vasos no coração é complexa. Novas ferramentas de imagem, como a RNM, podem identificar melhor as sub-regiões do coração, mas a sua aplicabilidade no planejamento da radioterapia ainda é limitada.
É importante ter em mente que a dose liberada ao coração deve ser a mais baixa possível e o volume do órgão englobado nos campos de radioterapia o menor possível, mantendo a dose adequada ao volume-alvo planejado (PTV).
Ainda existe um grande hiato a ser preenchido, no conhecimento das estruturas cardíacas em risco e nos mecanismos de dano induzido pela radioterapia. A dose recebida pelo coração, na maioria dos casos, não é homogênea e não se sabe qual parte do órgão é mais radiossensível, nem qual estrutura cardíaca deveria ser considerada como ponto de referência de dose de tolerância na prática clínica79.
Também a relação entre efeitos observados em curto e longo prazo não é muito bem conhecida, assim como a extensão do risco cardíaco provocado por outros fatores como doença cardiovascular preexistente, irradiação de outros órgãos (pulmões, rins), estilo de vida, fumo, consumo de drogas etc80.
Modelos experimentais e estudos pré-clínicos são de enorme interesse para melhorar o entendimento dos mecanismos celulares e moleculares do dano provocado pela radioterapia. As linhas atuais de investigação estão predominantemente voltadas para a disfunção endotelial e a injúria vascular, a ação e interação de mastócitos ao sistema neuroimune cardíaco e o papel do sistema renina-angiotensina. A elucidação do significado destes mecanismos e sua influência na doença cardíaca induzida por radioterapia poderão ser úteis como alvos para intervenção no futuro.
7.2. Tratamento das complicações e monitoração da função cardíaca após a radioterapia
A doença cardíaca induzida por radioterapia é tratada da mesma forma que a não relacionada à radiação, mas com especial atenção às alterações eventualmente provocadas ao coração e às estruturas torácicas.
Toxicidade cardíaca é extremamente rara durante a radioterapia e não existem recomendações definitivas que suportem os vários testes e suas frequências.
Guias baseados em consensos e opiniões de especialistas são disponíveis para o acompanhamento de sobreviventes de câncer com risco de problemas cardíacos e variam em relação à população-alvo80,81.
À parte da história médica e do exame clínico, exames normalmente recomendados dependem da anormalidade estudada, como vistos na Tabela 3.
Os estudos com biomarcadores em pacientes submetidos à radioterapia são poucos, constituem excelente campo de pesquisa, mas o seu real papel necessita ser determinado em séries com grande número de pacientes. No atual estado do conhecimento, biomarcadores cardíacos não são recomendados para identificação de pacientes de alto risco ou para predizer os eventos futuros. Similarmente, na ausência de fatores de risco, o papel da terapia preventiva antiplaquetária, de agentes redutores de lipídios e ACE inibidores permanece incerto.
O emprego de CT-scan cardíaco e estudos perfusionais tem permitido identificar alterações coronarianas radioinduzidas em pacientes assintomáticos, possibilitando o tratamento precoce e reduzindo a ocorrência de eventos cardiovasculares futuros.
7.3. Estudos e graduação de toxicidade
A predição de toxicidade requer estudos prospectivos baseados em dosimetria 3D e o acompanhamento cuidadoso dos pacientes que receberam quimioterapia potencialmente cardiotóxica e radioterapia.
Ainda carecem de esclarecimento definitivo, a ser determinado em longos estudos futuros: a) se as modernas técnicas de radioterapia reduzem realmente o risco de dano cardíaco; b) a relação entre a dose liberada em subvolumes do coração e a evolução clínica; c) a potencial interação entre fatores de risco cardíaco de base; d) o impacto do hipofracionamento (administração da radiação em poucas frações com dose elevada/ fração); e) o melhor entendimento dos efeitos fisiológicos da radioterapia torácica (interação entre irradiação pulmonar e cardíaca).
Sugere-se que os sistemas de escores do RTOG/EORTC ou LENT-SOMA sejam considerados para a descrição dos efeitos adversos, na tentativa de padronizar a linguagem e facilitar o registro das disfunções cardíacas por radioterapia81,82,83.
O Quadro 5 apresenta os escores que quantificam os efeitos da radioterapia no coração na população pediátrica, de acordo com o RTOG/EORTC.
Não existem dados suficientes que relacionem as sequelas pós-radioterapia em crianças e adolescentes, com ênfase aos efeitos órgão-volume. Por causa da deficiência da detalhada avaliação da dose liberada aos órgãos normais na era pré-planejamento 3D, análises retrospectivas podem ser realizadas com estimativas incertas da dose recebida por órgãos especiais. As doses liberadas ao coração e outros órgãos com as técnicas contemporâneas de radioterapia são mais baixas que aquelas de décadas passadas. Estudos multicêntricos e protocolos de documentação de registros de dose devem ser implantados para se obter resultados mais rápidos e estabelecer parâmetros que envolvam a relação dose-resposta, o impacto de terapias complementares e o risco cardíaco específico de cada paciente. A cooperação entre as sociedades científicas de especialidades e de grupos de estudos internacionais deve ser cada vez mais encorajada84. Protocolos de registro das doses recebidas pelos diferentes órgãos com o conhecimento de histogramas dose-volume individualizados são indispensáveis na radioterapia de crianças, adolescentes e adultos jovens do século XXI, expandindo a cardio-oncologia85, a atenção multidisciplinar e o cuidar integral do paciente oncológico.
8. Apresentações clínicas da cardiotoxicidade
8.1. Insuficiência cardíaca (IC)
8.1.1. Definição
Entidade complexa e dinâmica que ocorre na infância como resultado de patologia congênita ou adquirida. Desencadeia uma série de eventos morfológicos e hemodinâmicos que podem levar a sinais e sintomas clínicos decorrentes da injúria miocárdica.
Várias patologias podem levar a IC por doenças do miocárdio. No caso da criança oncológica, o acometimento se deve particularmente ao uso de fármacos quimioterápicos, mais frequentemente as antraciclinas45,86.
8.1.2. Fisiopatologia da IC
Os avanços no manuseio e na terapêutica medicamentosa de crianças portadoras de câncer têm possibilitado a sobrevida desta população em 80% em relação a 50% na década de 197087,88. No entanto, sabe-se que um terço delas apresenta o risco de evoluir com pelo menos uma condição clínica crônica9. Lipshultz e cols.15 referem que estas crianças apresentam risco de doença cardiovascular 5 a 10 vezes mais quando comparadas com seus irmãos, e risco 15 vezes maior de desenvolverem insuficiência cardíaca congestiva. Armostrong e cols.89 descrevem que causas cardíacas estão entre as mais frequentes de mortalidade tardia. Os protocolos terapêuticos do câncer variam de acordo com o tipo do tumor e estágio da doença. A maioria dos cânceres em pediatria é tratada por combinação de drogas terapêuticas. Na população pediátrica, as drogas mais utilizadas que podem causar cardiotoxicidade e que levam à insuficiência cardíaca congestiva com disfunção ventricular são: antraciclinas (doxorrubicina, epirrubicina), agentes alquilantes (ciclofosfamida), anticorpos monoclonais e inibidores da tirosina-quinase (bevacizumabe)52,69. No entanto, as antraciclinas são as que com maior frequência causam eventos cardiovasculares provavelmente por ser uma das drogas mais utilizadas na faixa etária pediátrica, podendo explicar seu impacto na morbidade e mortalidade nesta população90. Pacientes expostos a antraciclinas apresentam risco de desenvolvimento de insuficiência cardíaca congestiva que aumenta com o efeito cumulativo da dose empregada, sendo que o risco pode persistir até 45 anos após o tratamento91. Estudos referem que os efeitos da antraciclina mostram que mais da metade dos pacientes que receberam a medicação apresentaram alterações cardiológicas como diminuição da função ventricular, da massa ventricular e da espessura da parede ventricular9.
Os principais mecanismos de ação das antraciclinas são pela sua interposição entre as bases de DNA, evitando a replicação de células cancerígenas e a inibição da enzima topoisomerase II, impedindo o processo de "uncoiling" do DNA que é necessário na replicação e transcrição9. Entretanto, o mecanismo da cardiotoxicidade da antraciclina é complexo. A hipótese do estresse oxidativo que parece ser a mais aceita é o evento inicial que desencadeia a série da cascata que leva ao remodelamento miocárdio e a disfunção ventricular9 (conforme Tabela 4).
Os efeitos cardiotóxicos dos agentes quimioterápicos podem ocorrer durante, imediatamente ou meses a anos após o tratamento. Fatores de risco associados à cardiotoxicidade da antraciclina são conforme9 (vide Quadro 3):
8.1.3. Manifestação clínica da IC aguda
Os principais sinais e sintomas da IC são: taquicardia, extremidades frias, palidez, taquidispneia, oligúria, dor abdominal e edema. É importante ressaltar que alguns destes achados podem estar relacionados à própria neoplasia.
É importante salientar que na criança oncológica, em regime de quimioterapia (QT), fatores como infecção, distúrbios hidroeletrolíticos e síndrome de lise tumoral devem ser diagnósticos diferenciais.
8.1.4. Insuficiência cardíaca crônica
A incidência de insuficiência cardíaca congestiva crônica em crianças tratadas com antraciclina varia de 1 a 16%9. A manifestação clínica da insuficiência cardíaca (IC) na criança varia de acordo com a faixa etária de recém-nascidos a adolescentes. Em crianças até a adolescência as manifestações da IC são semelhantes à população adulta. Pode-se classificar a IC de acordo com a classificação de Ross (Tabela 5) ou da Classificação da International Society of Heart and Lung Transplantation (ISHLT) (Tabela 6)92.
8.1.4.1. Tratamento da insuficiência cardíaca crônica
O tratamento medicamentoso da insuficiência cardíaca crônica em crianças com insuficiência cardíaca congestiva secundária a disfunção ventricular por cardiotoxicidade a agentes quimioterápicos tem como principal objetivo atuar no remodelamento ventricular e incluem a ação de drogas que atuam na diminuição da pré-carga com aumento da diurese (diuréticos), redução da pós-carga e aumento da contratilidade miocárdica9,15,92.
8.1.4.2. Transplante cardíaco
O transplante cardíaco tem sido indicado em crianças que evoluem com insuficiência cardíaca refratária. Levitt e cols.92 reportam que 43 pacientes necessitaram de transplante cardíaco, sendo que todos haviam recebido antraciclina e 15 deles também receberam radiação cardíaca. Neste estudo a faixa etária variou de 3,2 a 23,9 anos, com mediana de 14,8 anos. A indicação de transplante cardíaco em crianças por cardiotoxicidade a agentes quimioterápicos ocorre pela disfunção ventricular que estes pacientes podem apresentar levando à insuficiência cardíaca refratária a terapêutica convencional93,94 (Tabela 8). Deve-se ter, no entanto, avaliação em relação à cura do câncer e o rastreamento da doença avaliados pela oncologia. Há controvérsias na literatura em relação ao momento de indicação do transplante cardíaco na população pediátrica pelo risco de recidiva da doença ou surgimento de segunda neoplasia secundária à imunossupressão. Em adultos é recomendado após 5 anos livre de evento.
8.1.5. Insuficiência cardíaca descompensada
8.1.5.1. IC aguda descompensada
O paciente oncológico pode apresentar insuficiência cardíaca aguda por sobrecarga volêmica (graças à hiper-hidratação necessária em diversos esquemas quimioterápicos), toxicidade por quimioterápicos (ciclofosfamida, ácido transretinoico, antracíclicos, 5-fluoracil, citarabina, cisplatina etc.), infecções do tecido miocárdico secundárias à leucopenia induzida pela quimioterapia, sendo mais comuns as virais (Coxsackie e outros enterovírus, H1N1), bacterianas (Streptococcus) e fungos (Candida e Aspergillus)9,95-97.
Na maioria das vezes o comprometimento agudo do miocárdio no curso da QT apresenta boa evolução.
O paciente pediátrico oncológico também está mais sujeito a quadros sépticos, por causa de imunossupressão e maior exposição a quadros infecciosos, próprios da faixa etária. Este grupo de pacientes evolui rapidamente para choque séptico, com disfunção cardíaca associada. Estudos em crianças com choque séptico mostram o predomínio de um perfil hemodinâmico com baixo débito cardíaco e alta resistência vascular sistêmica (RVS)98,99, diferentemente da população adulta, em que prevalece estados hiperdinâmicos com vasoplegia. O paciente pediátrico em geral apresenta-se em hipovolemia relativa, respondendo bem à reposição volêmica agressiva. Entretanto, o paciente pediátrico oncológico pode necessitar de suporte inotrópico mais precocemente que o paciente não oncológico, por causa da cardiotoxicidade dos quimioterápicos
O manejo dos pacientes com IC aguda não difere do manejo habitual do choque cardiogênico, sendo baseado em diuréticos (essencialmente furosemida), inotrópicos, inodilatadores, vasodilatadores e suporte clínico: restrição hídrica quando possível, ventilação mecânica quando necessário, suporte nutricional, monitorização hemodinâmica, controle de temperatura e diurese.
É importante determinar, assim que é feito o diagnóstico da IC, se há ou não congestão sistêmica e/ou pulmonar e avaliar a perfusão periférica. Divide-se, assim, o manejo em 3 categorias100:
1) Congestão presente com perfusão periférica normal ("Quente e Úmido"):
Maioria dos casos. Apresenta boa resposta ao manejo farmacológico. É essencial o uso de diuréticos para reduzir a congestão, sempre se evitando a hipovolemia (manter PVC de 8-12mmHg) a fim de não causar síndrome cardiorrenal. Geralmente o uso de inotrópicos endovenosos é desnecessário.
Introduzir betabloqueadores e IECA após a compensação do quadro.
2) Congestão presente com perfusão periférica lentificada ("Frio e Úmido"):
Importante reduzir a pós-carga nestes pacientes, com a utilização de vasodilatadores (nitroprussiato, nitroglicerina) e diuréticos. Inotrópicos (dopamina, dobutamina, milrinone) devem ser utilizados com cautela por causa da possibilidade de induzir taquiarritmias e piorarem o quadro clínico. Milrinone (pelos efeitos lusinotrópico) pode ser uma opção nesses casos.
Nesiritide, um peptídio natriurético B recombinante, está sendo utilizado no tratamento de IC descompensada em adultos, porém ainda não há evidências para uso pediátrico101.
3) Congestão ausente com perfusão lentificada ("Frio e Seco"):
Prognóstico ruim, geralmente necessita de suporte mecânico para a recuperação da função miocárdica.
Utilização de inotrópicos e reposição dos estoques endógenos de cálcio na fase aguda parecem ser a melhor escolha terapêutica nestes casos. A utilização de adrenalina em baixas doses (0,1-0,2mcg/kg/min) pode ser benéfica se utilizada isoladamente100,102.
8.1.5.1.1. Drogas no manejo da IC Aguda
8.1.5.1.1.1. Diuréticos
8.1.5.1.1.1.1. Furosemida - Infusão contínua (com equipo protegido da luz), ou intermitente.
Dose: 0,5 a 8mg/kg/dia
8.1.5.1.1.2.1. Dobutamina - Preferencialmente em acesso venoso central.
Dose: 5 a 20mcg/kg/min
8.1.5.1.1.2.2. Milrinone - Em acesso venoso central.
Ataque: 50mcg/kg. Manutenção: 0,25 a 0,75mcg/kg/min
8.1.5.1.1.2.3. Dopamina - Pode ser utilizada em veia periférica.
Dose: 5 a 10mcg/kg/min
8.1.5.1.1.3. Vasopressores
8.1.5.1.1.3.1. Adrenalina - Sempre em acesso central. Primeira escolha na hipotensão do choque frio.
Dose: 0,1 a 1mcg/kg/min
8.1.5.1.1.3.2. Noradrenalina - Sempre em acesso central. Primeira escolha na hipotensão do choque quente.
Dose: 0,1 a 1mcg/kg/min
8.1.5.1.1.3.3. Vasopressina - Uso habitual ainda não recomendado.
Dose: 0,0003 a 0,02U/kg/min
8.1.5.1.1.4. Vasodilatadores
8.1.5.1.1.4.1. Nitroprussiato de sódio - Atenção quanto à possibilidade de poder levar à intoxicação por tiocianato.
Dose: 0,3 a 10mcg/kg/min
8.1.5.1.1.4.2. Nitroglicerina - Efeito venodilatador preponderante.
Dose: 5 a 200mcg/min
8.1.5.1.1.5. Sensibilizador de canal de cálcio
8.1.5.1.1.5.1. Levosimendan - Estudos iniciais em crianças não oncológicas com insuficiência cardíaca refratária à dobutamina mostraram resultados encorajadores em termos de fração de ejeção e descontinuação de terapia com catecolaminas e efeitos adversos, mas ainda não há recomendação como terapia habitual101.
Dose: 3 a 6mcg/kg em 10 minutos, repetir em 24h. Efeito com duração de até 7 dias.
8.1.5.2. IC crônica descompensada
A descompensação da IC crônica pode ocorrer por um evento desencadeante ou por refratariedade ao tratamento existente.
No primeiro caso, o tratamento envolve suporte clínico até estabilização da doença de base e manejo dos eventos desencadeantes da descompensação. Tais eventos geralmente são infecções típicas da faixa etária, mas também incluem distúrbios eletrolíticos, anemia, arritmias, tromboembolismo pulmonar, interações medicamentosas resultando em menor eficácia das drogas utilizadas no tratamento habitual da IC, toxicidade das drogas, má adesão ao tratamento, dentre outros103. Especificamente na cardiomiopatia induzida por antracíclicos, pode haver descompensação da IC crônica em períodos que requerem maior trabalho cardíaco, como o estirão do crescimento, puberdade, tratamento com estrógenos ou gestação104.
Estes pacientes têm indicação de inotrópicos por se tratar de descompensação potencialmente reversível, na qual o uso de inotrópicos se dará por um curto período de tempo105. Entretanto, tais pacientes fazem uso crônico de betabloqueadores e apresentam também disfunção diastólica. Neste grupo, o uso de adrenalina e outros beta-agonistas pode não apresentar boa resposta, podendo ser utilizados inibidores de fosfodiesterase (milrinone).
Como terapia de resgate nesta fase, há relatos de sucesso com o uso de levosimendan106 e ressincronização cardíaca, inclusive com QRS estreito107-110.
8.2. Hipertensão arterial sistêmica (HAS)
8.2.1. Definição
A hipertensão arterial sistêmica (HAS) na infância é definida como pressão arterial (PA) maior ou igual ao percentil 95 de distribuição da pressão arterial para sexo, altura e idade111. Na infância, a HAS está, na maioria das vezes, associada a causas secundárias. A prevalência da HAS entre crianças na população geral está entre 1 a 3%. Dados da literatura sugerem que crianças portadoras de leucemias e linfomas têm uma prevalência de HAS de até 60%111,112.
8.2.2. Agentes mais envolvidos/Fisiopatologia
Há na literatura uma escassez de trabalhos que relacionem os efeitos colaterais dos quimioterápicos em crianças e adolescentes. De forma geral, na atualidade, os agentes reconhecidamente mais associados com HAS são os inibidores da angiogênese (bevacizumabe, sunitinibe, sorafenibe, vatalanibe), ainda pouco utilizados na prática pediátrica59. A teoria mais aceita é que a fisiopatologia da hipertensão esteja ligada a inibição do fator de crescimento endotelial vascular, que diminui a produção de óxido nítrico na parede das arteríolas e outros vasos de resistência. Outra hipótese é a de que estas drogas atuam em fatores neuro-hormonais como no sistema renina-angiotensina-aldosterona e na liberação de catecolaminas, resultando no aumento da pressão arterial112,113.
A cisplatina, um inibidor da síntese do DNA, tem como um de seus principais efeitos adversos a nefrotoxicidade causada pela injúria da célula tubular renal. A hiper-hidratação, necessária para diminuir este efeito indesejado, bem como a própria lesão renal podem induzir ao aparecimento de hipertensão113.
Além dos quimioterápicos, outras drogas utilizadas como adjuvantes na terapia do paciente oncológico como corticoides, ciclosporina, anti-inflamatórios não hormonais, inibidores da cicloxigenase e eritropoetina também podem causar hipertensão59. Devemos estar sempre atentos aos pacientes em uso destas medicações.
Afora os efeitos colaterais dos quimioterápicos e outras drogas, a HAS pode estar presente em pacientes oncológicos antes do tratamento por fatores relacionados ao próprio tumor, como é o caso da infiltração leucêmica renal ou da liberação de catecolaminas por tumores como o neuroblastoma e tumores adrenais110-112.
8.2.3. Manifestações clínicas/Diagnóstico
Na maioria dos casos a HAS é assintomática, no entanto, a elevação severa da PA aumenta o risco de eventos adversos como encefalopatia hipertensiva, convulsões, acidente vascular cerebral, sangramentos e insuficiência cardíaca. Estes sintomas, quando presentes, geralmente indicam hipertensão grave114. Mesmo a hipertensão menos severa contribui para o aparecimento em lesão em órgão alvo como hipertrofia miocárdica e doença renal, que podem ser flagrados em exames de rotina.
A recomendação atual é que a PA deve ser aferida em toda criança maior de 3 anos na consulta pediátrica de rotina, pelo menos uma vez ao ano, ou antes desta idade em situações especiais114. Desta forma, todo paciente oncológico que vai se submeter a tratamento quimioterápico deve ter sua PA aferida rotineiramente.
O procedimento de aferição da PA deve seguir as orientações da VI Diretrizes Brasileiras de Hipertensão111. Para que sejam obtidos valores fidedignos de PA na criança, faz-se necessário a utilização de manguito adequado para o tamanho e circunferência do braço da criança. Este é um importante aspecto a ser considerado para que se evitem erros no diagnóstico.
O diagnóstico de HAS é dado quando a PA encontra-se maior ou igual ao percentil 95 para sexo, idade e altura com aferições em ocasiões diferentes conforme as recomendações.
8.2.4. Prevenção
No que diz respeito à prevenção, um dos maiores avanços é a elaboração de documentos como este, no qual cardiologistas e oncologistas trabalham juntos a fim de melhorar o prognóstico da doença, qualidade de vida do paciente e sua sobrevida.
A prevenção da hipertensão deverá começar antes do tratamento oncológico, com avaliação multidisciplinar objetivando a busca, na história clínica do paciente, de fatores de risco para hipertensão, aferição da PA e reavaliações periódicas. Além disso, a realização de exames de rotina para monitorizar precocemente o aparecimento de sinais e sintomas da hipertensão111.
Estes pacientes devem ser orientados a mudanças no estilo de vida, como ingerir menor quantidade de sal, praticar atividade física quando possível, e adequação de peso naqueles com sobrepeso ou obesidade. Aqueles que já têm fatores predisponentes para HAS devem ter especial atenção durante o tratamento oncológico. Da mesma forma, após o término do mesmo, todos devem ter seguimento continuado também com o objetivo de detectar precocemente o aparecimento de HAS115.
8.2.5. Tratamento
Os objetivos do tratamento da hipertensão são diminuir morbidade, mortalidade e o risco de lesão em órgão alvo. A meta a ser atingida é manter a PA abaixo do percentil 95 e quando há alguma comorbidade como doença renal, diabetes, insuficiência cardíaca ou hipertrofia ventricular esquerda, abaixo do percentil 90. As indicações para tratamento medicamentoso da HAS em crianças incluem resposta inadequada a mudanças do estilo de vida ou hipertensão secundária (CR: I NE: C). Os pacientes oncológicos que desenvolvem hipertensão durante o tratamento por causa do uso de medicações pertencem a esta última indicação.
A terapêutica medicamentosa deve seguir as recomendações do The Fourth Report on the Diagnosis, Evaluation and Treatment of High Blood Pressure in Children and Adolescents e ser iniciada, preferencialmente, com monodroga.
Os grupos de drogas atualmente aceitos para o tratamento em crianças são: inibidores da enzima conversora da angiotensina (IECA), bloqueadores dos receptores da angiotensina (BRA), betabloqueadores, bloqueadores dos canais de cálcio e diuréticos, vasodilatadores arteriais (prazosin).
Graças à possível teratogenicidade, deve-se evitar a prescrição de IECA e BRA para adolescentes do sexo feminino (CR: 1 NE: C). Do mesmo modo, portadores de disfunção renal não poderão fazer uso dessa classe de drogas.
Pacientes em uso de sorafenib ou sunitinibe não devem receber como terapêutica anti-hipertensiva os bloqueadores de canais de cálcio dihidropiridínicos como verapamil e diltiazem, pois estas drogas competem entre si na inibição da isoenzima CYP3A4 (CR: 2 NE: B)20,59. A hipertensão arterial severa ou sintomática deve ser tratada com medicação intravenosa114. Especial atenção aos pacientes portadores de disfunção sistólica, limitando o uso dos bloqueadores dos canais de cálcio.
De forma geral, a medicação deve ser iniciada na menor dose recomendada e aumentada até que a meta de pressão arterial seja alcançada. Se a dose máxima for atingida e o efeito esperado não, uma segunda medicação de uma classe diferente deve ser associada114.
Crianças em uso de anti-hipertensivos devem ser monitorizadas periodicamente quanto à alteração de eletrólitos, lesão de órgão alvo e resposta terapêutica.
8.3. Arritmias
8.3.1. Incidência no paciente oncológico
Em pacientes com câncer, as arritmias são motivos de consultas por causa do tratamento quimioterápico e/ ou cirurgia. A relação entre a quimioterapia e arritmias não está bem estabelecida117, pois estudos que determinam a incidência de arritmias são realizados após o início da quimioterapia e não antes, sendo assim difícil determinar se estas arritmias refletem o estado inicial do paciente ou são efeitos colaterais provocados pela toxicidade de medicamentos quimioterápicos e/ou outras medicações potencialmente arritmogênicas utilizadas, o que torna difícil decidir qual deles causou este efeito adverso (vide Tabela 10).
A arritmia mais frequentemente encontrada é a fibrilação atrial (FA) e o quimioterápico mais relacionado com arritmias são as antraciclinas, com taxa de alterações ao eletrocardiograma (ECG) variando de 6 a 38,6%117.
8.3.2. Fisiopatologia
No paciente com câncer e em uso de quimioterapia, as arritmias podem ser causadas por diferentes situações: o câncer como fator arritmogênico118,119, infecções, distúrbios hidroeletrolíticos120, drogas quimioterápicas, medicações coadjuvantes a esse tratamento e período pós-operatório.
Contribuindo ainda para a arritmogênese a fibrose, inflamação crônica, efeitos das drogas sobre o sistema de condução, insuficiência cardíaca, miocardiopatia dilatada com disfunção ventricular.
O mecanismo de cardiotoxicidade se deve à geração de espécies de radicais de oxigênio e peroxidação lipídica da membrana celular. As antraciclinas entram nas mitocôndrias e inibem a cadeia respiratória por intermédio da ligação à cardiolipina ou da interação com o DNA mitocondrial, diminui a produção de ATP, levando à depleção de energia, podendo levar à morte celular. Um ciclo de interligados no DNA mitocondrial e insultos à cadeia respiratória podem continuar após o final do tratamento e na ausência de antraciclinas. Estes insultos podem explicar, em parte, a manifestação tardia de cardiomiopatia. Os cardiomiócitos, que se dividem muito lentamente, não podem substituir as células danificadas durante o tratamento121.
O intervalo QT no ECG corresponde à duração total da ativação ventricular e recuperação (despolarização e repolarização). A despolarização ocorre por meio de canais dentro da membrana das células do miocárdio que regulam o fluxo de íons para dentro e para fora das células cardíacas. Quando a saída de íons de potássio excede a entrada de sódio e de cálcio, ocorre repolarização do miocárdio. Quando há carga positiva em excesso intracelular, estende a repolarização ventricular resultando em um intervalo QT prolongado122. As variâncias biológicas do intervalo QT incluem sexo (as mulheres têm intervalos mais longos que os homens QT), os efeitos diurnos, tônus autonômico, níveis de atividade, a ingestão de alimentos, e FC (duração do intervalo QT diminui à medida que a frequência cardíaca aumenta)118,122.
Prolongamentos patológicos do intervalo QT podem resultar de uma anomalia genética nos canais (síndrome do QT longo congênita)118, remodelamento elétrico em resposta ao bloqueio atrioventricular, hipertrofia cardíaca e insuficiência, ou administração de medicamentos que prolongam o potencial de ação ventricular em miócitos, desequilíbrios de eletrólitos incluindo hipocalemia, hipomagnesemia, hipocalcemia e hipotermia122,123. O QTc prolongado e patológico pode causar arritmia cardíaca maligna como taquicardias ventriculares polimórficas do tipo Torsades de Pointes118,122,123, que é uma taquiarritmia ventricular polimórfica potencialmente fatal; aparece no ECG como uma torção contínua do vetor QRS em torno de uma linha de base isoelétrica. Ela pode degenerar em fibrilação ventricular, levando à morte súbita. Torsades de Pointes são correlacionados com uma medida do intervalo QTc de maior de 500ms118,122.
Desconhece-se um mecanismo definido para explicar os efeitos de prolongamento dos novos agentes oncológicos. Mecanismos indiretos incluem a variabilidade inerente da repolarização da população com câncer, presença de comorbidades, uma alta prevalência de uso de medicação concomitante criando o potencial para interações medicamentosas, e a predisposição do paciente a fatores adicionais que são conhecidos por aumentar o intervalo QT provocado por qualquer doença subjacente ou tratamento de câncer122,123.
Esses pacientes experimentam frequentemente náuseas, vômitos, diarreia e diminuição da ingestão oral, quer por causa de sua doença ou do tratamento desses fatores, que por si só podem predispor ao prolongamento do intervalo QT, mas também causar distúrbios eletrolíticos que aumentam o risco de arritmia ventricular118,122.
8.3.3. Manifestações clínicas
Os sintomas e manifestações clínicas estarão relacionados com o tipo de distúrbio do ritmo.
No caso de bradicardias, os sintomas são: fadiga, limitação da atividade física, pré-síncope e síncope.
Em relação às taquicardias, os sintomas são: palpitações, dor no peito, dor abdominal, pré-síncope. A taquicardia sinusal é a mais frequente e pode representar disfunção autonômica. Os sintomas geralmente desaparecem quando a terapia é interrompida.
8.3.4. Diagnóstico
É de grande importância, antes do tratamento quimioterápico, a realização da avaliação cardiológica.
Por intermédio do ECG basal, a identificação prévia de alguma alteração do ritmo indica a realização de Holter 24 horas. Recomenda-se a realização do ECG antes de cada ciclo quimioterápico.
Durante o tratamento quimioterápico na suspeita de arritmia, deve-se realizar um novo ECG e Holter 24 horas com monitorização cardíaca contínua nestes pacientes.
As alterações eletrocardiográficas mais frequentes são: alterações não específicas do segmento ST e alterações de onda T, diminuição da amplitude QRS e intervalo QT prolongado, bradicardias118, arritmias atriais e ventriculares. A fórmula de Bazett ainda é a mais utilizada para a determinação do QTc, sendo considerado aumentado o QTc maior de 450ms em homens e maior de 460ms em mulheres122,123.
As bradicardias são descritas como FC menor que 60bpm e as taquicardias como FC maior que 100bpm. Porém devemos correlacionar a FC do paciente pediátrico de acordo com tabelas que correlacionam FC e idade.
As taquiarritmias podem ser dividas de acordo coma a localização em supraventriculares e ventriculares, de acordo com a duração do QRS (QRS estreito menor que 90ms e QRS largo maior ou igual a 90ms) e de acordo com estado hemodinâmico (estável ou instável)124.
8.3.5. Prevenção
Monitoramento dos pacientes que receberam drogas quimioterápicas, especialmente naqueles com anormalidades ECG ou arritmias documentadas durante a exposição passada117,118,123.
As crianças ou adultos jovens mais sensíveis às antraciclinas devem ser observados cuidadosamente, incluindo o monitoramento de eletrólitos, principalmente de potássio118.
Zeltser descreveu 249 casos de Torsades de Pointes (TdP) provocados por medicamentos não cardíacos. Praticamente todos os pacientes tiveram um fator de risco e 71% apresentavam múltiplos fatores de risco.
No sexo feminino, o risco mais comum estava presente em 71%, e os fatores de risco já foram mencionados.
Alguns medicamentos prolongam QTc e podem induzir TdP de forma dose-dependente118. Outros podem precipitar TdP em qualquer dose.
As drogas que podem estar associadas à TdP são várias, entre elas: medicamentos antiarrítmicos, cisaprida, antibióticos macrolídeos como eritromicina e claritromicina, antibióticos fluoroquinolonas, pentamidina (antiprotozoário), antifúngicos utilizados no tratamento de infecções parasitárias e Pneumocystis carinii; outros antifúngicos sistêmicos (fluconazole, itraconazol, cetoconazol e voriconazol), antimaláricos, antipsicóticos (tioridazina, clorpromazina e mesoridazine), butirofenona (droperidol e haloperidol), e pimozida diphenylpiperidine, neurolépticos, antidepressivos tricíclicos, metadona e até suplementos nutricionais como o Césio. Por causa da diversidade de medicamentos implicados no prolongamento do intervalo QT, recomendamos o acesso às listas, disponíveis na internet: www.torsades.org, www.qtdrugs.org, www.longqt.org, www.sads.org124,125.
Apesar das limitações, o tratamento com medicamentos que prolongam o QT, se necessários, devem ser pesados contra os benefícios na avaliação do risco de terapia. Tratamentos alternativos devem ser considerados. Fatores de risco subjacentes precisam ser avaliados, e condições reversíveis devem ser corrigidas antes do início da droga. Polifarmácia, múltiplas medicações que prolongam o QT ou agentes que interferem com o metabolismo, devem ser evitados. Pacientes têm de ser aconselhados sobre o risco de pró-arrítmicos123. Muitos autores acreditam que pacientes que tomam o trióxido de arsênio devem ter monitorização com ECG frequente, pois são doentes que podem desenvolver um QTc >500ms; sintomas tais como palpitações ou síncope devem ser hospitalizados e monitorados122.
8.3.6. Tratamento
Quando um paciente realizando diagnóstico de taquiarritmias apresenta uma arritmia, excluir e tratar fatores agravantes como: distúrbios hidroeletrolíticos, infecções, hipovolemia e interação medicamentosa. Considerar o tratamento específico da arritmia e, dependendo do quadro, fazer uma avaliação conjunta das medidas a serem tomadas entre equipe cardiológica e oncológica (vide Tabela 11).
O tratamento agudo das taquiarritmias com QRS estreito sustentadas (supraventriculares), se o paciente estiver hemodinamicamente estável: manobra vagal, adenosina (não deve ser utilizada em pacientes sabidamente portadores de Wolff-Parkinson-White), e no caso de não reverter a utilização de outras drogas antiarrítmicas (amiodarona, propafenona, procainamida). Se o paciente for hemodinamicamente instável, realizar cardioversão elétrica sincronizada. Se o paciente tiver taquiarritmia de QRS largo (considerar taquicardia ventricular), com QRS organizado e paciente estável: adenosina, amioadarona, lidocaína. Se o paciente for instável hemodinamicamente e com QRS organizado, utilizar cardioversão elétrica sincronizada; se com QRS desorganizado, utilizar desfibrilação (sem sincronizar)124.
QT prolongado e Torsades de Pointes: Sulfato de Magnésio = 25 a 50mg/kg em 10 a 20min, independentemente do nível sérico123,124. Potássio sérico deve ser mantido na faixa normal alta (4,5-5mmol/L)123. Medicamentos que prolongam o QT e drogas interferindo com o seu metabolismo devem ser imediatamente interrompidas117. Marcapasso provisório com estimulação é altamente eficaz para encurtar o QTc e é altamente eficaz na prevenção de recorrências. É especialmente útil em casos refratários ao magnésio ou quando TdP é precipitada por uma pausa ou bradicardia125-127.
8.4. Eventos tromboembólicos (ET)
8.4.1. Incidência no paciente oncológico
Embora considerado raro na população pediátrica, o diagnóstico de eventos tromboembólicos (ET), que incluem o tromboembolismo venoso (TEV) e tromboembolismo pulmonar (TEP), tem aumentado consideravelmente e é considerado epidêmico nas crianças atendidas em hospitais terciários128.
A incidência de ET na população pediátrica geral é de 0,07 a 0,14 casos/10.000 crianças ou 5,3/10.000 por encaminhamento hospitalar. A curva de distribuição etária tem um comportamento bimodal, com picos de incidência em neonatos e adolescentes129.
Nos registros canadenses de trombose em pediatria, o câncer foi relacionado à etiologia dos ET em 22,6% dos casos130. O diagnóstico de TEV tem importante implicação clínica uma vez que o paciente oncológico com diagnóstico de TEV apresenta maior morbidade e mortalidade.
A incidência média de trombose em criança com doença maligna é de 8%. Entre os tumores pediátricos o TEV ocorre mais frequentemente nas leucemias agudas (LLA), seguida pelos sarcomas, linfomas, leucemia mieloide aguda (LMA), tumor de Wilms, neuroblastomas e tumor de sistema nervoso central.
A incidência de ET em crianças com LLA varia de 1,1 a 36,7%, com uma média de risco de 5,2% entre o diagnóstico e o final da fase de manutenção131. A ampla variação da taxa de incidência resulta dos diferentes protocolos quimioterápicos utilizados, da definição de ET (trombose sintomática ou assintomática) do desenho do estudo e do método de diagnóstico utilizado para a detecção do TEV.
Em pacientes com linfomas, tumores sólidos e tumor de SNC a incidência estimada é de 7 a 16%. A prevalência de ET sintomática em crianças com sarcomas é maior nos sarcoma de Ewing, seguida de rabdomiosarcoma e osteossarcoma132.
No registro canadense, TEP teve uma incidência de 0,86 por 10.000 admissões hospitalares133. Esta incidência é menor que a estimada para adolescentes (7,8 por 10.000) e muito menor que a documentada para adultos hospitalizados. Entretanto a baixa incidência pode ser secundária a um baixo índice de suspeita diagnóstica de TEP nos pacientes pediátricos. As consequências em longo prazo do TEP para as crianças ainda são desconhecidas.
Trombose do átrio direito é uma complicação potencialmente fatal e mais de 80% dos casos estão associados à presença de cateter e 2 a 9% dos casos de trombose associada à cateter também tem trombose presente no átrio direito134.
8.4.2. Agentes mais envolvidos
A etiologia nas crianças difere da população adulta uma vez que 40% dos adultos apresentam ET idiopático e, nas crianças, os fatores de risco adquiridos precipitam 60 a 96% dos eventos. Várias condições clínicas são relacionadas à etiologia dos ET tais como cirurgias recentes, doença cardíaca congênita, imobilização, trauma, síndrome nefrótica, uso de contraceptivos orais, trombofilia congênita e a presença de cateter venoso central (CVC), que é o fator predisponente isolado mais importante.
Nos casos de linfomas, a alteração do fluxo sanguíneo decorrente da presença de massa mediastinal ao diagnóstico é um fator de risco para o diagnóstico de TEV135.
O uso de L-asparaginase tem sido relacionado a uma supressão natural de anticoagulantes, particularmente antitrombina e plasminogênio. Uso de corticosteroide pode elevar à ativação do complexo FVIII-von Willebrand e à ativação do inibidor plasminogênio (PAI-1). A combinação de L-asparaginase e corticoide utilizada em protocolos de tratamento das LLA é um fator de risco alto para o desenvolvimento de ET, principalmente na fase de indução onde ocorre uma redução da capacidade de inibir a trombina.
Um risco adicional para o desenvolvimento de ET em crianças com câncer está relacionado com as características genéticas do hospedeiro. A deficiência de anticoagulantes naturais tais como a antitrombina, proteína C e proteína S são os fatores genéticos mais frequentemente relacionados à ET na população pediátrica131. Uma recente meta-análise relaciona um risco até 8 vezes maior em crianças com LLA, e pelo menos um fator genético associado.
A história de trombose é um fator predisponente para recorrência de ET. Na população pediátrica, a proporção de recorrência é de 3% em neonatos e 8% em crianças, podendo chegar a 21% em crianças cujo ET foi idiopático.
8.4.3. Trombose e cateteres
Cateter Venoso Central (CVC) pode provocar trombose pelos mais diferentes mecanismos: lesão da parede da veia durante a inserção, irritação relacionada ao material do cateter, tamanho do cateter em relação ao diâmetro do vaso, tempo de permanência do cateter, infusão de substâncias que podem causar lesão do endotélio. A presença do cateter pode dificultar o fluxo sanguíneo causando estase e obstrução.
Um estudo sobre profilaxia antitrombótica em crianças com LLA tratadas com L-asparaginase que usou testes radiológicos no diagnóstico de trombose identificou uma incidência de 33% de TEV assintomático relacionado a cateter136. Na população pediátrica os ET assintomáticos assumem importância clínica, pois esses eventos estão quase sempre associados a fatores de risco e a persistência desses fatores propagará o estímulo pró-trombótico até que os sintomas se tornem evidentes.
8.4.4. Fisiopatologia
O câncer pode provocar um estado de hipercoagulação por muitos mecanismos, estase sanguínea pela imobilização, secreção de pró-coagulantes, fibrinolíticos, liberação de citocinas inflamatórias pelas células tumorais, lesão vascular como resultado do uso de cateter, quimioterapia, invasão tumoral etc. Estudos recentes demonstram que as propriedades pró-coagulantes das células tumorais conferem uma vantagem seletiva para a invasão tumoral e as metástases137.
O Quadro 7 resume alguns dos principais fatores biológicos envolvidos no estado pró-coagulante associado ao câncer.
8.4.5. Manifestações clínicas
Edema, dor e descoloração das extremidades são sinais e sintomas agudos de TEV. A trombose da veia cava inferior se manifesta com veias proeminentes cutâneas e possivelmente disfunção hepática ou renal, dependendo da extremidade e extensão do trombo129. A trombose de veia cava superior leva a cianose e edema da cabeça e tórax superior, com veias colaterais importantes e pode finalmente resultar em insuficiência cardíaca aguda. A trombose de veia porta, na maioria dos casos causada por cateteres centrais, e a trombose de veia renal com hematúria podem resultar em prejuízo da função hepática e renal, respectivamente. Dor torácica aguda e dispneia podem sugerir TEP. Cefaleia, deficiência visual, convulsões cerebrais e sinais de congestão venosa podem indicar trombose de seio venoso.
Fatores preditores do risco associado à TEP utilizados em adultos não foram validados na população pediátrica.
Um ET associado ao cateter pode se manifestar de diversas maneiras como: disfunção do cateter, bacteremias, edema do membro e/ou região, formação de vasos colaterais e quilotórax.
Emergências trombóticas ocorrem em decorrência de uma obstrução total da veia cava superior, TEP, trombose cerebral de seio venoso, isquemia de membros, ou mais raramente, eventos trombóticos intracardíacos.
8.4.6. Diagnóstico
O ultrassom Doppler venoso (USG) é o exame recomendado como método de imagem para avaliação inicial de uma suspeita de TEV. É um método não invasivo que não necessita de contraste, tem baixo custo e possibilidade de ser realizado na beira do leito, tem boa acurácia no TEV de veias poplíteas e femorais, mas há dificuldade de avaliação de veias mais centrais. Outras desvantagens são que a sensibilidade do método depende do segmento venoso acometido, há limitações associadas a dor local e à técnica do operador.
Em caso de USG negativo e forte suspeita clínica de TEV pode-se realizar angiotomografia com contraste, ecocardiograma transtorácico, venografia por ressonância magnética e venografia invasiva.
Os resultados do PARKAA, estudo que comparou o USG com a venografia para o diagnóstico de TEV assintomático nas veias superiores em crianças em tratamento de LLA, demonstram que, embora o USG seja uma técnica viável para o diagnóstico de TEV em membros inferiores e vasos do pescoço, houve uma baixa sensibilidade do USG comparado à venografia para o diagnóstico de TEV no sistema venoso superior138. A combinação de USG e venografia é a melhor estratégia para investigar TEV no sistema superior.
Para o diagnóstico de TEP em crianças dispomos do mesmo arsenal de imagem que o utilizado na população adulta, a saber: estudo de ventilação/perfusão e angiografia pulmonar por tomografia computadorizada, considerada a técnica de "padrão ouro" para o diagnóstico. Entretanto sua realização é limitada pelos riscos de morbidade e mortalidade associados. A tomografia computadorizada oferece uma boa imagem das estruturas e pode auxiliar no diagnóstico diferencial de TEP.
O Ecodopplercardiograma deve ser realizado em todos os casos de trombose associado à CVC, trombo intracardíaco e tromboembolismo pulmonar.
Todo ET inicia uma resposta em particular para restabelecer o equilíbrio do sistema hemostático, e o uso de marcadores da fibrinólise, como o D-dímero, pode ser detectado na circulação. A especificidade da dosagem do D-dímero é baixa, mas o valor preditivo negativo do teste é alto o suficiente para excluir a hipótese de TEV em adultos. Estudo realizado em crianças mostrou que D-dímero foi negativo em 36 a 40% das crianças com TEP133. No entanto, a elevação desses marcadores no diagnóstico e durante o acompanhamento são significativamente correlacionados com a persistência e/ou recorrência do ET.
8.4.7. Tratamento
A maior parte das recomendações terapêuticas para a população pediátrica são diretamente extrapoladas das orientações para a população adulta139.
O relativo aumento da incidência dos ET na população pediátrica, sobretudo nas crianças com neoplasias, permitirá a execução de estudos clínicos controlados para que se conheça melhor o diagnóstico, profilaxia e opções terapêuticas específicas para esta faixa etária.
O objetivo do tratamento dos ET é interromper o processo e, quando possível, permitir a recanalização do vaso. E o maior desafio é conseguir um adequado equilíbrio entre os riscos e benefícios do tratamento em crianças que receberão quimioterapia com consequente plaquetopenia intermitente e um sistema hemostático com um equilíbrio instável.
Existem três categorias de terapia antitrombótica: os anticoagulantes, os agentes antiplaquetários e os fibrinolíticos. Os agentes antifibrinolíticos e os antiplaquetários, usados sobretudo no tratamento de ET arteriais, não representam foco dessa diretriz.
8.4.7.1. Anticoagulantes
Os principais anticoagulantes utilizados são a heparina não fracionada (HNF), a heparina de baixo peso molecular (HBPM) e os antagonistas da vitamina K (AVK).
A atividade de anticoagulação da HNF pode ser monitorada com a medida da tromboplastina parcial ativada (TTPa) ou pelo anti-Xa. Em crianças não há uma forte correlação entre esses dois exames e a dose pode ser ajustada conforme esquema ilustrado na Tabela 12. Uma das vantagens da HNF é que ela pode ter seu efeito totalmente reversível com o uso de sulfato de protamina (1mg de protamina pode neutralizar aproximadamente 100 unidades de HNF). Essa droga deve ser administrada lentamente por causa do risco de bradicardia e hipotensão. Entre as principais complicações ressaltam-se sangramentos (o risco de sangramento maior associado a UNF é de aproximadamente 12%), osteoporose, alterações das enzimas hepáticas e a trombocitopenia induzida pela heparina, o que deve ser fortemente considerado para os pacientes que utilizam quimioterapia mielossupressora.
A dosagem do anti-Xa é o exame recomendado para monitorar o uso de HBPM. O risco de sangramento em crianças em uso de HBPM é de 3% para sangramento maior e 23% para pequenos sangramentos. Osteoporose, plaquetopenia e alteração das enzimas hepáticas ocorrem bem menos frequentemente quando comparada a HNF. O sulfato de protramina pode reverter 60 a 70% da atividade da HBPM em até 8 horas; neste caso recomenda-se uso de 1mg de protamina para cada 1mg de HBPM, e a metade da dose (0,5mg de protamina) caso o sangramento persista. As Tabelas 13 e 14 ilustram as doses recomendadas e ajustes de HBPM para tratamento de acordo com a faixa etária.
Os AVK têm sua atividade monitorada pelo tempo de protrombina e a relação padrão internacional (INR) que deve ser mantida entre 2 e 3. O uso de vitamina K ou plasma são usados para reverter a ação deste anticoagulante.
Segundo recomendações da American College of Chest Physicians (CHEST) deve-se iniciar o tratamento de ET em crianças com câncer com HBPM na dose de 1mg/kg/dose a cada 12 horas com dose ajustada para atingir um nível de anti-Xa de 0,5 a 1,0U/ml como ilustrado no Quadro 4, por um período mínimo de 3 meses ou até que o fator predisponente tenha sido removido (CR:II NE:C)136,139. O uso da heparina convencional fica restrito aos casos de progressão do trombo em uso de HBPM com dosagem correta (anti-Xa 0,5 a 1,0U/ml).
O curso do tratamento oncológico e a necessidade de cirurgias, quimioterapia ou outros tratamentos podem modificar o risco/benefício do tratamento do TEV e o oncologista e o hematologista devem considerar um tratamento individualizado.
O uso profilático de antitrombóticos em crianças com CVC não é recomendado - (CR:I NE:B)136. Entretanto, se a trombose estiver associada ao CVC este deve ser removido após três a cinco dias da anticoagulação.
Em crianças com peso corporal acima de 10 quilos com o diagnóstico de TEV em membros inferiores e com contraindicação para a anticoagulação: sangramento ativo, história de sangramento em sistema nervoso central ou lesão espinal, com plaquetopenia menor que 50.000/mm3; recomenda-se o uso de filtros de veia cava inferior (CR: II NE:C). Outras indicações para o uso de filtro são: pacientes com intolerância à anticoagulação, por exemplo, sangramentos graves ou dificuldade em atingir o nível terapêutico e recorrência do ET apesar da terapia adequada. A trombectomia só deve ser aventada nos casos de risco de morte.
A duração e intensidade do tratamento ainda permanecem controversas na literatura, pelo menos para este grupo específico de crianças. Após o primeiro episódio de TEV, deve-se manter profilaxia secundária por pelo menos 6 meses ou enquanto durar o tratamento do câncer, o que acontecer por último. Todos os estudos mostram um bom perfil de segurança com o uso de HBPM em pacientes com câncer, ressaltando que esta medicação é mais segura que o uso de AVK neste grupo de pacientes. Profilaxia perene é indicada após TEP ou recidiva do ET.
8.5. Isquemia miocárdica
A prevalência da isquemia do miocárdio em jovens é difícil de ser estabelecida, já que de maneira geral apresenta-se como uma doença silenciosa. Os poucos estudos disponíveis são os de necropsia em jovens vítimas de acidentes, suicídio ou homicídio140.
Apesar da incidência baixa da isquemia do miocárdio em jovens, estimada em oito a nove vezes menor que nos pacientes com mais de 50 anos, discute-se a repercussão da doença isquêmica na qualidade de vida desses pacientes. Os fatores de risco, as manifestações clínicas e prognóstico diferem dos pacientes mais velhos.
8.5.1. Fatores de risco:
1 - Tabagismo: é o fator de risco mais comum nos pacientes jovens com isquemia do miocárdio.
2 - História familiar: estudo demonstrou a alta incidência de doença isquêmica familiar140.
3 - Dislipidemia: nos jovens com doença isquêmica a incidência de dislipidemia é semelhante aos pacientes mais velhos.
4 - Diabetes mellitus e a hipertensão arterial parecem ter uma importância menor como fatores de risco para isquemia do miocárdio nos pacientes jovens140.
5 - Obesidade: índice de massa corpórea aumentado está associado com um maior risco de aterosclerose em coronárias140.
6 - Outros fatores: contraceptivos, adição de cocaína, doença de Kawasaki (lesão da camada íntima com risco de estenose e aneurisma de coronária em jovens e crianças).
7 - Antecedente de quimioterapia sistêmica ou radioterapia de tórax.
8.5.2. Isquemia do miocárdio no paciente oncológico
8.5.2.1. Radioterapia
A radioterapia torácica está associada com a toxicidade cardiovascular. O risco de infarto agudo do miocárdio é três vezes maior na população submetida à radioterapia torácica que na população geral. Apesar dos avanços no tratamento radioterápico, o campo e a dose de radiação determinam o grau de injúria ao coração. A radiação torácica pode induzir ou acelerar a doença coronariana, afetando as principais artérias como o tronco da coronária esquerda ou a artéria descendente anterior140. O risco de toxicidade cardíaca aumenta nos pacientes com doença cardiovascular preexistente. Nos hipertensos, nos tabagistas, nos dependentes de cocaína e nos portadores de dislipidemia, esses fatores de risco devem ser agressivamente controlados para reduzir o risco de dano ao coração pela radiação. Os pacientes20 que necessitam de radioterapia torácica e foram previamente tratados com antracíclicos, platina ou fluoracil, devem ser observados com mais cuidado, pois apresentam maior risco de desenvolverem cardiopatia.
O aumento do risco de cardiopatia grave persiste por 20 anos após o tratamento de câncer na infância. A incidência de doença coronariana 20 anos após a radioterapia é de 21%. A incidência de infarto agudo do miocárdio 30 anos após a radioterapia do manto no tratamento dos linfomas é de 13%141,142.
O comprometimento de porções proximais das artérias coronárias está relacionado com a incidência de infarto do miocárdio fatal e morte súbita143.
Muitos pacientes são assintomáticos. Investigação sistemática com "stress", ecocardiograma ou cintilografia miocárdica deve ser instituída nos pacientes que receberam a dose de 35Gy ou mais de radiação mediastinal, a partir de cinco anos após o tratamento144.
8.5.2.2. Quimioterapia
Paciente do sexo masculino tratado de câncer de testículo com 850mg ou mais de cisplatina tem três a quatro vezes maior risco de doença cardiovascular e morte súbita141. Os mecanismos propostos para doença isquêmica do miocárdio em pacientes submetidos à quimioterapia com cisplatina são: espasmo de coronária, proliferação fibrosa da camada íntima, trombogênese, dissecção hemorrágica da camada média, resultando num falso lúmen e isquemia distal.
A cisplatina pode ser detectada no soro, muitos anos após a administração, causando um processo inflamatório no endotélio e aterosclerose145,146.
Pacientes submetidos à quimioterapia com fluoracil apresentam risco de toxicidade cardíaca147 (1,2 a 18%), cuja mortalidade relacionada a esse quimioterápico varia entre 2,2 a 13,3%. Pacientes com coronariopatia prévia têm maior predisposição. Mecanismos envolvidos: injúria miocárdica, trombogênese, reação imunológica ou espasmo da coronária (mecanismo mais aceito). A infusão contínua aumenta o risco quando comparada com a infusão em "bolus". A pró-droga do fluoracil, capecitabine, também está associada com a doença isquêmica do miocárdio. O tratamento com fluoracil ou capecitabine deve ser suspenso se o paciente apresentar angina durante a infusão ou infarto agudo do miocárdio, recomendando-se a monitorização eletrocardiográfica contínua durante sua infusão.
8.5.2.3. Manifestação clínica
A primeira manifestação da doença isquêmica no jovem pode ser o infarto agudo do miocárdio. Esses pacientes em geral não apresentam angina péctoris148. Alterações eletrocardiográficas observadas nos jovens com isquemia do miocárdiose assemelham-se aos pacientes idosos: elevação ou depressão do segmento ST, ondas de necrose, elevação e queda lenta da troponina, elevação e queda rápida da CK-MB.
8.5.2.4. Diagnóstico diferencial
Pacientes com miocardite podem apresentar quadro clínico que pode ser confundido com infarto agudo do miocárdio, principalmente se apresentarem cinecoronariografia normal149.
8.5.2.5. Achados na cinecoronariografia
Coronárias normais foram observadas em 18% dos pacientes jovens com infarto agudo do miocárdio. Comprometimento de uma artéria em 55 a 60% dos pacientes jovens com infarto agudo do miocárdio149, sendo que a artéria descendente anterior foi o vaso mais frequentemente observado.
8.5.2.6. Tratamento
8.5.2.6.1. Tratamento da doença coronariana aguda
Pacientes jovens com elevação do segmento ST no eletrocardiograma devem ser tratados com angioplastia ou trombólise química (caso a angioplastia não esteja disponível). Estudos prospectivos randomizados demonstraram que a sobrevida é maior nos pacientes submetidos à angioplastia.
Pacientes com dor torácica, alteração de enzimas, sem alteração eletrocardiográfica (elevação do segmento ST ou onda de necrose) a princípio devem ser tratados com medicamentos; a indicação de tratamento invasivo é incerta, já que há poucos pacientes com menos de 40 anos nos grandes estudos de referência. Por outro lado, se esses pacientes apresentarem angina instável, alterações dinâmicas no eletrocardiograma, alterações cinéticas no ecocardiograma, disfunção ventricular severa, instabilidade hemodinâmica ou taquicardia ventricular sustentada, indica-se cinecoronariografia, angioplastia e implante de stent150.
8.5.2.6.2. Tratamento da doença coronariana crônica
Nos pacientes com angina estável não indicamos estudo cinecoronariográfico. Quando necessárias, tanto a angioplastia como a cirurgia de revascularização do miocárdio são eficazes e associadas a baixas complicações nos pacientes jovens quando comparadas com os pacientes mais velhos.
A angioplastia percutânea com taxa de sucesso de mais de 90% e taxa de re-estenose de 28%, acompanhando-se de redução rigorosa nos lípides plasmáticos, terapia antiplaquetária agressiva e stents farmacológicos reduziram a progressão e o risco da doença coronária fatal.
Os jovens com doença isquêmica do miocárdio toleram bem o stress cirúrgico e anestésico, além de apresentarem, de maneira geral, condições melhores que os pacientes mais velhos.
8.5.2.7. Prognóstico após infarto agudo do miocárdio
Inicialmente se considerava que o infarto agudo do miocárdio no paciente jovem estava relacionado com um prognóstico adverso, entretanto, muitos pacientes não apresentam doença coronariana severa, o que predispõe a uma evolução e prognóstico tardio favorável. Recomendamos abolir o uso do tabaco e da cocaína (quando presentes), atividade física regular e terapia agressiva para controle dos lípides, do diabetes mellitus e da hipertensão arterial quando presentes151,152.
8.6. Pericardiopatias
O pericárdio é uma membrana de origem mesotelial que recobre o coração e a porção inicial dos grandes vasos da base. Possui dois componentes: o epicárdio, ou pericárdio visceral (mais interno), e o pericárdio parietal (mais externo). Os nervos, artérias, veias e vasos linfáticos localizam-se sob o epicárdio. Entre o pericárdio visceral e o parietal existe um espaço contendo um ultrafiltrado do plasma que permite a livre movimentação do coração dentro do saco pericárdico. Quando submetido a uma agressão, o pericárdio reage com quadro inflamatório representado por exsudação de líquido, fibrina ou células, dependendo da intensidade do processo e do agente causal. Os vasos linfáticos são a principal via de acesso de tumores ao pericárdio153.
8.6.1. Incidência
Dentre as pericardiopatias decorrentes do tratamento oncológico, o derrame pericárdico pode atingir até 21% de incidência, dependendo do tipo de câncer, do seu comportamento e do tipo de tratamento submetido. Leucemias, linfoma não Hodgkin e doença de Hodgkin são os que mais causam pericardites na infância. A efusão pericárdica também pode ser encontrada em pacientes com linfossarcoma, por causa de sua disseminação direta. Sem dúvida alguma, a radioterapia é a terapia mais causadora de derrame pericárdico (20 a 40%)153.
8.6.2. Manifestações clínicas
Em geral, as doenças neoplásicas afetam o pericárdio de quatro maneiras153,154:
Neoplasias secundárias, sejam metastáticas e/ou causadas pela extensão de lesões em estruturas vizinhas (relativamente comum);
Tumores pericárdicos primários, benignos ou malignos (incomuns);
Efusões pericárdicas não neoplásicas com etiologia desconhecida (supostamente autoimunes), porém com algum componente neoplásico em outra parte do corpo;
Relacionadas a complicações da terapia: associadas com radioterapia, quimioterapia e imunossupressão.
Os corações de crianças e adolescentes são particularmente vulneráveis à ação de agentes quimioterápicos cardiotóxicos, bem como radioterapia mediastinal, podendo em algum momento desenvolver algumas das formas de acometimento pericárdico mencionadas acima, com consequentes alterações eletrocardiográficas, efusões (derrames até o tamponamento), inflamações, infecções, doença por aderência entre os folhetos e constricção, arritmias e parada cardíaca97. Como os efeitos tóxicos podem ocorrer durante, imediatamente após ou mais tardiamente ao seu uso, os clínicos devem estar sempre alertas quanto a essas possibilidades, que literalmente expõem os pacientes a alto risco20,97,152.
Algumas drogas utilizadas na quimioterapia podem determinar o aparecimento de pericardite e derrame pericárdico, tais como doxorrubicina, ciclofosfamida, imatiniba, busulfan, citarabina, ácido transretinoico e bleomicina154.
Em casos de tumores primários do coração, o líquido pericárdico acumulado pode ser seroso ou hemorrágico, geralmente associado a tumores pericárdicos mas, eventualmente, secundários a outros tumores, incluindo os intracavitários, como o rabdomioma. No pericárdio, os tumores primários são raros, sendo o mais comum o teratoma que se apresenta de forma cística e multiloculada. Constitui um tumor benigno mediastinal extracardíaco, porém pode ocasionar compressão extrínseca das cavidades cardíacas. O lipoma é outro tumor benigno que pode comprimir externamente o coração, se a localização for no pericárdio. Os angiomas consistem em formações cavernosas grandes ou apenas pequenos pontos de hemorragias na superfície atrial, nas valvas atrioventriculares e também no pericárdio151.
Dos tumores cardíacos malignos primários, os mais freqüentes são os sarcomas. Em geral, originam-se no átrio esquerdo, provenientes do endocárdio ou do miocárdio, mais raramente do saco pericárdico.
Os tumores metastáticos malignos são raros no coração, como os linfomas, as leucemias, os linfossarcomas, os carcinomas boncogênicos e carcinoma de mama, melanoma ou qualquer outra neoplasia sistêmica. O epicárdio é o sitio de maior incidência de acometimento nestes casos. A invasão pode ser direta das estruturas adjacentes, como o pulmão, a pleura e o timo, ou pela disseminação pelo sistema linfático.
Pode ocorrer compressão extrínseca de cavidades cardíacas direitas determinando restrição ao enchimento diastólico destas cavidades. A restrição é maior em caso de formação de derrame pericárdico, o qual é seroso em tumores benignos e hemorrágicos nos malignos. É importante ressaltar que o tamponamento cardíaco pode ser a primeira manifestação clínica de tumores pericárdicos ou mediastinais, incluindo os de etiologia maligna.
As doenças pericárdicas podem ser difíceis de diferenciar de algumas condições miocárdicas.
A infiltração pericárdica pode não ser a manifestação inicial da doença neoplásica, e o tamponamento pode ocorrer tardiamente durante o curso da doença.
A pericardite pode ser aguda com derrame pericárdico, às vezes com tamponamento cardíaco, necessitando de alívio com pericardiocentese. Evolutivamente, poderá ocorrer espessamento pericárdico com fibrose e progressão para pericardite constritiva, necessitando de pericardiectomia.
8.6.3. Diagnóstico
No comprometimento pericárdico causado por tumores primários ou secundários, em que as cavidades cardíacas são comprimidas, a manifestação eletrocardiográfica pode ser de sobrecarga de cavidades ventriculares: esquerda, quando a compressão se dá nas câmaras direitas (mais frequente); e direita em casos de compressão das cavidades esquerdas (mais rara). Da mesma forma, quando o envolvimento é provocado pela ação tóxica quimio ou radioterápica sobre o miocárdio e pericárdio, os sinais eletrocardiográficos de sobrecargas de câmaras cardíacas e subsequentes alterações na repolarização ventricular são evidentes. Quando o quadro predominante é o de derrame, a baixa voltagem dos complexos eletrocardiográficos além das alterações na repolarização ventricular levantam a suspeita150,155.
Os tumores pericárdicos ou a presença de derrame podem alargar a área cardíaca no exame radiológico do tórax (cardiomegalia) e deformar a silhueta cardíaca e o pedículo vascular, dependendo de sua extensão e localização. A presença de calcificação tumoral é rara e pode ser evidenciada nos teratomas. Nos casos de pericardite constritiva, evidenciamos um predomínio da silhueta atrial esquerda e direita em comparação aos diâmetros ventriculares, bem como sinais de aumento da trama capilar pulmonar. Apesar disso, a radiografia do tórax não consegue determinar o grau de disfunção cardíaca ou tamponamento cardíaco150.
O ecocardiograma com Doppler colorido é o método diagnóstico inicial mais útil na presença de pericardiopatias. Na maioria dos casos, evidencia a presença de líquido patológico entre os folhetos do pericárdio (derrame), definindo seu grau de repercussão hemodinâmica (comprometimento restritivo) e grau de comprometimento sistólico da função miocárdica. Nos casos de tumores pericárdicos, permite também avaliar o comportamento do mesmo sugerindo uma orientação inicial quanto ao aspecto benigno ou maligno e sua extensão ao longo das estruturas cardíacas156,157.
Na avaliação da doença pericárdica, a tomografia computadorizada e a ressonância nuclear magnética tradicionalmente têm sido usadas como adjuntos ao ecocardiograma. Esses métodos são particularmente sensíveis e não invasivos na avaliação do derrame pericárdico loculado ou hemorrágico, pericardite constritiva e massas pericárdicas. Ambos os métodos permitem excelente delineação da anatomia pericárdica e podem ajudar na localização precisa e caracterização de várias lesões pericárdicas, incluindo derrame, pericardite constritiva e espessamento pericárdico, massas pericárdicas e anomalias congênitas, tais como ausência completa ou parcial de pericárdio, permitindo maior campo de visão que o ecocardiograma158.
8.6.4. Tratamento
O tratamento das complicações pericárdicas visa o alívio dos sintomas e a estabilização hemodinâmica do paciente, dependendo da presença de sinais clínicos e ecocardiográficos de comprometimento funcional, até o tamponamento cardíaco. Algumas vezes, a recorrência do problema deverá ser considerada156-158.
Medicamentos anti-inflamatórios: No caso de derrame, se não houverem sinais imediatos de tamponamento cardíaco, ou ameaça de evolução para tal, pode-se usar anti-inflamatórios não esteroides ou até mesmo uso de corticoides, mediante discussão antecipada com a equipe oncológica;
Pericardiocentese: procedimento que remove o excesso de fluido do pericárdio causando o alívio dos sintomas. Pode ser guiado pela ecocardiografia que auxilia no trajeto da agulha e reduz a possibilidade acidental de perfurar o ventrículo direito. A análise do líquido pericárdico por meio de punção ou drenagem também auxilia no diagnóstico da neoplasia;
Esclerose intrapericárdica: raramente indicada hoje, atua através de injeção de substâncias químicas (bleomicina, antibióticos, agentes quimioterápicos) no pericárdio após esvaziamento por meio da pericardiocentese, causando inflamação e colabamento dos folhetos;
Pericardiectomia: remoção cirúrgica de todo pericárdio ou parte dele. Deve ser considerado em casos de derrames recorrentes ou em situações de fibrose com comportamento restritivo. Permite análise por biópsia.
Remoção cirúrgica do tumor, propriamente dito, com consequente esquema terapêutico oncológico específico.
9. Cardioproteção
Agentes citotóxicos como as antraciclinas são quimioterápicos frequentemente utilizados no tratamento de neoplasias em crianças e adultos jovens. Desde a sua introdução nos protocolos terapêuticos, observamos melhoras nas taxas de sucesso terapêutico, atingindo 75 a 80% de cura. Estima-se que dois terços dos pacientes tratados com antracíclicos venham a apresentar eventos adversos tardios, sendo a cardiotoxicidade o mais temido nestes casos, podendo surgir anos depois do término da quimioterapia9,159,160.
Reduzir a morbidade e a mortalidade associada à cardiotoxicidade sem, no entanto, perder o potencial terapêutico das antraciclinas, faz com que se busquem formas de prevenir o surgimento desta temida complicação. O reconhecimento dos fatores de risco para cardiotoxicidade (sexo feminino, extremo das idades, presença de outras cardiopatias, dose acumulada utilizada e associação com outras drogas cardiotóxicas) e a monitorização cardiológica durante e após o término da quimioterapia são os primeiros passos. Na prática, a variabilidade na susceptibilidade individual e a ausência de um esquema de monitorização sensível para identificação do comprometimento subclínico nos leva ainda a depender de outras formas de cardioproteção9,159,160.
Três formas de prevenir a injúria miocárdica foram testadas na população pediátrica12,160-164:
1 - Redução da concentração celular das antraciclinas ou de seus metabólitos, quer por limitação da dose acumulada ou pelo aumento do tempo de infusão;
2 - Utilização de drogas ou formulações menos cardiotóxicas, modificadas estruturalmente (epirrubicina, idarrubicina, antraciclina lipossomal);
3 - Administração de drogas consideradas cardioprotetoras.
A utilização de vários critérios para o diagnóstico de cardiotoxicidade dificulta a interpretação do momento em que a quantidade da dose aumenta o risco de cardiotoxicidade. Na década de 1970, a utilização de doses superiores a 400mg/m2 foi relacionada à elevada incidência de insuficiência cardíaca165,166. Posteriormente, já na década de 1990, os resultados do Dana-Farber Cancer Institute167 demonstraram uma redução da incidência de disfunção ventricular esquerda em pacientes tratados com doses inferiores a 300mg/m2.. Entretanto, as recentes descrições de elevação de troponina após o primeiro ciclo com doxorrubicina, o comprometimento da função sistólica identificada por métodos mais sensíveis que o cálculo da fração de ejeção e sinais de cardiotoxicidade subclínica ao estudo pela ressonância nuclear magnética e ecocardiografia com speckle tracking derrubaram o conceito de dose segura de antraciclina.
Lipshultz, em 2002, ao comparar a infusão em bolus de doxorrubicina versus infusão contínua em 48 horas em crianças com LLA, não identificou diferença significativa na incidência de cardiotoxicidade; entretanto, essa foi mais frequente em ambos os grupos quando comparados com a população em geral51.
Dentre os análogos à doxorrubicina, tais como epirrubicina e idarrubicina, a apresentação de doxorrubicina lipossomal é a que apresenta resultados mais favoráveis. Apesar do número limitado de estudos em crianças, estudos com biópsia endomiocárdica já comprovaram um perfil de segurança maior do que nas antraciclinas convencionais.
Outras formas de cardioproteção demonstradas em estudos na população adulta, apesar de promissores resultados em curto prazo, tais como o uso profilático de inibidores da IECA ou do carvedilol161 ainda não foram evidenciadas na população pediátrica. Da mesma forma, citações quanto ao emprego de agentes considerados cardioprotetores (N-acetilcisteína, fenetilaminas, coenzima Q10, vitamina E e C, L-carnitina e amifostina) também não apresentaram evidências suficientes em ambas as populações159.
Das diversas drogas testadas para cardioproteção quando associadas ao tratamento com antracíclicos, apenas o dexrazoxane mostrou-se eficaz em estudos randomizados e com comprovada relação custo-efetividade. Este quelante de ferro inibe a formação do complexo ferro-antraciclina intracelular responsável pela geração dos radicais superóxidos envolvidos na lesão por estresse oxidativo. Achados consistentes do efeito cardioprotetor em crianças foram descritos por Wexler em 1996 com uma incidência de cardiotoxicidade subclínica de 67% no grupo placebo contra 22% no grupo tratado com dexrazoxane163. Lipshultz, em 2004, demonstrou em pacientes com LLA de alto risco, randomizados para receber dexrazoxane associado ou não com doxorrubicina na proporção de 10:1, 30 minutos antes da quimioterapia, que após 6 a 8 meses do início do protocolo quase 50% dos pacientes no grupo controle contra menos de 10% no grupo com dexrazoxane apresentavam elevação de troponina168,169. Durante o acompanhamento de 4 anos desta amostra, observou-se uma menor queda da fração de encurtamento, menor perda da massa ventricular esquerda e da espessura miocárdica do ventrículo esquerdo no grupo tratado com dexrazoxane. Tais achados foram significativos na população do sexo feminino e sem diferença no masculino169. A hipótese de interferência no resultado do tratamento oncológico assim como o aumento na incidência de segunda neoplasia restringe o uso mais frequente do dexrazoxane. Entretanto, em nenhum estudo realizado na população pediátrica foi demonstrada interferência na resposta tumoral quando associado tratamento com dexrazoxane e em apenas um estudo, com desenho reconhecidamente rebatido pelas evidências de grandes centros, em pacientes com doença de Hodgkin, aventou-se aumento na incidência de segunda neoplasia167,168. Em outros estudos, tal achado não foi reproduzido, sendo que no acompanhamento de mais de 8 anos de pacientes com LLA, a sobrevida livre de eventos foi semelhante entre os grupos com e sem dexrazoxane e sem aumento do risco de segunda neoplasia165-171.
Em recente revisão161, 10 reconhecidos estudos randomizados foram citados empregando o dexrazoxane versus placebo, além de trabalhos retrospectivos utilizando a ecocardiografia convencional e sob stress farmacológico172 como métodos de identificação de disfunção ventricular160. Dentre eles, duas metanálises na população pediátrica. Tais estudos demonstraram benefícios estatisticamente favoráveis quanto ao emprego deste cardioprotetor no que se refere à prevenção de insuficiência cardíaca, nenhuma evidência em termos de interferência na resposta terapêutica oncológica, sobrevida dos pacientes ou ocorrência de segunda neoplasia, quando comparados aos grupos controle51,161,164, 171.
Assim, sempre que possível, recomenda-se tentar restringir a dose acumulada de doxorrubicina ao máximo de 300mg/m2.
Diante de vários estudos relacionados à cardioproteção no paciente com câncer tratado com antraciclinas, inclusive na população pediátrica159-173, em que o risco de lesão cardíaca é alto, e que alterações nos parâmetros cardiovasculares clínicos e/ou funcionais precisam ser precocemente identificados para atuação em tempo hábil, independentemente do estágio terapêutico, recomendamos a associação do dexrazoxane, preferencialmente desde o início da terapia, na proporção de 10:1, 30 minutos antes da infusão do antracíclico. Considerando-se que não há dose totalmente segura de antracíclicos, a cardioproteção deverá ser avaliada individualmente, mesmo em protocolos terapêuticos com baixa dosagem cumulativa (CR:II A; NE: A).
10. Endocrinopatias e o coração no tratamento do câncer infanto-juvenil
10.1. Efeitos endócrinos do tratamento do câncer na infância
Nos últimos 20 anos, com os avanços no tratamento de crianças e adolescentes com câncer, as taxas de sobrevida aumentaram satisfatoriamente e muitos desses pacientes tornaram-se adultos, com risco potencial para desenvolver precocemente doenças na vida adulta174. Mais recentemente, entende-se que os efeitos endócrinos do tratamento do câncer dependem de uma interação entre diversos fatores: doença per si, fatores inerentes ao hospedeiro (sexo e genética), versus a terapia, cirurgia, quimioterapia (QT) ou radioterapia (RT). Particularmente, o atraso de crescimento, a obesidade e a síndrome metabólica (SM) configuram as complicações mais comuns após o tratamento para o câncer175-177.
10.2. Deficiência de hormônio do crescimento, crescimento linear e metabolismo
A RT cranial é a grande causa de diminuição da estatura adulta nesse grupo de pacientes, resultando em deficiência do hormônio do crescimento (GH), frequentemente permanente, sendo dose e tempo-dependente178. Além do crescimento linear, o GH também está implicado na regulação do metabolismo. A deficiência de GH induz geralmente distúrbios que lembram requerimentos da SM178.O aumento da espessura íntima-média (EIM), um marcador intermediário para doença cardiovascular (DCV), tem sido descrito nas artérias carótida comum de crianças não tratadas e adultos com deficiência de GH, sendo inversamente correlacionada com os níveis de fator de crescimento insulina-like tipo 1 (IGF-1), que por sua vez reflete o estado de secreção de GH179,180. Em relação aos pacientes oncológicos, sobreviventes de LLA não demonstraram aumento da EIM e nem uma relação entre ela e a dose de RT cranial181. Por outro lado, pacientes adultos tratados por tumores cerebrais na infância que receberam altas doses de RT cranial (>45Gy), apresentaram aumento da EIM no bulbo carotídeo181. Em estudo recente, adolescentes e adultos jovens tratados por meduloblastoma com RT cranioespinhal >54Gy, portanto mais jovens e com menos tempo fora de terapia, não apresentaram aumento da EIM, nem associação com o estado de secreção de GH180.
10.3. Adiposidade e síndrome metabólica
A obesidade é uma complicação endócrina bem reconhecida, considerada tanto um efeito precoce quanto tardio do tratamento do câncer na infância, e relacionada a outras desordens endócrino-metabólicas, associada ao aumento da morbimortalidade por DCV176. Alguns tumores são importantes no que se refere a adiposidade e alterações metabólicas, sejam eles a LLA e os tumores cerebrais, especialmente os craniofaringiomas e os submetidos a altas doses de RT cranial. Entretanto, outros tipos de tumores pediátricos também têm sido associados à ocorrência de obesidade (especialmente a obesidade visceral), bem como a outras características da SM, sejam elas aumento de triglicérides, diminuição da lipoproteína de alta densidade (HDL) colesterol, hipertensão arterial e hiperglicemia/resistência à insulina (RI). Esse tumores incluem: sarcomas, linfomas, câncer de testículo disseminado, neuroblastomas, tumor de Wilms, e transplante de medula óssea (TMO), especialmente os submetidos à irradiação de corpo total (TBI)176-182.De acordo com a recomendação da Associação de Cardiologia Americana, em colaboração com o Conselho para Doença Cardiovascular no Jovem, os pacientes tratados por câncer na infância são classificados como classe III, o que significa aumento do risco para DCV após os 30 anos de idade, o que tem por base evidências epidemiológicas179,181,182.
Diversos mecanismos têm sido assinalados como causa de ganho de peso e fatores de risco para SM nesse grupo de pacientes, tais como o efeito direto da QT e da RT no sistema nervoso central (SNC), resultando em modificações na sensibilidade à insulina e deficiências hormonais (deficiência de GH) e na regulação do apetite, alterações no metabolismo lipídico, insensibilidade à leptina, menor gasto energético (causado pela inatividade física), problemas psicossociais, alterações em sistemas não hormonais (metabolismo de magnésio), disfunção endotelial, do tecido adiposo e hiperhomocistinemia176,177 (Quadros 8 e 9).
Por outro lado, trabalhos recentes não encontraram obesidade nos sobreviventes de LLA, apesar do emprego da RT e independentemente das suas doses, sugerindo que outros fatores (dentre eles, uma característica genética individual), além da RT cranial e do dimorfismo sexual, interagindo em conjunto com a doença e a terapia, possam modular o ganho de peso (e alterações metabólicas) nesses indivíduos176.
10.4. Hipotireoidismo
A disfunção da tireoide é um importante efeito tardio da terapia do câncer, especialmente após RT cervical (linfomas ou tumores cervicais), RT cranioespinhal (meduloblastomas) ou TBI (total body irradiation)175. O hipotireoidismo afeta o sistema cardiovascular, seja através da influência sobre o coração ou dos efeitos adversos sobre os lipídios séricos, aumentando o risco de desenvolvimento de DCV. O hipotireoidismo subclínico, um estado com níveis normais de tiroxina (T4), mas aumento do hormônio estimulante da tireoide (TSH) em concentrações acima de 5mUI/L, em indivíduos assintomáticos, está comumente presente em sobreviventes de câncer submetidos à RT cervical. Entretanto, esta condição não foi associada a maior risco para DCV na população pediátrica179.
10.5. Hipogonadismo
No geral, a deficiência de hormônio sexual, em ambos os sexos, está relacionada ao risco de desenvolver características de SM. Pode ocorrer como consequência de gonadectomia, dano direto da RT nas gônadas e/ou QT compreendendo drogas alquilantes ou compostos de platina. Até agora, os estrogênios e a testosterona são conhecidos por influenciar a composição corporal, metabolismo lipídico, tônus vascular e a pressão arterial181. Nas gônadas masculinas, a produção de testosterona pelas células de Leydig é relativamente resistente a danos, mas a função reprodutiva pode ser prejudicada após RT ou QT alquilante. Por outro lado, nas mulheres, a RT e o tratamento citotóxico pode (parcial ou definitivamente) afetar tanto a função reprodutiva quanto a produção hormonal, resultando em falência ovariana prematura (FOP), com amenorreia ou menstruação irregular. No sexo feminino, a QT parece ser mais destrutiva para os ovários durante a puberdade, quando comparada com a mesma terapia durante a infância182.
10.6. Intervenções para redução do risco cardiovascular
As recomendações para evitar a SM e a aterosclerose precoce em sobreviventes de câncer são a reposição hormonal e a prevenção primária (ou secundária) da disfunção endotelial. A prevenção primária compreende a prevenção de deficiências hormonais e/ou lesão endotelial direta com medidas, tais como: cirurgias mais limitadas, redução da dose da QT, evitar QT gonadotóxica, além da administração de medicamentos alternativos. A prevenção secundária abrange a reposição das deficiências hormonais, o tratamento da disfunção endotelial relacionada com a terapia (RI, dislipidemia, suplementação de Mg+2) e, finalmente, a triagem para SM, além do tratamento específico da condição alterada183,184.
11. Nefropatias e o coração no tratamento do câncer infanto-juvenil
A associação de câncer com cardiopatia e nefropatia é relativamente comum.
A interação fisiológica entre rins e coração é complexa e não muito bem compreendida, embora seja bem conhecido que doenças em um dos sistemas frequentemente leva a complicações no outro185.
Em pacientes adultos com insuficiência cardíaca (IC) existe uma alta probabilidade de desenvolvimento de insuficiência renal (IR) durante a internação, de forma aguda ou crônica, levando à piora de prognóstico. Esses pacientes apresentam maior tempo de hospitalização e maior mortalidade intra-hospitalar186.
Em crianças, entretanto, esta relação não está bem definida na literatura, com poucos estudos demonstrando achados de lesão renal e relação com mortalidade em pacientes internados em unidades de terapia intensiva (UTIP)187,188.
Estima-se que um terço dos pacientes com câncer apresente insuficiência renal (IR). Destes, mesmo com pequenos incrementos no valor da creatinina sérica (>0,3mg/dl), um quinto deles poderá apresentar lesões subclínicas189.
Alguns do agentes rotineiramente utilizados no tratamento do câncer são nefrotóxicos, além de cardiotóxicos, fazendo com que essa relação se apresente nas duas vias188,189.
Os pacientes nefropatas podem ser divididos em três categorias:
1 - Pacientes com nefropatia conhecida, causada pela baixa excreção de agentes antineoplásicos, apresentam um limiar mais sensível, mesmo em doses abaixo das indicadas em seu protocolo;
2 - Pacientes com função renal normal, mas que por causa da nefrotoxicidade da quimioterapia desenvolve nefropatia; alguns revertem o quadro.
3 - Pacientes com função renal normal, que permanecem bem (no máximo com leve microalbuminúria ou leve elevação da creatinina sérica);
Dessa forma é fundamental a avaliação anatômica e funcional renal previamente ao início do protocolo terapêutico como forma comparativa da evolução durante todo o processo do tratamento. Alterações basais iniciais deixam esses pacientes mais susceptíveis a lesões adicionais.
Fatores adicionais importantes no estabelecimento das nefropatias:
Mudança no volume corporal;
Uso de contrastes venosos;
Uso de anti-inflamatórios não hormonais;
Infecções;
Uso de antibióticos (oxacilina, vancomicina, aminoglicosídeos);
Cardiopatia prévia;
Hipertensão arterial sistêmica;
Diabetes mellitus.
Quando as alterações cardiorenais ocorrem, um alerta quanto a mudanças no esquema quimioterápico deverá ocorrer e a diálise deverá ser considerada.
A sobrecarga volumétrica aumenta a pré-carga com consequências na função miocárdica. As alterações no metabolismo do potássio (hipo ou hiperpotassemia) poderão ocasionar arritmias fatais. A acidose metabólica interfere na contratilidade miocárdica.
Uma vez que a doença renal encontre-se estabelecida, danos permanentes poderão já estar presentes. Os néfrons restantes assumem a função e são progressivamente sobrecarregados. Com as necessidades corporais diárias mais a permanência dos agravantes, ocorre queda no número de néfrons, acelerando o processo de deterioração.
Sinais de doença renal crônica em instalação:
Alteração na velocidade na filtração glomerular (não obrigatória);
Alteração no nível de creatinina (associada aos outros sinais);
Diminuição do tamanho renal;
Afinamento da córtex renal com aumento da ecogenicidade;
Proteinúria.
11.1. Agentes e situações comumente relacionadas à interação nefrocardíaca:
11.1.1. Metotrexato: nefropatia, hepatopatia, derrame pericárdico.
11.1.2. Ifosfamida: tubulopatia proximal aguda e reversível: síndrome de Fanconi. Tubulopatia proximal crônica, comum em crianças (até 90%). Tubulopatia distal é mais rara, dependente da dose cumulativa ou quando associada à cisplatina. Disfunção miocárdica severa (rara, dependente da dose cumulativa). Mesna (2-mercaptoetano sulfonato): neurotoxicidade, cistite hemorrágica.
11.1.3. Cisplatina: nefrotoxicidade; porém, quando há incorporação desta dentro de complexo molecular contendo carbono (carboplatina), o risco diminui. Disfunção miocárdica. Insuficiência cardíaca por síndrome de secreção inapropriada do hormônio antidiurético. Ototoxicidade que poderá ser exacerbada quando houver associação com furosemida. Arritmias cardíacas provocadas pela expoliação de eletrólitos (magnésio, potássio e cálcio).
11.1.4. Interferon: glomerulonefrite; cardiotoxicidade, hipertensão arterial sistêmica.
11.1.5. Síndrome hemolítico-urêmica: anemia hemolítica microangiopática associada à insuficiência renal.
11.1.6. Síndrome de lise tumoral: fragmentação rápida de grande parte tumoral induzida pela quimioterapia, com elevação sérica de ácido úrico, fósforo, potássio e desidrogenase láctica, levando à oligúria; pode ser evitada pela hidratação e pela alcalinização da urina (alopurinol).
11.1.7. Síndrome de secreção inapropriada do hormônio antidiurético: hiponatremia severa com hipervolemia; leva à insuficiência renal e insuficiência cardíaca. Pode ser ocasionada por cisplatina, ciclofosfamida, melfalano, vincristina.
11.1.8. Sobrecarga volumétrica: insuficiência cardíaca, hiponatremia relativa.
11.1.9. Anemia: acentua a deterioração cardiorrenal.
11.1.10. Hipovolemia: provocada por perdas tais como vômitos, diarreia, sudorese excessiva e aumento de perdas insensíveis (febre, perda para o terceiro espaço, ingesta inadequada) levam ao aumento da ureia nitrogenada e da creatinina, e queda da filtração glomerular, taquicardia e alterações na pressão arterial.
11.2. Síndrome cardiorrenal
A definição da síndrome cardiorrenal (SCR) constituiu um desafio no meio médico pela sua etiologia multifatorial e possibilidade de os sintomas clínicos poderem ser desencadeados por falência de um ou outro órgão.
11.2.1. Classificação
Assim, em 2008, Ronco e cols.189 propuseram uma classificação para essa condição, amplamente utilizada nos dias atuais (Tabela 15).
11.2.1.1. Síndrome Cardiorrenal tipo 1 (SCR aguda) - caracterizada por piora aguda da função cardíaca, levando à lesão renal aguda (LRA). Tipo mais comum e geralmente de fácil reconhecimento. É estimado que metade das crianças com IC descompensada evoluirão com piora da função renal durante a internação hospitalar187. Causas: choque cardiogênico, descompensação aguda de IC, insuficiência cardíaca direita.
11.2.1.2. Síndrome Cardiorrenal tipo 2 (SCR crônica) - neste tipo, a IC crônica leva à doença renal crônica progressiva. Cerca de 25% dos pacientes com IC crônica possuem uma taxa de filtração glomerular (TFG) menor que 44ml/min188, sendo esta queda fator independente associado a maior mortalidade189.
11.2.1.3. Síndrome Cardiorrenal tipo 3 (Síndrome renocardíaca aguda) - no tipo 3 a LRA (induzida por glomerulonefrite aguda ou necrose tubular aguda, por exemplo) leva à disfunção cardíaca aguda, como piora da IC ou arritmia.
Causas: síndrome hemolítico-urêmica, síndrome da lise tumoral, cirurgia cardíaca, isquemia renal aguda, nefrotoxicidade por fármacos, sepse185.
11.2.1.4. Síndrome Cardiorrenal tipo 4 (Síndrome renocardíaca crônica) - aqui a insuficiência renal crônica (IRC) leva à piora na função miocárdica, hipertrofia ventricular ou a um aumento no risco de eventos isquêmicos. Em crianças, as glomerulonefrites ou displasias/hipoplasias renais congênitas são as causas mais comuns de IRC.
11.2.1.5.Síndrome Cardiorrenal tipo 5 (SCR secundária) - se manifesta por combinação de IC e IR cujas causas sejam doenças sistêmicas. É a forma mais rara e está associada, em adultos, com sarcoidose, diabetes ou amiloidose; já em crianças, relaciona-se com síndrome da resposta inflamatória sistêmica (SRIS), tumores sólidos/hematológicos e lúpus eritematoso sistêmico (LES).
11.2.2 Fisiopatologia da SCR
A insuficiência renal que ocorre em pacientes portadores de insuficiência cardíaca é geralmente atribuída ao chamado "estado pré-renal": baixo débito cardíaco que leva à má perfusão renal. Tal explicação simplifica muito a complexa interação entre esses dois órgãos e não elucida as ativações neuro-hormonais e os elementos vasorreativos encontrados na IC descompensada190.
Na SCR tipo 1, a piora na função cardíaca leva à LRA e à disfunção renal. A baixa pressão de enchimento arterial leva à redução na ativação dos baroceptores no ventrículo esquerdo, seio carotídeo e nas arteríolas renais aferentes. Sinais enviados pelo sistema nervoso central (SNC), então, ativam as vias simpáticas eferentes, levando a um up regulation do sistema neuro-hormonal. Ativação do sistema nervoso simpático da vasculatura periférica e das artérias renais, além de ativação do sistema renina-angiotensina-aldosterona e da arginina-vasopressina servem como mecanismos adaptativos para restaurar a pressão sanguínea e o volume intravascular. Simultaneamente, vasoconstrição e redução na excreção de sódio são contrarregulados por vasodilatadores endógenos, como óxido nítrico, bradicininas e peptídios natriuréticos. Ao longo do tempo, entretanto, esses mecanismos regulatórios se perpetuam, levando a aumento na resistência vascular periférica, sobrecarga volumétrica e redução da função renal191.
O uso de diuréticos de alça, terapia de primeira linha no tratamento destes doentes com IC descompensada, pode também ativar o sistema renina-angiotensina-aldosterona, levando a vasoconstrição sistêmica e retenção fluídica, piorando a azotemia pré-renal192,193.
A esse quadro, somam-se outros fatores que podem levar à LRA durante o tratamento da IC descompensada190:
Vasoconstrição persistente;
Uso de drogas nefrotóxicas (antibióticos, contrastes, anti-inflamatórios);
Estenose de artéria renal;
Hipertensão da veia renal.
Na SCR tipo 2, existe um estado de hipoperfusão renal de longo prazo, estável, secundária à IC crônica. Esta hipoperfusão crônica leva a um estado de resistência vascular renal aumentada que induz, juntamente com os já ativados sistemas neuro-humorais e inflamatórios (pela IC crônica) e a disfunção endotelial mais aterosclerose acelerada (pelos fatores de risco que levaram ao quadro cardíaco), a necrose/apoptose das células renais, com consequente evolução para esclerose glomerular e fibrose194.
Mais comum em pacientes criticamente enfermos, a SRC tipo 3 se caracteriza por LRA primária, levando a sobrecarga de volume (produzindo edema agudo pulmonar), hipercalemia (induzindo arritmias cardíacas), uremia (redução na contratibilidade miocárdica e/ou pericardite) e acidemia (vasoconstrição pulmonar com descompensação do coração direito, indução de arritmias, efeito inotrópico negativo). A própria isquemia renal pode induzir inflamação e apoptose dos miocardiócitos194.
Na SCR do tipo 4, uma doença renal crônica leva à piora da função cardíaca, hipertrofia ventricular, disfunção diastólica e/ou aumento no risco de eventos cardiovasculares. Os mecanismos para chegar a essas alterações variam desde anemia crônica, alterações no balanço cálcio/fósforo, desnutrição, uremia/acidemia crônica, status inflamatório cronicamente ativado, entre outras194.
Finalmente, na SRC tipo 5, doenças sistêmicas, agudas ou crônicas, levam a disfunção cardíaca e renal por ativação neuro-humoral e imunológica, alterações hemodinâmicas, metabólitos tóxicos e uso de drogas para seu tratamento194.
11.3. Lesão Renal Aguda (LRA; SCR tipo 1)
A LRA tem etiologia multifatorial e pode levar a graves repercussões clínicas, manifestando-se desde assintomaticamente até quadros graves de oligoanúria; daí a importância de seu pronto diagnóstico e manejo. Outra importância se deve ao fato de evidências recentes mostrarem que, mesmo aumentos discretos na creatinina sérica (>0,3mg/dl), tanto em adultos como em crianças hospitalizadas, são fatores de risco independentemente de morbimortalidade desses pacientes.
Sua definição é variável: desde aumento no nível de creatinina sérica, passando por redução do débito urinário até necessidade de terapia renal substitutiva, o que leva a imprecisões em relação à sua incidência (1 a 21% dos pacientes pediátricos internados em UTI, dependendo da definição utilizada)190.
Em 2004 criou-se o critério RIFLE para adultos, posteriormente modificado e validado para Pediatria (Tabela 16). Tal classificação utiliza mudanças nos valores de creatinina (ou na TFG) a partir dos níveis basais ou alteração do débito urinário (utilizando-se o pior dos dois critérios), definindo três níveis crescentes de disfunção renal ("R" - risk/risco, "I" - injury/ lesão, "F" - failure/falência) e dois critérios clínicos e evolutivos ("L" - loss/perda e "E" - end/estágio final).
Esse critério se baseia na redução do clearence de creatinina (Clcrea) estimado pela fórmula de Schwartz e no débito urinário em relação ao peso corpóreo185.
Estudos nacionais e internacionais mostram, após a utilização deste critério, uma incidência de LRA variando entre 4,5 a 82% em pacientes internados em UTIP185,186,195, com mortalidade crescente conforme a classificação (R<I<F).
11.3.1. Biomarcadores da LRA184
Um grande estudo multicêntrico196 recentemente mostrou que o início precoce da terapia renal substitutiva em crianças com disfunção de múltiplos órgãos está associado à melhora na sobrevida. Isso faz com que a detecção precoce da LRA tenha implicações importantes no prognóstico final destes pacientes. Assim sendo, muitos biomarcadores têm sido utilizados e alguns recentemente estudados a fim de permitir a detecção precoce da LRA e a avaliação para início da terapia dialítica.
Creatinina - marcador mais utilizado na detecção da LRA, porém não parece ser o melhor para pacientes criticamente enfermos, uma vez que seus níveis séricos são determinados pela massa muscular do paciente e pela oferta diária de proteínas na dieta; ou seja, pacientes amputados ou desnutridos podem demonstrar níveis séricos baixos, enquanto eventos como trauma ou febre podem elevar tais níveis. Além disso, o Clcrea pode se reduzir em 50% antes que se detecte um aumento na creatinina sérica197.
Cistatina C13 - biomarcador urinário que parece ter elevação mais precoce que a creatinina em quadros de LRA, além de ter pouca variação em relação a sexo, idade e raça; aparentemente muito útil em pacientes submetidos à cirurgia cardíaca. Entretanto, seus níveis podem sofrer alterações em pacientes com altos valores de proteína C-reativa, em uso de corticoide, com disfunção tiroidiana ou com diabetes mellitus descompensado. Além disso, seu custo ainda é elevado e não está facilmente disponível no mercado.
Outros marcadores - promissores, mas ainda necessitam maiores estudos para validação:
Molécula de injúria renal 1 (KIM-1)
N-acetil-β-D-glucosaminidase (NAG)
Lipocalina gelatinase associda a neutrófilos (NGAL)
Interleucina 18 urinária (IL-18)
11.3.2. Tratamento
Crianças internadas por IC descompensada costumam desenvolver LRA no curso de 3 a 4 dias do início do tratamento190; assim sendo, tais pacientes devem ser cuidadosamente monitorados para a detecção precoce da piora na função renal. Isso inclui controle de balanço hídrico, pesagens diárias e dosagem sérica diária de ureia e creatinina enquanto houver uso de diuréticos intravenosos. Controle de pressão venosa central (PVC) pode ser útil em alguns casos.
Como não existem protocolos de tratamento graças à complexidade fisiopatológica da síndrome, o manejo deve ser individualizado levando-se em conta a possibilidade de insuficiência renal preexistente pelo uso de medicações nefrotóxicas, infecções ou anormalidades estruturais (estenose de artéria renal, p. ex.).
O ponto principal é otimizar a terapêutica buscando a compensação cardíaca, e os diuréticos de alça são a principal droga para tal. A dose intravenosa pode ser aumentada gradativamente até o máximo permitido para a idade; em caso de baixa resposta, transiciona-se o uso de intermitente para contínuo. Deve-se evitar o instinto de suspender o diurético quando o paciente começa a apresentar aumento dos níveis séricos de creatinina e diminuição no débito urinário, onde parece que o mesmo atingiu um estado normo ou hipovolêmico e doses adicionais da medicação poderiam exacerbar a disfunção renal. Existem evidências que sugerem que, a essa altura, as crianças ainda mantêm um estado de retenção fluídica e que se beneficiariam do uso contínuo de diuréticos198- 200.
A resistência a diuréticos é um problema comum durante o tratamento da SCR, e pode ser clinicamente notada quando há manutenção da congestão pulmonar a despeito das altas doses da medicação utilizada. É mais comum que isso ocorra em pacientes com LRA prévia, causa pela baixa perfusão renal que diminui a chegada da droga nos túbulos: crianças em uso crônico de diuréticos por causa da hipertrofia das células tubulares associado ao aumento na recaptação de sódio pelo bloqueio do transporte de sódio e potássio; pacientes com hipoalbuminemia, pela necessidade dos diuréticos de alça em se ligar a essa proteína para alcançarem os túbulos proximais201,202. Nesses casos, a associação de diuréticos de alça com outra classe de diuréticos pode ser benéfica, como, por exemplo, hidroclorotiazida (alta probabilidade de indução de hipocalemia) ou, mais recentemente, denoldopam (dopa-1 agonista com propriedades natriuréticas e de vasodilatação renal) e nesiritide (peptídio natriurético humano tipo-B recombinante com propriedades de vasodilatação sistêmica, natriurese e diuréticas)185,203,204.
Drogas vasoativas que tendem a fazer vasoconstrição generalizada como dopamina ou adrenalina devem ser reservadas para os quadros de choque cardiogênico ou choque descompensado. O uso de vasodilatadores sistêmicos (nitroprussiato) ou inotrópicos com propriedades vasodilatadoras, como o milrinone, são capazes de reduzir a sobrecarga cardíaca sem comprometer a perfusão renal190.
A diálise peritoneal é uma alternativa para remoção de fluidos em pacientes com IC descompensada que desenvolvem resistência a diuréticos. Em casos ainda mais refratários, deve-se considerar a utilização de hemodiálise com ultrafiltração veno-venosa190.
Os efeitos cardiovasculares sistêmicos associados ao comprometimento renal acarretam em alterações funcionais do ventrículo esquerdo (diastólicas ou sistólicas), hipertensão arterial sistêmica, queda no débito cardíaco, calcificação da vasculatura e perda do restante função renal. O monitorização constante da função renal exerce caráter preventivo das situações subclínicas ou evolutiva das previamente elucidadas205-207.
É essencial que oncologistas, enfermeiros, nefrologistas, cardiologistas e pacientes aprendam a reconhecer os efeitos adversos progressivos da nefropatia subclínica e trabalhem conjuntamente na tentativa de minimizar essa grave sequela.
12. Exames complementares no diagnóstico das cardiopatias decorrentes do tratamento do câncer infanto-juvenil
12.1. Biomarcadores
Existe clara evidência que a lesão miocárdica decorrente do uso das antraciclinas surge bem antes da dose total acumulada necessária para acarretar a queda da fração de ejeção. Desta forma os biomarcadores, capazes de identificar precocemente a lesão miocárdica e predizer a disfunção ventricular, surgem como uma proposta interessante para monitorização dos pacientes em uso de quimioterapia com risco de cardiotoxicidade208.
12.1.1. Troponinas
Utilizadas no diagnóstico e prognóstico de pacientes com síndrome coronariana aguda e mais recentemente no tromboembolismo pulmonar, insuficiência cardíaca, miocardite, sepsis, trauma e uso de drogas cardiotóxicas desde 2000. O mecanismo pelo qual ocorre a liberação da troponina ainda não está completamente elucidado, porém difere do que acontece na isquemia miocárdica tanto pelo grau de elevação quanto pela persistência da mesma (até 30 dias)208. Em recente revisão da literatura, a análise de quase 1.500 pacientes, nos quais foram utilizadas as troponinas I (cTnI) e T(cTnT), sugeriu-se que aproximadamente um terço dos pacientes apresentam valores alterados de troponina, em especial após QT em altas doses. Foram considerados valores de corte entre 0,01 e 0,08µg/l. O padrão indefinido para a elevação da troponina torna necessária a coleta de diversas dosagens nas primeiras 48h a 72h (dosagem precoce) (vide Tabela 17) e após 3 a 4 semanas (dosagem tardia). A elevação precoce é capaz de prever a disfunção ventricular tardia enquanto a persistência da mesma por um mês está associada a maior ocorrência de eventos cardiovasculares graves em um acompanhamento de 3,5 anos. Por outro lado, o valor preditivo negativo da dosagem (-) tanto precoce como tardia é de 99%, indicando um grupo de baixo risco de cardiotoxicidade futura. Outra aplicação é a avaliação precoce de estratégias de cardioproteção. Em estudo recente, pacientes com leucemia linfoblástica aguda (LLA) em uso de antraciclina apresentaram uma liberação de cTnT significativamente menor no grupo que recebeu dexrazoxane208,209.
12.1.2. Peptídeos natriuréticos
O fator natriurético cerebral (BNP) e o fragmento aminoterminal de seu precursor (NT-pró-BNP) são produzidos pelos ventrículos e em menor parte pelos átrios, em resposta à sobrecarga de pressão, volume e aumento da tensão parietal. Inicialmente úteis no diagnóstico, hoje são reconhecidos também na avaliação prognóstica em especial de pacientes com insuficiência cardíaca210. A dosagem dos peptídeos natriuréticos parece colaborar mais na identificação precoce da disfunção ventricular subclínica, sugerindo para este grupo a necessidade de um acompanhamento mais próximo e medidas de cardioproteção210. Lipshultz et cols. demonstraram em recente publicação na população pediátrica tratada por leucemia linfoblática aguda que a dosagem e monitoramento regular dos biomarcadores TnT e NT-Pro-BNP foram considerados elementos úteis na investigação de cardiotoxicidade aguda subclínica210-212.
Em virtude do número pequeno de pacientes estudados, de problemas na metodologia, observamos uma grande variabilidade nos resultados. Em recente revisão da literatura, a utilização dos mesmos na população pediátrica para monitorização de cardiotoxicidade induzida por antraciclina ainda encontra se restrita aos protocolos (Tabela 17).
12.2. Métodos de imagem
Os métodos de imagem não invasivos apresentam utilidade tanto no diagnóstico como no acompanhamento dos pacientes com neoplasia. Em relação à avaliação cardíaca, além dos tumores primários e metástases acometendo o coração, temos a possibilidade de avaliar as complicações que se seguem ao tratamento, especialmente na avaliação das complicações cardíacas de longo prazo nos indivíduos que sobrevivem ao câncer. Sabemos que a chance de desenvolver insuficiência cardíaca, infarto do miocárdio, doença pericárdica e doença valvar encontra-se aumentada nestes indivíduos213. Ainda assim, não é claro se diretrizes para o monitoramento cardíaco nestes indivíduos melhoram a evolução e se as mesmas são custo-efetivas, sendo fato que a maioria dos sobreviventes de neoplasias na infância não recebe acompanhamento médico direcionado para estas doenças15,214.
12.2.1. Radiografia do tórax (RX)
A radiografia do tórax permanece muito utilizada no acompanhamento de diversas condições clínicas. Isto ocorre por sua ampla disponibilidade, baixo custo e capacidade de fornecer informações a respeito dos pulmões, dos vasos pulmonares e, em menor grau, do coração. Além disso, é amplamente utilizada no controle pós-passagem de drenos, tubos e catéteres, frequentemente utilizados ao longo do tratamento neoplásico.
Uma das possíveis complicações cardíacas relacionada ao tratamento quimioterápico é a insuficiência cardíaca215 e, neste contexto, embora forneça informações limitadas quanto à avaliação do miocárdio e da função cardíaca, a radiografia de tórax pode ser útil no acompanhamento da área cardíaca e na avaliação dos sinais de congestão pulmonar, no entanto não devendo ser utilizada como único método de avaliação para a realização deste tipo de diagnóstico. Da mesma forma, derrames pericárdicos podem ser suspeitados na radiografia e confirmados posteriormente por outro método de imagem216.
A radiografia do tórax apresenta baixa sensibilidade para a detecção de tromboembolismo pulmonar, no entanto, alguns sinais clássicos devem ser conhecidos, pois quando presentes podem sugerir este diagnóstico. São eles a proeminência da artéria pulmonar (sinal de Fleishner), a hipertransparência pulmonar (sinal de Westermark) e a consolidação pulmonar periférica denotando infarto pulmonar (sinal de Hampton)217.
12.2.2. Eletrocardiografia
O eletrocardiograma (ECG) é uma representação gráfica da atividade elétrica do coração. Desde o início do século XX esse exame complementar não invasivo, de baixo custo econômico e simples execução tem sido utilizado como complemento importante no diagnóstico de uma grande variedade de situações clínicas como arritmias cardíacas, bloqueios de ramos e hemibloqueios, isquemia miocárdica e necrose, sobrecarga de câmaras cardíacas, cardiopatias congênitas, valvopatias, miocardiopatias, miopericardites, distúrbios eletrolíticos e ação de drogas sobre o miocárdio218,219.
Entretanto, seus achados deverão ser sempre analisados à luz da clínica.
As alterações eletrocardiográficas dependerão da etiologia e do grau do comprometimento cardíaco. Além do mais, a interpretação do ECG na infância depende de conhecimentos em eletrocardiografia pediátrica, uma vez que a idade representa o principal fator de variação do padrão de normalidade. Outros fatores fisiológicos que podem alterar os parâmetros de normalidade do ECG são os ciclos respiratórios, o tônus simpático-vagal, peso, altura, circunferência e espessura torácica, além da variabilidade individual218.
O ECG é um dos exames complementares fundamentais para avaliação e monitoração cardiológica de pacientes oncológicos, pois o tratamento quimioterápico e radioterápico tem efeito tóxico e causa frequentemente lesão miocárdica inflamatória e necrótica, podendo desencadear dilatação e disfunção ventricular esquerda com consequente insuficiência cardíaca congestiva, além de arritmias. Os primeiros sinais de comprometimento cardíaco poderão ser detectados no ECG antes mesmo de qualquer alteração anátomo-funcional visível no ecocardiograma graças às alterações elétricas que ocorrem ao nível celular em consequência ao processo inflamatório inicial possuindo, portanto, elevada sensibilidade na detecção de lesão subclínica. O comprometimento miocárdico poderá se manifestar de forma aguda ou subaguda levando ao aparecimento de alterações eletrocardiográficas durante o tratamento ou até mesmo um ano após mesmo9. Em médio e longo prazo, áreas de fibrose cicatricial resultantes de lesão miocárdica residual funcionarão como focos arritmogênicos e de bloqueios da condução do impulso elétrico218. Assim sendo, todos os pacientes submetidos ao tratamento quimioterápico deverão realizar ECG antes, durante e após o tratamento como complemento do exame cardiológico clínico.
Durante o tratamento, eletrocardiogramas sequenciais deverão ser realizados com intervalos de tempo variados dependendo do perfil do paciente, tipo e dose cumulativa do quimioterápico, e tempo de tratamento. Os efeitos tóxicos agudos são os mais temidos por causa dos riscos de arritmias graves e letais. A cardiotoxicidade das antraciclinas, os principais quimioterápicos utilizados na prática clínica, é acumulativa e tem-se observado disfunção ventricular mesmo em dose abaixo de 300mg/m2. Além do mais, a toxicidade das antraciclinas aumenta com a associação de outros quimioterápicos e com a radioterapia, e com os distúrbios eletrolíticos de ocorrência comum durante o tratamento, reforçando a necessidade de monitorização desses pacientes218,219.
Após a alta hospitalar, os pacientes submetidos ao tratamento oncológico deverão ser acompanhados ambulatorialmente por cardiologistas pediátricos para monitorização a médio e longo prazo, pois o tratamento quimioterápico, particularmente com as antraciclinas, pode levar ao aparecimento tardio de cardiomiopatia, arritmias, além de aumentar de forma significante o risco de eventos cardiovasculares futuros.
12.2.2.1. Alterações eletrocardiográficas por cardiotoxicidade
As alterações eletrocardiográficas por cardiotoxicidade podem ser das mais variadas. Inicialmente pode ocorrer taquicardia sinusal e distúrbios do ritmo. Arritmias graves como taquicardia ventricular podem ser sinalizadoras de toxicidade intensa devendo-se proceder a interrupção da droga. Bloqueios de ramo direito e esquerdo e hemibloqueios, além de sobrecarga de câmaras cardíacas, dependem do grau de comprometimento miocárdico e tempo de tratamento. Complexos QRS de baixa voltagem podem ser indicadores da presença de derrame pericárdico ou miocardiopatia dilatada. A presença de ondas Q em derivações onde elas não deveriam estar presentes, geralmente indicam zonas de fibrose miocárdica. As miopericardites manifestam-se pelas alterações da repolarização ventricular, visíveis sobre o segmento ST e a onda T, sendo as principais alterações os supradesnivelamentos do segmento ST, indicadoras de processo inflamatório miocárdico agudo e subagudo, um dos sinais mais precoces de lesão celular. Geralmente é de manifestação difusa, ou seja, aparece na maioria das derivações. Em seguida, ocorre a inversão da polaridade da onda T. O intervalo QTc é uma das variáveis mais importantes no acompanhamento dos pacientes em tratamento quimioterápico, uma vez que certas drogas podem levar ao prolongamento desse intervalo favorecendo o aparecimento de arritmias graves e letais como Torsades de Pointes. As seguintes alterações eletrocardiográficas deverão ser motivo de monitorização frequente, reavaliação das drogas utilizadas no tratamento e investigação mais acurada do caso218,219:
1 - Frequência cardíaca: taquicardia sinusal, bradicardia sinusal
2 - Ritmo: extrassístoles supraventriculares e ventriculares
3 - Onda P: sobrecarga de câmaras atriais
4 - Intervalo PR: bloqueios atrioventriculares de 1º, 2º e 3º grau
5 - Complexo QRS: sobrecarga de câmaras ventriculares, bloqueios de ramo e hemibloqueios; complexos de baixa voltagem
6 - Segmento ST: retificado, supradesnivelado e infradesnivelado
7 - Onda T: achatada, pontiaguda, negativa
8 - Intervalo QTc: prolongamento acima de 450ms ou aumento do QTc >60ms em relação ao ECG basal
12.2.2.2. Metodologia: O eletrocardiograma verifica, através do registro gráfico (traçado eletrocardiográfico), os fenômenos elétricos para comandos nas devidas fases dos ciclos cardíacos. A realização deste exame é baseada no posicionamento preciso de eletrodos nas extremidades e superfície torácica do corpo (vide também Sessão 18.1).
Alguns fatores podem interferir na qualidade do resultado do ECG:
Limpeza inadequada da pele;
Adesão inadequada dos eletrodos;
Posicionamento incorreto dos eletrodos;
Conexão incorreta dos cabos (inversão);
Contato com metais (maca, relógio, pulseira, colar);
Interferência por aparelhos eletrônicos (monitores, respiradores);
Choro, agitação, ansiedade, movimentos respiratórios intensos;
Movimentação das extremidades.
O ECG é normalmente registrado em 12 derivações, sendo seis no plano frontal (três derivações bipolares dos membros - D1, D2 e D3 - e três unipolares dos membros - AVR, AVL e AVF); e seis no plano horizontal, as unipolares precordiais - V1, V2, V3, V4, V5 e V6. Ao analisar-se o ECG, sugere-se inicialmente verificar a calibração do eletrocardiógrafo que deverá ser de 1 milivolt (10mm na vertical) e velocidade de 25mm/segundo. Os registros devem ser feitos em papel milimetrado correspondendo a 1mm na vertical e 0,04seg na linha horizontal. Em seguida, avalia-se as seguintes variáveis: ritmo, frequência cardíaca (FC), onda P, intervalo PR, complexo QRS, segmento ST, onda T, intervalo QT corrigido para FC (QTc) segundo a fórmula de Bazzet e análise da onda U. O intervalo QTc é medido preferencialmente na derivação D2 e V5, mas poderá ser analisado em outras derivações caso esse intervalo não esteja bem visualizado nessas derivações. Recomenda-se a utilização de tabelas com valores de normalidade para análise dessas variáveis na população pediátrica220,221.
12.2.3. Ecocardiografia
A ecocardiografia transtorácica (ETT) é extremamente útil na avaliação de pacientes que serão submetidos a tratamento quimioterápico, radioterápico ou a complementações terapêuticas (transplante de medula óssea, cirurgias). Ao fornecer dados sobre a anatomia cardíaca, parâmetros de função diastólica e sistólica e estimativas hemodinâmicas, possibilita tanto a avaliação do diagnóstico etiológico da situação cardiovascular do momento, quanto dados prognósticos e acompanhamento da resposta terapêutica cardiológica222-224.
Deve ser realizada como parte da avaliação anatômica e funcional inicial do processo de diagnóstico e estadiamento oncológico, antes que o paciente seja submetido aos procedimentos quimio ou radioterápicos, sabidamente ou potencialmente cardiotóxicos, identificando precocemente alterações cardíacas estruturais (anomalias congênitas) ou funcionais pregressas, subclínicas ou manifestas, interferindo, inclusive, na escolha e condução do protocolo ideal222.
Os achados ecocardiográficos habitualmente utilizados e relacionados aos efeitos cardiovasculares do tratamento oncológico são:
1 - Anatômicos: dilatação das cavidades cardíacas, redução da espessura miocárdica e do índice de massa ventricular; alterações funcionais das valvas cardíacas; espessamento e/ou derrame pericárdico;
2 - Função diastólica: disfunção diastólica leve ou alteração de relaxamento (grau I) em 50% dos casos; disfunção diastólica moderada ou fluxo pseudonormal (grau II); e disfunção diastólica importante ou fluxo restritivo (grau III);
3 - Função sistólica: disfunção sistólica com queda na fração de ejeção global (método de Simpson ou método de Teichholz (valor de referência >55%), e fração de encurtamento (valor de referência >28%); alterações na contratilidade segmentar222;
4 - Alterações nas pressões venocapilar e arterial pulmonar.
Recentemente, tem-se questionado o valor da fração de ejeção global no acompanhamento do uso de drogas cardiotóxicas, uma vez que a identificação da lesão miocárdica significativa por vezes acaba ocorrendo de forma segmentar progressiva, subclínica e tardiamente, limitando a sensibilidade desse método na identificação de lesões incipientes. A incorporação de novos parâmetros tais como o índice de performance miocárdica (IPM), Doppler tecidual e, mais recentemente, avaliação da deformidade miocárdica global e segmentar pelas técnicas de strain, strain rate e speckle tracking, ecocardiografia sob estresse (para o estudo da reserva contrátil) e a ecocardiografia tridimensional (eco 3D) e em tempo real (4D) trazem possibilidades de auxílio na identificação precoce da disfunção miocárdica, possibilitando a antecipação de estratégias de suporte terapêutico cardiológico223-230.
Diretrizes recomendam o seguimento de pacientes, sem disfunção ventricular pré-quimioterapia (fração de ejeção basal >50%), através da avaliação da função sistólica e diastólica do ventrículo esquerdo (VE). Além da avaliação inicial antes da quimioterapia, após metade da dose total acumulada prevista no protocolo de tratamento ou ao atingir 200mg/m2 de doxorrubicina; posteriormente, a cada 100mg/m2 em diante. No caso de pacientes com fração de ejeção basal abaixo de 30%, devemos avaliar risco-benefício em relação ao tratamento proposto, sendo desaconselhado o uso de drogas cardiotóxicas, em especial de antraciclinas. Já nos pacientes com fração de ejeção basal entre 50 e 30%, a avaliação ecocardiográfica deverá ser realizada antes de cada ciclo de quimioterapia9. É de fundamental importância a constante comunicação entre o cardiologista e o oncologista acompanhante, no sentido de discutir os achados, introdução de medidas clínicas cardiológicas preventivas ou terapêuticas, continuidade ou alteração do esquema terapêutico oncológico, individualizando cada caso.
São critérios aceitos e validados para a interrupção do tratamento oncológico vigente, a redução maior que 10% (valor absoluto) em relação à fração de ejeção basal ou reduções menores, porém atingindo uma fração de ejeção inferior a 50%60.
Avaliações ecocardiográficas em intervalos menores dependerão do quadro clínico de cada paciente, considerando sinais de cardiotoxidade aguda ou subaguda, tendo em vista a possibilidade de evolução muitas vezes subclínica da disfunção miocárdica.
Atentar quanto a alguns aspectos que possam interferir na avaliação ecocardiográfica funcional do momento, confundindo com achados de cardiotoxicidade, tais como: anemia, dor, hiper-hidratação, desidratação, estado febril e estado séptico, insuficiência renal, drogas que interfiram nos sistemas simpático ou parassimpático, distúrbios eletrolíticos, arritmias e limitações das janelas transtorácicas.
Nova avaliação deverá ser feita ao término do protocolo terapêutico, e controles subsequentes, individualizados conforme a evolução ecocardiográfica durante todo o tratamento231.
Controles tardios, em indivíduos sem disfunção detectada, devem ser realizados de rotina, após 6 meses a 1 ano e, depois, periodicamente, uma vez que a incidência de insuficiência cardíaca relacionada ao uso de antraciclina, assim como após radioterapia, aumenta com o acompanhamento tardio, podendo surgir depois de 15 anos ou mais232- 234.
Além dos métodos ecocardiográficos anteriormente citados e usados nas fases iniciais do tratamento ou durante o mesmo, salientamos a importância da avaliação dos pacientes que se encontram em fase de acompanhamento após o término do protocolo terapêutico e clinicamente livres de complicações que os limitem fisicamente. Estudos recomendam também a avaliação por meio da associação da ecocardiografia imediatamente após a realização de teste ergométrico ou ergo-expirométrico, que demonstrará a real condição física desse paciente, proporcionando medidas mais seguras para a indicação de atividades físicas, tão importantes na qualidade de vida233,234.
Como o tratamento quimioterápico desses pacientes é realizado, em grande parte, por intermédio de cateteres venosos de longa permanência, totalmente implantados ou semi-implantados, além de outros cateteres de curta duração, devemos estar atentos ao risco de infecção e trombos. A ecocardiografia é de grande ajuda na investigação e detecção de trombos e vegetações nos pacientes com suspeita destes eventos. A ponta do cateter idealmente deve estar localizada na veia cava superior, raramente na veia cava inferior, perto da junção com o átrio direito, para evitar arritmias e a formação de trombos. A investigação de endocardite inclui avaliação do cateter, do seu trajeto venoso, comportamento do fluxo local, cavidades e valvas cardíacas222.
Diante da suspeita de endocardite infecciosa com critérios bem estabelecidos, e estando o ETT aparentemente normal ou não suficientemente claro (sensibilidade de 80% e especificidade de 98% para detecção de vegetações), ou quando as condições clínicas do paciente limitem o adequado acesso através das janelas transtorácicas, deve-se realizar o ecocardiograma transesofágico (ETE), que para o diagnóstico de vegetações valvares apresenta sensibilidade de 97% e especificidade de 91%222.
O pericárdio também poderá ser acometido, seja no início do processo de investigação diagnóstica (derrame) especialmente nos casos de leucemias e linfomas, ou secundário às compressões extrínsecas ao coração por massas mediastinais, ou após a radioterapia (espessamento pericárdico levando à pericardite constritiva). A avaliação ecocardiográfica do comprometimento pericárdico permite determinar o tipo de lesão (efusão, espessamento, massa), localização, dimensão, extensão para estruturas vizinhas, além de informar sobre a presença e gravidade de sinais de restrição diastólica tanto pelo aspecto bidimensional quanto pela análise Dopplerfluxométrica222,223.
12.2.4. Teste ergométrico
Sobreviventes ao câncer na idade pediátrica são particularmente predispostos a apresentar problemas secundários de saúde, principalmente por terem recebido quimioterapia com antraciclinas e/ou radioterapia, expondo-os ao risco de distúrbios pulmonares e instalação de cardiotoxicidade tardia235.
Sabe-se que a incidência de anormalidades cardíacas aumenta com o tempo e mais da metade dos pacientes expostos às antraciclinas desenvolverão anormalidades em 10-20 anos do diagnóstico.
Sendo assim, a capacidade ao exercício poderá estar reduzida. Apesar do risco de cardiotoxicidade estar relacionado à dose cumulativa recebida, geralmente relacionada à dose cumulativa >350-400mg/m2, não há dose segura, existindo variações na resposta individual quanto à sensibilidade de instalação desse problema. Exames em repouso não garantem a ausência de lesões inexpressivas.
Crianças assintomáticas, aparentemente saudáveis, mesmo tendo sido tratadas com doses consideradas baixas a moderadas de antracíclicos, apresentam baixa reserva sistólica funcional evidenciada ao exercício, sugerindo a presença de alterações cardiotóxicas subclínicas236.
Os pacientes sobreviventes ao câncer apresentam tendência ao aumento do peso, aumento do índice de massa corporal e do percentual de gordura corporal, especialmente nos primeiros anos após o término do tratamento. Um dos principais fatores é a queda na atividade física, que, em alguns casos, está diretamente relacionada a razões psicológicas237.
A capacidade ao exercício físico pode ser reduzida também por causa de vários fatores além da cardiotoxicidade: disfunções respiratórias ou músculo-esqueléticas, deficiências endócrinas, fadiga crônica ou neuropatias periféricas237.
Segundo a III Diretriz da Sociedade Brasileira de Cardiologia sobre Teste Ergométrico (TE), esse exame é método hoje universalmente aceito para o diagnóstico de doenças cardiovasculares, sendo também útil na determinação prognóstica na avaliação da resposta terapêutica, da tolerância ao esforço e de sintomas compatíveis com arritmias ao exercício238.
Seu baixo custo no Brasil e alta reprodutibilidade possibilitam sua disseminação por todas as regiões do país, tornando-o instrumento importante na tomada de decisão em várias situações clínicas.
Cumming e cols.239,240 estudaram o desempenho ergométrico de crianças normais e portadoras de cardiopatias através do protocolo de Bruce, reconhecendo que este preenchia os requisitos necessários à avaliação dessa população. O mesmo vem sendo aplicado na prática diária, apesar de alguns autores também demonstrarem a utilidade do teste em rampa ou a combinação dos mesmos, dependendo do perfil do paciente241.
No TE, o indivíduo é submetido a um esforço programado e individualizado com a finalidade de se avaliar as respostas clínica, hemodinâmica, autonômica, eletrocardiográfica, metabólica e, eventualmente, ventilatória ao exercício (teste cardiopulmonar ou ergoexpirométrico - TCP). Esta avaliação permite detectar isquemia miocárdica, reconhecer arritmias cardíacas e distúrbios hemodinâmicos induzidos pelo esforço, avaliar a capacidade funcional e a condição aeróbica, diagnosticar e estabelecer o prognóstico de determinadas doenças cardiovasculares, prescrever exercício, avaliar objetivamente o resultado de intervenções terapêuticas, demonstrar aos pacientes e aos seus familiares as suas reais condições físicas e fornecer dados para a perícia médica.
Pacientes com insuficiência cardíaca podem apresentar capacidade normal ou próxima do normal ao exercício (resposta adaptativa fisiológica global), dependendo de uma série de fatores que induzam a mudanças positivas a nível muscular, vascular e neuro-hormonal (mecanismos compensatórios da anormalidade funcional cardíaca). Disfunções miocárdicas subclínicas poderão ser desmascaradas sob o estresse236.
Desse modo, o TE ou o TCP podem elucidar tais anormalidades, geralmente ausentes ou pouco expressivas em exames de repouso, avaliando a capacidade física com a finalidade de definir sua potencialidade para as atividades diárias de trabalho e lazer.
O VO2 máximo é importante índice de avaliação da capacidade funcional ao exercício. Caso o teste cardiopulmonar inicial seja ineficaz, recomenda-se que, após um período de programa aeróbico de condicionamento físico, novas avaliações sejam realizadas, comparando a evolução do VO2 máximo progressivamente até níveis próximos do ideal a cada caso.
Desse modo, os testes podem guiar o médico em dois sentidos: no diagnóstico da sua condição cardiopulmonar e na prescrição de exercícios. A presença de VO2 máximo normal e todas as outras variáveis do teste cardiopulmonar asseguram que não há anormalidade funcional significativa no paciente. Esses pacientes deverão ser conduzidos a atividades físicas dinâmicas sem limitações específicas. Na maioria das vezes, os achados de complicações clínicas não somente não contraindicam, mas podem responder positivamente através de atividade física regular, mesmo de moderada intensidade236,242.
Pacientes aparentemente saudáveis podem participar de atividades físicas esportivas se apresentarem resposta normal ao teste cardiopulmonar; enquanto aqueles que apresentarem redução do VO2 máximo poderão ser reavaliados após programa aeróbico de condicionamento físico e então progredir para atividades dinâmicas adaptadas às suas limitações235.
Pacientes com insuficiência cardíaca poderão melhorar sua capacidade ao exercício através de um programa de treinamento individualizado e planejado240.
Stevinson e cols.243, em revisão sistemática de 33 estudos controlados objetivando mostrar o efeito do exercício em pacientes pediátricos com câncer, mostraram que a capacidade física melhorou nos indivíduos que se submeteram a treinamento físico. A revisão mostrou ainda que, nos indivíduos submetidos a treinamento, pareceu não haver aumento do sintoma de cansaço e, ainda, poucos efeitos adversos. Porém, com os dados obtidos nesse estudo, não foi possível determinar os efeitos de longo prazo do exercício na recorrência do câncer ou na sobrevida dos pacientes.
Van Brussel e cols.244 também realizaram revisão sistemática da literatura, cujo objetivo era determinar se a capacidade física avaliada pelo VO2 máximo estava diminuída nos pacientes portadores de leucemia linfoblástica aguda (LLA) na infância quando comparados a crianças saudáveis. Dados de 3 dos 17 estudos avaliados mostraram que o VO2 máximo tendia a ser menor nos pacientes que foram portadores de LLA.
A prática de atividades físicas tem sido uma das estratégias recomendadas por muitas das associações de pediatria e cardiologia, com o intuito de promover a saúde cardiovascular na infância. Atividades que desprendam >50-60% da capacidade de esforço máximo deverão ser encorajadas, e crianças com limitações físicas devem ser incluídas em atividades especialmente desenvolvidas a sua habilidade física240.
12.2.5. Tomografia computadorizada (TC)
A tomografia computadorizada do tórax, frequentemente solicitada para o paciente portador de neoplasia por permitir a avaliação de metástases pulmonares e para linfonodos mediastinais, também pode fornecer informações importantes quanto à avaliação do sistema cardiovascular destes indivíduos.
Uma aplicação importante encontra-se relacionada à pesquisa de tromboembolismo pulmonar, uma vez que a incidência de trombose encontra-se aumentada em pacientes com diversos tipos de neoplasias e frequentemente estes pacientes apresentam fatores de risco conhecidos, como cateteres venosos centrais, imobilização, desidratação e tratamento quimioterápico245. A tomografia computadorizada do tórax com a injeção de contraste iodado endovenoso desempenha papel central no diagnóstico de tromboembolismo pulmonar, sendo o exame de escolha para esta pesquisa246.
A tomografia computadorizada do coração também apresenta alta acurácia na exclusão de doença coronariana. Desta forma, explorando o alto valor preditivo negativo deste método, o mesmo pode ser utilizado para avaliação de pacientes com suspeita de doença isquêmica, que é outra complicação relacionada a diferentes formas de tratamento oncológico247.
Afecções do pericárdio também podem ser avaliadas pela tomografia, embora tal avaliação pela ressonância magnética permita diagnóstico mais acurado das afecções do miocárdio, frequentemente associadas.
12.2.6. Ressonância nuclear magnética
A ressonância magnética, por proporcionar alto contraste tecidual, tem a capacidade de discriminar diferentes tecidos, fazendo com que este método seja de grande ajuda na avaliação dos tumores primários do coração, assim como na suspeita de invasão do coração e dos grandes vasos mediastinais por parte de tumores extracardíacos que se encontrem adjacentes.
Além disto, atualmente a ressonância magnética do coração é considerada o padrão áureo para avaliação da função sistólica ventricular. Isso se dá pelo alto grau de resolução das imagens e pela pequena variabilidade de avaliação intra e interobservadores248,249. Desta forma, este tipo de estudo, quando disponível, pode ser considerado no acompanhamento dos pacientes em tratamento oncológico com suspeita para insuficiência cardíaca. É recomendável que se obtenha um primeiro estudo antes do início do tratamento e que o acompanhamento da função cardíaca seja realizado com o mesmo método, dada a variabilidade de resultados já conhecida quando alternamos diferentes tipos de estudo250.
A ressonância magnética também permite a avaliação das afecções do pericárdio e do miocárdio, não tendo limitações relacionadas à janela acústica e nem ao biotipo do paciente, tornando-se uma excelente opção diagnóstica para este tipo de indicação249,250.
Apesar de a tomografia computadorizada ser o método de escolha na suspeita de tromboembolismo pulmonar, para os pacientes com história de alergia ao contraste iodado a ressonância magnética com a injeção de contraste paramagnético (gadolínio) pode ser um método alternativo para esta avaliação, proporcionando a observação dos vasos pulmonares até os seus ramos segmentares251.
12.2.7. Radioisótopos
Pacientes em regime de quimioterapia, sobretudo com antracíclicos, exigem um rigoroso acompanhamento após ou mesmo durante o tratamento. O objetivo deste acompanhamento é a identificação precoce dos primeiros sinais de cardiotoxicidade, a fim de poder modificar o plano terapêutico, visando diminuir os riscos de uma doença cardíaca. Essas modificações da terapia devem ser equilibradas com o risco de queda do efeito antitumoral da terapia252. A medicina nuclear pode contribuir no monitoramento desses possíveis efeitos cardiotóxicos ao longo da vida, especialmente em pacientes que receberam radiação mediastinal em altas doses de antracíclicos.
12.2.7.1. Imagem neural
Entre os métodos convencionais, vários novos agentes têm sido avaliados para predizer a falência cardíaca secundária à cardiotoxicidade induzida pelos antracíclicos. O MIBG-Iodo 123 (metaiodobenzil-guanedina ligado ao iodo 123), um agente usado para imagem neuronal cardíaca, tem sido muito utilizado uma vez que mapeia a função adrenérgica; consequentemente, muito tem contribuído no entendimento da patogênese da cardiotoxicidade induzida pelos antracíclicos, bem como na função adrenérgica anormal que se instala no coração252. O estudo desta inervação poderá mostrar seu envolvimento na regulação da contratilidade e da possível associação entre a hipersensibilidade às catecolaminas e arritmias ventriculares252. O MIBG-iodo 123, um análogo do falso neurotransmissor guanetidina, fixa-se fisiologicamente nos terminais nervosos adrenérgicos, primeiramente na via transportadora de norepinefrina252. Apesar do grande número de publicações na área de insuficiência cardíaca, ainda não há uma padronização da sua indicação. Sua classe de recomendação é a IIa (a evidência é insuficiente, mas já há consenso sobre a utilidade entre experts no Japão e Europa) e seu nível de evidência "C"253.
12.2.7.1.1. Preparo do paciente e dose:
Interação com drogas:
A injeção do MIBG-iodo 123 deve ser feita em repouso e lentamente. A preparação é mínima: medicamentos que potencialmente interferem com a captação das catecolaminas, como antidepressivos, antipsicóticos e alguns bloqueadores do canal de cálcio, devem ser suspensos 24h antes da injeção.
Por causa do risco da presença de iodo livre, a tireoide deve ser bloqueada: recomenda-se o uso do iodeto de potássio (200mg em solução a 10%), de 40 a 300mg/dia, durante três dias254. No Brasil alguns centros têm administrado dose única de iodeto de potássio xarope, na posologia de 5 a 10mg/kg uma hora antes da injeção do radiofármaco.
A dose apropriada do MIBG-Iodo 123 ainda não foi definida. Muitos autores têm preconizado dose pediátrica que varia de 20 a 75MBq255, injetada durante um minuto, a fim de se evitar os efeitos indesejáveis do aumento de catecolaminas circulantes.
12.2.7.1.2. Aquisição de imagens e análise dos dados:
Imagens anteriores de tórax são realizadas 15min e 3,5 a 4h após a injeção endovenosa do MIBG-Iodo 123, com 2 milhões de contagens. Sequencialmente às imagens estáticas tardias são adquiridas as imagens tomográficas (SPECT).
Áreas de interesse (ROI) são desenhadas contornando o coração e no mediastino superior (169 pixels), nas imagens estáticas precoces e tardias. Com este procedimento calcula-se as médias de contagens em cada ROI e, na sequência, calcula-se a relação coração/mediastino e taxa de wash out (Figura 1). A taxa de wash out é assim calculada255:
12.2.7.2. Ventriculografia radioisotópica
A fração de ejeção do ventrículo esquerdo reflete a função ventricular esquerda (FEVE) e é considerado o parâmetro isolado de maior importância na avaliação cardíaca, além de fornecer informações prognósticas aos pacientes256. A ventriculografia radioisotópica (também conhecida como estudo cintilográfico das câmaras cardíacas) é considerada o método padrão-ouro para a aferição da FEVE. Ela permite a análise de vários parâmetros da função ventricular (curva de atividade versus tempo, análise de fase e amplitude), possibilitando uma fina avaliação das regiões de melhor desempenho contrátil (amplitude) e o momento temporal em que esta contração ocorreu (análise de fase), detectando a presença de assincronismo contrátil entre os ventrículos direito e esquerdo e intraventricular esquerdo257. Ao contrário do ecocardiograma, há uma baixa variação de interpretação intraindividual e intraobservador. No entanto, em relação à função diastólica, as informações fornecidas são limitadas258. Sua classe de recomendação na investigação da cardiotoxicidade é IIa e seu nível de evidência B259,260.
12.2.7.2.1. Monitorização
A fim de se minimizar as variáveis que possam confundir a investigação, é recomendado que a ventriculografia radioisotópica seja realizada pelo menos três semanas após a terapia com antraciclina, quando os pacientes estão afebris e com hemoblobina superior a 9g/dL261.
Durante a terapia, um recente estudo (http://www.survivorshipguidelines.org/)221 sugere a seguinte frequência de acompanhamento:
12.2.7.2.2. Técnica e radiofármaco
O paciente é injetado com hemáceas marcadas com 99mTc (pertecnetato de sódio), com atividade na faixa de 0,3mCi/kg (11 a 13 MBq/kg), com dose máxima de 20 a 30mCi/70kg. A dosimetria para pacientes que receberam dose de 20mCi é de 0,3 a 0,52rem. Os métodos de marcação podem ser: in vivo, in vitro ou in vitro modificado (in vitro)263-265.
12.3. Biópsia endomiocárdica
As drogas para tratamento dos tumores malignos na criança são potencialmente cardiotóxicas como a adriamicina, ciclofosfamida, cisplatina, fluorouracil, taxanos, retuximabe etc. A radioterapia, associada ou isolada, pode também produzir efeitos agressivos sobre a musculatura cardíaca, acarretando ou potencializando os efeitos deletérios cardíacos das drogas oncológicas266.
O mecanismo de toxicidade varia, pois algumas drogas interferem/inibem o metabolismo celular, outras bloqueiam ou alteram o transporte celular e outras, ainda, induzem a alterações hemodinâmicas que propiciam a isquemia. A toxicidade das drogas está relacionada a essa patogenia e tem efeito geralmente cumulativo267.
Dentre todas as drogas, como a adriamicina é, potencialmente, a de maior poder cardiotóxico; teceremos comentários relativos a ela, que poderão daí ser generalizados em menor grau, para as outras drogas com menor agressividade sobre o músculo cardíaco.
Tempos atrás o método da biópsia endomiocárdica foi utilizado para monitorizar os efeitos cardiotóxicos da terapêutica com antraciclina.
Considera-se (Quadro 11) a relativa graduação da cardiotoxicidade de 0 a 3,0, tendo como base os achados histopatológicos.
Este quadro representa um sistema gradual para exame de cardiotoxicidade da adriamicina, analisado em 10 ou mais blocos de parafina da biópsia endomiocárdica. Os graus são baseados nas alterações dos miócitos, como determinação da proporção de células acometidas, obtidas no microscópio de luz. Até o grau 2,5 recomendava-se não administrar doses maiores de antraciclina e no grau 3,0 recomendava-se suspender o tratamento.
Enfim, através desses achados norteava-se a dosagem ou mesmo a suspensão da adriamicina do paciente submetido à quimioterapia.
Os efeitos adversos de elevadas doses da ciclofosfamida podem ocorrer secundariamente à destruição do endotélio capilar. Isto leva a depósito de fibrina, edema intersticial, extravasamento sanguíneo e focos de necrose no miocárdio adjacente. Na microscopia eletrônica, quase sempre complementando os achados da microscopia óptica, caracteriza-se estruturalmente por extensa contração de bandas, lise miofibrilar e inclusões mitocondriais eletrodensas. Essas lesões cicatrizam-se por fibrose. A droga pode causar também pericardite fibrinosa.
O comprometimento miocárdico na fase inicial da radioterapia desenvolve-se, basicamente, em três fases: 1) agressão aos pequenos vasos do miocárdio; 2) inflamação aguda das artérias de pequeno e médio calibre, seguida de infiltração de neutrófilos que envolvem todas as camadas do coração e que podem se desenvolver após seis horas de exposição; 3) a fase latente, que se inicia dois dias após a exposição, pode acarretar discreto grau de fibrose, tanto no miocárdio como no pericárdio. Nas fases tardias pode ocorrer isquemia, que acarreta morte celular e fibrose extensa que são características dessa fase, comprometendo tanto a função sistólica como a diastólica do músculo cardíaco.
A radioterapia pode também acarretar comprometimento valvar do coração.
A biópsia endomiocárdica é um método diagnóstico que permite analisar um fragmento do miocárdio in vivo. A técnica atualmente utilizada é por punção percutânea da veia jugular interna direita, com o biótomo de Caves-Schultz, em sala de hemodinâmica. Este é posicionado no ventrículo direito, sob visão fluoroscópica, onde serão obtidos de 4 a 6 amostras do miocárdio fixadas em solução de formalina a 10% e processadas para exame histológico. Os cortes desses fragmentos serão corados pela hematoxilina-eosina. Poderão também ser coletados a fresco para microscopia eletrônica267.
É um método invasivo, não totalmente isento de riscos para a criança com disfunção ventricular, que requer anestesia geral e que permite analisar fragmentos do miocárdio, que não necessariamente expressariam aspectos histológicos de todo músculo cardíaco268.
Atualmente não se utiliza a biópsia endomiocárdica como exame de rotina nos pacientes pediátricos submetidos ao tratamento oncológico.
Nos últimos anos surgiu novo método diagnóstico através do aprimoramento das técnicas da ressonância magnética do coração269 como a cinerressonância, que evidencia morfologia e função, com a imagem pesada T2 que detecta aumento da água tecidual, que está associada a edema e infiltrado inflamatório, bem como o realce tardio com gadolínio que permite inferir a presença de fibrose, bem como da viabilidade celular. Desta forma, é um método não invasivo que permite monitorar e obter informações bastante precisas sobre áreas de inflamação, viabilidade miocárdica e fibrose. Permite monitorar, com elevada acurácia, os efeitos deletérios da adriamicina e de outras drogas utilizadas no tratamento de tumores, bem como a radioterapia, permitindo assim avaliação precoce e tardia das condições cardíacas dos pacientes submetidos à quimioterapia e/ou à radioterapia. Da mesma forma, com o aprimoramento do ecocardiograma com Doppler270,271, passou-se a dispor de métodos não invasivos que permitem avaliar a resposta miocárdica à administração precoce e tardia das medicações cardiotóxicas ou potencialmente cardiotóxicas em crianças portadoras de neoplasias.
Assim, atualmente não se recomenda a biópsia endomiocárdica como exame de rotina na avaliação dessas crianças. No entanto, ela poderá ser utilizada em situações especiais, principalmente quando os achados dos métodos não invasivos, em especial da ressonância nuclear magnética, não forem conclusivos.
13. Avaliação perioperatória da criança oncológica
13.1. Abordagem Inicial
O paciente com câncer é frequentemente submetido a vários procedimentos cirúrgicos que requerem anestesia. Estes procedimentos podem ocorrer no início do tratamento, durante o tratamento, anos após sua remissão, ou mesmo durante o estágio final da doença.
A avaliação pré-operatória da criança com câncer segue a avaliação preconizada para os pacientes de uma maneira geral, enfatizando-se os problemas que possam existir decorrentes do próprio tumor ou de seu tratamento, pois não existe na literatura uma recomendação específica para esses pacientes272.
Ela é de fundamental importância para a elaboração da estratégia anestésica a ser tomada e para a diminuição da morbimortalidade perioperatória.
Devemos levar em consideração o tipo e a gravidade do tumor, assim como eventuais metástases e lembrar dos efeitos da quimio e radioterapia nos diversos orgãos e tecidos do organismo da criança273.
Devemos salientar que, como na criança saudável, não existem dados na literatura que recomendem uma rotina de exames pré-operatórios na criança com câncer274,275. A solicitação dos exames laboratoriais e de imagem deve ser guiada pela história clínica, exame físico do paciente e tipo de cirurgia a ser realizada276.
13.2. Avaliação cardiovascular
Durante a anamnese, devemos buscar fatores que levem ao aumento do risco anestésico cirúrgico tais como: tipo e localização do tumor, principalmente quando se trata de tumores localizados na caixa torácica, sinais e sintomas de insuficiência cardíaca, uso de quimioterápicos e radioterapia.
Os tumores de mediastino podem levar à síndrome da veia cava superior (SVCS), ou síndrome do mediastino superior, com compressão da traqueia. Os sinais e sintomas mais frequentes na criança são: dispneia, tosse, rouquidão, chiado e estridor277,278. Tomografia de tórax e avaliação das curvas e volumes pulmonares ajudam na quantificação do grau de compressão da traqueia, carina e brônquios278. A presença de algum dos sinais e sintomas da Tabela 19 sugere uma avaliação cuidadosa antes do procedimento anestésico277.
As crianças que recebem tratamento quimioterápico potencialmente cardiotóxico fazem um acompanhamento da função cardíaca com ecocardiograma antes, durante e ao final do tratamento. As classes das antraciclinas são as mais cardiotóxicas. O paciente pode apresentar hipotensão, insuficiência cardíaca congestiva e arritmias.
A radioterapia afeta todas as estruturas do coração, podendo levar à pericardite, derrame pleural, fibrose valvular e distúrbios de condução.
Uma avaliação cardíaca no pré-operatório é de suma importância para o preparo e manejo anestésico, levando-se em consideração a diminuição de suas reservas fisiológicas.
13.3. Avaliação respiratória
Na avaliação pré-operatória, devemos procurar sinais e sintomas de comprometimento pulmonar causado pelo próprio tumor ou pelo uso de quimioterápicos e radioterapia. Durante o tratamento do câncer, especialmente nos estados de imunossupressão e de transplante de medula óssea, a criança muitas vezes apresenta insuficiência respiratória. Os testes de função pulmonar são utilizados para quantificar o grau de comprometimento pulmonar279.
A bleomicina é o quimioterápico que mais comumente induz a toxicidade pulmonar, causando pneumonia intersticial, fibrose pulmonar e edema pulmonar não cardiogênico.
A pneumonite por radiação é reportada nos pacientes que receberam radioterapia para tumores de pulmão, linfomas de Hodgkin e não Hodgkin, dentre outros, numa incidência entre 5 e 15%.
A avaliação da via aérea no pré-operatório é mandatória em qualquer paciente. A classificação de Mallampati e a avaliação da distância esterno-mento são parâmetros que podem ser utilizados em crianças maiores. Devemos avaliar também a abertura da boca assim como a mobilidade cervical, que podem estar prejudicadas nos tumores de orofaringe e pescoço. Numa série de crianças que receberam transplante de medula óssea e que necessitaram de ventilação mecânica, 30% apresentaram dificuldade de intubação. Mucosites que levam a sangramento e edema são causas frequentes de dificuldade de manuseio de via aérea279.
13.4. Avaliação da função renal
Os rins podem ser acometidos por tumores primários ou por tumores de origem não renal, sendo o mais comum o neuroblastoma. Linfomas e leucemias também podem infiltrar e obstruir o trato urinário280.
A insuficiência renal aguda (IRA) é, na maioria das vezes, resultado da toxicidade do tratamento. Quase todas as drogas quimioterápicas podem levar à nefrotoxicidade nas crianças. Cisplatina, carboplatina e ifosfamida são os agentes que mais comumente causam comprometimento renal. Porém, a ciclofosfamida em altas doses e o methotrexate podem levar à IRA280.
Os pacientes submetidos ao transplante de medula oósea, apresentam IRA com relativa frequência. Vários trabalhos na literatura reportam uma incidência entre 20 e 45%282,283.
É fundamental no período perioperatório evitar drogas que tenham potencial nefrotóxico (ex.: anti-inflamatórios), evitar hipovolemia, ajustar as drogas de acordo com a função renal, monitorizar a diurese e o equilíbrio hidroeletrolítico.
13.5. Avaliação do sistema hematológico
A mielossupressão e sua manifestação com diversos graus de anemia, neutropenia e trombocitopenia é muito comum nos diversos tipos de câncer nas crianças272. A anemia é a mais comumente encontrada na fase inicial de investigação diagnóstica, podendo atingir 50 a 74% no diagnóstico dos neuroblastomas, rabdomiossarcomas, doença de Hodgkin, sarcoma de Ewing e osteossarcoma, e 80% na leucemia linfoide aguda (LLA)280.
A incidência de complicações hemorrágicas durante o tratamento da criança com câncer é desconhecida. A causa de morte por hemorragia nas crianças em tratamento por LLA e leucemia mieloide aguda é multifatorial277,280.
A fibrinólise e a alteração dos fatores de coagulação podem ocorrer por causa de disfunção hepática, deficiência de vitamina K, infecção e ação de medicamentos281. O tromboembolismo é um evento raro na população infantil, mas a trombofilia e a trombose aguda podem estar presentes nas crianças com câncer, especialmente nos sarcomas e nas doenças hematológicas280.
A administração de plaquetas, plasma fresco ou outros fatores de coagulação depende do exame laboratorial pré-operatório, assim como do tipo de cirurgia a ser realizado. Cada hospital deve ter um protocolo para transfusão nestes pacientes. A tática requer um balanço delicado entre os fatores de coagulação e anticoagulantes. Alguns pacientes, ainda considerados de risco para fenômenos tromboembólicos, são tratados com heparina e warfarina, o que deve ser discutido na avaliação pré-operatória com o hematologista, levando-se em consideração o risco de hemorragia e trombose.
13.6. Considerações anestésicas
13.6.1. Técnica anestésica
A escolha da técnica anestésica deve levar em consideração o estado clínico do paciente, assim como exames laboratoriais.
Apesar de estudos em adultos sugerirem que a anestesia regional esteja associada com maior tempo de sobrevida em alguns tipos de tumores, em criança isso não é documentado.
A avaliação da coagulação destes pacientes é de suma importância quanto à escolha por uma anestesia regional ou anestesia geral.
13.6.2. Agente anestésico
Atualmente dispomos dentre o arsenal de medicações anestésicas, medicamentos que causam menor depressão miocárdica e hipotensão. Principalmente naqueles pacientes com função cardíaca comprometida e instabilidade do estado hemodinâmico, a cetamina e o etomidato devem ser os agentes de escolha na indução da anestesia.
O efeito das drogas anestésicas na progressão da doença ainda é motivo de estudo em modelos animais.
Os opioides morfina e fentanil mostraram inibir a atividade das células natural killers em humanos, e o tramadol estimula essa atividade tanto em animais como em humanos.
O propofol leva ao aumento da atividade das células T citotóxicas e inibe o fator de transcrição nuclear Kappa, que está relacionado com o crescimento tumoral.
13.7. Manutenção do estado hemodinâmico e monitorização
A prevenção e o tratamento da hipotensão e hipovolemia estão associados a uma menor ocorrência de complicações nos pacientes em estado crítico272,273.
A monitorizacão do débito cardíaco e da perfusão tecidual como medida da saturação venosa central ajudam na avaliação do estado volêmico e na terapêutica com reposição de fluidos, hemocomponentes e drogas vasoativas.
13.8. Analgesia no perioperatório
A dor na criança com câncer está frequentemente presente desde o momento do seu diagnóstico. Estudos relatam uma incidência de até 78% neste momento. A dor é causada pelo envolvimento dos órgãos, nervos, ossos, e pelo efeito do tratamento da doença272. A criança se beneficia com uma abordagem multimodal, incluindo a anestesia regional.
A dor no pós-operatório está relacionada com o maior número de complicações respiratórias, como por exemplo atelectasia. A analgesia eficaz no pós-operatório, seja por via peridural ou endovenosa, diminui o risco dessas complicações273.
A Tabela 20 resume as recomendações analgésicas e anestésicas no paciente pediátrico com câncer.
14. Transplante de medula óssea e complicações cardiovasculares
Os transplantes de células-tronco hematopoiéticas - mais conhecidos como transplantes de medula óssea (TMO) - vêm sendo realizados há mais de três décadas, chegando hoje a mais de 60 mil procedimentos realizados anualmente em todo o mundo281.
As células-tronco hematopoéticas utilizadas nos transplantes podem ser provenientes da medula óssea, do sangue periférico ou do sangue de cordão umbilical/placenta. As células podem ser do próprio indivíduo (transplante autólogo) ou de um doador (transplante alogênico), irmão ou indivíduo não aparentado, mas com compatibilidade na tipagem HLA (human leukocyte antigen). Em pediatria, indicações comuns de transplante alogênico são leucemias, alguns tumores sólidos, aplasia de medula, imunodeficiências e outras doenças hereditárias do sistema hematopoético282-287.
A toxicidade associada aos transplantes depende do tratamento que o paciente recebeu antes da indicação do transplante, do tipo de doador e do regime de condicionamento utilizado. Transplantes autólogos são os mais seguros, enquanto não aparentados apresentam mais complicações. Regimes de condicionamento com altas doses de quimioterapia - mieloablativos - e a irradiação corporal total (total body irradiation - TBI) têm mais riscos que aqueles com intensidade reduzida288,289.
Todos os pacientes que recebem células-tronco alogênicas estão sujeitos a desenvolver a doença do enxerto contra o hospedeiro - DECH, reação imunológica em que linfócitos T do doador reconhecem como estranho e atacam o receptor. Os órgãos mais afetados pela DECH aguda são pele, fígado e trato gastrointestinal. A profilaxia é realizada com ciclosporina ou tacrolimus e metotrexate e o tratamento com associação de metilprednisolona290,291.
A DECH crônica envolve vários órgãos e sistemas e sua apresentação assemelha-se a doenças autoimunes. Usualmente envolve pele, fígado, olhos e mucosa oral, mas também pode acometer pulmão e sistema neuromuscular. A DECH crônica representa uma das principais causas de morbidade após transplantes alogênicos292,293.
Em comparação com outras complicações pós-TMO, a incidência de efeitos tardios cardiovasculares é menor. Contudo, à medida que aumentam os índices de cura e o tempo de acompanhamento, a sua incidência tende a aumentar294-296, atingindo até 17% dos pacientes 15 anos após o TMO297-299. Complicações precoces estão relacionadas à doença e ao seu tratamento antes do TMO, idade, tipo de transplante e comorbidades. As complicações tardias, até décadas após o TMO, estão associadas à quimioterapia cardiotóxica utilizada, principalmente ao uso de ciclofosfamida no regime de condicionamento, à irradiação mediastinal, sexo, idade ao TMO, presença de DECH e de fatores de risco cardiovascular clássicos. Complicações cardiovasculares tardias ocorrem mais comumente após TMO alogênico, sugerindo um papel imunológico no desenvolvimento da aterosclerose. A injúria endotelial pode resultar da inflamação vascular persistente e da morte das células endoteliais provocadas pela DECH, levando a aterosclerose e complicações cardiovasculares. A DECH cardíaca é muito rara e pode cursar com derrame pericárdico, disritmia (principalmente bradicardia), doença coronariana e cardiomiólise296,299,300.
Os eventos cardiovasculares após o TMO ocorrem em pacientes mais jovens do que na população em geral e estão principalmente relacionados à hipertensão arterial sistêmica, doenças cerebrovasculares (acidente vascular cerebral, ataque isquêmico transitório, oclusão da carótida e infartos lacunares sintomáticos) e coronarianas (infarto do miocárdio, doença aterosclerótica cardíaca e angina)289.
Além dos fatores de risco habituais (fumo, hipertensão arterial, obesidade, diabetes, dislipidemias e o sedentarismo), pacientes transplantados têm riscos adicionais como irradiação corporal total, dano endotelial causado pela quimioterapia, DECH, uso prolongado de corticoide e de outros imunossupressores290.
A prevalência de fatores endocrinológicos que aumentam a chance de complicações cardiovasculares, tais como resistência à insulina, intolerância à glicose, diabetes tipo 2, hipertrigliceridemia e obesidade central, estão aumentados nos pacientes transplantados, mesmo em jovens com peso adequado, em consequência de terapias imunossupressoras prolongadas, exposição à radioterapia ou a outras complicações frequentes, como deficiência do hormônio de crescimento e hipotireoidismo293,297,299.
Em transplantados, o risco de desenvolver complicações cardiovasculares é cinco vezes maior e de morrer por causas cardíacas é duas a quatro vezes maior do que na população em geral. Eventos cardiovasculares são a segunda causa de óbito tardio em algumas séries, perdendo apenas para a recidiva da doença neoplásica301.
O depósito de ferro no miocárdio, causado pelas múltiplas transfusões, pode persistir por anos após o TMO302,303. Portanto, é imprescindível que os pacientes com ferritina elevada sejam submetidos à terapia para remover o excesso de ferro do organismo através de flebotomia regular (sangria terapêutica) ou de quelantes do ferro302.
São raras as publicações de complicações cardíacas tardias em crianças transplantadas301. Em estudo prospectivo multicêntrico europeu, a incidência de dano cardíaco em cinco anos foi de 26% em 119 crianças submetidas à TMO alogênico. O uso de irradiação corporal total e de antraciclinas na quimioterapia antes do TMO pioraram significativamente a função cardíaca302. Outro estudo mostrou que as crianças/adolescentes mais susceptíveis a complicações cardíacas foram as submetidas a TMO alogênico não aparentado, irradiação corporal total e com DECH crônica em atividade304.
Como a injúria endotelial causada pela ateroesclerose ocorre anos antes da doença cardiovascular propriamente dita303, a identificação de sinais indiretos de aterosclerose após o TMO é extremamente importante, com potencial de beneficiar as crianças, melhorando sua sobrevida e qualidade de vida305.
O acompanhamento cardiovascular deve ser realizado por toda vida com o envolvimento de equipes multiprofissionais (cardiologista, endocrinologista, oncologista pediátrico, nutricionista, dentre outros), na tentativa de detectar precocemente e intervir no estilo de vida destes pacientes para prevenir efeitos cardiovasculares.
As recomendações referentes a avaliação e acompanhamento da função cardiovascular e perfil metabólico antes, durante e após o transplante de medula óssea autólogo e alogênico estão descritas na Tabela 21.
15. Seguimento tardio dos pacientes fora de tratamento oncológico (follow up)
O prognóstico do câncer pediátrico melhorou significativamente nas últimas três décadas. Atualmente mais de 70% das crianças e adolescentes com câncer sobrevivem mais de cinco anos após o diagnóstico da doença, e isto resultou em um aumento do foco nos efeitos tardios da terapia e na qualidade de vida dessa crescente população de sobreviventes. O termo "efeito tardio" é utilizado para sequelas, tanto físicas quanto psicológicas, que persistem ou se desenvolvem após cinco anos do diagnóstico do câncer. Aproximadamente 70% dos sobreviventes do câncer experimentam pelo menos um efeito tardio, porém menos de 40% desenvolvem condições graves, incapacitantes ou ameaçadoras de vida306.
Cardiotoxicidade é uma das complicações mais graves da terapia oncológica. A mortalidade relacionada à cardiopatia é quase 10 vezes mais alta entre os sobreviventes do câncer infantil do que um grupo-controle da mesma idade307.
Doenças cardiopulmonares são a terceira causa de morte nesta população, depois de recidiva do câncer primário e segunda neoplasia307,308.
Pela definição original de cardiotoxicidade de início tardio, há um período durante o qual nenhuma disfunção ventricular esquerda ou arritmia é detectada, a função cardíaca parece normal e o paciente é assintomático. Seguindo esse período de latência, há deterioração progressiva da função ventricular esquerda, com surgimento de sintomas clínicos, que são associados à alta incidência de morbidade e mortalidade. Esse período de latência, antes do diagnóstico de cardiotoxicidade tardia, tem-se tornado relativo, já que a cardiomiopatia assintomática tem sido detectada por meio de exames ecocardiográficos - convencional em repouso e sob estresse farmacológico, avaliação da deformidade miocárdica -, testes eletrofisiológicos e angiocardiografia com radionuclídeo.
A cardiotoxicidade tardia em crianças é presumivelmente causada pela redução do potencial de crescimento do miocárdio, secundária à lesão dos miócitos pelas antraciclinas. Com o crescimento somático dessas crianças, há uma inadequação da massa ventricular esquerda, com excessiva pós-carga e função diminuída308. Uma terapia com hormônio de crescimento poderia desencadear descompensação cardíaca, por exacerbar esse mecanismo309. O reconhecimento dessa forma de cardiotoxicidade tardia tem levado à necessidade de monitorização por tempo indeterminado dos sobreviventes de câncer infantil.
Conforme exposto anteriormente nesta Diretriz, a cardiotoxicidade pode manifestar-se como cardiomiopatia, pericardite, insuficiência cardíaca congestiva, doença valvar ou doença coronariana prematura. Quimioterapia com antracíclicos e radioterapia mediastinal e/ou cervical são as causas mais comuns de complicações cardiovasculares nos sobreviventes de câncer infantil, porém uma variedade de outros agentes também podem estar implicados.
O Childrens Oncology Group (COG), um grupo cooperativo norte-americano que coordena pesquisas relacionadas à oncologia pediátrica, publicou em 2008 diretrizes especificamente desenhadas para dirigir o seguimento de pacientes tratados por neoplasia pediátrica310. A Diretriz do COG é baseada no risco que cada sobrevivente tem de desenvolver determinado efeito tardio tendo como base a exposição terapêutica, incluindo cirurgia, quimioterapia, radioterapia e transplante de células-tronco hematopoiéticas. Nós propomos a utilização dessas diretrizes no nosso meio (Quadro 12)310. Lembramos que essas são recomendações conservadoras para triagem periódica do sobrevivente de câncer pediátrico baseada na idade do paciente ao diagnóstico, tratamento recebido e dose cumulativa de radiação e antraciclinas. O conhecimento adquirido por meio do seguimento contínuo dos sobreviventes deve ajudar a refinar essas recomendações no futuro.
O escore utilizado foi o National Comprehensive Cancer Network (NCCN) Categories of Consensus modificado311. O escore reflete o peso da evidência na literatura médica, ligando a doença cardiovascular a exposições terapêuticas específicas durante o tratamento oncológico, considera também a adequação da recomendação de triagem de acordo com a experiência clínica do painel de especialistas. Considerou-se evidência de alto nível aquela derivada de estudos caso-controle ou de coorte de alta qualidade, com amostragem adequada e poder estatístico suficiente para provar a hipótese. Considerou-se evidência de baixo nível aquela derivada de estudos não analíticos, séries ou relato de caso, e experiência clínica dos autores. Para as diretrizes do COG foram avaliados cerca de 500 estudos, publicados entre 1985 e 2005. As recomendações foram graduadas de acordo com o nível de evidência mostrado no Quadro 13.
16. Profilaxia contra endocardite infecciosa
A endocardite infecciosa (EI) é uma doença grave, de difícil diagnóstico e tratamento, podendo apresentar diversas manifestações, sejam elas cardíacas, embólicas, sistêmicas, autoimunes e vasculares. Os pacientes oncológicos apresentam maior susceptibilidade ao desenvolvimento de EI por causa das peculiaridades imunológicas e do alto índice de procedimentos invasivos, sejam eles de curta ou longa duração, principalmente quando aliados ao reconhecimento prévio de lesões cardíacas predisponentes.
A despeito dos avanços no diagnóstico e tratamento, sua incidência permanece constante, com média em torno de 1,7 a 6,2 (variando de 0,3 a 22,4) casos a cada 100 mil pessoas nos Estados Unidos e Europa, e a mortalidade, mesmo quando tratada adequadamente, varia de 20 a 30%, alcançando taxas de até 40% em um ano. Classicamente, os estreptococos são os agentes etiológicos mais comuns (30 a 50% dos casos), entretanto, a porcentagem dos estafilococos vem aumentando, encontrando-se em taxas superiores a 30% em algumas séries. Bactérias gram-negativas, fungos e bactérias do grupo HACEK são outros micro-organismos que podem causar EI. O diagnóstico da endocardite infecciosa baseia-se fundamentalmente na identificação de micro-organismos habitualmente relacionados a esta doença em hemoculturas e na visualização de vegetação pelo ecocardiograma.
Desde 1955, há recomendações da American Heart Association para prevenção de EI antes de procedimentos dentários, nos tratos digestivo e geniturinário. Inicialmente, grande destaque foi dado aos procedimentos que habitualmente cursam com bacteremia, principalmente se realizados em pacientes portadores de cardiopatias valvares ou congênitas, uma vez que a fisiopatologia incluía a lesão endotelial (secundária a lesão em jato) associada à formação da endocardite trombótica não bacteriana e à consequente contaminação da mesma. Entretanto, aproximadamente 15 a 25% dos casos de endocardite são relacionados a procedimentos médicos-odontológicos invasivos. Dos que evoluem com EI, apenas 50% eram considerados de alto risco para a mesma, sendo assim, apenas 10% poderiam se beneficiar de antibioticoterapia profilática. Desta forma, a manutenção de uma boa higiene bucal é a profilaxia mais efetiva em relação a antibioticoterapia previamente aos procedimentos odontológicos312.
De acordo com as diretrizes de valvulopatia do ACC/AHA em 2006 e atualizadas em 2008312, os pacientes considerados de alto risco para endocardite grave (portadores de próteses valvares cardíacas, antecedente de EI, cardiopatia congênita cianogênica complexa, shunts sistêmico-pulmonares cirurgicamente construídos, valvulopatias congênitas ou adquiridas, com antecedente de plástica valvar, cardiomiopatia hipertrófica obstrutiva e prolapso da valva mitral com insuficiência mitral associada) foram reclassificados como classe IIA, e apenas para procedimentos odontológicos com alta probabilidade de bacteremia significativa. Foram excluídos os procedimentos do trato gastrointestinal e geniturinário (na ausência de infecção) e aqueles onde não há penetração de mucosa (broncoscopia, ecocardiografia transesofágica, endoscopia digestiva alta e colonoscopia).
A assepsia e o cuidado com cateteres intravasculares se justifica pela alta incidência de EI nosocomial. Em nosso meio, conforme a II Diretriz de Avaliação Perioperatória da Sociedade Brasileira de Cardiologia313, levando em consideração a experiência dos serviços de referência no tratamento de EI e à má higiene bucal aliada às condições socioeconômicas da maioria da população, deveremos estender a profilaxia a todos os pacientes com valvulopatia anatomicamente significativa e aos procedimentos geniturinários ou de trato gastrointestinal contaminados ou com penetração de mucosa.
Grau de recomendação I
Profilaxia para pacientes com risco elevado para EI grave (Quadro 13) e que serão submetidos a procedimentos odontológicos de alta probabilidade de bacteremia significativa (Quadro 14). Esquema antibiótico na Tabela 22. Nível de evidência C.
Grau de recomendação IIa
Profilaxia para pacientes com valvopatia ou cardiopatia congênita risco moderado (Quadro 13) e que serão submetidos a procedimentos odontológicos de alta probabilidade de bacteremia significativa (Quadro 14). Esquema antibiótico na Tabela 22. Nível de evidência C.
Profilaxia para pacientes com risco elevado para EI grave (Quadro 13) e que serão submetidos a procedimentos geniturinários ou gastrointestinais associados a lesão de mucosa. Esquema antibiótico na Tabela 22. Nível de evidência C.
Profilaxia para pacientes com risco elevado para EI grave (Quadro 13) e que serão submetidos a procedimentos esofagianos ou do trato respiratório associado a lesão de mucosa. Esquema antibiótico na Tabela 22. Nível de evidência C.
Grau de recomendação IIb
Profilaxia para pacientes com valvulopatia ou cardiopatia congênita de risco moderado (Quadro 13) e que serão submetidos a procedimentos odontológicos que não se enquadrem na Quadro 14. Esquema antibiótico na Tabela 22. Nível de evidência C.
Profilaxia para pacientes com valvulopatia ou cardiopatia congênita de risco moderado (Quadro 13) e que serão submetidos a procedimentos geniturinários ou gastrointestinais associados a lesão de mucosa. Esquema antibiótico na Tabela 22. Nível de evidência C.
Profilaxia para pacientes com valvulopatia ou cardiopatia congênita de risco moderado (Quadro 13) e que serão submetidos a procedimentos esofagianos ou do trato respiratório associado a lesão de mucosa. Esquema antibiótico na Tabela 22. Nível de evidência C.
Grau de recomendação III
Não há indicação para profilaxia de EI em pacientes com comunicação interatrial (CIA) isolada; comunicação interventricular ou persistência do canal arterial corrigidas e sem fluxo residual; cirurgia de revascularização miocárdica; prolapso de valva mitral sem regurgitação; após colocação de stents; sopros cardíacos inocentes; portadores de marca-passo ou CDI; história de doença de Kawasaki ou febre reumática sem disfunção valvar, que serão submetidos a procedimentos odontológicos, esofagianos, trato respiratório, geniturinário ou gastrointestinal.
Não há indicação para procedimentos que não envolvam risco de bacteremia.
17. Reabilitação física nos sobreviventes ao câncer infanto-juvenil
Os avanços no tratamento do câncer infantil têm aumentado significativamente as taxas de cura, com sobrevida de cinco anos ao redor de 70 a 80% na maioria dos casos. Desse modo, um número cada vez maior de crianças acometidas por doenças malignas estão sobrevivendo e, assim, têm-se observado ampla variedade de efeitos tardios, incluindo retardo do crescimento e desenvolvimento, disfunção cognitiva, comprometimento da função neurológica, cardiopulmonar, sequelas musculoesqueléticas e segunda neoplasia314,315.
Cerca de 30% dos sobreviventes de neoplasia maligna na infância, avaliados por décadas em seguimento, evoluem com alguma sequela ou complicação, com 5 a 10 vezes mais problemas cardiovasculares quando comparados aos seus irmãos saudáveis316,317.
Cardiotoxicidade resultando em cardiomiopatia e associada à insuficiência cardíaca é apenas uma das causas de morbimortalidade nestes pacientes. A correta avaliação do risco cardiovascular é fundamental, uma vez que são frequentes os achados de aterosclerose precoce, síndrome metabólica, obesidade, inatividade física, dislipidemia, resistência à insulina, hipertensão, diabetes. A hipertrigliceridemia induzida pela asparaginase, durante a terapia, pode resultar na manutenção deste quadro fora do tratamento, assim como a elevação da homocisteína durante o tratamento com metotrexate possui o potencial para disfunção endotelial tardia. Da mesma forma, crianças que receberam radioterapia encontram-se em maior risco de desenvolver diabetes, a despeito da manutenção do peso ou de atividade física317.
Estratégias preventivas nesta população, como a manutenção de um estilo de vida saudável e realização de atividade física, parecem reduzir o risco cardiovascular e a morbimortalidade por causas cardíacas semelhante ao que ocorre na população geral, embora não existam grandes estudos de risco populacional em sobreviventes de câncer infantil317.
A reduzida atividade física durante e após o tratamento, também contribui para o descondicionamento físico e atrofia muscular, impedindo a participação em atividades recreativas próprias desta faixa etária. A intervenção precoce do ponto de vista da reabilitação apresenta como objetivos principais o aumento e a manutenção da capacidade cardiopulmonar e função musculoesquelética318-320.
Outro fator relacionado à imobilidade em sobreviventes de câncer é a presença de fadiga, durante e após o tratamento. Foram descritos efeitos positivos da atividade física no funcionamento orgânico e sensação de bem-estar em crianças e adolescentes durante e após o tratamento315-317.
A melhor modalidade, intensidade e duração ainda são difíceis de serem determinadas. Poucas intervenções na atividade física foram relatadas, tanto fora quanto durante o tratamento. Em pequenas séries de casos, e quase que exclusivamente em pacientes com leucemia linfoide aguda, foram implementados componentes aeróbicos, resistidos e de flexibilidade, com diferentes intensidades, frequência e periodicidade, demonstrando que a atividade física pode ser realizada com segurança mesmo durante o tratamento da doença313,316-319.
Durante o tratamento oncológico, a intolerância ao exercício deve-se ao estado nutricional, alteração do sono, alterações bioquímicas e/ou hematológicas secundárias à doença ou à quimioterapia320,321.
Porém, o paciente deve ser estimulado para deambular e realizar suas atividades da vida diária assim que for possível para evitar a síndrome do imobilismo, pois para cada semana de imobilidade implicará em mais de um mês de reabilitação para a total recuperação funcional321.
Às vezes é difícil mobilizar o paciente em quimioterapia ou após o procedimento cirúrgico, mas alguns graus de mobilidade podem reduzir significativamente a morbidade. Para o paciente moderadamente restrito ao leito pela doença ou pelo seu tratamento, deve-se estimular a deambulação duas vezes por dia. Se não for possível, devem ser feitos exercícios no leito, utilizando resistência. Uma prancha ortostática pode ser usada para a manutenção ou para a restauração do condicionamento cardiovascular do paciente que não consegue ficar em pé. Pacientes com membros inferiores edemaciados deverão usar meias elásticas para diminuir o edema e facilitar a deambulação. Exercícios de fortalecimento juntamente com a facilitação do retorno venoso ajudam na manutenção do volume cardiovascular. Os exercícios físicos serão contraindicados quando houver distúrbios eletrolíticos.
Efeitos tardios físicos e funcionais podem ocorrer após o tratamento e persistir por muito tempo, como diminuição do consumo máximo de oxigênio (VO2 max), diminuição da força muscular, fadiga e limitação física. Alguns estudos demonstraram que a terapia com antracíclicos em doses baixas a moderadas podem causar uma disfunção cardíaca subclínica, entretanto essa alteração não levou a uma resposta significante do sistema cardiovascular durante o exercício dinâmico322.
Após o tratamento oncológico, o programa de condicionamento deve ser realizado juntamente com exercícios de amplitude de movimento e força323,324. Pacientes que não apresentam cardiomiopatia podem seguir o Guidelines da American College of Sports Medicine e realizar exercício aeróbico de 30 a 40 minutos com 65 a 80% da frequência cardíaca, três vezes por semana. Exercícios de fortalecimento de grandes grupos musculares com 8 a 12 repetições, duas vezes por semana, com aumento gradativo (5%) da resistência. Pacientes com cardiomiopatia, após avaliação adequada, devem iniciar o treinamento com 40 a 60% do VO2 max, observando-se a presença de sintomas como angina, hipotensão, arritmias e dispneia. A duração da atividade aeróbica deve ser aumentada gradualmente até atingir 30 minutos de atividade ou mais, de acordo com a tolerância do paciente, com frequência de 2 a 3 vezes por semana325,326.
Ressaltamos que, tanto na fase do tratamento oncológico quanto após o término deste, adequada avaliação cardiovascular em repouso e ao esforço deverá ser realizada pela equipe de cardiologia e todas as prescrições de exercícios e de atividades aeróbicas deverão ser orientadas por um fisioterapeuta especializado.
Evidências sugerem impacto positivo do exercício na força, resistência muscular e flexibilidade e são conflitantes quanto à melhora da capacidade cardiopulmonar durante o tratamento e naqueles fora de tratamento submetidos à quimioterapia cardiotóxica. Melhora na fadiga e sensação de bem-estar na atividade física fazem-se presentes quando o paciente adquire melhora na capacidade cardiopulmonar327.
Estudos demonstram que o treinamento supervisionado intra-hospitalar é efetivo, principalmente pelo aspecto motivacional com melhor controle da intensidade. Programas de atividade física em casa ou na comunidade mostraram ser menos efetivos.
A participação em atividades físicas adequadas deve fazer parte do seguimento e manejo de crianças portadoras de condições crônicas como meio do processo de "normalização", permitindo a reintegração nas atividades escolares e sociais327,328.
Reabilitação cardiovascular: Classe de recomendação I; Nível de evidência B.
18. Abordagem multiprofissional
18.1. Enfermagem
Tanto a suspeita quanto o diagnóstico de uma alteração cardíaca podem ser baseados na observação clínica da criança/adoslescente com câncer em vigência ou após o tratamento quimioterápico. A adequada capacitação do profissional de enfermagem permite a identificação precoce e em tempo hábil de possíveis situações de risco inerentes ao tratamento oncológico.
É de fundamental importância o conhecimento integral do diagnóstico do paciente bem como da fase do tratamento em que se encontra (estadiamento, pré-operatório, vigência de quimioterapia ou radioterapia, fora de tratamento etc.).
Uma anamnese bem elaborada identifica ou levanta suspeitas de provável complicação cardiovascular iminente329,330.
O enfermeiro exerce importante papel no reconhecimento de manifestações clínicas e riscos potenciais de cardiotoxicidade, por intermédio das seguintes ações:
1. Identificar, através de sinais e/ou sintomas, quais são as manifestações clínicas presentes (vide Capítulo 8);
2. Identificar dentre as medicações administradas (quimioterápicos, analgésicos, antibióticos, interações medicamentosas) quais oferecem riscos de cardiotoxicidade (vide Capítulo 6);
3. Monitorar o paciente através dos sinais vitais (temperatura, verificação do ritmo cardíaco, frequência cardíaca e respiratória, pressão arterial, saturação de oxigênio)329;
4. Realizar o ECG de maneira tecnicamente correta, identificando e interpretando possíveis alterações significativas antes da apresentação deste paciente à equipe médica (Anexo 1, Figura 1)331,332;
5. Identificar outros fatores de risco relacionados ao comprometimento cardiovascular (insuficiência respiratória, insuficiência renal, distúrbios hidroeletrolíticos e alterações do sistema nervoso central);
6. Realizar anotação de enfermagem corretamente, lembrando-se de anotar o horário da realização dos procedimentos para situar a equipe acompanhante quanto aos fatos precedentes e posteriores.
Outro exame que faz parte da rotina cardiológica, o ecocardiograma avalia a anatomia cardíaca e a função miocárdica sendo, portanto, de extrema importância no diagnóstico da situação hemodinâmica do paciente. O enfermeiro destaca-se por ter conhecimento dos parâmetros ecocardiográficos principais (por exemplo, a fração de ejeção), além de outros aspectos concernentes à situação do paciente.
Testes adicionais (biomarcadores, Holter, MAPA e outros métodos diagnósticos) também deverão ser compreendidos pelo profissional de enfermagem, visto que este participa diretamente de todas as etapas do processo terapêutico (vide sessão métodos diagnósticos)330,332.
Quanto aos eventos tromboembólicos, sabe-se que um dos fatores predisponentes é a presença de cateter venoso central (CVC). Sendo assim, o conhecimento e treinamento da equipe para escolha desses dispositivos, bem como os cuidados de enfermagem no manuseio desses cateteres, são de extrema importância na assistência a esses pacientes. O CVC pode ser instalado por meio de uma punção percutânea ou de ato cirúrgico; deve ser posicionado em porção inferior da veia cava superior ou porção inferior da veia cava inferior333,334.
A indicação do dispositivo venoso deve ser feita precocemente, por uma equipe multiprofissional, através de uma avaliação individualizada, considerando o diagnóstico do paciente, risco cirúrgico na implantação do cateter, disponibilidade da instituição e recursos para ajudar a família a manter o cateter. Quanto à seleção devemos considerar a avaliação da terapia intravenosa prescrita: proposta terapêutica, tipo de cateter (vias e calibre), tipo de suporte, preferência do paciente, habilidade em cooperar/cuidar do dispositivo (Figura 2) 333:
Tipos de cateter venoso central:
- Cateter Percutâneo: mono, duplo e triplo-lúmen
- Cateter Central de Inserção Periférica: (PICC)
- Cateter Totalmente Implantado: Port-a-Cath
Possíveis complicações durante a inserção do dispositivo venoso central:
a) Torácica: hemotórax, pneumotórax, hidrotórax, enfisema subcutâneo;
b) Venosas: hematoma subcutâneo, trombose venosa, embolia gasosa, laceração venosa;
c) Arteriais: fístula artério-venosa, hematoma subcutâneo, laceração arterial;
d) Cardíacas: arritmia, perfuração cardíaca;
e) Neurológicas: traumatismo do plexo.
18.2. Nutrição
Durante muitas décadas concedeu-se importância para a avaliação do estado nutricional apenas durante a doença oncológica, não se atendo ao estado nutricional do paciente após o processo de cura da doença. No passado, a sobrevida era bem menor do que nos dias atuais. Porém, por meio dos avanços no tratamento oncológico, a cura tem sido alcançada em número cada vez maior de pacientes e doenças como obesidade, dislipidemias, diabetes, dentre outras, têm ocorrido com maior frequência 335.
Em tese de mestrado do grupo GEPETTO (Grupo de Estudos Pediátricos dos Efeitos Tardios do Tratamento Oncológico), observou-se numa amostra de 921 pacientes que a prevalência de sobrepeso e obesidade cinco anos após o término do tratamento foi de 12,5 e 6,5%, respectivamente335.
Uma pesquisa realizada com 209 crianças e adolescentes portadoras de leucemia, linfoma e carcinomas do sistema nervoso central, após tratamento, mostrou frequência de excesso de peso em 42% dos pacientes. Este mesmo estudo também constatou hábito alimentar inadequado em que 68% dos curados não atingiam a recomendação em cálcio, 79% não alcançava o consumo recomendado de frutas e hortaliças e 84% ainda apresentavam consumo de lipídios maior que 30% do recomendado336.
A doença cardiovascular tem sido observada em pacientes pós-tratamento oncológico que obtiveram cura. O estudo de Talvensaari et cols., de 1996337, observou aumento de massa gorda em 51 pacientes que obtiveram cura da doença oncológica. Outra pesquisa feita por Gurney et cols., em 2003338, como parte do CCSS, verificou o aumento para o risco de doenças cardiovasculares em 1607 pacientes curados de tumores cerebrais, principalmente os tratados com radio e quimioterapia.
É sabido que são vários os fatores que podem influenciar no aparecimento de doenças cardiovasculares na infância e na adolescência. O estilo de vida atual exerce grande contribuição, como o sedentarismo, a obesidade e o mau hábito alimentar339. Para este último, destacam-se o elevado consumo de ácidos graxos saturados, açúcares e baixo consumo de fibras alimentares340,341. Por outro lado, há outros alimentos que podem ser considerados preventivos, tais como o consumo de ácidos graxos poli e monoinsaturados, fibras solúveis, fitoesteróis e antioxidantes340,341 (Tabela 23).
Há evidências de que o tratamento clínico oncológico exerce riscos para problemas cardíacos e que, provavelmente aliado a maus hábitos alimentares, resulta em alto número de pacientes pós-tratamento com obesidade e suas doenças associadas. Desta forma, acredita-se que um aconselhamento nutricional adequado possa promover um hábito alimentar saudável, prevenindo o aparecimento da aterosclerose ou minimizando este processo (Figura 3).
18.3. Psicologia - A psicologia e os pacientes oncológicos marcados pelo efeito da cardiotoxicidade
18.3.1. Introdução
A taxa de sobrevida do câncer infantil cresceu significativamente nas últimas décadas342. De 1950 a 1960, sobreviventes de câncer eram raros. De 1970 a 1980 ainda havia a ameaça pela doença, mas a cura já era possível. Em torno de 1990, os estudos eram centrados no enfrentamento da doença e na sobrevivência do câncer em longo prazo. Em torno de 2000, iniciaram-se investigações sobre efeitos tardios, com o intuito de identificar os fatores de risco durante o tratamento343.
Nesse contexto, as doenças cardiovasculares são eventos frequentes, decorrentes de avanços na terapêutica oncológica, sugerindo que os pacientes necessitam de cuidados por uma ampla variedade de profissionais da saúde.
Durante o tratamento são realizadas diversas intervenções no corpo que deixam marcas. Além disso, os pacientes sofrem perdas sociais, problemáticas na relação parental, entre outras. Retomar suas vidas e ao mesmo tempo, por vezes, ter que aderir ao tratamento cardiológico em função da cardiotoxicidade, torna-se mais uma questão, o que enfatiza a importância da atuação da psicologia.
18.3.2. Marcas que são para sempre
Medín344 afirma que o tratamento de câncer é algo que deixa marcas. A autora nomeia como sequelas pós-traumáticas, desde déficits cognitivos a desajustes diversos. Mas o que seria o trauma?
Freud345 descreve trauma como algo não elaborado. Aquilo que surpreende a vida do sujeito, levando em conta a falta de recursos subjetivos para lidar com a carga emocional desencadeada, impedindo-o de colocar em palavras (simbolizar) tal conteúdo. O autor ressaltou a importância das primeiras marcas na infância, para a determinação do traumático ao sujeito.
Mas será que é possível generalizar de "traumático" o tratamento de câncer para todos os sujeitos? O que explica o fato de alguns passarem pelo tratamento de forma mais "tranquila" e outros não conseguirem sair do discurso "Tenho ou tive câncer"?
O que a experiência clínica mostra é que o tratamento de câncer, assim como seus efeitos, serão simbolizados de forma singular. A tentativa de categorização da subjetividade diante da doença orgânica não é suficiente, se as histórias de vida não forem levadas em conta. As possíveis lesões na subjetividade não podem ser vistas, nem mensuradas, apenas ouvidas. A este fato justifica-se o trabalho da psicologia, proporcionando um lugar de elaboração às situações vivenciadas.
18.3.3. O serviço de psicologia
O serviço de psicologia deve atuar junto à equipe multiprofissional, atendendo pacientes e seus cuidadores. O atendimento pode ser ambulatorial ou durante as internações.
Numa clínica de efeitos tardios, por exemplo, recomenda-se que o psicólogo realize uma triagem através de entrevistas semidirigidas, visando avaliar possíveis efeitos psíquicos relacionados ao tratamento. Investigar como se encontra o sujeito frente a sua estrutura familiar, relações sociais e recordações sobre o tratamento. Nesse contexto, pacientes com efeitos da cardiotoxicidade podem ser encaminhados pela equipe multiprofissional ou chegar ao serviço de psicologia durante internações causadas pelas sequelas orgânicas ou por falta de adesão ao tratamento cardiológico proposto.
18.3.4. Efeitos tardios: presença ou ausência de angústias?
No levantamento bibliográfico realizado por Teles e Valle342 com amostras de sobreviventes de câncer infantil, verificou-se um "funcionamento psicossocial sem nenhum tipo de comprometimento"342. A experiência dos atendimentos psicológicos com os pacientes fora de tratamento traz um elemento importante que coincide com o dado apontado nesse levantamento. A prática em psicanálise nos traz uma possibilidade de leitura desse dado: em triagens da clínica de efeitos tardios, os pacientes e familiares quase nunca trazem queixas ou angústias acerca de aspectos da dinâmica familiar e/ou relações sociais. Porém, ao fazer uma análise aprofundada das posições subjetivas, constatam-se dificuldades na prospecção de vida desses sujeitos, sem que se tenha consciência disso e sem manifestar qualquer incômodo.
Outro aspecto de grande relevância é em relação à baixa adesão ao tratamento dos pacientes acometidos pela cardiotoxicidade. É comum a chegada desses pacientes em estado de emergência de cuidados por não seguirem corretamente a prescrição médica e mais uma vez sem queixas, e se dizendo "bem" no que compete ao seu estado "psicossocial"342.
18.3.5. A direção do tratamento psicológico frente aos efeitos tardios
Pela ausência de queixas frente às questões "psicossociais" e ao mesmo tempo a erupção da sequela da cardiotoxicidade como marcas que ficam para sempre na vida do sujeito, recomenda-se a criação de um espaço de escuta voltado para questões não só da doença, mas sim que possibilite uma forma de expressar (através do ato de falar ou brincar) aquilo que acomete o corpo.
Indica-se que a direção de tratamento seja pautada nas problemáticas familiares que antecedem o diagnóstico, visto que ao longo do adoecimento podem ficar mais latentes, tornando para o sujeito e/ou cuidadores uma questão a ser trabalhada. Conforme Moura346, é na urgência subjetiva que se tem a possibilidade da construção de uma demanda.
É fundamental para lidar com a adesão dos pacientes ao tratamento cardiológico, escutar os pais e implicá-los na necessidade desses cuidados. Lacan347 afirma que a criança responde a uma estrutura familiar na qual está imersa.
A relevância do tema também sugere necessidade de mais pesquisas com abordagens e metodologias de estudos focados na subjetividade dos sobreviventes de câncer infantil, bem como de serviços ambulatoriais que permitam a assistência psicológica para os pacientes acometidos pela cardiotoxicidade.
O tratamento oncológico traz consigo sequelas orgânicas e marcas subjetivas, marcas essas que Medín344 denomina "silenciosas", por serem difíceis de serem representadas em palavras.
O psicólogo, diante dessas lesões silenciosas, tem o compromisso de abrir espaço para que o sujeito se manifeste e traga ali em sua fala aquilo que há de mais elementar sobre si mesmo. Ao falar, o sujeito tem a oportunidade de existir, de ser, de se situar como desejante. Onde há palavra há vida. É ao falar que o sujeito consegue fazer articulações simbólicas e construir novas possibilidades diante daquilo que lhe resta: Viver.
19. Considerações finais
As complicações cardiovasculares decorrentes do tratamento do câncer na infância e adolescência poderão manifestar-se clínica ou laboratorialmente de modo subclínico, precoce ou tardio, decorrentes tanto do tratamento quimioterápico, radioterápico, cirúrgico, ou da associação entre estes.
Essa população apresenta oito vezes mais chances de morte por eventos cardiovasculares que a população geral.
Cerca de 30 anos ou mais após o diagnóstico, aproximadamente 75% dos sobreviventes ao câncer nessa faixa etária poderão sofrer alguma condição cardiovascular crônica como insuficiência cardíaca, hipertensão arterial sistêmica, arritmias, tromboembolismo isquemia ou infarto do miocárdio.
As crianças tratadas com antraciclinas são particularmente susceptíveis aos efeitos tóxicos apresentando significativo risco de desenvolverem insuficiência cardíaca, não havendo, no entanto, dose considerada segura nessa população.
Buscamos através de estudos sobre polimorfismos genéticos e farmacogenômica, a identificação de indivíduos predispostos aos efeitos tóxicos do tratamento oncológico, alertando o corpo clínico quanto à necessidade de medidas cardioprotetoras eficazes.
É dever de todos os que integram a equipe de apoio ao paciente oncológico infanto-juvenil ter como intuito a busca constante de conhecimentos científicos aprofundados sobre o arsenal terapêutico vigente e perspectivas futuras, mantendo constante atenção quanto à identificação em tempo hábil de situações com potencial de risco que interfiram no sucesso terapêutico e evolução em longo prazo. Esse é o principal objetivo da Cardio-Oncologia Pediátrica.
20. Agradecimentos
Durante todo o processo de elaboração desta I Diretriz Brasileira de Cardio-Oncologia Pediátrica, contamos com a participação ativa de alguns profissionais de apoio à pesquisa clínica, sem os quais a atuação dos diversos autores não teria sido possível. Registramos aqui nossos sinceros agradecimentos a: Ana Helena Dutra Rodrigues (SOBOPE), Arnaldo Pires (GRAACC), Cássia Silva (SOBOPE), Débora Ugayama Bassi (SOBOPE), Maria Aparecida Sampaio Batista Camilo (SOBOPE), Maria do Carmo Cavarette Barreto (Incor-FMUSP), Mariana Grings (GRAACC), Reinaldo Ramos (BIREME), William Robert Duraes (SBC).
21. Referências bibliográficas
- 1. Ministério da Saúde. Instituto Nacional de Câncer (INCA). Coordenação de prevenção e vigilância de câncer. Câncer da criança e adolescente no Brasil: dados dos registros de base populacional e de mortalidade. Rio de Janeiro: INCA; 2008.
- 2. Instituto Brasileiro de Geografia e Estatística (IBGE). Censo demográfico. [Acesso em 2011 dez 12]. Disponível em: http://www.censo2010.ibge.gov.br
-
3National Cancer Institute. Surveillance and end results. Age-adjusted SEER cancer incidence rates 2009 (1975-2008). [Access in 2011 Dec 12]. Available from: http://seer.cancer.gov
-
4Ministério da Saúde. Instituto Nacional de Câncer (INCA). Câncer no Brasil. Dados dos registros de base populacional. Rio de Janeiro: INCA; 2010.
- 5. Petrilli AS, Carneiro Jr JL, Cypriano M, Angel A, Toledo S. Diferenças clínicas, epidemiológicas e biológicas entre o câncer na criança e no adulto. Rev Bras Cancerol. 1997;43(3):191-203.
- 6. Barry E, Alvarez JA, Scully RE, Miller TL, Lipshultz SE. Anthracycline-induced cardiotoxicity: course, pathophysiology, prevention and management. Expert Opin Pharmacother. 2007;8(8):1039-58.
- 7. Iarussi D, Indolfi P, Casale F, Martino V, Di Tulio MT, Calabro R. Anthracycline-induced cardiotoxicity in children with cancer: strategies for prevention and management. Pediatr Drugs. 2005;7(2):67-76.
- 8. Shankar SM, Marina N, Hudson MM, Hodgson DC, Adams MJ, Landier W, et al; Cardiovascular Disease Task Force of the Children's Oncology Group. Monitoring for cardiovascular disease in survivors of childhood cancer: report from the Cardiovascular Disease Task Force of the Children's Oncology Group. Pediatrics. 2008;121(2):e387-96.
- 9. Franco VI, Henkel JM, Miller TL, Lipshultz SE. Cardiovascular effects in childhood cancer survivors treated with anthracyclines. Cardiol Res Pract. 2011 Feb 10;2011:134679.
- 10. Zhang YW, Shi J, Li YJ, Wei L. Cardiomyocyte death in doxorubicin-induced cardiotoxicity. Arch Immunol Ther Exp (Warsz). 2009;57(6):435-45.
- 11. Albini A, Pennesi G, Donatelli F, Cammarota R, De Flora S, Noonan DM. Cardiotoxicity of anticancer drugs: the need for cardio-oncology and cardio-oncological prevention. J Natl Cancer Inst. 2010;102(1):14-25.
- 12. Kremer LC, van der Pal HJ, Offringa M, van Dalen EC, Voûte PA. Frequency and risk factors of subclinical cardiotoxicity after anthracycline therapy in children: a systematic review. Ann Oncol. 2002;13(6):819-29.
- 13. de Matos Neto RP, Petrilli AS, Silva CM, Campos Filho O, Oporto VM, Gomes Lde F, et al. Função sistólica do ventrículo esquerdo pela ecocardiografia em crianças e adolescentes com osteossarcoma tratados com doxorrubicina com e sem dexrazoxane. Arq Bras Cardiol. 2006;87(6):763-71.
- 14. Simbre VC, Duffy SA, Dadlani GH, Miller TL, Lipshultz SE. Cardiotoxicity of cancer chemotherapy: implications for children. Paediatr Drugs. 2005;7(3):187-202.
- 15. Lipshultz SE, Adams MJ. Cardiotoxicity after childhood cancer: beginning with the end in mind. J Clin Oncol. 2010;28(8):1276-81.
- 16. Chen MH, Colan SD, Diller L. Cardiovascular disease: cause of morbidity and mortality in adult survivors of childhood cancers. Circ Res. 2011;108(5):619-28.
- 17. Fulbright JM. Review of cardiotoxicity in pediatric cancer patients: during and after therapy. Cardiol Res Pract. 2011;2011:942090.
- 18. Monsuez JJ. Detection and prevention of cardiac complications of cancer chemotheraphy. Arch Cardiovasc Dis. 2012;105(11):593-604.
- 19. Chatterjee K, Zhang J, Honbo N, Karliner JS. Doxorubicin cardiomyopathy. Cardiology. 2010;115(2):155-62.
- 20. Yeh ET, Tong AT, Lenihan DJ, Yusuf SW, Swafford J, Champion C, et al. Cardiovascular complications of cancer therapy: diagnosis, pathogenesis, and management. Circulation. 2004;109(25):3122-31.
- 21. Yusuf SW, Razeghi P, Yeh ET. The diagnosis and management of cardiovascular disease in cancer patients. Curr Probl Cardiol. 2008;33(4):163-96.
- 22. Isner JM, Ferrans VJ, Cohen SR, Witkind BG, Virmani R, Gottdiener JS, et al. Clinical and morphologic cardiac findings after anthracycline chemotherapy: analysis of 64 patients studied at necropsy. Am J Cardiol. 1983;51(7):1167-74.
- 23. Darby SC, Cutter DJ, Boerma M, Constine LS, Farjardo LF, Kodama K, et al. Radiation-related heart disease: current knowledge and future prospects. Int J Radiat Oncol Biol Phys. 2010;76(3):656-65.
- 24. Bernaba BN, Chan JB, Lai CK, Fishbein MC. Pathology of late-onset anthracycline cardiomyopathy. Cardiovasc Pathol. 2010;19(5):308-11.
- 25. Zhang J, Yu ZX, Hilbert SL, Yamaguchi M, Chadwick DP, Herman EH, et al. Cardiotoxicity of human recombinant interleukin-2 in rats: a morphological study. Circulation. 1993;87(4):1340-53.
- 26. Miyata S, Takemura G, Kosai K, Takahashi T, Esaki M, Li L, et al. Anti-Fas gene therapy prevents doxorubicin-induced acute cardiotoxicity through mechanisms independent of apoptosis. Am J Pathol. 2010;176(2):687-98.
- 27. Jain D, Maleszewski JJ, Halushka MK. Benign cardiac tumors and tumorlike conditions. Ann Diagn Pathol. 2010;14(3):215-30.
- 28. Yu K, Liu Y, Wang H, Hu S, Long C. Epidemiological and pathological characteristics of cardiac tumors: a clinical study of 242 cases. Interact Cardiovasc Thorac Surg. 2007;6(5):636-9.
- 29. Ferrari A, Miceli R, Casanova M, Gronchi A, Collini P, Meazza C, et al. Adult-type soft tissue sarcomas in paediatric age: a nomogram-based prognostic comparison with adult sarcoma. Eur J Cancer. 2007;43(18):2691-7.
- 30. Thomas-de-Montpréville V, Nottin R, Dulmet E, Serraf A. Heart tumors in children and adults: clinicopathological study of 59 patients from a surgical center. Cardiovasc Pathol. 2007;16(1):22-8.
- 31. Isaacs H Jr. Fetal and neonatal cardiac tumors. Pediatr Cardiol. 2004;25(3):252-73.
- 32. Leja MJ, Shah DJ, Reardon MJ. Primary cardiac tumors Tex Heart Inst J. 2011;38(3):261-2.
- 33. Maraj S, Pressman GS, Figueredo VM. Primary cardiac tumors. Int J Cardiol. 2009;133(2):152-6.
- 34. Bakaeen FG, Reardon MJ, Coselli JS, Miller CC, Howell JF, Lawrie GM, et al. Surgical outcome in 85 patients with primary cardiac tumors. Am J Surg. 2003;186(6):641-7.
- 35. Degueldre SC, Chockalingam P, Mivelaz Y, Di Bernardo S, Pfammatter JP, Barrea C, et al. Considerations for prenatal counselling of patients with cardiac rhabdomyomas based on their cardiac and neurologic outcomes. Cardiol Young. 2010;20(1):18-24.
- 36. Sun JP, Asher CR, Yang XS, Cheng GG, Scalia GM, Massed AG, et al. Clinical and echocardiographic characteristics of papillary fibroelastomas: a retrospective and prospective study in 162 patients. Circulation. 2001;103(22):2687-93.
- 37. Gowda RM, Khan IA, Nair CK, Mehta NJ, Vasavada BC, Sacchi TJ. Cardiac papillary fibroelastoma: a comprehensive analysis of 725 cases. Am Heart J. 2003;146(3):404-10.
- 38. Talukder M, Joyce L, Marks R, Kaplan K. Primary cardiac synovial sarcoma. Interact Cardiovasc Thorac Surg. 2010;11(4):490-2.
- 39. Hadley GP, Sheik-Gafoor MH, Buckels NJ. The management of nephroblastoma with cavo-atrial disease at presentation: experience from a developing country. Pediatr Surg Int. 2010;26(12):1169-72.
- 40. Santos MV, Bergamo M, Senerchia A, Macedo CR, Petrilli AS, Seixas MT, et al. Metástase cardíaca de osteossarcoma: experiência de uma instituição de referência em oncologia pediátrica. In: 12ş Congresso Brasileiro de Oncologia Pediátrica da Sociedade de Oncologia Pediátrica; setembro 29 - outubro 02, 2009. Curitiba (PR).
- 41. De Santi CS, Santos MV, Macedo CR, Carmona PC, Bergamo M, Alves MT, et al. Left-sided cardiac metastasis of osteosarcoma. In: 41ş Congresso da Sociedade Internacional de Pediatria Oncológica; outubro 5-10, 2009. Santo Amaro (SP).
- 42. Lipshultz SE, Colan SD, Gelber RD, Perez-Atayde AR, Sallan SE, Sanders SP. Late effects of doxorubicin therapy for acute lymphoblastic leukemia in childhood. N Eng J Med. 1991;324(12):808-15.
- 43. Menna P, Salvatorelli E, Minotti G. Cardiotoxicity of antitumor drugs. Chem Res Toxicol. 2008;21(5):978-89.
- 44. Olson RD, Mushlin PS. Doxorubicin cardiotoxicity: analysis of prevailing hypotheses. FASEB J. 1990;4(13):3076-86.
- 45. Goormaghtigh E, Huart P, Praet M, Brasseur R, Ruysschaert JM. Structure of the adriamycin-cardiolipin complex: role in mitochondrial toxicity. Biophys Chem.1990;35(2-3):247-57.
- 46. Shan K, Lincoff AM, Young JB. Anthracycline-induced cardiotoxicity. Ann Intern Med. 1996;125(1):47-58.
- 47. Lefrak EA, Pitha J, Rosenheim S, Gottlieb JA. A clinicopathologic analysis of adriamycin cardiotoxicity. Cancer. 1973;32(2):302-14.
- 48. Kremer LC, van Dalen EC, Offringa M, Otenkamp J, Voute PA. Anthracycline-induced clinical heart failure in a cohort of 607 children: long-term follow-up study. J Clin Oncol. 2001;19(1):191-6.
- 49. Legha SS, Benjamin RS, Mackay B, Ewer M, Wallace S, Valdivieso M, et al. Reduction of doxorubicin cardiotoxicity by prolonged continuous intravenous infusion. Ann Intern Med. 1982;96(2):133-9.
- 50. Levitt GA, Dorup I, Sorensen K, Sullivan I. Does anthracycline administration by infusion in children affect late cardiotoxicity? Br J Haematol. 2004;124(4):463-8.
- 51. Lipshultz SE, Giantris AL, Lipsitz SR, Kimball Dalton V, Asselin BL, Barr RD, et al. Doxorubicin administration by continuous infusion is not cardioprotective: the Dana-Farber 91-01 acute lymphoblastic leukemia protocol. J Clin Oncol. 2002;20(6):1677-82.
- 52. Pai VB, Nahata MC. Cardiotoxicity of chemotherapeutic agents: incidence, treatment and prevention. Drug Saf. 2000;22(4):263-302.
- 53. Gharib MI, Burnett AK. Chemotherapy induced cardiotoxicity: current practice and prospects of prophylaxis. Eur J Heart Fail. 2002;4(3):235-42.
- 54. Goldberg MA, Antin JH, Guinan EC, Rappeport JM. Cyclophosphamide cardiotoxicity: an analysis of dosing as a risk factor. Blood. 1986;68(5):1114-8.
- 55. Kandylis K, Vassilomanolakis M, Tsoussis S, Efremidis AP. Ifosfamide cardiotoxicity in humans. Cancer Chemother Pharmacol. 1989;24(6):395-6.
- 56. Ritchie DS, Seymour JF, Roberts AW, Szer J, Grigg AP. Acute left ventricular failure following melphalan and fludarabine conditioning. Bone Marrow Transplant. 2001;28(1):101-3.
- 57. Cheng CF, Juan SH, Chen JJ, Chao YC, Chen HH, Lian WS, et al. Pravastatin attenuates carboplatin-induced cardiotoxicity via inhibition of oxidative stress associated apoptosis. Apoptosis. 2008;13(7):883-94.
- 58. Floyd JD, Nguyen DT, Lobins RL, Bashir Q, Doll DC, Perry MC. Cardiotoxicity of cancer therapy. J Clin Oncol. 2005;23(30):7685-96.
- 59. Van Besien K, Devine S, Wickrema A, Jessop E, Amin K, Yassine M, et al. Regimen-related toxicity after fludarabine-melphalan conditioning: a prospective study of 31 patients with hematologic malignancies. Bone Marrow Transplant. 2003;32(5):471-6.
- 60. Kalil Filho R, Hajjar LA, Bacal F, Hoff PM, Diz M del P, Galas FRBG, et al. I Diretriz brasileira de cardio-oncologia da Sociedade Brasileira de Cardiologia. Arq Bras Cardiol. 2011;96(2 supl.1):1-52.
- 61. Rezkalla S, Kloner RA, Ensley J, al-Sarraf M, Revels S, Olivenstein A, et al. Continuous ambulatory ECG monitoring during fluorouracil therapy: a prospective study. J Clin Oncol. 1989;7(4):509-14.
- 62. Cappellano AM, Bouffet E, Silva F. Vinorelbine in progressive unresectable low-grade glioma in children. In: Annual'11 Meeting of American Society of Clinical Oncology (ASCO). Chicago (Illinois), June 3-7; 2011. Abstract 9524.
- 63. Vassal G, Couanet D, Stockdale E, Geoffray A, Geoerger B, Orbach D, et al; French Society of Pediatric Oncology; United Kingdom Children's Cancer Study Group. Phase II trial of irinotecan in children with relapsed or refractory rhabdomyosarcoma: a joint study of the French Society of Pediatric Oncology and the United Kingdom Children´s Cancer Study Group. J. Clin Oncol. 2007;25(4):356-61.
- 64. Miya T, Fujikawa R, Fukushima J, Nogami H, Koshiishi Y, Goya T. Bradycardia induced by irinotecan: a case report. Jpn J Clin Oncol. 1998;28(11)709-11.
- 65. Saylors RL 3rd, Stine KC, Sullivan J, Kepner JL, Wall DA, Bernstein ML, et al; Pediatric Oncology Group. Cyclophosphamide plus topotecan in children with recurrent or refractory solid tumors: a Pediatric Oncology Group phase II study. J Clin Oncol. 2001;19(15):3463-9.
- 66. Escoto H, Ringewald J, Kalpatthi R. Etoposide-related cardiotoxicity in a child with haemophagocytic lymphohistiocytosis. Cardiol Young. 2010;20(1):105-7.
- 67. Lenihan DJ, Alencar AJ, Yang D, Kurzrock R, Keating MJ, Duvic M. Cardiac toxicity of alemtuzumabe in patients with mycosis fungoides/Sézary syndrome. Blood. 2004;104(3):655-8.
- 68. Floyd J, Morgan JP, Perry MC. Cardiotoxicity of nonatracycline câncer chemotherapy agents uptodate. [Access in 2011 Oct 11]. Available from: http://www.uptodate.com/contents/cardiotoxicity-of-nonantracycline-cancer-chemotherapy-agents
- 69. Force T, Krause DS, Van Etten RA. Molecular mechanisms of cardiotoxicity of tyrosine kynase inhibition. Nat Rev Cancer. 2007;7(5):332-44.
- 70. Kerkela R, Grazette L, Yacobi R, Iliescu C, Patten R, Beahm C, et al. Cardiotoxicity of the cancer therapeutic agent imatinib mesylate. Nat Med. 2006;12(8):908-16.
- 71. Martino S, Ratanatharathorn V, Karanes C, Samal BA, Sohn YH, Rudnick SA. Reversible arrhythmias observed in patients treated with recombinant alpha 2 interferon. J Cancer Res Clin Oncol. 1987;113(4):376-8.
- 72. Bhatia S, Landier W. Evaluating survivors of pediatric cancer. Cancer J. 2005;11(4):340-54.
- 73. Rigon H, Lopes LF, do Rosario Latorre M, de Camargo B. The GEPETTO program for surveillance of long-term survivors of childhood cancer: preliminary report from a single institution in Brazil. Med Pediatr Oncol. 2003;40(6):405-6.
- 74. Ng AK. Review of the cardiac long-term effects of therapy for Hodgkin lymphoma. Br J Haematol. 2011;154(1):23-31.
- 75. Heidenreich PA, Schnittger I, Strauss WH, Vagelos RH, Lee BK, Mariscal CS, et al. Screening for coronary artery disease after mediastinal irradiation for Hodgkin's disease. J Clin Oncol. 2007;25(1):43-9.
- 76. Yusuf WS, Sami S, Daher IN. Radiation-induced heart disease: a clinical update. Cardiol Res Pract. 2011;2011:317659.
- 77. Andratschke N, Maurer J, Molls M, Trott KR. Late radiation-induced heart disease after radiotherapy: clinical importance, radiobiological mechanisms and strategies of prevention. Radiother Oncol. 2011;100(2):160-6.
- 78. Gagliardi G, Constine LS, Moiseenko V, Correa C, Pierce LJ, Allen AM, et al. Radiation dose-volume effects in the heart. Int J Radiat Oncol Biol Phys. 2010;76(3 Suppl.):S77-85.
- 79. Boerma M, Hauer-Jensen M. Preclinical research into basic mechanisms of radiation-induced heart disease. Cardiol Res Pract. 2010;2011:858262.
- 80. Darby SC, Cutter DJ, Boerma M, Constine LS, Fajardo LF, Kodama K, et al. Radiation-related heart disease: current knowledge and future prospects. Int J Radiat Oncol Phys. 2010;76(3):656-65.
- 81. Bovelli D, Plataniotis G, Roila F; ESMO Guidelines Working Group. Cardiotoxicity of chemotherapeutic agents and radiotherapy-related heart disease: ESMO clinical practice guidelines. Ann Oncol. 2010;21 Suppl. 5:s277-82.
- 82. Bentzen SM, Dorr W, Anscher MS, Denham JW, Hauer-Jensen M, Marks LB, et al. Normal tissue effects: reporting and analysis. Semin Radiat Oncol. 2003;13(3):189-202.
- 83. Cox JD, Stetz J, Pajak TF. Toxicity criteria of the Radiation Therapy Oncology Group (RTOG) and the European Organization for Research and Treatment of Cancer (EORTC). Int J Radiat Oncol Biol Phys. 1995;31(5):1341-6.
- 84. Pavy JJ, Denekamp J, Letschert J, Littbrand B, Mornex F, Bernier J, et al. EORTC Late Effects Working Group. Late effects toxicity scoring: the SOMA scale. Radiother Oncol. 1995;35(1):11-60.
- 85. Bolling T, Schuck A, Pape H, Rube C, Pollinger B, Timmermann B, et al. Study protocol of the German "Registry for the detection of late sequelae after radiotherapy in childhood and adolescence" (RiSK). Radiat. Oncol. 2008;3:10.
- 86. Hong RA, Iimura T, Sumida KN, Eager RM. Cardio-oncology/onco-cardiology. Clin Cardiol. 2010;33(12):733-7.
- 87. Krischer JP, Epstein S, Cuthbertson DD, Goorin AM, Epstein ML, Lipshultz SE, et al. Clinical cardiotoxicity following anthracycline treatment for childhood cancer: the Pediatric Oncology Group experience. J Clin Oncol. 1997;15(4):1544-52.
- 88. Curigliano G, Mayer EL, Burstein HJ, Winer EP, Goldhirsch A. Cardiac toxicity from systemic cancer therapy: a comprehensive review. Prog Cardiovasc Dis. 2010;53(2):94-104.
- 89. Armstrong GT, Liu Q, Yasui Y, Neglia JP, Leisenring W, Robison LL, et al. Late mortality among 5-year survivors of childhood cancer: a summary from the Childhood Cancer Survivors Study. J Clin Oncol. 2009;27(14):2328-38.
- 90. Latham GJ, Greenberg RS. Anesthetic considerations for the pediatric oncology patient-part 1: a review of antitumor therapy. Paediatr Anaesth. 2010;20(4):295-304.
- 91. Oeffinger KC, Mertens AC, Sklar CA, Kawashima T, Hudson MM, Meadows AT, et al; Childhood Cancer survivor Study. Chronic health conditions in adults survivors of childhood cancer. N Engl J Med. 2006;355(15):1572-82.
- 92. Bocchi EA, Marcondes-Braga FG, Ayub-Ferreira SM, Rohde LE, Oliveira WA, Almeida DR, et al.; Sociedade Brasileira de Cardiologia. III Diretriz brasileira de insuficiência cardíaca crônica. Arq Bras Cardiol. 2009;93(1 supl.1):1-71.
- 93. Levitt G, Anazodo A, Burch M, Bunch K. Cardiac or cardiopulmonary transplantion in childhood cancer survivors: an increasing need? Eur J Cancer. 2009;45(17):3027-34.
- 94. Bacal F, Souza-Neto JD, Fiorelli AI, Mejia J, Marcondes-Braga FG, Mangini S, et al; Sociedade Brasileira de Cardiologia. II Diretriz brasileira de transplante cardíaco. Arq Bras Cardiol. 2009;94(1 supl.1):e16-e73.
- 95. Azeka E, Franchini Ramires JA, Valler C, Alcides Bocchi E. Delisting of infants and children from the heart transplantation waiting list after carvedilol treatment. J Am Coll Cardiol. 2002;40(11):2034-8.
- 96. Monsuez JJ, Charniot JC, Vignat N, Artigou JY. Cardiac side effects of cancer chemotherapy. Int J Cardiol. 2010;144(1):3-15.
- 97. Fulbright JM, Huh W, Anderson P, Chandra J. Can anthracycline therapy for pediatric malignancies be less cardiotoxic? Curr Oncol Rep. 2010;12(6):411-9.
- 98. Temming P, Qureshi A, Hardt J, Leiper AD, Levitt G, Ancliff PJ, et al. Prevalence and predictors of anthracycline cardiotoxicity in children treated for acute myeloid leukaemia: retrospective cohort study in a single centre in the United Kingdom. Pediatr Blood Cancer. 2011;56(4):625-30.
- 99. Ceneviva G, Paschall JA, Maffei F, Carcillo JA. Hemodynamic support in fluid-refractory pediatric septic shock. Pediatrics. 1998;102(2):e19.
- 100. Carcillo JA, Fields AI; Comitê de Força-Tarefa. [Clinical practice parameters for hemodynamic support of pediatric and neonatal patients in septic shock]. J Pediatr (Rio J). 2002;78(6):449-66.
- 101. Nichols DG, Ackerman AD, Carcillo JA, Dalton HJ. Rogers textbook of pediatric intensive care. 4th ed. Philadelphia: Lippincot Williams & Wilkins; 2008.
- 102. Beggs S, Thompson A, Nash R, Tompson A, Peterson G. Cardiac failure in children. World Health Organization; 2009.
- 103. Overgaard CB, Dzavik B. Inotropes and vasopressors: review of physiology and clinical use in cardiovascular disease. Circulation. 2008;118(10):1047-56.
- 104. Sharma M, Nair MN, Jatana SK, Shahi BN. Congestive heart failure in infants and children. MJAFI. 2003;59(3):228-33.
- 105. Temming P, Jenney ME. The neurodevelopmental sequelae of childhood leukaemia and its treatment. Arch Dis Child. 2010;95(11):936-40. Erratum in Arch Dis Child. 2011;96(8):787.
- 106. Lipshultz SE. Exposure to anthracyclines during childhood causes cardiac injury. Semin Oncol. 2006;33(3 Suppl 8):S8-14.
- 107. Balfour I. Management of chronic congestive heart failure in children. Cur Treat Options Cardiovasc Med. 2004;6(5):407-16.
- 108. Santos MV, Oliveira PM, Arduini RG, Silva DC. Uso de levosimendan na insuficiência cardíaca induzida por quimioterápicos. In: XII Congresso Paulista de Terapia Intensiva (COPATI). São Paulo; 2011.
- 109. Cecchin F, Frangini PA, Brown DW, Fynn-Thompson F, Alexander ME, Triedman JK, et al. Cardiac resynchronization therapy (and multisite pacing) in pediatrics and congenital heart disease: five years experience in a single institution. J Cardiovasc Electrophysiol. 2009;20(1):58-65.
- 110. Ahlehoff O, Galloe AM, Hansen PR. Anthracycline-induced cardiomyopathy: favourable effects of cardiac resynchronization therapy. Int J Cardiol. 2010;142(2):e23-4.
- 111. Sociedade Brasileira de Cardiologia/ Sociedade Brasileira de Hipertensão / Sociedade Brasileira de Nefrologia. VI Diretrizes Brasileiras de Hipertensão. Arq Bras Cardiol. 2010;95(1 supl.1):1-51.
- 112. Louis CU, Butani L. High blood pressure and hypertension in children with newly diagnosed acute leukemia and lymphoma. Pediatr Nephrol. 2008;23(4):603-9.
- 113. Olgar S, Yetgin S, Cetin M, Aras T. Can renal leukemic infiltration cause hypertension in children? J Pediatr Hematol Oncol. 2006;28(9):579-84.
- 114. Attard-Montalto SP, Saha V, Ng YY, Kingston JE, Eden OB. High incidence of hypertension in children presenting with acute lymphoblastic leukemia. Pediatr Hematol Oncol. 1994;11(5):519-25.
- 115. Minami M, Matsumoto S, Horiuchi H. Cardiovascular side effects of modern cancer therapy. Circ J. 2010;74(9):1779-86.
- 116. National High Blood Pressure Education Program Working Group on High Blood Pressure in Children and Adolescents. The fourth report on the diagnosis, evaluation and treatment of high blood pressure in children and adolescents. Pediatrics. 2004;114(2 Suppl 4th Report):555-76.
- 117. Oeffinger KC, Buchanan GR, Eshelman DA, Denke MA, Andrews TC, Germak JA, et al. Cardiovascular risk factors in young adult survivors of childhood acute lymphoblastic leukemia. J Pediatr Hematol Oncol. 2001;23(7):424-30.
- 118. Guglin M, Aljayeh M, Saiyad S, Ali R, Curtis AB. Introducing a new entity: chemotherapy-induced arrhythmia. Europace. 2009;11(12):1579-86.
- 119. Yeh ET, Bickford CL. Cardiovascular complications of cancer therapy: incidence, pathogenesis, diagnosis, and management. J Am Coll Cardiol. 2009;53(24):2231-47.
- 120. Kaur A, Yu SS, Lee AJ, Chiao TB. Thalidomide-induced sinus bradycardia. Ann Pharmacother. 2003;37(7-8):1040-3.
- 121. Yilmaz U, Oztop I, Ciloglu A, Okan T, Tekin U, Yaren A, et al. 5-fluorouracil increases the number and complexity of premature complexes in the heart: a prospective study using ambulatory ECG monitoring. Int J Clin Pract. 2007;61(5):795-801.
- 122. Kishi S, Yoshida A, Yamauchi T, Tsutani H, Lee JD, Nakamura T, et al. Torsade de pointes associated with hypokalemia after anthracycline treatment in a patient with acute lymphocytic leukemia. Int J Hematol. 2000;71(2):172-9.
- 123. Lipshultz SE, Alvarez JA, Scully RE. Anthracycline associated cardiotoxicity in survivors of childhood cancer. Heart. 2008;94(4):525-33.
- 124. Strevel EL, Ing DJ, Siu LL. Molecularly targeted oncology therapeutics and prolongation of the QT interval. J Clin Oncol. 2007;25(22):3362-71.
- 125. Gupta A, Lawrence AT, Krishnan K, Kavinsky CJ, Trohman RG. Current concepts in the mechanisms and management of drug-induced QT prolongation and torsade de pointes. Am Heart J. 2007;153(6):891-9.
- 126. Kleinman ME, Chameides L, Schexnayder SM, Samson RA, Hazinski MF, Atkins DL, et al; American Heart Association. Pediatric advanced life support: 2010 American Heart Association Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care. Pediatrics. 2010;126(5):e1361-99.
- 127. Berg RA, Samson RA, Berg MD, Chapman FW, Hilwig RW, Banville I, et al. Better outcome after pediatric defibrillation dosage than adult dosage in a swine model of pediatric ventricular fibrillation. J Am Coll Cardiol. 2005;45(5):786-9.
- 128. Andrew M. Tromboembolic disease in children: a new epidemic in tertiary care peditarics. Pediatr Res. 1999;45(5):764.
- 129. Schneppenheim R, Greiner J. Thrombosis in infants and children. Hematology Am Soc Hematol Educ Program. 2006:86-96.
- 130. Athale U, Siciliano S, Thabane L, Pai N, Cox S, Lathia A, et al. Epidemiology and clinical risk factors predisposing to thromboembolism in children with cancer. Pediatr Blood Cancer. 2008;51(6):792-7.
- 131. Caruso V, Iacoviello L, Di Castelnuovo A, Storti S, Mariani G, de Gaetano G, et al. Thrombotic complications in childhood acute lymphoblastic leukemia: a meta-analysis of 17 prospective studies comprising 1752 pediatric patients. Blood. 2006;108(7):2216-22.
- 132. Paz-Priel I, Long L, Helman LJ, Mackall CL, Wayne AS. Thromboembolic events in children and young adults with pediatric sarcoma. J Clin Oncol. 2007;25(12):1519-24.
- 133. Biss TT, Brandão LR, Kahr WH, Chan AK, Williams S. Clinical features and outcome of pulmonary embolism in children. Br J Haematol. 2008;142(5):808-18.
- 134. Avila Ml, Brandão LR. Thrombotic events in children with cancer: a pratical review. Toronto (Canada). [Access in 2011 Oct 10]. Available from: http://www.cure4kids.org/private/oncochap/ocrev_227/onco-ch47_Throm_event.pdf
- 135. Athale UH, Nagel K, Khan AA, Chan AK. Thromboembolism in children with lymphoma. Thromb Res. 2008;122(4):459-65.
- 136. Mitchell LG, Andrew M, Hanna K, Abshire T, Halton J, Anderson R, et al. Prophylactic Antithrombin Replacement in Kids with Acute Lymphoblastic Leukemia Treated with Asparaginase Group (PARKAA). A prospective cohort study determining the prevalence of thrombotic events in children with acute lymphoblastic leukemia and a central venous line who are treated with L-asparaginase: results of the Prophylactic Antithrombin Replacement in Kids with Acute Lymphoblastic Leukemia Treated with Asparaginase (PARKAA) Study. Cancer. 2003;97(2):508-16.
- 137. Falanga A, Marchetti M. Venous thromboembolism in the hematologic malignancies. J Clin Oncol. 2009;27(29):4848-57.
- 138. Male C, Chait P, Ginsberg JS, Hanna K, Andrew M, Halton J, et al. Comparison of venography and ultrasound for the diagnosis of asymptomatic deep vein thrombosis in the upper body in children: results of the PARKAA study. Prophylactic Antithrombin Replacement in Kids with ALL treated with Asparaginase. Thromb Haemost. 2002;87(4):593-8.
- 139. Monagle P, Chalmers E, Chan A, De Veber G, Kirkham F, Massicotte P, et al. Antithrombotic therapy in neonates and children: American College of Chest physicians Evidence-Based Clinical Practice Guidelines (8th Edition). Chest. 2008;133(6 Suppl):887S-968S.
- 140. McGill HC Jr, McMahan CA, Zieske AW, Tracy RE, Malcom GT, Herderick EE, et al. Association of coronary heart disease risk factors with microscopic qualities of coronary atherosclerosis in youth. Circulation. 2000;102(4):374-9.
- 141. Cole JH, Miller JI 3rd, Sperling LS, Weintraub WS. Long-term follow up of coronary artery disease presenting in young adults. J Am Coll Cardiol. 2003;41(4):521-8.
- 142. McGill HC Jr, McMahan CA, Herderic EE, Zieske AW, Malcom GT, Tracy RE, et al; Pathobiological Determinants of Atherosclerosis in Youth (PDAY) Research Group. Obesity accelerates the progression of coronary atherosclerosis in young man. Circulation. 2002;105(23):2712-8.
- 143. Oeffinger KC, Tonorezos ES. The cancer is over, now what?: Understanding risk, changing outcomes. Cancer. 2011;117(10 Suppl):2250-7.
- 144. Aleman BM, van den Bell-Dusebout AW, Klokman WJ, Van't Veer MB, Bartelink H, van Leeuwen FE. Long-term cause-specific mortality of patient treated for Hodgkin's disease. J Clin Oncol. 2003;21(18):3431-9.
- 145. Galper SL, Yu JB, Mauch PM, Strasser JF, Silver B, Lacasce A, et al. Clinically significant cardiac disease in patients with Hodgkin lymphoma treated with mediastinal irradiation. Blood. 2011;117(2):412-8.
- 146. Heidenreich PA, Kapoor JR. Radiation induced heart disease: systemic disorders in heart disease. Heart. 2009;95(3):252-8.
- 147. Lee PJ, Mallik R. Cardiovascular effects of radiation therapy: practical approach to radiation therapy-induced heart disease. Cardiol Rev. 2005;13(2):80-6.
- 148. Ghosh N, Chow CM, Korley V, Chisholm R. An usual case of chronic coronary artery dissection: did cisplatin play a role? Can J Cardiol. 2008;24(10):795-7.
- 149. Haugnes HS, Wethal T, Aass N, Dahl O, Klepp O, Langberg CW, et al. Cardiovascular risk factors and morbidity in long-term survivors of testicular cancer: a 20 year follow-up study. J Clin Oncol. 2010;28(30):4649-57.
- 150. Cerny J, Hassan A, Smith C, Piperdi B. Coronary vasospasm with myocardial stunning in a patient with colon cancer receiving adjuvant chemotherapy with FOLFOX regimen. Clin Colorectal Cancer. 2009;8(1):55-8.
- 151. Doughty M, Mehta R, Buckman D, Das S, Karavite D, Tsai T, et al. Acute myocárdical infarction in the young -- The University of Michigan experience. Am Heart J. 2002;143(1):56-62.
- 152. Sarda L, Colin P, Boccara F, Daou D, Lebtahi R, Faraggi M, et al. Myocarditis in patients with clinical presentation of myocardial infarction and normal coronary angiograms. J Am Coll Cardiol. 2001;37(3):786-92.
- 153. Ewer MS, Yeh E. Cancer and the heart. Leviston (NY): BC Decker Inc; 2006.
- 154. Atik, E. Tumores cardíacos em cardiología pediátrica. In: Góngora GF, Reyes NS, Moreno JF. (org.). Cardiología pediátrica. Bogotá: McGraw-Hill Interamericana SA; 2003. p. 747-55.
- 155. Ramyar A, Shafiei M, Moazzami K, Rezaei N. Severe valvular toxicity and pericarditis early after radiation therapy in a patient treated for Hodgkin's lymphoma. Turk J Pediatr. 2010;52(4):423-5.
- 156. Simbre VC, Duffy SA, Dadlani GH, Miller TL, Lipshultz SE. Cardiotoxicity of cancer chemotherapy: implications for children. Paediatr Drugs. 2005;7(3):187-202.
- 157. Hancock SL, Donaldson SS, Hoppe RT. Cardiac disease following treatment of Hodgkin's disease in children and adolescents. J Clin Oncol. 1993;11(7):1208-15.
- 158. Dahl C, Fuursted K, Schroder H. A paediatric case of Candida pericarditis and eosophagus stricture during treatment for acute lymphatic leukaemia. Acta Oncol. 2007;46(6):859-61.
- 159. Galderisi M, Marra F, Esposito R, Lomoriello VS, Pardo M, de Divitiis O. Cancer therapy and cardiotoxicity: the need of serial Doppler echocardiography. Cardiovasc Ultrasound. 2007,5:4.
- 160. Porea TJ, Dreyer ZE, Bricker JT, Mahoney DH Jr. Evaluation of left ventricular function in asymptomatic children about to undergo antracycline-based chemotherapy for acute leukemia: an outcome study. J Pediatr Hematol Oncol. 2001;23(7):420-3.
- 161. van Dalen EC, Caron HN, Dickinson HO, Kremer LC. Cardioprotective interventions for cancer patients receiving anthracyclines. Cochrane Database Syst Rev. 2011 jun 15(6):CD003917.
- 162. Smith LA, Cornelius VR, Plummer CJ, Levitt G, Verrill M, Canney P, et al. Cardiotoxicity of anthracycline agents for the treatment of cancer: systematic review and meta-analysis of randomized controlled trials. BMC Cancer. 2010;10:337.
- 163. Cardinale D, Colombo A, Cipolla CM. Prevention and treatment of cardiomyopathy and heart failure in patients receiving cancer chemotherapy. Curr Treat Options Cardiovasc Med. 2008;10(6):486-95.
- 164. Harake D, Franco VI, Henkel JM, Miller TL, Lipshultz SE. Cardiotoxicity in childhood cancer survivors: strategies for prevention and management. Future Cardiol. 2012;8(4):647-70.
- 165. Wexler LH, Andrich MP, Venzon D, Berg SL, Weaver-McClure L, Chen CC, et al. Randomized trial of the cardioprotective agent ICRF-187 in pediatric sarcoma patients treated with doxorubicin. J Clin Oncol. 1996;14(2):362-72.
- 166. Lipshultz SE, Scully RE, Lipsitz SR, Sallan SE, Silverman LB, Miller TL, Barry EV, et al. Assessment of dexrazoxane as a cardioprotectant in doxorubicin-treated children with high-risk acute lymphoblastic leukaemia: long-term follow-up of a prospective, randomised, multicentre trial. Lancet Oncol. 2010;11(10):950-61.
- 167. Vrooman LM, Neuberg DS, Stevenson KE, Asselin BL, Athale UH, Clavell L, et al. The low incidence of secondary acute myelogenous leukaemia in children and adolescents treated with dexrazoxane for acute lunphpblastic leulaemia: a report from the Dana-Farber Cancer Institute ALL Consortium. Eur J Cancer. 2011;47(9):1373-9.
- 168. Barry EV, Vrooman LM, Dahlberg SE, Neuberg DS, Asselin BL, Athale UH, et al. Absence of secondary malignant neoplasms in children with high-risk acute lymphoblastic leukemia treated with dexrazoxane. J Clin Oncol. 2008;26(7):1106-11.
- 169. Lipshultz SE, Lipsitz SR, Orav EJ. Dexrazoxane-associated risk for secondary malignancies in pediatric Hodgkin's disease: a claim without compelling evidence. J Clin Oncol. 2007;25(21):3179.
- 170. Hellmann K. Dexrazoxane-associated risk for secondary malignancies in pediatric Hodgkin's disease: a claim without evidence. J Clin Oncol. 2007;25(29):4689-90.
- 171. Bryant J, Picot J, Levitt G, Sullivan I, Baxter L, Clegg A. Cardioprotection against the toxic effects of anthracyclines given to children with cancer: a systematic review. Health Technol Assess. 2007;11(27):iii, ix-x,1-84.
- 172. Paiva MG, Petrilli AS, Moisés VA, Macedo CR, Tanaka C, Campos O. Cardioprotective effect of dexrazoxane during treatment with doxorubicin: a study using low-dose dobutamine stress echocardiography. Pediatr Blood Cancer. 2005;45(7):902-8.
- 173. van Dalen EC, van den Berg H, Raphaël MF, Caron HN, Kremer LC. Should anthracyclines and dexrazoxane be used for children with cancer? Lancet Oncol. 2011;12(1):12-3.
- 174. Siviero-Miachon AA, Spinola-Castro AM, Guerra-Junior G. Adiposity in childhood cancer survivors: insights into obesity physiopathology. Arq Bras Endocrinol Metabol. 2009;53(2):190-200.
- 175. Srinivasan S, Ogle GD, Garnett SP, Briody JN, Lee JW, Cowell CT. Features of the metabolic syndrome after childhood craniopharyngioma. J Clin Endocrinol Metab. 2004;89(1):81-6.
- 176. Siviero-Miachon AA, Spinola-Castro AM, Guerra-Junior G. Detection of metabolic syndrome features among childhood cancer survivors: a target to prevent disease. Vasc Health Risk Manag. 2008;4(4):825-36.
- 177. Spinola-Castro AM, Siviero-Miachon AA, Guerra-Junior G, geloneze-Neto B. Insulin resistance in childhood cancer survivors: a link between metabolic syndrome features. In: Yao EB. (editor). Insulin resistance: new research. New York: Nova Science Publishers; 2009. p. 235-51.
- 178. Link K, Moëll C, Garwicz S, Cavallin-Ståhl E, Björk J, Thilén U, et al. Growth hormone deficiency predicts cardiovascular risk in young adults treated for acute lymphoblastic leukemia in childhood. J Clin Endocrinol Metab. 2004;89(10):5003-12.
- 179. Maradia K, Guglin M. Pharmacologic prevention of anthracycline-induced cardiomyopathy. Cardiol Rev. 2009;17(5):243-52. Erratum in Cardiol Rev. 2009;17(6):299.
- 180. Colao A, Di Somma C, Rota F, Di Maio S, Salerno M, Klain A, et al. Common carotid intima-media thickness in growth hormone (GH)-deficient adolescents: a prospective study after GH withdrawal and restarting GH replacement. J Clin Endocrinol Metab. 2005;90(5):2659-65.
- 181. Siviero-Miachon AA, Monteiro CM, Pires LV, Rozalem AC, Silva NS, Petrilli AS, et al. Early features of metabolic syndrome in pediatric post-cancer survivors: outcomes in adolescents and young adults treated for childhood medulloblastoma. Arq Bras Endocrinol Metabol. 2011;55(8):653-60.
- 182. Kavey RE, Allada V, Daniels SR, Hayman LL, McCrindle BW, Newburger JW, et al; American Heart Association Expert Panel on Population and Prevention Science; American Heart Association Council on Cardiovascular Disease in the Young; American Heart Association Council on Epidemiology and Prevention; American Heart Association Council on Nutrition, Physical Activity and Metabolism; American Heart Association Council on High Blood Pressure Research; American Heart Association Council on Cardiovascular Nursing; American Heart Association Council on the Kidney in Heart Disease; Interdisciplinary Working Group on Quality of Care and Outcomes Research. Cardiovascular risk reduction in high-risk pediatric patients: a scientific statement from the American Heart Association Expert Panel on Population and Prevention Science; the Councils on Cardiovascular Disease in the Young, Epidemiology and Prevention, Nutrition, Physical Activity and Metabolism, High Blood Pressure Research, Cardiovascular Nursing, and the Kidney in Heart Disease; and the Interdisciplinary Working Group on Quality of Care and Outcomes Research: endorsed by the American Academy of Pediatrics. Circulation. 2006;114(24):2710-38.
- 183. Meacham LR, Chow EJ, Ness KK, Kamdar KY, Chen Y, Yasui Y, et al. Cardiovascular risk factors in adult survivors of pediatric cancer--a report from the childhood cancer survivor study. Cancer Epidemiol Biomarkers Prev. 2010;19(1):170-81.
- 184. Van Waas M, Neggers SJ, Pieters R, van den Heuvel-Eibrink MM. Components of the metabolic syndrome in 500 adult long-term survivors of childhood cancer. Ann Oncol. 2010;21(5):1121-6.
- 185. Gottlieb SS, Abraham W, Butler J, Forman DE, Loh E, Massie BM, et al. The prognostic importance of different definitions of worsening renal function in congestive heart failure. J Card Fail. 2002;8(3):136-41.
- 186. Bailey D, Phan V, Litalien C, Ducruet T, Mérouani A, Lacroix J, et al. Risk factors of acute renal failure in critically ill children: a prospective descriptive epidemiological study. Pediatr Crit Care Med. 2007;8(1):29-35.
- 187. Akcan-Arikan A, Zappitelli M, Loftis LL, Washburn KK, Jefferson LS, Goldstein SL. Modified RIFLE criteria in critically ill children with acute kidney injury. Kidney Int. 2007;71(10):1028-35.
- 188. Dormans TP, Gerlag PG, Russel FG, Smits P. Combination diuretic therapy in severe congestive heart failure. Drugs. 1998;55(2):165-72.
- 189. Ronco C, Haapio M, House AA, Anavekar N, Bellomo R. CardiorrenalCardiorrenal syndrome. J Am Coll Cardiol. 2008;52(19):1527-39.
- 190. Price JF, Mott AR, Dickerson HA, Jefferies JL, Nelson DP, Chang AC, et al. Worsening renal function in children hospitalized with decompensated heart failure: evidence for a pediatric cardiorenal syndrome? Ped Crit Care Med. 2008;9(3):279-84.
- 191. Hillege HL, Girbes AR, de Kam PJ, Boomsma F, de Zeeuw D, Charlesworth A, et al. Renal function, neurohormonal activation, and survival in patients with chronic heart failure. Circulation. 2000;102(2):203-10.
- 192. Dries DL, Exner DV, Domanski MJ, Greenberg B, Stevenson LW. The prognostic implications of renal insufficiency in asymptomatic and symptomatic patients with left ventricular systolic dysfunction. J Am Coll Cardiol. 2000;35(3):681-9.
- 193. Price JF, Goldstein SL. Cardiorenal syndrome in children with heart failure. Curr Heart Fail Rep. 2009;6(3):191-8.
- 194. Schrier RW, Abraham WT. Hormones and hemodynamics in heart failure. N Engl J Med. 1999;341(8):577-85.
- 195. Bayliss J, Norell M, Canepa-Anelson R, Sutton G, Poole-Wilson P, et al. Untreated heart failure: clinical and neuroendocrine effects of introducing diuretics. Br Heart J. 1987;57(1):17-22.
- 196. Butler J, Forman DE, Abraham WT, Gottlieb SS, Loh E, Massie BM, et al. Relationship between heart failure treatment and development of worsening renal function among hospitalized patients. Am Heart J. 2004;147(2):331-8.
- 197. Ronco C, McCullough PA, Anker SD, Anand I, Aspromonte N, Bagshaw SM, et al.; Acute Dialysis Quality Initiative (ADQI) consensus group. Cardiorenal syndromes: an executive summary from the consensus conference of the Acute Dialysis Quality Initiative (ADQI). Contrib Nephrol. 2010;165:54-67.
- 198. Abreu KL, Silva Junior GB, Daher EF. Novas classificações RIFLE e AKIN: fatores preditivos de gravidade da lesão renal aguda. In: Cruz HM, Kirsztajn GM, Barros RT. (editores). Atualidades em nefrologia. 11a ed. São Paulo: Sarvier; 2010. p 110-8.
- 199. Goldstein SL, Somers MJ, Baum MA, Symons JM, Brophy PD, Blowey D, et al. Pediatric patients with multi-organ dysfunction syndrome receiving continuous renal replacement therapy. Kidney Int. 2005;67(2):653-8.
- 200. Bresolin NL. Classificação da insuficiência renal aguda. In: Piva JP, de Carvalho WB. (editores). PROTIPED - Programa de atualização em terapia intensiva pediátrica. Ciclo 2, Módulo 4. Porto Alegre: Artmed; 2011. p. 53-74.
- 201. Hoste EA, Damen J, Vanholder RC, Lameire NH, Delanghe JR, Van den Hauwe K, et al. Assessment of renal function in recently admitted critically ill patients with normal serum creatinine. Nephrol Dial Transplant. 2005;20(4):747-53.
- 202. Luciani GB, Nichani S, Chang AC, Wells WJ, Newth CJ, Starnes VA. Continuous versus intermittent furosemide infusion in critically ill infants after open heart operations. Ann Thorac Surg. 1997;64(4):1133-9.
- 203. Salvador DR, Rey NR, Ramos GC, Punzalan FE. Continuous infusion versus bolus injection of loop diuretics in congestive heart failure. Cochrane Database Syst Rev. 2005 Jul 20;(3):CD003178.
- 204. Liang KV, Williams AW, Greene EL, Redfield MM. Acute decompensated heart failure and the cardiorenal syndrome. Crit Care Med. 2008;36(1 Suppl):S75-88.
- 205. Swan SK. Diuretic strategies in patients with renal failure. Drugs. 1994;48(3):380-5.
- 206. Colucci WS, Elkayam U, Horton DP, Abraham WT, Bourge RC, Johnson AD, et al. Intravenous nesiritide, a natriuretic peptide, in the treatment of decompensated congestive heart failure. Nesiritide Study Group. N Engl J Med. 2000;343(4):246-53.
- 207. Moffett BS, Mott AR, Nelson DP, Goldstein SL, Jefferies JL. Renal effects of fenoldopam in critically ill pediatric patients: a retrospective review. Pediatr Crit Care Med. 2008;9(4):403-6.
- 208. Lipshultz SE, Rifai N, Dalton VM, Levy DE, Silverman LB, Lipsitz SR, et al. The effect of dexrazoxane on myocardial injury in doxorubicin-treated children with acute lymphoblastic leukemia. N Engl J Med. 2004;351(2):145-53.
- 209. Cardinale D, Sandri MT, Colombo A, Colombo N, Boeri M, Lamantia G, et al. Prognostic value of troponin I in cardiac risk stratification of cancer patients undergoing high-dose chemotherapy. Circulation. 2004;109(22):2749-54.
- 210. Nousiainen T, Jantunen E, Vanninen E, Remes J, Vuolteenaho O, Hartikainen J. Natriuretic peptides as markers of cardiotoxicity during doxorubicin treatment for non-Hodgkin's lymphoma. Eur J Haematol. 1999;62(2):135-41.
- 211. Januzzi JL Jr. The role of natriuretic peptide testing in guiding chronic heart failure management: review of available data and recommendations for use. Arch Cardiovasc Dis. 2012;105(1):40-50.
- 212. Lipshultz SE, Miller TL, Scully RE, Lipsitz SR, Rifai N, Silverman LB, et al. Changes in cardiac biomarkers during doxorubicin treatment of pediatric patients with high-risk acute lymphoblastic leukemia: associations with long-term echocardiographic outcomes. J Clin Oncol. 2012;30(10):1042-9.
- 213. Mulrooney DA, Yeazel MW, Kawashima T, Mertens AC, Mitby P, Stovall M, et al. Cardiac outcomes in a cohort of adult survivors of childhood and adolescent cancer: retrospective analysis of the Childhood Cancer Survivor Study cohort. BMJ. 2009;339:b4606.
- 214. Zhang S, Liu X, Bawa-Khalfe T, Lu LS, Lyu YL, Liu LF, et al. Identification of the molecular basis of doxorubicin-induced cardiotoxicity. Nat Med. 2012;18(11):1639-42.
- 215. Nathan PC, Greenberg ML, Ness KK, Hudson MM, Mertens AC, Mahoney MC, et al. Medical care in long-term survivors of childhood cancer: a report from the childhood cancer survivor study. J Clin Oncol. 2008;26(27):4401-9.
- 216. Grenier MA, Lipshultz SE. Epidemiology of anthracycline cardiotoxicity in children and adults. Semin Oncol. 1998;25(4 Suppl 10):72-85.
- 217. Worsley DF, Alavi A, Aronchick JM, Chen JT, Greenspan RH, Ravin CE. Chest radiographic findings in patients with acute pulmonary embolism: observations from the PIOPED Study. Radiology. 1993;189(1):133-6.
- 218. Pastore CA, Pinho C, Germiniani H, Samesima N, Mano R, et al. Sociedade Brasileira de Cardiologia. Diretrizes da Sociedade Brasileira de Cardiologia sobre análise e emissão de laudos eletrocardiográficos (2009). Arq Bras Cardiol. 2009;93(3 supl.2):1-19.
- 219. TukenovaM, Guibout C, Oberlin O, Doyon F, Mousannif A, Haddy N, et al. Role of cancer treatment in long-term overall and cardiovascular mortality after childhood cancer. J Clin Oncol. 2010;28(8):1308-15.
- 220. Lipshultz SE, Sallan SE. Cardiovascular abnormalities in long-term survivors of childhood malignancy. J Clin Oncol. 1993;11(7):1199-203.
-
221Agency for Healthcare Research and Quality. Long-term follow-up guidelines for survivors of childhood, adolescents, and young adult cancers. children oncology group. National Guideline Clearinghouse. [Access in 2011 Nov 10]. Available from: http://guideline.gov/content.aspx?id=15470
- 222. Karanth NV, Roy A, Joseph M, de Pasquale C, Karapetis C, Koczwara B. Utility of prechemotherapy echocardiographical assessment of cardiac abnormalities. Support Care Cancer. 2011;19(12):2021-6.
- 223. Otto CM. Fundamentos da ecocardiografia clínica. 4Ş ed. Rio de Janeiro: Elsevier Editora Ltda; 2010.
- 224. Lopez L, Colan SD, Frommelt PC, Ensing GJ, Kendall K, Younoszai AK, Lai WW, Geva T. Recommendations for quantification methods during the performance of a pediatric echocardiogram: a report from the Pediatric Measurements Writing Group of the American Society of Echocardiography, Pediatric and Congenital Heart Disease Council. J Am Soc Echocardiogr. 2010;23(5):465-95.
- 225. Di Lisi D, Bonura F, Macaione F, Cuttitta F, Peritore A, Meschisi M, et al. Chemotherapy-induced cardiotoxicity: role of the conventional echocardiography and the tissue Doppler. Minerva Cardioangiol. 2011;59(4):301-8.
- 226. Mohan JC, Tomar D, Mohan V. Prime time use of tissue Doppler echocardiography: what have we gained? Indian Heart J. 2008;60(3 Suppl C):C10-25.
- 227. Ishii M, Tsutsumi T, Himeno W, Eto G, Furui J, Hashino K, et al. Sequential evaluation of left ventricular myocardial performance in children after anthracycline theraphy. Am J Cardiol. 2000;86(11):1279-81.
- 228. Karakurt C, Koçak G, Ozgen U. Evaluation of the left ventricular function with tissue tracking and tissue Doppler echocardiography in pediatric malignancy survivors after anthracycline therapy. Echocardiography. 2008;25(8):880-7.
- 229. de Matos Neto RP, Petrilli AS, Silva CM, Campos Filho O, Oporto VM, Gomes L de F, et al. Left ventricular systolic function assessed by echocardiography in children and adolescents with osteosarcoma treated with doxorubicin alone or in combination with dexrazoxane. Arq Bras Cardiol. 2006;87(6):763-71.
- 230. Marwick TH. Measurement of strain and strain rate by echocardiography: ready for prime time? J Am Coll Cardiol. 2006;47(7):1313-27.
- 231. Teske AJ, De Boeck BW, Melman PG, Sieswerda GT, Doevendans PA, Cramer MJ. Echocardiographic quantification of myocardium function using tissue deformation imaging, a guide to image acquisition and analysis using tissue Doppler and speckle tracking. Cardiovasc Ultrasound. 2007;5:27.
- 232. Tsai HR, Gjesdal O, Wethal T, Haugaa KH, Fosså A, Fosså SD, et al. Left ventricular function assessed by two-dimensional speckle tracking echocardiography in long-term survivors of Hodgkin's lymphoma treated by mediastinal radiotherapy with or without anthracycline therapy. Am J Cardiol. 2011;107(3):472-7.
- 233. Marwick TH, Leano RL, Brown J, Sun JP, Hoffmann R, Lysyansky P, et al. Myocardial strain measurement with 2-dimensional speckle-tracking echocardiography. JACC Cardiovasc Imaging. 2009;2(1):80-4.
- 234. Mavinkurve-Groothuis AM, Groot-Loonen J, Marcus KA, Bellersen L, Feuth T, Bökkerink JP, et al. Myocardial strain and strain rate in monitoring subclinical heart failure in asymptomatic long-term survivors of childhood cancer. Ultrasound Med Biol. 2010;36(11):1783-91.
- 235. Guimarães-Filho F, Tan D, Braga J, Rodrigues A, Waib P, Matsubara B. Ventricular systolic reserve in asymptomatic children previously treated with low doses of anthracyclines. Am J Cardiol. 2007;100(8):1303-6.
- 236. De Caro E, Smeraldi A, Trocchio G, Calevo M, Hanau G, Pongiglione G. Subclinical cardiac dysfunction and exercise performance in childhood cancer survivors. Pediatr Blood Cancer. 2011;56(1):122-6.
- 237. De Caro E, Fioredda F, Calevo MG, Smeraldi A, Saitta M, Hanau G, et al. Exercise capacity in apparently healthy survivors of cancer. Arch Dis Child. 2006;91(1):47-51.
- 238. Meneghelo RS, Araújo CG, Stein R, Mastrocolla LE, Albuquerque PF, Serra SM, et al. Sociedade Brasileira de Cardiologia. III Diretrizes da Sociedade Brasileira de Cardiologia sobre teste ergométrico. Arq Bras Cardiol. 2010;95(5 supl.1):1-26.
- 239. Cumming GR, Everatt D, Hastman L. Bruce treadmill test in children: normal values in a clinic population. Am J Cardiol. 1978;41(1):69-75.
- 240. Cumming GR. Maximal exercise capacity of children with heart defects. Am J Cardiol. 1978;42(4):613-9.
- 241. Barbosa e Silva O, Saraiva LC, Sobral Filho DC. Teste ergométrico em crianças e adolescentes: maior tolerância ao esforço com o protocolo em rampa. Arq Bras Cardiol. 2007;89(6):391-7.
- 242. Velensek V, Mazic U, Krzisnik C, Demsar D, Jazbec J, Jereb B. Cardiac damage after treatment of childhood cancer: a long-term follow-up. BMC Cancer. 2008;8:141.
- 243. Stevinson C, Lawlor DA, Fox KR. Exercise interventions for cancer patients: systematic review of controlled trials. Cancer Causes Control. 2004;15(10):1035-56.
- 244. van Brussel M, Takken T, Lucia A, van der Net J, Helders PJ. Is physical fitness decreased in survivors of childhood leukemia? A systematic review. Leukemia. 2005;19(1):13-7.
- 245. Landier W, Bhatia S, Eshelman DA, Forte KJ, Sweeney T, Hester AL, et al. Development of risk-based guidelines for pediatric cancer survivors: the Children's Oncology Group Long-Term Follow-Up Guidelines from the Children's Oncology Group Late Effects Committee and Nursing Discipline. J Clin Oncol. 2004;22(24):4979-90.
- 246. Stein PD, Woodard PK, Weg JG, Wakefield TW, Tapson VF, Sostman HD, et al; PIOPED II Investigators. Diagnostic pathways in acute pulmonary embolism: recommendations of the PIOPED II Investigators. Radiology. 2007;242(1):15-21.
- 247. Van Cutsem E, Hoff PM, Blum JL, Abt M, Osterwalder B. Incidence of cardiotoxicity with the oral fluoropyrimidine capecitabine is typical of that reported with 5-fluorouracil. Ann Oncol. 2002;13(3):484-5.
- 248. Cranney GB, Lotan CS, Dean L, Baxley W, Bouchard A, Pohost GM. Left ventricular volume measurement using cardiac axis nuclear magnetic resonance imaging: validation by calibrated ventricular angiography. Circulation. 1990;82(1):154-63.
- 249. Chuang ML, Hibberd MG, Salton CJ, Beaudin RA, Riley MF, Parker RA, et al. Importance of imaging method over imaging modality in noninvasive determination of left ventricular volumes and ejection fraction: assessment by two- and three-dimensional echocardiography and magnetic resonance imaging J Am Coll Cardiol. 2000;35(2):477-84.
- 250. Stein PD, Woodard PK, Hull RD, Kayali F, Weg JG, Olson RE, et al. Gadolinium-enhanced magnetic resonance angiography for detection of acute pulmonary embolism: an in-depth review. Chest. 2003;124(6):2324-8.
- 251. Benjelloun H, Cranney GB, Kirk KA, Blackwell GG, Lotan CS, Pohost GM. Interstudy reproducibility of biplane cine nuclear magnetic resonance measurements of left ventricular function. Am J Cardiol. 1991;67(16):1413-20.
- 252. Panjrath GS, Jain D. Monitoring chemotherapy-induced cardiotoxicity: role of cardiac nuclear imaging. J Nucl Cardiol. 2006;13(3):415-26.
- 253. Agostini D, Verberne HJ, Burchert W, Knuuti J, Povinec P, Sambuceti G, et al. I-123-mIBG myocardial imaging for assessment of risk for a major cardiac event in heart failure patients: insights from a retrospective European multicenter study. Eur J Nucl Med Mol Imaging. 2008;35(3):535-46.
- 254. Yamashina S, Yamazaki J. Neuronal imaging using SPECT. Eur J Nucl Med Mol Imaging. 2007;34 Suppl 1:S62-73.
- 255. Maunoury C, Agostini D, Acar P, Antonietti T, Sidi D, Bouvard G, et al. Impairment of cardiac neuronal function in childhood dilated cardiomyopathy: an 123I-MIBG scintigraphic study. J Nucl Med. 2000;41(3):400-4.
- 256. Chirumamilla A, Travin MI. Cardiac applications of 123I-mIBG imaging. Semin Nucl Med. 2011;41(5):374-87.
- 257. Hattori N, Tamaki N, Hayashi T, Masuda I, Kudoh T, Tateno M, et al. Regional abnormality of iodine-123-MIBG in diabetic hearts. J Nucl Med. 1996;37(12):1985-90.
- 258. Thom AF, Smanio PE. (editores). Medicina nuclear em cardiologia. São Paulo: Atheneu; 2007.
- 259. Bryant J, Picot J, Baxter L, Levitt G, Sullivan I, Clegg A. Clinical and cost-effectiveness of cardioprotection against the toxic effects of anthracyclines given to children with cancer: a systematic review. Br J Cancer. 2007;96(2):226-30.
- 260. Corbett JR, Akinboboye OO, Bacharach SL, Borer JS, Botvinick EH, DePuey EG, et al. Equilibrium radionuclide angiocardiography. J Nucl Cardiol. 2006;13(6):e56-79.
- 261. Lewis L, Silver MD. Adverse effects of drugs on the cardiovascular system. In: Silver M, Gotlieb AI, Schoen F. (editors). Cardiovascular pathology. 3rd ed. Philadelphia: Churchill Livingstone; 2001. p.541-61.
- 262. Albini A, Donatelli F, Noonan D, D'Elios MM, Prisco D. Bringing new players into the field: onco-pharmacovigilance in the era of cardio-oncology. Intern Emerg Med. 2012;7(2):99-101.
- 263. Lipshultz SE. Cancer treatment-related cardiotoxicities. In: Shaddy RE, Wernovsky G. (editors). Pediatric heart failure. Boca Raton: Taylor & Franci; 2005. p. 665-737.
- 264. Trachtenberg BH, Landy DC, Franco VI, Henkel JM, Pearson EJ, Miller TL, et al. Anthracycline-associated cardiotoxicity in survivors of childhood cancer. Pediatr Cardiol. 2011;32(3):342-53.
- 265. Tantawy AA, Elmasry OA, Shaaban M, Toaima DN, El Shahat AM. Radionuclide ventriculography detects early anthracycline cardiotoxicity in children with Hodgkin lymphoma. J Pediatr Hematol Oncol. 2011;33(4):e132-7.
- 266. Baughman KL. Cardiomyopathies, myocarditis, and pericardial disease. In: Braunwald E, Abelmann W. Essential atlas of heart disease. Philadelphia: McGraw Hill; 2001. p. 12-9.
- 267. Mason JW. Techniques for right and left ventricular endomyocardial biopsy. Am J Cardiol. 1978;41(5):887-92.
- 268. Cooper LT, Baughman KL, Feldman AM, Frustaci A, Jessup M, Kuhl U, et al. American Heart Association; American College of Cardiology; European Society of Cardiology. The role of endomyocardial biopsy in the management of cardiovascular disease: a scientific statement from the American Heart Association, the American College of Cardiology, and the European Society of Cardiology. Circulation. 2007;116(19):2216-33.
- 269. Semelka RC, Tomei E, Wagner S, Mayo J, Caputo G, O'Sullivan M, et al. Interstudy reproducibility of dimensional and functional measurements between cine magnetic resonance studies in the morphologically abnormal left ventricle. Am Heart J. 1990;119(6):1367-73.
- 270. Watts RG, George M, Johnson WH Jr. Pretreatment and routine echocardiogram monitoring during chemotherapy for anthracycline-induced cardiotoxicity rarely identifies significant cardiac dysfunction or alters treatment decisions: a 5-year review at a single pediatric oncology center. Cancer. 2012;118(7):1919-24.
- 271. Fallah-Rad N, Walker JR, Wassef A, Lytwyn M, Bohonis S, Fang T, et al. The utility of cardiac biomarkers, tissue velocity and strain imaging, and cardiac magnetic resonance imaging in predicting early left ventricular dysfunction in patients with human epidermal growth factor receptor II-positive breast cancer treated with adjuvant trastuzumab therapy. J Am Coll Cardiol. 2011;57(22):2263-70.
- 272. Fleisher LA, Beckman JA, Brown KA, Calkins H, Chaikof EL, Fleischmann KE, et al; American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines; American Society of Echocardiography; American Society of Nuclear Cardiology; Heart Rhythm Society; Society of Cardiovascular Anesthesiologists; Society for Cardiovascular Angiography and Interventions; Society for Vascular Medicine; Society for Vascular Surgery. 2009ACCF/AHA focused update on perioperative beta blockade incorporated into the ACC/AHA 2007 Guidelines on peraoperative cardiovascular evaluation and care for noncardiac surgery. J Am Coll Cardiol. 2009;54(22):e13-e118.
- 273. Latham GJ, Grenberg RS. Anesthetic consideration for the pediatric oncology patient- part 2: systems-based approach to anesthesia. Pediatr Anaesth. 2010;20(5):396-420.
- 274. Evaluation and preparation of pediatric patients undergoing anesthesia. American Academy of Pediatrics. Section on Anesthesiology. Pediatrics. 1996;98(3 Pt 1):502-8.
- 275. American Society of Anesthesiologists Task Force on Preanesthesia Evaluation. Practice advisory for preanesthesia evaluation: a report by the American Society of Anesthesiologists Task Force on Preanesthesia Evaluation. Anesthesiology. 2002;96(2):485-96.
- 276. Latham GJ, Grenberg RS. Anesthetic considerations for the pediatric oncology patient - Part 3: pain, cognitive dysfunction, and preoperative evaluation. Pediatr Anesth. 2010;20(6):479-89.
- 277. Rheingold SR, Lange BJ. Oncologic emergencies. In: Pizzo PA, Poplack DG. (editors). Principles and practice of pediatric oncology. 5th ed. Philadelphia: Lippincott Williams & Wilkins; 2006. p. 1202-30.
- 278. Ricketts RR. Clinical management of anterior mediastinal tumors in children. Semin Pediatr Surg. 2001;10(3):161-8.
- 279. Kaya Z, Weiner DJ, Yilmaz D, Rowan J, Goyal RK. Lung function, pulmonary complications, and mortality after allogeneic blood and marrow transplantation in children. Biol Blood Marrow Transplant. 2009;15(7):817-26.
- 280. Yahalom J, Portlock CS. Long-term cardiac and pulmonary complications of cancer therapy. Hematol Oncol Clin North Am. 2008;22(2):305-18.
- 281. Drew B, Peters C, Rimell F. Upper airway complications in children after bone marrow transplantation. Laryngoscope. 2000;110(9):1446-51.
- 282. Rossi R, Kleta R, Ehrich JH. Renal involvement in children with malignancies. Pediatr Nephrol. 1999;13(2):153-62.
- 283. Dome JS, Perlman EJ, Ritchey ML. Renal tumors. In: Pizzo PA, Poplack DG. (editors). Principles and practice of pediatric oncology. 5th ed. Philadelphia: Lippincott Williams & Wilkins; 2006. p. 905-32.
- 284. Hazar V, Gungor O, Guven AG, Aydin F, Akbas H, Gungor F, et al. Renal function after hematopoietic stem cell transplantation in children. Pediatr Blood Cancer. 2009;53(2):197-202.
- 285. Frisk P, Bratteby LE, Carlson K, Lönnerholm G. Renal function after autologous bone marrow transplantation in children: a long-term prospective study. Bone Marrow Transplant. 2002;29(2):129-36.
- 286. Hastings CA, Lubin BH, Feusner J. Hematologic supportive care for children with cancer. In: Pizzo PA, Poplack DG. (editors). Principles and practice of pediatric oncology. 5th ed. Philadelphia: Lippincott Williams & Wilkins; 2006. p. 1229-31.
- 287. Hockenberry MJ, Hinds PS, Barrera P, Billups C, Rodriguez-Galindo C, Tan M, et al. Incidence of anemia in children with solid tumors or Hodgkin disease. J Pediatr Hematol Oncol. 2002;24(1):35-7.
- 288. Athale UH, Chan AK. Hemorrhagic complications in pediatric hematologic malignancies. Semin Thromb Hemost. 2007;33(4):408-15.
- 289. Green D. Management of bleeding complications of hematologic malignancies. Semin Thromb Hemost. 2007;33(4):427-34.
- 290. Athale UH, Chan AK. Thromboembolic complications in pediatric hematologic malignancies. Semin Thromb Hemost. 2007;33(4):416-26.
- 291. Jhanji S, Lee C, Watson D, Hinds C, Pearse RM. Microvascular flow and tissue oxygenation after major abdominal surgery: association with post -operative complications. Intensive Care Med. 2009;35(4):671-7.
- 292. Miser AW, McCalla J, Dothage JA, Wesley M, Miser JS. Pain as a presenting symptom in children and young adults with newly diagnosed malignancy. Pain. 1987;29(1):85-90.
- 293. Warner DO. Preventing postoperative pulmonary complications: the role of the anesthesiologist. Anesthesiology. 2000;92(5):1467-72.
- 294. Pasquini MC, Wang Z. Current use and outcome of hematopoietic stem cell transplantation: summary slides, 2010. [Access in 2012 Apr 10]. Available from: http://www.cibmtr.org
- 295. Seber A, Bonfim CM, Daudt LE, Gouveia RV, Ginani VC, Mauad M, et al. Indicações de transplante de células-tronco hematopoéticas em pediatria: Consenso apresentado no I Encontro de Diretrizes Brasileiras em Transplante de Células-Tronco Hematopoéticas - Sociedade Brasileira de Transplante de Medula Óssea, Rio de Janeiro, 2009. Rev Bras Hematol Hemoter. 2010;32(3):225-39.
- 296. Tichelli A, Bhatia S, Socié G. Cardiac and cardiovascular consequences after haematopoietic stem cell transplantation. Br J Haematol. 2008;142(1):11-26.
- 297. Tichelli A, Passweg J, Wójcik D, Rovó A, Harousseau JL, Masszi T, et al. Late cardiovascular events after allogeneic hematopoietic stem cell transplantation: a retrospective multicenter study of the Late Effects Working Party of the European Group for Blood and Marrow Transplantation. Haematologica. 2008;93(8):1203-10.
- 298. Norkin M, Ratanatharathor V, Ayash L, Abidi MH, Al-Kadhimi Z, Lum LG, et al. Large pericardial effusion as a complication in adults undergoing SCT. Bone Marrow Transplant. 2011;46(10):1353-6.
- 299. Armenian SH, Sun CL, Mills G, Teh JB, Francisco L, Durand JB, et al. Predictors of late cardiovascular complications in survivors of hematopoietic cell transplantation. Biol Blood Marrow Transplant. 2010;16(8):1138-44.
- 300. Armenian SH, Sun CL, Kawashima T, Arora M, Leisenring W, Sklar CA, et al. Long-term health-related outcomes in survivors of childhood cancer treated with HSCT versus conventional therapy: a report from the Bone Marrow Transplant Survivor Study (BMTSS) and Childhood Cancer Survivor Study (CCSS). Blood. 2011;118(5):1413-20.
- 301. Baker KS, Armenian S, Bhatia S. Long-term consequences of hematopoietic stem cell transplantation: current state of the science. Biol Blood Marrow Transplant. 2010;16(1 Suppl):S90-6.
- 302. Armand P, Kim HT, Cutler CS, Ho VT, Koreth J, Alyea EP, et al. Prognostic impact of elevated pretransplantation serum ferritin in patients undergoing myeloablative stem cell transplantation. Blood. 2007;109(10):4586-8.
- 303. Leung W, Ahn H, Rose SR, Phipps S, Smith T, Gan K, et al. A prospective cohort study of late sequelae of pediatric allogeneic hematopoietic stem cell transplantation. Medicine (Baltimore). 2007;86:215-24.
- 304. Uderzo C, Pillon M, Corti P, Tridello G, Tana F, Zintl F, et al. Impact of cumulative anthracycline dose, preparative regimen and chronic graft-versus-host disease on pulmonary and cardiac function in children 5 years after allogeneic hematopoietic stem cell transplantation: a prospective evaluation on behalf of the EBMT Pediatric Diseases and Late Effects Working Parties. Bone Marrow Transplant. 2007;39(11):667-75.
- 305. Santos MV, Cioni CH, Gouveia RV, Moises VA, Lederman HM, Carvalho AC, et al. Fatores de risco na predição de sinais precoces de aterosclerose em pacientes pediátricos submetidos a transplante de medula óssea. Rev Bras Hematol Hemoter. 2009;31(5):265.
- 306. Mertens AC, Yasui Y, Neglia JP, Potter JD, Nesbit ME Jr, Ruccione K, et al. Late mortality experience in five-year survivors of childhood and adolescent cancer: the Childhood Cancer Survivor Study. J Clin Oncol. 2001;19(13):3163-72.
- 307. Green DM, Hyland A, Chung CS, Zevon MA, Hall BC. Cancer and cardiac mortality among 15-year survivors of cancer diagnosed during childhood or adolescence. J Clin Oncol. 1999;17(10):3207-15.
- 308. Leandro J, Dyck J, Poppe D, Shore R, Airhart C, Greenberg M, et al. Cardiac dysfunction late after cardiotoxic therapy for childhood cancer. Am J Cardiol. 1994;74(11):1152-6.
- 309. Lipshultz SE, Colan SD, Sanders SP, Sallan SE. Cardiac mechanics after growth hormone therapy in pediatric adriamycin recipients (Abstract). Pediatr Res. 1989;(25):153 A.
- 310. Kremer LC, Mulder RL, Oeffinger KC, Bhatia S, Landier W, Levitt G, et al. A worlwide collaboration to harmonize guidelines for the long-term follow-up of chilhood and young adult cancer survivors: a report from the international late effects of Childhood Cancer Guideline Harmonization Group. Pediatr Blood Cancer. 2012 Dec 31. [Epub ahead of print]
- 311. Winn RJ, Botnick WZ. The NCCN Guideline Program: a conceptual framework. Oncology (Williston Park). 1997;11(11A):25-32.
- 312. Nishimura RA, Carabello BA, Faxon DP, Freed MD, Lytle BW, O'Gara PT, et al. ACC/AHA 2008 Guideline update on valvular heart disease: focused update on infective endocarditis: a report of the American college of Cardiology/American Heart Association Task Force on Practice Guidelines endorsed by the Society of Cardiovascular Anesthesiologists, Society for Cardiovascular Angiography and Interventions, and Society of Thoracic Surgeons. Circulation. 2008;118(8):887-96.
- 313. Gualandro DM, Yu PC, Calderaro D, Marques AC, Pinho C, Caramelli B, et al. II Diretriz de Avaliação Perioperatória da Sociedade Brasileira de Cardiologia. Arq Bras Cardiol. 2011;96(3 supl.1):1-68.
- 314. Bhatia S, Lange BJ, Meadows At. Late effects of childhood cancer and its treatment. In: Pizzo PA, Poplack DG. Principles and practice of pediatric oncology. Philadephia, PA: Lippincott Williams & Wilkins; 2006. p. 1490-514.
- 315. San Juan AF, Chamorro-Viña C, Maté-Muñoz JL, Fernández del Valle M, Cardona C, Hernández M, et al. Functional capacity of children with leukemia. Int J Sports Med. 2008;29(2):163-7.
- 316. Adams MJ, Hardenbergh PH, Constine LS, Lipshultz SE. Radiation-associated cardiovascular disease. Crit Rev Oncol Hematol. 2003;45(1):55-75.
- 317. Lipshultz SE, Lipsitz SR, Sallan SE, Dalton VM, Mone SM, Gelber RD, et al. Chronic progressive cardiac dysfunction years after doxorubicin therapy for childhood acute lymphoblastic leukemia. J Clin Oncol. 2005;23(12):2629-36.
- 318. Liu RD, Chinapaw MJ, Huijgens PC, Van Mechelen W. Physical exercise interventions in haematological cancer patients, feasible to conduct but effectiveness to be established: a systematic literature review. Cancer Treat Rev. 2009;35(2):185-92.
- 319. San Juan AF, Wolin K, Lucia A. Physical activity and pediatric cancer survivorship. Recent Results Cancer Res. 2011;186:319-47.
- 320. Wolin KY, Ruiz JR, Tuchman H, Lucia A. Exercise in adult and pediatric hematological cancer survivors: an intervention review. Leukemia. 2010;24(6):1113-20.
- 321. Winter C, Muller C, Hoffmann C, Boss J, Rosenbaum D. Physical activity and childhood cancer. Pediatric Blood Cancer. 2010;54(4):501-10.
- 322. van Weert E, Hoeskstra-Weebers JE, May AM, Korstjens I, Ros WJ, van der Schans CP. The development of an evidence-based physical self-management rehabilitation programme for cancer survivors. Patient Educ Couns. 2008;71(2):169-90.
- 323. Braith RW. Role of exercise in rehabilitation of cancer survivors. Pediatr Blood Cancer. 2005;44(7):595-9.
- 324. Gerber LH, Levinson S, Hicks JE, Gallelli P, Whitehurtst J, Sheib D, et al. Evaluation and management of disability: rehabilitation aspects of cancer. In: DeVita V, Lawrence TS, Rosenberg SA. Cancer: principles & practice of oncology. Philadelphia: Lippincott Williams & Wilkins; 1993. p. 2538-69.
- 325. Rathe M, Carlsen NL, Oxhøj H. Late cardiac effects of anthracycline containing therapy for childhood acute lymphoblastic leukemia. Pediatr Blood Cancer. 2007;15 48(7):663-7.
- 326. Pizzo PA, Poplack DG. Rehabilitation of the child with cancer. In: Pizzo PA, Poplack DG. Principles and practice of pediatric oncology. 6th ed. Philadelphia: Lippincott Williams & Wilkins; 2010.
- 327. van Brussel M, van der Net J, Hulzebos E, Helders PJ, Takken T. The Utrecht approach to exercise in chronic childhood conditions: the decade in review. Pediatr Phys Ther. 2011;23(1):2-14.
- 328. Jãrvelã LS, Niinikoski H, Lahteenmki PM, Heinonen OJ, Kapanen J, Arola M, et al. Physical activity and fitness in adolescent and young adult long-term survivors of childhood acute lymphoblastic leukaemia. J Cancer Surviv. 2010;4(4):339-45.
- 329. João PR, Faria Junior F. Cuidados imediatos no pós-operatório de cirurgia cardíaca. J Pediatr (Rio J). 2003;79(Supl. 2):S213-22.
- 330. Sociedade Brasileira de Cardiologia, Sociedade Brasileira de Hipertensão, Sociedade Brasileira de Nefrologia. V Diretrizes Brasileiras de Monitorização Ambulatorial da Pressão Arterial (MAPA) e III Diretrizes Brasileiras de Monitorização Residencial de Pressão Arterial (MRPA). Arq Bras Cardiol. 2011;97(3 supl.3):1-24.
- 331. Guimarães JI. Normatização dos equipamentos e técnicas para a realização de exames de eletrocardiografia e eletrocardiografia de alta resolução. Arq Bras Cardiol. 2003;80(supl. 5):572-8.
- 332. Jones SA. ECG notes: interpretation and management guide. FA Davies, Philadelphia: FA Davis Company; 2005.
- 333. Harada MJ, Carneiro IA. Cateter venoso periférico de uso intermitente. In: Chaud MN, Peterlini MAS, Harada MJ, Pedreira ML. O cotidiano da prática de enfermagem pediátrica. São Paulo: Editora Atheneu; 1999. p. 155-60.
- 334. Bottomley SJ, Kassner E. Late effects of childhood cancer therapy. J Pediatr Nurs. 2003;18(2):126-33.
- 335. Leonetti N. Descrição do índice de massa corporal em pacientes submetidos a tratamento oncológico na infância. [Tese]. São Paulo: Fundação Antônio Prudente; 2010.
- 336. Demark-Wahnefried W, Werner C, Clipp EC, Guill AB, Bonner M, Jones LW, et al. Survivors of childhood cancer and their guardians. Cancer. 2005;103(10):2171-80.
- 337. Talvensaari KK, Lanning M, Tapanainen P, Knip M. Long-term survivors of childhood cancer have an increased risk of manifesting the metabolic syndrome. J Clin Endocrinol Metab. 1996;81(8):3051-5.
- 338. Gurney JG, Kadan-Lottick NS, Packer RJ, Neglia JP, Sklar CA, Punyko JA, et al. Endocrine and cardiovascular late effects among adult survivors of childhood brain tumors: Childhood Cancer Survivor Study. Cancer. 2003;97(3):663-73.
- 339. Sociedade Brasileira de Cardiologia. Departamento de Aterosclerose. I Diretriz de prevenção da aterosclerose na infância e na adolescência da Sociedade Brasileira de Cardiologia. Arq Bras Cardiol. 2005;85(supl 6):1-35.
- 340. Sposito AC, Caramelli B, Fonseca FA, Bertolami MC, Afiune Neto A, Souza AD, et al.; Sociedade Brasileira de Cardiologia. IV Diretriz brasileira sobre dislipidemias e prevenção da aterosclerose. Arq Bras Cardiol. 2007;88(supl 1):1-18.
- 341. DRI - Dietary Reference Intakes for Energy, Carbohydrate, Fiber, Fat, Fatty Acids, Cholesterol, Protein, and Amino Acids. Washington: National Academy of Sciences. Institute of Medicine. Food and Nutrition Board; 2005.
- 342. Teles SS, Valle ER. Adulto sobrevivente de câncer Infantil: uma revisão bibliográfica. Psicologia em Estudo (Maringá). 2009;14(2):355-63.
- 343. Teles SS, Valle ERM. Adulto sobrevivente de câncer Infantil: uma revisão bibliográfica. Psicologia em Estudo. Maringá. 2009;14(2):355-63.
- 344. Medín G. Supervivientes de câncer infantil: efectos em el tiempo: um estúdio cualitativo. Psicooncología. 2009;6(2-3):429-43.
- 345. Freud S. Conferência XVIII "Fixação em traumas - o inconsciente" (1915 -1916). Rio de Janeiro: Imago Editora Ltda; 1976.
- 346. Moura MD. Psicanálise e hospital. 2Ş ed. Rio de Janeiro: Revinter; 2000.
- 347. Lacan J. Outros Escritos. Rio de Janeiro: Jorge Zahar; 2003.
Correspondência:
Datas de Publicação
-
Publicação nesta coleção
18 Jun 2013 -
Data do Fascículo
Maio 2013