1. Introdução
Os distúrbios de sono compreendem uma vasta gama de condições clínicas capazes de interferir negativamente em todos orgãos e sistemas, e, em particular, no sistema cardiovascular. As consequências são inúmeras e não limitadas à fase em que estamos dormindo; pelo contrário, os distúrbios de sono causam importantes repercussões também no período da vigília, comprometendo a qualidade de vida e contribuindo para o surgimento de muitas doenças.
A importância deste tema tem ganhado cada vez mais a atenção da sociedade, principalmente por mudanças drásticas do estilo de vida da população mundial nas últimas décadas: estamos dormindo cada vez menos, e o excesso de peso contribui para o aumento da prevalência dos distúrbios respiratórios do sono.
Nesta diretriz, abordaremos as principais evidências que sugerem, cada vez de forma mais consistente, o impacto dos distúrbios de sono nas doenças cardiovasculares.
Estamos cada vez mais convencidos de que os distúrbios de sono são novos fatores de risco cardiovascular. No entanto, na prática clínica, o subdiagnóstico e o consequente subtratamento são frequentes. Como veremos, a prevalência dos distúrbios de sono é muito alta em pacientes com doenças cardiovasculares. Mais do que frequente, há evidências consistentes sugerindo que os distúrbios de sono aumentam o risco de diversas doenças cardiovasculares.
Fica claro que o cardiologista tem um papel fundamental na identificação de pacientes portadores de distúrbios de sono. Desta forma, este profissional (que não é habitualmente treinado em Medicina do Sono) pode beneficiar-se deste documento. No entanto, nossa intenção não é transformar o Cardiologista que lê este documento em um especialista em sono, mas em um profissional importante e atuante, que pode ajudar a identificar os pacientes que devem ser tratados em conjunto com especialistas da área. Uma proposta do papel do Cardiologsta no manejo dos distúrbios de sono está descrita no setor de considerações finais deste documento.
Acreditamos, assim, que melhoraremos não só a qualidade do sono, mas, potencialmente, o risco cardiovascular dos pacientes. Como será observado neste documento, a maioria das evidências do potential benefício do tratamento de um dos principais distúrbios de sono, a Apneia Obstrutiva do Sono (AOS), refere-se ao uso da Pressão Positiva Contínua de Vias Aéreas (CPAP) superiores. Procuraremos, no entanto, mostrar o benefício de outras modalidades terapêuticas sempre que as evidencias estiverem disponíveis.
Para a seleção dos artigos que constam em cada seção, elegemos coordenadores com reconhecida experiência na área para realizar uma revisão sistemática da literatura. Para os casos de recomendações de procedimentos ou de tratamentos, adotamos os seguintes critérios adotados pela Sociedade Brasileira de Cardiologia:
1.1. Classes (graus) de Recomendação
-
Classe I: condições para as quais há evidências conclusivas ou, em sua falta, consenso geral de que o procedimento é seguro, e útil/eficaz.
-
Classe II: condições para as quais há evidências conflitantes e/ou divergência de opinião sobre segurança, e utilidade/eficácia do procedimento.
-
Classe IIA: peso ou evidência/opinião a favor do procedimento. A maioria aprova.
-
Classe IIB: segurança e utilidade/eficácia menos bem estabelecida, não havendo predomínio de opiniões a favor.
-
Classe III: condições para as quais há evidências e/ou consenso de que o procedimento não é útil/eficaz e, em alguns casos, pode ser prejudicial.
1.2. Níveis de Evidência
-
Nível A: dados obtidos a partir de múltiplos estudos randomizados de bom porte, concordantes e/ou de metanálise robusta de estudos clínicos randomizados.
-
Nível B: dados obtidos a partir de metanálise menos robusta, a partir de um único estudo randomizado ou de estudos não randomizados (observacionais).
-
Nível C: dados obtidos de opiniões consensuais de especialistas
Para fins didáticos, os seguintes termos precisam ser definidos nesta seção para melhor compreensão desta diretriz:
Apneia: redução da amplitude do sinal de fluxo aéreo ≥ 90% da linha de base utilizando um sensor térmico oronasal. A duração da redução ≥ 90% no sinal do sensor precisa ter duração mínima de 10 segundos. Não há necessidade de dessaturação de oxigênio relacionada ao evento.11 Berry RB, Brooks R, Gamaldo CE, Harding SM, Lloyd RM, Marcus CL, et al. American Academy of Sleep Medicine. The AASM Manual for the Scoring of Sleep and Associated Events: Rules, Terminology and Technical Specifications, Version 2.3. www.aasmnet.org. Darien, Illinois: American Academy of Sleep Medicine; 2016.
www.aasmnet.org...
Apneia central: evento que atenda aos critérios de apneia e esteja associado com ausência de esforço inspiratório contínuo ou aumentado ao longo de todo o período de ausência de fluxo respiratório.
Apneia mista: evento que atenda aos critérios de apneia e esteja associado com ausência de esforço inspiratório contínuo ou aumentado no início do evento, e com retomada do esforço respiratório no final do período de ausência de fluxo respiratório.
Apneia obstrutiva: evento que atenda aos critérios de apneia e esteja associado com esforço inspiratório contínuo ou aumentado ao longo de todo o período de ausência de fluxo respiratório.
Apneia obstrutiva do sono: de acordo com a Classificação Internacional dos Distúrbios de Sono (CIDS-3),22 American Academy of Sleep Medicine, International Classification of Sleep Disorders. 3rd ed. Darien, Illinois; 2014. o critério diagnóstico da AOS envolve a presença dos tópicos A e B ou C, descritos conforme quadro 1.
Critério diagnóstico da apneia obstrutiva do sono, de acordo com a a Classificação Internacional dos Distúrbios do Sono
Curta duração do sono: em linhas gerais, a curta duração de sono no adulto, frequentemente associada à privação de sono, é conceituada quando a duração do sono for inferior à média de 7 a 8 horas por noite. O principal sintoma é a sonolência excessiva diurna, mas outros sintomas incluem o humor deprimido, prejuízo na memória e na concentração. A privação crônica do sono pode trazer sérias consequências para a saúde, performance e segurança no dia a dia.
Hipopneia: redução na amplitude do sinal de fluxo ≥ 30% da linha de base utilizando a pressão nasal. A duração da redução ≥ 30% no sinal do sensor é ≥ 10 segundos. Há necessidade de dessaturação de oxigênio ≥ 3% da linha de base OU o evento é associado a um despertar.11 Berry RB, Brooks R, Gamaldo CE, Harding SM, Lloyd RM, Marcus CL, et al. American Academy of Sleep Medicine. The AASM Manual for the Scoring of Sleep and Associated Events: Rules, Terminology and Technical Specifications, Version 2.3. www.aasmnet.org. Darien, Illinois: American Academy of Sleep Medicine; 2016.
www.aasmnet.org...
A hipopneia pode ser classificada em obstrutiva ou central. Esta classificação é opcional e segue os seguintes critérios:
-
Hipopneia obstrutiva: quando apresentar ronco, achatamento da curva de fluxo ou respiração paradoxal durante o período de queda do fluxo respiratório.
-
Hipopneia central: quando não apresentar ronco, achatamento da curva de fluxo ou respiração paradoxal durante o período de queda do fluxo respiratório.
Índice de Apneia e Hipopneia (IAH): número médio dos eventos de apneia e hipopneia por hora do sono. É a partir deste índice que determinamos a gravidade da apneia do sono (seja a apneia do tipo obstrutiva ou central).
Narcolepsia: o diagnóstico pode ser feito pela soma dos critérios A + B descritos a seguir:
A. O paciente tem períodos diários de necessidade irreprimível de dormir ou, durante o dia, tem lapsos de sono, ocorrendo há pelo menos 3 meses.
B. A presença de uma ou ambas as seguintes características: (1) cataplexia (definida como perda de tônus) e (2) latência média do sono de ≤ 8 minutos e dois ou mais períodos de início precoce do sono REM (SOREMPs) no Teste das Múltiplas Latências do Sono (TMLS), realizado de acordo com as técnicas padronizadas.33 Littner MR, Kushida C, Wise M, Davila DG, Morgenthaler T, Lee-Chiong T, et al; Standards of Practice Committee of the American Academy of Sleep Medicine. Practice parameters for clinical use of the multiple sleep latency test and the maintenance of wakefulness test. Sleep. 2005;28(1):113-21. PMID: 15700727.
Respiração de Cheyne-Stokes (RCS): condição clínica caracterizada por:11 Berry RB, Brooks R, Gamaldo CE, Harding SM, Lloyd RM, Marcus CL, et al. American Academy of Sleep Medicine. The AASM Manual for the Scoring of Sleep and Associated Events: Rules, Terminology and Technical Specifications, Version 2.3. www.aasmnet.org. Darien, Illinois: American Academy of Sleep Medicine; 2016.
www.aasmnet.org...
-
Episódios com três ou mais apneias centrais consecutivas e/ou hipopneias centrais, separados por um padrão “crescendo-decrescendo” na amplitude do registro do fluxo respiratório, com a duração do ciclo de ≥40 segundos.
-
Presença de cinco ou mais apneias e/ou hipopneias centrais por hora de sono associados com o padrão “crescendo-decrescendo” na amplitude do registro do fluxo respiratório registrados por mais de 2 horas de monitoramento.
Síndrome das Pernas Inquietas (SPI): é uma doença neurológica sensório-motora com um claro impacto na qualidade do sono e na qualidade de vida do paciente. A SPI é diagnosticada por determinar padrões de sintomas que satisfazem os cinco critérios essenciais seguintes, acrescentando especificadores clínicos, sempre que necessário. Todos os seguintes critérios essenciais devem ser atendidos:22 American Academy of Sleep Medicine, International Classification of Sleep Disorders. 3rd ed. Darien, Illinois; 2014.
-
Desejo irresistível de mover as pernas, geralmente (mas nem sempre) acompanhado por sensações desconfortáveis e desagradáveis nas pernas.
-
Necessidade de movimentar as pernas, e as sensações desagradáveis começam ou pioram durante períodos de repouso ou inatividade, como deitado ou sentado.
-
A necessidade de movimentar as pernas e as sensações desagradáveis são parcial ou totalmente aliviadas pelo movimento, como caminhada ou alongamento.
-
A necessidade de movimentar as pernas e as sensações desagradáveis durante o repouso ou inatividade só ocorrem ou são piores à noite.
-
A ocorrência das características anteriores não são explicadas por outras condições clínicas, como mialgia, estase venosa, edema nas pernas, artrite, cãibras nas pernas, desconforto posicional etc.
Algumas considerações:
-
A SPI é considerada persistente quando os sintomas ocorreram, em média, pelo menos duas vezes por semana, no ano anterior.
-
Na SPI intermitente, os sintomas ocorreram, em média, menos que duas vezes na semana durante o ano anterior, em pelo menos cinco episódios.
2. Epidemiologia dos Distúrbios Respiratórios do Sono na População Geral e em Pacientes com Doenças Cardiovasculares
2.1. Distúrbios Respiratórios do Sono na População Geral
Apesar do crescente reconhecimento de que os distúrbios respiratórios do sono, particularmente a AOS, representam condição relativamente comum, evidências baseadas em dados populacionais estimando sua prevalência datam das últimas duas décadas. Estudos prévios, com amostras representativas da população em geral, mostraram que a prevalência da AOS em adultos pode variar de 1,2 a 7,5%, considerando como critérios diagnósticos a presença do IAH acima de cinco eventos por hora de sono e sonolência excessiva diurna.44 Young T, Palta M, Dempsey J, Skatrud J, Weber S, Badr S. The occurrence of sleep-disordered breathing among middle-aged adults. N Engl J Med. 1993;328(17):1230-5. doi: 10.1056/NEJM199304293281704.
https://doi.org/10.1056/NEJM199304293281...
5 Bearpark H, Elliott L, Grunstein R, Cullen S, Schneider H, Althaus W, et al. Snoring and sleep apnea: a population study in Australian men. Am J Respir Crit Care Med. 1995;151(5):1459-65. doi: 10.1164/ajrccm.151.5.7735600.
https://doi.org/10.1164/ajrccm.151.5.773...
6 Bixler EO, Vgontzas AN, Ten Have T, Tyson K, Kales A. Effects of age on sleep apnea in men: I. Prevalence and severity. Am J Respir Crit Care Med. 1998;157(1):144-8. doi: 10.1164/ajrccm.157.1.9706079.
https://doi.org/10.1164/ajrccm.157.1.970...
7 Bixler EO, Vgontzas AN, Lin HM, Ten Have T, Rein J, Vela-Bueno A, et al. Prevalence of sleep-disordered breathing in women: effects of gender. Am J Respir Crit Care Med. 2001;163(3 Pt 1):608-13. doi: 10.1164/ajrccm.163.3.9911064.
https://doi.org/10.1164/ajrccm.163.3.991...
8 Durán J, Esnaola S, Rubio R, Iztueta A. Obstructive sleep apnea-hypopnea and related clinical features in a population-based sample of subjects aged 30 to 70 yr. Am J Respir Crit Care Med. 2001;163(3 Pt 1):685-9. doi: 10.1164/ajrccm.163.3.2005065.
https://doi.org/10.1164/ajrccm.163.3.200...
9 Ip MS, Lam B, Lauder IJ, Tsang KW, Chung KF, Mok YW, et al. A community study of sleep-disordered breathing in middle-aged Chinese men in Hong Kong. Chest. 2001;119(1):62-9. PMID: 11157585.
10 Ip MS, Lam B, Tang LC, Lauder IJ, Ip TY, Lam WK. A community study of sleep-disordered breathing in middle-aged Chinese women in Hong Kong: prevalence and gender differences. Chest. 2004;125(1):127-34. PMID: 14718431.
11 Kim J, In K, Kim J, You S, Kang K, Shim J, et al. Prevalence of sleep-disordered breathing in middle-aged Korean men and women. Am J Respir Crit Care Med. 2004;170(10):1108-13. doi: 10.1164/rccm.200404-519OC.
https://doi.org/10.1164/rccm.200404-519O...
12 Udwadia ZF, Doshi AV, Lonkar SG, Singh CI. Prevalence of sleep disordered breathing and sleep apnea in middle-aged urban Indian men. Am J Respir Crit Care Med. 2004;169(2):168-73. doi: 10.1164/rccm.200302-265OC.
https://doi.org/10.1164/rccm.200302-265O...
-1313 Sharma SK, Kumpawat S, Banga A, Goel A. Prevalence and risk factors of obstructive sleep apnea syndrome in a population of Delhi, India. Chest. 2006;130(1):149-56. doi: 10.1378/chest.130.1.149.
https://doi.org/10.1378/chest.130.1.149...
Porém,estudos mais recentes apontam taxas de prevalência mais altas, e isto pode ser explicado por alguns motivos como: a epidemia de sobrepeso e obesidade, que tem sido verificada nas últimas 2 décadas; a melhora nos métodos diagnósticos; a mudança nos critérios adotados para a definição da AOS. Por exemplo, estudo epidemiológico realizado na cidade de São Paulo (SP) observou que a prevalência da AOS foi de 32,9%.1414 Tufik S, Santos-Silva R, Taddei JA, Bittencourt LR. Obstructive sleep apnea syndrome in the Sao Paulo Epidemiologic Sleep Study. Sleep Med. 2010;11(5):441-6. doi: 10.1016/j.sleep.2009.10.005.
https://doi.org/10.1016/j.sleep.2009.10....
Outro estudo, utilizando os dados do Wisconsin Sleep Cohort (WSC), mostrou que a prevalência geral da AOS foi de 10% e, para homens entre 30 e 49 anos, foi de 17%. Estes autores relataram que houve aumento de 14 a 55% na prevalência da AOS nos dois períodos estudados (1988-1994 e 2007-2010), dependendo do subgrupo analisado.1515 Peppard PE, Young T, Barnet JH, Palta M, Hagen EW, Hla KM. Increased prevalence of sleep-disordered breathing in adults. Am J Epidemiol. 2013;177(9):1006-14. doi: 10.1093/aje/kws342.
https://doi.org/10.1093/aje/kws342...
Recentemente, estudo realizado em Lausanne (Suíça), entre 2009 e 2013, denominado HypnoLaus, corroborou estas altas taxas de prevalência da AOS, observando prevalência de 23,4% em mulheres e de 49,7% em homens, com gravidade entre moderada à grave.1616 Heinzer R, Vat S, Marques-Vidal P, Marti-Soler H, Andries D, Tobback N, et al. Prevalence of sleep-disordered breathing in the general population: the HypnoLaus study. Lancet Respir Med. 2015;3(4):310-8. doi: 10.1016/S2213-2600(15)00043-0
https://doi.org/10.1016/S2213-2600(15)00...
Os estudos populacionais são unâmimes em estimar que a prevalência da AOS é maior em diferentes subgrupos, incluindo sexo masculino, indivíduos mais velhos e aqueles com sobrepeso ou obesidade.44 Young T, Palta M, Dempsey J, Skatrud J, Weber S, Badr S. The occurrence of sleep-disordered breathing among middle-aged adults. N Engl J Med. 1993;328(17):1230-5. doi: 10.1056/NEJM199304293281704.
https://doi.org/10.1056/NEJM199304293281...
,77 Bixler EO, Vgontzas AN, Lin HM, Ten Have T, Rein J, Vela-Bueno A, et al. Prevalence of sleep-disordered breathing in women: effects of gender. Am J Respir Crit Care Med. 2001;163(3 Pt 1):608-13. doi: 10.1164/ajrccm.163.3.9911064.
https://doi.org/10.1164/ajrccm.163.3.991...
,1010 Ip MS, Lam B, Tang LC, Lauder IJ, Ip TY, Lam WK. A community study of sleep-disordered breathing in middle-aged Chinese women in Hong Kong: prevalence and gender differences. Chest. 2004;125(1):127-34. PMID: 14718431.,1111 Kim J, In K, Kim J, You S, Kang K, Shim J, et al. Prevalence of sleep-disordered breathing in middle-aged Korean men and women. Am J Respir Crit Care Med. 2004;170(10):1108-13. doi: 10.1164/rccm.200404-519OC.
https://doi.org/10.1164/rccm.200404-519O...
Apesar da consideravel elevada prevalência da AOS na população geral, estima-se que cerca de 75 a 80% desta população permaneça sem diagnóstico nos Estados Unidos.1717 Young T, Evans L, Finn L, Palta M. Estimation of the clinically diagnosed proportion of sleep apnea syndrome in middle-aged men and women. Sleep. 1997;20(9):705-6. PMID: 9406321.
2.2. Distúrbios Respiratórios do Sono nas Doenças Cardiovasculares
2.2.1. AOS e Hipertensão Arterial Sistêmica
A frequência de AOS varia de 30 a 56% entre os pacientes com Hipertensão arterial Sistêmica (HAS) em geral.1818 Worsnop CJ, Naughton MT, Barter CE, Morgan TO, Anderson AI, Pierce RJ. The prevalence of obstructive sleep apnea in hypertensives. Am J Respir Crit Care Med. 1998;157(1):111-5. doi: 10.1164/ajrccm.157.1.9609063.
https://doi.org/10.1164/ajrccm.157.1.960...
19 Sjöström C, Lindberg E, Elmasry A, Hägg A, Svärdsudd K, Janson C. Prevalence of sleep apnea and snoring in hypertensive men: a population based study. Thorax. 2002;57(7):602-7. PMID: 12096203.-2020 Drager LF, Genta PR, Pedrosa RP, Nerbass FB, Gonzaga CC, Krieger EM, et al. Characteristics and predictors of obstructive sleep apnea in patients with systemic hypertension. Am J Cardiol. 2010;105(8):1135-9. doi: 10.1016/j.amjcard.2009.12.017.
https://doi.org/10.1016/j.amjcard.2009.1...
No entanto, esta prevalência é ainda mais expressiva entre os pacientes com a HAS resistente, variando entre 64 a 83%.2121 Logan AG, Perlikowski SM, Mente A, Tisler A, Tkacova R, Niroumand M, et al. High prevalence of unrecognized sleep apnea in drug-resistant hypertension. J Hypertens. 2001;19(12):2271-7. PMID: 11725173.
22 Gonçalves SC, Martinez D, Gus M, de Abreu-Silva EO, Bertoluci C, Dutra I, et al. Obstructive sleep apnea and resistant hypertension: a case-control study. Chest. 2007;132(6):1858-62. doi: 10.1378/chest.07-1170.
https://doi.org/10.1378/chest.07-1170...
23 Pedrosa RP, Drager LF, Gonzaga CC, Sousa MG, de Paula LK, Amaro AC, et al. Obstructive sleep apnea: the most common secondary cause of hypertension associated with resistant hypertension. Hypertension. 2011;58(5):811-7. doi: 10.1161/HYPERTENSIONAHA.111.179788
https://doi.org/10.1161/HYPERTENSIONAHA....
-2424 Muxfeldt ES, Margallo VS, Guimarães GM, Salles GF. Prevalence and associated factors of obstructive sleep apnea in patients with resistant hypertension. Am J Hypertens. 2014;27(8):1069-78. doi: 10.1093/ajh/hpu023.
https://doi.org/10.1093/ajh/hpu023...
Em uma das evidências, a AOS foi a condição clínica mais comumente associada à HAS resistente.2323 Pedrosa RP, Drager LF, Gonzaga CC, Sousa MG, de Paula LK, Amaro AC, et al. Obstructive sleep apnea: the most common secondary cause of hypertension associated with resistant hypertension. Hypertension. 2011;58(5):811-7. doi: 10.1161/HYPERTENSIONAHA.111.179788
https://doi.org/10.1161/HYPERTENSIONAHA....
Investigação longitudinal dos indivíduos incluídos na WSC demonstrou maior incidência de HAS em pessoas com a AOS após 4 anos de acompanhamento.2525 Peppard PE, Young T, Palta M, Skatrud J. Prospective study of the association between sleep-disordered breathing and hypertension. N Engl J Med. 2000;342(19):1378-84. doi: 10.1056/NEJM200005113421901.
https://doi.org/10.1056/NEJM200005113421...
De forma interessante, a razão de chance de HAS aumentou com a elevação do IAH basal.2525 Peppard PE, Young T, Palta M, Skatrud J. Prospective study of the association between sleep-disordered breathing and hypertension. N Engl J Med. 2000;342(19):1378-84. doi: 10.1056/NEJM200005113421901.
https://doi.org/10.1056/NEJM200005113421...
Análises prospectivas do SHHS (Sleep Heart Health Study) mostraram a relação entre a linha de base do IAH e o risco aproximado de desenvolvimento de HAS, porém sem significância estatística após ajuste para o Índice de Massa Corporal (IMC).2626 O'Connor GT, Caffo B, Newman AB, Quan SF, Rapoport DM, Redline S, et al. Prospective study of sleep-disordered breathing and hypertension: the Sleep Heart Health Study. Am J Respir Crit Care Med. 2009;179(12):1159-64. doi: 10.1164/rccm.200712-1809OC.
https://doi.org/10.1164/rccm.200712-1809...
Chama a atenção que a média de idade dos indivíduos desta coorte foi em torno de 60 anos. As evidências do impacto da AOS sobre a HAS em pessoas idosas não são claras. De fato, outro estudo, da mesma coorte, mostrou que existia associação com a hipertensão sistólica ou diastólica somente em indivíduos com menos de 60 anos.2727 Haas DC, Foster GL, Nieto FJ, Redline S, Resnick HE, Robbins JA, et al. Age-dependent associations between sleep-disordered breathing and hypertension: importance of discriminating between systolic/diastolic hypertension and isolated systolic hypertension in the Sleep Heart Health Study. Circulation. 2005;111(5):614-21. doi: 10.1161/01.CIR.0000154540.62381.CF.
https://doi.org/10.1161/01.CIR.000015454...
Por outro lado, os resultados do Sleep Disorders in Older Men Study revelaram chances 1,6 vez maior de HAS em homens idosos com AOS.2828 Mehra R, Stone KL, Blackwell T, Ancoli Israel S, Dam TT, Stefanick ML, et al. Prevalence and correlates of sleep-disordered breathing in older men: osteoporotic fractures in men sleep study. J Am Geriatr Soc. 2007;55(9):1356-64. doi: 10.1111/j.1532-5415.2007.01290.x.
https://doi.org/10.1111/j.1532-5415.2007...
2.2.2. Apneia Obstrutiva do Sono e Doença Arterial Coronariana
Evidências indicaram que a prevalência de AOS em pacientes com Doença Arterial Coronariana (DAC) é alta, variando entre 38 a 87%, dependendo do tipo de paciente com DAC estudado e o critério diagnóstico.2929 Andreas S, Schulz R, Werner GS, Kreuzer H. Prevalence of obstructive sleep apnoea in patients with coronary artery disease. Coron Artery Dis. 1996;7(7):541-5. PMID: 8913673.
30 Mehra R, Principe-Rodriguez K, Kirchner HL, Strohl KP. Sleep apnea in acute coronary syndrome: high prevalence but low impact on 6-month outcome. Sleep Med. 2006;7(6):521-8. doi: 10.1016/j.sleep.2006.03.012.
https://doi.org/10.1016/j.sleep.2006.03....
31 Lee CH, Khoo SM, Tai BC, Chong EY, Lau C, Than Y, et al. Obstructive sleep apnea in patients admitted for acute myocardial infarction: prevalence, predictors, and effect on microvascular perfusion. Chest. 2009;135(6):1488-95. doi: 10.1378/chest.08-2336.
https://doi.org/10.1378/chest.08-2336...
-3232 Danzi-Soares NJ, Genta PR, Nerbass FB, Pedrosa RP, Soares FS, César LA, et al. Obstructive sleep apnea is common among patients referred for coronary artery bypass grafting and can be diagnosed by portable monitoring. Coron Artery Dis. 2012;23(1):31-8. doi: 10.1097/MCA.0b013e32834df5d0.
https://doi.org/10.1097/MCA.0b013e32834d...
Na população de angina refratária, a frequência da AOS em casos consecutivos foi de 73%.3333 Geovanini GR, Gowdak LH, Pereira A, Danzi-Soares N, Dourado L, Poppi N, et al. OSA and depression are common and independently associated with refractory angina in patients with coronary artery disease. Chest. 2014;146(1):73-80. doi: 10.1378/chest.13-2885.
https://doi.org/10.1378/chest.13-2885...
Foi observada que a presença e a gravidade da AOS estão independentemente associadas com a presença e a extensão de calcificação arterial coronariana, que é um marcador subclínico de DAC.3434 Sorajja D, Gami AS, Somers VK, Behrenbeck TR, Garcia-Touchard A, Lopez-Jimenez F. Independent association between obstructive sleep apnea and subclinical coronary artery disease. Chest. 2008;133(4):927-33. doi: 10.1378/chest.07-2544.
https://doi.org/10.1378/chest.07-2544...
Análises transversais dos dados do SHHS revelaram maiores chances de DAC em indivíduos com IAH elevado.3535 Shahar E, Whitney CW, Redline S, Lee ET, Newman AB, Nieto FJ, et al. Sleep-disordered breathing and cardiovascular disease: cross-sectional results of the Sleep Heart Health Study. Am J Respir Crit Care Med. 2001;163(1):19-25. doi: 10.1164/ajrccm.163.1.2001008.
https://doi.org/10.1164/ajrccm.163.1.200...
Ainda, análises longitudinais dos dados do SHHS, em um seguimento de 8,7 anos e após ajuste de múltiplos fatores de risco, indicam que a AOS é um preditor significativo para maior incidência de DAC, principalmente em homens com menos de 70 anos de idade.
2.2.3. Apneia Obstrutiva do Sono, Apneia Central e Insuficiência Cardíaca
Em comparação com a população geral, a prevalência da AOS é geralmente mais elevada em populações com Insuficiência Cardíaca (IC). Por exemplo, a prevalência de AOS em pacientes com IC é de 12 a 26% considerando o corte do IAH ≥ 15 eventos/hora.3737 Javaheri S. Sleep disorders in systolic heart failure: a prospective study of 100 male patients. The final report. Int J Cardiol. 2006;106(1):21-8. doi: 10.1016/j.ijcard.2004.12.068.
https://doi.org/10.1016/j.ijcard.2004.12...
,3838 Yumino D, Wang H, Floras JS, Newton GE, Mak S, Ruttanaumpawan P, et al. Prevalence and physiological predictors of sleep apnea in patients with heart failure and systolic dysfunction. J Card Fail. 2009;15(4):279-85. doi: 10.1016/j.cardfail.2008.11.015.
https://doi.org/10.1016/j.cardfail.2008....
Também foi observada alta frequência de apneia central do sono (estimada entre 21 a 56% quando considera-se IAH ≥15 eventos/hora) nos pacientes com IC, tanto naqueles com quadro sintomático ou descompensado,3939 Khayat RN, Jarjoura D, Patt B, Yamokoski T, Abraham WT. In-hospital testing for sleep-disordered breathing in hospitalized patients with decompensated heart failure: report of prevalence and patient characteristics. J Card Fail. 2009;15(9):739-46. doi: 10.1016/j.cardfail.2009.05.005.
https://doi.org/10.1016/j.cardfail.2009....
,4040 Oldenburg O, Lamp B, Faber L, Teschler H, Horstkotte D, Topfer V. Sleep-disordered breathing in patients with symptomatic heart failure: a contemporary study of prevalence in and characteristics of 700 patients. Eur J Heart Fail. 2007;9(3):251-7. doi: 10.1016/j.ejheart.2006.08.003.
https://doi.org/10.1016/j.ejheart.2006.0...
quanto naqueles com IC crônica estável.4141 Paulino A, Damy T, Margarit L, Stoïca M, Deswarte G, Khouri L, et al. Prevalence of sleep-disordered breathing in a 316-patient French cohort of stable congestive heart failure. Arch Cardiovasc Dis. 2009;102(3):169-75. doi: 10.1016/j.acvd.2008.12.006.
https://doi.org/10.1016/j.acvd.2008.12.0...
42 Silva RS, Figueiredo AC, Mady C, Lorenzi Filho G. Breathing disorders in congestive heart failure: gender, etiology and mortality. Braz J Med Biol Res. 2008;41(3):215-22. PMID: 18575711.-4343 Javaheri S, Shukla R, Zeigler H, Wexler L. Central sleep apnea, right ventricular dysfunction, and low diastolic blood pressure are predictors of mortality in systolic heart failure. J Am Coll Cardiol. 2007;49(20):2028-34. doi: 10.1016/j.jacc.2007.01.084.
https://doi.org/10.1016/j.jacc.2007.01.0...
A presença de apneia central nos pacientes com IC geralmente é descrita em associação com a RCS.4242 Silva RS, Figueiredo AC, Mady C, Lorenzi Filho G. Breathing disorders in congestive heart failure: gender, etiology and mortality. Braz J Med Biol Res. 2008;41(3):215-22. PMID: 18575711.
Não são muitas as evidências baseadas em estudos longitudinais, mas as análises do SHHS indicam que os homens, mas não as mulheres, têm Risco Relativo (RR) aumentado (1,13 [1,02-1,26]) de incidência de IC como consequência da AOS. Em estudo clínico longitudinal, o risco de mortalidade precoce em pacientes com IC e apneia central do sono foi 2,1 vezes maior em comparação ao grupo sem apneia central.4343 Javaheri S, Shukla R, Zeigler H, Wexler L. Central sleep apnea, right ventricular dysfunction, and low diastolic blood pressure are predictors of mortality in systolic heart failure. J Am Coll Cardiol. 2007;49(20):2028-34. doi: 10.1016/j.jacc.2007.01.084.
https://doi.org/10.1016/j.jacc.2007.01.0...
A prevalência de distúrbios respiratórios do sono parece ser alta não apenas em pacientes com IC sistólica, mas também naqueles com IC e fração de ejeção normal. Um estudo avaliando 247 pacientes com IC e fração de ejeção normal revelou a presença de distúrbios respiratórios do sono em 69%, sendo que 40% apresentaram AOS e 29% mostraram apneia central.4444 Bitter T, Faber L, Hering D, Langer C, Horstkotte D, Oldenburg O. Sleep-disordered breathing in heart failure with normal left ventricular ejection fraction. Eur J Heart Fail. 2009;11(6):602-8. doi: doi: 10.1093/eurjhf/hfp057.
https://doi.org/10.1093/eurjhf/hfp057...
2.2.4. Apneia Obstrutiva do Sono e Arritmias
Estima-se que prevalência de AOS em pacientes com Fibrilação Atrial (FA) varie entre 32 a 82%.4545 Porthan KM, Melin JH, Kupila JT, Venho KK, Partinen MM. Prevalence of sleep apnea syndrome in lone atrial fibrillation: a case-control study. Chest. 2004;125(3):879-85. PMID: 15006945.
46 Braga B, Poyares D, Cintra F, Guilleminault C, Cirenza C, Horbach S, et al. Sleep-disordered breathing and chronic atrial fibrillation. Sleep Med 2009;10(2):212-6. doi: 10.1016/j.sleep.2007.12.007.
https://doi.org/10.1016/j.sleep.2007.12....
-4747 Hoyer FF, Lickfett LM, Mittmann-Braun E, Ruland C, Kreuz J, Pabst S, et al. High prevalence of obstructive sleep apnea in patients with resistant paroxysmal atrial fibrillation after pulmonary vein isolation. J Interv Card Electrophysiol. 2010;29(1):37-41. doi: 10.1007/s10840-010-9502-8.
https://doi.org/10.1007/s10840-010-9502-...
Análises recentes do SHHS demonstraram probabilidade 17 vezes maior de uma arritmia (FA e taquicardia ventricular não sustentada) ocorrer após evento respiratório do que após a respiração normal durante o sono.4848 Monahan K, Storfer-Isser A, Mehra R, Shahar E, Mittleman M, Rottman J, et al. Triggering of nocturnal arrhythmias by sleep-disordered breathing events. J Am Coll Cardiol. 2009;54(19):1797-804. doi: 10.1016/j.jacc.2009.06.038.
https://doi.org/10.1016/j.jacc.2009.06.0...
2.2.5. Apneia Obstrutiva do Sono e Acidente Vascular Cerebral
Alguns estudos sugerem que a AOS é um fator de risco para acidente vascular cerebral (AVC).4949 Good D, Henkle J, Gelber D, Welsh J, Verhulst S. Sleep disordered breathing and poor functional outcome after stroke. Stroke. 1996;27(2):252-9. PMID: 8571419. Muitos destes estudos têm relatado que a prevalência de AOS em pacientes com AVC varia de 32 a 91%, considerando avaliações realizadas desde 24 horas até 3 meses após o evento.4949 Good D, Henkle J, Gelber D, Welsh J, Verhulst S. Sleep disordered breathing and poor functional outcome after stroke. Stroke. 1996;27(2):252-9. PMID: 8571419.
50 Dyken M, Somers V, Ymada T, Ren Z, Zimmerman B. Investigating the relationship between stroke and obstructive sleep apnea. Stroke. 1996;27(3):401-7. PMID: 8610303.
51 Parra O, Arboix A, Bechich S, García-Eroles L, Montserrat JM, López JA, et al. Time course of sleep-related breathing disorders in first-ever stroke or transient ischemic attack. Am J Respir Crit Care Med. 2000;161(2 Pt 1):375-80. doi: 10.1164/ajrccm.161.2.9903139.
https://doi.org/10.1164/ajrccm.161.2.990...
52 Turkington PM, Bamford J, Wanklyn P, Elliott MW. Prevalence and predictors of upper airway obstruction in the first 24 hours after acute stroke. Stroke. 2002;33(8):2037-42. PMID: 12154259.
53 Hui DS, Choy DK, Wong LK, Ko FW, Li TS, Woo J, et al. Prevalence of sleep-disordered breathing and continuous positive airway pressure compliance: results in chinese patients with first-ever ischemic stroke. Chest. 2002;122(3):852-60. PMID: 12226023.-5454 Joo BE, Seok HY, Yu SW, Kim BJ, Park KW, Lee DH, et al. Prevalence of sleep-disordered breathing in acute ischemic stroke as determined using a portable sleep apnea monitoring device in Korean subjects. Sleep Breath. 2011;15(1):77-82. doi: 10.1007/s11325-009-0325-8.
https://doi.org/10.1007/s11325-009-0325-...
No entanto, a maior parte das evidências tem sido principalmente baseada em casos clínicos, estudos caso-controle ou usaram o ronco como um substituto à documentação objetiva de AOS.
Um estudo observacional prospectivo, em população de pacientes consecutivos encaminhados ao laboratório do sono para diagnóstico de AOS, observou aumento de incidência de AVC ou morte em pacientes com AOS, em seguimento médio de 3,4 anos, em comparação àqueles sem AOS, com RR ajustado de 1,97.5555 Yaggi HK, Concato J, Kernan WN, Lichtman JH, Brass LM, Mohsenin V. Obstructive sleep apnea as a risk factor for stroke and death. N Engl J Med. 2005;353(19):2034-41. doi: 10.1056/NEJMoa043104.
https://doi.org/10.1056/NEJMoa043104...
Resultados similares foram observados na WSC, ao longo de um intervalo de 4 anos, embora a razão de chance ajustada, ainda que alta, não tenha atingido significância estatística (3,08; 0,74-12,81; p = 0,12).5656 Arzt M, Young T, Finn L, Skatrud JB, Bradley TD. Association of sleep-disordered breathing and the occurrence of stroke. Am J Respir Crit Care Med. 2005;172(11):1447-51. doi: 10.1164/rccm.200505-702OC.
https://doi.org/10.1164/rccm.200505-702O...
A análise dos dados prospectivos de SHHS mostrou que a presença de AOS grave é fator de risco independente para a incidência de AVC isquêmico, em homens, após seguimento médio de 8,7 anos.5757 Redline S, Yenokyan G, Gottlieb DJ, Shahar E, O'Connor GT, Resnick HE, et al. Obstructive sleep apnea hypopnea and incident stroke: the Sleep Heart Health Study. Am J Respir Crit Care Med. 2010;182(2):269-77. doi: 10.1164/rccm.200911-1746OC.
https://doi.org/10.1164/rccm.200911-1746...
Embora existam evidências indicando que a AOS é fator de risco para AVC, o inverso também pode ser verdadeiro, ou seja, o AVC parece ser fator de risco para o desenvolvimento da AOS.5858 Javaheri S, Barbe F, Campos-Rodriguez F, Dempsey JA, Khayat R, Javaheri S, et al. Sleep apnea: types, mechanisms, and clinical cardiovascular consequences. J Am Coll Cardiol. 2017;69(7):841-58. doi: 10.1016/j.jacc.2016.11.069.
https://doi.org/10.1016/j.jacc.2016.11.0...
A figura 1 mostra a frequência da AOS entre diversas condições cardiovasculares. A variabilidade observada tem direta relação com o critério adotado para conceituar a AOS e características da população estudada.
Frequência da apneia obstrutiva do sono em diversas doenças cardiovasculares. HAS: hipertensão arterial sistêmica; AVC: acidente vascular cerebral.
A despeito da variabilidade de frequência entre os estudos, fica evidente que a AOS é muito comum no espectro das doenças cardiovasculares. No entanto, como recentemente apontado por um estudo brasileiro realizado em um hospital cardiológico, boa parte dos pacientes com AOS permanecem sem diagnóstico e, como consequência, sem tratamento.5959 Costa LE, Uchôa CH, Harmon RR, Bortolotto LA, Lorenzi-Filho G, Drager LF. Potential underdiagnosis of obstructive sleep apnoea in the cardiology outpatient setting. Heart. 2015;101(16):1288-92. doi: 10.1136/heartjnl-2014-307276.
https://doi.org/10.1136/heartjnl-2014-30...
3. Classificação e Quadro Clínico
3.1. Classificação da Apneia Obstrutiva do Sono
De acordo com o relatório da força-tarefa da American Academy of Sleep Medicine (AASM),6060 Sleep-related breathing disorders in adults: recommendations for syndrome definition and measurements techniques in clinical research; the report of an American Academy of Sleep Medicine Task Force. Sleep. 1999;22(5):667-89. PMID: 10450601. o critério de gravidade da AOS é assim dividido:
-
Leve: 5 a 14,9 eventos obstrutivos por hora de sono.
-
Moderada: 15 a 29,9 eventos obstrutivos por hora de sono.
-
Importante (ou grave): 30 ou mais eventos obstrutivos por hora de sono.
3.2. Quadro Clínico
3.2.1. Fatores Predisponentes
Em estudos de base populacional, o excesso de peso corporal aparece como principal fator de risco para AOS no adulto, seguido pelo sexo masculino e, subsequentemente, pelas anormalidades craniofaciais e pela idade.44 Young T, Palta M, Dempsey J, Skatrud J, Weber S, Badr S. The occurrence of sleep-disordered breathing among middle-aged adults. N Engl J Med. 1993;328(17):1230-5. doi: 10.1056/NEJM199304293281704.
https://doi.org/10.1056/NEJM199304293281...
,1414 Tufik S, Santos-Silva R, Taddei JA, Bittencourt LR. Obstructive sleep apnea syndrome in the Sao Paulo Epidemiologic Sleep Study. Sleep Med. 2010;11(5):441-6. doi: 10.1016/j.sleep.2009.10.005.
https://doi.org/10.1016/j.sleep.2009.10....
,6161 Dempsey JA, Veasey SC, Morgan BJ, O'Donnell CP. Pathophysiology of sleep apnea. Physiol Rev. 2010;90(1):47-112. doi: 10.1152/physrev.00043.2008. Erratum in: Physiol Rev. 2010;90(2):797-8.
https://doi.org/10.1152/physrev.00043.20...
62 Peppard PE, Young T, Palta M, Dempsey J, Skatrud J. Longitudinal study of moderate weight change and sleep-disordered breathing. JAMA. 2000;284(23):3015-21. PMID: 11122588.-6363 Young T, Finn L, Austin D, Peterson A. Menopausal status and sleep-disordered breathing in the Wisconsin Sleep Cohort Study. Am J Respir Crit Care Med. 2003;167(9):1181-5. doi: 10.1164/rccm.200209-1055OC.
https://doi.org/10.1164/rccm.200209-1055...
Além disto, algumas condições clínicas são reconhecidas como fatores de risco para AOS. O hipotireoidismo, que pode acompanhar-se de obesidade, macroglossia e redução do estímulo ventilatório, é reconhecido como fator predisponente mais importante em mulheres.6464 Skjodt NM, Atkar R, Easton PA. Screening for hypothyroidism in sleep apnea. Am J Respir Crit Care Med. 1999;160(2):732-5. doi: 10.1164/ajrccm.160.2.9802051.
https://doi.org/10.1164/ajrccm.160.2.980...
,6565 Shepertycky MR; Banno K; Kryger MH. Differences between men and women in the clinical presentation of patients diagnosed with obstructive sleep apnea syndrome. Sleep. 2005;28(3):309-14. PMID: 16173651. A acromegalia é outra endocrinopatia na qual a frequência da AOS é elevada − provavelmente superior a 60%.6666 Grunstein RR, Ho KY, Sullivan CE. Sleep apnea in acromegaly. Ann Intern Med. 1991;115(7):527-32. PMID: 1883121. Obstrução nasal de diversas etiologias também pode se acompanhar de ronco e distúrbios respiratório do sono.6767 Watanabe T, Isono S, Tanaka A, Tanzawa H, Nishino T. Contribution of body habitus and craniofacial characteristics to segmental closing pressures of the passive pharynx in patients with sleep disordered breathing. Am J Respir Crit Care Med. 2002;165(2):260-5. doi: 10.1164/ajrccm.165.2.2009032.
https://doi.org/10.1164/ajrccm.165.2.200...
Hipertrofia adenotonsilar pode acompanhar-se de AOS, particularmente em crianças.6868 Zonato AI, Martinho FL Bittencourt LR, de Oliveira Camponês Brasil O, Gregório LC, Tufik S. Head and neck physical examination: comparison between non-apneic and obstructive sleep apnea patients. Laryngoscope. 2005;115(6):1030-4. doi: 10.1097/01.MLG.0000163494.19965.DC.
https://doi.org/10.1097/01.MLG.000016349...
Doenças congênitas, que afetam o calibre da via aérea, como, trissomia 21, acondroplasia, mucopolissacaridoses e as síndromes de Pierre Robin, Klippel-Feil, Alpert, Treacher-Collins e Marfan também exibem forte associação com distúrbios respiratórios do sono.6969 Young T, Peppard PE, Gottlieb DJ. Epidemiology of obstructive sleep apnea: a population health perspective. Am J Respir Cirt Care Med. 2002;165(9):1217-39. PMID: 11991871.
O uso de sedativos e o consumo de álcool próximo ao início do sono aumentam a frequência e a duração dos eventos respiratórios anormais, além de poderem desencadear AOS nos roncadores.7070 Scanlan MF, Roebuck T, Little PJ, Redman JR, Naughton MT. Effect of moderate alcohol upon obstructive sleep apnoea. Eur Respir J. 2000;16(5):909-13. PMID: 11153591. Fumantes apresentam RR quatro a cinco vezes maior de distúrbios respiratórios do sono.7171 Wetter DW, Young TB, Bidwell TR, Badr MS, Palta M. Smoking as a risk factor for sleep-disordered breathing. Arch Intern Med. 1994;154(19):2219-24. PMID: 7944843.
3.2.2. Sintomas
Os pacientes com AOS podem apresentar uma gama de manifestações clínicas, frequentemente classificadas em diurnas e noturnas (Quadro 2). De forma geral, os sintomas noturnos, quase sempre relatados por quem vê o paciente dormir, tendem a ser mais específicos. Dentre as várias formas de apresentação, as principais manifestações são de ronco associado à apneias presenciadas por terceiros, o qual deve ser considerado fortemente sugestivo de AOS. Fadiga e sonolência excessiva são as principais e mais frequentes queixas nos pacientes com AOS, podendo, no entanto, resultar de anormalidades do sono de outras etiologias.7272 Chokroverty S. Overview of sleep and sleep disorders. Indian J Med Res. 2010 Feb;131:126-40. PMID: 20308738.
Ronco é o sintoma mais comum na AOS, porém sua prevalência é bem superior à da AOS na população geral e indica que sua presença, isoladamente, é insuficiente para o diagnóstico, independentemente da intensidade. Por outro lado, o relato de ronco ressuscitativo, isto é, pausa respiratória seguida de ronco explosivo, engasgos noturnos e/ou despertar com sensação de sufocamento, deve ser considerado forte indício de AOS.7373 Tsai WH, Remmers JE, Brant R, Flemons WW, Davies J, Macarthur C. A decision rule for diagnostic testing in obstructive sleep apnea. Am J Respir Crit Care Med. 2003;167(10):1427-32. doi: 10.1164/rccm.200112-110OC.
https://doi.org/10.1164/rccm.200112-110O...
A sonolência excessiva diurna é uma queixa importante no adulto com AOS. Costuma ser mais evidente quando o paciente encontra-se relaxado e/ou em estado de inatividade, embora, nos casos mais graves, os pacientes possam adormecer enquanto realizam atividades que envolvem maior grau de atenção, como conversar ou conduzir veículo. A correlação entre a frequência de eventos respiratórios anormais, medida na polissonografia, e a intensidade da sonolência costuma ser baixa.88 Durán J, Esnaola S, Rubio R, Iztueta A. Obstructive sleep apnea-hypopnea and related clinical features in a population-based sample of subjects aged 30 to 70 yr. Am J Respir Crit Care Med. 2001;163(3 Pt 1):685-9. doi: 10.1164/ajrccm.163.3.2005065.
https://doi.org/10.1164/ajrccm.163.3.200...
Na prática clínica, sonolência de qualquer intensidade pode ser encontrada em qualquer nível de gravidade da AOS. É importante ter em mente que sonolência crônica, além de possuir uma repercussão clínica variável, é frequentemente subrelatada, seja porque muitos pacientes, ao longo tempo, conseguem adaptar-se a um dado nível de sonolência e deixar de percebê-la como anormal, ou até por fatores socioeconômicos e culturais.7474 Engleman HM, Hirst WS Douglas NJ. Under reporting of sleepiness and driving impairment in patients with sleep apnoea/hypopnoea syndrome. J Sleep Res. 1997;6(4):272-5. PMID: 9493528. Alguns instrumentos simples e de fácil aplicabilidade podem ser úteis na avaliação de sonolência excessiva crônica (não sendo específico para a AOS). A Escala de Sonolência de Epworth7575 Johns MW. A new method for measuring daytime sleepiness: the Epworth sleepiness scale. Sleep. 1991;14(6):540-5. PMID: 1798888. (Figura 2) é um questionário traduzido e validado para uso no Brasil,7676 Bertolazi AN, Fagondes SC, Hoff LS, Pedro VD, Menna-Barreto SS, JohnsMW. Portuguese-language version of the Epworth sleepiness scale: validation for use in Brazil. J Bras Pneumol. 2009;35(9):877-83. PMID: 19820814. que avalia a chance de cochilar, em uma escala progressiva de zero até 3 pontos, em oito situações hipotéticas, que requerem graus variados de atenção. Um escore total maior do que 10 é considerado sugestivo sonolência excessiva diurna.7575 Johns MW. A new method for measuring daytime sleepiness: the Epworth sleepiness scale. Sleep. 1991;14(6):540-5. PMID: 1798888.
Queixas de queda no desempenho acadêmico, profissional ou mesmo dificuldade na realização de atividades cotidianas podem estar presentes, sobretudo em casos mais graves e são devidas às alterações do processamento cognitivo, da atenção sustentada e da atenção dividida, das funções executivas e da memória, que podem ser mensuradas por testes neuropsicológicos.7777 Quan SF, Wright R, Baldwin CM, Kaemingk KL, Goodwin JL, Kuo TF, et al. Obstructive sleep apnea-hypopnea and neurocognitive functioning in the Sleep Heart Health Study. Sleep Med. 2006;7(6):498-507. doi: 10.1016/j.sleep.2006.02.005.
https://doi.org/10.1016/j.sleep.2006.02....
,7878 Bruin PF, Bagnato MC. Cognitive impairment in obstructive sleep apnea syndrome. J Bras Pneumol. 2010;36(Suppl 2):32-7. doi: http://dx.doi.org/10.1590/51806-37132010001400010.
http://dx.doi.org/10.1590/51806-37132010...
Alterações mentais, incluindo irritabilidade, agressividade, redução da libido, disfunção erétil, ansiedade e depressão também podem ser encontradas.6969 Young T, Peppard PE, Gottlieb DJ. Epidemiology of obstructive sleep apnea: a population health perspective. Am J Respir Cirt Care Med. 2002;165(9):1217-39. PMID: 11991871.,7979 Zias N, Bezwada V, Gilman S, Chroneou A. Obstructive sleep apnea and erectile dysfunction: still a neglected risk factor? Sleep Breath. 2009;13(1):3-10. doi: 10.1007/s11325-008-0212-8.
https://doi.org/10.1007/s11325-008-0212-...
Cefaleia crônica, matinal ou ao despertar devem ser consideradas sugestiva AOS e foi descrita em 15 a 74% dos pacientes, em vários estudos.8080 Rains JC, Poceta JS. Headache and sleep disorders: review and clinical implications for headache management. Headache. 2006;46(9):1344-61. doi: 10.1111/j.1526-4610.2006.00578.x.
https://doi.org/10.1111/j.1526-4610.2006...
É importante notar que, em consequência de diferenças hormonais e das características anatômicas, colapsibilidade e resistência da via aérea superior, não apenas a frequência de AOS, são menores nas mulheres.77 Bixler EO, Vgontzas AN, Lin HM, Ten Have T, Rein J, Vela-Bueno A, et al. Prevalence of sleep-disordered breathing in women: effects of gender. Am J Respir Crit Care Med. 2001;163(3 Pt 1):608-13. doi: 10.1164/ajrccm.163.3.9911064.
https://doi.org/10.1164/ajrccm.163.3.991...
,8181 Mohsenin V. Gender differences in the expression of sleep-disordered breathing. Role of upper airway dimensions. Chest. 2001;120(5):1442-7. PMID: 11713117.
3.2.3. Achados do Exame Físico
No exame físico, atenção especial deve ser dada às características antropométricas e à avaliação das vias aéreas superiores.8282 Epstein LJ, Kristo D, Strollo PJ Jr, Friedman N, Malhotra A, Patil SP, et al; Adult Obstructive Sleep Apnea Task Force of the American Academy of Sleep Medicine. Clinical guideline for the evaluation, management and long-term care of obstructive sleep apnea in adults. J Clin Sleep Med. 2009;5(3):263-76. PMID: 19960649. IMC superior a 30 kg/m2 é sugestivo de AOS, particularmente quando a deposição de gordura assume padrão central, caracterizado pelo aumento do perímetro cervical (> 43 cm nos homens e > 38 cm nas mulheres) e/ou da circunferência abdominal (>102 cm em homens e > 88 cm nas mulheres).8383 Bittencourt LR. Diagnóstico e tratamento da síndrome da apneia obstrutiva do sono (SAOS): Guia Prático. São Paulo: Livraria Médica Paulista; 2008.,8484 Lorenzo C, Williams K, Hunt KJ, Haffner SM. The National Cholesterol Education Program-Adult Treatment Panel III, International Diabetes Federation, and World Health Organization Definitions of the Metabolic Syndrome as Predictors of Incident Cardiovascular Disease and Diabetes. Diabetes Care. 2007;30(1):8-13. doi: 10.2337/dc06-1414.
https://doi.org/10.2337/dc06-1414...
Na avaliação da via aérea superior, é frequente a observação de uma desproporção entre tecidos da cavidade oral e arcabouço ósseo maxilo-mandibular (Classificação de Mallampati III e VI), que tem valor preditivo importante da doença. Outros achados na AOS são retrognatia, extrusão dos incisivos superiores além dos incisivos inferiores (overjet), macroglossia, inserção baixa dos pilares posteriores na úvula (palatoweb), hipertrofia tonsilar, úvula aumentada ou alongada, palato ogival. Alterações nasais, como pólipos, desvio septal, conchas hipertrofiadas ou anormalidades valvares, podem contribuir para o aumento da resistência da via aérea superior, embora, raramente sejam causa isolada de AOS.6868 Zonato AI, Martinho FL Bittencourt LR, de Oliveira Camponês Brasil O, Gregório LC, Tufik S. Head and neck physical examination: comparison between non-apneic and obstructive sleep apnea patients. Laryngoscope. 2005;115(6):1030-4. doi: 10.1097/01.MLG.0000163494.19965.DC.
https://doi.org/10.1097/01.MLG.000016349...
,8585 Roumbaux PH, Bertrand B, Boudewyns A, Deron P, Goffart Y, Hassid S, et al; Royal Belgian Society for Ear, Nose, Throat, Head and Neck Surgery. Standard ENT evaluation of sleep-disordered breathing patient: a consensus report. Acta Otorhinolaryngol Belg. 2002;56(2):127-37. PMID: 12092321.
3.3. Diagnóstico
Diante da mencionada variabilidade clínica e da elevada prevalência, a possibilidade de AOS deve ser considerada nos mais diversos contextos da atenção médica. Perguntas sobre ronco e sonolência diurna deveriam ser incluídas rotineiramente na história clínica. Durante o exame, achados de obesidade, retrognatia e mesmo hipertensão arterial podem chamar a atenção para a AOS. Nestes casos, deve ser conduzida uma avaliação detalhada, incluindo a caracterização do ronco, o relato de apneias presenciadas por terceiros e a ocorrência de episódios de sufocamento ou engasgos noturno. Estimativas do Tempo Total de Sono (TTS) e da presença e gravidade da sonolência diurna pela Escala de Sonolência de Epworth precisam ser obtidas. Noctúria, cefaleia matinal, fragmentação do sono, défice de memória e concentração estão entre os sintomas a serem ativamente investigados. Como já descrito, o exame físico, com ênfase nos sistemas neurológico, respiratório e cardiovascular, é importante para identificar pacientes com risco aumentado de AOS. Alguns subgrupos específicos devem receber também atenção especial, como motoristas profissionais, seja pela alta prevalência quanto pelos riscos de acidentes que a AOS acarreta nesses indivíduos (Quadro 3).
É necessário enfatizar que a impressão clínica, baseada na anamnese e no exame físico, é importante, porém insuficiente para o diagnóstico da AOS, que requer confirmação objetiva pela polissonografia ou pelo monitor portátil.8383 Bittencourt LR. Diagnóstico e tratamento da síndrome da apneia obstrutiva do sono (SAOS): Guia Prático. São Paulo: Livraria Médica Paulista; 2008. Estudo de 594 pacientes encaminhados para o laboratório do sono demonstrou que a impressão subjetiva tem apenas 60% de sensibilidade e 63% de especificidade. Os sintomas e sinais isolados também não possuem valor preditivo satisfatório para AOS.8686 Hoffstein V, Szalai JP. Predictive value of clinical features in diagnosing obstructive sleep apnea. Sleep. 1993;16(2):118-22. PMID: 8446830.
Algoritmos têm sido propostos no intuito de facilitar a identificação de casos de AOS, embora, em sua maioria, tenham se mostrado de utilidade limitada.8787 Bianchi MT. Screening for obstructive sleep apnea: bayes weighs in. Open Sleep J. 2009;2:56-9.,8888 Eiseman NA, Westover MB, Mietus JE, Thomas RJ, Bianchi MT. Classification algorithms for predicting sleepiness and sleep apnea severity. J Sleep Res. 2012;21(1):101-12. doi: 10.1111/j.1365-2869.2011.00935.x.
https://doi.org/10.1111/j.1365-2869.2011...
O STOP (Snoring, Tiredness, Observed apnea, high blood Pressure), que avalia ronco, fadiga, apneia presenciada e pressão arterial elevada usando como padrão-ouro o IAH acima de cinco eventos por hora, tem sensibilidade de 65,6% e especificidade de 60%.8989 Chung F, Yegneswaran B, Liao P, Chung SA, Vairavanathan S, Islam S, et al. STOP questionnaire: a tool to screen patients for obstructive sleep apnea. Anesthesiology. 2008,108(5):812-21. doi: 10.1097/ALN.0b013e31816d83e4.
https://doi.org/10.1097/ALN.0b013e31816d...
O STOP-BANG (Body mass index, Age, Neck circumference, Gender), que incorpora aos parâmetros anteriores IMC, idade, perímetro cervical e sexo, pode aumentar a sensibilidade para 83,6%, porém com especificidade mais baixa − de 56,4%.9090 Abrishami A, Khajehdehi A, Chung F. A systematic review of screening questionnaires for obstructive sleep apnea. Can J Anaesth. 2010;57(5):423-38. doi: 10.1007/s12630-010-9280-x.
https://doi.org/10.1007/s12630-010-9280-...
O Questionário de Berlim (Figura 3) visa identificar pacientes com risco elevado de AOS pela combinação de itens que incluem dados antropométricos, ronco, apneias presenciadas por terceiros, sonolência excessiva diurna e hipertensão arterial. Este instrumento foi validado originalmente para aplicação na população geral, ao nível da Atenção Primária, e mais estudos são necessários para definir sua utilidade em paciente com doenças cardiovasculares. Em pacientes hipertensos, o Questionário de Berlim mostrou ter alta sensibilidade, mas especificidade relativamente baixa.2020 Drager LF, Genta PR, Pedrosa RP, Nerbass FB, Gonzaga CC, Krieger EM, et al. Characteristics and predictors of obstructive sleep apnea in patients with systemic hypertension. Am J Cardiol. 2010;105(8):1135-9. doi: 10.1016/j.amjcard.2009.12.017.
https://doi.org/10.1016/j.amjcard.2009.1...
Já em pacientes com hipertensão resistente9292 Margallo VS, Muxfeldt ES, Guimarães GM, Salles GF. Diagnostic accuracy of the Berlin questionnaire in detecting obstructive sleep apnea in patients with resistant hypertension. J Hypertens. 2014;32(10):2030-6. doi: 10.1097/HJH.0000000000000297.
https://doi.org/10.1097/HJH.000000000000...
e Infarto Agudo do Miocárdio (IAM),9393 Sert Kuniyoshi FH, Zellmer MR, Calvin AD, Lopez-Jimenez F, Albuquerque FN, van der Walt C, et al. Diagnostic accuracy of the Berlin Questionnaire in detecting sleep-disordered breathing in patients with a recent myocardial infarction. Chest. 2011;140(5):1192-7. doi: 10.1378/chest.10-2625.
https://doi.org/10.1378/chest.10-2625...
o Questionário de Berlim não foi útil na triagem da AOS. Recentemente, outro questionário, mais simples, o escore NoSAS (Figura 4),9494 Marti-Soler H, Hirotsu C, Marques-Vidal P, Vollenweider P, Waeber G, Preisig M, et al. The NoSAS score for screening of sleep-disordered breathing: a derivation and validation study. Lancet Respir Med. 2016;4(9):742-8. doi: 10.1016/S2213-2600(16)30075-3.
https://doi.org/10.1016/S2213-2600(16)30...
foi validado na população brasileira, mostrando algumas vantagens em relação ao Berlim e ao STOP-BANG incluindo a consistência de desempenho nas diferentes gravidades da AOS. No entanto, ainda não há evidências se este questionário é uma boa ferramenta para triagem da AOS em pacientes com doenças cardiovasculares.
Questionário de Berlim. Fonte: Adaptado de Netzer et al.9191 Netzer NC, Stoohs RA, Netzer CM, Clark K, Strohl KP. Using the Berlin Questionnaire to identify patients at risk for sleep apnea syndrome. Ann Intern Med. 1999;131(7):485-91. PMID: 10507956.
3.3.1. Polissonografia Noturna
A polissonografia é o exame recomendado para identificar e descartar os diferentes distúrbios de sono, incluindo os respiratórios. “Polissonografia” é um termo genérico, que se refere ao registro simultâneo de algumas variáveis fisiológicas durante o sono, como Eletroencefalograma (EEG), Eletro-Oculograma (EOG), Eletromiograma (EMG), Eletrocardiograma (ECG), fluxo aéreo (nasal e oral), esforço respiratório (torácico e abdominal), movimentos corporais (pelo EMG), gases sanguíneos (saturação da oxi-hemoglobina - saturação periférica de oxigênio capilar − SpO2 − e concentração de dióxido de carbono), posição corporal, entre outras. É considerada, pela AASM,9595 Kushida CA, Littner MR, Morgenthaler T, Alessi CA, Bailey D, Coleman J Jr, et al. Practice parameters for the indications for polysomnography and related procedures: an update for 2005. Sleep. 2005;28(4):499-521. PMID: 16171294. o método diagnóstico padrão-ouro para os distúrbios de sono. O registro polissonográfico é realizado no laboratório, durante uma noite inteira de sono, com acompanhamento de um técnico especializado.9595 Kushida CA, Littner MR, Morgenthaler T, Alessi CA, Bailey D, Coleman J Jr, et al. Practice parameters for the indications for polysomnography and related procedures: an update for 2005. Sleep. 2005;28(4):499-521. PMID: 16171294.
3.3.2. Monitores Portáteis
Além da polissonografia, outros tipos de monitorização ambulatorial ou domiciliar têm sido utilizados para diagnóstico da AOS. A AASM9696 Practice parameters for use of portable recording in the assessment of obstructive sleep apnea. Standards of Practice Committee of the American Sleep Disorders Association. Sleep. 1994;17(4):372-7. PMID: 7973322. descreveu a polissonografia como o registro tipo 1, além dos outros seguintes tipos de monitores portáteis:
-
tipo 2: possui, no mínimo, sete canais de registro, incluindo EEG, EOG, EMG da região mentoniana, ECG, fluxo aéreo, esforço respiratório e SpO2. O registro é realizado na casa do paciente, sem acompanhamento técnico. A literatura ainda não apresenta evidências, validando esse método de registro.
-
tipo 3: possui, pelo menos, quatro canais de registro, incluindo fluxo aéreo, esforço respiratório, frequência cardíaca e SpO2. É considerado uma alternativa para diagnóstico em pacientes selecionados com alta probabilidade clínica de AOS. O relatório de uma força tarefa da AASM9797 Collop NA, Anderson WM, Boehlecke B, Claman D, Goldberg R, Gottlieb DJ, et al; Portable Monitoring Task Force of the American Academy of Sleep Medicine. Clinical guidelines for the use of unattended portable monitors in the diagnosis of obstructive sleep apnea in adult patients. Portable monitoring task force of the American Academy of Sleep Medicine. J Clin Sleep Med. 2007;3(7):737-47. PMID: 18198809. recomendou o uso dos monitores tipo 3 apenas em adultos, referindo-se à inexistência de dados que validem seu uso na população acima de 65 anos, crianças e indivíduos com comorbidades (pneumopatas, neuropatas e pacientes com doença cardiovascular).
-
tipo 4: monitora a SpO2 e/ou o fluxo aéreo. Não há evidências definitivas que suportem a recomendação deste tipo de monitor para diagnóstico de AOS.9797 Collop NA, Anderson WM, Boehlecke B, Claman D, Goldberg R, Gottlieb DJ, et al; Portable Monitoring Task Force of the American Academy of Sleep Medicine. Clinical guidelines for the use of unattended portable monitors in the diagnosis of obstructive sleep apnea in adult patients. Portable monitoring task force of the American Academy of Sleep Medicine. J Clin Sleep Med. 2007;3(7):737-47. PMID: 18198809.
Devido à alta prevalência de AOS e à tentativa de agilizar seu diagnóstico e tratamento, várias marcas e modelos de monitores portáteis estão disponíveis no mercado, que incluem diferentes parâmetros de registro. Uma classificação mais recente dos monitores portáteis, denominada SCOPER, foi baseada nos diferentes parâmetros de avaliação disponíveis nos diferentes modelos: sono, cardiovascular, oximetria, posição, esforço e respiração.9898 Collop NA, Tracy SL, Kapur V, Mehra R, Kuhlmann D, Fleishman SA, et al. Obstructive sleep apnea devices for out-of-center (OOC) testing: technology evaluation. J Clin Sleep Med. 2011;7(5):531-48. doi: 10.5664/JCSM.1328.
https://doi.org/10.5664/JCSM.1328...
O monitor utilizado para estudo ambulatorial deve ser escolhido com cuidado. Os fatores a serem considerados são a facilidade de uso pelo paciente, parâmetros de registro, facilidade de transmissão dos dados, capacidade de personalização da exibição dos dados brutos e do relatório, custo do dispositivo, custo dos itens consumíveis (cânulas e sensores descartáveis), recursos do banco de dados e disponibilidade de suporte técnico pelo fabricante.
3.4. Considerações desta Seção
Por sua elevada prevalência e heterogeneidade clínica, a AOS deve ser considerada dentro dos mais variados contextos da atenção médica. Pesquisa dos sintomas mais comumente relacionados à AOS deve ser incluída em qualquer avaliação de rotina. Pacientes com manifestações sugestivas e aqueles que pertencem a grupos de risco requerem avaliação mais detalhada. O exame físico, com ênfase nos sistemas neurológico, respiratório e cardiovascular, é importante para identificar os pacientes e as complicações da AOS. Apesar de sua importância, a impressão clínica isolada é insuficiente para o diagnóstico da AOS, de modo que os casos suspeitos devem ser encaminhados para confirmação diagnóstica, pela da realização da polissonografia ou, quando bem indicado, da monitorização portátil. Este último é custo eficaz e pode ser usado para a maioria dos casos suspeitos de AOS, conforme sugerido em publicação recente.9999 Corral J, Sánchez-Quiroga MA, Carmona-Bernal C, Sánchez-Armengol A, Sánchez-de-la-Torre A, Durán-Cantolla J, et al; Spanish Sleep Network. Conventional polysomnography is not necessary for the management of most patients with suspected obstructive sleep apnea. Noninferiority, Randomized Controlled Trial. Am J Respir Crit Care Med. 2017;196(9):1181-1190. doi: 10.1164/rccm.201612-2497OC.
https://doi.org/10.1164/rccm.201612-2497...
Algoritmos e questionários atualmente disponíveis apresentam valor limitado na identificação de casos e estratificação de risco. Como discutiremos nas repercussões cardiovasculares da AOS, em virtude dos resultados de recentes estudos randomizados, documento recente e polêmico do US Preventive Services Task Force (USPSTF) sugere que não há evidências definitivas que justifiquem o rastreamento da AOS em pacientes assintomáticos.100100 Bibbins-Domingo K, Grossman DC, Curry SJ, Davidson KW, Epling JW Jr, García FA, et al; US Preventive Services Task Force. Screening for obstructive sleep apnea in adults: US Preventive Services Task Force Recommendation Statement. JAMA. 2017;317(4):407-14. doi: 10.1001/jama.2016.20325.
https://doi.org/10.1001/jama.2016.20325...
4. Apneia Obstrutiva do Sono e Doenças Cardiovasculares
4.1. Efeitos Agudos da Apneia Obstrutiva do Sono
Pacientes portadores da AOS apresentam alterações hemodinâmicas agudas,101101 Weiss JW, Remsburg S, Garpestad E, Ringler J, Sparrow D, Parker JA. Hemodynamic consequences of obstructive sleep apnea. Sleep. 1996;19(5):388-97. PMID: 8843530. que, se perpetuadas, podem ocasionar prejuízo na função cardiovascular documentada pelo aumento na taxa de mortalidade nesta população.102102 Marin JM, Carrizo SJ, Vicente E, Agusti AG. Long-term cardiovascular outcomes in men with obstructive sleep apnoea-hypopnoea with or without treatment with continuous positive airway pressure: an observational study. Lancet. 2005;365(9464):1046-53. doi: 10.1016/S0140-6736(05)71141-7
https://doi.org/10.1016/S0140-6736(05)71...
Vários fatores contribuem para o dano cardiovascular e, possivelmente, inúmeros mecanismos estão envolvidos. No entanto, agudamente três fatores principais merecem destaque: hipóxia intermitente, despertares frequentes e alterações na pressão intratorácica. Estas alterações acabam por desencadear hiperatividade do sistema nervoso simpático, disfunção endotelial e inflamação.6161 Dempsey JA, Veasey SC, Morgan BJ, O'Donnell CP. Pathophysiology of sleep apnea. Physiol Rev. 2010;90(1):47-112. doi: 10.1152/physrev.00043.2008. Erratum in: Physiol Rev. 2010;90(2):797-8.
https://doi.org/10.1152/physrev.00043.20...
Na vigência de um evento respiratório obstrutivo, as variáveis hemodinâmicas e a atividade autonômica oscilam entre os períodos de normalidade ventilatória e obstrução. Aumentos na frequência cardíaca e na pressão arterial ocorrem tipicamente 5 a 7 segundos após o final da apneia, coincidindo com o microdespertar, o pico da ventilação e o nadir da saturação.103103 O'Donnell CP, Ayuse T, King ED, Schwartz AR, Smith PL, Robotham JL. Airway obstruction during sleep increases blood pressure without arousal. J Appl Physiol (1985). 1996;80(3):773-81. PMID: 8964736.,104104 Poyares D, Guilleminault C, Rosa A, Ohayon M, Koester U. Arousal, EEG spectral power and pulse transit time in UARS and mild OSAS subjects. Clin Neurophysiol. 2002;113(10):1598-606. PMID: 12350436. Estas alterações hemodinâmicas contrariam a fisiológica queda destas variáveis hemodinâmicas, que acompanham o sono normal e possivelmente corroboram o dano cardiovascular observado nestes pacientes. Durante o evento de apneia, ocorre estimulação parassimpática com observação de alentecimento no ciclo de frequência cardíaca e ocorrência de bradiarritmia. Após a abertura da via aérea, ocorre elevação da frequência cardíaca, possivelmente secundária à inibição do vago e ao microdespertar.
Esforços inspiratórios inefetivos acarretam redução na pressão intratorácica com consequente aumento na pressão transmural do Ventrículo Esquerdo (VE) e da pós-carga.105105 Carlson JT, Hedner J, Elam M, Ejnell H, Sellgren J, Wallin BG. Augmented resting sympathetic activity in awake patientes with obstructive sleep apnea. Chest. 1993;103(6):1763-8. PMID: 8404098. Além disto, as alterações na pressão intratorácica parecem intensificar a regurgitação mitral em pacientes que já apresentam esta condição, sendo um potencial mecanismos de piora da IC em pacientes portadores de AOS.106106 Pressman GS, Orban M, Leinveber P, Parekh K, Singh M, Kara T, et al. Effects of the Mueller maneuver on functional mitral regurgitation and implications for obstructive sleep apnea. Am J Cardiol. 2015;115(11):1563-7. doi: 10.1016/j.amjcard.2015.02.061.
https://doi.org/10.1016/j.amjcard.2015.0...
Concomitantemente, há aumento no retorno venoso ao Ventrículo Direito (VD), com comprometimento de seu relaxamento e deslocamento do septo interventricular para a esquerda, prejudicando o enchimento ventricular esquerdo.107107 Brinker JA, Weiss JL, Lappe DL, Rabson JL, Summer WR, Permutt S, et al. Leftward septal displacement during right ventricular loading in man. Circulation. 1980;61(3):626-33. PMID: 7353253. O uso da ecocardiografia durante a manobra de Müller, que mimetiza um evento de apneia obstrutiva, demonstra que as deformações longitudinais ventriculares direita e esquerda são comprometidas durante o evento respiratório, corroborando os efeitos deletérios exercidos pelas alterações das pressões torácicas no coração.108108 Koshino Y, Villarraga HR, Orban M, Bruce CJ, Pressman GS, Leinveber P, et al. Changes in left and right ventricular mechanics during the Mueller maneuver in healthy adults: a possible mechanism for abnormal cardiac function in patients with obstructive sleep apnea. Circ Cardiovasc Imaging. 2010;3(3):282-9. doi: 10.1161/CIRCIMAGING.109.901561.
https://doi.org/10.1161/CIRCIMAGING.109....
Pacientes com AOS experimentam episódios repetidos de hipóxia e reoxigenação durante a cessação transitória da respiração, o que acaba por estimular o sistema nervoso simpático, acarretando estresse oxidativo, disfunção endotelial e, possivelmente, vários outros mecanismos ainda em investigação.109109 Zamarrón C, Valdés Cuadrado L, Alvarez-Sala R. Pathophysiologic mechanisms of cardiovascular disease in obstructive sleep apnea syndrome. Pulm Med. 2013;2013:521087. doi: 10.1155/2013/521087.
https://doi.org/10.1155/2013/521087...
Modelos animais de hipóxia intermitente/reoxigenação apresentam resultados promissores em relaçãos aos potenciais mecanismos associados às suas consequências deletérias. Ratos expostos à hipóxia intermitente desenvolvem hipertensão,110110 Fletcher EC, Bao G, Miller CC 3rd. Effect of recurrent episodic hypocapnic, eucapnic, and hypercapnic hypoxia on systemic blood pressure. J Appl Physiol. 1995;78(4):1516-21. PMID: 7615464. mas esta resposta é atenuada quando há denervação do seio carotídeo, demonstrando que o acionamento desta via e a estimulação simpática são importantes vias para a hipertensão.111111 Fletcher EC, Bao G. Influence of hypoxia, chemoreceptors, and sympathic activity in chronic hypertension in the rat. In: Lenfant C, Bradley TD, Floras JS. (editors). Sleep apnea: implications in cardiovascular and cerebrovascular disease. New York: Marcel Dekker; 2000. p. 181-211.
Finalmente, o microdespertar participa ativamente na estimulação autonômica produzindo resposta hipertensiva aguda adicional ao evento respiratório.3 Estudo com voluntários normais demonstrou que o estimulo de despertar durante o sono causou aumento na atividade nervosa simpática, observada pela microneurografia, associada a aumentos transitórios da pressão arterial.112112 Somers VK, Dyken ME, Mark AL, Abboud FM. Sympathetic-nerve activity during sleep in normal subjects. N Engl J Med. 1993;328(5):303-7. doi: 10.1056/NEJM199302043280502.
https://doi.org/10.1056/NEJM199302043280...
4.2. Efeitos Crônicos da Apneia Obstrutiva do Sono
4.2.1. Hipertensão Arterial Sistêmica
Até o momento, a relação mais bem definida no impacto cardiovascular da AOS é com a HAS. De forma resumida, os potenciais mecanismos agudos e crônicos que associam a AOS com a HAS são múltiplos (Quadro 4).113113 Pedrosa RP, Krieger EM, Lorenzi-Filho G, Drager LF. Recent advances of the impact of obstructive sleep apnea on systemic hypertension. Arq Bras Cardiol. 2011;97(2):e40-7. doi: http://dx.doi.org/10.1590/S0066-782X2011005000017.
http://dx.doi.org/10.1590/S0066-782X2011...
,114114 Nicholl DD, Hanly PJ, Poulin MJ, Handley GB, Hemmelgarn BR, Sola DY, et al. Evaluation of continuous positive airway pressure therapy on renin-angiotensin system activity in obstructive sleep apnea. Am J Respir Crit Care Med. 2014;190(5):572-80. doi: 10.1164/rccm.201403-0526OC.
https://doi.org/10.1164/rccm.201403-0526...
Mecanismos fisiopatológicos da hipertensão arterial sistêmica (HAS) e apneia obstrutiva do sono (AOS)
Estudos com grande número de indivíduos demontraram clara associação entre a presença e a gravidade da AOS e o aumento na incidência de HAS.2525 Peppard PE, Young T, Palta M, Skatrud J. Prospective study of the association between sleep-disordered breathing and hypertension. N Engl J Med. 2000;342(19):1378-84. doi: 10.1056/NEJM200005113421901.
https://doi.org/10.1056/NEJM200005113421...
,115115 Marin JM, Agusti A, Villar I, Forner M, Nieto D, Carrizo SJ, et al. Association between treated and untreated obstructive sleep apnea and risk of hypertension. JAMA. 2012;307(20):2169-76. doi: 10.1001/jama.2012.3418.
https://doi.org/10.1001/jama.2012.3418...
Importante salientar que, apesar da AOS acontecer apenas no período noturno, seu impacto negativo na pressão arterial se dá nas 24 horas.
4.2.1.1. Descenso Pressórico do Sono e Apneia Obstrutiva do Sono
Os episódios de apneia e hipopneia promovem uma série de fenômenos que contribuem para a elevação da pressão arterial durante o sono. Estas elevações se dão particularmente ao final de cada evento obstrutivo.116116 Somers VK, Dyken ME, Clary MP, Abboud FM. Sympathetic neural mechanisms in obstructive sleep apnea. J Clin Invest. 1995;96(4):1897-904. doi: 10.1172/JCI118235.
https://doi.org/10.1172/JCI118235...
Por causa deste comportamento, pacientes com AOS podem apresentar alterações no padrão do descenso fisiológico da pressão arterial pela Monitorização Ambulatorial da Pressão Arterial (MAPA),117117 Davies CW, Crosby JH, Mullins RL, Barbour C, Davies RJ, Stradling JR. Case-control study of 24 hour ambulatory blood pressure in patients with obstructive sleep apnoea and normal matched control subjects. Thorax. 2000;55(9):736-40. PMID: 10950890.,118118 Wolf J, Hering D, Narkiewicz K. Non-dipping pattern of hypertension and obstructive sleep apnea syndrome. Hypertens Res. 2010;33(9):867-71. doi: 10.1038/hr.2010.153.
https://doi.org/10.1038/hr.2010.153...
podendo até mesmo ter o diagnóstico de hipertensão noturna por esta monitorização na ausência de hipertensão conhecida.119119 Baguet JP, Hammer L, Lévy P, Pierre H, Rossini E, Mouret S, et al. Night-time and diastolic hypertension are common and underestimated conditions in newly diagnosed apnoeic patients. J Hypertens. 2005;23(3):521-7. PMID: 15716692. Esta alteração do descenso noturno parece ser mais frequentemente observada em pacientes hipertensos da raça negra120120 Ancoli-Israel S, Stepnowsky C, Dimsdale J, Marler M, Cohen-Zion M, Johnson S. The effect of race and sleep-disordered breathing on nocturnal BP "dipping": analysis in an older population. Chest. 2002;122(4):1148-55. PMID: 12377835. ou em idosos normotensos com AOS.121121 Onen SH, Lesourd B, Ouchchane L, Lin JS, Dubray C, Gooneratne NS, et al. Occult nighttime hypertension in daytime normotensive older patients with obstructive sleep apnea. J Am Med Dir Assoc. 2012;13(8):752-6. doi: 10.1016/j.jamda.2012.07.003.
https://doi.org/10.1016/j.jamda.2012.07....
Em estudo recente, Seif et al.122122 Seif F, Patel SR, Walia HK, Rueschman M, Bhatt DL, Blumenthal RS, et al. Obstructive sleep apnea and diurnal nondipping hemodynamic indices in patients at increased cardiovascular risk. J Hypertens. 2014;32(2):267-75. doi: 10.1097/HJH.0000000000000011.
https://doi.org/10.1097/HJH.000000000000...
mostraram aumento de 4% e 10% da probabilidade de alteração no descenso da pressão arterial sistólica e diastólica, respectivamente, para cada aumento de uma unidade no IAH. A despeito destas evidências, ainda não se sabe se as alterações do descenso noturno têm boa acurácia na predição da AOS.
4.2.1.2. Pré-hipertensão e Hipertensão Arterial Sistêmica Mascarada
Existem evidências sugerindo que a presença de pré-hipertensão e a HAS mascarada são comuns em pacientes com AOS considerados normotensos.123123 Baguet JP, Lévy P, Barone-Rochette G, Tamisier R, Pierre H, Peeters M, et al. Masked hypertension in obstructive sleep apnea syndrome. J Hypertens. 2008;26(5):885-92. doi: 10.1097/HJH.0b013e3282f55049.
https://doi.org/10.1097/HJH.0b013e3282f5...
124 Drager LF, Diegues-Silva L, Diniz PM, Bortolotto LA, Pedrosa RP, Couto RB, et al. Obstructive sleep apnea, masked hypertension, and arterial stiffness in men. Am J Hypertens. 2010;23(3):249-54. doi: 10.1038/ajh.2009.246.
https://doi.org/10.1038/ajh.2009.246...
-125125 Drager LF, Pedrosa RP, Diniz PM, Diegues-Silva L, Marcondes B, Couto RB, et al. The effects of continuous positive airway pressure on prehypertension and masked hypertension in men with severe obstructive sleep apnea. Hypertension. 2011;57(3):549-55. doi: 10.1161/HYPERTENSIONAHA.110.165969.
https://doi.org/10.1161/HYPERTENSIONAHA....
De forma interesante, estudo randomizado mostrou que a porcentagem de pacientes com AOS importante com pré-hipertensão e HAS mascarada reduziu após o tratamento com o CPAP.125125 Drager LF, Pedrosa RP, Diniz PM, Diegues-Silva L, Marcondes B, Couto RB, et al. The effects of continuous positive airway pressure on prehypertension and masked hypertension in men with severe obstructive sleep apnea. Hypertension. 2011;57(3):549-55. doi: 10.1161/HYPERTENSIONAHA.110.165969.
https://doi.org/10.1161/HYPERTENSIONAHA....
4.2.1.3. Hipertensão Arterial Sistêmica Resistente
A HAS resistente é definida como a situação clínica caracterizada pelo descontrole da pressão arterial, apesar do uso concomitante de três agentes anti-hipertensivos, incluindo um diurético, ou a necessidade de mais do que três medicamentos para controlar a pressão arterial.126126 Rimoldi SF, Messerli FH, Bangalore S, Scherrer U. Resistant hypertension: what the cardiologist needs to know. Eur Heart J. 2015;36(40):2686-95. doi: 10.1093/eurheartj/ehv392.
https://doi.org/10.1093/eurheartj/ehv392...
A prevalência de HAS resistente tem aumentado ao longo dos últimas décadas, mas muitos pacientes têm baixa adesão ao tratamento medicamentoso e apenas pequena proporção deles é verdadeiramente hipertensa resistente.
Os pacientes com HAS resistente são aqueles de maior risco cardiovascular e pior prognóstico, ou seja, aqueles que têm maior benefício do controle rigoroso da pressão arterial.126126 Rimoldi SF, Messerli FH, Bangalore S, Scherrer U. Resistant hypertension: what the cardiologist needs to know. Eur Heart J. 2015;36(40):2686-95. doi: 10.1093/eurheartj/ehv392.
https://doi.org/10.1093/eurheartj/ehv392...
Neste sentido, é de fundamental importância o reconhecimento de causas potencialmente reversíveis de HAS nesta população. A AOS é a causa secundária de hipertensão mais comumente associada à HAS resistente, sendo encontrada em 64% dos pacientes.2323 Pedrosa RP, Drager LF, Gonzaga CC, Sousa MG, de Paula LK, Amaro AC, et al. Obstructive sleep apnea: the most common secondary cause of hypertension associated with resistant hypertension. Hypertension. 2011;58(5):811-7. doi: 10.1161/HYPERTENSIONAHA.111.179788
https://doi.org/10.1161/HYPERTENSIONAHA....
Nesta população, roncos frequentes, circunferência cervical aumentada (> 41 cm para mulheres e > 43 cm para homens) e idade >50 anos são preditores de AOS.2323 Pedrosa RP, Drager LF, Gonzaga CC, Sousa MG, de Paula LK, Amaro AC, et al. Obstructive sleep apnea: the most common secondary cause of hypertension associated with resistant hypertension. Hypertension. 2011;58(5):811-7. doi: 10.1161/HYPERTENSIONAHA.111.179788
https://doi.org/10.1161/HYPERTENSIONAHA....
O fato da AOS ser muito frequente entre os pacientes com HAS resistente não quer dizer necessariamente que a AOS não tratada esteja causando a HAS, mas ela pode estar contribuindo para o descontrole pressórico.
Dentre os indivíduos com HAS resistente, observa-se também prevalência significativa de hiperaldosteronismo, chegando a 28% de concomitância destas comorbidades.127127 Gonzaga CC, Gaddam KK, Ahmed MI, Pimenta E, Thomas SJ, Harding SM, et al. Severity of obstructive sleep apnea is related to aldosterone status in subjects with resistant hypertension. J Clin Sleep Med. 2010;6(4):363-8. PMID: 20726285. O excesso de aldosterona promoveria maior retenção de volume nos indivíduos com HAS resistente, piorando ainda mais a AOS quando presente, que, por sua vez, poderia ativar ainda mais o sistema nervoso simpático e sistema renina-angiotensina-aldosterona, fechando um ciclo em que AOS e HAS resistente estariam interligadas também pelo excesso de aldosterona.128128 Genta-Pereira DC, Pedrosa RP, Lorenzi-Filho G, Drager LF. Sleep disturbances and resistant hypertension: association or causality? Curr Hypertens Rep. 2014;16(8):459. doi: 10.1007/s11906-014-0459-3.
https://doi.org/10.1007/s11906-014-0459-...
Contribui com esta hipótese o fato de que, em estudo preliminar, 12 pacientes com HAS resistente tiveram boa resposta ao tratamento com espironolactona (25 a 50 mg ao dia), obtendo-se melhora da gravidade da AOS, que saiu da forma grave para a moderada.129129 Gaddam K, Pimenta E, Thomas SJ, Cofield SS, Oparil S, Harding SM, et al. Spironolactone reduces severity of obstructive sleep apnoea in patients with resistant hypertension: a preliminary report. J Hum Hypertens. 2010;24(8):532-7. doi: 10.1038/jhh.2009.96.
https://doi.org/10.1038/jhh.2009.96...
Estudo randomizado mostrou recentemente que a excreção de aldosterona foi reduzida em pacientes com AOS e HAS resistente, mas somente no grupo que teve boa adesão ao tratamento com o CPAP.130130 de Souza F, Muxfeldt ES, Margallo V, Cortez AF, Cavalcanti AH, Salles GF. Effects of continuous positive airway pressure treatment on aldosterone excretion in patients with obstructive sleep apnoea and resistant hypertension: a randomized controlled trial. J Hypertens. 2017;35(4):837-844. doi: 10.1097/HJH.0000000000001254.
https://doi.org/10.1097/HJH.000000000000...
Novos estudos randomizados e com poder estatístico adequado são necessários para avaliar o papel da aldosterona na AOS e HAS, especialmente no contexto da HAS resistente, possibilitando futuramente novas opções terapêuticas para ambas as comorbidades.
4.2.1.4. Impacto do Tratamento da Apneia Obstrutiva do Sono (CPAP e Avanço Mandibular) na Pressão Arterial
Até o momento, diversos estudos randomizados demonstram redução média da pressão arterial de cerca de 2,5 mmHg com o tratamento com CPAP.131131 Fatureto-Borges F, Lorenzi-Filho G, Drager LF. Effectiveness of continuous positive airway pressure in lowering blood pressure in patients with obstructive sleep apnea: a critical review of the literature. Integr Blood Press Control. 2016;9:43-7. doi: 10.2147/IBPC.S70402.
https://doi.org/10.2147/IBPC.S70402...
Em geral, esta resposta é maior quanto maior for o uso do CPAP.132132 Bazzano LA, Khan Z, Reynolds K, He J. Effect of nocturnal nasal continuous positive airway pressure on blood pressure in obstructive sleep apnea. Hypertension. 2007;50(2):417-23. doi: 10.1161/HYPERTENSIONAHA.106.085175.
https://doi.org/10.1161/HYPERTENSIONAHA....
No entanto, existe grande confusão na literatura, pois diversos estudos envolveram indivíduos normotensos, misturaram normotensos com hipertensos, estudaram hipertensos controlados e alguns poucos hipertensos não controlados.131131 Fatureto-Borges F, Lorenzi-Filho G, Drager LF. Effectiveness of continuous positive airway pressure in lowering blood pressure in patients with obstructive sleep apnea: a critical review of the literature. Integr Blood Press Control. 2016;9:43-7. doi: 10.2147/IBPC.S70402.
https://doi.org/10.2147/IBPC.S70402...
Curiosamente, há evidências de que a redução na pressão arterial com o CPAP é maior para pacientes com sintomas relacionados à AOS (como sonolência) em relação àqueles com AOS assintomáticos ou oligossintoáticos.133133 Bratton DJ, Stradling JR, Barbé F, Kohler M. Effect of CPAP on blood pressure in patients with minimally symptomatic obstructive sleep apnoea: a meta-analysis using individual patient data from four randomized controlled trials. Thorax. 2014;69(12):1128-1135. doi: 10.1136/thoraxjnl-2013-204993.
https://doi.org/10.1136/thoraxjnl-2013-2...
As razões para estas diferenças não são claras e nem podem ser explicadas por diferenças na adesão ao CPAP. Esta heterogeneidade de pacientes pode, em parte, explicar esta modesta redução na pressão arterial promovida pelo CPAP.
No campo da HAS resistente, a magnitude do efeito da redução da pressão arterial parece mais significativa. Dos seis estudos randomizados disponíveis, sendo três deles brasileiros, somente um não mostrou benefício.134134 Lozano L, Tovar JL, Sampol G, Romero O, Jurado MJ, Segarra A, et al. Continuous positive airway pressure treatment in sleep apnea patients with resistant hypertension: a randomized, controlled trial. J Hypertens. 2010;28(10):2161-2168. doi: 10.1097/HJH.0b013e32833b9c63.
https://doi.org/10.1097/HJH.0b013e32833b...
135 Pedrosa RP, Drager LF, de Paula LK, Amaro AC, Bortolotto LA, Lorenzi-Filho G. Effects of OSA treatment on BP in patients with resistant hypertension: a randomized trial. Chest. 2013;144(5):1487-94. doi: 10.1378/chest.13-0085.
https://doi.org/10.1378/chest.13-0085...
136 de Oliveira AC, Martinez D, Massierer D, Gus M, Gonçalves SC, Ghizzoni F, et al. The antihypertensive effect of positive airway pressure on resistant hypertension of patients with obstructive sleep apnea: a randomized, double-blind, clinical trial. Am J Respir Crit Care Med. 2014;190(3):345-7. doi: 10.1164/rccm.201403-0479LE.
https://doi.org/10.1164/rccm.201403-0479...
137 Muxfeldt ES, Margallo V, Costa LM, Guimarães G, Cavalcante AH, Azevedo JC, et al. Effects of continuous positive airway pressure treatment on clinic and ambulatory blood pressures in patients with obstructive sleep apnea and resistant hypertension: a randomized controlled trial. Hypertension. 2015;65(4):736-42. doi: 10.1161/HYPERTENSIONAHA.
https://doi.org/10.1161/HYPERTENSIONAHA...
138 Iftikhar IH, Valentine CW, Bittencourt LR, Cohen DL, Fedson AC, Gíslason T, et al. Effects of continuous positive airway pressure on blood pressure in patients with resistant hypertension and obstructive sleep apnea: a meta-analysis. J Hypertens. 2014;32(12):2341-50. doi: 10.1097/HJH.0000000000000372.
https://doi.org/10.1097/HJH.000000000000...
-139139 Martinez-Garcia MA, Capote F, Campos-Rodriguez F, Lloberes P, Díaz de Atauri MJ, Somoza M, et al; Spanish Sleep Network. Effect of CPAP on blood pressure in patients with obstructive sleep apnea and resistant hypertension: the HIPARCO randomized clinical trial. JAMA. 2013;310(22):2407-15. doi: 10.1001/jama.2013.281250.
https://doi.org/10.1001/jama.2013.281250...
Uma metanálise recente sintetizou os dados de estudos randomizados em pacientes com HAS resistente, demonstrando redução da pressão arterial sistólica e diastólica de 24 horas de -4,78 mmHg (Intervalo de Confiança de 95% − IC95% -7,95 - -1,61) e -2,95 mmHg (IC95% -5,37 - -0,53) favorecendo o grupo CPAP, respectivamente.140140 Liu L, Cao Q, Guo Z, Dai Q. Continuous positive airway pressure in patients with obstructive sleep apnea and resistant hypertension: a meta-analysis of randomized controlled trials. J Clin Hypertens (Greenwich). 2016;18(2):153-8. doi: 10.1111/jch.12639.
https://doi.org/10.1111/jch.12639...
Na prática clínica, no entanto, os resultados são muito variáveis: alguns pacientes têm reduções de 20 mmHg ou mais com o tratamento da AOS, enquanto outros não apresentam qualquer benefício com o CPAP. A identificação de marcadores de resposta pressórica tem sido uma área de interesse recente na literatura.141141 Sánchez-de-la-Torre M, Khalyfa A, Sánchez-de-la-Torre A, Martinez-Alonso M, Martinez-García MA, Barceló A, et al; Spanish Sleep Network. Precision medicine in patients with resistant hypertension and obstructive sleep apnea: blood pressure response to continuous positive airway pressure treatment. J Am Coll Cardiol. 2015;66(9):1023-32. doi: 10.1016/j.jacc.2015.06.1315.
https://doi.org/10.1016/j.jacc.2015.06.1...
No que se refere aos outros tratamentos da AOS, o uso de dispositivos de avanço mandibular, que tracionam a mandíbula para frente e, consequentemente, a base da língua, mostraram, em geral, reduções da pressão arterial e devem ser considerados como tratamento alternativo em pacientes não aderentes ao CPAP ou em pacientes com AOS leve/moderada. Recente metanálise demonstrou redução similar na pressão arterial sistólica e na diastólica após tratamento da AOS com estes dispositivos de avanço mandibular (~ 2,5 mmHg).142142 Bratton DJ, Gaisl T, Wons AM, Kohler M. CPAP vs mandibular advancement devices and blood pressure in patients with obstructive sleep apnea: a systematic review and meta-analysis. JAMA. 2015;314(21):2280-93. doi: 10.1001/jama.2015.16303.
https://doi.org/10.1001/jama.2015.16303...
No entanto, o número de estudos é menor, e a mesma questão de misturar pacientes com diferentes características também é observada com a avaliação do avanço mandibular na pressão arterial. Em estudo randomizado com 150 pacientes, o avanço mandibular melhorou a gravidade da AOS, mas não foi capaz de melhorar a função endotelial e nem a pressão arterial quando comparado ao grupo placebo.143143 Gagnadoux F, Pépin JL, Vielle B, Bironneau V, Chouet-Girard F, Launois S, et al. Impact of mandibular advancement therapy on endothelial function in severe obstructive sleep apnea. Am J Respir Crit Care Med. 2017;195(9):1244-1252. doi: 10.1164/rccm.201609-1817OC.
https://doi.org/10.1164/rccm.201609-1817...
4.2.1.5. Impacto de Tratamentos da Hipertensão Arterial Sistêmica na Gravidade da Apneia Obstrutiva do Sono
Não existem estudos definitivos quanto ao uso de medicações anti-hipertensivas específicas para os pacientes hipertensos portadores de AOS. A clonidina pode reduzir o sono REM e, então, diminuir os episódios de apneia durante esta fase do sono e melhorar a hipoxemia noturna.144144 Issa FG. Effect of clonidine in obstructive sleep apnea. Am Rev Respir Dis. 1992;145(2 Pt 1):435-9. doi: 10.1164/ajrccm/145.2_Pt_1.435.
https://doi.org/10.1164/ajrccm/145.2_Pt_...
Uma comparação entre cinco classes de drogas comumente utilizadas (atenolol, amlodipino, enalapril, losartan e hidroclorotiazida) não mostrou diferença na gravidade da AOS. Todas as drogas tiveram efeitos similares na pressão arterial diurna, mas o atenolol apresentou discreta melhora na pressão arterial noturna, em comparação às demais.145145 Kraiczi H, Hedner J, Peker Y, Grote L. Comparison of atenolol, amlodipine, enalapril, hydrochlorothiazide, and losartan for antihypertensive treatment in patients with obstructive sleep apnea. Am J Respir Crit Care Med. 2000;161(5):1423-8. doi: 10.1164/ajrccm.161.5.9909024.
https://doi.org/10.1164/ajrccm.161.5.990...
Em termos comparativos, um estudo destacou que o impacto de medicação anti-hipertensiva (losartan) na redução da pressão arterial foi melhor que os efeitos com o uso do CPAP isoladamente.146146 Pépin JL, Tamisier R, Barone-Rochette G, Launois SH, Levy P, Baguet JP. Comparison of continuous positive airway pressure and valsartan in hypertensive patients with sleep apnea. Am J Respir Crit Care Med. 2010;182(7):954-60. doi: 10.1164/rccm.200912-1803OC.
https://doi.org/10.1164/rccm.200912-1803...
No entanto, a combinação de medicamentos anti-hipertensivos com o CPAP foi associada com efeitos aditivos na pressão arterial.146146 Pépin JL, Tamisier R, Barone-Rochette G, Launois SH, Levy P, Baguet JP. Comparison of continuous positive airway pressure and valsartan in hypertensive patients with sleep apnea. Am J Respir Crit Care Med. 2010;182(7):954-60. doi: 10.1164/rccm.200912-1803OC.
https://doi.org/10.1164/rccm.200912-1803...
O uso da espironolactona pode ter benefícios no tratamento da pressão arterial em pacientes com AOS e HAS resistente.129129 Gaddam K, Pimenta E, Thomas SJ, Cofield SS, Oparil S, Harding SM, et al. Spironolactone reduces severity of obstructive sleep apnoea in patients with resistant hypertension: a preliminary report. J Hum Hypertens. 2010;24(8):532-7. doi: 10.1038/jhh.2009.96.
https://doi.org/10.1038/jhh.2009.96...
Além do efeito pressórico per se, este beneficio da espironolactona pode ser mediado pela redução do edema em vias aéreas superiores e, consequentemente, da gravidade da AOS.147147 White LH, Bradley TD, Logan AG. Pathogenesis of obstructive sleep apnoea in hypertensive patients: role of fluid retention and nocturnal rostral fluid shift. J Hum Hypertens. 2015;29(6):342-50. doi: 10.1038/jhh.2014.94.
https://doi.org/10.1038/jhh.2014.94...
A despeito destas evidências, não existem estudos comparando a espironolactona vs. outros anti-hipertensivos para chancelar a preferência pelo uso desta medicação em pacientes hipertensos com AOS.
Finalmente, a denervação renal para controle da pressão arterial tem sido sugerida com possível efeito benéfico na redução da pressão arterial e na gravidade da AOS.148148 Witkowski A, Prejbisz A, Florczak E, Kadziela J, Sliwinski P, Bielen P, et al. Effects of renal sympathetic denervation on blood pressure, sleep apnea course, and glycemic control in patients with resistant hypertension and sleep apnea. Hypertension. 2011;58(4):559-65. doi: 10.1161/HYPERTENSIONAHA.111.173799.
https://doi.org/10.1161/HYPERTENSIONAHA....
,149149 Kario K, Bhatt DL, Kandzari DE, Brar S, Flack JM, Gilbert C, et al. Impact of renal denervation on patients with obstructive sleep apnea and resistant hypertension: insights from the SYMPLICITY HTN-3 Trial. Circ J. 2016;80(6):1404-12. doi: 10.1253/circj.CJ-16-0035.
https://doi.org/10.1253/circj.CJ-16-0035...
Atribuiu-se este achado, entre outros fatores, à obtenção de menor ativação simpática renal e sistêmica, levando à diminuição da ativação do sistema renina-angiotensina e, consequentemente, à redução da retenção de volume, conforme mecanismo previamente citado. No entanto, diante de resultados controversos,150150 Bhatt DL, Kandzari DE, O'Neill WW, D'Agostino R, Flack JM, Katzen BT, et al; SYMPLICITY HTN-3 Investigators. A controlled trial of renal denervation for resistant hypertension. N Engl J Med. 2014;370(15):1393-401. doi: 10.1056/NEJMoa1402670.
https://doi.org/10.1056/NEJMoa1402670...
as evidências atuais sugerem que a denervação renal só deva ser utilizada em estudos clínicos, e não deve ser sugerida também para o paciente com AOS na prática clínica.
4.2.2. Arritmias
Evidências apontam que até 60% dos pacientes portadores de AOS apresentam algum tipo de arritmia cardíaca.151151 Guilleminault C, Connolly SJ, Winkle RA. Cardiac arrhythmia and conduction disturbances during sleep in 400 patients with sleep apnea syndrome Am J Cardiol. 1983;52(5):490-4. PMID: 6193700. Quando se avalia a ocorrência de anormalidades do ritmo cardíaco durante à noite, pacientes portadores de AOS apresentam mais frequentemente esta anormalidade, e a prevalência de arritmias cardíacas aumenta em paralelo à elevação da gravidade da AOS.152152 Cintra FD, Leite RP, Storti LJ, Bittencourt LA, Poyares D, Castro LD, et al. Sleep apnea and nocturnal cardiac arrhythmia: a populational study. Arq Bras Cardiol. 2014;103(5):368-74. doi: http://dx.doi.org/10.5935/abc.20140142
http://dx.doi.org/10.5935/abc.20140142...
Os mecanismos envolvidos na ocorrência de arritmias cardíacas nos pacientes com AOS provavelmente são multifatoriais. A hipóxia intermitente e as alterações da pressão intratorácica são potentes estímulos para o sistema nervoso simpático, o que pode contribuir com o desencadeamento de arritmias catecolaminérgicas. Além disto, estudos avaliando a estrutura cardíaca pela ecocardiografia tridimensional demonstram importante disfunção e remodelamento atrial esquerdo em pacientes portadores de AOS, o que poderia contribuir para o desencadeamento de arritmias atriais.153153 Oliveira W, Campos O, Bezerra Lira-Filho E, Cintra FD, Vieira M, Ponchirolli A, et al. Left atrial volume and function in patients with obstructive sleep apnea assessed by real-time three-dimensional echocardiography. J Am Soc Echocardiogr. 2008;21(12):1355-61. doi: 10.1016/j.echo.2008.09.007.
https://doi.org/10.1016/j.echo.2008.09.0...
,154154 Drager LF, Bortolotto LA, Pedrosa RP, Krieger EM, Lorenzi-Filho G. Left atrial diameter is independently associated with arterial stiffness in patients with obstructive sleep apnea: potential implications for atrial fibrillation. Int J Cardiol. 2010;144(2):257-9. doi: 10.1016/j.ijcard.2009.01.018.
https://doi.org/10.1016/j.ijcard.2009.01...
4.2.2.1. Fibrilação Atrial
A FA e a AOS guardam alguns fatores de risco em comum, como o aumento da idade e a obesidade. Dados epidemiológicos sugerem associação independente entre as duas condições. A prevalência de AOS é maior em pacientes com FA, indicando que a AOS pode contribuir para o desencadeamento e a manutenção de arritma cardíaca.4646 Braga B, Poyares D, Cintra F, Guilleminault C, Cirenza C, Horbach S, et al. Sleep-disordered breathing and chronic atrial fibrillation. Sleep Med 2009;10(2):212-6. doi: 10.1016/j.sleep.2007.12.007.
https://doi.org/10.1016/j.sleep.2007.12....
,155155 Gami AS, Pressman G, Caples SM, Kanagala R, Gard JJ, Davison DE, et al. Association of atrial fibrillation and obstructive sleep apnea. Circulation. 2004;110(4):364-7. doi: 10.1161/01.CIR.0000136587.68725.8E.
https://doi.org/10.1161/01.CIR.000013658...
De fato, em pacientes que foram submetidos à cardioversão elétrica da FA, observaram-se 82% de recorrência nos pacientes com AOS sem tratamento ou com tratamento inadequado, e 42% de recorrência nos pacientes tratados.156156 Kanagala R, Murali NS, Friedman PA, Ammash NM, Gersh BJ, Ballman KV, et al. Obstructive sleep apnea and recurrence of atrial fibrillation. Circulation. 2003;107(20):2589-94. doi: 10.1161/01.CIR.0000068337.25994.21.
https://doi.org/10.1161/01.CIR.000006833...
Além disto, no grupo de pacientes não tratados, a recorrência foi ainda maior entre aqueles que apresentavam maior queda na saturação de oxigênio durante o evento de apneia. Estes dados sugerem a importante participação da AOS nos mecanismos fisiopatológicos da FA, além de demonstrar a importância do reconhecimento e do tratamento adequado desta condição.
O tratamento da AOS reduz o risco de recorrência de FA também nos pacientes submetidos à ablação por cateter. Um estudo com 426 pacientes submetidos ao isolamento elétrico das veias pulmonares, 62 pacientes apresentaram AOS confirmada pela polissonografia (32 pacientes usaram o CPAP, e 30 pacientes permaneceram sem tratamento). O uso do CPAP foi associado a uma maior taxa de sobrevida livre de FA, quando comparado ao grupo sem uso do CPAP. Os autores concluíram que o tratamento com CPAP em pacientes apneicos submetidos a tratamento percutâneo da FA melhora a recorrência da arritmia e, nos casos de AOS sem tratamento adequado, o isolamento elétrico tem pouco valor clínico.157157 Fein AS, Shvilkin A, Shah D, Haffajee CI, Das S, Kumar K, et al. Treatment of obstructive sleep apnea reduces the risk of atrial fibrillation recurrence after catheter ablation. J Am Coll Cardiol. 2013;62(4):300-5. doi: 10.1016/j.jacc.2013.03.052.
https://doi.org/10.1016/j.jacc.2013.03.0...
Metanálise realizada para determinar o papel da AOS no paciente portador de FA submetido à ablação por cateter associou a AOS com o aumento no risco de recorrência após ablação (RR: 1,25; IC95% 1,08-1,45).158158 Ng CY, Liu T, Shehata M, Stevens S, Chugh SS, Wang X. Meta-analysis of obstructive sleep apnea as predictor of atrial fibrillation recurrence after catheter ablation. Am J Cardiol. 2011;108(1):47-51. doi: 10.1016/j.amjcard.2011.02.343.
https://doi.org/10.1016/j.amjcard.2011.0...
4.2.2.2. Bradiarritmias
A associação de AOS com bradiarritmias é controversa, porém a maioria dos estudos mostrou maior incidência de pausas sinusais e/ou distúrbios da condução atrioventricular durante o sono nestes pacientes. As bradiarritmias são mais frequentes no período do sono REM e durante episódios de queda da saturação de oxigênio ≥ 4%, e parecem estar correlacionadas com a gravidade da AOS.159159 Koehler U, Fus E, Grimm W, Pankow W, Schafer H, Stammnitz A, et al. Heart block in patients with obstructive sleep apnoea: pathogenetic factors and effects of treatment. Eur Respir J. 1998;11(2):434-9. PMID: 9551750. A fisiopatologia da ocorrência de bradiarritmias nos pacientes com AOS parece estar relacionada à hiperativação parassimpática cardíaca.160160 Somers VK, Dyken ME, Mark AL, Abboud FM. Parasympathetic hyperresponsiveness and bradyarrhythmias during apnoea in hypertension. Clin Auton Res. 1992;2(3):171-6. PMID: 1498563. Do ponto de vista estrutural, parece não haver alterações significativas no sistema de condução cardíaco, já que, mesmo em pacientes com bloqueio atrioventricular avançado, o estudo eletrofisiológico é normal.161161 Grimm W, Hoffmann J, Menz V, Kohler U, Heitmann J, Peter JH, et al. Electrophysiologic evaluation of sinus node function and atrioventricular conduction in patients with prolonged ventricular asystole during obstructive sleep apnea. Am J Cardiol. 1996;77(15):1310-4. PMID: 8677871.
Em 1983, Guillerminault et al.151151 Guilleminault C, Connolly SJ, Winkle RA. Cardiac arrhythmia and conduction disturbances during sleep in 400 patients with sleep apnea syndrome Am J Cardiol. 1983;52(5):490-4. PMID: 6193700. relataram a ocorrência de arritmias em 400 pacientes avaliados com Holter de 24 horas. As bradiarritmias foram observadas em 18,5% dos pacientes, secundárias a pausas sinusais de 2,5 a 13 segundos, ou bloqueio atrioventricular do segundo grau.151151 Guilleminault C, Connolly SJ, Winkle RA. Cardiac arrhythmia and conduction disturbances during sleep in 400 patients with sleep apnea syndrome Am J Cardiol. 1983;52(5):490-4. PMID: 6193700. Koehler et al.162162 Koehler U, Becker HF, Grimm W, Heitmann J, Peter JH, Schafer H. Relations among hypoxemia, sleep stage, and bradyarrhythmia during obstructive sleep apnea. Am Heart J. 2000;139(1 Pt 1):142-8. PMID: 10618575. avaliaram 239 pacientes portadores de AOS e observaram que 7% deles apresentavam bradiarritmias ao Holter de 48 horas. Roche et al.163163 Roche F, Xuong AN, Court-Fortune I, Costes F, Pichot V, Duverney D, et al. Relationship among the severity of sleep apnea syndrome, cardiac arrhythmias, and autonomic imbalance. Pacing Clin Electrophysiol. 2003;26(3):669-77. PMID: 12698666. relataram maior incidência de assistolias no período noturno em pacientes com AOS em relação aos pacientes sem AOS (10,6% vs. 1,2%, respectivamente; p < 0,02).163163 Roche F, Xuong AN, Court-Fortune I, Costes F, Pichot V, Duverney D, et al. Relationship among the severity of sleep apnea syndrome, cardiac arrhythmias, and autonomic imbalance. Pacing Clin Electrophysiol. 2003;26(3):669-77. PMID: 12698666. Ao contrário dos estudos anteriores, subanálise do SHHS não mostrou associação entre bradiarritmias e AOS.164164 Mehra R, Benjamin EJ, Shahar E, Gottlieb DJ, Nawabit R, Kirchner HL, et al. Association of nocturnal arrhythmias with sleep-disordered breathing: The Sleep Heart Health Study. Am J Respir Crit Care Med. 2006;173(8):910-6. doi: 10.1164/rccm.200509-1442OC.
https://doi.org/10.1164/rccm.200509-1442...
Foram incluídos 228 pacientes com AOS (definida por > 30 eventos por hora) e 338 pacientes sem AOS, porém a análise das arritmias foi realizada por meio de uma única derivação eletrocardiográfica gravada durante a polissonografia.164164 Mehra R, Benjamin EJ, Shahar E, Gottlieb DJ, Nawabit R, Kirchner HL, et al. Association of nocturnal arrhythmias with sleep-disordered breathing: The Sleep Heart Health Study. Am J Respir Crit Care Med. 2006;173(8):910-6. doi: 10.1164/rccm.200509-1442OC.
https://doi.org/10.1164/rccm.200509-1442...
A remissão ou redução significativa dos eventos de bradicardia durante o sono ocorre nos pacientes adequadamente tratados com CPAP. Abe et al.165165 Abe H, Takahashi M, Yaegashi H, Eda S, Tsunemoto H, Kamikozawa M, et al. Efficacy of continuous positive airway pressure on arrhythmias in obstructive sleep apnea patients. Heart Vessels. 2010;25(1):63-9. doi: 10.1007/s00380-009-1164-z.
https://doi.org/10.1007/s00380-009-1164-...
avaliaram a resposta ao CPAP em 316 pacientes com IAH > 20 eventos por hora, demonstrando redução dos eventos de bradicardia sinusal e de pausa sinusal.165165 Abe H, Takahashi M, Yaegashi H, Eda S, Tsunemoto H, Kamikozawa M, et al. Efficacy of continuous positive airway pressure on arrhythmias in obstructive sleep apnea patients. Heart Vessels. 2010;25(1):63-9. doi: 10.1007/s00380-009-1164-z.
https://doi.org/10.1007/s00380-009-1164-...
4.2.2.3. Taquiarritmias
A literatura ainda é pobre na avaliação das correlações existentes entre a AOS e as taquicardias supraventriculares. A taquicardia sinusal ocorre em pacientes com AOS potencialmente secundária à hipóxia, ao microdespertar e à estimulação simpática (e não decorrente de um distúrbio do ritmo primário). Por outro lado, parece existir relação entre arritmia ventricular e distúrbio respiratório do sono. Algumas evidências desta relação surgem da associação entre morte súbita e AOS. O mecanismo arrítmico com o desencadeamento de taquicardia ventricular rápida pode ser um dos fatores que aumentam a taxa de morte súbita nesta população, independente de outros fatores preditores. Em uma análise de 10.701 pacientes submetidos à polissonografia e acompanhados por 15 anos, observou-se taxa anual de morte súbita de 0,27%. Na análise multivariada, os fatores de risco independentes para morte súbita foram idade, hipertensão arterial, DAC, cardiomiopatia ou IC, arritmia ventricular e AOS.166166 Gami AS, Olson EJ, Shen WK, Wright RS, Ballman KV, Hodge DO, et al. Obstructive sleep apnea and the risk of sudden cardiac death: a longitudinal study of 10,701 adults. J Am Coll Cardiol. 2013;62(7):610-6. doi: 10.1016/j.jacc.2013.04.080.
https://doi.org/10.1016/j.jacc.2013.04.0...
Outra análise, com 472 pacientes com IC congestiva submetidos à avalição do sono antes do implante do Cardioverssor Desfibrilador (CDI), demonstrou que a AOS foi preditor independente de taquicardia ventricular e choque apropriado pelo dispositivo cardíaco implantado.167167 Bitter T, Westerheide N, Prinz C, Hossain MS, Vogt J, Langer C, et al. Cheyne-Stokes respiration and obstructive sleep apnoea are independent risk factors for malignant ventricular arrhythmias requiring appropriate cardioverter-defibrillator therapies in patients with congestive heart failure. Eur Heart J. 2011;32(1):61-74. doi: 10.1093/eurheartj/ehq327
https://doi.org/10.1093/eurheartj/ehq327...
Ainda, o tratamento adequado com CPAP pode diminuir o número de ectopias ventriculares durante o sono em pacientes com IC,168168 Ryan CM, Usui K, Floras JS, Bradley TD. Effect of continuous positive airway pressure on ventricular ectopy in heart failure patients with obstructive sleep apnoea. Thorax. 2005;60(9):781-5. doi: 10.1136/thx.2005.040972.
https://doi.org/10.1136/thx.2005.040972...
o que pode sugerir que o tratamento concomitante da AOS neste grupo de pacientes pode melhorar o prognóstico. No entanto, estudos randomizados são necessários nesta área de pesquisa.
4.2.3. Alteração Estrutural Cardíaca
4.2.3.1. Alterações Estruturais e de Desempenho do Ventrículo Esquerdo
Evidências consistentes sugerem que a AOS pode piorar ou potencialmente contribuir para o maior remodelamento do VE de forma independente da HAS.169169 Yumino D, Kasai T, Kimmerly D, Amirthalingam V, Floras JS, Bradley TD. Differing Effects of Obstrutive and Central Sleep Apneas on Stroke Volume in Patients with Heart Failure. Am J Respir Crit Care Med. 2012;187(4):433-43. doi: 10.1164/rccm.201205-0894OC.
https://doi.org/10.1164/rccm.201205-0894...
,170170 Laaban JP, Pascal-Sebaoun S, Bloch E, Orvoen-Frija E, Oppert JM, Huchon G. Left ventricular systolic dysfunction in patients with obstructive sleep apnea syndrome. Chest. 2002;122(4):1133-8. PMID: 12377833. Períodos de pressão negativa intratorácica, induzidos pelo esforço respiratório, ocasionado por uma via aérea superior obstruída parcial ou totalmente, associados ao aumento da rigidez arterial observado nos pacientes com apneia obstrutiva,171171 Drager LF, Bortolotto LA, Figueiredo AC, Silva BC, Krieger EM, Lorenzi-Filho G. Obstructive sleep apnea, hypertension, and their interaction on arterial stiffness and heart remodeling. Chest. 2007;131(5):1379-86. doi: 10.1378/chest.06-2703.
https://doi.org/10.1378/chest.06-2703...
podem aumentar a pós-carga do VE e a pressão transmural durante todo o ciclo cardíaco.153153 Oliveira W, Campos O, Bezerra Lira-Filho E, Cintra FD, Vieira M, Ponchirolli A, et al. Left atrial volume and function in patients with obstructive sleep apnea assessed by real-time three-dimensional echocardiography. J Am Soc Echocardiogr. 2008;21(12):1355-61. doi: 10.1016/j.echo.2008.09.007.
https://doi.org/10.1016/j.echo.2008.09.0...
,172172 Bradley TD, Hall MJ, Ando S, Floras JS. Hemodynamic effects of simulated obstructive apneas in humans with and without heart failure. Chest. 2001;119(6):1827-35. PMID: 11399711.,173173 Ross J Jr. Afterload mismatch and preload reserve: a conceptual frameworkfor the analysis of ventricular function. Prog Cardiovasc Dis. 1976;18(4):255-264. PMID: 128034. Por outro lado, os outros componente da AOS, incluindo a hipóxia intermitente e os microdespertares frequentes, provocam hiperestimulação do sistema nervoso simpático durante a noite, que permanece ativado durante o dia.174174 Svanborg E, Carlsson-Nordlander B, Larsson H, Sachs C, Kaijser L. Autonomic nervous system function in patients with primary obstructive sleep apnoea syndrome. Clin Auton Res. 1991;1(2):125-30. PMID: 1822759.,175175 Carlson JT, Hedner JA, Sellgren J, Elam M, Wallin BG. Depressed baroreflex sensitivity in patients with obstructive sleep apnea. Am J Respir Crit Care Med. 1996;154(5):1490-6. doi: 10.1164/ajrccm.154.5.8912770.
https://doi.org/10.1164/ajrccm.154.5.891...
Estes níveis elevados de catecolaminas podem contribuir para piora da função sistólica e agravamento da hipertrofia ventricular esquerda.116116 Somers VK, Dyken ME, Clary MP, Abboud FM. Sympathetic neural mechanisms in obstructive sleep apnea. J Clin Invest. 1995;96(4):1897-904. doi: 10.1172/JCI118235.
https://doi.org/10.1172/JCI118235...
,176176 Somers VK, Mark AL, Zavala DC, Abboud FM. Contrasting effects of hypoxia and hypercapnia on ventilation and sympathetic activity in humans. J Appl Physiol (1985). 1989;67(5):2101-6. PMID: 2513316.,177177 Chami HA, Devereux RB, Gottdiener JS, Mehra R, Roman MJ, Benjamin EJ, et al. Left ventricular morphology and systolic function in sleep-disordered breathing: the Sleep Heart Health Study. Circulation. 2008;117(20):2599-607. doi: 10.1161/CIRCULATIONAHA.107.717892.
https://doi.org/10.1161/CIRCULATIONAHA.1...
Em estudo recente, as reduções do volume sistólico e do débito cardíaco do VE nos episódios de apneia obstrutiva se mostraram independentemente associadas à menor fração de ejeção do VE, maior duração do evento respiratório e maior SpO22 American Academy of Sleep Medicine, International Classification of Sleep Disorders. 3rd ed. Darien, Illinois; 2014. em pacientes com IC.169169 Yumino D, Kasai T, Kimmerly D, Amirthalingam V, Floras JS, Bradley TD. Differing Effects of Obstrutive and Central Sleep Apneas on Stroke Volume in Patients with Heart Failure. Am J Respir Crit Care Med. 2012;187(4):433-43. doi: 10.1164/rccm.201205-0894OC.
https://doi.org/10.1164/rccm.201205-0894...
Pacientes com AOS grave apresentam maior frequência de disfunção sistólica do VE pela ecocardiografia.178178 Varol E, Akcay S, Ozaydin M, Ozturk O, Cerci SS, Sahin U. Influence of obstructive sleep apnea on left ventricular mass and global function: sleep apnea and myocardial performance index. Heart Vessels. 2010;25(5):400-4. doi: 10.1007/s00380-009-1225-3.
https://doi.org/10.1007/s00380-009-1225-...
Outros estudos demonstram pior índice de desempenho miocárdico do VE nos pacientes com AOS grave,179179 Romero-Corral A, Somers VK, Pellikka PA, Olson EJ, Bailey KR, Korinek J, et al. Decreased right and left ventricular myocardial performance in obstructive sleep apnea. Chest. 2007;132(6):1863-70. doi: 10.1378/chest.07-0966.
https://doi.org/10.1378/chest.07-0966...
,180180 Cho KI, Kwon JH, Kim SM, Park TJ, Lee HG, Kim TI. Impact of obstructive sleep apnea on the global myocardial performance beyond obesity. Echocardiography. 2012;29(9):1071-80. doi: 10.1111/j.1540-8175.2012.01762.x.
https://doi.org/10.1111/j.1540-8175.2012...
que melhoraram após 6 meses de uso do CPAP em pacientes não hipertensos.181181 Moro JA, Almenar L, Fernández-Fabrellas E, Ponce S, Blanquer R, Salvador A. Hypertension and sleep apnea-hypopnea syndrome: changes in echocardiographic abnormalities depending on the presence of hypertension and treatment with CPAP. Sleep Med. 2009;10(3):344-52. doi: 10.1016/j.sleep.2008.03.008.
https://doi.org/10.1016/j.sleep.2008.03....
,182182 Dursunoglu N, Dursunoglu D, Ozkurt S, Kuru O, Gür S, Kiter G, et al. Effects of CPAP on left ventricular structure and myocardial performance index in male patients with obstructive sleep apnoea. Sleep Med. 2007;8(1):51-9. doi: 10.1016/j.sleep.2006.04.007.
https://doi.org/10.1016/j.sleep.2006.04....
Em pacientes com disfunção sistólica, trabalhos apontam melhora da fração de ejeção do VE após uso do CPAP,183183 Malone S, Liu PP, Holloway R, Rutherford R, Xie A, Bradley TD. Obstructive sleep apnoea in patients with dilated cardiomyopathy: effects of continuous positive airway pressure. Lancet. 1991;338(8781):1480-4. PMID: 1683918.,184184 Kaneko Y, Floras JS, Usui K, Plante J, Tkacova R, Kubo T, et al. Cardiovascular effects of continuous positive airway pressure in patients with heart failure and obstructive sleep apnea. N Engl J Med. 2003;348(13):1233-41. doi: 10.1056/NEJMoa022479.
https://doi.org/10.1056/NEJMoa022479...
mas o efeito sobre melhora do prognóstico nestes pacientes com o tratamento é baseado somente em estudos observacionais.185185 Javaheri S, Caref EB, Chen E, Tong KB, Abraham WT. Sleep apnea testing and outcomes in a large cohort of Medicare beneficiaries with newlydiagnosed heart failure. Am J Respir Crit Care Med. 2011;183(4):539-46. doi: 10.1164/rccm.201003-0406OC.
https://doi.org/10.1164/rccm.201003-0406...
,186186 Khayat R, Jarjoura D, Porter K, Sow A, Wannemacher J, Dohar R, et al. Sleep disordered breathing and post-discharge mortality in patients with acute heart failure. Eur Heart J. 2015;36(23):1463-9. doi: 10.1093/eurheartj/ehu522.
https://doi.org/10.1093/eurheartj/ehu522...
Mesmo em pacientes normotensos, há associação entre AOS e aumento da espessura miocárdica.187187 Hedner J, Ejnell H, Caidahl K. Left ventricular hypertrophy independent of hypertension in patients with obstructive sleep apnea. J Hypertens. 1990;8(10):941-6. PMID: 2174947.
188 Noda A, Okada T, Yasuma F, Nakashima N, Yokota M. Cardiac hypertrophy in obstructive sleep apnea syndrome. Chest. 1995;107(6):1538-44. PMID: 7781343.
189 Sukhija R, Aronow WS, Sandhu R, Kakar P, Maguire GP, Ahn C, et al. Prevalence of left ventricularhypertrophy in persons with and without obstructive sleep apnea. Cardiol Rev. 2006;14(4):170-2. doi: 10.1097/01.crd.0000184455.52778.00.
https://doi.org/10.1097/01.crd.000018445...
-190190 Baguet JP, Nadra M, Barone-Rochette G, Ormezzano O, Pierre H, Pépin JL. Early cardiovascular abnormalities in newly diagnosed obstructive sleep apnea. Vasc Health Risk Manag. 2009;5:1063-73. PMID: 20057899. Tanto a AOS grave quanto a HAS estão relacionadas ao aumento da rigidez arterial e a alterações morfológicas cardíacas da mesma magnitude, com efeito aditivo quando coexistem.171171 Drager LF, Bortolotto LA, Figueiredo AC, Silva BC, Krieger EM, Lorenzi-Filho G. Obstructive sleep apnea, hypertension, and their interaction on arterial stiffness and heart remodeling. Chest. 2007;131(5):1379-86. doi: 10.1378/chest.06-2703.
https://doi.org/10.1378/chest.06-2703...
O padrão predominante de hipertofia na AOS parece ser o concêntrico,189189 Sukhija R, Aronow WS, Sandhu R, Kakar P, Maguire GP, Ahn C, et al. Prevalence of left ventricularhypertrophy in persons with and without obstructive sleep apnea. Cardiol Rev. 2006;14(4):170-2. doi: 10.1097/01.crd.0000184455.52778.00.
https://doi.org/10.1097/01.crd.000018445...
190 Baguet JP, Nadra M, Barone-Rochette G, Ormezzano O, Pierre H, Pépin JL. Early cardiovascular abnormalities in newly diagnosed obstructive sleep apnea. Vasc Health Risk Manag. 2009;5:1063-73. PMID: 20057899.
191 Cioffi G, Russo TE, Stefenelli C, Selmi A, Furlanello F, Cramariuc D, et al. Severe obstructive sleep apnea elicits concentric left ventricular geometry. J Hypertens. 2010;28(5):1074-82. PMID: 20411620.-192192 Hla KM, Young T, Finn LA, Peppard PE, Kinsey TJ, Ende D. Electrocardiographically indicated cardiovascular disease in sleep-disordered breathing. Sleep Breath. 2008;12(3):251-8. doi: 10.1007/s11325-007-0168-0.
https://doi.org/10.1007/s11325-007-0168-...
e os efeitos iniciais do tratamento da AOS na diminuição da espessura miocárdica do VE começa a ser observado a partir de 3 meses de tratamento.193193 Koga S, Ikeda S, Nakata T, Yasunaga T, Maemura K. Effects of nasal continuous positive airway pressure on left ventricular concentric hypertrophy in obstructive sleep apnea syndrome. Intern Med. 2012;51(20):2863-8. PMID: 23064559.
194 Shivalkar B, Van de Heyning C, Kerremans M, Rinkevich D, Verbraecken J, De Backer W, et al. Obstructive sleep apnea syndrome: more insights on structural and functional cardiac alterations, and the effects of treatment with continuous positive airway pressure. J Am Coll Cardiol. 2006;47(7):1433-9. doi: 10.1016/j.jacc.2005.11.054.
https://doi.org/10.1016/j.jacc.2005.11.0...
-195195 Cloward TV, Walker JM, Farney RJ, Anderson JL. Left ventricular hypertrophy is a common echocardiographic abnormality in severe obstructive sleep apnea and reverses with nasal continuous positive airway pressure. Chest. 2003;124(2):594-601. PMID: 12907548. No entanto, é importante destacar que a literatura ainda carece de estudos randomizados envolvendo um número representativo de pacientes e com maior seguimento, para uma avaliação do real benefício do CPAP na hipertrofia do VE.
A AOS grave pode, por si só, contribuir para disfunção diastólica, principalmente em seus estágios iniciais.190190 Baguet JP, Nadra M, Barone-Rochette G, Ormezzano O, Pierre H, Pépin JL. Early cardiovascular abnormalities in newly diagnosed obstructive sleep apnea. Vasc Health Risk Manag. 2009;5:1063-73. PMID: 20057899.,196196 Usui Y, Takata Y, Inoue Y, Tomiyama H, Kurohane S, Hashimura Y, et al. Severe obstructive sleep apnea impairs left ventricular diastolic function in non-obese men. Sleep Med. 2013;14(2):155-9. doi: 10.1016/j.sleep.2010.09.014.
https://doi.org/10.1016/j.sleep.2010.09....
197 Yang SQ, Han LL, Dong XL, Wang CY, Xia H, Liu P, et al. Mal-effects of obstructive sleep apnea on the heart. Sleep Breath. 2012;16(3):717-22. doi: 10.1007/s11325-011-0566-1.
https://doi.org/10.1007/s11325-011-0566-...
198 Cicek D, Lakadamyali H, Yagbasan BD, Sapmaz I, Müderrisoglu H. Obstructive sleep apnoea and its association with left ventricular function and aortic root parameters in newly diagnosed, untreated patients: a prospective study. J Int Med Res. 2011;39(6):2228-38. doi: 10.1177/147323001103900619.
https://doi.org/10.1177/1473230011039006...
199 Kim SH, Cho GY, Shin C, Lim HE, Kim YH, Song WH, et l. Impact of obstructive sleep apnea on left ventricular diastolic function. Am J Cardiol. 2008;101(11):1663-8. doi: 10.1016/j.amjcard.2008.01.056.
https://doi.org/10.1016/j.amjcard.2008.0...
-200200 Fung JW, Li TS, Choy DK, Yip GW, Ko FW, Sanderson JE, et al. Severe obstructive sleep apnea is associated with left ventricular diastolic dysfunction. Chest. 2002;121(2):422-9. PMID: 11834652. Recentemente, análises ecocardiográficas do VE por speckle tracking confirmam a relação entre a gravidade da AOS e a progressão da disfunção miocárdica subclínica em pacientes com fração de ejeção do VE preservada.201201 Altekin RE, Yanikoglu A, Baktir AO, Karakas MS, Ozel D, Cilli A, et al. Assessment of subclinical left ventricular dysfunction in obstructive sleep apnea patients with speckle tracking echocardiography. Int J Cardiovasc Imaging. 2012;28(8):1917-30. doi: 10.1007/s10554-012-0026-4.
https://doi.org/10.1007/s10554-012-0026-...
,202202 Vitarelli A, D'Orazio S, Caranci F, Capotosto L, Rucos R, Iannucci G, et al. Left ventricular torsion abnormalities in patients with obstructive sleep apnea syndrome: an early sign of subclinical dysfunction. Int J Cardiol. 2013;165(3):512-8. doi: 10.1016/j.ijcard.2011.09.030.
https://doi.org/10.1016/j.ijcard.2011.09...
Estudos sugerem melhora dos índices ecocardiográficos para análise da diástole, principalmente alterações na relação E/e’ e do fluxo diastólico mitral, a partir de 3 meses de tratamento com CPAP, porém com número limitado de pacientes.203203 Haruki N, Takeuchi M, Kanazawa Y, Tsubota N, Shintome R, Nakai H, et al. Continuous positive airway pressure ameliorates sleep-induced subclinical left ventricular systolic dysfunction: demonstration by two-dimensional speckle-tracking echocardiography. Eur J Echocardiogr. 2010;11(4):352-8. doi: 10.1093/ejechocard/jep215.
https://doi.org/10.1093/ejechocard/jep21...
204 Butt M, Dwivedi G, Shantsila A, Khair OA, Lip GY. Left ventricular systolic and diastolic function in obstructive sleep apnea: impact of continuous positive airway pressure therapy. Circ Heart Fail 2012;5(2):226-33. doi: 10.1161/CIRCHEARTFAILURE.111.964106.
https://doi.org/10.1161/CIRCHEARTFAILURE...
205 Akar Bayram N, Ciftci B, Durmaz T, Keles T, Yeter E, Akcay M, et al. Effects of continuous positive airway pressure therapy on left ventricular function assessed by tissue Doppler imaging in patients with obstructive sleep apnoea syndrome. Eur J Echocardiogr. 2009;10(3):376-82. doi: 10.1093/ejechocard/jen257.
https://doi.org/10.1093/ejechocard/jen25...
-206206 Arias MA, García-Río F, Alonso-Fernández A, Mediano O, Martínez I, Villamor J. Obstructive sleep apnea syndrome affects left ventricular diastolic function: effects of nasal continuous positive airway pressure in men. Circulation. 2005;112(3):375-83. doi: 10.1161/CIRCULATIONAHA.104.501841.
https://doi.org/10.1161/CIRCULATIONAHA.1...
4.2.3.2. Alterações Estruturais e de Desempenho do Átrio Esquerdo
A AOS tem sido associada com o aumento do Átrio Esquerdo (AE).154154 Drager LF, Bortolotto LA, Pedrosa RP, Krieger EM, Lorenzi-Filho G. Left atrial diameter is independently associated with arterial stiffness in patients with obstructive sleep apnea: potential implications for atrial fibrillation. Int J Cardiol. 2010;144(2):257-9. doi: 10.1016/j.ijcard.2009.01.018.
https://doi.org/10.1016/j.ijcard.2009.01...
O aumento da pós-carga e a pressão transmural do VE, associados à disfunção diastólica e observados na AOS, podem levar à sobrecarga atrial esquerda.154154 Drager LF, Bortolotto LA, Pedrosa RP, Krieger EM, Lorenzi-Filho G. Left atrial diameter is independently associated with arterial stiffness in patients with obstructive sleep apnea: potential implications for atrial fibrillation. Int J Cardiol. 2010;144(2):257-9. doi: 10.1016/j.ijcard.2009.01.018.
https://doi.org/10.1016/j.ijcard.2009.01...
,171171 Drager LF, Bortolotto LA, Figueiredo AC, Silva BC, Krieger EM, Lorenzi-Filho G. Obstructive sleep apnea, hypertension, and their interaction on arterial stiffness and heart remodeling. Chest. 2007;131(5):1379-86. doi: 10.1378/chest.06-2703.
https://doi.org/10.1378/chest.06-2703...
Oliveira et al.153153 Oliveira W, Campos O, Bezerra Lira-Filho E, Cintra FD, Vieira M, Ponchirolli A, et al. Left atrial volume and function in patients with obstructive sleep apnea assessed by real-time three-dimensional echocardiography. J Am Soc Echocardiogr. 2008;21(12):1355-61. doi: 10.1016/j.echo.2008.09.007.
https://doi.org/10.1016/j.echo.2008.09.0...
analisaram o AE de 56 pacientes com AOS não tratada por ecocardiografia tridimensional. Comparada ao grupo controle e ao grupo com AOS leve, os pacientes com AOS grave apresentavam aumento significativo do volume atrial esquerdo indexado pela superfície corpórea.153153 Oliveira W, Campos O, Bezerra Lira-Filho E, Cintra FD, Vieira M, Ponchirolli A, et al. Left atrial volume and function in patients with obstructive sleep apnea assessed by real-time three-dimensional echocardiography. J Am Soc Echocardiogr. 2008;21(12):1355-61. doi: 10.1016/j.echo.2008.09.007.
https://doi.org/10.1016/j.echo.2008.09.0...
Neste estudo, foram demonstradas, além do aumento volumétrico, alteração funcional do AE e alterações na análise da função diastólica por Doppler tecidual no grupo com AOS.153153 Oliveira W, Campos O, Bezerra Lira-Filho E, Cintra FD, Vieira M, Ponchirolli A, et al. Left atrial volume and function in patients with obstructive sleep apnea assessed by real-time three-dimensional echocardiography. J Am Soc Echocardiogr. 2008;21(12):1355-61. doi: 10.1016/j.echo.2008.09.007.
https://doi.org/10.1016/j.echo.2008.09.0...
Após randomização duplo-cega para tratamento dos pacientes com IAH > 20 eventos por hora de sono com CPAP nasal ou placebo, foram observados, após 24 semanas, redução na relação E/e’, aumento da fração de esvaziamento passivo do AE e redução da fração de esvaziamento ativo do AE.207207 Oliveira W, Campos O, Cintra F, Matos L, Vieira ML, Rollim B, et al. Impact of continuous positive airway pressure treatment on left atrial volume and function in patients with obstructive sleep apnoea assessed by real-time three-dimensional echocardiography. Heart. 2009;95(22):1872-8. doi: 10.1136/hrt.2009.173625.
https://doi.org/10.1136/hrt.2009.173625...
Anormalidades de condução eletromecânica por estudo eletrofisiológico no AE em pacientes com AOS moderada à grave foram relatadas em alguns estudos, fato que poderia, em parte, explicar e predizer o risco futuro de FA neste grupo de pacientes.208208 Dimitri H, Ng M, Brooks AG, Kuklik P, Stiles MK, Lau DH, et al. Atrial remodeling in obstructive sleep apnea: implications for atrial fibrillation. Heart Rhythm. 2012;9(3):321-7. doi: 10.1016/j.hrthm.2011.10.017.
https://doi.org/10.1016/j.hrthm.2011.10....
,209209 Yagmur J, Yetkin O, Cansel M, Acikgoz N, Ermis N, Karakus Y, et al. Assessment of atrial electromechanical delay and influential factors in patients with obstructive sleep apnea. Sleep Breath. 2012;16(1):83-8. doi: 10.1007/s11325-010-0477-6.
https://doi.org/10.1007/s11325-010-0477-...
Estudos multicêntricos envolvendo maior número de pacientes são necessários para melhor avaliação do impacto das alterações morfológicas nas câmaras esquerdas demonstradas até o momento na AOS, especialmente se moderada ou grave, e os benefícios cardiovasculares do tratamento em longo prazo com o CPAP neste grupo de pacientes.
4.2.3.3. Alterações no Desempenho do Ventrículo Direito
A AOS tem sido associada à disfunção ventricular direita, mesmo após correção para idade, IMC, sexo, pressão da artéria pulmonar e função ventricular esquerda, segundo estudos com ventriculografia por radionuclídeos.210210 Sanner BM, Konermann M, Sturm A, Muller HJ, Zidek W. Right ventricular dysfunction in patients with obstructive sleep apnoea syndrome. Eur Respir J. 1997;10(9):2079-83. PMID: 9311506. Há vários fatores estreitamente relacionados à AOS que podem incorrer em alteração da estrutura e função do VD, os quais incluem obesidade, elevações nos níveis absolutos de pressão negativa intratorácica e aumento na resistência vascular pulmonar que, por sua vez, estão diretamente associados à frequência e à gravidade dos eventos de apneia.179179 Romero-Corral A, Somers VK, Pellikka PA, Olson EJ, Bailey KR, Korinek J, et al. Decreased right and left ventricular myocardial performance in obstructive sleep apnea. Chest. 2007;132(6):1863-70. doi: 10.1378/chest.07-0966.
https://doi.org/10.1378/chest.07-0966...
,211211 Dursunoglu N, Dursunoglu D, Kilic M. Impact of obstructive sleep apnea on right ventricular global function: sleep apnea and myocardial performance index. Respiration. 2005;72(3):278-84. doi: 10.1159/000085369.
https://doi.org/10.1159/000085369...
,212212 Tugcu A, Yildirimturk O, Tayyareci Y, Demiroglu C, Aytekin S. Evaluation of subclinical right ventricular dysfunction in obstructive sleep apnea patients using velocity vector imaging. Circ J. 2010;74(2):312-9. PMID: 20009388.
Em relação ao tratamento da AOS, Oliveira et al.213213 Oliveira W, Poyares D, Cintra F, Vieira ML, Fischer CH, Moises V, et al. Impact of continuous positive airway pressure treatment on right ventricle performance in patients with obstructive sleep apnoea, assessed by three-dimensional echocardiography. Sleep Med. 2012;13(5):510-6. doi: 10.1016/j.sleep.2011.12.010.
https://doi.org/10.1016/j.sleep.2011.12....
determinaram, em estudo randomizado duplo-cego placebo controlado, uma relação direta entre a gravidade da apneia e a alteração da dinâmica ventricular direita, por meio da ecocardiografia tridimensional. O principal achado deste estudo foi a significante melhora do desempenho ventricular direito, evidenciado pelo aumento na fração de ejeção desta câmara, após tratamento com CPAP, em pacientes com AOS. Este achado pareceu estar diretamente associado à melhora da resistência vascular pulmonar após o tratamento efetivo com CPAP. Adicionalmente, os dados obtidos do grupo com intervenção placebo controlada com variáveis clínico-demográficas semelhantes reforçam a ideia de que AOS é significativamente associada ao desempenho ventricular direito.
4.2.4. Insuficiência Cardíaca
Os distúrbios de sono são comuns em pacientes com IC. No caso da AOS, a presença deste distúrbio do sono pode tanto aumentar a incidência na ocorrência da IC (especialmente em homens), quanto piorar a evolução do paciente portador desta insuficiência. Por exemplo, em 164 pacientes com IC estável crônica, a presença da AOS foi associada ao aumento da mortalidade na análise multivariada.214214 Wang H, Parker JD, Newton GE, Floras JS, Mak S, Chiu KL, et al. Influence of obstructive sleep apnea on mortality in patients with heart failure. J Am Coll Cardiol. 2007;49(15):1625-31. doi: 10.1016/j.jacc.2006.12.046.
https://doi.org/10.1016/j.jacc.2006.12.0...
Estudo ramdomizado mostrou que o tratamento da AOS com o CPAP promoveu melhora da classe funcional, bem como um aumento significante da fração da ejeção com apneas 1 mês de tratamento.184184 Kaneko Y, Floras JS, Usui K, Plante J, Tkacova R, Kubo T, et al. Cardiovascular effects of continuous positive airway pressure in patients with heart failure and obstructive sleep apnea. N Engl J Med. 2003;348(13):1233-41. doi: 10.1056/NEJMoa022479.
https://doi.org/10.1056/NEJMoa022479...
Como tanto a AOS quanto a IC per se aumentam a pós-carga e a demanda metabólica, parte desta melhora da função ventricular pelo tratamento da AOS é justificada pela diminuição do metabolismo oxidativo, pela melhora da energética miocárdica, e pela redução da atividade simpática e da pressão arterial.215215 Yoshinaga K, Burwash IG, Leech JA, Haddad H, Johnson CB, deKemp RA, et al. The effects of continuous positive airway pressure on myocardial energetics in patients with heart failure and obstructive sleep apnea. J Am Coll Cardiol. 2007;49(4):450-8. doi: 10.1016/j.jacc.2006.08.059.
https://doi.org/10.1016/j.jacc.2006.08.0...
,216216 Hall AB, Ziadi MC, Leech JA, Chen SY, Burwash IG, Renaud J, et al. Effects of short-term continuous positive airway pressure on myocardial sympathetic nerve function and energetics in patients with heart failure and obstructive sleep apnea: a randomized study. Circulation. 2014;130(11):892-901. doi: 10.1161/CIRCULATIONAHA.113.005893.
https://doi.org/10.1161/CIRCULATIONAHA.1...
A despeito destas evidências, faltam ainda estudos randomizados que avaliem se o tratatmento da AOS pode previnir o desenvolvimento da IC em pacientes com coração estruturalmente normal, e se o tratamento da AOS reduz a mortalidade em pacientes com IC.
4.2.5. Cardiomiopatia Hipertrófica
A cardiomiopatia hipertrófica (CMH) é uma doença cardíaca genética transmitida por herança autossômica dominante, que acomete cerca de um em cada 500 habitantes da população geral.217217 Maron BJ. Hypertrophic cardiomyopathy: a systematic review. JAMA. 2002;287(10):1308-20. PMID: 11886323.,218218 Zou Y, Song L, Wang Z, Ma A, Liu T, Gu H, et al. Prevalence of idiopathic hypertrophic cardiomyopathy in China: a population-based echocardiographic analysis of 8080 adults. Am J Med. 2004;116(1):14-8. PMID: 14706660. Caracteriza-se por hipertrofia do VE,219219 Maron BJ. Hypertrophic cardiomyopathy. Lancet. 1997;350(9071):127-33. doi: 10.1016/S0140-6736(97)01282-8. Erratum in: Lancet. 1997;350(9087):1330.
https://doi.org/10.1016/S0140-6736(97)01...
,220220 Gersh BJ, Maron BJ, Bonow RO, Dearani JA, Fifer MA, Link MS, et al; American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines; American Association for Thoracic Surgery; American Society of Echocardiography; American Society of Nuclear Cardiology; Heart Failure Society of America; Heart Rhythm Society; Society for Cardiovascular Angiography and Interventions; Society of Thoracic Surgeons. 2011 ACCF/AHA guideline for the diagnosis and treatment of hypertrophic cardiomyopathy: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. Circulation. 2011;124(24):e783-831. doi: 10.1161/CIR.0b013e318223e2bd.
https://doi.org/10.1161/CIR.0b013e318223...
decorrente de mutações nos genes que codificam proteínas do sarcômero e seus componentes de miofilamentos, os quais possuem funções contráteis, estruturais e regulatórias.218218 Zou Y, Song L, Wang Z, Ma A, Liu T, Gu H, et al. Prevalence of idiopathic hypertrophic cardiomyopathy in China: a population-based echocardiographic analysis of 8080 adults. Am J Med. 2004;116(1):14-8. PMID: 14706660.,220220 Gersh BJ, Maron BJ, Bonow RO, Dearani JA, Fifer MA, Link MS, et al; American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines; American Association for Thoracic Surgery; American Society of Echocardiography; American Society of Nuclear Cardiology; Heart Failure Society of America; Heart Rhythm Society; Society for Cardiovascular Angiography and Interventions; Society of Thoracic Surgeons. 2011 ACCF/AHA guideline for the diagnosis and treatment of hypertrophic cardiomyopathy: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. Circulation. 2011;124(24):e783-831. doi: 10.1161/CIR.0b013e318223e2bd.
https://doi.org/10.1161/CIR.0b013e318223...
,221221 Maron BJ, Seidman CE, Ackerman MJ, Towbin JA, Maron MS, Ommen SR, et al. How should hypertrophic cardiomyopathy be classified?: What's in a name? Dilemmas in nomenclature characterizing hypertrophic cardiomyopathy and left ventricular hypertrophy. Circ Cardiovasc Genet. 2009;2(1):81-5. doi: 10.1161/CIRCGENETICS.108.788703.
https://doi.org/10.1161/CIRCGENETICS.108...
De forma geral, os casos de apresentação mais precoce apresentam pior prognóstico, sendo importante causa de morte súbita em jovens.222222 Miller MA, Gomes JA, Fuster V. Risk stratification of sudden cardiac death in hypertrophic cardiomyopathy. Nat Clin Pract Cardiovasc Med. 2007;4(12):667-76. doi: 10.1038/ncpcardio1057.
https://doi.org/10.1038/ncpcardio1057...
Estudos apontam que entre 32 e 71% dos pacientes com CMH apresentam AOS.223223 Banno K, Shiomi T, Sasanabe R, Otake K, Hasegawa R, Maekawa M, et al. Sleep-disordered breathing in patients with idiopathic cardiomyopathy. Circ J. 2004;68(4):338-42. PMID: 15056831.
224 Pedrosa RP, Drager LF, Genta PR, Amaro AC, Antunes MO, Matsumoto AY, et al. Obstructive sleep apnea is common and independently associated with atrial fibrillation in patients with hypertrophic cardiomyopathy. Chest. 2010;137(5):1078-84. doi: 10.1378/chest.09-2335.
https://doi.org/10.1378/chest.09-2335...
225 Konecny T, Brady PA, Orban M, Lin G, Pressman GS, Lehar F, et al. Interactions between sleep disordered breathing and atrial fibrillation in patients with hypertrophic cardiomyopathy. Am J Cardiol. 2010;105(11):1597-602. doi: 10.1016/j.amjcard.2010.01.023.
https://doi.org/10.1016/j.amjcard.2010.0...
226 Eleid MF, Konecny T, Orban M, Sengupta PP, Somers VK, Parish JM, et al. High prevalence of abnormal nocturnal oximetry in patients with hypertrophic cardiomyopathy. J Am Coll Cardiol. 2009;54(19):1805-9. doi: 10.1016/j.jacc.2009.07.030.
https://doi.org/10.1016/j.jacc.2009.07.0...
-227227 Prinz C, Bitter T, Oldenburg O, Horstkotte D, Faber L. Incidence of sleep-disordered breathing in patients with hypertrophic cardiomyopathy. Congest Heart Fail. 2011;17(1):19-24. doi: 10.1111/j.1751-7133.2010.00196.x.
https://doi.org/10.1111/j.1751-7133.2010...
No entanto, os estudos apresentam algumas limitações, como o tamanho amostral ou o uso de oximetria de pulso noturna ou monitor portátil para o diagnóstico da AOS. Pacientes com CMH apresentam pior qualidade do sono quando comprados a controles sadios, e a má qualidade do sono associa-se, de forma independente, com pior qualidade de vida entre os portadores de CMH.228228 Pedrosa RP, Lima SG, Drager LF, Genta PR, Amaro AC, Antunes MO, et al. Sleep quality and quality of life in patients with hypertrophic cardiomyopathy. Cardiology. 2010;117(3):200-6. doi: 10.1159/000321718.
https://doi.org/10.1159/000321718...
Porém, a AOS ainda é subdiagnosticada nesta população, pois existe uma carência de preditores clínicos específicos, que ajudem na suspeita de AOS em pacientes com CMH. Em recente estudo, Nerbass et al.229229 Nerbass FB, Pedrosa RP, Genta PR, Antunes MO, Arteaga-Fernández E, Drager LF, et al. Lack of reliable clinical predictors to identify obstructive sleep apnea in patients with hypertrophic cardiomyopathy. Clinics. 2013;68(7):992-6. doi: http://dx.doi.org/10.6061/clinics/2013(07)17.
http://dx.doi.org/10.6061/clinics/2013(0...
apontam que a ausência de sonolência diurna excessiva e o IMC relativamente reduzido em comparação a outras populações com AOS são possíveis explicações para a escassez de preditores clínicos. Nesse estudo, apenas idade ≥ 45 anos e FA foram associadas de forma independente com a AOS.
Além da AOS ser comum e piorar a qualidade de vida nos pacientes com CMH, evidências crescentes sugerem que a AOS pode amplificar o risco cardiovascular dos pacientes com CMH. Pacientes com AOS sofrem de hiperestimulação do sistema nervoso simpático durante todo o dia, o que também é encontrado na CMH. O aumento do tônus simpático pode não ser apenas um marcador de gravidade da doença,230230 Limbruno U, Strata G, Zucchi R, Baglini R, Mengozzi G, Balbarini A, et al. Altered autonomic cardiac control in hypertrophic cardiomyopathy. Role of outflow tract obstruction and myocardial hypertrophy. Eur Heart J. 1998;19(1):146-53. PMID: 9503188. mas um fator de risco adicional. Isto porque elevados níveis de catecolaminas circulantes podem influenciar no aumento da hipertrofia ventricular esquerda e suas pressões de enchimento, diminuindo o débito cardíaco. Esta redução no débito cardíaco pode iniciar ou agravar a obstrução na via de saída do VE e a regurgitação mitral.231231 Sengupta PP, Sorajja D, Eleid MF, Somers VK, Ommen SR, Parish JM, et al. Hypertrophic obstructive cardiomyopathy and sleep-disordered breathing: an unfavorable combination. Nat Clin Pract Cardiovasc Med. 2009;6(1):14-5. doi: 10.1038/ncpcardio1401.
https://doi.org/10.1038/ncpcardio1401...
Além disto, a hiperestimulação simpática pode contribuir para o aumento da incidência de arritmias ventriculares e supraventriculares em portadores de CMH. Neste contexto, dois estudos indicaram associação da AOS com uma chance quatro a cinco vezes maior para presença de FA em pacientes com CMH.224224 Pedrosa RP, Drager LF, Genta PR, Amaro AC, Antunes MO, Matsumoto AY, et al. Obstructive sleep apnea is common and independently associated with atrial fibrillation in patients with hypertrophic cardiomyopathy. Chest. 2010;137(5):1078-84. doi: 10.1378/chest.09-2335.
https://doi.org/10.1378/chest.09-2335...
,225225 Konecny T, Brady PA, Orban M, Lin G, Pressman GS, Lehar F, et al. Interactions between sleep disordered breathing and atrial fibrillation in patients with hypertrophic cardiomyopathy. Am J Cardiol. 2010;105(11):1597-602. doi: 10.1016/j.amjcard.2010.01.023.
https://doi.org/10.1016/j.amjcard.2010.0...
Os preditores de FA nesta população de pacientes com CMH foram IAH, tamanho do AE224224 Pedrosa RP, Drager LF, Genta PR, Amaro AC, Antunes MO, Matsumoto AY, et al. Obstructive sleep apnea is common and independently associated with atrial fibrillation in patients with hypertrophic cardiomyopathy. Chest. 2010;137(5):1078-84. doi: 10.1378/chest.09-2335.
https://doi.org/10.1378/chest.09-2335...
e índice de dessaturação noturna.225225 Konecny T, Brady PA, Orban M, Lin G, Pressman GS, Lehar F, et al. Interactions between sleep disordered breathing and atrial fibrillation in patients with hypertrophic cardiomyopathy. Am J Cardiol. 2010;105(11):1597-602. doi: 10.1016/j.amjcard.2010.01.023.
https://doi.org/10.1016/j.amjcard.2010.0...
Estes achados sugerem que a AOS pode ter efeito aditivo negativo sobre a estrutura e a função cardíaca dos pacientes com CMH.
Os pacientes com CMH frequentemente apresentam sinais de remodelamento atrial, com dilatação do AE, que pode ser um preditor de morbimortalidade.232232 Nistri S, Olivotto I, Betocchi S, Losi MA, Valsecchi G, Pinamonti B, et al. Prognostic significance of left atrial size in patients with hypertrophic cardiomyopathy (from the Italian Registry for Hypertrophic Cardiomyopathy). Am J Cardiol. 2006;98(7):960-5. doi: 10.1016/j.amjcard.2006.05.013.
https://doi.org/10.1016/j.amjcard.2006.0...
Quando existe a associação entre a AOS e a CMH, a dimensão do AE é maior do que em pacientes com CMH isoladamente.224224 Pedrosa RP, Drager LF, Genta PR, Amaro AC, Antunes MO, Matsumoto AY, et al. Obstructive sleep apnea is common and independently associated with atrial fibrillation in patients with hypertrophic cardiomyopathy. Chest. 2010;137(5):1078-84. doi: 10.1378/chest.09-2335.
https://doi.org/10.1378/chest.09-2335...
225 Konecny T, Brady PA, Orban M, Lin G, Pressman GS, Lehar F, et al. Interactions between sleep disordered breathing and atrial fibrillation in patients with hypertrophic cardiomyopathy. Am J Cardiol. 2010;105(11):1597-602. doi: 10.1016/j.amjcard.2010.01.023.
https://doi.org/10.1016/j.amjcard.2010.0...
-226226 Eleid MF, Konecny T, Orban M, Sengupta PP, Somers VK, Parish JM, et al. High prevalence of abnormal nocturnal oximetry in patients with hypertrophic cardiomyopathy. J Am Coll Cardiol. 2009;54(19):1805-9. doi: 10.1016/j.jacc.2009.07.030.
https://doi.org/10.1016/j.jacc.2009.07.0...
No estudo de Pedrosa et al.,224224 Pedrosa RP, Drager LF, Genta PR, Amaro AC, Antunes MO, Matsumoto AY, et al. Obstructive sleep apnea is common and independently associated with atrial fibrillation in patients with hypertrophic cardiomyopathy. Chest. 2010;137(5):1078-84. doi: 10.1378/chest.09-2335.
https://doi.org/10.1378/chest.09-2335...
pacientes com AOS e CMH apresentaram aumento em 9% do AE quando comparados aos sem AOS, sendo o IAH o único preditor deste aumento atrial. Houve correlação positiva entre o volume do AE e a gravidade da AOS.225225 Konecny T, Brady PA, Orban M, Lin G, Pressman GS, Lehar F, et al. Interactions between sleep disordered breathing and atrial fibrillation in patients with hypertrophic cardiomyopathy. Am J Cardiol. 2010;105(11):1597-602. doi: 10.1016/j.amjcard.2010.01.023.
https://doi.org/10.1016/j.amjcard.2010.0...
,226226 Eleid MF, Konecny T, Orban M, Sengupta PP, Somers VK, Parish JM, et al. High prevalence of abnormal nocturnal oximetry in patients with hypertrophic cardiomyopathy. J Am Coll Cardiol. 2009;54(19):1805-9. doi: 10.1016/j.jacc.2009.07.030.
https://doi.org/10.1016/j.jacc.2009.07.0...
Tal achado pode ser explicado pelo fato de que, durante as apneias obstrutivas, é gerada uma pressão intratorácica negativa contra a via aérea superior fechada. Este esforço inspiratório aumenta a pressão transmural do VE, que é um importante determinante da pós-carga ventricular e atrial esquerda e pode refletir em maiores diâmetros atriais.233233 Nerbass FB, Pedrosa RP, Danzi-Soares NJ, Drager LF, Arteaga-Fernández E, Lorenzi-Filho G. Obstructive sleep apnea and hypertrophic cardiomyopathy: A common and potential harmful combination. Sleep Med Rev. 2013;17(3):201-6. doi: 10.1016/j.smrv.2012.06.006.
https://doi.org/10.1016/j.smrv.2012.06.0...
4.2.5.1. Tratamento da Apneia Obstrutiva do Sono em Pacientes com Cardiomiopatia Hipertrófica
Até o momento, há apenas um relato de três casos de pacientes com AOS e CMH na forma obstrutiva que foram tratados com CPAP por aproximadamente 18 meses, os quais apresentaram melhora na classe funcional da IC, e reduções no volume do AE e no gradiente pressórico na via de saída do VE.231231 Sengupta PP, Sorajja D, Eleid MF, Somers VK, Ommen SR, Parish JM, et al. Hypertrophic obstructive cardiomyopathy and sleep-disordered breathing: an unfavorable combination. Nat Clin Pract Cardiovasc Med. 2009;6(1):14-5. doi: 10.1038/ncpcardio1401.
https://doi.org/10.1038/ncpcardio1401...
Em termos de interação cardiopulmonar, o CPAP produz uma redução aguda do retorno venoso cardíaco, devido ao aumento da pressão intratorácica. Assim, os pacientes com CMH que apresentam obstrução da via de saída do VE podem cursar com aumento expressivo do gradiente pressórico na via de saída do VE, o que já é demonstrado em situações que diminuem o retorno venoso cardíaco.234234 Geske JB, Sorajja P, Ommen SR, Nishimura RA. Left ventricular outflow tract gradient variability in hypertrophic cardiomyopathy. Clin Cardiol. 2009;32(7):397-402. doi: 10.1002/clc.20594.
https://doi.org/10.1002/clc.20594...
Sabe-se que, ao menos de forma aguda, o tratamento com 10 cmH2O de pressão de CPAP é seguro para pacientes com CMH, com ou sem obstrução da via de saída do VE.235235 Nerbass FB, Salemi VM, Pedrosa RP, Portilho NP, Ferreira-Filho JC, Moriya HT, et al. Acute effects of nasal CPAP in patients with hypertrophic cardiomyopathy. Chest. 2016;150(5):1050-8. doi: 10.1016/j.chest.2016.05.004.
https://doi.org/10.1016/j.chest.2016.05....
4.2.6. Metabolismo Lipídico, Glicídico e Síndrome Metabólica
Estudos apontam que a frequência da AOS em pacientes com Síndorme Metabólica (SM) é de cerca de 65%.236236 Drager LF, Lopes HF, Maki-Nunes C, Trombetta IC, Toschi-Dias E, Alves MJ, et al. The impact of obstructive sleep apnea on metabolic and inflammatory markers in consecutive patients with metabolic syndrome. PLoSOne. 2010;5(8):e12065. doi: 10.1371/journal.pone.0012065.
https://doi.org/10.1371/journal.pone.001...
Em 1988, Wilcox et al.237237 Wilcox I, McNamara SG, Collins FL, Grunstein RR, Sullivan CE. "Syndrome Z": the interaction of sleepapnoea, vascular risk factors and heart disease. Thorax. 1998;53 Suppl 3:S25-8. PMID: 10193357. propuseram que a AOS fizesse fazer parte do espectro da SM, sugerindo o nome de “síndrome Z” para esta associação. No entanto, o grande desafio está no entendimento de a AOS ser um epifenômeno da obesidade e da SM, ou ter efeito em agravar o risco cardiometabólico da obesidade e da SM. De forma resumida, analisaremos a associação da AOS com alguns componentes da SM (a relação com a pressão arterial foi aborada em outra seção), bem como as evidências em pacientes com SM propriamente dita.
4.2.6.1. Apneia Obstrutiva do Sono e Dislipidemia
Estudos experimentais têm consistentemente demonstrado que a hipóxia intermitente, uma característica marcante da AOS, induz dislipidemia, por meio da ativação de genes no fígado envolvidos na biossíntese lipídica,238238 Li J, Thorne LN, Punjabi NM, Sun CK, Schwartz AR, Smith PL, et al. Intermittent hypoxia induces hyperlipidemia in lean mice. Circ Res. 2005;97(7):698-706. doi: 10.1161/01.RES.0000183879.60089.a9.
https://doi.org/10.1161/01.RES.000018387...
239 Li J, Grigoryev DN, Ye SQ, Thorne L, Schwartz AR, Smith PL et al. Chronic intermittent hypoxia upregulatesgenes of lipid biosynthesis in obese mice. J Appl Physiol (1985). 2005;99(5):1643-8. doi: 10.1152/japplphysiol.00522.2005.
https://doi.org/10.1152/japplphysiol.005...
-240240 Savransky V, Jun J, Li J, Nanayakkara A, Fonti S, Moser AB, et al. Dyslipidemia and atherosclerosis induced by chronic intermittent hypoxia are attenuated by deficiency of stearoyl coenzyme A desaturase. Circ Res. 2008;103(10):1173-80. doi: 10.1161/CIRCRESAHA.108.178533.
https://doi.org/10.1161/CIRCRESAHA.108.1...
bem como promove um retardo no clearance de lipoproteínas ricas em triglicérides, por inativação de lipase lipropoteica no tecido adiposo;241241 Drager LF, Li J, Shin MK, Reinke C, Aggarwal NR, Jun JC, et al. Intermittent hypoxia inhibits clearance of triglyceride-rich lipoproteins and inactivates adipose lipoprotein lipase in a mouse model of sleep apnoea. Eur Heart J. 2012;33(6):783-90. doi: 10.1093/eurheartj/ehr097.
https://doi.org/10.1093/eurheartj/ehr097...
,242242 Drager LF, Yao Q, Hernandez KL, Shin MK, Bevans-Fonti S, Gay J, et al. Chronic Intermittent Hypoxia InducesAtherosclerosis via Activation of Adipose Angiopoietin-like 4. Am J Respir Crit Care Med. 2013;188(2):240-8. doi: 10.1164/rccm.201209-1688OC
https://doi.org/10.1164/rccm.201209-1688...
as evidências em humanos, porém, são contraditórias.243243 Drager LF, Jun J, Polotsky VY. Obstructive sleep apnea and dyslipidemia: implications foratherosclerosis. Curr Opin Endocrinol Diabetes Obes. 2010;17(2):161-5. doi: 10.1097/MED.0b013e3283373624. Erratum in: Curr Opin Endocrinol Diabetes Obes. 2010;17(4):394.
https://doi.org/10.1097/MED.0b013e328337...
,244244 Togeiro SM, Carneiro G, Ribeiro Filho FF, Zanella MT, Santos-Silva R, Taddei JA, et al. Consequences of obstructive sleep apnea on metabolic profile: a population-based survey. Obesity (Silver Spring). 2013;21(4):847-51. doi: 10.1002/oby.20288.
https://doi.org/10.1002/oby.20288...
A maioria dos estudos é transversal, com resultados conflitantes (alguns mostram aumento de colesterol total, colesterol ligado à lipoproteína de baixa densidade (LDL-c), triglicerídes e redução do colesterol ligado à lipoproteína de alta densidade (HDL); outros não mostraram alterações em relação ao grupo sem AOS).243243 Drager LF, Jun J, Polotsky VY. Obstructive sleep apnea and dyslipidemia: implications foratherosclerosis. Curr Opin Endocrinol Diabetes Obes. 2010;17(2):161-5. doi: 10.1097/MED.0b013e3283373624. Erratum in: Curr Opin Endocrinol Diabetes Obes. 2010;17(4):394.
https://doi.org/10.1097/MED.0b013e328337...
Ainda, boa parte dos estudos não randomizados disponíveis sugere o benefício do CPAP no perfil lipídico, mas as evidências em estudos randomizados são inconsistentes.243243 Drager LF, Jun J, Polotsky VY. Obstructive sleep apnea and dyslipidemia: implications foratherosclerosis. Curr Opin Endocrinol Diabetes Obes. 2010;17(2):161-5. doi: 10.1097/MED.0b013e3283373624. Erratum in: Curr Opin Endocrinol Diabetes Obes. 2010;17(4):394.
https://doi.org/10.1097/MED.0b013e328337...
No entanto, é importante destacar que a maioria dos estudos não foi primariamente desenhada para avaliar este desfecho, de tal forma que dados como dieta, atividade física e mesmo uso de medicações não foram totalmente controlados. No que diz respeito ao metabolismo lipídico, Phillips et al.245245 Phillips CL, Yee BJ, Marshall NS, Liu PY, Sullivan DR, Grunstein RR. Continuous positive airway pressure reduces postprandial lipidemia in obstructive sleep apnea: a randomized, placebo-controlled crossover trial. Am J RespirCrit Care Med. 2011;184(3):355-61. doi: 10.1164/rccm.201102-0316OC.
https://doi.org/10.1164/rccm.201102-0316...
realizaram estudo randomizado mostrando que o CPAP melhorou triglicérides pós-prandial e os níveis de colesterol total.
4.2.6.2. Apneia Obstrutiva do Sono e Metabolismo Glicídico
Estudos transversais e longitudinais relatam associação independente entre AOS e intolerância à glicose, resistência insulínica e Diabetes Melito (DM) tipo 2.246246 Punjabi NM, Shahar E, Redline S, Gottlieb DJ, Givelber R, Resnick HE. Sleep disordered breathing, glucose intolerance, and insulin resistance: The Sleep Heart Health Study. Am J Epidemiol. 2004;160(6):521-30. doi: 10.1093/aje/kwh261
https://doi.org/10.1093/aje/kwh261...
247 Marshall NS, Wong KK, Phillips CL, Liu PY, Knuiman MW, Grunstein RR. Is sleep apnea an independent risk factor for prevalent and incident diabetes in the Busselton Health Study? J Clin Sleep Med. 2009;5(1):15-20. PMID: 19317376-248248 Reichmuth KJ, Austin D, Skatrud JB, Young T. Association of sleep apnea and type II diabetes: a population-based study. Am J Respir Crit Care Med. 2005;172(12):1590-5. doi: 10.1164/rccm.200504-637OC.
https://doi.org/10.1164/rccm.200504-637O...
Os mecanismos implicados estão principalmente relacionados à hipóxia intermitente, que promove ativação de fatores inflamatórios, do sistema nervoso simpático e do eixo hipotálamo-hipófise adrenal; diminuição dos níveis de adiponectina; e aumento do stress oxidativo.249249 Drager LF, Togeiro SM, Polotsky VY, Lorenzi-Filho G. Obstructive sleep apnea: a cardiometabolic risk in obesity and the metabolic syndrome. J Am Coll Cardiol. 2013;62(7):569-76. doi: 10.1016/j.jacc.2013.05.045.
https://doi.org/10.1016/j.jacc.2013.05.0...
As evidências quanto aos benefícios do tratamento com CPAP na AOS sobre o metabolismo glicídico ainda são controversas, embora exista consistência quando os níveis basais de glicemia são elevados e há boa adesão ao CPAP.250250 Martínez-Ceron E, Fernández-Navarro I, Garcia-Rio F. Effects of continuous positive airway pressure treatment on glucose metabolism in patients with obstructive sleep apnea. Sleep Med Rev. 2016;25:121-30. doi: 10.1016/j.smrv.2015.03.002.
https://doi.org/10.1016/j.smrv.2015.03.0...
Aspectos metodológicos podem explicar os resultados conflitantes da literatura, como o tamanho da amostra, o tipo de paciente selecionado, a gravidade da AOS, a presença de comorbidades, o uso de medicações, a duração do estudo, e a falta do grupo controle e de randomização para o tratamento.
4.2.6.3. Apneia Obstrutiva do Sono e Adiposidade Visceral
Evidências sugerem que tanto a gordura cervical, como a adiposidade abdominal podem contribuir para a AOS.249249 Drager LF, Togeiro SM, Polotsky VY, Lorenzi-Filho G. Obstructive sleep apnea: a cardiometabolic risk in obesity and the metabolic syndrome. J Am Coll Cardiol. 2013;62(7):569-76. doi: 10.1016/j.jacc.2013.05.045.
https://doi.org/10.1016/j.jacc.2013.05.0...
De fato, a adiposidade abdominal reduz o volume pulmonar, diminuindo a tração caudal da faringe, o que predispõe ao colapso desta.249249 Drager LF, Togeiro SM, Polotsky VY, Lorenzi-Filho G. Obstructive sleep apnea: a cardiometabolic risk in obesity and the metabolic syndrome. J Am Coll Cardiol. 2013;62(7):569-76. doi: 10.1016/j.jacc.2013.05.045.
https://doi.org/10.1016/j.jacc.2013.05.0...
Além de contribuir para a AOS, existem evidências de que os componentes da AOS (destacadamente a hipóxia intermitente) possam interagir com a adiposidade visceral, piorando o metabolismo glicídico e lipídico, e amplificar o processo inflamatório, contribuindo para a aterosclerose.240240 Savransky V, Jun J, Li J, Nanayakkara A, Fonti S, Moser AB, et al. Dyslipidemia and atherosclerosis induced by chronic intermittent hypoxia are attenuated by deficiency of stearoyl coenzyme A desaturase. Circ Res. 2008;103(10):1173-80. doi: 10.1161/CIRCRESAHA.108.178533.
https://doi.org/10.1161/CIRCRESAHA.108.1...
,250250 Martínez-Ceron E, Fernández-Navarro I, Garcia-Rio F. Effects of continuous positive airway pressure treatment on glucose metabolism in patients with obstructive sleep apnea. Sleep Med Rev. 2016;25:121-30. doi: 10.1016/j.smrv.2015.03.002.
https://doi.org/10.1016/j.smrv.2015.03.0...
251 Drager LF, Li J, Reinke C, Bevans-Fonti S, Jun JC, Polotsky VY. Intermittent hypoxia exacerbates metabolic effects of diet-induced obesity. Obesity (Silver Spring). 2011;19(11):2167-74. doi: 10.1038/oby.2011.240.
https://doi.org/10.1038/oby.2011.240...
252 Murphy AM, Thomas A, Crinion SJ, Kent BD, Tambuwala MM, Fabre A, et al. Intermittent hypoxia in obstructive sleep apnoea mediates insulin resistance through adipose tissue inflammation. Eur Respir J. 2017;49(4). pii: 1601731. doi: 10.1183/13993003.01731-2016.
https://doi.org/10.1183/13993003.01731-2...
-253253 Poulain L, Thomas A, Rieusset J, Casteilla L, Levy P, Arnaud C, et al. Visceral white fat remodelling contributes to intermittent hypoxia-induced atherogenesis. Eur Respir J. 2014;43(2):513-22. doi: 10.1183/09031936.00019913.
https://doi.org/10.1183/09031936.0001991...
No entanto, o tratamento com o CPAP, embora tenha resultados metabólicos favoráveis, não promove redução do peso e da gordura visceral, como sugerem estudos randomizados e metanálise.254254 Hoyos CM, Sullivan DR, Liu PY. Effect of CPAP on the metabolic syndrome: a randomised sham-controlled study. Thorax. 2013;68(6):588-9. doi: 10.1136/thoraxjnl-2012-203074.
https://doi.org/10.1136/thoraxjnl-2012-2...
255 Sivam S, Phillips CL, Trenell MI, Yee BJ, Liu PY, Wong KK, et al. Effects of 8 weeks of continuous positive airway pressure on abdominal adiposity in obstructive sleep apnoea. Eur Respir J. 2012;40(4):913-8. doi: 10.1183/09031936.00177011.
https://doi.org/10.1183/09031936.0017701...
-256256 Drager LF, Brunoni AR, Jenner R, Lorenzi-Filho G, Benseñor IM, Lotufo PA. Effects of CPAP on body weight in patients with obstructive sleep apnoea: a meta-analysis of randomised trials. Thorax. 2015;70(3):258-64. doi: 10.1136/thoraxjnl-2014-205361.
https://doi.org/10.1136/thoraxjnl-2014-2...
4.2.6.4. Apneia Obstrutiva do Sono na Síndrome Metabólica
A AOS parece exacerbar as alterações metabólicas, inflamatórias e marcadores de aterosclerose precoce em pacientes com SM.236236 Drager LF, Lopes HF, Maki-Nunes C, Trombetta IC, Toschi-Dias E, Alves MJ, et al. The impact of obstructive sleep apnea on metabolic and inflammatory markers in consecutive patients with metabolic syndrome. PLoSOne. 2010;5(8):e12065. doi: 10.1371/journal.pone.0012065.
https://doi.org/10.1371/journal.pone.001...
,257257 Drager LF, Bortolotto LA, Maki-Nunes C, Trombetta IC, Alves MJ, Fraga RF, et al. The incremental role of obstructive sleep apnoea on markers of atherosclerosis in patients with metabolic syndrome. Atherosclerosis. 2010;208(2):490-5. doi: 10.1016/j.atherosclerosis.2009.08.016.
https://doi.org/10.1016/j.atherosclerosi...
Poucos estudos avaliaram o efeito do CPAP nos vários componentes da SM simultaneamente.254254 Hoyos CM, Sullivan DR, Liu PY. Effect of CPAP on the metabolic syndrome: a randomised sham-controlled study. Thorax. 2013;68(6):588-9. doi: 10.1136/thoraxjnl-2012-203074.
https://doi.org/10.1136/thoraxjnl-2012-2...
,258258 Dorkova Z, Petrasova D, Molcanyiova A, Popovnakova M, Tkacova R. Effects of continuous positive airway pressure on cardiovascular risk profile in patients with severe obstructive sleep apnea and metabolic syndrome. Chest. 2008;134(4):686-692. doi: 10.1378/chest.08-0556.
https://doi.org/10.1378/chest.08-0556...
Em estudo não randomizado, 8 semanas de CPAP (> 4 horas por noite em média) foram associadas com reduções da pressão arterial, triglicérides e glicemia.258258 Dorkova Z, Petrasova D, Molcanyiova A, Popovnakova M, Tkacova R. Effects of continuous positive airway pressure on cardiovascular risk profile in patients with severe obstructive sleep apnea and metabolic syndrome. Chest. 2008;134(4):686-692. doi: 10.1378/chest.08-0556.
https://doi.org/10.1378/chest.08-0556...
Hoyos et al.,254254 Hoyos CM, Sullivan DR, Liu PY. Effect of CPAP on the metabolic syndrome: a randomised sham-controlled study. Thorax. 2013;68(6):588-9. doi: 10.1136/thoraxjnl-2012-203074.
https://doi.org/10.1136/thoraxjnl-2012-2...
porém, não encontraram diferenças na sensibilidade insulínica e na gordura abdominal após 12 semanas de CPAP, mas houve melhora da sensibilidade insulínica em 24 semanas. Outro estudo randomizado não mostrou diferenças no perfil metabólico em caucasianos obesos após 6 semanas de CPAP.254254 Hoyos CM, Sullivan DR, Liu PY. Effect of CPAP on the metabolic syndrome: a randomised sham-controlled study. Thorax. 2013;68(6):588-9. doi: 10.1136/thoraxjnl-2012-203074.
https://doi.org/10.1136/thoraxjnl-2012-2...
Novos estudos randomizados, com maior tempo de seguimento e controle de fatores relacionados à dieta e à atividade física são necessários.
Dentro do contexto de outros tratamentos, a combinação de dieta e atividade física reduz alguns componentes da SM, em paralelo à melhora do controle autonômico e quimiorreflexo.259259 Maki-Nunes C, Toschi-Dias E, Cepeda FX, Rondon MU, Alves MJ, Fraga RF, et al. Diet and exercise improve chemoreflex sensitivity in patients with metabolic syndrome and obstructive sleep apnea. Obesity (Silver Spring). 2015;23(8):1582-90. doi: 10.1002/oby.21126.
https://doi.org/10.1002/oby.21126...
No entanto, o impacto sobre a AOS é, em média parcial, ou seja, muitos pacientes com SM ainda permanecem com uma AOS residual.259259 Maki-Nunes C, Toschi-Dias E, Cepeda FX, Rondon MU, Alves MJ, Fraga RF, et al. Diet and exercise improve chemoreflex sensitivity in patients with metabolic syndrome and obstructive sleep apnea. Obesity (Silver Spring). 2015;23(8):1582-90. doi: 10.1002/oby.21126.
https://doi.org/10.1002/oby.21126...
Como a maioria dos estudos foi de curta duração (assim como o CPAP), novos trabalhos são necessários para, inclusive, avaliar a adesão a longo prazo às medidas de mudança de estilo de vida.
4.2.7. Aterosclerose
Evidências crescentes têm apontado a AOS como um fator de risco emergente para a aterosclerose.260260 Drager LF, Polotsky VY, Lorenzi-Filho G. Obstructive sleep apnea: an emerging risk factor for atherosclerosis. Chest. 2011;140(2):534-42. doi: 10.1378/chest.10-2223.
https://doi.org/10.1378/chest.10-2223...
De fato, especula-se que a progressão da aterosclerose possa explicar, em grande parte, a ocorrência mais frequente do IAM e do AVC, observada em pacientes com AOS − especialmente nas formas mais graves deste distúrbio do sono. Existem diversos mecanismos potencialmente aterogênicos desencadeados pelos componentes da AOS, destacadamente pela hipoxemia crônica intermitente. Dentre estes mecanismos, podemos citar a disfunção endotelial,261261 Jelic S, Padeletti M, Kawut SM, Higgins C, Canfield SM, Onat D, et al. Inflammation, oxidative stress, and repair capacity of the vascular endothelium in obstructive sleep apnea. Circulation. 2008;117(17):2270-8. doi: 10.1161/CIRCULATIONAHA.107.741512.
https://doi.org/10.1161/CIRCULATIONAHA.1...
o aumento da pressão arterial,113113 Pedrosa RP, Krieger EM, Lorenzi-Filho G, Drager LF. Recent advances of the impact of obstructive sleep apnea on systemic hypertension. Arq Bras Cardiol. 2011;97(2):e40-7. doi: http://dx.doi.org/10.1590/S0066-782X2011005000017.
http://dx.doi.org/10.1590/S0066-782X2011...
o aumento da inflamação262262 Shamsuzzaman AS, Winnicki M, Lanfranchi P, Wolk R, Kara T, Accurso V, et al. Elevated C-reactive protein in patients with obstructive sleep apnea. Circulation. 2002;105(21):2462-4. PMID: 12034649. e de espécies reativas de oxigênio,263263 Lavie L, Lavie P. Molecular mechanisms of cardiovascular disease in OSAHS: the oxidative stress link. Eur Respir J. 2009;33(6):1467-84. doi: 10.1183/09031936.00086608.
https://doi.org/10.1183/09031936.0008660...
a resistência à insulina251251 Drager LF, Li J, Reinke C, Bevans-Fonti S, Jun JC, Polotsky VY. Intermittent hypoxia exacerbates metabolic effects of diet-induced obesity. Obesity (Silver Spring). 2011;19(11):2167-74. doi: 10.1038/oby.2011.240.
https://doi.org/10.1038/oby.2011.240...
,264264 Carneiro G, Ribeiro Filho FF, Togeiro SM, Tufik S, Zanella MT. [Interactions between obstructive sleep apnea syndrome and insulin resistance]. Arq Bras Endocrinol Metabol. 2007;51(7):1035-40. doi: http://dx.doi.org/10.1590/S0004-27302007000700003.
http://dx.doi.org/10.1590/S0004-27302007...
e a dislipidemia,243243 Drager LF, Jun J, Polotsky VY. Obstructive sleep apnea and dyslipidemia: implications foratherosclerosis. Curr Opin Endocrinol Diabetes Obes. 2010;17(2):161-5. doi: 10.1097/MED.0b013e3283373624. Erratum in: Curr Opin Endocrinol Diabetes Obes. 2010;17(4):394.
https://doi.org/10.1097/MED.0b013e328337...
principalmente a dislipidemia pós-prandial por redução do clearance de lipoproteínas ricas em triglicérides.2121 Logan AG, Perlikowski SM, Mente A, Tisler A, Tkacova R, Niroumand M, et al. High prevalence of unrecognized sleep apnea in drug-resistant hypertension. J Hypertens. 2001;19(12):2271-7. PMID: 11725173.,242242 Drager LF, Yao Q, Hernandez KL, Shin MK, Bevans-Fonti S, Gay J, et al. Chronic Intermittent Hypoxia InducesAtherosclerosis via Activation of Adipose Angiopoietin-like 4. Am J Respir Crit Care Med. 2013;188(2):240-8. doi: 10.1164/rccm.201209-1688OC
https://doi.org/10.1164/rccm.201209-1688...
,245245 Phillips CL, Yee BJ, Marshall NS, Liu PY, Sullivan DR, Grunstein RR. Continuous positive airway pressure reduces postprandial lipidemia in obstructive sleep apnea: a randomized, placebo-controlled crossover trial. Am J RespirCrit Care Med. 2011;184(3):355-61. doi: 10.1164/rccm.201102-0316OC.
https://doi.org/10.1164/rccm.201102-0316...
Até o momento existem mais de 50 artigos que avaliaram a associação da AOS com marcadores precoces de aterosclerose,3434 Sorajja D, Gami AS, Somers VK, Behrenbeck TR, Garcia-Touchard A, Lopez-Jimenez F. Independent association between obstructive sleep apnea and subclinical coronary artery disease. Chest. 2008;133(4):927-33. doi: 10.1378/chest.07-2544.
https://doi.org/10.1378/chest.07-2544...
,190190 Baguet JP, Nadra M, Barone-Rochette G, Ormezzano O, Pierre H, Pépin JL. Early cardiovascular abnormalities in newly diagnosed obstructive sleep apnea. Vasc Health Risk Manag. 2009;5:1063-73. PMID: 20057899.,257257 Drager LF, Bortolotto LA, Maki-Nunes C, Trombetta IC, Alves MJ, Fraga RF, et al. The incremental role of obstructive sleep apnoea on markers of atherosclerosis in patients with metabolic syndrome. Atherosclerosis. 2010;208(2):490-5. doi: 10.1016/j.atherosclerosis.2009.08.016.
https://doi.org/10.1016/j.atherosclerosi...
,265265 Friedlander AH, Yueh R, Littner MR. The prevalence of calcified carotid artery atheromas in patients with obstructive sleep apnea syndrome. J Oral Maxillofac Surg. 1998;56(8):950-4. PMID: 9710189.
266 Friedlander AH, Friedlander IK, Yueh R, Littner MR. The prevalence of carotid atheromas seen on panoramic radiographs of patients with obstructive sleep apnea and their relation to risk factors for atherosclerosis. J Oral Maxillofac Surg. 1999;57(5):516-21. PMID: 10319824.
267 Cilli A, Tatlicioglu T, Köktürk O. Nocturnal oxygen desaturation in coronary artery disease. Jpn Heart J. 1999;40(1):23-9. PMID: 10370394.
268 Silvestrini M, Rizzato B, Placidi F, Baruffaldi R, Bianconi A, Diomedi M. Carotid artery wall thickness in patients with obstructive sleep apnea syndrome. Stroke. 2002;33(7):1782-5. PMID: 12105352.
269 Nachtmann A, Stang A, Wang YM, Wondzinski E, Thilmann AF. Association of obstructive sleep apnea and stenotic artery disease in ischemic stroke patients. Atherosclerosis. 2003;169(2):301-7. PMID: 12921982.
270 Hayashi M, Fujimoto K, Urushibata K, Uchikawa S, Imamura H, Kubo K. Nocturnal oxygen desaturation correlates with the severity of coronary atherosclerosis in coronary artery disease. Chest. 2003;124(3):936-41. PMID: 12970020.
271 Suzuki T, Nakano H, Maekawa J, Okamoto Y, Ohnishi Y, Yamauchi M, et al. Obstructive sleep apnea and carotid-artery intima-media thickness. Sleep. 2004;27(1):129-33. PMID: 14998249.
272 Schulz R, Seeger W, Fegbeutel C, Hüsken H, Bödeker RH, Tillmanns H, et al. Changes in extracranial arteries in obstructive sleep apnoea. Eur Respir J. 2005;25(1):69-74. doi: 10.1183/09031936.04.00030004.
https://doi.org/10.1183/09031936.04.0003...
273 Altin R, Ozdemir H, Mahmutyazicioglu K, Kart L, Uzun L, Ozer T, et al. Evaluation of carotid artery wall thickness with high-resolution sonography in obstructive sleep apnea syndrome. J Clin Ultrasound. 2005;33(2):80-6. doi: 10.1002/jcu.20093.
https://doi.org/10.1002/jcu.20093...
274 Drager LF, Bortolotto LA, Lorenzi MC, Figueiredo AC, Krieger EM, Lorenzi-Filho G. Early signs of atherosclerosis in obstructive sleep apnea. Am J Respir Crit Care Med. 2005;172(5):613-8. doi: 10.1164/rccm.200503-340OC.
https://doi.org/10.1164/rccm.200503-340O...
275 Minoguchi K, Yokoe T, Tazaki T, Minoguchi H, Tanaka A, Oda N, et al. Increased carotid intima-media thickness and serum inflammatory markers in obstructive sleep apnea.Am J Respir Crit Care Med. 2005;172(5):625-30. doi: 10.1164/rccm.200412-1652OC.
https://doi.org/10.1164/rccm.200412-1652...
276 Tian JL, Zhang Y, Wang Z, Cao L, Chen BY. [A study on non-invasive indexes of atherosclerosis in obstructive sleep apnea-hypopnea syndrome patients]. Zhonghua Jie He He Hu Xi Za Zhi. 2006;29(6):395-8. PMID: 17045022.
277 Tanriverdi H, Evrengul H, Kara CO, Kuru O, Tanriverdi S, Ozkurt S, et al. Aortic stiffness, flow-mediated dilatation and carotid intima-media thickness in obstructive sleep apnea: non-invasive indicators of atherosclerosis. Respiration. 2006;73(6):741-50. doi: 10.1159/000093531.
https://doi.org/10.1159/000093531...
278 Saletu M, Nosiska D, Kapfhammer G, Lalouschek W, Saletu B, Benesch T, et al. Structural and serum surrogate markers of cerebrovascular disease in obstructive sleep apnea (OSA): association of mild OSA with early atherosclerosis. J Neurol. 2006;253(6):746-52. doi: 10.1007/s00415-006-0110-6.
https://doi.org/10.1007/s00415-006-0110-...
279 Lu G, Xu ZW, Zhang YL, Yang ZJ, Zhang XL, Yin KS. Correlation among obstructive sleep apnea syndrome, coronary atherosclerosis and coronary heart disease.Chin Med J (Engl). 2007;120(18):1632-4. PMID: 17908485.
280 Lu G, Xu ZW, Liu JN, Zhang YL, Yang ZJ, Zhang XL, et al. [A study on the association of obstructive sleep apnea hypopnea syndrome with coronary atherosclerosis and coronary heart disease]. Zhonghua Jie He He Hu Xi Za Zhi. 2007;30(3):178-81. PMID: 17572995.
281 Szabóová E, Tomori Z, Donic V, Petrovicová J, Szabó P. Sleep apnoea inducing hypoxemia is associated with early signs of carotid atherosclerosis in males.Respir Physiol Neurobiol. 2007;155(2):121-7. doi: 10.1016/j.resp.2006.05.004.
https://doi.org/10.1016/j.resp.2006.05.0...
282 Dziewas R, Ritter M, Usta N, Boentert M, Hor H, Dittrich R, et al. Atherosclerosis and obstructive sleep apnea in patients with ischemic stroke. Cerebrovasc Dis. 2007;24(1):122-6. doi: 10.1159/000103611.
https://doi.org/10.1159/000103611...
283 Drager LF, Bortolotto LA, Figueiredo AC, Krieger EM, Lorenzi GF. Effects of continuous positive airway pressure on early signs of atherosclerosis in obstructive sleep apnea. Am J Respir Crit Care Med. 2007;176(7):706-12. doi: 10.1164/rccm.200703-500OC.
https://doi.org/10.1164/rccm.200703-500O...
284 Wattanakit K, Boland L, Punjabi NM, Shahar E. Relation of sleep-disordered breathing to carotid plaque and intima-media thickness. Atherosclerosis. 2008;197(1):125-31. doi: 10.1016/j.atherosclerosis.2007.02.029.
https://doi.org/10.1016/j.atherosclerosi...
285 Lefebvre B, Pépin JL, Baguet JP, Tamisier R, Roustit M, Riedweg K, et al. Leukotriene B4: early mediator of atherosclerosis in obstructive sleep apnoea? Eur Respir J. 2008;32(1):113-20. doi: 10.1183/09031936.00137107.
https://doi.org/10.1183/09031936.0013710...
286 Saletu M, Sauter C, Lalouschek W, Saletu B, Kapfhammer G, Benesch T, et al. Is excessive daytime sleepiness a predictor of carotid atherosclerosis in sleep apnea? Atherosclerosis. 2008;196(2):810-6. doi: 10.1016/j.atherosclerosis.2007.01.016.
https://doi.org/10.1016/j.atherosclerosi...
287 Protogerou AD, Laaban JP, Czernichow S, Kostopoulos C, Lekakis J, Safar ME, et al. Structural and functional arterial properties in patients with obstructive sleep apnoea syndrome and cardiovascular comorbidities. J Hum Hypertens. 2008;22(6):415-22. doi: 10.1038/sj.jhh.1002318.
https://doi.org/10.1038/sj.jhh.1002318...
288 Drager LF, Bortolotto LA, Krieger EM, Lorenzi-Filho G. Additive effects of obstructive sleep apnea and hypertension on early markers of carotid atherosclerosis. Hypertension. 2009;53(1):64-9. doi: 10.1161/HYPERTENSIONAHA.108.119420.
https://doi.org/10.1161/HYPERTENSIONAHA....
289 Kong L, Guo XH. [The relation between obstructive sleep apnea hypopnea syndrome and the severity of coronary atherosclerosis in coronary artery disease]. Zhonghua Nei Ke Za Zhi. 2009;48(8):638-42. PMID: 19954054.
290 Li C, Zhang XL, Liu H, Wang ZG, Yin KS. Association among plasma interleukin-18 levels, carotid intima- media thickness and severity of obstructive sleep apnea. Chin Med J (Engl). 2009;122(1):24-9. PMID: 19187612.
291 Turmel J, Sériès F, Boulet LP, Poirier P, Tardif JC, Rodés-Cabeau J, et al. Relationship between atherosclerosis and the sleep apnea syndrome: an intravascular ultrasound study. Int J Cardiol. 2009;132(2):203-9. doi: 10.1016/j.ijcard.2007.11.063.
https://doi.org/10.1016/j.ijcard.2007.11...
292 Kim SH, Cho GY, Baik I, Kim J, Kim SJ, Lee JB, et al. Association of coronary artery calcification with obstructive sleep apnea and obesity in middle-aged men. Nutr Metab Cardiovasc Dis. 2010;20(8):575-82. doi: 10.1016/j.numecd.2009.05.011.
https://doi.org/10.1016/j.numecd.2009.05...
293 Monneret D, Pepin JL, Godin-Ribuot D, Ducros V, Baguet JP, Levy P, et al. Association of urinary 15-F2t-isoprostane level with oxygen desaturation and carotid intima-media thickness in nonobese sleep apnea patients. Free Radic Biol Med. 2010;48(4):619-25. doi: 10.1016/j.freeradbiomed.2009.12.008
https://doi.org/10.1016/j.freeradbiomed....
294 Tsuda H, Almeida FR, Tsuda T, Moritsuchi Y, Lowe AA. Cephalometric calcified carotid artery atheromas in patients with obstructive sleep apnea. Sleep Breath. 2010;14(4):365-70. doi: 10.1007/s11325-009-0324-9.
https://doi.org/10.1007/s11325-009-0324-...
295 Yun CH, Jung KH, Chu K, Kim SH, Ji KH, Park HK, et al. Increased circulating endothelial microparticles and carotid atherosclerosis in obstructive sleep apnea. J Clin Neurol. 2010;6(2):89-98. doi: 10.3988/jcn.2010.6.2.89.
https://doi.org/10.3988/jcn.2010.6.2.89...
296 Steiropoulos P, Bogiatzi C, Archontogeorgis K, Nena E, Xanthoudaki M, Boglou P, et al. Is there evidence of early vascular disease in patients with obstructive sleep apnoea without known comorbidities? Preliminary findings. Open Cardiovasc Med J. 2013;7:61-8. doi: 10.2174/1874192401307010061.
https://doi.org/10.2174/1874192401307010...
297 Akyuz A, Oran M, Alpsoy S, Mutlu LC, Akkoyun DC, Guzel S, et al. Association between serum fetuin-A levels, carotid artery stiffness, and intima-media thickness in patients with normotensive obstructive sleep apnea syndrome. Angiology. 2014;65(7):607-13. doi: 10.1177/0003319713497421.
https://doi.org/10.1177/0003319713497421...
298 Iannuzzi A, Licenziati MR, De Michele F, Verga MC, Santoriello C, Di Buono L, et al. C-reactive protein and carotid intima-media thickness in children with sleep disordered breathing. J Clin Sleep Med. 2013;9(5):493-8. doi: 10.5664/jcsm.2674.
https://doi.org/10.5664/jcsm.2674...
299 Apaydin M, Ayik SO, Akhan G, Peker S, Uluc E. Carotid intima-media thickness increase in patients with habitual simple snoring and obstructive sleep apnea syndrome is associated with metabolic syndrome. J Clin Ultrasound. 2013;41(5):290-6. doi: 10.1002/jcu.22040.
https://doi.org/10.1002/jcu.22040...
300 Kent BD, Garvey JF, Ryan S, Nolan G, Dodd JD, McNicholas WT. Severity of obstructive sleep apnoea predicts coronary artery plaque burden: a coronary computed tomographic angiography study. Eur Respir J. 2013;42(5):1263-70. doi: 10.1183/09031936.00094812.
https://doi.org/10.1183/09031936.0009481...
301 Arik B, Inci MF, Gumus C, Varol K, Ege MR, Dogan OT, et al. Advanced age and apnea-hypopnea index predict subclinical atherosclerosis in patients with obstructive sleep apnea syndrome. Multidiscip Respir Med. 2013;8(1):9. doi: 10.1186/2049-6958-8-9.
https://doi.org/10.1186/2049-6958-8-9...
302 Sforza E, Boissier C, Martin MS, Feasson S, Barthélémy JC, Roche F. Carotid artery atherosclerosis and sleep disordered breathing in healthy elderly subjects: the Synapse cohort. Sleep Med. 2013;14(1):66-70. doi: 10.1016/j.sleep.2012.08.016.
https://doi.org/10.1016/j.sleep.2012.08....
303 Sharma S, Gebregziabher M, Parker AT, Abro JA, Armstrong AM, Schoepf UJ. Independent association between obstructive sleep apnea and noncalcified coronary plaque demonstrated by noninvasive coronary computed tomography angiography. Clin Cardiol. 2012;35(10):641-5. doi: 10.1002/clc.22057.
https://doi.org/10.1002/clc.22057...
304 Tan TY, Liou CW, Friedman M, Lin HC, Chang HW, Lin MC. Factors associated with increased carotid intima-media thickness in obstructive sleep apnea/hypopnea syndrome. Neurologist. 2012;18(5):277-81. doi: 10.1097/NRL.0b013e3182675344.
https://doi.org/10.1097/NRL.0b013e318267...
305 Stanke-Labesque F, Pépin JL, de Jouvencel T, Arnaud C, Baguet JP, Petri MH, et al. Leukotriene B4 pathway activation and atherosclerosis in obstructive sleep apnea. J Lipid Res. 2012;53(9):1944-51. doi: 10.1194/jlr.P022814.
https://doi.org/10.1194/jlr.P022814...
306 Chang TI, Tanner JM, Harada ND, Garrett NR, Friedlander AH. Prevalence of calcified carotid artery atheromas on the panoramic images of patients with syndrome Z, coexisting obstructive sleep apnea, and metabolic syndrome. Oral Surg Oral Med Oral Pathol Oral Radiol. 2012;113(1):134-41. doi: 10.1016/j.tripleo.2011.07.039.
https://doi.org/10.1016/j.tripleo.2011.0...
307 Kylintireas I, Craig S, Nethononda R, Kohler M, Francis J, Choudhury R, et al. Atherosclerosis and arterial stiffness in obstructive sleep apnea--a cardiovascular magnetic resonance study. Atherosclerosis. 2012;222(2):483-9. doi: 10.1016/j.atherosclerosis.2012.03.036.
https://doi.org/10.1016/j.atherosclerosi...
308 Ciccone MM, Scicchitano P, Mitacchione G, Zito A, Gesualdo M, Caputo P, et al. Is there a correlation between OSAS duration/severity and carotid intima-media thickness? Respir Med. 2012;106(5):740-6. doi: 10.1016/j.rmed.2011.12.016.
https://doi.org/10.1016/j.rmed.2011.12.0...
309 Monneret D, Tamisier R, Ducros V, Garrel C, Levy P, Baguet JP, et al. The impact of obstructive sleep apnea on homocysteine and carotid remodeling in metabolic syndrome. Respir Physiol Neurobiol. 2012;180(2-3):298-304. doi: 10.1016/j.resp.2011.12.009.
https://doi.org/10.1016/j.resp.2011.12.0...
310 Kepez A, Niksarlioglu EY, Hazirolan T, Hayran M, Kocabas U, Demir AU, et al. Evaluation of association between obstructive sleep apnea and coronary risk scores predicted by tomographic coronary calcium scoring in asymptomatic patients. Anadolu Kardiyol Derg. 2011;11(5):428-35. doi: 10.5152/akd.2011.106.
https://doi.org/10.5152/akd.2011.106...
311 Weinreich G, Wessendorf TE, Erdmann T, Moebus S, Dragano N, Lehmann N, et al; Heinz Nixdorf Recall (HNR) study group. Association of obstructive sleep apnoea with subclinical coronary atherosclerosis. Atherosclerosis. 2013;231(2):191-7. doi: 10.1016/j.atherosclerosis.2013.09.011.
https://doi.org/10.1016/j.atherosclerosi...
312 Kwon Y, Duprez DA, Jacobs DR, Nagayoshi M, McClelland RL, Shahar E, et al. Obstructive sleep apnea and progression of coronary artery calcium: the multi-ethnic study of atherosclerosis study. J Am Heart Assoc. 2014;3(5):e001241. doi: 10.1161/JAHA.114.001241.
https://doi.org/10.1161/JAHA.114.001241...
-313313 Gunnarsson SI, Peppard PE, Korcarz CE, Barnet JH, Aeschlimann SE, Hagen EW, et al. Obstructive sleep apnea is associated with future subclinical carotid artery disease: thirteen-year follow-up from the Wisconsin sleep cohort. Arterioscler Thromb Vasc Biol. 2014;34(10):2338-42. doi: 10.1161/ATVBAHA.114.303965.
https://doi.org/10.1161/ATVBAHA.114.3039...
e a maioria mostrou relação positiva da presença da AOS com um aumento dos marcadores de aterosclerose. O território mais estudado foi o carotídeo, embora existam estudos que avaliaram a aterosclerose coronariana. No que diz respeito ao tratamento, três estudos (um randomizado e dois não) exploraram o impacto do tratamento da AOS com o CPAP. Dois deles (incluindo o randomizado)283283 Drager LF, Bortolotto LA, Figueiredo AC, Krieger EM, Lorenzi GF. Effects of continuous positive airway pressure on early signs of atherosclerosis in obstructive sleep apnea. Am J Respir Crit Care Med. 2007;176(7):706-12. doi: 10.1164/rccm.200703-500OC.
https://doi.org/10.1164/rccm.200703-500O...
mostraram atenuação da espessura íntima média da carótida após o tratamento. Nenhum estudo avaliou o impacto do tratamento da AOS sobre placas ateroscleróticas. Estudos recentes começaram a dar indícios sobre o papel da AOS na evolução da doença aterosclerótica. Na coorte do MESA (Multi-Ethnic Study of Atherosclerosis), 2.603 participantes que responderam no periodo basal um questionário do sono (2002-2004) e foram submetidos à angiotomografia de coronárias no basal, e oito participantes após (2010-2011) demonstraram que a suspeita da AOS não foi associada com a progressão da aterosclerose após ajustes para outros fatores de risco cardiovascular.312312 Kwon Y, Duprez DA, Jacobs DR, Nagayoshi M, McClelland RL, Shahar E, et al. Obstructive sleep apnea and progression of coronary artery calcium: the multi-ethnic study of atherosclerosis study. J Am Heart Assoc. 2014;3(5):e001241. doi: 10.1161/JAHA.114.001241.
https://doi.org/10.1161/JAHA.114.001241...
A maior limitação deste estudo foi a ausência da realização sistemática de um estudo do sono nestes participantes.312312 Kwon Y, Duprez DA, Jacobs DR, Nagayoshi M, McClelland RL, Shahar E, et al. Obstructive sleep apnea and progression of coronary artery calcium: the multi-ethnic study of atherosclerosis study. J Am Heart Assoc. 2014;3(5):e001241. doi: 10.1161/JAHA.114.001241.
https://doi.org/10.1161/JAHA.114.001241...
Gunnarsson et al.313313 Gunnarsson SI, Peppard PE, Korcarz CE, Barnet JH, Aeschlimann SE, Hagen EW, et al. Obstructive sleep apnea is associated with future subclinical carotid artery disease: thirteen-year follow-up from the Wisconsin sleep cohort. Arterioscler Thromb Vasc Biol. 2014;34(10):2338-42. doi: 10.1161/ATVBAHA.114.303965.
https://doi.org/10.1161/ATVBAHA.114.3039...
encontraram que a presença da AOS foi independentemente associada com um aumento da espessura e placa carotídea 10 anos após.No entanto, este estudo é limitado pela ausência de dados sobre os marcadores de aterosclerose no período basal (próximo à realização da polissonografia), o que impede avaliar a verdadeira extensão da progressão da aterosclerose. Desta forma, novos estudos são necessários para avaliar se a AOS acelera a progressão e o tratamento da AOS pode retardar a evolução da doença aterosclerótica.
4.2.8. Doença Arterial Coronariana
Conforme discutido, há evidências crescentes de que a AOS pode contribuir para o processo de aterosclerose e, portanto, da DAC. Além disto, a AOS parece estar associada com mecanismos relacionados à ocorrência da DAC, como a trombose. Estudos têm demonstrado o aumento da atividade plaquetária, a atividade fibrinolítica reduzida e o aumento da concentração de fibrinogênio em pacientes com AOS.314314 Rahangdale S, Yeh SY, Novack V, Stevenson K, Barnard MR, Furman MI, et al. The influence of intermittent hypoxemia on platelet activation in obese patients with obstructive sleep apnea. J Clin Sleep Med. 2011;7(2):172-8. PMID: 21509332.,315315 von Känel R, Dimsdale JE. Hemostatic alterations in patients with obstructive sleep apnea and the implications for cardiovascular disease. Chest. 2003;124(5):1956-67. PMID: 14605073. Estas alterações também foram revertidas após tratamento da AOS com CPAP.316316 Hui DS, Ko FW, Fok JP, Chan MC, Li TS, Tomlinson B, et al. The effects of nasal continuous positive airway pressure on platelet activation in obstructive sleep apnea syndrome. Chest. 2004;125(5):1768-75. PMID: 15136389.,317317 von Känel R, Loredo JS, Ancoli-Israel S, Dimsdale JE. Association between sleep apnea severity and blood coagulability: treatment effects of nasal continuous positive airway pressure. Sleep Breath. 2006;10(3):139-46. doi: 10.1007/s11325-006-0060-3.
https://doi.org/10.1007/s11325-006-0060-...
No entanto, os mecanismos exatos para este estado de hipercoagulabilidade na AOS ainda precisam ser melhor esclarecidos.
A AOS pode ser considerada uma situação de estresse noturno, na qual há maior consumo de oxigênio pelo miocárdio e, em indivíduos em que a reserva coronária já é insuficiente, como na população de DAC, este mecanismo de maior consumo de oxigênio pode gerar isquemia noturna. Durante o colapso recorrente da via aérea superior nos pacientes com AOS, a pressão intratorácica negativa fica mais negativa e aumenta o gradiente pressórico transmural para o VE. Isto eleva a pós-carga e, consequentemente, aumenta o consumo de oxigênio pelo miocárdio. Nos pacientes com DAC, este desbalanço de oxigênio pelo maior consumo em um miocárdio que já apresenta défice na reserva coronária gera isquemia miocárdica.318318 Bradley TD, Floras JS. Obstructive sleep apnoea and its cardiovascular consequences. Lancet. 2009;373(9657):82-93. doi: 10.1016/S0140-6736(08)61622-0.
https://doi.org/10.1016/S0140-6736(08)61...
Também, a AOS, como resultado dos eventos de apneia e de hipopneia, gera hipoxemia e hipercapnia. Em resposta aos eventos apneicos, ocorre tentativa de resturar a respiração com esforços contra uma via aérea superior ocluída. Então, ocorrem despertares com consequente fragmentação do sono, além de maior ativação simpática, resultando na elevação da pressão arterial e da frequência cardíaca de repouso, o que também pode acentuar a isquemia miocárdica noturna na população vulnerável de DAC.318318 Bradley TD, Floras JS. Obstructive sleep apnoea and its cardiovascular consequences. Lancet. 2009;373(9657):82-93. doi: 10.1016/S0140-6736(08)61622-0.
https://doi.org/10.1016/S0140-6736(08)61...
A evidência clínica da isquemia miocárdica noturna induzida por AOS já foi descrita em alguns estudos, mas ainda precisa de mais pesquisa neste tópico, visto que os estudos relacionados têm limitações importantes − a maioria é observacional, transversal e com número reduzido de participantes. Angina noturna com gatilho pela AOS319319 Franklin KA, Nilsson JB, Sahlin C, Naslund U. Sleep apnoea and nocturnal angina. Lancet. 1995;345(8957):1085-7. PMID: 7715342. e alterações isquêmicas do segmento ST no ECG (depressão do segmento ST) foram observadas em pacientes com AOS e DAC,320320 Peled N, Abinader EG, Pillar G, Sharif D, Lavie P. Nocturnal ischemic events in patients with obstructive sleep apnea syndrome and ischemic heart disease: effects of continuous positive air pressure treatment. J Am Coll Cardiol. 1999;34(6):1744-9. PMID: 10577565. mas estas alterações também foram reportadas em pacientes com AOS e sem DAC, ou seja, apenas pela presença da AOS.321321 Hanly P, Sasson Z, Zuberi N, Lunn K. ST-segment depression during sleep in obstructive sleep apnea. Am J Cardiol. 1993;71(15):1341-5. PMID: 8498378.,322322 Philip P, Guilleminault C. ST segment abnormality, angina during sleep and obstructive sleep apnea. Sleep. 1993;16(6):558-9. PMID: 8235241. No entanto, se a AOS é o gatilho para isquemia noturna, isto ainda precisa ser mais investigado, já que há conflitos na literatura sobre este tema.323323 Araújo CM, Solimene MC, Grupi CJ, Genta PR, Lorenzi-Filho G, Da Luz PL. Evidence that the degree of obstructive sleep apnea may not increase myocardial ischemia and arrhythmias in patients with stable coronary artery disease. Clinics (Sao Paulo). 2009;64(3):223-30. doi: http://dx.doi.org/10.1590/S1807-59322009000300013.
http://dx.doi.org/10.1590/S1807-59322009...
,324324 Gami AS, Svatikova A, Wolk R, Olson EJ, Duenwald CJ, Jaffe AS, et al. Cardiac troponin T in obstructive sleep apnea. Chest. 2004;125(6):2097-100. PMID: 15189927. Por exemplo, estudo brasileiro, que avaliou pacientes com DAC estável pela polissonografia noturna e também com Holter 24 horas, após período de 3 a 7 dias de retirada da medicação antiangionosa desta população, não observou diferença nos eventos de isquemia de acordo com as alterações do segmento ST do ECG, entre pacientes com ou sem AOS.323323 Araújo CM, Solimene MC, Grupi CJ, Genta PR, Lorenzi-Filho G, Da Luz PL. Evidence that the degree of obstructive sleep apnea may not increase myocardial ischemia and arrhythmias in patients with stable coronary artery disease. Clinics (Sao Paulo). 2009;64(3):223-30. doi: http://dx.doi.org/10.1590/S1807-59322009000300013.
http://dx.doi.org/10.1590/S1807-59322009...
Gami et al.324324 Gami AS, Svatikova A, Wolk R, Olson EJ, Duenwald CJ, Jaffe AS, et al. Cardiac troponin T in obstructive sleep apnea. Chest. 2004;125(6):2097-100. PMID: 15189927. também estudaram a presença de isquemia miocárdica em pacientes com DAC e AOS moderada à importante, por meio da coleta de troponina cardíaca T. Apesar da população do estudo ter mostrado média de IAH de 41 eventos por hora de sono e nadir médio de desaturação de oxigênio de 83%, as dosagens de troponina T antes do sono, 4 horas após dormir e na manhã seguinte ao exame não apresentaram alterações.324324 Gami AS, Svatikova A, Wolk R, Olson EJ, Duenwald CJ, Jaffe AS, et al. Cardiac troponin T in obstructive sleep apnea. Chest. 2004;125(6):2097-100. PMID: 15189927. No entanto, o ensaio desta troponina não era ultrassensível, o que pode ter sido a causa da não detecção dos níveis da troponina neste estudo. Estudos populacionais,325325 Querejeta Roca G, Redline S, Punjabi N, Claggett B, Ballantyne CM, Solomon SD, et al. Sleep apnea is associated with subclinical myocardial injury in the community. The ARIC-SHHS study. Am J Respir Crit Care Med. 2013;188(12):1460-5. doi: 10.1164/rccm.201309-1572OC.
https://doi.org/10.1164/rccm.201309-1572...
,326326 Einvik G, Røsjø H, Randby A, Namtvedt SK, Hrubos-Strøm H, Brynildsen J, et al. Severity of obstructive sleep apnea is associated with cardiac troponin I concentrations in a community-based sample: data from the Akershus Sleep Apnea Project. Sleep. 2014;37(6):1111-6, 1116A-1116B. doi: 10.5665/sleep.3772.
https://doi.org/10.5665/sleep.3772...
mesmo na ausência de DAC, já mostraram elevação da troponina cardíaca de forma independente associada a AOS, evidenciando injúria miocárdica subclínica pela presença da AOS. Geovanini et al.327327 Geovanini GR, Pereira AC, Gowdak LH, Dourado LO, Poppi NT, Venturini G, et al. Obstructive sleep apnoea is associated with myocardial injury in patients with refractory angina. Heart. 2016;102(15):1193-9. doi: 10.1136/heartjnl-2015-309009.
https://doi.org/10.1136/heartjnl-2015-30...
estudaram pacientes com angina refratária. Tratava-se de população de DAC crônica, com queixa persistente de angina pectoris, apesar de terapia médica otimizada, tratamento de revasculariazação miocárdica cirúrgico e percutâneo. Nesta população homogênea, eles evidenciaram que o grupo de AOS mais importante apresentou variação da tropopnina T cardíaca, com elevação dos níveis de troponina na manhã seguinte ao exame do sono em relação à coleta pré-sono, o que não foi visto no grupo sem AOS ou nos grupos com AOS leve a moderada Portanto, a AOS pode não só causar injúria miocárdica.327327 Geovanini GR, Pereira AC, Gowdak LH, Dourado LO, Poppi NT, Venturini G, et al. Obstructive sleep apnoea is associated with myocardial injury in patients with refractory angina. Heart. 2016;102(15):1193-9. doi: 10.1136/heartjnl-2015-309009.
https://doi.org/10.1136/heartjnl-2015-30...
,321321 Hanly P, Sasson Z, Zuberi N, Lunn K. ST-segment depression during sleep in obstructive sleep apnea. Am J Cardiol. 1993;71(15):1341-5. PMID: 8498378.,322322 Philip P, Guilleminault C. ST segment abnormality, angina during sleep and obstructive sleep apnea. Sleep. 1993;16(6):558-9. PMID: 8235241.,325325 Querejeta Roca G, Redline S, Punjabi N, Claggett B, Ballantyne CM, Solomon SD, et al. Sleep apnea is associated with subclinical myocardial injury in the community. The ARIC-SHHS study. Am J Respir Crit Care Med. 2013;188(12):1460-5. doi: 10.1164/rccm.201309-1572OC.
https://doi.org/10.1164/rccm.201309-1572...
,326326 Einvik G, Røsjø H, Randby A, Namtvedt SK, Hrubos-Strøm H, Brynildsen J, et al. Severity of obstructive sleep apnea is associated with cardiac troponin I concentrations in a community-based sample: data from the Akershus Sleep Apnea Project. Sleep. 2014;37(6):1111-6, 1116A-1116B. doi: 10.5665/sleep.3772.
https://doi.org/10.5665/sleep.3772...
mas também pode levar à isquemia miocárdica em pacientes com DAC. 319319 Franklin KA, Nilsson JB, Sahlin C, Naslund U. Sleep apnoea and nocturnal angina. Lancet. 1995;345(8957):1085-7. PMID: 7715342.,320320 Peled N, Abinader EG, Pillar G, Sharif D, Lavie P. Nocturnal ischemic events in patients with obstructive sleep apnea syndrome and ischemic heart disease: effects of continuous positive air pressure treatment. J Am Coll Cardiol. 1999;34(6):1744-9. PMID: 10577565.,327327 Geovanini GR, Pereira AC, Gowdak LH, Dourado LO, Poppi NT, Venturini G, et al. Obstructive sleep apnoea is associated with myocardial injury in patients with refractory angina. Heart. 2016;102(15):1193-9. doi: 10.1136/heartjnl-2015-309009.
https://doi.org/10.1136/heartjnl-2015-30...
Um dado interessante é o padrão circadiano da ocorrência de DAC em pacientes com AOS. De fato, há evidências tanto no cenário do IAM,328328 Kuniyoshi FH, Garcia-Touchard A, Gami AS, Romero-Corral A, van der Walt C, Pusalavidyasagar S, et al. Day-night variation of acute myocardial infarction in obstructive sleep apnea. J Am Coll Cardiol. 2008;52(5):343-6. doi: 10.1016/j.jacc.2008.04.027.
https://doi.org/10.1016/j.jacc.2008.04.0...
como no da morte súbita,329329 Gami AS, Howard DE, Olson EJ, Somers VK. Day-night pattern of sudden death in obstructive sleep apnea. N Engl J Med. 2005;352(12):1206-14. doi: 10.1056/NEJMoa041832.
https://doi.org/10.1056/NEJMoa041832...
de que estes eventos foram mais frequentes à noite em pacientes com AOS, contrariando o padrão circadiano do IAM na população geral, que é diurno (entre 6h às 12h). Por exemplo, no estudo da variação circadiana do padrão de IAM,328328 Kuniyoshi FH, Garcia-Touchard A, Gami AS, Romero-Corral A, van der Walt C, Pusalavidyasagar S, et al. Day-night variation of acute myocardial infarction in obstructive sleep apnea. J Am Coll Cardiol. 2008;52(5):343-6. doi: 10.1016/j.jacc.2008.04.027.
https://doi.org/10.1016/j.jacc.2008.04.0...
os casos de IAM no período noturno (de 0h até 6h) foram mais frequentes no grupo com AOS (32%) do que no grupo sem AOS (7%) com significancância estatística (p=0.01). A chance de ter AOS naqueles com IAM no período noturno foi seis vezes maior do que naqueles com IAM nas restantes 18 horas do dia.328328 Kuniyoshi FH, Garcia-Touchard A, Gami AS, Romero-Corral A, van der Walt C, Pusalavidyasagar S, et al. Day-night variation of acute myocardial infarction in obstructive sleep apnea. J Am Coll Cardiol. 2008;52(5):343-6. doi: 10.1016/j.jacc.2008.04.027.
https://doi.org/10.1016/j.jacc.2008.04.0...
4.2.8.1. Apneia Obstrutiva do Sono Como Potencial Fator de Risco para Doença Arterial Coronariana
Dados de mais de 6.000 pacientes da população do SHHS encontraram associação entre AOS e DAC naqueles pacientes com AOS importante. Apesar de as associações com AOS terem sido mais significativas no contexto da IC e do AVC do que no da DAC, a chance de ter DAC aumentou linearmente em comparação com o grau de AOS na análise multivariada.3535 Shahar E, Whitney CW, Redline S, Lee ET, Newman AB, Nieto FJ, et al. Sleep-disordered breathing and cardiovascular disease: cross-sectional results of the Sleep Heart Health Study. Am J Respir Crit Care Med. 2001;163(1):19-25. doi: 10.1164/ajrccm.163.1.2001008.
https://doi.org/10.1164/ajrccm.163.1.200...
Assim, as consequências cardiovasculares da AOS são heterogêneas e variam de acordo com a gravidade da AOS. Recente análise da mesma coorte do SHHS, com seguimento de 8,7 anos, não encontrou associação de DAC e AOS após ajuste para outros fatores de risco, a não ser na população masculina com menos de 70 anos de idade; ainda, a associação foi maior naqueles com AOS de grau importante. Os resultados foram de que aqueles com AOS importante têm 68% mais chance de desenvolver DAC em comparação àqueles sem AOS. Marin et al.102102 Marin JM, Carrizo SJ, Vicente E, Agusti AG. Long-term cardiovascular outcomes in men with obstructive sleep apnoea-hypopnoea with or without treatment with continuous positive airway pressure: an observational study. Lancet. 2005;365(9464):1046-53. doi: 10.1016/S0140-6736(05)71141-7
https://doi.org/10.1016/S0140-6736(05)71...
mostraram que, no seguimento médio de 10 anos, em estudo observacional e apenas com população masculina, formas graves de AOS foram associadas com maior incidência de IAM do que pacientes sem AOS e do que pacientes com AOS, porém tratados com CPAP. Resultados similares também foram demonstrados no cenário da população feminina, em que o grupo com AOS importante foi associado a maior risco de morte cardiovascular, e o grupo com tratamento da AOS teve risco reduzido de morte, em comparação com grupo sem tratamento de AOS.330330 Campos-Rodriguez F, Martinez-Garcia MA, de la Cruz-Moron I, Almeida-Gonzalez C, Catalan-Serra P, Montserrat JM. Cardiovascular mortality in women with obstructive sleep apnea with or without continuous positive airway pressure treatment: a cohort study. Ann Intern Med. 2012;156(2):115-22. doi: 10.7326/0003-4819-156-2-201201170-00006.
https://doi.org/10.7326/0003-4819-156-2-...
Em pacientes com DAC estabelecida, a AOS parece estar associada com maior risco de AVC naqueles com DAC e AOS. Pacientes com DAC e AOS moderada à importante tinham cerca de 2,4 vezes mais risco de desenvolver AVC do que os com DAC e sem AOS.331331 Valham F, Mooe T, Rabben T, Stenlund H, Wiklund U, Franklin KA. Increased risk of stroke in patients with coronary artery disease and sleep apnea: a 10-year follow-up. Circulation. 2008;118(9):955-60. doi: 10.1161/CIRCULATIONAHA.108.783290.
https://doi.org/10.1161/CIRCULATIONAHA.1...
Mais recentemente, uma coorte de pacientes com DAC de cinco países, incluindo o Brasil, mostrou que a presença de AOS moderada à importante foi associada com mais eventos cardiovasculares do que em pacientes sem AOS no seguimento médio de aproximadamente 2 anos após o implante de stent coronariano.332332 Lee CH, Sethi R, Li R, Ho HH, Hein T, Jim MH, et al. Obstructive sleep apnea and cardiovascular events after percutaneous coronary intervention. Circulation. 2016;133(21):2008-17. doi: 10.1161/CIRCULATIONAHA.115.019392.
https://doi.org/10.1161/CIRCULATIONAHA.1...
Visto que a AOS e a DAC parecem estar independentemente associadas,3535 Shahar E, Whitney CW, Redline S, Lee ET, Newman AB, Nieto FJ, et al. Sleep-disordered breathing and cardiovascular disease: cross-sectional results of the Sleep Heart Health Study. Am J Respir Crit Care Med. 2001;163(1):19-25. doi: 10.1164/ajrccm.163.1.2001008.
https://doi.org/10.1164/ajrccm.163.1.200...
,3636 Gottlieb DJ, Yenokyan G, Newman AB, O'Connor GT, Punjabi NM, Quan SF, et al. Prospective study of obstructive sleep apnea and incident coronary heart disease and heart failure: the sleep heart health study. Circulation. 2010;122(4):352-60. doi: 10.1161/CIRCULATIONAHA.109.901801
https://doi.org/10.1161/CIRCULATIONAHA.1...
,102102 Marin JM, Carrizo SJ, Vicente E, Agusti AG. Long-term cardiovascular outcomes in men with obstructive sleep apnoea-hypopnoea with or without treatment with continuous positive airway pressure: an observational study. Lancet. 2005;365(9464):1046-53. doi: 10.1016/S0140-6736(05)71141-7
https://doi.org/10.1016/S0140-6736(05)71...
,330330 Campos-Rodriguez F, Martinez-Garcia MA, de la Cruz-Moron I, Almeida-Gonzalez C, Catalan-Serra P, Montserrat JM. Cardiovascular mortality in women with obstructive sleep apnea with or without continuous positive airway pressure treatment: a cohort study. Ann Intern Med. 2012;156(2):115-22. doi: 10.7326/0003-4819-156-2-201201170-00006.
https://doi.org/10.7326/0003-4819-156-2-...
e que a AOS parece aumentar o risco de desfechos cardiovasculares na população de DAC,102102 Marin JM, Carrizo SJ, Vicente E, Agusti AG. Long-term cardiovascular outcomes in men with obstructive sleep apnoea-hypopnoea with or without treatment with continuous positive airway pressure: an observational study. Lancet. 2005;365(9464):1046-53. doi: 10.1016/S0140-6736(05)71141-7
https://doi.org/10.1016/S0140-6736(05)71...
,330330 Campos-Rodriguez F, Martinez-Garcia MA, de la Cruz-Moron I, Almeida-Gonzalez C, Catalan-Serra P, Montserrat JM. Cardiovascular mortality in women with obstructive sleep apnea with or without continuous positive airway pressure treatment: a cohort study. Ann Intern Med. 2012;156(2):115-22. doi: 10.7326/0003-4819-156-2-201201170-00006.
https://doi.org/10.7326/0003-4819-156-2-...
331 Valham F, Mooe T, Rabben T, Stenlund H, Wiklund U, Franklin KA. Increased risk of stroke in patients with coronary artery disease and sleep apnea: a 10-year follow-up. Circulation. 2008;118(9):955-60. doi: 10.1161/CIRCULATIONAHA.108.783290.
https://doi.org/10.1161/CIRCULATIONAHA.1...
-332332 Lee CH, Sethi R, Li R, Ho HH, Hein T, Jim MH, et al. Obstructive sleep apnea and cardiovascular events after percutaneous coronary intervention. Circulation. 2016;133(21):2008-17. doi: 10.1161/CIRCULATIONAHA.115.019392.
https://doi.org/10.1161/CIRCULATIONAHA.1...
o tratamento da AOS poderia reduzir eventos futuros. Estudos observacionais mostraram o benefício do tratamento do CPAP na prevenção de desfechos cardiovasculares.102102 Marin JM, Carrizo SJ, Vicente E, Agusti AG. Long-term cardiovascular outcomes in men with obstructive sleep apnoea-hypopnoea with or without treatment with continuous positive airway pressure: an observational study. Lancet. 2005;365(9464):1046-53. doi: 10.1016/S0140-6736(05)71141-7
https://doi.org/10.1016/S0140-6736(05)71...
,330330 Campos-Rodriguez F, Martinez-Garcia MA, de la Cruz-Moron I, Almeida-Gonzalez C, Catalan-Serra P, Montserrat JM. Cardiovascular mortality in women with obstructive sleep apnea with or without continuous positive airway pressure treatment: a cohort study. Ann Intern Med. 2012;156(2):115-22. doi: 10.7326/0003-4819-156-2-201201170-00006.
https://doi.org/10.7326/0003-4819-156-2-...
Também, pacientes com AOS moderada à importante tratados com CPAP apresentaram menor risco de revascularização de repetição, após procedimento percuntâneo de intervenção coronária, comparados com o mesmo grupo de AOS sem tratamento.333333 Wu X, Lv S, Yu X, Yao L, Mokhlesi B, Wei Y. Treatment of OSA reduces the risk of repeat revascularization after percutaneous coronary intervention. Chest. 2015;147(3):708-18. doi: 10.1378/chest.14-1634.
https://doi.org/10.1378/chest.14-1634...
No contexto de evidência de ensaios clínicos randomizados, dois estudos (um deles de centro único;334334 Peker Y, Glantz H, Eulenburg C, Wegscheider K, Herlitz J, Thunström E. Effect of positive airway pressure on cardiovascular outcomes in coronary artery disease patients with nonsleepy obstructive sleep apnea. The RICCADSA Randomized Controlled Trial. Am J Respir Crit Care Med. 2016;194(5):613-20. doi: 10.1164/rccm.201601-0088OC.
https://doi.org/10.1164/rccm.201601-0088...
o outro, multicêntrico335335 McEvoy RD, Antic NA, Heeley E, Luo Y, Ou Q, Zhang X, et al; SAVE Investigators and Coordinators. CPAP for prevention of cardiovascular events in obstructive sleep apnea. N Engl J Med. 2016;375(10):919-31. doi: 10.1056/NEJMoa1606599.
https://doi.org/10.1056/NEJMoa1606599...
) falharam em demonstrar redução de eventos cardiovasculares em pacientes com DAC prévia. Vale ressaltar que ambos os estudos mostraram redução de eventos quando a análise foi limitada aos pacientes que tiveram boa adesão ao tratamento com CPAP.334334 Peker Y, Glantz H, Eulenburg C, Wegscheider K, Herlitz J, Thunström E. Effect of positive airway pressure on cardiovascular outcomes in coronary artery disease patients with nonsleepy obstructive sleep apnea. The RICCADSA Randomized Controlled Trial. Am J Respir Crit Care Med. 2016;194(5):613-20. doi: 10.1164/rccm.201601-0088OC.
https://doi.org/10.1164/rccm.201601-0088...
,335335 McEvoy RD, Antic NA, Heeley E, Luo Y, Ou Q, Zhang X, et al; SAVE Investigators and Coordinators. CPAP for prevention of cardiovascular events in obstructive sleep apnea. N Engl J Med. 2016;375(10):919-31. doi: 10.1056/NEJMoa1606599.
https://doi.org/10.1056/NEJMoa1606599...
Portanto, mais evidências são necessárias para uma indicação formal do CPAP na população de DAC, principalmente com avaliação do efeito em longo prazo no subgrupo aderente ao tratamento. A seção sobre mortalidade cardiovascular discute em mais detalhes estes estudos.
4.2.9. Acidente Vascular Cerebral
O AVC é uma importante causa de morbimortalidade no mundo. A prevalência da AOS em pacientes com AVC é superior a 60%.5151 Parra O, Arboix A, Bechich S, García-Eroles L, Montserrat JM, López JA, et al. Time course of sleep-related breathing disorders in first-ever stroke or transient ischemic attack. Am J Respir Crit Care Med. 2000;161(2 Pt 1):375-80. doi: 10.1164/ajrccm.161.2.9903139.
https://doi.org/10.1164/ajrccm.161.2.990...
,336336 Bassetti C, Aldrich MS. Sleep apnoea in acute cerebrovascular diseases: final report on 128 patients. Sleep. 1999;22(2):217-23. PMID: 10201066. Vale salientar que esta associação está descrita para episódios de AVC isquêmico. Faltam estudos que relacionem de maneira consistente a AOS com AVC hemorrágico.
A AOS está associada a vários fatores de risco para AVC isquêmico, como a HAS, FA, DAC, IC congestiva e DM, sendo difícil estabelecer uma relação de causa-efeito direta entre as duas entidades.337337 Somers VK, White DP, Amin R, Abraham WT, Costa F, Culebras A, et al; American Heart Association Council for High Blood Pressure Research Professional Education Committee, Council on Clinical Cardiology; American Heart Association Stroke Council; American Heart Association Council on Cardiovascular Nursing; American College of Cardiology Foundation. Sleep apnea and cardiovascular disease: an American Heart Association/American College of Cardiology Foundation Scientific Statement from the American Heart Association Council for High Blood Pressure Research Professional Education Committee, Council on Clinical Cardiology, Stroke Council, and Council on Cardiovascular Nursing. In collaboration with the National Heart, Lung, and Blood Institute National Center on Sleep Disorders Research (National Institutes of Health). Circulation. 2008;118(10):1080-111. doi: 10.1161/CIRCULATIONAHA.107.189375. Erratum in: Circulation. 2009;119(12):e380.
https://doi.org/10.1161/CIRCULATIONAHA.1...
,338338 Capampangan DJ, Wellik KE, Parish JM, Aguilar MI, Snyder CR, et al. Is obstructive sleep apnea an independent risk factor for stroke? A critically appraised topic. Neurologist. 2010;16(4):269-73. doi: 10.1097/NRL.0b013e3181e5a66c.
https://doi.org/10.1097/NRL.0b013e3181e5...
Em estudo epidemiológico com 1.022 pacientes, aqueles com AOS apresentaram menor sobrevida que o grupo controle. Pacientes com AOS importante apresentaram três vezes mais chance de desenvolver AVC e morte, independente da idade, etnia, HAS, DM e FA.5555 Yaggi HK, Concato J, Kernan WN, Lichtman JH, Brass LM, Mohsenin V. Obstructive sleep apnea as a risk factor for stroke and death. N Engl J Med. 2005;353(19):2034-41. doi: 10.1056/NEJMoa043104.
https://doi.org/10.1056/NEJMoa043104...
Metanálises sobre o assunto demonstram risco duas vezes maior para o desenvolvimento de AVC em pacientes portadores de AOS importante, além de maior associação com o sexo masculino.339339 Loke YK, Brown JW, Kwok CS, Niruban A, Myint PK. Association of obstructive sleep apnea with risk of serious cardiovascular events: a systematic review and meta-analysis. Circ Cardiovasc Qual Outcomes. 2012;5(5):720-8. doi: 10.1161/CIRCOUTCOMES.111.964783.
https://doi.org/10.1161/CIRCOUTCOMES.111...
,340340 Dong JY, Zhang YH, Qin LQ. Obstructive sleep apnea and cardiovascular risk: meta-analysis of prospective cohort studies. Atherosclerosis. 2013;229(2):489-95. doi: 10.1016/j.atherosclerosis.2013.04.026.
https://doi.org/10.1016/j.atherosclerosi...
Além disto, dados de estudos observacionais sugerem que o uso da terapia com CPAP, tanto na fase aguda do AVC, quanto no seguimento, traz benefícios não só na recuperação funcional e motora, mas também na prevenção de novos eventos e redução da mortalidade.341341 Ryan CM, Bayley M, Green R, Murray BJ, Bradley TD. Influence of continuous positive airway pressure on outcomes of rehabilitation in stroke patients with obstructive sleep apnea. Stroke. 2011;42(4):1062-7. doi: 10.1161/STROKEAHA.110.597468.
https://doi.org/10.1161/STROKEAHA.110.59...
,342342 Martínez-García MA, Campos-Rodríguez F, Soler-Cataluña JJ, Catalán-Serra P, Román-Sánchez P, Montserrat JM. Increased incidence of nonfatal cardiovascular events in stroke patients with sleep apnoea: effect of CPAP treatment. Eur Respir J. 2012;39(4):906-12. doi: 10.1183/09031936.00011311.
https://doi.org/10.1183/09031936.0001131...
O uso precoce do CPAP levou ainda a um melhor desempenho nas escalas de recuperação neurológica.343343 Parra O, Sánchez-Armengol A, Bonnin M, Arboix A, Campos-Rodríguez F, Pérez-Ronchel J, et al. Early treatment of obstructive apnoea and stroke outcome: a randomised controlled trial. Eur Respir J. 2011;37(5):1128-36. doi: 10.1183/09031936.00034410.
https://doi.org/10.1183/09031936.0003441...
No entanto, como discutimos na seção de mortalidade, o SAVE (Sleep Apnea Cardiovascular Endpoints), que envolveu pacientes com DAC ou AVC prévios, falhou em demonstrar um efeito favorável do CPAP na redução da incidência de AVC em pacientes com AOS. No entanto, na análise pré-especificada dos pacientes que tiveram boa adesão ao tratamento com o CPAP (> 4 horas de uso em média), o CPAP promoveu redução de eventos cerebrovasculares.335335 McEvoy RD, Antic NA, Heeley E, Luo Y, Ou Q, Zhang X, et al; SAVE Investigators and Coordinators. CPAP for prevention of cardiovascular events in obstructive sleep apnea. N Engl J Med. 2016;375(10):919-31. doi: 10.1056/NEJMoa1606599.
https://doi.org/10.1056/NEJMoa1606599...
4.2.10. Mortalidade Total e Cardiovascular
4.2.10.1. Mortalidade Total
Em relação à mortalidade total, diversas coortes apontam de forma consistente uma maior mortalidade geral em pacientes com AOS.344344 Young T, Finn L, Peppard PE, Szklo-Coxe M, Austin D, Nieto FJ, et al. Sleep disordered breathing and mortality: eighteen-year follow-up of the Wisconsin sleep cohort. Sleep. 2008;31(8):1071-8. PMID: 18714778.
345 Marshall NS, Wong KK, Liu PY, Cullen SR, Knuiman MW, Grunstein RR. Sleep apnea as an independent risk factor for all-cause mortality: the Busselton Health Study.Sleep. 2008;31(8):1079-85. PMID: 18714779.
346 Punjabi NM, Caffo BS, Goodwin JL, Gottlieb DJ, Newman AB, O'Connor GT, et al. Sleep-disordered breathing and mortality: a prospective cohort study. PLoS Med. 2009;6(8):e1000132. doi: 10.1371/journal.pmed.1000132.
https://doi.org/10.1371/journal.pmed.100...
347 Martínez-García MA, Soler-Cataluña JJ, Ejarque-Martínez L, Soriano Y, Román-Sánchez P, Illa FB, et al. Continuous positive airway pressure treatment reduces mortality in patients with ischemic stroke and obstructive sleep apnea: a 5-year follow-up study. Am J Respir Crit Care Med. 2009;180(1):36-41. doi: 10.1164/rccm.200808-1341OC.
https://doi.org/10.1164/rccm.200808-1341...
348 Martínez-García MA, Campos-Rodríguez F, Catalán-Serra P, Soler-Cataluña JJ, Almeida-Gonzalez C, De la Cruz Morón I, et al. Cardiovascular mortality in obstructive sleep apnea in the elderly: role of long-term continuous positive airway pressure treatment: a prospective observational study. Am J Respir Crit Care Med. 2012;186(9):909-16. doi: 10.1164/rccm.201203-0448OC.
https://doi.org/10.1164/rccm.201203-0448...
349 Ge X, Han F, Huang Y, Zhang Y, Yang T, Bai C, et al. Is obstructive sleep apnea associated with cardiovascular and all-cause mortality? PLoS One. 2013;8(7):e69432. doi: 10.1371/journal.pone.0069432.
https://doi.org/10.1371/journal.pone.006...
-350350 Lavie P, Lavie L, Herer P. All-cause mortality in males with sleep apnoea syndrome: declining mortality rates with age. Eur Respir J. 2005;25(3):514-20. doi: 10.1183/09031936.05.00051504.
https://doi.org/10.1183/09031936.05.0005...
Cabe destacar aqui algumas particularidades quanto a estes achados. Primeiramente, o aumento da mortalidade foi observado especialmente nas formas mais graves deste distúrbio do sono. Young et al.,344344 Young T, Finn L, Peppard PE, Szklo-Coxe M, Austin D, Nieto FJ, et al. Sleep disordered breathing and mortality: eighteen-year follow-up of the Wisconsin sleep cohort. Sleep. 2008;31(8):1071-8. PMID: 18714778. estudando a população de Wisconsin, não encontraram elevação significante na mortalidade total de pacientes com AOS moderada, mas verificaram aumento de 2,7 a 3,8 vezes na mortalidade para pacientes com AOS grave, dependendo das variáveis de confusão incluídas nas análises.344344 Young T, Finn L, Peppard PE, Szklo-Coxe M, Austin D, Nieto FJ, et al. Sleep disordered breathing and mortality: eighteen-year follow-up of the Wisconsin sleep cohort. Sleep. 2008;31(8):1071-8. PMID: 18714778. Já estudo da Austrália encontrou aumento de 4,4 a 6,2 vezes maior para pacientes com AOS moderada à grave.345345 Marshall NS, Wong KK, Liu PY, Cullen SR, Knuiman MW, Grunstein RR. Sleep apnea as an independent risk factor for all-cause mortality: the Busselton Health Study.Sleep. 2008;31(8):1079-85. PMID: 18714779. A coorte do SHHS, envolvendo 6.441 adultos da comunidade, mostrou que o risco de mortalidade total foi de 0,93 (IC95% 0,80-1,08) para AOS leve, 1,17 (IC95% 0,97-1,42) para moderada e 1,46 (IC 95% 1,14-1,86) para grave.346346 Punjabi NM, Caffo BS, Goodwin JL, Gottlieb DJ, Newman AB, O'Connor GT, et al. Sleep-disordered breathing and mortality: a prospective cohort study. PLoS Med. 2009;6(8):e1000132. doi: 10.1371/journal.pmed.1000132.
https://doi.org/10.1371/journal.pmed.100...
Assim, somente a AOS grave atingiu significância estatística neste estudo. Em pacientes com AVC, a AOS moderada à grave foi associada de forma independente com a mortalidade total.347347 Martínez-García MA, Soler-Cataluña JJ, Ejarque-Martínez L, Soriano Y, Román-Sánchez P, Illa FB, et al. Continuous positive airway pressure treatment reduces mortality in patients with ischemic stroke and obstructive sleep apnea: a 5-year follow-up study. Am J Respir Crit Care Med. 2009;180(1):36-41. doi: 10.1164/rccm.200808-1341OC.
https://doi.org/10.1164/rccm.200808-1341...
Em pacientes idosos, o estudo de Martinez-Garcia et al.347347 Martínez-García MA, Soler-Cataluña JJ, Ejarque-Martínez L, Soriano Y, Román-Sánchez P, Illa FB, et al. Continuous positive airway pressure treatment reduces mortality in patients with ischemic stroke and obstructive sleep apnea: a 5-year follow-up study. Am J Respir Crit Care Med. 2009;180(1):36-41. doi: 10.1164/rccm.200808-1341OC.
https://doi.org/10.1164/rccm.200808-1341...
avaliou a mortalidade total como um objetivo secundário deste estudo. Pacientes com AOS importante apresentaram aumento de 1,99 (IC95% 1,42-2,81). Uma metanálise mostrou que a mortalidade total foi de 1,19 (IC95% 1,00 - 1,41) para AOS moderada e 1,90 (IC 95% 1,29-2,81) para AOS grave.349349 Ge X, Han F, Huang Y, Zhang Y, Yang T, Bai C, et al. Is obstructive sleep apnea associated with cardiovascular and all-cause mortality? PLoS One. 2013;8(7):e69432. doi: 10.1371/journal.pone.0069432.
https://doi.org/10.1371/journal.pone.006...
. Em segundo lugar, o aumento da mortalidade total foi verificado principalmente em homens de 40 a 70 anos no SHHS346346 Punjabi NM, Caffo BS, Goodwin JL, Gottlieb DJ, Newman AB, O'Connor GT, et al. Sleep-disordered breathing and mortality: a prospective cohort study. PLoS Med. 2009;6(8):e1000132. doi: 10.1371/journal.pmed.1000132.
https://doi.org/10.1371/journal.pmed.100...
e em homens com < 50 anos em um estudo israelense.350350 Lavie P, Lavie L, Herer P. All-cause mortality in males with sleep apnoea syndrome: declining mortality rates with age. Eur Respir J. 2005;25(3):514-20. doi: 10.1183/09031936.05.00051504.
https://doi.org/10.1183/09031936.05.0005...
Não está claro se o impacto da AOS na mortalidade total é menor ou ausente em mulheres. Não existem estudos randomizados que avaliam o impacto do CPAP na redução da mortalidade total.
4.2.10.2. Mortalidade Cardiovascular
Até o momento, cerca de quatro estudos mostraram um aumento na mortalidade cardiovascular em pacientes com AOS moderada à importante.102102 Marin JM, Carrizo SJ, Vicente E, Agusti AG. Long-term cardiovascular outcomes in men with obstructive sleep apnoea-hypopnoea with or without treatment with continuous positive airway pressure: an observational study. Lancet. 2005;365(9464):1046-53. doi: 10.1016/S0140-6736(05)71141-7
https://doi.org/10.1016/S0140-6736(05)71...
,330330 Campos-Rodriguez F, Martinez-Garcia MA, de la Cruz-Moron I, Almeida-Gonzalez C, Catalan-Serra P, Montserrat JM. Cardiovascular mortality in women with obstructive sleep apnea with or without continuous positive airway pressure treatment: a cohort study. Ann Intern Med. 2012;156(2):115-22. doi: 10.7326/0003-4819-156-2-201201170-00006.
https://doi.org/10.7326/0003-4819-156-2-...
,344344 Young T, Finn L, Peppard PE, Szklo-Coxe M, Austin D, Nieto FJ, et al. Sleep disordered breathing and mortality: eighteen-year follow-up of the Wisconsin sleep cohort. Sleep. 2008;31(8):1071-8. PMID: 18714778.,348348 Martínez-García MA, Campos-Rodríguez F, Catalán-Serra P, Soler-Cataluña JJ, Almeida-Gonzalez C, De la Cruz Morón I, et al. Cardiovascular mortality in obstructive sleep apnea in the elderly: role of long-term continuous positive airway pressure treatment: a prospective observational study. Am J Respir Crit Care Med. 2012;186(9):909-16. doi: 10.1164/rccm.201203-0448OC.
https://doi.org/10.1164/rccm.201203-0448...
De forma interessante, estes dados foram consistentes em homens de meia-idade,102102 Marin JM, Carrizo SJ, Vicente E, Agusti AG. Long-term cardiovascular outcomes in men with obstructive sleep apnoea-hypopnoea with or without treatment with continuous positive airway pressure: an observational study. Lancet. 2005;365(9464):1046-53. doi: 10.1016/S0140-6736(05)71141-7
https://doi.org/10.1016/S0140-6736(05)71...
idosos348348 Martínez-García MA, Campos-Rodríguez F, Catalán-Serra P, Soler-Cataluña JJ, Almeida-Gonzalez C, De la Cruz Morón I, et al. Cardiovascular mortality in obstructive sleep apnea in the elderly: role of long-term continuous positive airway pressure treatment: a prospective observational study. Am J Respir Crit Care Med. 2012;186(9):909-16. doi: 10.1164/rccm.201203-0448OC.
https://doi.org/10.1164/rccm.201203-0448...
e em mulheres.330330 Campos-Rodriguez F, Martinez-Garcia MA, de la Cruz-Moron I, Almeida-Gonzalez C, Catalan-Serra P, Montserrat JM. Cardiovascular mortality in women with obstructive sleep apnea with or without continuous positive airway pressure treatment: a cohort study. Ann Intern Med. 2012;156(2):115-22. doi: 10.7326/0003-4819-156-2-201201170-00006.
https://doi.org/10.7326/0003-4819-156-2-...
Recente metanálise destes estudos encontrou hazard ratio de 2,21 para mortalidade cardiovascular (IC95% 1,61-3,04; p = 0,0001). No entanto, na análise individual, a mortalidade não encontrou aumento da mortalidade cardiovascular em pacientes com AOS moderada (hazard ratio 1,40; IC95% 0,77-2,53), mas foi positiva para a AOS importante (hazard ratio 2,65; IC95% 1,82-3,85).349349 Ge X, Han F, Huang Y, Zhang Y, Yang T, Bai C, et al. Is obstructive sleep apnea associated with cardiovascular and all-cause mortality? PLoS One. 2013;8(7):e69432. doi: 10.1371/journal.pone.0069432.
https://doi.org/10.1371/journal.pone.006...
Em relação ao efeito do tratamento da AOS na mortalidade cardiovascular, pelo menos três estudos não randomizados102102 Marin JM, Carrizo SJ, Vicente E, Agusti AG. Long-term cardiovascular outcomes in men with obstructive sleep apnoea-hypopnoea with or without treatment with continuous positive airway pressure: an observational study. Lancet. 2005;365(9464):1046-53. doi: 10.1016/S0140-6736(05)71141-7
https://doi.org/10.1016/S0140-6736(05)71...
,330330 Campos-Rodriguez F, Martinez-Garcia MA, de la Cruz-Moron I, Almeida-Gonzalez C, Catalan-Serra P, Montserrat JM. Cardiovascular mortality in women with obstructive sleep apnea with or without continuous positive airway pressure treatment: a cohort study. Ann Intern Med. 2012;156(2):115-22. doi: 10.7326/0003-4819-156-2-201201170-00006.
https://doi.org/10.7326/0003-4819-156-2-...
,347347 Martínez-García MA, Soler-Cataluña JJ, Ejarque-Martínez L, Soriano Y, Román-Sánchez P, Illa FB, et al. Continuous positive airway pressure treatment reduces mortality in patients with ischemic stroke and obstructive sleep apnea: a 5-year follow-up study. Am J Respir Crit Care Med. 2009;180(1):36-41. doi: 10.1164/rccm.200808-1341OC.
https://doi.org/10.1164/rccm.200808-1341...
mostraram, de forma consistente, que o tratamento com o CPAP nos casos de AOS importante reduziram a mortalidade cardiovascular para taxas observadas em indivíduos sem AOS. Isto foi verificado tanto em homens102102 Marin JM, Carrizo SJ, Vicente E, Agusti AG. Long-term cardiovascular outcomes in men with obstructive sleep apnoea-hypopnoea with or without treatment with continuous positive airway pressure: an observational study. Lancet. 2005;365(9464):1046-53. doi: 10.1016/S0140-6736(05)71141-7
https://doi.org/10.1016/S0140-6736(05)71...
quanto em mulheres.330330 Campos-Rodriguez F, Martinez-Garcia MA, de la Cruz-Moron I, Almeida-Gonzalez C, Catalan-Serra P, Montserrat JM. Cardiovascular mortality in women with obstructive sleep apnea with or without continuous positive airway pressure treatment: a cohort study. Ann Intern Med. 2012;156(2):115-22. doi: 10.7326/0003-4819-156-2-201201170-00006.
https://doi.org/10.7326/0003-4819-156-2-...
Nenhum destes pacientes tinha história de eventos prévios (contexto, portanto, de prevenção primária do CPAP). Como já destacado, dois recentes estudos randomizados334334 Peker Y, Glantz H, Eulenburg C, Wegscheider K, Herlitz J, Thunström E. Effect of positive airway pressure on cardiovascular outcomes in coronary artery disease patients with nonsleepy obstructive sleep apnea. The RICCADSA Randomized Controlled Trial. Am J Respir Crit Care Med. 2016;194(5):613-20. doi: 10.1164/rccm.201601-0088OC.
https://doi.org/10.1164/rccm.201601-0088...
,335335 McEvoy RD, Antic NA, Heeley E, Luo Y, Ou Q, Zhang X, et al; SAVE Investigators and Coordinators. CPAP for prevention of cardiovascular events in obstructive sleep apnea. N Engl J Med. 2016;375(10):919-31. doi: 10.1056/NEJMoa1606599.
https://doi.org/10.1056/NEJMoa1606599...
não mostraram efeito benéfico do CPAP na redução da mortalidade cardiovascular em pacientes com AOS e alto risco cardiovascular (presença de DAC ou AVC prévios). Estes estudos, em geral, envolveram pacientes com AOS moderada à importante com poucos sintomas de sonolência diurna (foi considerado antiético envolver pacientes com AOS muito sintomáticos). Ambos os estudos tiveram adesão ao CPAP longe do ideal, por conta das dificuldades de adaptação ótima em uma porcentagem dos pacientes. Este foi um dos fatores que pode ter influenciado neste resultado neutro. Um artigo de revisão recente destaca este importante ponto, conforme desrito na figura 5. Não existem estudos que avaliaram o impacto de outros tratamentos para a AOS na mortalidade total e cardiovascular.
Efeito da pressão positiva contínua de vias aéreas (CPAP) na redução do risco cardiovascular (incluindo mortalidade cardiovascular) em pacientes com apneia obstrutiva do sono. Notem que os três estudos não mostraram benefícios do tratamento quando se analisa o grupo como um estudo (intenção de tratar), mas, na análise daqueles pacientes que tiveram uma boa adesão ao CPAP, todos os três estudos sugerem benefícios cardiovasculares.
5. Impacto Cardiovascular da Apneia Obstrutiva do Sono em Crianças
A AOS acomete cerca de 1 a 4% da população pediátrica.351351 Marcus CL, Brooks LJ, Draper KA, Gozal D, Halbower AC, Jones J, et al; American Academy of Pediatrics. Diagnosis and management of childhood obstructive sleep apnea syndrome. Pediatrics. 2012;130(3):e714-55. doi: 10.1542/peds.2012-1672.
https://doi.org/10.1542/peds.2012-1672...
Nas crianças, além dos achados típicos (ronco alto e frequente durante o sono, desconforto respiratório, pausas, ronco ressuscitativo e movimento paradoxal de caixa torácica), podem ocorrer cianose, sudorese profusa, enurese e sono agitado.351351 Marcus CL, Brooks LJ, Draper KA, Gozal D, Halbower AC, Jones J, et al; American Academy of Pediatrics. Diagnosis and management of childhood obstructive sleep apnea syndrome. Pediatrics. 2012;130(3):e714-55. doi: 10.1542/peds.2012-1672.
https://doi.org/10.1542/peds.2012-1672...
A AOS na criança e no adolescente pode acarretar défice de crescimento, alterações do desenvolvimento, problemas de comportamento, diminuição do aproveitamento escolar e complicações cardíacas.351351 Marcus CL, Brooks LJ, Draper KA, Gozal D, Halbower AC, Jones J, et al; American Academy of Pediatrics. Diagnosis and management of childhood obstructive sleep apnea syndrome. Pediatrics. 2012;130(3):e714-55. doi: 10.1542/peds.2012-1672.
https://doi.org/10.1542/peds.2012-1672...
Apesar de parecer similar à síndrome descrita em adultos, a AOS em crianças difere em relação à fisiopatologia, ao quadro clínico, ao critério diagnóstico e ao tratamento. O diagnóstico AOS é feito quando a dessaturação da SpO2 for < 92% e o IAH > 2 eventos por hora.351351 Marcus CL, Brooks LJ, Draper KA, Gozal D, Halbower AC, Jones J, et al; American Academy of Pediatrics. Diagnosis and management of childhood obstructive sleep apnea syndrome. Pediatrics. 2012;130(3):e714-55. doi: 10.1542/peds.2012-1672.
https://doi.org/10.1542/peds.2012-1672...
Os níveis de gravidade da AOS, diferentemente dos adultos, são baseados nos seguintes parâmetros do IAH: AOS leve (IAH, de dois a cinco eventos por hora; AOS moderada, de cinco a dez eventos por hora; e AOS importante (ou grave), > 10 eventos por hora. Diferente dos adultos com AOS, a maioria das crianças e adolescentes com AOS se beneficia da cirurgia de remoção de amígdalas e adenoide.351351 Marcus CL, Brooks LJ, Draper KA, Gozal D, Halbower AC, Jones J, et al; American Academy of Pediatrics. Diagnosis and management of childhood obstructive sleep apnea syndrome. Pediatrics. 2012;130(3):e714-55. doi: 10.1542/peds.2012-1672.
https://doi.org/10.1542/peds.2012-1672...
Estudos recentes em crianças e adolescentes com AOS mostram alterações da função endotelial, inflamação, tromboembolismo, hipertensão arterial pulmonar, HAS, mudanças da geometria e da função ventricular esquerda. Os mecanismos que levam a estas alterações parecem estar relacionados ao efeito crônico e interativo da hipoxemia intermitente, hipercapnia, despertares frequentes e variações na pressão intratorácica.352352 Pack AI, Gislason T. Obstructive sleep apnea and cardiovascular disease: a perspective and future directions. Prog Cardiovasc Dis. 2009;51(5):434-51. doi: 10.1016/j.pcad.2009.01.002.
https://doi.org/10.1016/j.pcad.2009.01.0...
Os efeitos da hipoxemia, hipercapnia e/ou despertares levam ao aumento da atividade simpática, resultando em vasoconstrição arterial periférica e aumento da resistência vascular periférica e/ou pulmonar.353353 Vlahandonis A, Walter LM, Horne RS. Does treatment of SDB in children improve cardiovascular outcome? Sleep Med Rev. 2013 ;17(1):75-85. doi: 10.1016/j.smrv.2012.04.004.
https://doi.org/10.1016/j.smrv.2012.04.0...
A disfunção autonômica em crianças com distúrbio respiratório do sono tem sido demonstrada por vários autores. Walter et al.354354 Walter LM, Nixon GM, Davey MJ, Anderson V, Walker AM, Horne RS. Autonomic dysfunction in children with sleep disordered breathing. Sleep Breath. 2013;17(2):605-13. doi: 10.1007/s11325-012-0727-x.
https://doi.org/10.1007/s11325-012-0727-...
descreveram que crianças escolares (7 a 12 anos) com AOS, comparadas com controles saudáveis, apresentavam redução da sensitividade do barorreflexo, atraso na resposta de frequência cardíaca, mudanças de pressão arterial e aumento da variabilidade da pressão arterial. Crianças com AOS também podem apresentar alteração da variabilidade da frequência cardíaca,355355 Walter LM, Yiallourou SR, Vlahandonis A, Sands SA, Johnson CA, Nixon GM, et al. Impaired blood pressure control in children with obstructive sleep apnea. Sleep Med. 2013;14(9):858-66. doi: 10.1016/j.sleep.2013.01.015.
https://doi.org/10.1016/j.sleep.2013.01....
que melhora após adenotonsilectomia.356356 Muzumdar HV, Sin S, Nikova M, Gates G, Kim D, Arens R. Changes in heart rate variability after adenotonsillectomy in children with obstructive sleep apnea. Chest. 2011;139(5):1050-9. doi: 10.1378/chest.10-1555.
https://doi.org/10.1378/chest.10-1555...
Utilizando tonometria arterial em vigília, O’Brien e Gozal observaram que a resposta vascular a suspiros, frio e compressão arterial esá diminuída em crianças com AOS.357357 O'Brien LM, Gozal D. Autonomic dysfunction in children with sleep-disordered breathing. Sleep. 2005;28(6):747-52. PMID: 16477962. O tratamento com adenotonsilectomia melhora a resposta à compressão vascular, porém tal melhora não é observada nas crianças com AOS com história familiar de doença cardiovascular.358358 Gozal D, Kheirandish-Gozal L, Serpero LD, Sans Capdevila O, Dayyat E. Obstructive sleep apnea and endothelial function in school-aged nonobese children: effect of adenotonsillectomy. Circulation. 2007;116(20):2307-14. doi: 10.1161/CIRCULATIONAHA.107.696823.
https://doi.org/10.1161/CIRCULATIONAHA.1...
A inflamação é um dos mecanismos que contribuem para os desfechos cardiovasculares. Crianças com AOS apresentam elevação de diversos marcadores inflamatórios, incluindo proteína C-reativa (PCR),359359 Kheirandish-Gozal L, Capdevila OS, Tauman R, Gozal D. Plasma C-reactive protein in nonobese children with obstructive sleep apnea before and after adenotonsillectomy. J Clin Sleep Med. 2006;2(3):301-4. PMID: 17410279.,360360 Li AM, Chan MH, Yin J, So HK, Ng SK, Chan IH, et al. C-reactive protein in children with obstructive sleep apnea and the effects of treatment. Pediatr Pulmonol. 2008;43(1):34-40. doi: 10.1002/ppul.20732.
https://doi.org/10.1002/ppul.20732...
Fator de Necrose Tumoral Alfa (TNF-a),361361 Gozal D, Serpero LD, Kheirandish-Gozal L, Capdevila OS, Khalyfa A, Tauman R. Sleep measures and morning plasma TNF-alpha levels in children with sleep-disordered breathing. Sleep. 2010;33(3):319-25. PMID: 20337189. Interleucinas (IL) 6,362362 Gozal D, Serpero LD, Sans Capdevila O, Kheirandish-Gozal L. Systemic inflammation in non-obese children with obstructive sleep apnea. Sleep Med. 2008;9(3):254-9. doi: 10.1016/j.sleep.2007.04.013.
https://doi.org/10.1016/j.sleep.2007.04....
sCD4 ligante358358 Gozal D, Kheirandish-Gozal L, Serpero LD, Sans Capdevila O, Dayyat E. Obstructive sleep apnea and endothelial function in school-aged nonobese children: effect of adenotonsillectomy. Circulation. 2007;116(20):2307-14. doi: 10.1161/CIRCULATIONAHA.107.696823.
https://doi.org/10.1161/CIRCULATIONAHA.1...
e óxido nítrico exalado.363363 Verhulst SL, Aerts L, Jacobs S, Schrauwen N, Haentjens D, Claes R, et al. Sleep-disordered breathing, obesity, and airway inflammation in children and adolescents. Chest 2008;134(6):1169-75. doi: 10.1378/chest.08-0535.
https://doi.org/10.1378/chest.08-0535...
Diversos estudos demonstraram que as citoquinas inflamatórias diminuem após adenotonsilectomia,360360 Li AM, Chan MH, Yin J, So HK, Ng SK, Chan IH, et al. C-reactive protein in children with obstructive sleep apnea and the effects of treatment. Pediatr Pulmonol. 2008;43(1):34-40. doi: 10.1002/ppul.20732.
https://doi.org/10.1002/ppul.20732...
,364364 Chu L, Li Q. The evaluation of adenotonsillectomy on TNF-? and IL-6 levels in obese children with obstructive sleep apnea. Int J Pediatr Otorhinolaryngol. 2013;77(5):690-4. doi: 10.1016/j.ijporl.2013.01.019.
https://doi.org/10.1016/j.ijporl.2013.01...
porém, podem permanecer alteradas se houver AOS residual após adenotonsilectomia.358358 Gozal D, Kheirandish-Gozal L, Serpero LD, Sans Capdevila O, Dayyat E. Obstructive sleep apnea and endothelial function in school-aged nonobese children: effect of adenotonsillectomy. Circulation. 2007;116(20):2307-14. doi: 10.1161/CIRCULATIONAHA.107.696823.
https://doi.org/10.1161/CIRCULATIONAHA.1...
,365365 Gozal D, Capdevila OS, Kheirandish-Gozal L. Metabolic alterations and systemic inflammation in obstructive sleep apnea among nonobese and obese prepubertal children. Am J Respir Crit Care Med. 2008;177(10):1142-9. doi: 10.1164/rccm.200711-1670OC.
https://doi.org/10.1164/rccm.200711-1670...
O tecido adiposo é uma importante fonte de citoquinas inflamatórias, sendo fator de confusão comum na avaliação de desfecho cardiovasculares na AOS. Para esclarecer estas controvérsias, Gozal et al.365365 Gozal D, Capdevila OS, Kheirandish-Gozal L. Metabolic alterations and systemic inflammation in obstructive sleep apnea among nonobese and obese prepubertal children. Am J Respir Crit Care Med. 2008;177(10):1142-9. doi: 10.1164/rccm.200711-1670OC.
https://doi.org/10.1164/rccm.200711-1670...
investigaram o efeito da adenotonsilectomia nas citoquinas inflamatórias, no metabolismo dos lipídicos e no metabolismo da glicose, em crianças obesas e não obesas. O LDL-colesterol e o HDL-colesterol melhoraram tanto nas crianças obesas como nas não obesas. A PCR e a apolipoproteína C estavam elevadas em ambos os grupos pré-tratamento, mas a melhora após adenotonsilectomia foi mais importante nas crianças não obesas. Os níveis de insulina e glicemia estavam elevados somente no grupo obeso, e seus níveis diminuíram após tratamento. Quando as crianças com AOS residual foram comparadas com as que tiveram resolução completa após adenotonsilectomia, observou-se persistência da elevação de PCR, apolipoproteína C, LDL-colesterol e HDL-colesterol nas crianças com AOS residual.365365 Gozal D, Capdevila OS, Kheirandish-Gozal L. Metabolic alterations and systemic inflammation in obstructive sleep apnea among nonobese and obese prepubertal children. Am J Respir Crit Care Med. 2008;177(10):1142-9. doi: 10.1164/rccm.200711-1670OC.
https://doi.org/10.1164/rccm.200711-1670...
Em estudo longitudinal, Waters et al.366366 Waters KA, Sitha S, O'brien LM, Bibby S, de Torres C, Vella S, et al. Follow-up on metabolic markers in children treated for obstructive sleep apnea. Am J Respir Crit Care Med. 2006;174(4):455-60. doi: 10.1164/rccm.200401-110OC.
https://doi.org/10.1164/rccm.200401-110O...
avaliaram o efeito de marcadores inflamatórios no tratamento da AOS. O grupo de crianças que resolveram a AOS após adenotonsilectomia melhorou os níveis de colesterol total, quando comparado ao grupo com AOS residual.366366 Waters KA, Sitha S, O'brien LM, Bibby S, de Torres C, Vella S, et al. Follow-up on metabolic markers in children treated for obstructive sleep apnea. Am J Respir Crit Care Med. 2006;174(4):455-60. doi: 10.1164/rccm.200401-110OC.
https://doi.org/10.1164/rccm.200401-110O...
Não foram observadas diferenças quanto à insulina, à glicemia e ao HDL. Houve tendência do grupo obeso com AOS residual de manter níveis de insulina elevados.
Assim como adultos, crianças com AOS apresentam elevações súbitas da pressão arterial sistêmica e da frequência cardíaca imediatamente após eventos respiratórios obstrutivos durante o sono.367367 O'Driscoll DM, Foster AM, Ng ML, Yang JS, Bashir F, Nixon GM, et al. Acute cardiovascular changes with obstructive events in children with sleep disordered breathing. Sleep. 2009;32(10):1265-71. PMID: 19848356. Diversos estudos têm demonstrando elevação da pressão arterial em crianças com distúrbio respiratório do sono por meio da medida isolada no consultório,368368 Enright PL, Goodwin JL, Sherrill DL, Quan JR, Quan SF; Tucson Children's Assessment of Sleep Apnea study. Blood pressure elevation associated with sleep-related breathing disorder in a community sample of white and Hispanic children: the Tucson Children's Assessment of Sleep Apnea study. Arch Pediatr Adolesc Med. 2003;157(9):901-4. doi: 10.1001/archpedi.157.9.901.
https://doi.org/10.1001/archpedi.157.9.9...
,369369 Kwok KL, Ng DK, Cheung YF. BP and arterial distensibility in children with primary snoring. Chest. 2003;123(5):1561-6. PMID: 12740274. pela MAPA,370370 Li AM, Au CT, Ho C, Fok TF, Wing YK. Blood pressure is elevated in children with primary snoring. J Pediatr. 2009;155(3):362-8. doi: 10.1016/j.jpeds.2009.03.041.
https://doi.org/10.1016/j.jpeds.2009.03....
371 Amin RS, Carroll JL, Jeffries JL, Grone C, Bean JA, Chini B, et al. Twenty-four-hour ambulatory blood pressure in children with sleep-disordered breathing. Am J Respir Crit Care Med. 2004;169(8):950-6. doi: 10.1164/rccm.200309-1305OC.
https://doi.org/10.1164/rccm.200309-1305...
372 Leung LC, Ng DK, Lau MW, Chan CH, Kwok KL, Chow PY, et al. Twenty-four-hour ambulatory BP in snoring children with obstructive sleep apnea syndrome. Chest. 2006;130(4):1009-17. doi: 10.1378/chest.130.4.1009.
https://doi.org/10.1378/chest.130.4.1009...
-373373 Kang KT, Chiu SN, Weng WC, Lee PL, Hsu WC. comparisons of office and 24-hour ambulatory blood pressure monitoring in children with obstructive sleep apnea. J Pediatr. 2017 Mar;182:177-83. doi: 10.1016/j.jpeds.2016.11.032
https://doi.org/10.1016/j.jpeds.2016.11....
e por medida contínua batimento a batimento.374374 Horne RS, Yang JS, Walter LM, Richardson HL, O'Driscoll DM, Foster AM, et al. Elevated blood pressure during sleep and wake in children with sleep-disordered breathing. Pediatrics. 2011;128(1):e85-92. doi: 10.1542/peds.2010-3431.
https://doi.org/10.1542/peds.2010-3431...
As crianças com ronco primário, ou seja, aquelas com história de ronco habitual e polissonografia normal, também podem apresentar aumento da pressão arterial.369369 Kwok KL, Ng DK, Cheung YF. BP and arterial distensibility in children with primary snoring. Chest. 2003;123(5):1561-6. PMID: 12740274.,375375 Kwok KL, Ng DK, Chan CH. Cardiovascular changes in children with snoring and obstructive sleep apnoea. Ann Acad Med Singapore. 2008;37(8):715-21. PMID: 18797568. Uma revisão sistemática relatou que a AOS em crianças está consistentemente associada à HAS e à regulação anormal da pressão arterial.375375 Kwok KL, Ng DK, Chan CH. Cardiovascular changes in children with snoring and obstructive sleep apnoea. Ann Acad Med Singapore. 2008;37(8):715-21. PMID: 18797568. Utilizando medida de pressão arterial batimento a batimento (Finapres), Horne et al.374374 Horne RS, Yang JS, Walter LM, Richardson HL, O'Driscoll DM, Foster AM, et al. Elevated blood pressure during sleep and wake in children with sleep-disordered breathing. Pediatrics. 2011;128(1):e85-92. doi: 10.1542/peds.2010-3431.
https://doi.org/10.1542/peds.2010-3431...
avaliaram crianças de 7 a 13 anos em diversos níveis de gravidade da AOS. Independente da intensidade do distúrbio respiratório do sono (ronco primário, AOS leve ou AOS moderado/grave), a pressão arterial esteve elevada de 10 a 15 mmHg em relação às crianças saudáveis, tanto em vigília relaxada no início da noite, como durante o sono. Os mesmos autores avaliaram indiretamente a pressão arterial de crianças pré-escolares (3 a 5 anos), utilizando o Tempo de Trânsito de Pulso (TTP).376376 Nisbet LC, Yiallourou SR, Nixon GM, Biggs SN, Davey MJ, Trinder J, et al. Characterization of the acute pulse transit time response to obstructive apneas and hypopneas in preschool children with sleep-disordered breathing. Sleep Med. 2013;36(8):1219-26. doi: 10.5665/sleep.2890.
https://doi.org/10.5665/sleep.2890...
O TTP mede o intervalo de tempo entre a contração ventricular (onda R do ECG) e transmissão da onda pletismográfica do oxímetro de pulso. O TTP é um derivativo da velocidade da onda de pulso, que depende da rigidez das paredes das artérias. Ele é inversamente proporcional aos níveis de pressão arterial. No sono REM, o TTP esteve menor nas crianças com AOS moderada/grave em relação às crianças com ronco primário e AOS leve.376376 Nisbet LC, Yiallourou SR, Nixon GM, Biggs SN, Davey MJ, Trinder J, et al. Characterization of the acute pulse transit time response to obstructive apneas and hypopneas in preschool children with sleep-disordered breathing. Sleep Med. 2013;36(8):1219-26. doi: 10.5665/sleep.2890.
https://doi.org/10.5665/sleep.2890...
Assim, fica sugerido que o aumento da pressão arterial durante o sono REM, momento em que crianças têm mais apneias obstrutivas, seria o estágio inicial de desenvolvimento da HAS propriamente dita. Como as elevações da pressão arterial na infância predizem HAS em adultos,377377 Bao W, Threefoot SA, Srinivasan SR, Berenson GS. Essential hypertension predicted by tracking of elevated blood pressure from childhood to adulthood: the Bogalusa Heart Study. Am J Hypertens. 1995;8(7):657-65. doi: 10.1016/0895-7061(95)00116-7.
https://doi.org/10.1016/0895-7061(95)001...
,378378 Sun SS, Grave GD, Siervogel RM, Pickoff AA, Arslanian SS, Daniels SR. Systolic blood pressure in childhood predicts hypertension and metabolic syndrome later in life. Pediatrics. 2007;119(2):237-46. doi: 10.1542/peds.2006-2543.
https://doi.org/10.1542/peds.2006-2543...
estudos longitudinais necessitam ser feitos para comprovar esta hipótese. Até o momento, existe um estudo longitudinal que investigou a incidência e prevalência de HAS em um período de 5 anos. Em uma coorte de 344 crianças e adolescentes, Archbold et al.379379 Archbold KH, Vasquez MM, Goodwin JL, Quan SF. Effects of sleep patterns and obesity on increases in blood pressure in a 5-year period: report from the Tucson Children's Assessment of Sleep Apnea Study. J Pediatr. 2012;161(1):26-30. doi: 10.1016/j.jpeds.2011.12.034.
https://doi.org/10.1016/j.jpeds.2011.12....
encontraram um aumento da incidência de HAS de 3,6% para 4,2%, concomitante ao aumento da prevalência de obesidade de 15% para 19%. Os aumentos da obesidade e a redução do TTS estiveram significantemente associados à HAS nos adolescentes, enquanto que houve uma tendência de estar associado ao distúrbio respiratório do sono.
Existem poucas evidências sobre o efeito da adenotonsilectomia na pressão arterial de crianças com AOS. Ng et al.380380 Ng DK, Wong JC, Chan CH, Leung LC, Leung SY. Ambulatory blood pressure before and after adenotonsillectomy in children with obstructive sleep apnea. Sleep Med. 2010;11(7):721-5. doi: 10.1016/j.sleep.2009.10.007.
https://doi.org/10.1016/j.sleep.2009.10....
realizaram MAPA pré e pós-adenotonsilectomia em 44 crianças. As medidas da pressão arterial sistólica e diastólica não foram diferentes antes e após o tratamento, provavelmente porque a melhora da AOS não foi completa (IAH reduziu de 14 a 3/hora). No entanto, as medidas de carga diastólica global reduziram significantemente de 15+18% para 10+10%. Ainda, seis das oito crianças sem descenso noturno da pressão arterial, melhoram após o tratamento.380380 Ng DK, Wong JC, Chan CH, Leung LC, Leung SY. Ambulatory blood pressure before and after adenotonsillectomy in children with obstructive sleep apnea. Sleep Med. 2010;11(7):721-5. doi: 10.1016/j.sleep.2009.10.007.
https://doi.org/10.1016/j.sleep.2009.10....
Apostolidou et al. também não encontraram melhora da pressão arterial, medida no consultório, após adenotonsilectomia em crianças escolares e pré-escolares.381381 Apostolidou MT, Alexopoulos EI, Damani E, Liakos N, Chaidas K, Boultadakis E, et al. Absence of blood pressure, metabolic, and inflammatory marker changes after adenotonsillectomy for sleep apnea in Greek children. Pediatr Pulmonol. 2008;43(6):550-60. doi: 10.1002/ppul.20808.
https://doi.org/10.1002/ppul.20808...
No entanto, as crianças que tiveram resolução completa da AOS (IAH < 1/hora) tiveram redução do índice de pressão arterial diastólica. Outro estudo avaliou a pressão arterial no consultório 6 meses e 1 anos após adenotonsilectomia. Houve redução significativa da pressão arterial diastólica 6 meses e 1 ano após o tratamento.382382 Amin R, Anthony L, Somers V, Fenchel M, McConnell K, Jefferies J, et al. Growth velocity predicts recurrence of sleep-disordered breathing 1 year after adenotonsillectomy. Am J Respir Crit Care Med 2008;177(6):654-9. doi: 10.1164/rccm.200710-1610OC.
https://doi.org/10.1164/rccm.200710-1610...
As crianças que melhoram da AOS após 6 meses, mas tiveram recorrência da AOS após 1 ano, apresentaram elevação da pressão arterial sistólica quando comparadas a crianças que permaneceram sem AOS.382382 Amin R, Anthony L, Somers V, Fenchel M, McConnell K, Jefferies J, et al. Growth velocity predicts recurrence of sleep-disordered breathing 1 year after adenotonsillectomy. Am J Respir Crit Care Med 2008;177(6):654-9. doi: 10.1164/rccm.200710-1610OC.
https://doi.org/10.1164/rccm.200710-1610...
Os efeitos cardiovasculares dos movimentos periódicos de membros e da SPI têm sido sugeridos em adultos.383383 Espinak-Sierra J, Vela-Bueno A, Luque-Otero M. Periodic leg movements in sleep in essential hypertension. Psychiatry Clin Neurosci. 1997;51(3):103-7. PMID: 9225372.,384384 Winkelman JW, Shahar E, Sharief I, Gottlieb DJ. Association of restless legs syndrome and cardiovascular disease in the Sleep Heart Health Study. Neurology. 2008;70(1):35-42. doi: 10.1212/01.wnl.0000287072.93277.c9.
https://doi.org/10.1212/01.wnl.000028707...
Recentemente, Hartzell et al.385385 Hartzell K, Avis K, Lozano D, Feig D. Obstructive sleep apnea and periodic limb movement disorder in a population of children with hypertension and/or nocturnal nondipping blood pressures. J Am Soc Hypertens. 2016;10(2):101-7. doi: 10.1016/j.jash.2015.11.010.
https://doi.org/10.1016/j.jash.2015.11.0...
avaliaram 54 crianças e adolescentes de 5 a 18 anos encaminhados a polissonografia que realizaram MAPA no último ano. Os autores encontraram maior frequência de AOS (64% vs. 20%) e movimentos periódicos de membros (20% vs. 10%) quando comparados a prevalência daquele laboratório de sono.385385 Hartzell K, Avis K, Lozano D, Feig D. Obstructive sleep apnea and periodic limb movement disorder in a population of children with hypertension and/or nocturnal nondipping blood pressures. J Am Soc Hypertens. 2016;10(2):101-7. doi: 10.1016/j.jash.2015.11.010.
https://doi.org/10.1016/j.jash.2015.11.0...
Eles também reforçam a necessidade de avaliar distúrbios de sono em crianças com HAS, mas ressaltam as limitações do estudo (retrospectivo, amostra pequena e alta prevalência de obesidade).
Estudos com ecocardiografia, que avaliam a função e a estrutura cardíaca, mostraram que crianças com AOS apresentam hipertrofia386386 Amin RS, Kimball TR, Bean JA, Jeffries JL, Willging JP, Cotton RT, et al. Left ventricular hypertrophy and abnormal ventricular geometry in children and adolescents with obstructive sleep apnea. Am J Respir Crit Care Med. 2002;165(10):1395-9. doi: 10.1164/rccm.2105118.
https://doi.org/10.1164/rccm.2105118...
e disfunção ventricular esquerda.387387 Amin RS, Kimball TR, Kalra M, Jeffries JL, Carroll JL, Bean JA, et al. Left ventricular function in children with sleep-disordered breathing. Am J Cardiol. 2005;95(6):801-4. doi: 10.1016/j.amjcard.2004.11.044.
https://doi.org/10.1016/j.amjcard.2004.1...
Gorur et al.,388388 Görür K, Döven O, Unal M, Akkus N, Ozcan C. Preoperative and postoperative cardiac and clinical findings of patients with adenotonsillar hypertrophy. Int J Pediatr Otorhinolaryngol. 2001;59(1):41-6. PMID: 11376817. em estudo sem polissonografia, encontraram que crianças com hipertrofia adenotonsilar, quando comparadas ao grupo controle, apresentavam disfunção de VE e hipertrofia de VD e VE. Já Ugur et al.389389 Ugur MB, Dogan SM, Sogut A, Uzun L, Cinar F, Altin R, Aydin M. Effect of adenoidectomy and/or tonsillectomy on cardiac functions in children with obstructive sleep apnea. ORL J Otorhinolaryngol Relat Spec. 2008;70(3):202-8. doi: 10.1159/000124295.
https://doi.org/10.1159/000124295...
encontraram melhora das funções de VE e VD após adenotonsilectomia em crianças com hipertrofia adenotonsilar. Os autores realizaram ecocardiografia modo-M e Doppler tecidual em 29 crianças com AOS e 26 crianças com ronco primário. A pressão arterial pulmonar estimada diminuiu significativamente após adenotonsilectomia. As medidas de Doppler tecidual revelaram, após tratamento, melhora da função diastólica do VE e do VD.389389 Ugur MB, Dogan SM, Sogut A, Uzun L, Cinar F, Altin R, Aydin M. Effect of adenoidectomy and/or tonsillectomy on cardiac functions in children with obstructive sleep apnea. ORL J Otorhinolaryngol Relat Spec. 2008;70(3):202-8. doi: 10.1159/000124295.
https://doi.org/10.1159/000124295...
A hipóxia estimula diversos sensores na vasculatura pulmonar, levando à vasoconstrição das arteríolas pulmonares e ao consequente aumento da resistência vascular pulmonar. Apesar da hipertensão arterial pulmonar ocorrer com maior frequência em crianças com doença pulmonar crônica, ela também já foi descrita em crianças com AOS isolada.375375 Kwok KL, Ng DK, Chan CH. Cardiovascular changes in children with snoring and obstructive sleep apnoea. Ann Acad Med Singapore. 2008;37(8):715-21. PMID: 18797568. Se a hipertensão arterial pulmonar estiver associada à disfunção ventricular direita, temos o cor pulmonale. Vários estudos demonstram que a adenotonsilectomia reverte a função ventricular direita e a pressão arterial pulmonar a níveis normais.390390 Miman MC, Kirazli T, Ozyurek R. Doppler echocardiography in adenotonsillar hypertrophy. Int J Pediatr Otorhinolaryngol. 2000;54(1):21-6. PMID: 10960692.
391 Ramakrishna S, Ingle VS, Patel S, Bhat P, Dada JE, Shah FA, et al. Reversible cardio-pulmonary changes due to adeno-tonsilar hypertrophy. Int J Pediatr Otorhinolaryngol. 2000;55(3):203-6. PMID: 11035178.-392392 Sofer S, Weinhouse E, Tal A, Wanderman KL, Margulis G, Leiberman A, et al. Cor pulmonale due to adenoidal or tonsillar hypertrophy or both in children. Noninvasive diagnosis and follow-up. Chest. 1988;93(1):119-22. PMID: 3335141. Miman et al.390390 Miman MC, Kirazli T, Ozyurek R. Doppler echocardiography in adenotonsillar hypertrophy. Int J Pediatr Otorhinolaryngol. 2000;54(1):21-6. PMID: 10960692. avaliaram 17 crianças com hipertrofia adenotonsilar e sintomas de obstrução de vias aéreas superiores. A avaliação com Eco Doppler 2D colorido antes e 3 meses após adenotonsilectomia mostrou queda da pressão arterial pulmonar estimada de 29,1 ± 4,4 para 12,1 ± 3mmHg.
Na anemia falciforme, condição que pode estar associada com o AVC em crianças e adolescentes,393393 Switzer AJ, Hess DC, Nichols FT, Adams RJ. Pathophysiology and treatment of stroke in sickle-cell disease: present and future. Lancet Neurol. 2006;5(6):501-12. doi: 10.1016/S1474-4422(06)70469-0.
https://doi.org/10.1016/S1474-4422(06)70...
a AOS pode ter papel desfavorável. Os portadores de anemia falciforme apresentam aumento do fluxo sanguíneo cerebral, medido por Doppler transcraniano.394394 Kral MC, Brown RT, Nietert PJ, Abboud MR, Jackson SM, Hynd GW. Transcranial Doppler ultrasonography and neurocognitive functioning in children with sickle cell disease. Pediatrics. 2003;112(2):324-31. PMID: 12897282. Este aumento também foi documentado em crianças com distúrbio respiratório do sono.395395 Hill CM, Hogan AM, Onugha N, Harrison D, Cooper S, McGrigor VJ, et al. Increased cerebral blood flow velocity in children with mild sleep-disordered breathing: a possible association with abnormal neuropsychological function. Pediatrics. 2006;118(4):e1100-8. doi: 10.1542/peds.2006-0092.
https://doi.org/10.1542/peds.2006-0092...
Em estudo caso-controle, crianças com AOS leve apresentaram alterações de comportamento e das funções executivas, associadas a aumento do fluxo sanguíneo nas artérias cerebrais médias.395395 Hill CM, Hogan AM, Onugha N, Harrison D, Cooper S, McGrigor VJ, et al. Increased cerebral blood flow velocity in children with mild sleep-disordered breathing: a possible association with abnormal neuropsychological function. Pediatrics. 2006;118(4):e1100-8. doi: 10.1542/peds.2006-0092.
https://doi.org/10.1542/peds.2006-0092...
É de se imaginar que a combinação de anemia falciforme e AOS aumente a chance de AVC em crianças e adolescentes. Kirhman et al.396396 Kirkham FJ, Hewes DK, Prengler M, Wade A, Lane R, Evans JP. Nocturnal hypoxaemia and central-nervous-system events in sickle-cell disease. Lancet 2001;357(9269):1656-9. PMID: 11425370. observaram que a média da saturação percutânea da SpO2 noturna, os níveis elevados de hematócrito e a velocidade sanguínea nas artérias cerebrais médias e carótidas internas estiveram associadas ao AVC. O índice de saturação, um indicativo de AOS, não foi preditor de AVC. A SpO2 não é um indicador fidedigno de hipoxemia na anemia falciforme, pois é um resultado de combinação da mistura de carboxiemoglobina, metaemoglobina e SpO2.397397 Moreira GA. Respiratory repercussions of sickle cell anemia. J Bras Pneumol. 2007;33(3):18-20. doi: http://dx.doi.org/10.1590/S1806-37132007000300002.
http://dx.doi.org/10.1590/S1806-37132007...
Nestas circunstâncias, a SpO2 revela mais a gravidade da anemia falciforme, e não da doença respiratória. Por isto, esses dados não permitem concluir sobre o risco de AVC em crianças com AOS. Até o momento não há estudos que avaliem o efeito da adenotonsilectomia na função cerebral e/o risco de AVC em portadores de anemia falciforme e AOS.
6. Apneia Central do Sono
Pacientes com IC com baixa fração de ejeção frequentemente apresentam apneia central associada a RCS. A apneia central assocada à RCS é uma condição caracterizada por um padrão oscilatório de ventilação, em que as apneas centrais e as hipopneias alternam com períodos de hiperventilação.398398 Bradley TD, Floras JS. Sleep apnea and heart failure: Part II: central sleep apnea. Circulation. 2003;107(13):1822-6. doi: 10.1161/01.CIR.0000061758.05044.64.
https://doi.org/10.1161/01.CIR.000006175...
O principal mecanismo que leva à instabilidade do centro respiratório e à RCS em pacientes com IC é a hiperventilação que, por sua vez, causa baixos níveis de pressão parcial de dióxido de carbono (PaCO2), tanto durante a vigília quanto durante o sono.398398 Bradley TD, Floras JS. Sleep apnea and heart failure: Part II: central sleep apnea. Circulation. 2003;107(13):1822-6. doi: 10.1161/01.CIR.0000061758.05044.64.
https://doi.org/10.1161/01.CIR.000006175...
,399399 Naughton MT, Kee K. Sleep apnoea in heart failure: To treat or not to treat? Respirology. 2017;22(2):217-229. doi: 10.1111/resp.12964.
https://doi.org/10.1111/resp.12964...
Acredita-se que a congestão pulmonar característica da IC cause hiperventilação por estímulo de receptores J no interstício pulmonar. Durante a vigília, vários mecanismos, como, por exemplo, o estímulo do sistema reticular ascendente, tendem a manter a respiração estável.398398 Bradley TD, Floras JS. Sleep apnea and heart failure: Part II: central sleep apnea. Circulation. 2003;107(13):1822-6. doi: 10.1161/01.CIR.0000061758.05044.64.
https://doi.org/10.1161/01.CIR.000006175...
Em contraste, durante o sono, o centro respiratório é mais propenso à instabilidade, pois a ventilação passa a depender dos quimiorreceptores que detectam os níveis arteriais de dióxido de carbono e oxigênio. Na transição vigília-sono, níveis baixos de PaCO2 característico dos pacientes com IC podem desencader apneias centrais.
A apneia central do sono é uma consequência da IC. Ela ocorre na ausência de obstrução das vias aéreas superiores, comumente refletindo a quimiossensibilidade respiratória exagerada associada à disfunção cardíaca e à congestão pulmonar.398398 Bradley TD, Floras JS. Sleep apnea and heart failure: Part II: central sleep apnea. Circulation. 2003;107(13):1822-6. doi: 10.1161/01.CIR.0000061758.05044.64.
https://doi.org/10.1161/01.CIR.000006175...
A prevalência da apneia central varia entre 30 a 50% dos pacientes com IC.398398 Bradley TD, Floras JS. Sleep apnea and heart failure: Part II: central sleep apnea. Circulation. 2003;107(13):1822-6. doi: 10.1161/01.CIR.0000061758.05044.64.
https://doi.org/10.1161/01.CIR.000006175...
Alguns estudos sugerem que a disfunção diastólica também possa estar associada à RCS, mas o padrão é muito mais comum em pacientes com disfunção sistólica.398398 Bradley TD, Floras JS. Sleep apnea and heart failure: Part II: central sleep apnea. Circulation. 2003;107(13):1822-6. doi: 10.1161/01.CIR.0000061758.05044.64.
https://doi.org/10.1161/01.CIR.000006175...
Independente da causa, uma vez estabelecida, a RCS está associada a quedas recorrentes da saturação de oxigênio e fragmentação do sono, com oscilações recorrentes na frequência cardíaca, pressão arterial, aumento da atividade simpática e risco aumentado de taquicardia ventricular.399399 Naughton MT, Kee K. Sleep apnoea in heart failure: To treat or not to treat? Respirology. 2017;22(2):217-229. doi: 10.1111/resp.12964.
https://doi.org/10.1111/resp.12964...
A RCS é um marcador independente de mau prognóstico e provavelmente participa de um ciclo vicioso, que contribui para a deterioração cardíaca.400400 Lanfranchi PA, Braghiroli A, Bosimini E, Mazzuero G, Colombo R, Donner CF, et al. Prognostic value of nocturnal Cheyne-Stokes respiration in chronic heart failure. Circulation. 1999;99(11):1435-40. PMID: 10086966. Portanto, o tratamento da RCS pode melhorar o prognóstico dos pacientes com IC.
6.1. Tratamento da Apneia Central
Inúmeros tratamentos foram propostos para a apneia central associada à RCS. Em primeiro lugar, a otimização do tratamento da IC pode trazer melhora significante deste distúrbio respiratório.398398 Bradley TD, Floras JS. Sleep apnea and heart failure: Part II: central sleep apnea. Circulation. 2003;107(13):1822-6. doi: 10.1161/01.CIR.0000061758.05044.64.
https://doi.org/10.1161/01.CIR.000006175...
,399399 Naughton MT, Kee K. Sleep apnoea in heart failure: To treat or not to treat? Respirology. 2017;22(2):217-229. doi: 10.1111/resp.12964.
https://doi.org/10.1111/resp.12964...
Estimulantes respiratórios, como a acetazolamida e teofilina (que estimulariam o centro respiratório independente dos níveis de PaCO2) podem diminuir a RCS.401401 Javaheri S, Parker TJ, Wexler L, Liming JD, Lindower P, Roselle GA. Effect of theophylline on sleep-disordered breathing in heart failure. N Engl J Med. 1996;335(8):562-7. doi: 10.1056/NEJM199608223350805.
https://doi.org/10.1056/NEJM199608223350...
402 Javaheri S. Acetazolamide improves central sleep apnea in heart failure: a double-blind, prospective study. Am J Respir Crit Care Med. 2006;173(2):234-7. doi: 10.1164/rccm.200507-1035OC.
https://doi.org/10.1164/rccm.200507-1035...
-403403 Fontana M, Emdin M, Giannoni A, Iudice G, Baruah R, Passino C. Effect of acetazolamide on chemosensitivity, Cheyne-Stokes respiration, and response to effort in patients with heart failure. Am J Cardiol. 2011;107(11):1675-80. doi: 10.1016/j.amjcard.2011.01.060.
https://doi.org/10.1016/j.amjcard.2011.0...
No entanto estudos clínicos sugerem que estes estimulantes podem aumentar a chance de arritimia cardíaca, e nenhum benefício clínico prático foi comprovado. Alguns estudos recentes conseguiram a estabilização parcial da ventilação em pacientes com RCS por meio de do marca-passo no nervo frênico.404404 Costanzo MR, Ponikowski P, Javaheri S, Augostini R, Goldberg L, Holcomb R, et al; remedé System Pivotal Trial Study Group. Transvenousneurostimulation for central sleep apnoea: a randomised controlled trial. Lancet. 2016;388(10048):974-82. doi: 10.1016/S0140-6736(16)30961-8.
https://doi.org/10.1016/S0140-6736(16)30...
Apesar de potencialmente promissor, o método é caro e invasivo, a melhora da RCS é, em geral, parcial e esta forma de tratamento permanece no campo experimental.404404 Costanzo MR, Ponikowski P, Javaheri S, Augostini R, Goldberg L, Holcomb R, et al; remedé System Pivotal Trial Study Group. Transvenousneurostimulation for central sleep apnoea: a randomised controlled trial. Lancet. 2016;388(10048):974-82. doi: 10.1016/S0140-6736(16)30961-8.
https://doi.org/10.1016/S0140-6736(16)30...
Outro tramento proposto é a adminstração noturna de oxigênio. Além de atenuar as quedas cíclicas da hipóxia causada pelas apneias recorrentes, o oxigênio pode estabilizar parcialmente a ventilação e diminuir a RCS, pois inibe parcialmente a hiperventilação.399399 Naughton MT, Kee K. Sleep apnoea in heart failure: To treat or not to treat? Respirology. 2017;22(2):217-229. doi: 10.1111/resp.12964.
https://doi.org/10.1111/resp.12964...
No entanto, o real benefício da suplementação de oxigênio em pacientes com IC não está claro. Em pacientes com IC e bloqueio de ramo esquerdo, a melhora da função cardíaca após a ressincronização cardíaca está associada à drástica diminuição da RCS.405405 Sinha AM, Skobel EC, Breithardt OA, Norra C, Markus KU, Breuer C, et al. Cardiac resynchronization therapy improves central sleep apnea and Cheyne-Stokes respiration in patients with chronic heart failure. J Am Coll Cardiol. 2004;44(1):68-71. doi: 10.1016/j.jacc.2004.03.040.
https://doi.org/10.1016/j.jacc.2004.03.0...
Em relação à pressão positiva, o CPAP atua não somente na via aérea superior, mas a pressão positiva transmitida nos pulmões pode ser benéfica para pacientes com IC. Por exemplo, o CPAP é uma forma de tratamento do edema agudo dos pulmões. Existem vários mecanismos potenciais que podem explicar o efeito benéfico do CPAP na RCS, incluindo a diminuição da pré-carga e da pós-carga do VE, levando à melhora do desempenho cardíaco e da diminuição da congestão pulmonar, à insuflação pulmonar com aumento da capacidade resdiual funcional, à estabilização dos gases sanguineos e à elevação da PaCO2, por conta do espaço morto introduzido pela máscara.399399 Naughton MT, Kee K. Sleep apnoea in heart failure: To treat or not to treat? Respirology. 2017;22(2):217-229. doi: 10.1111/resp.12964.
https://doi.org/10.1111/resp.12964...
Vários estudos pequenos nos últimos 20 anos demonstraram que o CPAP pode reduzir a RCS, hipóxia intermitente noturna, reduzir a hiperativação simpática e melhorar o desempenho cardíaco em pacientes com IC.399399 Naughton MT, Kee K. Sleep apnoea in heart failure: To treat or not to treat? Respirology. 2017;22(2):217-229. doi: 10.1111/resp.12964.
https://doi.org/10.1111/resp.12964...
No entanto, um estudo multicêntrico randomizado não foi capaz de demonstrar impacto do CPAP na mortalidade em pacientes com IC (CANPAP).406406 Bradley TD, Logan AG, Kimoff RJ, Sériès F, Morrison D, Ferguson K, et al; CANPAP Investigators. Continuous positive airway pressure for central sleep apnea and heart failure. N Engl J Med. 2005;353(19):2025-33. doi: 10.1056/NEJMoa051001
https://doi.org/10.1056/NEJMoa051001...
Uma análise post hoc demonstrou que o CPAP foi capaz de reduzir a mortalidade somente nos pacientes em que ela foi capaz de tratar eficazmente a RCS.407407 Arzt M, Floras JS, Logan AG, Kimoff RJ, Series F, Morrison D, et al; CANPAP Investigators. Suppression of central sleep apnea by continuous positive airway pressure and transplant-free survival in heart failure: a post hoc analysis of the Canadian Continuous Positive Airway Pressure for Patients with Central Sleep Apnea and Heart Failure Trial (CANPAP). Circulation. 2007;115(25):3173-80. doi: 10.1161/CIRCULATIONAHA.106.683482.
https://doi.org/10.1161/CIRCULATIONAHA.1...
Como o CPAP atua na RCS somente de forma indireta, esta observação levou a esperança de que novas formas ventilatórias não invasivas capazes de eliminar a RCS seriam benéficas para os pacientes com IC e RCS. Neste contexto, o servo ventilador é uma nova forma de ventilação não invasiva com dois níveis de pressão (binível), em que a Pressão Expiratória (EPAP) é utilizada em níveis relativamente baixos (somente para eliminar o componente obstrutivo), e a Pressão Inspiratória (IPAP) é variável e aplicada de forma “inteligente”, com o intuito de estabilizar o centro respiratório.408408 Teschler H, Döhring J, Wang YM, Berthon-Jones M. Adaptive pressure support servo-ventilation: a novel treatment for Cheyne-Stokes respiration in heart failure. Am J Respir Crit Care Med. 2001;164(4):614-9. doi: 10.1164/ajrccm.164.4.9908114.
https://doi.org/10.1164/ajrccm.164.4.990...
,409409 Javaheri S, Brown LK, Randerath WJ. Positive airway pressure therapy with adaptive servoventilation: part 1: operational algorithms. Chest. 2014;146(2):514-23. doi: 10.1378/chest.13-1776.
https://doi.org/10.1378/chest.13-1776...
O aparelho detecta o padrão respiratório do paciente e passa a administrar uma pressão inspiratória que muda respiração a respiração. Quando o paciente faz pouco esforço inspiratório, que levaria a um volume corrente pequeno, o aparelho administra uma pressão inspiratória maior, garantindo a manutenção do volume corrente. Em contraste, quando o paciente tem um volume corrente grande, o aparelho simplesmente não aciona a pressão inspiratória, mantendo somente a pressão expiratória.408408 Teschler H, Döhring J, Wang YM, Berthon-Jones M. Adaptive pressure support servo-ventilation: a novel treatment for Cheyne-Stokes respiration in heart failure. Am J Respir Crit Care Med. 2001;164(4):614-9. doi: 10.1164/ajrccm.164.4.9908114.
https://doi.org/10.1164/ajrccm.164.4.990...
,409409 Javaheri S, Brown LK, Randerath WJ. Positive airway pressure therapy with adaptive servoventilation: part 1: operational algorithms. Chest. 2014;146(2):514-23. doi: 10.1378/chest.13-1776.
https://doi.org/10.1378/chest.13-1776...
O servo ventilador é capaz de abolir a RCS de forma mais eficaz do que o CPAP.410410 Arzt M, Wensel R, Montalvan S, Schichtl T, Schroll S, Budweiser S, et al. Effects of dynamic bilevel positive airway pressure support on central sleep apnea in men with heart failure. Chest. 2008;134(1):61-6. doi: 10.1378/chest.07-1620.
https://doi.org/10.1378/chest.07-1620...
Da mesma forma que o CPAP, estudos iniciais com o servo ventilador demonstram melhora não só do padrão respiratório durante o sono, mas também diminuição da atividade simpática e melhora da função cardíaca.411411 D'Elia E, Vanoli E, La Rovere MT, Fanfulla F, Maggioni A, Casali V, et al. Adaptive servo ventilation reduces central sleep apnea in chronic heart failure patients: beneficial effects on autonomic modulation of heart rate. J Cardiovasc Med (Hagerstown). 2013;14(4):296-300. doi: 10.2459/JCM.0b013e32835364b2.
https://doi.org/10.2459/JCM.0b013e328353...
412 Oldenburg O, Schmidt A, Lamp B, Bitter T, Muntean BG, Langer C, et al. Adaptive servoventilation improves cardiac function in patients with chronic heart failure and Cheyne-Stokes respiration. Eur J Heart Fail. 2008;10(6):581-6. doi: 10.1016/j.ejheart.2008.04.007.
https://doi.org/10.1016/j.ejheart.2008.0...
-413413 Hastings PC, Vazir A, Meadows GE, Dayer M, Poole-Wilson PA, McIntyre HF, et al. Adaptive servo-ventilation in heart failure patients with sleep apnea: a real world study. Int J Cardiol. 2010;139(1):17-24. doi: 10.1016/j.ijcard.2008.08.022.
https://doi.org/10.1016/j.ijcard.2008.08...
No entanto, o SERVE-HF (Adaptive Servo-Ventilation for Central Sleep Apnea in Systolic Heart Failure), grande estudo multicêntrico usando o servo ventilador para pacientes com IC e apneia central, não demonstrou impacto do servo ventilador no desfecho primário (causa combinada de mortalidade).414414 Cowie MR, Woehrle H, Wegscheider K, Angermann C, d'Ortho MP, Erdmann E, et al. Adaptive servo-ventilation for central sleep apnea in systolic heart failure. N Engl J Med. 2015;373(12):1095-105. doi: 10.1056/NEJMoa1506459.
https://doi.org/10.1056/NEJMoa1506459...
No entanto, o estudo mostrou dados preocupantes, pois os pacientes randomizados para o servo ventilador apresentaram aumento de mortalidade cardiovascular (um dos desfechos secundários).414414 Cowie MR, Woehrle H, Wegscheider K, Angermann C, d'Ortho MP, Erdmann E, et al. Adaptive servo-ventilation for central sleep apnea in systolic heart failure. N Engl J Med. 2015;373(12):1095-105. doi: 10.1056/NEJMoa1506459.
https://doi.org/10.1056/NEJMoa1506459...
O estudo teve várias limitações, pois a adesão ao servo ventilador foi muito baixa, e muitos pacientes cruzaram para o braço alternativo de tratamento.415415 Javaheri S, Brown LK, Randerath W, Khayat R. SERVE-HF: more questions than answers. Chest. 2016;149(4):900-4. doi: 10.1016/j.chest.2015.12.021.
https://doi.org/10.1016/j.chest.2015.12....
,416416 Bradley TD, Floras JS; ADVENT-HF Investigators. The SERVE-HF Trial. Can Respir J. 2015;22(6):313. PMID: 26474274. Outro estudo, utilizando o mesmo equipamento, foi interrompido precocemente em decorrência dos resultados do estudo SERVE-HF.417417 O'Connor CM, Whellan DJ, Fiuzat M, Punjabi NM, Tasissa G, Anstrom KJ, et al. Cardiovascular outcomes with minute ventilation-targeted adaptive servo-ventilation therapy in heart failure: the CAT-HF Trial. J Am Coll Cardiol. 2017;69(12):1577-87. doi: 10.1016/j.jacc.2017.01.041.
https://doi.org/10.1016/j.jacc.2017.01.0...
Os mecanismos pelos quais o servo ventilador é potencialmente deletério não são conhecidos. Uma especulação é que a pressão positiva poderia ter efeitos hemodinâmicos negativos em pacientes com IC agressivamente tratados com vasodilatadores e diuréticos.414414 Cowie MR, Woehrle H, Wegscheider K, Angermann C, d'Ortho MP, Erdmann E, et al. Adaptive servo-ventilation for central sleep apnea in systolic heart failure. N Engl J Med. 2015;373(12):1095-105. doi: 10.1056/NEJMoa1506459.
https://doi.org/10.1056/NEJMoa1506459...
Um outro estudo multicêntrico, o ADVENT-HF (Survival and Hospital Admissions in Heart Failure),418418 Lyons OD, Floras JS, Logan AG, Beanlands R, Cantolla JD, Fitzpatrick M, et al; ADVENT-HF Investigators. Design of the effect of adaptive servo-ventilation on survival and cardiovascular hospital admissions in patients with heart failure and sleep apnoea: the ADVENT-HF trial. Eur J Heart Fail. 2017;19(4):579-587. doi: 10.1002/ejhf.790.
https://doi.org/10.1002/ejhf.790...
testando outro modelo do servo ventilador em pacientes com IC e distúrbios de sono, está atualmente em andamento e pode esclarecer muitos das questões polêmicas envolvidas no estudo SERVE-HF.
7. Alterações Cardiovasculares em Outros Distúrbios de Sono
7.1. Privação do Sono
O aspecto “quantidade” refere ao TTS adequado para cada indivíduo. Atualmente, ainda existem discordâncias a respeito da média normal do número de horas dormidas da população. A maioria dos estudos considera como média normal entre 7 e 8 horas de sono por noite. Ainda, boa parte das pesquisas usa a média inferior a aproximadamente 6 horas de sono por noite como critério para privação crônica.419419 National Sleep Foundation [Internet]. [Accessed in 2016 Dec 10]. Available from: https://sleepfoundation.org/
https://sleepfoundation.org/...
Embora algumas pessoas necessitam de poucas horas de sono (os chamados short sleepers), a maioria daquelas que dormem pouco, na verdade, estão privando o sono, e as causas para tal são multifatoriais.420420 Taskar V, Hirshkowitz M. Health effects of sleep deprivation. Clin Pulm Med. 2003;10(1):47-52. Esta privação parcial de sono cada vez mais comum na nossa sociedade pode levar a sonolência diurna, défices de desempenho cognitivo e motor, alterações de humor e irritabilidade, com consequente prejuízo nas funções diárias.420420 Taskar V, Hirshkowitz M. Health effects of sleep deprivation. Clin Pulm Med. 2003;10(1):47-52.
Na avaliação das consequências cardiovasculares, é importante destacar que a maioria dos estudos usou critérios subjetivos para quantificar a duração de sono (autorrelato). Sabe-se que a concordância com medidas objetivas (como a actigrafia) não é muito satisfatória. Outros estudos usaram o TTS calculado pela polissonografia, o que também não reflete a realidade, por se tratar de um momento que não reproduz a rotina do paciente.
Dito isto, diversos estudos têm mostrado associação entre a curta duração do sono (em geral, citados como menos de 6 ou 5 horas) e as diversas doenças cardiovasculares. Especificamente, a privação do sono tem sido associada com prevalência e incidência de HAS,421421 Gangwisch JE. A review of evidence for the link between sleep duration and hypertension. Am J Hypertens. 2014;27(10):1235-42. doi: 10.1093/ajh/hpu071.
https://doi.org/10.1093/ajh/hpu071...
obesidade,422422 Theorell-Haglöw J, Berglund L, Berne C, Lindberg E. Both habitual short sleepers and long sleepers are at greater risk of obesity: a population-based 10-year follow-up in women. Sleep Med. 2014;15(10):1204-11. doi: 10.1016/j.sleep.2014.02.014.
https://doi.org/10.1016/j.sleep.2014.02....
resistência à insulina,423423 Spiegel K, Leproult R, Cauter EV. Impact of sleep debt on metabolic and endocrine function. Lancet. 1999;354(9188):1435-9. doi: 10.1016/S0140-6736(99)01376-8.
https://doi.org/10.1016/S0140-6736(99)01...
DM,424424 Shan Z, Ma H, Xie M, Yan P, Guo Y, Bao W, et al. Sleep duration and risk of type 2 diabetes: a meta-analysis of prospective studies. Diabetes Care. 2015;38(3):529-37. doi: 10.2337/dc14-2073.
https://doi.org/10.2337/dc14-2073...
incidência de calcificação coronariana425425 King CR, Knutson KL, Rathouz PJ, Sidney S, Liu K, Lauderdale DS. Short sleep duration and incident coronary artery calcification. JAMA. 2008;300(24):2859-66. doi: 10.1001/jama.2008.867
https://doi.org/10.1001/jama.2008.867...
e eventos cardiovasculares fatais e não fatais.426426 Ayas NT, White DP, Manson JE, Stampfer MJ, Speizer FE, Malhotra A, et al. Aprospective study of sleep duration and coronary heart disease in women. Arch Intern Med. 2003;163(2):205-9. PMID: 12546611.
427 Ikehara S, Iso H, Date C, Kikuchi S, Watanabe Y, Wada Y, et al. Association of sleep duration with mortality from cardiovascular disease and other causes for Japanese men and women: the JACC study. Sleep. 2009;32(3):295-301. PMID: 19294949.-428428 Cappuccio FP, Cooper D, D'Elia L, Strazzullo P, Miller MA. Sleep duration predicts cardiovascular outcomes: a systematic review and meta-analysis of prospective studies. Eur Heart J. 2011;32(12):1484-92. doi: 10.1093/eurheartj/ehr007.
https://doi.org/10.1093/eurheartj/ehr007...
Apesar de os mecanismos pelos quais a privação do sono promove a doença cardiovascular não serem totalmente reconhecidos, há evidências de que dormir pouco aumenta a grelinae reduz a leptina, o que contribui para o aumento do apetite e ganho de peso, a hiperatividade simpática, a inflamação e o estresse oxidativo, entre outros.429429 Méier-Ewert HK, Ridker PM, Rifai N, Regan MM, Price NJ, Dinges DF, et al. Effect of sleep loss on C-reative protein, an inflammatory marker of cardiovascular risk. J Am Coll Cardiol. 2004;43(4):678-83. doi: 10.1016/j.jacc.2003.07.050.
https://doi.org/10.1016/j.jacc.2003.07.0...
,430430 Miller MA, Cappuccio FP. Biomarkers of cardiovascular risk in sleep-deprived people. J Hum Hypertens. 2013;27(10):583-8. doi: 10.1038/jhh.2013.27.
https://doi.org/10.1038/jhh.2013.27...
A despeito destas evidências, não está claro se o aumento da duração do sono em pacientes com privação do sono está associado com uma redução dos eventos cardiovasculares fatais e não fatais.
De forma intrigante, a longa duração do sono (usualmente referida nos trabalhos como a duração do sono > 8 a 9 horas cronicamente) também parece estar associada com diversas doenças cardiovasculares descritas anteriormente.428428 Cappuccio FP, Cooper D, D'Elia L, Strazzullo P, Miller MA. Sleep duration predicts cardiovascular outcomes: a systematic review and meta-analysis of prospective studies. Eur Heart J. 2011;32(12):1484-92. doi: 10.1093/eurheartj/ehr007.
https://doi.org/10.1093/eurheartj/ehr007...
As explicações não são claras. Especula-se que a longa duração do sono pode ser um marcador de alguma doença subjacente, e não propriamente dito um potencial fator de risco cardiovascular.
7.2. Insônia
A insônia crônica pode ser definida como a dificuldade em iniciar o sono e/ou dificuldade em mantê-lo e/ou acordar mais cedo do que o desejado ocorrendo no mínimo duas vezes por semana por, no mínimo, 3 meses, acompanhada de insatisfação com o sono e prejuízos de funcionamento durante o dia, como fadiga/mal-estar; prejuízo na atenção, concentração ou memória; prejuízo social, familiar, profissional, ou no desempenho acadêmico; perturbação do humor/irritabilidade; sonolência diurna; impulsividade; agressividade; redução da motivação/energia/iniciativa/propensão para erros/acidentes.431431 American Psychiatric Association. Diagnostic and statistical manual of mental disorders. 5th ed. Arlington (VA); 2013.,432432 Ohayon MM, Reynolds CF 3rd. Epidemiological and clinical relevance of insomnia diagnosis algorithms according to the DSM-IV and the International Classification of Sleep Disorders (ICSD). Sleep Med. 2009;10(9):952-60. doi: 10.1016/j.sleep.2009.07.008. Erratum in: Sleep Med. 2010;11(2):227.
https://doi.org/10.1016/j.sleep.2009.07....
Embora frequentemente seja associada com a curta duração do sono, muitos pacientes apresentam, em média, duração do sono dentro da faixa tradicional de 7 a 8 horas.433433 Fernandez-Mendoza J, Calhoun SL, Bixler EO, Karataraki M, Liao D, Vela-Bueno A, et al. Sleep misperception and chronic insomnia in the general population: role of objective sleep duration and psychological profiles. Psychosom Med. 2011;73(1):88-97. doi: 10.1097/PSY.0b013e3181fe365a.
https://doi.org/10.1097/PSY.0b013e3181fe...
Por outro lado, vários pacientes com duração curta do sono não têm insônia, mas sim privam o sono por estilo de vida.432432 Ohayon MM, Reynolds CF 3rd. Epidemiological and clinical relevance of insomnia diagnosis algorithms according to the DSM-IV and the International Classification of Sleep Disorders (ICSD). Sleep Med. 2009;10(9):952-60. doi: 10.1016/j.sleep.2009.07.008. Erratum in: Sleep Med. 2010;11(2):227.
https://doi.org/10.1016/j.sleep.2009.07....
No entanto, parece que a presença da insônia e a curta duração do sono são fenótipos de maior risco cardiovascular434434 Fernandez-Mendoza J, Baker JH, Vgontzas AN, Gaines J, Liao D, Bixler EO. Insomnia symptoms with objective short sleep duration are associated with systemic inflammation in adolescents. Brain Behav Immun. 2017 Mar;61:110-6. doi: 10.1016/j.bbi.2016.12.026.
https://doi.org/10.1016/j.bbi.2016.12.02...
435 Lin CL, Tsai YH, Yeh MC. The relationship between insomnia with short sleep duration is associated with hypercholesterolemia: a cross-sectional study. J Adv Nurs. 2016;72(2):339-47. doi: 10.1111/jan.12844.
https://doi.org/10.1111/jan.12844...
436 Cespedes EM, Dudley KA, Sotres-Alvarez D, Zee PC, Daviglus ML, Shah NA, et al. Joint associations of insomnia and sleep duration with prevalent diabetes: the Hispanic Community Health Study/Study of Latinos (HCHS/SOL). J Diabetes. 2016;8(3):387-97. doi: 10.1111/1753-0407.12308.
https://doi.org/10.1111/1753-0407.12308...
437 Bathgate CJ, Edinger JD, Wyatt JK, Krystal AD. Objective but not subjective short sleep duration associated with increased risk for hypertension in individuals with insomnia. Sleep. 2016;39(5):1037-45. doi: 10.5665/sleep.5748.
https://doi.org/10.5665/sleep.5748...
438 Fernandez-Mendoza J, Vgontzas AN, Liao D, Shaffer ML, Vela-Bueno A, Basta M, et al. Insomnia with objective short sleep duration and incident hypertension: the Penn State Cohort. Hypertension. 2012;60(4):929-35. doi: 10.1161/HYPERTENSIONAHA.112.193268
https://doi.org/10.1161/HYPERTENSIONAHA....
439 Vgontzas AN, Fernandez-Mendoza J, Liao D, Bixler EO. Insomnia with objective short sleep duration: the most biologically severe phenotype of the disorder. Sleep Med Rev. 2013;17(4):241-54. doi: 10.1016/j.smrv.2012.09.005.
https://doi.org/10.1016/j.smrv.2012.09.0...
-440440 Chien KL, Chen PC, Hsu HC, Su TC, Sung FC, Chen MF, et al. Habitual sleep duration and insomnia and the risk of cardiovascular events and all-cause death: report from a community-based cohort. Sleep. 2010;33(2):177-84. PMID: 20175401. e mortalidade,441441 Vgontzas AN, Liao D, Pejovic S, Calhoun S, Karataraki M, Basta M, et al. Insomnia with short sleep duration and mortality: the Penn State cohort. Sleep. 2010;33(9):1159-64. PMID: 20857861. além de apresentar menor resposta de medidas terapêuticas para a insônia.442442 Bathgate CJ, Edinger JD, Krystal AD. Insomnia patients with objective short sleep duration have a blunted response to cognitive behavioral therapy for insomnia. Sleep. 2017 Jan 1;40(1). doi: 10.1093/sleep/zsw012.
https://doi.org/10.1093/sleep/zsw012...
A insônia é um dos distúrbios de sono mais comuns na prática médica. Sua prevalência tem sido estimada em muitos estudos em torno de 5 a 15%, porém varia de acordo com o critério usado.432432 Ohayon MM, Reynolds CF 3rd. Epidemiological and clinical relevance of insomnia diagnosis algorithms according to the DSM-IV and the International Classification of Sleep Disorders (ICSD). Sleep Med. 2009;10(9):952-60. doi: 10.1016/j.sleep.2009.07.008. Erratum in: Sleep Med. 2010;11(2):227.
https://doi.org/10.1016/j.sleep.2009.07....
Vários estudos também avaliam a associação entre insônia e incidência de doença cardiovascular, incluindo hipertensão arterial, DAC e IC,443443 Javaheri S, Redline S. Insomnia and risk of cardiovascular disease. Chest. 2017;152(2):435-44. doi: 10.1016/j.chest.2017.01.026.
https://doi.org/10.1016/j.chest.2017.01....
principalmente naquele fenótipo de curta duração do sono. Os mecanismos propostos se relacionam com a desregulação do eixo hipotálamo-hipofisário, aumento da atividade do sistema nervoso simpático e inflamação.443443 Javaheri S, Redline S. Insomnia and risk of cardiovascular disease. Chest. 2017;152(2):435-44. doi: 10.1016/j.chest.2017.01.026.
https://doi.org/10.1016/j.chest.2017.01....
Vários estudos também relatam a insônia associada ao risco de mortalidade cardiovascular. Uma revisão sistemática e metanálise444444 Sofi F, Cesari F, Casini A, Macchi C, Abbate R, Gensini GF. Insomnia and risk of cardiovascular disease: a meta-analysis. Eur J Prev Cardiol. 2014;21(1):57-64. doi: 10.1177/2047487312460020.
https://doi.org/10.1177/2047487312460020...
de estudos prospectivos de coorte mostrou que, em 122.501 indivíduos livres de doença cardiovascular no momento da avaliação inicial − porém com insônia (avaliada usando questionário), tiveram risco aumentado de 45% (IC95% 1,29-1,62) de desenvolver ou morrer de doença cardiovascular durante seguimento de 3 a 20 anos.444444 Sofi F, Cesari F, Casini A, Macchi C, Abbate R, Gensini GF. Insomnia and risk of cardiovascular disease: a meta-analysis. Eur J Prev Cardiol. 2014;21(1):57-64. doi: 10.1177/2047487312460020.
https://doi.org/10.1177/2047487312460020...
Outra metanálise, de 17 estudos de coorte, com 311.260 indivíduos sem doença cardiovascular, inicialmente demonstrou 33% aumento de RR (IC95% 1,13-1,57) de mortalidade cardiovascular em pessoas com insônia.445445 Li M, Zhang XW, Hou WS, Tang ZY. Insomnia and risk of cardiovascular disease: a meta-analysis of cohort studies. Int J Cardiol. 2014;176(3):1044-7. doi: 10.1016/j.ijcard.2014.07.284.
https://doi.org/10.1016/j.ijcard.2014.07...
Recentemente, Parthasarathy et al.446446 Parthasarathy S, Vasquez MM, Halonen M, Bootzin R, Quan SF, Martinez FD, et al. Persistent insomnia is associated with mortality risk. Am J Med. 2015;128(3):268-75. doi: 10.1016/j.amjmed.2014.10.015.
https://doi.org/10.1016/j.amjmed.2014.10...
também demonstraram aumento de cerca de duas vezes no risco de mortalidade por doença cardíaca e mortalidade cardiopulmonar entre 1.409 pacientes com insônia crônica e persistente.446446 Parthasarathy S, Vasquez MM, Halonen M, Bootzin R, Quan SF, Martinez FD, et al. Persistent insomnia is associated with mortality risk. Am J Med. 2015;128(3):268-75. doi: 10.1016/j.amjmed.2014.10.015.
https://doi.org/10.1016/j.amjmed.2014.10...
A despeito destas evidências, não há conclusões de que o tratamento da insônia melhorou desfechos intermediários (como a HAS). Não há evidências de que também reduza eventos cardiovasculares fatais e não fatais.
7.3. Narcolepsia
A narcolepsia consiste em um distúrbio do sono caracterizado por sonolência excessiva diurna, cataplexia e presença de alterações durante o sono REM, como paralisia do sono e alucinações hipnagógicas.447447 American Academy of Sleep Medicine. International classification of sleep disorders. diagnostic and coding manual. 2nd ed. Westchester, IL; 2005. A cataplexia é outro sintoma da narcolepsia caracterizado por perda súbita e bilateral do tônus muscular durante as emoções. São característicos também a fragmentação do ciclo sono-vigília com presença de sono REM precoce diurno e os numerosos despertares durante o sono noturno.448448 Dauvilliers Y, Billiard M, Montplaisir J. Clinical aspects and pathophysiology of narcolepsy. Clin Neurophysiol. 2003;114(11):2000-17. PMID: 14580598.,449449 Plazzi G, Ferri R, Antelmi E, Bayard S, Franceschini C, Cosentino FI, et al. Restless legs syndrome is frequent in narcolepsy with cataplexy patients. Sleep. 2010;33(5):689-94. PMID: 20469811.
A prevalência de Narcolepsia com Cataplexia (NC) varia entre 25 a 50 por 100 mil habitantes,450450 Longstreth WT Jr, Koepsell TD, Ton TG, Hendrickson AF, van Belle G. The epidemiology of narcolepsy. Sleep. 2007;30(1):13-26. PMID: 17310860. com pico de incidência na segunda década de vida. Ambos os sexos são afetados, na proporção de 1,4/1,80 homem/mulher.451451 Silber MH, Krahn LE, Olson EJ, Pankratz VS. The epidemiology of narcolepsy in Olmsted County, Minnesota: a population-based study. Sleep. 2002;25(2):197-202. PMID: 11902429.
Pacientes com NC apresentam deficiência de hipocretina-1, um peptídeo produzido por neurônios do hipotálamo lateral, cuja atividade está implicada no controle autonômico cardiovascular452452 Sachs C, Kaijser L. Autonomic regulation of cardiopulmonary functions in sleep apnea syndrome and narcolepsy. Sleep. 1982;5(3):227-38. PMID: 6813932. e endócrino.453453 Dauvilliers Y, Arnulf I, Mignot E. Narcolepsy with cataplexy. Lancet. 2007;369(9560):499-511. doi: 10.1016/S0140-6736(07)60237-2.
https://doi.org/10.1016/S0140-6736(07)60...
,454454 Nishino S. Clinical and neurobiological aspects of narcolepsy. Sleep Med. 2007;8(4):373-99. doi: 10.1016/j.sleep.2007.03.008.
https://doi.org/10.1016/j.sleep.2007.03....
Em relação às consequências cardiovasculares, não existem estudos prospectivos que estabeleçam relação entre a NC e deficiência de hipocretina-1 com o aumento das doenças cardiovasculares. Estudos observacionais sugerem alteração das respostas autonômicas e ausência do descenso noturno da pressão arterial.455455 Silvani A, Grimaldi D, Barletta G, Bastianini S, Vandi S, Pierangeli G, et al. Cardiovascular variability as a function of sleep-wake behaviour in narcolepsy with cataplexy. J Sleep Res. 2013;22(2):178-84. doi: 10.1111/jsr.12007.
https://doi.org/10.1111/jsr.12007...
,456456 Grimaldi D, Calandra-Buonaura G, Provini F, Agati P, Pierangeli G, Franceschini C, et al. Abnormal sleep-cardiovascular system interaction in narcolepsy with cataplexy: effects of hypocretin deficiency in humans. Sleep. 2012;35(4):519-28. doi: 10.5665/sleep.1738.
https://doi.org/10.5665/sleep.1738...
Em estudo controlado com 50 pacientes com NC, 31% dos pacientes não apresentaram o descenso noturno da pressão arterial de 10%, comparados a apenas 3% dos controles (p = 0,002). A ausência do descenso noturno da pressão arterial diastólica associou-se de forma independente com NC, sonolência diurna e presença de dislipidemia.457457 Dauvilliers Y, Jaussent I, Krams B, Scholz S, Lado S, Levy P, et al. Non-dipping blood pressure profile in narcolepsy with cataplexy. PLoS One. 2012;7(6):e38977. doi: 10.1371/journal.pone.0038977.
https://doi.org/10.1371/journal.pone.003...
Não existem evidências de que a narcolepsia aumenta o risco de eventos cardiovasculares fatais e não fatais.
Em relação ao tratamento da narcolepsia, não há estudos consistentes que mostrem efeitos deletérios sobre o sistema cardiovascular pelo uso de medicações estimulantes do sistema nervoso central no tratamento da NC. Auger et al.458458 Auger RR, Goodman SH, Silber MH, Krahn LE, Pankratz VS, Slocumb NL. Risks of high-dose stimulants in the treatment of disorders of excessive somnolence: a case-control study. Sleep. 2005;28(6):667-72. PMID: 16477952. demonstraram maior frequência de taquiarritmias com o uso em altas doses (OD = 3,3; IC95% 0,92-12,1). Em coorte retrospectiva de 45,6 meses, o tratamento com estimulantes não acarretou mudança significativa na PA sistólica e diastólica.459459 Wallin M, Mahowald M. Blood pressure effects of long term stimulant use in disorders of hypersomnolence. J Sleep Res. 1998;7(3):209-15. PMID: 9785276.
Não há evidência de que o tratamento da narcolepsia resuza o risco cardiovascular.
7.4. Síndrome das Pernas Inquietas
A SPI é um transtorno neurológico sensitivo-motor caracterizado por sensações desagradáveis nos membros que levam à urgência em movimentar as pernas.447447 American Academy of Sleep Medicine. International classification of sleep disorders. diagnostic and coding manual. 2nd ed. Westchester, IL; 2005. O diagnóstico é clínico, baseado em quatro critérios essenciais definidos pelo International Restless Legs Syndrome Study Group (IRLSSG):
-
Urgência em movimentar as pernas geralmente, mas nem sempre causada ou acompanhada por sensações desagradáveis ou desconfortáveis (podem ocorrer nos braços e em outras partes do corpo, associadamente às pernas).
-
A urgência ou as sensações desagradáveis começam ou pioram durante períodos de repouso ou inatividade, como em posição deitada ou sentada.
-
O movimento (por exemplo, caminhar e alongar-se) traz alívio total ou parcial da necessidade de mover as pernas ou sensações desagradáveis, pelo menos durante o período de realização da atividade.
-
A necessidade de mover as pernas ou as sensações desagradáveis surgem ou pioram no final do dia e à noite.460460 Allen RP, Picchietti D, Henning WA, Trenkwalder C, Walters AS, Montplaisi J; Restless Legs Syndrome Diagnosis and Epidemiology workshop at the National Institutes of Health; International Restless Legs Syndrome Study Group. Restless legs syndrome: diagnostic criteria, special considerations, and epidemiology. A report from the restless legs syndrome diagnosis and epidemiology workshop at the National Institutes of Health. Sleep Med. 2003;4(2):101-19. PMID: 14592341.
Em 2011, o IRLSSG revisou os critérios, adicionando um quinto critério essencial: excluir outra condição médica ou comportamental como causa primária dos sintomas acima (por exemplo: mialgia, estase venosa, edema em membros, artrite, câimbras, desconforto posicional, movimentação repetitiva de pés).461461 Allen RP, Picchietti DL, Garcia-Borreguero D, Ondo WG, Walters AS, Winkelman JW, et al. Restless Legs Syndrome Willis-Ekbom disease diagnostic criteria: updated International Restless Legs Syndrome Study Group (IRLSSG) consensus criteria history, rationale, description, and significance. Sleep Medicine. 2014;15:800-73. doi: http//dx.doi.org/10.1016/j.sleep.2014.03.025.
http//dx.doi.org/10.1016/j.sleep.2014.03...
A prevalência da SPI varia entre 7,4 a 11,9%, em análise de quatro coortes prospectivas, dependendo da população estudada e da metodologia para o diagnóstico da doença.462462 Szentkirályi A, Winter AC, Schürks M, Völzke H, Hoffmann W, E Buring J, et al. Restless legs syndrome and all-cause mortality in four prospective cohort studies. BMJ Open. 2012;2(6). pii: e001652. doi: 10.1136/bmjopen-2012-001652.
https://doi.org/10.1136/bmjopen-2012-001...
Sua prevalência aumenta com a idade,463463 Berger K, Kurth T. RLS epidemiology?frequencies, risk factors and methods in population studies. Mov Disord. 2007;22 Suppl 18:S420-3. doi: 10.1002/mds.21589.
https://doi.org/10.1002/mds.21589...
,464464 Rothdach AJ, Trenkwalder C, Haberstock J, Keil U, Berger K. Prevalence and risk factors of RLS in an elderly population: the MEMO study. Memory and Morbidity in Augsburg Elderly. Neurology. 2000;54(5):1064-8. PMID: 10720275. sendo duas vezes mais comum em mulheres.465465 Berger K, Luedemann J, Trenkwalder C, John U, Kessler C. Sex and the risk of restless legs syndrome in the general population. Arch Intern Med. 2004;164(2):196-202. doi: 10.1001/archinte.164.2.196.
https://doi.org/10.1001/archinte.164.2.1...
Não há dados de prevalência da SPI na população brasileira.
Vários estudos transversais de base populacional sugeriram associação entre doenças cardiovasculares e SPI. Em estudo com 4.000 homens de 18 a 64 anos,466466 Ulfberg J, Nystrom B, Carter N, Edling C. Prevalence of restless legs syndrome among men aged 18 to 64 years: an association with somatic disease and neuropsychiatric symptoms. Mov Disord. 2001;16(6):1159-63. PMID: 11748753. aqueles que apresentaram SPI relataram maior presença de doença cardíaca (OD=2,5; IC95% 1,4-4,3) e HAS (OR=1,5; IC95% 0,9-2,4). Um estudo transversal por entrevista por telefone com 18.980 indivíduos de cinco países europeus encontrou associação da SPI com a presença de HAS e DAC.467467 Ohayon MM, Roth T. Prevalence of restless legs syndrome and periodic limb movement disorder in the general population. J Psychosom Res. 2002;53(1):547-54. PMID: 12127170. Winkelman et al.468468 Winkelman JW, Finn L, Young T. Prevalence and correlates of restless legs syndrome symptoms in the Wisconsin Sleep Cohort. Sleep Med 2006;7(7):545-52. doi: 10.1016/j.sleep.2006.01.004.
https://doi.org/10.1016/j.sleep.2006.01....
encontraram 2,5 vezes mais história de doença cardiovascular em indivíduos com sintomas diários de SPI comparados aos sem SPI. De forma consistente, na coorte do SHHS, os indivíduos com SPI apresentaram chance ajustada de duas vezes maior de ter DAC ou doença cardiovascular comparados aos sem SPI.384384 Winkelman JW, Shahar E, Sharief I, Gottlieb DJ. Association of restless legs syndrome and cardiovascular disease in the Sleep Heart Health Study. Neurology. 2008;70(1):35-42. doi: 10.1212/01.wnl.0000287072.93277.c9.
https://doi.org/10.1212/01.wnl.000028707...
Esta aassociação foi maior em pacientes com sintomas de SPI pelo menos 16 vezes ao mês e naqueles que relataram sintomas intensos, quando comparados aos que relataram sintomas moderados. Em estudo transversal de 65.544 mulheres (41 a 58 anos), a presença de sintomas de SPI ≥ 15 vezes ao mês foi independentemente associada com 40% de aumento de ter HAS comparadas àquelas sem sintomas.469469 Batool-Anwar S, Malhotra A, Forman J, Winkelman J, Li Y, Gao X. Restless legs syndrome and hypertension in middle-aged women. Hypertension. 2011;58(5):791-6. doi: 10.1161/HYPERTENSIONAHA.111.174037.
https://doi.org/10.1161/HYPERTENSIONAHA....
No entanto, estudo transversal com 30.262 mulheres participantes do Women’s Health Study (WHS) não mostrou associação entre a presença da SPI e doenças cardiovasculares.470470 Winter AC, Schürks M, Glynn RJ, Buring JE, Gaziano JE, Berger K, et al. Vascular risk factors, cardiovascular disease, and restless legs syndrome in women. Am J Med. 2013;126(3):220-7. doi: 10.1016/j.amjmed.2012.06.040.
https://doi.org/10.1016/j.amjmed.2012.06...
Em homens, a SPI foi associada com o AVC,471471 Winter AC, Berger K, Glynn RJ, Buring JE, Gaziano JM, Schürks M, et al. Vascular risk factors, cardiovascular disease, and restless legs syndrome in men. Am J Med. 2013;126(3):228-35. doi: 10.1016/j.amjmed.2012.06.039.
https://doi.org/10.1016/j.amjmed.2012.06...
mas, por se tratar de um estudo transversal, não se pode afirmar que a SPI promoveu o AVC ou o evento cerebrovascular contribuiu para o surgimento da SPI.471471 Winter AC, Berger K, Glynn RJ, Buring JE, Gaziano JM, Schürks M, et al. Vascular risk factors, cardiovascular disease, and restless legs syndrome in men. Am J Med. 2013;126(3):228-35. doi: 10.1016/j.amjmed.2012.06.039.
https://doi.org/10.1016/j.amjmed.2012.06...
É importante destacar, no entanto, que estes e outros estudos transversais foram baseados em questionários de autorrelato, não apresentando análise detalhada e nem exclusão de pacientes com sintomas que mimetizam SPI.
Os dados prospectivos ainda não são consistentes. Estudo envolvendo duas coortes de profissionais de saúde (29.756 mulheres com 45 anos ou mais e 19.182 homens com 40 anos ou mais) não mostrou aumento do risco para eventos cardiovasculares em pacientes com SPI.472472 Winter AC, Schürks M, Glynn RJ, Buring JE, Gaziano JM, Berger K, et al. Restless legs syndrome and risk of incident cardiovascular disease in women and men: prospective cohort study. BMJ Open. 2012;2(2):e000866. doi: 10.1136/bmjopen-2012-000866.
https://doi.org/10.1136/bmjopen-2012-000...
Já em outro estudo com 70.977 mulheres (idade média de 67anos) inicialmente sem DAC ou AVC de 2002 a 2008.473473 Li Y, Walters AS, Chiuve SE, Rimm EB, Winkelman JW, Gao X. Prospective study of restless legs syndrome and coronary heart disease among women. Circulation. 2012;126(14):1689-94. doi: 10.1161/CIRCULATIONAHA.112.112698.
https://doi.org/10.1161/CIRCULATIONAHA.1...
As mulheres com SPI com duração de 3 anos ou mais apresentaram maior chance de eventos cardiovasculares fatais e não fatais.473473 Li Y, Walters AS, Chiuve SE, Rimm EB, Winkelman JW, Gao X. Prospective study of restless legs syndrome and coronary heart disease among women. Circulation. 2012;126(14):1689-94. doi: 10.1161/CIRCULATIONAHA.112.112698.
https://doi.org/10.1161/CIRCULATIONAHA.1...
Em uma coorte com 20 anos de seguimento, houve relato de aumento da mortalidade em mulheres de meia-idade com SPI e sonolência diurna.474474 Mallon L, Broman JE, Hetta J. Restless legs symptoms with sleepiness in relation to mortality: 20-year follow-up study of a middle-aged Swedish population. Psychiatry Clin Neurosci. 2008;62(4):472-5. doi: 10.1111/j.1440-1819.2008.01825.x.
https://doi.org/10.1111/j.1440-1819.2008...
Portanto, ainda há controvérsia sobre a relação entre a SPI e doenças cardiovasculares, com estudos robustos falando contra uma relação causal. A privação de sono nestes pacientes, o impacto da gravidade dos sintomas na qualidade de vida, o tempo de duração da SPI e a coexistência de fatores de risco vascular em pacientes com a doença podem ser fatores que contribuem para a associação com eventos cardiovasculares, sendo necessários estudos que esclareçam os mecanismos fisiopatológicos e o impacto da interação entre as comorbidades dos pacientes com SPI.
Em relação ao tratamento, não existem evidências de que o tratamento da SPI tenha benefício cardiovascular.
8. Papel da Equipe Multidisciplinar no Tratamento dos Distúrbios de Sono
Para que a Medicina do Sono tenha padrões elevados de eficiência, confiabilidade e segurança ao tratamento, é necessário o contínuo treinamento de toda a equipe multiprofissional. Todos devem desempenhar suas funções baseando-se em conhecimentos técnico-científicos sólidos e atualizados. Estas características, aliadas a valores éticos, humanistas e um bom trabalho em equipe, propicia melhores resultados em relação à satisfação da população atendida. Assim, a atuação da equipe multiprofissional no tratamento dos distúrbios respiratórios do sono é fundamental para os desafios que os distúrbios de sono oferecem. Destaca-se, a seguir, a ação de algumas áreas.
8.1. Fisioterapia
O CPAP é o tratamento padrão-ouro para a AOS moderada à grave, principalmente nos casos sintomáticos.475475 Grunstein RR. Sleep-related breathing disorders. 5. nasal continuous positive airway pressure treatment for obstructive sleep apnoea. Thorax. 1995;50:1106-13. PMID: 7491563. Pode também estar indicado em alguns casos de apneia leve com presença de sintomas e/ou outras comorbidades. O fisioterapeuta respiratório com experiência na área do sono atua na adaptação do paciente ao dispositivo de pressão positiva e em seu acompanhamento em curto, médio e longo prazo, no intuito de solucionar possíveis problemas e contribuir para melhorar a adesão.
A adaptação compreende a avaliação do paciente, do exame do sono e da prescrição médica, que pode indicar o equipamento de escolha. Com a seleção da interface, ajustes finos no dispositivo (tempo de rampa, rampa automática, alívio de pressão inspiratório e expiratório, e alívio de pressão sensível ao despertar) podem ser necessários, para proporcionar maior conforto, além da indicação do umidificador aquecido, que ajuda a minimizar queixas nasais.
A adesão ao CPAP ainda é um grande desafio, e a fase inicial parece ser crucial, uma vez que alguns estudos sugerem que a primeira semana de uso do CPAP pode predizer a adesão em longo prazo.476476 Kribbs NB, Pack AI, Kline LR, Smith PL, Schwartz AR, Schubert NM, et al. Objective measurement of pattern of nasal CPAP use by patients with obstructive sleep apnea. Am Rev Respir Dis. 1993;147(4):887-95. doi: 10.1164/ajrccm/147.4.887.
https://doi.org/10.1164/ajrccm/147.4.887...
,477477 Veasey SC, Guilleminault C, Strohl KP, Sanders MH, Ballard RD, Magalang UJ. Medical therapy for obstructive sleep apnea: a review by the Medical Therapy for Obstructive Sleep Apnea Task Force of the Standards of Practice Committee of the American Academy of Sleep Medicine. Sleep. 2006;29(8):1036-44. PMID: 16944672. Assim, quanto melhor for o primeiro contato do pacente com o CPAP e mais abrangente for o suporte profissional ele tiver neste início do tratamento, melhores devem ser os resultados.
A avaliação da ergonomia do sono (posição corporal e travesseiro utilizado) e as orientações a este respeito podem prevenir causas de desconforto, como abertura de boca, ressecamento oral e compressão externa da máscara contra o rosto por travesseiros de baixa densidade. Aliado a isso, os conhecimentos deste profissional sobre aspectos anatômicos e fisiológicos também podem esclarecer dúvidas do paciente, ajudando a alcançar melhores resultados no tratamento.
Durante o processo inicial do tratamento, o acompanhamento do fisioterapeuta permite identificar, corrigir e comunicar ao médico problemas relacionados ao uso do equipamento, como vazamento pela interface, aerofagia, fixação inadequada da máscara no rosto, queixas de irritação nasal e ocular, ressecamento de via aérea, lesões de pele, melhora ou piora de sintomas, além de orientar o paciente sobre a conservação do equipamento, a periodicidade de higienização e a troca de filtros. A monitoria da adesão ao CPAP é feita objetivamente, com o uso de cartões acoplados aos equipamentos. No entanto, o acesso remoto (wireless) aos dados registrados pelos equipamentos mais novos permite análise precoce e a distância dos resultados do tratamento, facilitando a atuação do profissional que pode, imediatamente, verificar o problema e corrigi-lo com maior rapidez. Esta parece ser a tendência mundial de monitorização do CPAP, visando identificar e intervir precocemente na tentativa de melhora da adesão ao tratamento.
No tratamento em médio e longo prazo, o acompanhamento com o fisioterapeuta possibilita realizar ajustes na máscara e no aparelho e identificar se a pressão de tratamento está adequada ou precisa ser reajustada. É importante ressaltar que um trabalho em conjunto do fisioterapeuta com o médico do sono e demais membros da equipe multiprofissional também é vital para o sucesso do tratamento.
8.2. Educação Física
A participação de pacientes com AOS em programas de treinamento físico regular com prescrição individualizada e supervisão do profissional de educação física tem sido reportada como importante estratégia não farmacológica e coadjuvante no tratamento dos distúrbios respiratórios de sono.478478 Barnes M, Goldsworthy UR, Cary BA, Hill CJ. A diet and exercise program to improve clinical outcomes in patients with obstructive sleep apnea--a feasibility study. J Clin Sleep Med. 2009;5(5):409-15. PMID: 19961023.
479 Norman JF, Von Essen SG, Fuchs RH, McElligott M. Exercise training effect on obstructive sleep apnoea syndrome. Sleep Res Online. 2000;3(3):121-9. PMID: 11382910.
480 Tuomilehto HP, Seppä JM, Partinen MM, Peltonen M, Gylling H, Tuomilehto JO, et al; Kuopio Sleep Apnea Group. Lifestyle intervention with weight reduction: first-line treatment in mild obstructive sleep apnea. Am J Respir Crit Care Med. 2009;179(4):320-7. doi: 10.1164/rccm.200805-669OC.
https://doi.org/10.1164/rccm.200805-669O...
-481481 Ueno LM, Drager LF, Rodrigues AC, Rondon MU, Braga AM, Mathias W Jr, et al. Effects of exercise training in patients with chronic heart failure and sleep apnea. Sleep. 2009;32(5):637-47. PMID: 19480231. A atividade física regular supervisionada pode contribuir para uma melhora na composição corporal, nos padrões de sono, na resposta vasodilatadora periférica, na modulação do controle autonômico e na melhora do condicionamento físico. De fato, programas de treinamento físico com exercícios aeróbios, mais exercícios de resistência muscular localizada, com frequência de três sessões por semana, por um período de 12 a 16 semanas, melhoraram significativamente a capacidade cardiorrespiratória de indivíduos com AOS (sobrepeso e obesos) sem doença cardiovascular,478478 Barnes M, Goldsworthy UR, Cary BA, Hill CJ. A diet and exercise program to improve clinical outcomes in patients with obstructive sleep apnea--a feasibility study. J Clin Sleep Med. 2009;5(5):409-15. PMID: 19961023.,482482 Sengul YS, Ozalevli S, Oztura I, Itil O, Baklan B. The effect of exercise on obstructive sleep apnea: a randomized and controlled trial. Sleep Breath. 2009;15(1):49-56. doi: 10.1007/s11325-009-0311-1.
https://doi.org/10.1007/s11325-009-0311-...
ou de pacientes com IC e AOS.481481 Ueno LM, Drager LF, Rodrigues AC, Rondon MU, Braga AM, Mathias W Jr, et al. Effects of exercise training in patients with chronic heart failure and sleep apnea. Sleep. 2009;32(5):637-47. PMID: 19480231.,483483 Yamamoto U, Mohri M, Shimada K, Origuchi H, Miyata K, Ito K, et al. Six-month aerobic exercise training ameliorates central sleep apnea in patients with chronic heart failure. J Card Fail. 2007;13(10):825-9. doi: 10.1016/j.cardfail.2007.08.001.
https://doi.org/10.1016/j.cardfail.2007....
Estes fatores associados atuam como coadjuvantes na redução do risco cardiovascular e proporcionam motivação do paciente para um estilo de vida mais ativo.478478 Barnes M, Goldsworthy UR, Cary BA, Hill CJ. A diet and exercise program to improve clinical outcomes in patients with obstructive sleep apnea--a feasibility study. J Clin Sleep Med. 2009;5(5):409-15. PMID: 19961023.,480480 Tuomilehto HP, Seppä JM, Partinen MM, Peltonen M, Gylling H, Tuomilehto JO, et al; Kuopio Sleep Apnea Group. Lifestyle intervention with weight reduction: first-line treatment in mild obstructive sleep apnea. Am J Respir Crit Care Med. 2009;179(4):320-7. doi: 10.1164/rccm.200805-669OC.
https://doi.org/10.1164/rccm.200805-669O...
481 Ueno LM, Drager LF, Rodrigues AC, Rondon MU, Braga AM, Mathias W Jr, et al. Effects of exercise training in patients with chronic heart failure and sleep apnea. Sleep. 2009;32(5):637-47. PMID: 19480231.-482482 Sengul YS, Ozalevli S, Oztura I, Itil O, Baklan B. The effect of exercise on obstructive sleep apnea: a randomized and controlled trial. Sleep Breath. 2009;15(1):49-56. doi: 10.1007/s11325-009-0311-1.
https://doi.org/10.1007/s11325-009-0311-...
A evidência de que a perda de peso é um importante tratamento para os casos de AOS leve480480 Tuomilehto HP, Seppä JM, Partinen MM, Peltonen M, Gylling H, Tuomilehto JO, et al; Kuopio Sleep Apnea Group. Lifestyle intervention with weight reduction: first-line treatment in mild obstructive sleep apnea. Am J Respir Crit Care Med. 2009;179(4):320-7. doi: 10.1164/rccm.200805-669OC.
https://doi.org/10.1164/rccm.200805-669O...
e um adjuvante ao uso do CPAP484484 Chirinos JA, Gurubhagavatula I, Teff K, Rader DJ, Wadden TA, Townsend R, et al. CPAP, weight loss, or both for obstructive sleep apnea. N Engl J Med. 2014;370(24):2265-75. doi: 10.1056/NEJMoa1306187.
https://doi.org/10.1056/NEJMoa1306187...
em parâmetros metabólicos e cardiovasculares reforça o papel do educador físico no manejo da AOS.
8.3. Nutrição
Como bem estabelecido, um dos maiores fatores para a AOS é a obesidade. Outro ponto a ser destacado na AOS que pode servir como um ciclo vicioso: por não conseguir ter um sono reparador, o paciente pode apresentar elevações do cortisol, favorecendo a compulsão alimentar, principalmente por carboidratos refinados. Neste caso, a saciedade fica prejudicada, e o paciente começa a comer mais sem perceber. Desta forma, uma alimentação adequada e saudável pode promover redução do peso e melhorar a gravidade da AOS,6262 Peppard PE, Young T, Palta M, Dempsey J, Skatrud J. Longitudinal study of moderate weight change and sleep-disordered breathing. JAMA. 2000;284(23):3015-21. PMID: 11122588.,480480 Tuomilehto HP, Seppä JM, Partinen MM, Peltonen M, Gylling H, Tuomilehto JO, et al; Kuopio Sleep Apnea Group. Lifestyle intervention with weight reduction: first-line treatment in mild obstructive sleep apnea. Am J Respir Crit Care Med. 2009;179(4):320-7. doi: 10.1164/rccm.200805-669OC.
https://doi.org/10.1164/rccm.200805-669O...
além de ter um efeito metabólico e cardiovascular adjuvante ao CPAP, conforme já destacado na seção anterior.484484 Chirinos JA, Gurubhagavatula I, Teff K, Rader DJ, Wadden TA, Townsend R, et al. CPAP, weight loss, or both for obstructive sleep apnea. N Engl J Med. 2014;370(24):2265-75. doi: 10.1056/NEJMoa1306187.
https://doi.org/10.1056/NEJMoa1306187...
Outro dado curioso na área de nutrição e sono: embora exista evidência de que uma dieta gordurosa pode prejudicar a qualidade do sono e contribuir para a piorar a AOS,485485 Trakada G, Steiropoulos P, Zarogoulidis P, Nena E, Papanas N, Maltezos E, t al. A fatty meal aggravates apnea and increases sleep in patients with obstructive sleep apnea. Sleep Breath. 2014;18(1):53-8. doi: 10.1007/s11325-013-0847-y.
https://doi.org/10.1007/s11325-013-0847-...
novos estudos são necessários.
8.4. Fonoaudiologia
A terapia fonoaudiológica para tratamento dos distúrbios respiratórios do sono atua na adequação da musculatura da via aérea superior. Quando o enfoque é dado na região orofarígea, reduz os eventos de apneia e hipopneia e/ou auxilia na adaptação ao CPAP. Quando o enfoque é na musculatura mandibular, auxilia na adaptação de placas de avanço mandibular, naqueles pacientes com AOS e desordens temporomandibulares, além de reduzir queixas de dores e melhorar na adesão ao tratamento, na qualidade de vida e de sono.486486 Cunali PA, Almeida FR, Santos CD, Valdrichi NY, Nascimento LS, Dal-Fabbro C, et al. Mandibular exercises improve mandibular advancement devide therapy for obstructive sleep apnea. Sleep Breath. 2011;15(4):717-27. doi: 10.1007/s11325-010-0428-2.
https://doi.org/10.1007/s11325-010-0428-...
Atualmente, a fonoaudiologia possui diversas áreas de atuação; a motricidade orofacial, por exemplo, é o campo voltado para estudo, pesquisa, prevenção, avaliação, diagnóstico, desenvolvimento, habilitação, aperfeiçoamento e reabilitação dos aspectos estruturais e funcionais das regiões orofacial e cervical. Esta área possui estudos recentes, que comprovam a eficácia da terapia fonoaudiológica em paciente com AOS. Estudos brasileiros, iniciados por Guimarães et al.,487487 Guimarães KC, Drager LF, Genta PR, Marcondes BF, Lorenzi-Filho G. Effects of oropharyngeal exercises on patients with moderate obstructive sleep apnea syndrome. Am J Respir Crit Care Med. 2009;179(10):962-6. doi: 10.1164/rccm.200806-981OC.
https://doi.org/10.1164/rccm.200806-981O...
Ieto et al.,488488 Ieto V, Kayamori F, Montes MI, Hirata RP, Gregório MG, Alencar AM, et al. Effects of oropharyngeal exercises on snoring: a randomized trial. Chest. 2015;148(3):683-91. doi: 10.1378/chest.14-2953
https://doi.org/10.1378/chest.14-2953...
e Diaféria et al.,489489 Diaferia G, Badke L, Santos-Silva R, Bommarito S, Tufik S, Bittencourt L. Effect of speech therapy as adjunct treatment to continuous positive airway pressure on the quality of life of patients with obstructive sleep apnea. Sleep Med. 2013;14(7):628-35. doi: 10.1016/j.sleep.2013.03.016.
https://doi.org/10.1016/j.sleep.2013.03....
mostraram que a terapia com exercícios orofaríngeos em pacientes com ronco primário e AOS leve a moderada foi capaz de reduzir em aproximadamente 50% o IAH. Estes estudos demonstraram redução na intensidade e na frequência do ronco, e melhora na sonolência diurna e na qualidade do sono.487487 Guimarães KC, Drager LF, Genta PR, Marcondes BF, Lorenzi-Filho G. Effects of oropharyngeal exercises on patients with moderate obstructive sleep apnea syndrome. Am J Respir Crit Care Med. 2009;179(10):962-6. doi: 10.1164/rccm.200806-981OC.
https://doi.org/10.1164/rccm.200806-981O...
488 Ieto V, Kayamori F, Montes MI, Hirata RP, Gregório MG, Alencar AM, et al. Effects of oropharyngeal exercises on snoring: a randomized trial. Chest. 2015;148(3):683-91. doi: 10.1378/chest.14-2953
https://doi.org/10.1378/chest.14-2953...
-489489 Diaferia G, Badke L, Santos-Silva R, Bommarito S, Tufik S, Bittencourt L. Effect of speech therapy as adjunct treatment to continuous positive airway pressure on the quality of life of patients with obstructive sleep apnea. Sleep Med. 2013;14(7):628-35. doi: 10.1016/j.sleep.2013.03.016.
https://doi.org/10.1016/j.sleep.2013.03....
Também a terapia fonoaudiológica concomitante ao uso do CPAP, auxilia objetivamente na melhora da adesão ao CPAP.489489 Diaferia G, Badke L, Santos-Silva R, Bommarito S, Tufik S, Bittencourt L. Effect of speech therapy as adjunct treatment to continuous positive airway pressure on the quality of life of patients with obstructive sleep apnea. Sleep Med. 2013;14(7):628-35. doi: 10.1016/j.sleep.2013.03.016.
https://doi.org/10.1016/j.sleep.2013.03....
,490490 Diaféria G, Santos-Silva R, Truksinas E, Haddad FL, Santos R, Bommarito S, et al. Myofunctional therapy improves adherence to continuous positive airway pressure treatment. Sleep Breath. 2017;21(2):387-395. doi: 10.1007/s11325-016-1429-6.
https://doi.org/10.1007/s11325-016-1429-...
8.5. Enfermagem
A atuação da enfermagem neste cenário é de fornecer as orientações necessárias aos pacientes sobre os exames diagnósticos, àqueles com diagnóstico definido e aos que estão em tratamento com o CPAP.491491 Weaver TE, Grunstein RR. Adherence to continuous positive airway pressure therapy: the challenge to effective treatment. Proc Am Thorac Soc. 2008;5(2):173-8. doi: 10.1513/pats.200708-119MG.
https://doi.org/10.1513/pats.200708-119M...
A função educativa do enfermeiro melhora significativamente a adesão ao uso do CPAP, pois conscientiza o indivíduo sobre as consequências deletérias da AOS, tornando-o figura ativa no tratamento.492492 Hoy CJ, Vennelle M, Kingshott RN, Engleman HM, Douglas NJ. Can intensive support improve continuous positive airway pressure use in patients with the sleep apnea/hypopnea syndrome? Am J Respir Crit Care Med. 1999;159(4 Pt 1):1096-100. doi: 10.1164/ajrccm.159.4.9808008.
https://doi.org/10.1164/ajrccm.159.4.980...
Idealmente, todo paciente que irá iniciar o uso do CPAP deve passar por uma consulta com um enfermeiro do sono para receber orientações sobre sua doença, objetivos do tratamento e, reforçar a necessidade do uso correto do CPAP, o que aumenta a adesão ao tratamento.493493 Richards D, Bartlett DJ, Wong K, Malouff J, Grunstein RR. Increased adherence to CPAP with a group cognitive behavioral treatment intervention: a randomized trial. Sleep. 2007;30(5):635-40. PMID: 17552379. Em situações que o paciente desenvolve lesão de pele secundária ao uso do CPAP, é papel do enfermeiro orientar adequadamente sobre o tratamento curativo e preventivo destas úlceras. O enfermeiro do sono deve sistematizar suas práticas, bem como possuir conhecimento específico para estimular os pacientes à continuidade do tratamento. A adesão ao tratamento e a qualidade do plano terapêutico são os focos da atuação do enfermeiro nos distúrbios de sono, que têm como objetivo final melhorar os desfechos relacionados à doença e suas complicações, além da saúde como um todo.
8.6. Odontologia
Os Aparelhos de Avanço Mandibular (AAM) constituem um dos tratamentos mais comuns e eficazes para tratamento da AOS. O aparelho intraoral é o mais comumente utilizado, pois mantém a mandíbula em uma posição avançada e fechada durante o sono. Embora tanto ao CPAP quanto os AAM melhorem a estabilidade das vias aéreas e reduzam seu colapso durante o sono, eles diferem em termos de eficácia, custo, conforto e efeitos colaterais.494494 Almeida FR, Henrich N, Marra C, Lynd LD, Lowe AA, Tsuda H, et al. Patient preferences and experiences of CPAP and oral appliances for the treatment of obstructive sleep apnea: a qualitative analysis. Sleep Breath. 2013 May;17(2):659-66. doi: 10.1007/s11325-012-0739-6.
https://doi.org/10.1007/s11325-012-0739-...
De acordo com as diretrizes da AASM,495495 Kushida CA, Morgenthaler TI, Littner MR, Alessi CA, Bailey D, Coleman J Jr, et al; American Academy of Sleep. Practice parameters for the treatment of snoring and Obstructive Sleep Apnea with oral appliances: an update for 2005. Sleep. 2006;29(2):240-3. PMID: 16494092. AAM são recomendados na população adulta como opção terapêutica de primeira linha para pacientes com ronco primário (sem apneia) e para pacientes com AOS leve à moderada que não se adaptaram ao CPAP.495495 Kushida CA, Morgenthaler TI, Littner MR, Alessi CA, Bailey D, Coleman J Jr, et al; American Academy of Sleep. Practice parameters for the treatment of snoring and Obstructive Sleep Apnea with oral appliances: an update for 2005. Sleep. 2006;29(2):240-3. PMID: 16494092. Além disso, AAM e CPAP também podem ser utilizados em conjunto, de modo que o paciente tenderá a utilizá-los alternadamente, aumentando sua adesão aos tratamentos.496496 Almeida FR, Mulgrew A, Ayas N, Tsuda H, Lowe AA, Fox N, et al. Mandibular advancement splint as short-term alternative treatment in patients with obstructive sleep apnea already effectively treated with continuous positive airway pressure. J Clin Sleep Med. 2013;9(4):319-24. doi: 10.5664/jcsm.2576.
https://doi.org/10.5664/jcsm.2576...
O papel do dentista no tratamento da AOS é coadjuvante e complementar ao proporcionado pelo médico especialista em sono.497497 Fleetham J, Almeida FR. Oral appliances and appliances and surgical techniques for obstructive sleep apnea syndrome therapy. [Accessed in 2017 May 05]. Available from: http://neupsykey.com/oral-appliances-and-surgical-techniques-fr-obstructive-sleep-apnea-syndrome-therapy.
http://neupsykey.com/oral-appliances-and...
Um dentista deve fornecer terapia com aparelhos intraorais somente após receber a solicitação por escrito ou a prescrição de um médico, mesmo que seja para ronco primário.498498 Gauthier L, Almeida F, Arcache JP, Ashton-McGregor C, Coté D, Driver HS, et al. Position paper by Canadian dental sleep medicine professionals on the role of different health care professionals in managing OSA and snoring with oral appliances. Can Respir J. 2012;19(5):307-9. PMID: 23061075. O dentista então deve escolher o aparelho ideal para o paciente, que deve ser customizado e possa ser titulado, proporcionando avanços progressivos da mandíbula.
Após a titulação do AAM, o encaminhamento dos pacientes para acompanhamento e avaliação médica, além de um novo estudo do sono são necessários, a fim de verificar a eficácia do tratamento e seus benefícios,499499 Almeida FR, Lowe AA. Principles of oral appliance therapy for the management of snoring and sleep disordered breathing. Oral Maxillofac Surg Clin North Am. 2009;21(4):413-20. doi: 10.1016/j.coms.2009.07.002.
https://doi.org/10.1016/j.coms.2009.07.0...
pois os aparelhos intraorais podem agravar a AOS em alguns pacientes, apesar da melhora dos sintomas, o que foi comprovado em alguns estudos que mostraram importante efeito placebo deste tipo de terapia.500500 Mehta A, Qian J, Petocz P, Darendeliler MA, Cistulli PA. A randomized, controlled study of a mandibular advancement splint for obstructive sleep apnea. Am J Respir Crit Care Med 2001;163(6):1457-61. doi: 10.1164/ajrccm.163.6.2004213.
https://doi.org/10.1164/ajrccm.163.6.200...
O acompanhamento com polissonografia não é indicado para pacientes com ronco primário,499499 Almeida FR, Lowe AA. Principles of oral appliance therapy for the management of snoring and sleep disordered breathing. Oral Maxillofac Surg Clin North Am. 2009;21(4):413-20. doi: 10.1016/j.coms.2009.07.002.
https://doi.org/10.1016/j.coms.2009.07.0...
a menos que os sintomas piorem ou o tratamento não traga melhora. Recomenda-se a manutenção de uma comunicação regular por escrito com o médico do paciente e outros profissionais de saúde sobre o plano de tratamento, o progresso e o acompanhamento em longo prazo a pacientes sendo tratado com AAM.
8.7. Psicologia
O papel da Psicologia no manejo dos distúrbios de sono é destacado principalmente para a área de insônia. O tratamento geral da insônia usualmente requer abordagem integrada do paciente, que incluiu intervenções psicológicas e comportamentais. A chamada Terapia Cognitiva Comportamental (TCC) permite acessar alvos específicos relacionados à insônia, e tem sido amplamente recomendada e utilizada para o tratamento desta condição. Ela engloba diferentes estratégias, incluindo terapia de controle de estímulos, higiene do sono e treinamento em relaxamento, entre outros.501501 Cunnington D, Junge M. Chronic insomnia: diagnosis and non-pharmacological management. BMJ. 2016;355:i5819. doi: 10.1136/bmj.i5819.
https://doi.org/10.1136/bmj.i5819...
Diversas metanálises demonstram o valor da TCC tanto para o tratamento da insônia crônica quanto para o auxílio na retirada do uso de medicamentos cronicamente usados para a insônia.502502 van Straten A, van der Zweerde T, Kleiboer A, Cuijpers P, Morin CM, Lancee J. Cognitive and behavioral therapies in the treatment of insomnia: A meta-analysis. Sleep Med Rev. 2017 Feb 9. pii: S1087-0792(17)30034-5. doi: 10.1016/j.smrv.2017.02.001. [Epub ahead of print].
https://doi.org/10.1016/j.smrv.2017.02.0...
503 Trauer JM, Qian MY, Doyle JS, Rajaratnam SM, Cunnington D. Cognitive Behavioral Therapy for Chronic Insomnia: a systematic review and meta-analysis. Ann Intern Med. 2015;163(3):191-204. doi: 10.7326/M14-2841.
https://doi.org/10.7326/M14-2841...
-504504 Zachariae R, Lyby MS, Ritterband LM, O'Toole MS. Efficacy of internet-delivered cognitive-behavioral therapy for insomnia - A systematic review and meta-analysis of randomized controlled trials. Sleep Med Rev. 2016 Dec;30:1-10. doi: 10.1016/j.smrv.2015.10.004.
https://doi.org/10.1016/j.smrv.2015.10.0...
No entanto, é importante que este profissional seja devidamente treinado nesta técnica para oferecer real benefício aos pacientes.
9. Considerações Finais
Este primeiro Posicionamento Brasileiro sobre o Impacto dos Distúrbios de Sono nas Doenças Cardiovasculares procurou, de forma objetiva, colocar não só o Cardiologista a par das evidêncas atuais desta importante área de pesquisa, bem como fornecer recomendações guiadas principalmente no oferecimento de melhoras no reconhecimento e tratamento dos distúrbios de sono. Muito desenvolvimento foi alcançado nas últimas décadas, mas muitas áreas ainda requerem mais estudos, antes que conclusões definitivas possam ser adequadamente colocadas.505505 Drager LF, McEvoy RD, Barbe F, Lorenzi-Filho G, Redline S; INCOSACT Initiative (International Collaboration of Sleep Apnea Cardiovascular Trialists). Sleep Apnea and Cardiovascular Disease: Lessons From Recent Trials and Need for Team Science. Circulation. 2017;136(19):1840-1850. doi: 10.1161/CIRCULATIONAHA.117.029400.
https://doi.org/10.1161/CIRCULATIONAHA.1...
9.1. Afinal Qual Deve Ser o Papel do Cardiologista no Manejo dos Distúrbios de Sono?
No geral, o cardiologista terá um importante papel se ele aumentar a atenção para os distúrbios de sono durante o dia a dia do consultório e encaminhar os pacientes para um tratamento apropriado com um especialista em Medicina do Sono. Isto porque os pacientes precisam ser avaliados individualmente, e o tratamento da AOS não se limita somente ao uso do CPAP. Existem importantes desafios nesta área, por dificuldade de adaptação e uso a longo prazo deste tratamento, com base nas evidências de que isto pode ter influenciado resultados neutros de alguns dos grandes estudos randomizados da área. No campo da insônia, conhecemos os desafios do uso crônico de indutores do sono e as dificuldades para o “desmame” destes tratamentos não isentos de riscos. Neste sentido, fazer parcerias com especialistas na área de Medicina do Sono pode garantir efetividade no tratamento destes distúrbios, trazendo, em últuima análise, benefício para a qualidade de vida e, em alguns casos, melhora do prognóstico cardiovascular para os pacientes. A figura 6 mostra uma proposta de atuação do Cardiologista em parceria com o especialista em Medicina do Sono no manejo dos distúrbios respiratórios do sono.
Proposta de atuação do cardiologista no manejo dos distúrbios respiratórios de sono (apneia obstrutiva do sono (AOS) e apneia central). * Questionários de triagem para a AOS (Berlim, NoSAS). Em algumas condições clínicas, como na hipertensão arterial sistêmica resistente e pacientes pós-infarto, o questionário de Berlim não é acurado em triar a AOS;# se o cardiologista tiver dúvida sobre qual exame pedir, encaminhar para o especialista logo após a suspeita diagnóstica; & casos selecionados. Em crianças, a cirurgia é muito utilizada no tratamento da AOS.
Para os demais distúrbios de sono, o encaminhamento precoce para o especialista pode evitar complicações, como dependência química de medicamentos para a insônia.
Por fim, para o cardiologista interessado em se aprofundar nesta área e tendo o título de especialista em Clínica Médica pela Associação Médica Brasileira (estamos em processo de solicitação para a Cardiologia), será possível aplicar para ter o Certificado na área de atuação em Medicina do Sono, após, obviamente, experiência comprovada na área (em breve, com exigência de residência médica de 1 ano de duração).
-
Nota: estas Diretrizes se prestam a informar e não a substituir o julgamento clínico do médico que, em última análise, deve determinar o tratamento apropriado para seus pacientes.
-
Errata
Considerar correta a seguinte numeração de página do sumário para os itens: onde lê-se pág. 3, considerar 292; respectivamente: 4, 293; 5, 294; 6, 295; 7, 296; 8, 297; 10, 299; 12, 301; 13, 302; 14, 303; 15, 304; 16, 305; 17, 306; 18, 307; 19, 308; 20, 309; 21, 310; 22, 311; 23, 312; 24, 313; 25, 314; 28, 317; 29, 318; 30, 319; 31, 320; 32, 321; 33, 322; 24, 323.
Referências
-
1Berry RB, Brooks R, Gamaldo CE, Harding SM, Lloyd RM, Marcus CL, et al. American Academy of Sleep Medicine. The AASM Manual for the Scoring of Sleep and Associated Events: Rules, Terminology and Technical Specifications, Version 2.3. www.aasmnet.org Darien, Illinois: American Academy of Sleep Medicine; 2016.
» www.aasmnet.org -
2American Academy of Sleep Medicine, International Classification of Sleep Disorders. 3rd ed. Darien, Illinois; 2014.
-
3Littner MR, Kushida C, Wise M, Davila DG, Morgenthaler T, Lee-Chiong T, et al; Standards of Practice Committee of the American Academy of Sleep Medicine. Practice parameters for clinical use of the multiple sleep latency test and the maintenance of wakefulness test. Sleep. 2005;28(1):113-21. PMID: 15700727.
-
4Young T, Palta M, Dempsey J, Skatrud J, Weber S, Badr S. The occurrence of sleep-disordered breathing among middle-aged adults. N Engl J Med. 1993;328(17):1230-5. doi: 10.1056/NEJM199304293281704.
» https://doi.org/10.1056/NEJM199304293281704 -
5Bearpark H, Elliott L, Grunstein R, Cullen S, Schneider H, Althaus W, et al. Snoring and sleep apnea: a population study in Australian men. Am J Respir Crit Care Med. 1995;151(5):1459-65. doi: 10.1164/ajrccm.151.5.7735600.
» https://doi.org/10.1164/ajrccm.151.5.7735600 -
6Bixler EO, Vgontzas AN, Ten Have T, Tyson K, Kales A. Effects of age on sleep apnea in men: I. Prevalence and severity. Am J Respir Crit Care Med. 1998;157(1):144-8. doi: 10.1164/ajrccm.157.1.9706079.
» https://doi.org/10.1164/ajrccm.157.1.9706079 -
7Bixler EO, Vgontzas AN, Lin HM, Ten Have T, Rein J, Vela-Bueno A, et al. Prevalence of sleep-disordered breathing in women: effects of gender. Am J Respir Crit Care Med. 2001;163(3 Pt 1):608-13. doi: 10.1164/ajrccm.163.3.9911064.
» https://doi.org/10.1164/ajrccm.163.3.9911064 -
8Durán J, Esnaola S, Rubio R, Iztueta A. Obstructive sleep apnea-hypopnea and related clinical features in a population-based sample of subjects aged 30 to 70 yr. Am J Respir Crit Care Med. 2001;163(3 Pt 1):685-9. doi: 10.1164/ajrccm.163.3.2005065.
» https://doi.org/10.1164/ajrccm.163.3.2005065 -
9Ip MS, Lam B, Lauder IJ, Tsang KW, Chung KF, Mok YW, et al. A community study of sleep-disordered breathing in middle-aged Chinese men in Hong Kong. Chest. 2001;119(1):62-9. PMID: 11157585.
-
10Ip MS, Lam B, Tang LC, Lauder IJ, Ip TY, Lam WK. A community study of sleep-disordered breathing in middle-aged Chinese women in Hong Kong: prevalence and gender differences. Chest. 2004;125(1):127-34. PMID: 14718431.
-
11Kim J, In K, Kim J, You S, Kang K, Shim J, et al. Prevalence of sleep-disordered breathing in middle-aged Korean men and women. Am J Respir Crit Care Med. 2004;170(10):1108-13. doi: 10.1164/rccm.200404-519OC.
» https://doi.org/10.1164/rccm.200404-519OC -
12Udwadia ZF, Doshi AV, Lonkar SG, Singh CI. Prevalence of sleep disordered breathing and sleep apnea in middle-aged urban Indian men. Am J Respir Crit Care Med. 2004;169(2):168-73. doi: 10.1164/rccm.200302-265OC.
» https://doi.org/10.1164/rccm.200302-265OC -
13Sharma SK, Kumpawat S, Banga A, Goel A. Prevalence and risk factors of obstructive sleep apnea syndrome in a population of Delhi, India. Chest. 2006;130(1):149-56. doi: 10.1378/chest.130.1.149.
» https://doi.org/10.1378/chest.130.1.149 -
14Tufik S, Santos-Silva R, Taddei JA, Bittencourt LR. Obstructive sleep apnea syndrome in the Sao Paulo Epidemiologic Sleep Study. Sleep Med. 2010;11(5):441-6. doi: 10.1016/j.sleep.2009.10.005.
» https://doi.org/10.1016/j.sleep.2009.10.005 -
15Peppard PE, Young T, Barnet JH, Palta M, Hagen EW, Hla KM. Increased prevalence of sleep-disordered breathing in adults. Am J Epidemiol. 2013;177(9):1006-14. doi: 10.1093/aje/kws342.
» https://doi.org/10.1093/aje/kws342 -
16Heinzer R, Vat S, Marques-Vidal P, Marti-Soler H, Andries D, Tobback N, et al. Prevalence of sleep-disordered breathing in the general population: the HypnoLaus study. Lancet Respir Med. 2015;3(4):310-8. doi: 10.1016/S2213-2600(15)00043-0
» https://doi.org/10.1016/S2213-2600(15)00043-0 -
17Young T, Evans L, Finn L, Palta M. Estimation of the clinically diagnosed proportion of sleep apnea syndrome in middle-aged men and women. Sleep. 1997;20(9):705-6. PMID: 9406321.
-
18Worsnop CJ, Naughton MT, Barter CE, Morgan TO, Anderson AI, Pierce RJ. The prevalence of obstructive sleep apnea in hypertensives. Am J Respir Crit Care Med. 1998;157(1):111-5. doi: 10.1164/ajrccm.157.1.9609063.
» https://doi.org/10.1164/ajrccm.157.1.9609063 -
19Sjöström C, Lindberg E, Elmasry A, Hägg A, Svärdsudd K, Janson C. Prevalence of sleep apnea and snoring in hypertensive men: a population based study. Thorax. 2002;57(7):602-7. PMID: 12096203.
-
20Drager LF, Genta PR, Pedrosa RP, Nerbass FB, Gonzaga CC, Krieger EM, et al. Characteristics and predictors of obstructive sleep apnea in patients with systemic hypertension. Am J Cardiol. 2010;105(8):1135-9. doi: 10.1016/j.amjcard.2009.12.017.
» https://doi.org/10.1016/j.amjcard.2009.12.017 -
21Logan AG, Perlikowski SM, Mente A, Tisler A, Tkacova R, Niroumand M, et al. High prevalence of unrecognized sleep apnea in drug-resistant hypertension. J Hypertens. 2001;19(12):2271-7. PMID: 11725173.
-
22Gonçalves SC, Martinez D, Gus M, de Abreu-Silva EO, Bertoluci C, Dutra I, et al. Obstructive sleep apnea and resistant hypertension: a case-control study. Chest. 2007;132(6):1858-62. doi: 10.1378/chest.07-1170.
» https://doi.org/10.1378/chest.07-1170 -
23Pedrosa RP, Drager LF, Gonzaga CC, Sousa MG, de Paula LK, Amaro AC, et al. Obstructive sleep apnea: the most common secondary cause of hypertension associated with resistant hypertension. Hypertension. 2011;58(5):811-7. doi: 10.1161/HYPERTENSIONAHA.111.179788
» https://doi.org/10.1161/HYPERTENSIONAHA.111.179788 -
24Muxfeldt ES, Margallo VS, Guimarães GM, Salles GF. Prevalence and associated factors of obstructive sleep apnea in patients with resistant hypertension. Am J Hypertens. 2014;27(8):1069-78. doi: 10.1093/ajh/hpu023.
» https://doi.org/10.1093/ajh/hpu023 -
25Peppard PE, Young T, Palta M, Skatrud J. Prospective study of the association between sleep-disordered breathing and hypertension. N Engl J Med. 2000;342(19):1378-84. doi: 10.1056/NEJM200005113421901.
» https://doi.org/10.1056/NEJM200005113421901 -
26O'Connor GT, Caffo B, Newman AB, Quan SF, Rapoport DM, Redline S, et al. Prospective study of sleep-disordered breathing and hypertension: the Sleep Heart Health Study. Am J Respir Crit Care Med. 2009;179(12):1159-64. doi: 10.1164/rccm.200712-1809OC.
» https://doi.org/10.1164/rccm.200712-1809OC -
27Haas DC, Foster GL, Nieto FJ, Redline S, Resnick HE, Robbins JA, et al. Age-dependent associations between sleep-disordered breathing and hypertension: importance of discriminating between systolic/diastolic hypertension and isolated systolic hypertension in the Sleep Heart Health Study. Circulation. 2005;111(5):614-21. doi: 10.1161/01.CIR.0000154540.62381.CF.
» https://doi.org/10.1161/01.CIR.0000154540.62381.CF -
28Mehra R, Stone KL, Blackwell T, Ancoli Israel S, Dam TT, Stefanick ML, et al. Prevalence and correlates of sleep-disordered breathing in older men: osteoporotic fractures in men sleep study. J Am Geriatr Soc. 2007;55(9):1356-64. doi: 10.1111/j.1532-5415.2007.01290.x.
» https://doi.org/10.1111/j.1532-5415.2007.01290.x -
29Andreas S, Schulz R, Werner GS, Kreuzer H. Prevalence of obstructive sleep apnoea in patients with coronary artery disease. Coron Artery Dis. 1996;7(7):541-5. PMID: 8913673.
-
30Mehra R, Principe-Rodriguez K, Kirchner HL, Strohl KP. Sleep apnea in acute coronary syndrome: high prevalence but low impact on 6-month outcome. Sleep Med. 2006;7(6):521-8. doi: 10.1016/j.sleep.2006.03.012.
» https://doi.org/10.1016/j.sleep.2006.03.012 -
31Lee CH, Khoo SM, Tai BC, Chong EY, Lau C, Than Y, et al. Obstructive sleep apnea in patients admitted for acute myocardial infarction: prevalence, predictors, and effect on microvascular perfusion. Chest. 2009;135(6):1488-95. doi: 10.1378/chest.08-2336.
» https://doi.org/10.1378/chest.08-2336 -
32Danzi-Soares NJ, Genta PR, Nerbass FB, Pedrosa RP, Soares FS, César LA, et al. Obstructive sleep apnea is common among patients referred for coronary artery bypass grafting and can be diagnosed by portable monitoring. Coron Artery Dis. 2012;23(1):31-8. doi: 10.1097/MCA.0b013e32834df5d0.
» https://doi.org/10.1097/MCA.0b013e32834df5d0 -
33Geovanini GR, Gowdak LH, Pereira A, Danzi-Soares N, Dourado L, Poppi N, et al. OSA and depression are common and independently associated with refractory angina in patients with coronary artery disease. Chest. 2014;146(1):73-80. doi: 10.1378/chest.13-2885.
» https://doi.org/10.1378/chest.13-2885 -
34Sorajja D, Gami AS, Somers VK, Behrenbeck TR, Garcia-Touchard A, Lopez-Jimenez F. Independent association between obstructive sleep apnea and subclinical coronary artery disease. Chest. 2008;133(4):927-33. doi: 10.1378/chest.07-2544.
» https://doi.org/10.1378/chest.07-2544 -
35Shahar E, Whitney CW, Redline S, Lee ET, Newman AB, Nieto FJ, et al. Sleep-disordered breathing and cardiovascular disease: cross-sectional results of the Sleep Heart Health Study. Am J Respir Crit Care Med. 2001;163(1):19-25. doi: 10.1164/ajrccm.163.1.2001008.
» https://doi.org/10.1164/ajrccm.163.1.2001008 -
36Gottlieb DJ, Yenokyan G, Newman AB, O'Connor GT, Punjabi NM, Quan SF, et al. Prospective study of obstructive sleep apnea and incident coronary heart disease and heart failure: the sleep heart health study. Circulation. 2010;122(4):352-60. doi: 10.1161/CIRCULATIONAHA.109.901801
» https://doi.org/10.1161/CIRCULATIONAHA.109.901801 -
37Javaheri S. Sleep disorders in systolic heart failure: a prospective study of 100 male patients. The final report. Int J Cardiol. 2006;106(1):21-8. doi: 10.1016/j.ijcard.2004.12.068.
» https://doi.org/10.1016/j.ijcard.2004.12.068 -
38Yumino D, Wang H, Floras JS, Newton GE, Mak S, Ruttanaumpawan P, et al. Prevalence and physiological predictors of sleep apnea in patients with heart failure and systolic dysfunction. J Card Fail. 2009;15(4):279-85. doi: 10.1016/j.cardfail.2008.11.015.
» https://doi.org/10.1016/j.cardfail.2008.11.015 -
39Khayat RN, Jarjoura D, Patt B, Yamokoski T, Abraham WT. In-hospital testing for sleep-disordered breathing in hospitalized patients with decompensated heart failure: report of prevalence and patient characteristics. J Card Fail. 2009;15(9):739-46. doi: 10.1016/j.cardfail.2009.05.005.
» https://doi.org/10.1016/j.cardfail.2009.05.005 -
40Oldenburg O, Lamp B, Faber L, Teschler H, Horstkotte D, Topfer V. Sleep-disordered breathing in patients with symptomatic heart failure: a contemporary study of prevalence in and characteristics of 700 patients. Eur J Heart Fail. 2007;9(3):251-7. doi: 10.1016/j.ejheart.2006.08.003.
» https://doi.org/10.1016/j.ejheart.2006.08.003 -
41Paulino A, Damy T, Margarit L, Stoïca M, Deswarte G, Khouri L, et al. Prevalence of sleep-disordered breathing in a 316-patient French cohort of stable congestive heart failure. Arch Cardiovasc Dis. 2009;102(3):169-75. doi: 10.1016/j.acvd.2008.12.006.
» https://doi.org/10.1016/j.acvd.2008.12.006 -
42Silva RS, Figueiredo AC, Mady C, Lorenzi Filho G. Breathing disorders in congestive heart failure: gender, etiology and mortality. Braz J Med Biol Res. 2008;41(3):215-22. PMID: 18575711.
-
43Javaheri S, Shukla R, Zeigler H, Wexler L. Central sleep apnea, right ventricular dysfunction, and low diastolic blood pressure are predictors of mortality in systolic heart failure. J Am Coll Cardiol. 2007;49(20):2028-34. doi: 10.1016/j.jacc.2007.01.084.
» https://doi.org/10.1016/j.jacc.2007.01.084 -
44Bitter T, Faber L, Hering D, Langer C, Horstkotte D, Oldenburg O. Sleep-disordered breathing in heart failure with normal left ventricular ejection fraction. Eur J Heart Fail. 2009;11(6):602-8. doi: doi: 10.1093/eurjhf/hfp057.
» https://doi.org/10.1093/eurjhf/hfp057 -
45Porthan KM, Melin JH, Kupila JT, Venho KK, Partinen MM. Prevalence of sleep apnea syndrome in lone atrial fibrillation: a case-control study. Chest. 2004;125(3):879-85. PMID: 15006945.
-
46Braga B, Poyares D, Cintra F, Guilleminault C, Cirenza C, Horbach S, et al. Sleep-disordered breathing and chronic atrial fibrillation. Sleep Med 2009;10(2):212-6. doi: 10.1016/j.sleep.2007.12.007.
» https://doi.org/10.1016/j.sleep.2007.12.007 -
47Hoyer FF, Lickfett LM, Mittmann-Braun E, Ruland C, Kreuz J, Pabst S, et al. High prevalence of obstructive sleep apnea in patients with resistant paroxysmal atrial fibrillation after pulmonary vein isolation. J Interv Card Electrophysiol. 2010;29(1):37-41. doi: 10.1007/s10840-010-9502-8.
» https://doi.org/10.1007/s10840-010-9502-8 -
48Monahan K, Storfer-Isser A, Mehra R, Shahar E, Mittleman M, Rottman J, et al. Triggering of nocturnal arrhythmias by sleep-disordered breathing events. J Am Coll Cardiol. 2009;54(19):1797-804. doi: 10.1016/j.jacc.2009.06.038.
» https://doi.org/10.1016/j.jacc.2009.06.038 -
49Good D, Henkle J, Gelber D, Welsh J, Verhulst S. Sleep disordered breathing and poor functional outcome after stroke. Stroke. 1996;27(2):252-9. PMID: 8571419.
-
50Dyken M, Somers V, Ymada T, Ren Z, Zimmerman B. Investigating the relationship between stroke and obstructive sleep apnea. Stroke. 1996;27(3):401-7. PMID: 8610303.
-
51Parra O, Arboix A, Bechich S, García-Eroles L, Montserrat JM, López JA, et al. Time course of sleep-related breathing disorders in first-ever stroke or transient ischemic attack. Am J Respir Crit Care Med. 2000;161(2 Pt 1):375-80. doi: 10.1164/ajrccm.161.2.9903139.
» https://doi.org/10.1164/ajrccm.161.2.9903139 -
52Turkington PM, Bamford J, Wanklyn P, Elliott MW. Prevalence and predictors of upper airway obstruction in the first 24 hours after acute stroke. Stroke. 2002;33(8):2037-42. PMID: 12154259.
-
53Hui DS, Choy DK, Wong LK, Ko FW, Li TS, Woo J, et al. Prevalence of sleep-disordered breathing and continuous positive airway pressure compliance: results in chinese patients with first-ever ischemic stroke. Chest. 2002;122(3):852-60. PMID: 12226023.
-
54Joo BE, Seok HY, Yu SW, Kim BJ, Park KW, Lee DH, et al. Prevalence of sleep-disordered breathing in acute ischemic stroke as determined using a portable sleep apnea monitoring device in Korean subjects. Sleep Breath. 2011;15(1):77-82. doi: 10.1007/s11325-009-0325-8.
» https://doi.org/10.1007/s11325-009-0325-8 -
55Yaggi HK, Concato J, Kernan WN, Lichtman JH, Brass LM, Mohsenin V. Obstructive sleep apnea as a risk factor for stroke and death. N Engl J Med. 2005;353(19):2034-41. doi: 10.1056/NEJMoa043104.
» https://doi.org/10.1056/NEJMoa043104 -
56Arzt M, Young T, Finn L, Skatrud JB, Bradley TD. Association of sleep-disordered breathing and the occurrence of stroke. Am J Respir Crit Care Med. 2005;172(11):1447-51. doi: 10.1164/rccm.200505-702OC.
» https://doi.org/10.1164/rccm.200505-702OC -
57Redline S, Yenokyan G, Gottlieb DJ, Shahar E, O'Connor GT, Resnick HE, et al. Obstructive sleep apnea hypopnea and incident stroke: the Sleep Heart Health Study. Am J Respir Crit Care Med. 2010;182(2):269-77. doi: 10.1164/rccm.200911-1746OC.
» https://doi.org/10.1164/rccm.200911-1746OC -
58Javaheri S, Barbe F, Campos-Rodriguez F, Dempsey JA, Khayat R, Javaheri S, et al. Sleep apnea: types, mechanisms, and clinical cardiovascular consequences. J Am Coll Cardiol. 2017;69(7):841-58. doi: 10.1016/j.jacc.2016.11.069.
» https://doi.org/10.1016/j.jacc.2016.11.069 -
59Costa LE, Uchôa CH, Harmon RR, Bortolotto LA, Lorenzi-Filho G, Drager LF. Potential underdiagnosis of obstructive sleep apnoea in the cardiology outpatient setting. Heart. 2015;101(16):1288-92. doi: 10.1136/heartjnl-2014-307276.
» https://doi.org/10.1136/heartjnl-2014-307276 -
60Sleep-related breathing disorders in adults: recommendations for syndrome definition and measurements techniques in clinical research; the report of an American Academy of Sleep Medicine Task Force. Sleep. 1999;22(5):667-89. PMID: 10450601.
-
61Dempsey JA, Veasey SC, Morgan BJ, O'Donnell CP. Pathophysiology of sleep apnea. Physiol Rev. 2010;90(1):47-112. doi: 10.1152/physrev.00043.2008. Erratum in: Physiol Rev. 2010;90(2):797-8.
» https://doi.org/10.1152/physrev.00043.2008 -
62Peppard PE, Young T, Palta M, Dempsey J, Skatrud J. Longitudinal study of moderate weight change and sleep-disordered breathing. JAMA. 2000;284(23):3015-21. PMID: 11122588.
-
63Young T, Finn L, Austin D, Peterson A. Menopausal status and sleep-disordered breathing in the Wisconsin Sleep Cohort Study. Am J Respir Crit Care Med. 2003;167(9):1181-5. doi: 10.1164/rccm.200209-1055OC.
» https://doi.org/10.1164/rccm.200209-1055OC -
64Skjodt NM, Atkar R, Easton PA. Screening for hypothyroidism in sleep apnea. Am J Respir Crit Care Med. 1999;160(2):732-5. doi: 10.1164/ajrccm.160.2.9802051.
» https://doi.org/10.1164/ajrccm.160.2.9802051 -
65Shepertycky MR; Banno K; Kryger MH. Differences between men and women in the clinical presentation of patients diagnosed with obstructive sleep apnea syndrome. Sleep. 2005;28(3):309-14. PMID: 16173651.
-
66Grunstein RR, Ho KY, Sullivan CE. Sleep apnea in acromegaly. Ann Intern Med. 1991;115(7):527-32. PMID: 1883121.
-
67Watanabe T, Isono S, Tanaka A, Tanzawa H, Nishino T. Contribution of body habitus and craniofacial characteristics to segmental closing pressures of the passive pharynx in patients with sleep disordered breathing. Am J Respir Crit Care Med. 2002;165(2):260-5. doi: 10.1164/ajrccm.165.2.2009032.
» https://doi.org/10.1164/ajrccm.165.2.2009032 -
68Zonato AI, Martinho FL Bittencourt LR, de Oliveira Camponês Brasil O, Gregório LC, Tufik S. Head and neck physical examination: comparison between non-apneic and obstructive sleep apnea patients. Laryngoscope. 2005;115(6):1030-4. doi: 10.1097/01.MLG.0000163494.19965.DC.
» https://doi.org/10.1097/01.MLG.0000163494.19965.DC -
69Young T, Peppard PE, Gottlieb DJ. Epidemiology of obstructive sleep apnea: a population health perspective. Am J Respir Cirt Care Med. 2002;165(9):1217-39. PMID: 11991871.
-
70Scanlan MF, Roebuck T, Little PJ, Redman JR, Naughton MT. Effect of moderate alcohol upon obstructive sleep apnoea. Eur Respir J. 2000;16(5):909-13. PMID: 11153591.
-
71Wetter DW, Young TB, Bidwell TR, Badr MS, Palta M. Smoking as a risk factor for sleep-disordered breathing. Arch Intern Med. 1994;154(19):2219-24. PMID: 7944843.
-
72Chokroverty S. Overview of sleep and sleep disorders. Indian J Med Res. 2010 Feb;131:126-40. PMID: 20308738.
-
73Tsai WH, Remmers JE, Brant R, Flemons WW, Davies J, Macarthur C. A decision rule for diagnostic testing in obstructive sleep apnea. Am J Respir Crit Care Med. 2003;167(10):1427-32. doi: 10.1164/rccm.200112-110OC.
» https://doi.org/10.1164/rccm.200112-110OC -
74Engleman HM, Hirst WS Douglas NJ. Under reporting of sleepiness and driving impairment in patients with sleep apnoea/hypopnoea syndrome. J Sleep Res. 1997;6(4):272-5. PMID: 9493528.
-
75Johns MW. A new method for measuring daytime sleepiness: the Epworth sleepiness scale. Sleep. 1991;14(6):540-5. PMID: 1798888.
-
76Bertolazi AN, Fagondes SC, Hoff LS, Pedro VD, Menna-Barreto SS, JohnsMW. Portuguese-language version of the Epworth sleepiness scale: validation for use in Brazil. J Bras Pneumol. 2009;35(9):877-83. PMID: 19820814.
-
77Quan SF, Wright R, Baldwin CM, Kaemingk KL, Goodwin JL, Kuo TF, et al. Obstructive sleep apnea-hypopnea and neurocognitive functioning in the Sleep Heart Health Study. Sleep Med. 2006;7(6):498-507. doi: 10.1016/j.sleep.2006.02.005.
» https://doi.org/10.1016/j.sleep.2006.02.005 -
78Bruin PF, Bagnato MC. Cognitive impairment in obstructive sleep apnea syndrome. J Bras Pneumol. 2010;36(Suppl 2):32-7. doi: http://dx.doi.org/10.1590/51806-37132010001400010
» http://dx.doi.org/10.1590/51806-37132010001400010 -
79Zias N, Bezwada V, Gilman S, Chroneou A. Obstructive sleep apnea and erectile dysfunction: still a neglected risk factor? Sleep Breath. 2009;13(1):3-10. doi: 10.1007/s11325-008-0212-8.
» https://doi.org/10.1007/s11325-008-0212-8 -
80Rains JC, Poceta JS. Headache and sleep disorders: review and clinical implications for headache management. Headache. 2006;46(9):1344-61. doi: 10.1111/j.1526-4610.2006.00578.x.
» https://doi.org/10.1111/j.1526-4610.2006.00578.x -
81Mohsenin V. Gender differences in the expression of sleep-disordered breathing. Role of upper airway dimensions. Chest. 2001;120(5):1442-7. PMID: 11713117.
-
82Epstein LJ, Kristo D, Strollo PJ Jr, Friedman N, Malhotra A, Patil SP, et al; Adult Obstructive Sleep Apnea Task Force of the American Academy of Sleep Medicine. Clinical guideline for the evaluation, management and long-term care of obstructive sleep apnea in adults. J Clin Sleep Med. 2009;5(3):263-76. PMID: 19960649.
-
83Bittencourt LR. Diagnóstico e tratamento da síndrome da apneia obstrutiva do sono (SAOS): Guia Prático. São Paulo: Livraria Médica Paulista; 2008.
-
84Lorenzo C, Williams K, Hunt KJ, Haffner SM. The National Cholesterol Education Program-Adult Treatment Panel III, International Diabetes Federation, and World Health Organization Definitions of the Metabolic Syndrome as Predictors of Incident Cardiovascular Disease and Diabetes. Diabetes Care. 2007;30(1):8-13. doi: 10.2337/dc06-1414.
» https://doi.org/10.2337/dc06-1414 -
85Roumbaux PH, Bertrand B, Boudewyns A, Deron P, Goffart Y, Hassid S, et al; Royal Belgian Society for Ear, Nose, Throat, Head and Neck Surgery. Standard ENT evaluation of sleep-disordered breathing patient: a consensus report. Acta Otorhinolaryngol Belg. 2002;56(2):127-37. PMID: 12092321.
-
86Hoffstein V, Szalai JP. Predictive value of clinical features in diagnosing obstructive sleep apnea. Sleep. 1993;16(2):118-22. PMID: 8446830.
-
87Bianchi MT. Screening for obstructive sleep apnea: bayes weighs in. Open Sleep J. 2009;2:56-9.
-
88Eiseman NA, Westover MB, Mietus JE, Thomas RJ, Bianchi MT. Classification algorithms for predicting sleepiness and sleep apnea severity. J Sleep Res. 2012;21(1):101-12. doi: 10.1111/j.1365-2869.2011.00935.x.
» https://doi.org/10.1111/j.1365-2869.2011.00935.x -
89Chung F, Yegneswaran B, Liao P, Chung SA, Vairavanathan S, Islam S, et al. STOP questionnaire: a tool to screen patients for obstructive sleep apnea. Anesthesiology. 2008,108(5):812-21. doi: 10.1097/ALN.0b013e31816d83e4.
» https://doi.org/10.1097/ALN.0b013e31816d83e4. -
90Abrishami A, Khajehdehi A, Chung F. A systematic review of screening questionnaires for obstructive sleep apnea. Can J Anaesth. 2010;57(5):423-38. doi: 10.1007/s12630-010-9280-x.
» https://doi.org/10.1007/s12630-010-9280-x -
91Netzer NC, Stoohs RA, Netzer CM, Clark K, Strohl KP. Using the Berlin Questionnaire to identify patients at risk for sleep apnea syndrome. Ann Intern Med. 1999;131(7):485-91. PMID: 10507956.
-
92Margallo VS, Muxfeldt ES, Guimarães GM, Salles GF. Diagnostic accuracy of the Berlin questionnaire in detecting obstructive sleep apnea in patients with resistant hypertension. J Hypertens. 2014;32(10):2030-6. doi: 10.1097/HJH.0000000000000297.
» https://doi.org/10.1097/HJH.0000000000000297 -
93Sert Kuniyoshi FH, Zellmer MR, Calvin AD, Lopez-Jimenez F, Albuquerque FN, van der Walt C, et al. Diagnostic accuracy of the Berlin Questionnaire in detecting sleep-disordered breathing in patients with a recent myocardial infarction. Chest. 2011;140(5):1192-7. doi: 10.1378/chest.10-2625.
» https://doi.org/10.1378/chest.10-2625 -
94Marti-Soler H, Hirotsu C, Marques-Vidal P, Vollenweider P, Waeber G, Preisig M, et al. The NoSAS score for screening of sleep-disordered breathing: a derivation and validation study. Lancet Respir Med. 2016;4(9):742-8. doi: 10.1016/S2213-2600(16)30075-3.
» https://doi.org/10.1016/S2213-2600(16)30075-3 -
95Kushida CA, Littner MR, Morgenthaler T, Alessi CA, Bailey D, Coleman J Jr, et al. Practice parameters for the indications for polysomnography and related procedures: an update for 2005. Sleep. 2005;28(4):499-521. PMID: 16171294.
-
96Practice parameters for use of portable recording in the assessment of obstructive sleep apnea. Standards of Practice Committee of the American Sleep Disorders Association. Sleep. 1994;17(4):372-7. PMID: 7973322.
-
97Collop NA, Anderson WM, Boehlecke B, Claman D, Goldberg R, Gottlieb DJ, et al; Portable Monitoring Task Force of the American Academy of Sleep Medicine. Clinical guidelines for the use of unattended portable monitors in the diagnosis of obstructive sleep apnea in adult patients. Portable monitoring task force of the American Academy of Sleep Medicine. J Clin Sleep Med. 2007;3(7):737-47. PMID: 18198809.
-
98Collop NA, Tracy SL, Kapur V, Mehra R, Kuhlmann D, Fleishman SA, et al. Obstructive sleep apnea devices for out-of-center (OOC) testing: technology evaluation. J Clin Sleep Med. 2011;7(5):531-48. doi: 10.5664/JCSM.1328.
» https://doi.org/10.5664/JCSM.1328 -
99Corral J, Sánchez-Quiroga MA, Carmona-Bernal C, Sánchez-Armengol A, Sánchez-de-la-Torre A, Durán-Cantolla J, et al; Spanish Sleep Network. Conventional polysomnography is not necessary for the management of most patients with suspected obstructive sleep apnea. Noninferiority, Randomized Controlled Trial. Am J Respir Crit Care Med. 2017;196(9):1181-1190. doi: 10.1164/rccm.201612-2497OC.
» https://doi.org/10.1164/rccm.201612-2497OC -
100Bibbins-Domingo K, Grossman DC, Curry SJ, Davidson KW, Epling JW Jr, García FA, et al; US Preventive Services Task Force. Screening for obstructive sleep apnea in adults: US Preventive Services Task Force Recommendation Statement. JAMA. 2017;317(4):407-14. doi: 10.1001/jama.2016.20325.
» https://doi.org/10.1001/jama.2016.20325 -
101Weiss JW, Remsburg S, Garpestad E, Ringler J, Sparrow D, Parker JA. Hemodynamic consequences of obstructive sleep apnea. Sleep. 1996;19(5):388-97. PMID: 8843530.
-
102Marin JM, Carrizo SJ, Vicente E, Agusti AG. Long-term cardiovascular outcomes in men with obstructive sleep apnoea-hypopnoea with or without treatment with continuous positive airway pressure: an observational study. Lancet. 2005;365(9464):1046-53. doi: 10.1016/S0140-6736(05)71141-7
» https://doi.org/10.1016/S0140-6736(05)71141-7 -
103O'Donnell CP, Ayuse T, King ED, Schwartz AR, Smith PL, Robotham JL. Airway obstruction during sleep increases blood pressure without arousal. J Appl Physiol (1985). 1996;80(3):773-81. PMID: 8964736.
-
104Poyares D, Guilleminault C, Rosa A, Ohayon M, Koester U. Arousal, EEG spectral power and pulse transit time in UARS and mild OSAS subjects. Clin Neurophysiol. 2002;113(10):1598-606. PMID: 12350436.
-
105Carlson JT, Hedner J, Elam M, Ejnell H, Sellgren J, Wallin BG. Augmented resting sympathetic activity in awake patientes with obstructive sleep apnea. Chest. 1993;103(6):1763-8. PMID: 8404098.
-
106Pressman GS, Orban M, Leinveber P, Parekh K, Singh M, Kara T, et al. Effects of the Mueller maneuver on functional mitral regurgitation and implications for obstructive sleep apnea. Am J Cardiol. 2015;115(11):1563-7. doi: 10.1016/j.amjcard.2015.02.061.
» https://doi.org/10.1016/j.amjcard.2015.02.061 -
107Brinker JA, Weiss JL, Lappe DL, Rabson JL, Summer WR, Permutt S, et al. Leftward septal displacement during right ventricular loading in man. Circulation. 1980;61(3):626-33. PMID: 7353253.
-
108Koshino Y, Villarraga HR, Orban M, Bruce CJ, Pressman GS, Leinveber P, et al. Changes in left and right ventricular mechanics during the Mueller maneuver in healthy adults: a possible mechanism for abnormal cardiac function in patients with obstructive sleep apnea. Circ Cardiovasc Imaging. 2010;3(3):282-9. doi: 10.1161/CIRCIMAGING.109.901561.
» https://doi.org/10.1161/CIRCIMAGING.109.901561 -
109Zamarrón C, Valdés Cuadrado L, Alvarez-Sala R. Pathophysiologic mechanisms of cardiovascular disease in obstructive sleep apnea syndrome. Pulm Med. 2013;2013:521087. doi: 10.1155/2013/521087.
» https://doi.org/10.1155/2013/521087 -
110Fletcher EC, Bao G, Miller CC 3rd. Effect of recurrent episodic hypocapnic, eucapnic, and hypercapnic hypoxia on systemic blood pressure. J Appl Physiol. 1995;78(4):1516-21. PMID: 7615464.
-
111Fletcher EC, Bao G. Influence of hypoxia, chemoreceptors, and sympathic activity in chronic hypertension in the rat. In: Lenfant C, Bradley TD, Floras JS. (editors). Sleep apnea: implications in cardiovascular and cerebrovascular disease. New York: Marcel Dekker; 2000. p. 181-211.
-
112Somers VK, Dyken ME, Mark AL, Abboud FM. Sympathetic-nerve activity during sleep in normal subjects. N Engl J Med. 1993;328(5):303-7. doi: 10.1056/NEJM199302043280502.
» https://doi.org/10.1056/NEJM199302043280502 -
113Pedrosa RP, Krieger EM, Lorenzi-Filho G, Drager LF. Recent advances of the impact of obstructive sleep apnea on systemic hypertension. Arq Bras Cardiol. 2011;97(2):e40-7. doi: http://dx.doi.org/10.1590/S0066-782X2011005000017
» http://dx.doi.org/10.1590/S0066-782X2011005000017 -
114Nicholl DD, Hanly PJ, Poulin MJ, Handley GB, Hemmelgarn BR, Sola DY, et al. Evaluation of continuous positive airway pressure therapy on renin-angiotensin system activity in obstructive sleep apnea. Am J Respir Crit Care Med. 2014;190(5):572-80. doi: 10.1164/rccm.201403-0526OC.
» https://doi.org/10.1164/rccm.201403-0526OC -
115Marin JM, Agusti A, Villar I, Forner M, Nieto D, Carrizo SJ, et al. Association between treated and untreated obstructive sleep apnea and risk of hypertension. JAMA. 2012;307(20):2169-76. doi: 10.1001/jama.2012.3418.
» https://doi.org/10.1001/jama.2012.3418 -
116Somers VK, Dyken ME, Clary MP, Abboud FM. Sympathetic neural mechanisms in obstructive sleep apnea. J Clin Invest. 1995;96(4):1897-904. doi: 10.1172/JCI118235.
» https://doi.org/10.1172/JCI118235 -
117Davies CW, Crosby JH, Mullins RL, Barbour C, Davies RJ, Stradling JR. Case-control study of 24 hour ambulatory blood pressure in patients with obstructive sleep apnoea and normal matched control subjects. Thorax. 2000;55(9):736-40. PMID: 10950890.
-
118Wolf J, Hering D, Narkiewicz K. Non-dipping pattern of hypertension and obstructive sleep apnea syndrome. Hypertens Res. 2010;33(9):867-71. doi: 10.1038/hr.2010.153.
» https://doi.org/10.1038/hr.2010.153 -
119Baguet JP, Hammer L, Lévy P, Pierre H, Rossini E, Mouret S, et al. Night-time and diastolic hypertension are common and underestimated conditions in newly diagnosed apnoeic patients. J Hypertens. 2005;23(3):521-7. PMID: 15716692.
-
120Ancoli-Israel S, Stepnowsky C, Dimsdale J, Marler M, Cohen-Zion M, Johnson S. The effect of race and sleep-disordered breathing on nocturnal BP "dipping": analysis in an older population. Chest. 2002;122(4):1148-55. PMID: 12377835.
-
121Onen SH, Lesourd B, Ouchchane L, Lin JS, Dubray C, Gooneratne NS, et al. Occult nighttime hypertension in daytime normotensive older patients with obstructive sleep apnea. J Am Med Dir Assoc. 2012;13(8):752-6. doi: 10.1016/j.jamda.2012.07.003.
» https://doi.org/10.1016/j.jamda.2012.07.003 -
122Seif F, Patel SR, Walia HK, Rueschman M, Bhatt DL, Blumenthal RS, et al. Obstructive sleep apnea and diurnal nondipping hemodynamic indices in patients at increased cardiovascular risk. J Hypertens. 2014;32(2):267-75. doi: 10.1097/HJH.0000000000000011.
» https://doi.org/10.1097/HJH.0000000000000011 -
123Baguet JP, Lévy P, Barone-Rochette G, Tamisier R, Pierre H, Peeters M, et al. Masked hypertension in obstructive sleep apnea syndrome. J Hypertens. 2008;26(5):885-92. doi: 10.1097/HJH.0b013e3282f55049.
» https://doi.org/10.1097/HJH.0b013e3282f55049 -
124Drager LF, Diegues-Silva L, Diniz PM, Bortolotto LA, Pedrosa RP, Couto RB, et al. Obstructive sleep apnea, masked hypertension, and arterial stiffness in men. Am J Hypertens. 2010;23(3):249-54. doi: 10.1038/ajh.2009.246.
» https://doi.org/10.1038/ajh.2009.246 -
125Drager LF, Pedrosa RP, Diniz PM, Diegues-Silva L, Marcondes B, Couto RB, et al. The effects of continuous positive airway pressure on prehypertension and masked hypertension in men with severe obstructive sleep apnea. Hypertension. 2011;57(3):549-55. doi: 10.1161/HYPERTENSIONAHA.110.165969.
» https://doi.org/10.1161/HYPERTENSIONAHA.110.165969 -
126Rimoldi SF, Messerli FH, Bangalore S, Scherrer U. Resistant hypertension: what the cardiologist needs to know. Eur Heart J. 2015;36(40):2686-95. doi: 10.1093/eurheartj/ehv392.
» https://doi.org/10.1093/eurheartj/ehv392 -
127Gonzaga CC, Gaddam KK, Ahmed MI, Pimenta E, Thomas SJ, Harding SM, et al. Severity of obstructive sleep apnea is related to aldosterone status in subjects with resistant hypertension. J Clin Sleep Med. 2010;6(4):363-8. PMID: 20726285.
-
128Genta-Pereira DC, Pedrosa RP, Lorenzi-Filho G, Drager LF. Sleep disturbances and resistant hypertension: association or causality? Curr Hypertens Rep. 2014;16(8):459. doi: 10.1007/s11906-014-0459-3.
» https://doi.org/10.1007/s11906-014-0459-3 -
129Gaddam K, Pimenta E, Thomas SJ, Cofield SS, Oparil S, Harding SM, et al. Spironolactone reduces severity of obstructive sleep apnoea in patients with resistant hypertension: a preliminary report. J Hum Hypertens. 2010;24(8):532-7. doi: 10.1038/jhh.2009.96.
» https://doi.org/10.1038/jhh.2009.96 -
130de Souza F, Muxfeldt ES, Margallo V, Cortez AF, Cavalcanti AH, Salles GF. Effects of continuous positive airway pressure treatment on aldosterone excretion in patients with obstructive sleep apnoea and resistant hypertension: a randomized controlled trial. J Hypertens. 2017;35(4):837-844. doi: 10.1097/HJH.0000000000001254.
» https://doi.org/10.1097/HJH.0000000000001254 -
131Fatureto-Borges F, Lorenzi-Filho G, Drager LF. Effectiveness of continuous positive airway pressure in lowering blood pressure in patients with obstructive sleep apnea: a critical review of the literature. Integr Blood Press Control. 2016;9:43-7. doi: 10.2147/IBPC.S70402.
» https://doi.org/10.2147/IBPC.S70402 -
132Bazzano LA, Khan Z, Reynolds K, He J. Effect of nocturnal nasal continuous positive airway pressure on blood pressure in obstructive sleep apnea. Hypertension. 2007;50(2):417-23. doi: 10.1161/HYPERTENSIONAHA.106.085175.
» https://doi.org/10.1161/HYPERTENSIONAHA.106.085175 -
133Bratton DJ, Stradling JR, Barbé F, Kohler M. Effect of CPAP on blood pressure in patients with minimally symptomatic obstructive sleep apnoea: a meta-analysis using individual patient data from four randomized controlled trials. Thorax. 2014;69(12):1128-1135. doi: 10.1136/thoraxjnl-2013-204993.
» https://doi.org/10.1136/thoraxjnl-2013-204993 -
134Lozano L, Tovar JL, Sampol G, Romero O, Jurado MJ, Segarra A, et al. Continuous positive airway pressure treatment in sleep apnea patients with resistant hypertension: a randomized, controlled trial. J Hypertens. 2010;28(10):2161-2168. doi: 10.1097/HJH.0b013e32833b9c63.
» https://doi.org/10.1097/HJH.0b013e32833b9c63 -
135Pedrosa RP, Drager LF, de Paula LK, Amaro AC, Bortolotto LA, Lorenzi-Filho G. Effects of OSA treatment on BP in patients with resistant hypertension: a randomized trial. Chest. 2013;144(5):1487-94. doi: 10.1378/chest.13-0085.
» https://doi.org/10.1378/chest.13-0085 -
136de Oliveira AC, Martinez D, Massierer D, Gus M, Gonçalves SC, Ghizzoni F, et al. The antihypertensive effect of positive airway pressure on resistant hypertension of patients with obstructive sleep apnea: a randomized, double-blind, clinical trial. Am J Respir Crit Care Med. 2014;190(3):345-7. doi: 10.1164/rccm.201403-0479LE.
» https://doi.org/10.1164/rccm.201403-0479LE -
137Muxfeldt ES, Margallo V, Costa LM, Guimarães G, Cavalcante AH, Azevedo JC, et al. Effects of continuous positive airway pressure treatment on clinic and ambulatory blood pressures in patients with obstructive sleep apnea and resistant hypertension: a randomized controlled trial. Hypertension. 2015;65(4):736-42. doi: 10.1161/HYPERTENSIONAHA.
» https://doi.org/10.1161/HYPERTENSIONAHA -
138Iftikhar IH, Valentine CW, Bittencourt LR, Cohen DL, Fedson AC, Gíslason T, et al. Effects of continuous positive airway pressure on blood pressure in patients with resistant hypertension and obstructive sleep apnea: a meta-analysis. J Hypertens. 2014;32(12):2341-50. doi: 10.1097/HJH.0000000000000372.
» https://doi.org/10.1097/HJH.0000000000000372 -
139Martinez-Garcia MA, Capote F, Campos-Rodriguez F, Lloberes P, Díaz de Atauri MJ, Somoza M, et al; Spanish Sleep Network. Effect of CPAP on blood pressure in patients with obstructive sleep apnea and resistant hypertension: the HIPARCO randomized clinical trial. JAMA. 2013;310(22):2407-15. doi: 10.1001/jama.2013.281250.
» https://doi.org/10.1001/jama.2013.281250 -
140Liu L, Cao Q, Guo Z, Dai Q. Continuous positive airway pressure in patients with obstructive sleep apnea and resistant hypertension: a meta-analysis of randomized controlled trials. J Clin Hypertens (Greenwich). 2016;18(2):153-8. doi: 10.1111/jch.12639.
» https://doi.org/10.1111/jch.12639 -
141Sánchez-de-la-Torre M, Khalyfa A, Sánchez-de-la-Torre A, Martinez-Alonso M, Martinez-García MA, Barceló A, et al; Spanish Sleep Network. Precision medicine in patients with resistant hypertension and obstructive sleep apnea: blood pressure response to continuous positive airway pressure treatment. J Am Coll Cardiol. 2015;66(9):1023-32. doi: 10.1016/j.jacc.2015.06.1315.
» https://doi.org/10.1016/j.jacc.2015.06.1315 -
142Bratton DJ, Gaisl T, Wons AM, Kohler M. CPAP vs mandibular advancement devices and blood pressure in patients with obstructive sleep apnea: a systematic review and meta-analysis. JAMA. 2015;314(21):2280-93. doi: 10.1001/jama.2015.16303.
» https://doi.org/10.1001/jama.2015.16303 -
143Gagnadoux F, Pépin JL, Vielle B, Bironneau V, Chouet-Girard F, Launois S, et al. Impact of mandibular advancement therapy on endothelial function in severe obstructive sleep apnea. Am J Respir Crit Care Med. 2017;195(9):1244-1252. doi: 10.1164/rccm.201609-1817OC.
» https://doi.org/10.1164/rccm.201609-1817OC -
144Issa FG. Effect of clonidine in obstructive sleep apnea. Am Rev Respir Dis. 1992;145(2 Pt 1):435-9. doi: 10.1164/ajrccm/145.2_Pt_1.435.
» https://doi.org/10.1164/ajrccm/145.2_Pt_1.435 -
145Kraiczi H, Hedner J, Peker Y, Grote L. Comparison of atenolol, amlodipine, enalapril, hydrochlorothiazide, and losartan for antihypertensive treatment in patients with obstructive sleep apnea. Am J Respir Crit Care Med. 2000;161(5):1423-8. doi: 10.1164/ajrccm.161.5.9909024.
» https://doi.org/10.1164/ajrccm.161.5.9909024 -
146Pépin JL, Tamisier R, Barone-Rochette G, Launois SH, Levy P, Baguet JP. Comparison of continuous positive airway pressure and valsartan in hypertensive patients with sleep apnea. Am J Respir Crit Care Med. 2010;182(7):954-60. doi: 10.1164/rccm.200912-1803OC.
» https://doi.org/10.1164/rccm.200912-1803OC -
147White LH, Bradley TD, Logan AG. Pathogenesis of obstructive sleep apnoea in hypertensive patients: role of fluid retention and nocturnal rostral fluid shift. J Hum Hypertens. 2015;29(6):342-50. doi: 10.1038/jhh.2014.94.
» https://doi.org/10.1038/jhh.2014.94 -
148Witkowski A, Prejbisz A, Florczak E, Kadziela J, Sliwinski P, Bielen P, et al. Effects of renal sympathetic denervation on blood pressure, sleep apnea course, and glycemic control in patients with resistant hypertension and sleep apnea. Hypertension. 2011;58(4):559-65. doi: 10.1161/HYPERTENSIONAHA.111.173799.
» https://doi.org/10.1161/HYPERTENSIONAHA.111.173799 -
149Kario K, Bhatt DL, Kandzari DE, Brar S, Flack JM, Gilbert C, et al. Impact of renal denervation on patients with obstructive sleep apnea and resistant hypertension: insights from the SYMPLICITY HTN-3 Trial. Circ J. 2016;80(6):1404-12. doi: 10.1253/circj.CJ-16-0035.
» https://doi.org/10.1253/circj.CJ-16-0035 -
150Bhatt DL, Kandzari DE, O'Neill WW, D'Agostino R, Flack JM, Katzen BT, et al; SYMPLICITY HTN-3 Investigators. A controlled trial of renal denervation for resistant hypertension. N Engl J Med. 2014;370(15):1393-401. doi: 10.1056/NEJMoa1402670.
» https://doi.org/10.1056/NEJMoa1402670 -
151Guilleminault C, Connolly SJ, Winkle RA. Cardiac arrhythmia and conduction disturbances during sleep in 400 patients with sleep apnea syndrome Am J Cardiol. 1983;52(5):490-4. PMID: 6193700.
-
152Cintra FD, Leite RP, Storti LJ, Bittencourt LA, Poyares D, Castro LD, et al. Sleep apnea and nocturnal cardiac arrhythmia: a populational study. Arq Bras Cardiol. 2014;103(5):368-74. doi: http://dx.doi.org/10.5935/abc.20140142
» http://dx.doi.org/10.5935/abc.20140142 -
153Oliveira W, Campos O, Bezerra Lira-Filho E, Cintra FD, Vieira M, Ponchirolli A, et al. Left atrial volume and function in patients with obstructive sleep apnea assessed by real-time three-dimensional echocardiography. J Am Soc Echocardiogr. 2008;21(12):1355-61. doi: 10.1016/j.echo.2008.09.007.
» https://doi.org/10.1016/j.echo.2008.09.007 -
154Drager LF, Bortolotto LA, Pedrosa RP, Krieger EM, Lorenzi-Filho G. Left atrial diameter is independently associated with arterial stiffness in patients with obstructive sleep apnea: potential implications for atrial fibrillation. Int J Cardiol. 2010;144(2):257-9. doi: 10.1016/j.ijcard.2009.01.018.
» https://doi.org/10.1016/j.ijcard.2009.01.018 -
155Gami AS, Pressman G, Caples SM, Kanagala R, Gard JJ, Davison DE, et al. Association of atrial fibrillation and obstructive sleep apnea. Circulation. 2004;110(4):364-7. doi: 10.1161/01.CIR.0000136587.68725.8E.
» https://doi.org/10.1161/01.CIR.0000136587.68725.8E -
156Kanagala R, Murali NS, Friedman PA, Ammash NM, Gersh BJ, Ballman KV, et al. Obstructive sleep apnea and recurrence of atrial fibrillation. Circulation. 2003;107(20):2589-94. doi: 10.1161/01.CIR.0000068337.25994.21.
» https://doi.org/10.1161/01.CIR.0000068337.25994.21 -
157Fein AS, Shvilkin A, Shah D, Haffajee CI, Das S, Kumar K, et al. Treatment of obstructive sleep apnea reduces the risk of atrial fibrillation recurrence after catheter ablation. J Am Coll Cardiol. 2013;62(4):300-5. doi: 10.1016/j.jacc.2013.03.052.
» https://doi.org/10.1016/j.jacc.2013.03.052 -
158Ng CY, Liu T, Shehata M, Stevens S, Chugh SS, Wang X. Meta-analysis of obstructive sleep apnea as predictor of atrial fibrillation recurrence after catheter ablation. Am J Cardiol. 2011;108(1):47-51. doi: 10.1016/j.amjcard.2011.02.343.
» https://doi.org/10.1016/j.amjcard.2011.02.343 -
159Koehler U, Fus E, Grimm W, Pankow W, Schafer H, Stammnitz A, et al. Heart block in patients with obstructive sleep apnoea: pathogenetic factors and effects of treatment. Eur Respir J. 1998;11(2):434-9. PMID: 9551750.
-
160Somers VK, Dyken ME, Mark AL, Abboud FM. Parasympathetic hyperresponsiveness and bradyarrhythmias during apnoea in hypertension. Clin Auton Res. 1992;2(3):171-6. PMID: 1498563.
-
161Grimm W, Hoffmann J, Menz V, Kohler U, Heitmann J, Peter JH, et al. Electrophysiologic evaluation of sinus node function and atrioventricular conduction in patients with prolonged ventricular asystole during obstructive sleep apnea. Am J Cardiol. 1996;77(15):1310-4. PMID: 8677871.
-
162Koehler U, Becker HF, Grimm W, Heitmann J, Peter JH, Schafer H. Relations among hypoxemia, sleep stage, and bradyarrhythmia during obstructive sleep apnea. Am Heart J. 2000;139(1 Pt 1):142-8. PMID: 10618575.
-
163Roche F, Xuong AN, Court-Fortune I, Costes F, Pichot V, Duverney D, et al. Relationship among the severity of sleep apnea syndrome, cardiac arrhythmias, and autonomic imbalance. Pacing Clin Electrophysiol. 2003;26(3):669-77. PMID: 12698666.
-
164Mehra R, Benjamin EJ, Shahar E, Gottlieb DJ, Nawabit R, Kirchner HL, et al. Association of nocturnal arrhythmias with sleep-disordered breathing: The Sleep Heart Health Study. Am J Respir Crit Care Med. 2006;173(8):910-6. doi: 10.1164/rccm.200509-1442OC.
» https://doi.org/10.1164/rccm.200509-1442OC -
165Abe H, Takahashi M, Yaegashi H, Eda S, Tsunemoto H, Kamikozawa M, et al. Efficacy of continuous positive airway pressure on arrhythmias in obstructive sleep apnea patients. Heart Vessels. 2010;25(1):63-9. doi: 10.1007/s00380-009-1164-z.
» https://doi.org/10.1007/s00380-009-1164-z -
166Gami AS, Olson EJ, Shen WK, Wright RS, Ballman KV, Hodge DO, et al. Obstructive sleep apnea and the risk of sudden cardiac death: a longitudinal study of 10,701 adults. J Am Coll Cardiol. 2013;62(7):610-6. doi: 10.1016/j.jacc.2013.04.080.
» https://doi.org/10.1016/j.jacc.2013.04.080 -
167Bitter T, Westerheide N, Prinz C, Hossain MS, Vogt J, Langer C, et al. Cheyne-Stokes respiration and obstructive sleep apnoea are independent risk factors for malignant ventricular arrhythmias requiring appropriate cardioverter-defibrillator therapies in patients with congestive heart failure. Eur Heart J. 2011;32(1):61-74. doi: 10.1093/eurheartj/ehq327
» https://doi.org/10.1093/eurheartj/ehq327 -
168Ryan CM, Usui K, Floras JS, Bradley TD. Effect of continuous positive airway pressure on ventricular ectopy in heart failure patients with obstructive sleep apnoea. Thorax. 2005;60(9):781-5. doi: 10.1136/thx.2005.040972.
» https://doi.org/10.1136/thx.2005.040972 -
169Yumino D, Kasai T, Kimmerly D, Amirthalingam V, Floras JS, Bradley TD. Differing Effects of Obstrutive and Central Sleep Apneas on Stroke Volume in Patients with Heart Failure. Am J Respir Crit Care Med. 2012;187(4):433-43. doi: 10.1164/rccm.201205-0894OC.
» https://doi.org/10.1164/rccm.201205-0894OC -
170Laaban JP, Pascal-Sebaoun S, Bloch E, Orvoen-Frija E, Oppert JM, Huchon G. Left ventricular systolic dysfunction in patients with obstructive sleep apnea syndrome. Chest. 2002;122(4):1133-8. PMID: 12377833.
-
171Drager LF, Bortolotto LA, Figueiredo AC, Silva BC, Krieger EM, Lorenzi-Filho G. Obstructive sleep apnea, hypertension, and their interaction on arterial stiffness and heart remodeling. Chest. 2007;131(5):1379-86. doi: 10.1378/chest.06-2703.
» https://doi.org/10.1378/chest.06-2703 -
172Bradley TD, Hall MJ, Ando S, Floras JS. Hemodynamic effects of simulated obstructive apneas in humans with and without heart failure. Chest. 2001;119(6):1827-35. PMID: 11399711.
-
173Ross J Jr. Afterload mismatch and preload reserve: a conceptual frameworkfor the analysis of ventricular function. Prog Cardiovasc Dis. 1976;18(4):255-264. PMID: 128034.
-
174Svanborg E, Carlsson-Nordlander B, Larsson H, Sachs C, Kaijser L. Autonomic nervous system function in patients with primary obstructive sleep apnoea syndrome. Clin Auton Res. 1991;1(2):125-30. PMID: 1822759.
-
175Carlson JT, Hedner JA, Sellgren J, Elam M, Wallin BG. Depressed baroreflex sensitivity in patients with obstructive sleep apnea. Am J Respir Crit Care Med. 1996;154(5):1490-6. doi: 10.1164/ajrccm.154.5.8912770.
» https://doi.org/10.1164/ajrccm.154.5.8912770 -
176Somers VK, Mark AL, Zavala DC, Abboud FM. Contrasting effects of hypoxia and hypercapnia on ventilation and sympathetic activity in humans. J Appl Physiol (1985). 1989;67(5):2101-6. PMID: 2513316.
-
177Chami HA, Devereux RB, Gottdiener JS, Mehra R, Roman MJ, Benjamin EJ, et al. Left ventricular morphology and systolic function in sleep-disordered breathing: the Sleep Heart Health Study. Circulation. 2008;117(20):2599-607. doi: 10.1161/CIRCULATIONAHA.107.717892.
» https://doi.org/10.1161/CIRCULATIONAHA.107.717892 -
178Varol E, Akcay S, Ozaydin M, Ozturk O, Cerci SS, Sahin U. Influence of obstructive sleep apnea on left ventricular mass and global function: sleep apnea and myocardial performance index. Heart Vessels. 2010;25(5):400-4. doi: 10.1007/s00380-009-1225-3.
» https://doi.org/10.1007/s00380-009-1225-3 -
179Romero-Corral A, Somers VK, Pellikka PA, Olson EJ, Bailey KR, Korinek J, et al. Decreased right and left ventricular myocardial performance in obstructive sleep apnea. Chest. 2007;132(6):1863-70. doi: 10.1378/chest.07-0966.
» https://doi.org/10.1378/chest.07-0966 -
180Cho KI, Kwon JH, Kim SM, Park TJ, Lee HG, Kim TI. Impact of obstructive sleep apnea on the global myocardial performance beyond obesity. Echocardiography. 2012;29(9):1071-80. doi: 10.1111/j.1540-8175.2012.01762.x.
» https://doi.org/10.1111/j.1540-8175.2012.01762.x -
181Moro JA, Almenar L, Fernández-Fabrellas E, Ponce S, Blanquer R, Salvador A. Hypertension and sleep apnea-hypopnea syndrome: changes in echocardiographic abnormalities depending on the presence of hypertension and treatment with CPAP. Sleep Med. 2009;10(3):344-52. doi: 10.1016/j.sleep.2008.03.008.
» https://doi.org/10.1016/j.sleep.2008.03.008 -
182Dursunoglu N, Dursunoglu D, Ozkurt S, Kuru O, Gür S, Kiter G, et al. Effects of CPAP on left ventricular structure and myocardial performance index in male patients with obstructive sleep apnoea. Sleep Med. 2007;8(1):51-9. doi: 10.1016/j.sleep.2006.04.007.
» https://doi.org/10.1016/j.sleep.2006.04.007 -
183Malone S, Liu PP, Holloway R, Rutherford R, Xie A, Bradley TD. Obstructive sleep apnoea in patients with dilated cardiomyopathy: effects of continuous positive airway pressure. Lancet. 1991;338(8781):1480-4. PMID: 1683918.
-
184Kaneko Y, Floras JS, Usui K, Plante J, Tkacova R, Kubo T, et al. Cardiovascular effects of continuous positive airway pressure in patients with heart failure and obstructive sleep apnea. N Engl J Med. 2003;348(13):1233-41. doi: 10.1056/NEJMoa022479.
» https://doi.org/10.1056/NEJMoa022479 -
185Javaheri S, Caref EB, Chen E, Tong KB, Abraham WT. Sleep apnea testing and outcomes in a large cohort of Medicare beneficiaries with newlydiagnosed heart failure. Am J Respir Crit Care Med. 2011;183(4):539-46. doi: 10.1164/rccm.201003-0406OC.
» https://doi.org/10.1164/rccm.201003-0406OC -
186Khayat R, Jarjoura D, Porter K, Sow A, Wannemacher J, Dohar R, et al. Sleep disordered breathing and post-discharge mortality in patients with acute heart failure. Eur Heart J. 2015;36(23):1463-9. doi: 10.1093/eurheartj/ehu522.
» https://doi.org/10.1093/eurheartj/ehu522 -
187Hedner J, Ejnell H, Caidahl K. Left ventricular hypertrophy independent of hypertension in patients with obstructive sleep apnea. J Hypertens. 1990;8(10):941-6. PMID: 2174947.
-
188Noda A, Okada T, Yasuma F, Nakashima N, Yokota M. Cardiac hypertrophy in obstructive sleep apnea syndrome. Chest. 1995;107(6):1538-44. PMID: 7781343.
-
189Sukhija R, Aronow WS, Sandhu R, Kakar P, Maguire GP, Ahn C, et al. Prevalence of left ventricularhypertrophy in persons with and without obstructive sleep apnea. Cardiol Rev. 2006;14(4):170-2. doi: 10.1097/01.crd.0000184455.52778.00.
» https://doi.org/10.1097/01.crd.0000184455.52778.00 -
190Baguet JP, Nadra M, Barone-Rochette G, Ormezzano O, Pierre H, Pépin JL. Early cardiovascular abnormalities in newly diagnosed obstructive sleep apnea. Vasc Health Risk Manag. 2009;5:1063-73. PMID: 20057899.
-
191Cioffi G, Russo TE, Stefenelli C, Selmi A, Furlanello F, Cramariuc D, et al. Severe obstructive sleep apnea elicits concentric left ventricular geometry. J Hypertens. 2010;28(5):1074-82. PMID: 20411620.
-
192Hla KM, Young T, Finn LA, Peppard PE, Kinsey TJ, Ende D. Electrocardiographically indicated cardiovascular disease in sleep-disordered breathing. Sleep Breath. 2008;12(3):251-8. doi: 10.1007/s11325-007-0168-0.
» https://doi.org/10.1007/s11325-007-0168-0 -
193Koga S, Ikeda S, Nakata T, Yasunaga T, Maemura K. Effects of nasal continuous positive airway pressure on left ventricular concentric hypertrophy in obstructive sleep apnea syndrome. Intern Med. 2012;51(20):2863-8. PMID: 23064559.
-
194Shivalkar B, Van de Heyning C, Kerremans M, Rinkevich D, Verbraecken J, De Backer W, et al. Obstructive sleep apnea syndrome: more insights on structural and functional cardiac alterations, and the effects of treatment with continuous positive airway pressure. J Am Coll Cardiol. 2006;47(7):1433-9. doi: 10.1016/j.jacc.2005.11.054.
» https://doi.org/10.1016/j.jacc.2005.11.054 -
195Cloward TV, Walker JM, Farney RJ, Anderson JL. Left ventricular hypertrophy is a common echocardiographic abnormality in severe obstructive sleep apnea and reverses with nasal continuous positive airway pressure. Chest. 2003;124(2):594-601. PMID: 12907548.
-
196Usui Y, Takata Y, Inoue Y, Tomiyama H, Kurohane S, Hashimura Y, et al. Severe obstructive sleep apnea impairs left ventricular diastolic function in non-obese men. Sleep Med. 2013;14(2):155-9. doi: 10.1016/j.sleep.2010.09.014.
» https://doi.org/10.1016/j.sleep.2010.09.014 -
197Yang SQ, Han LL, Dong XL, Wang CY, Xia H, Liu P, et al. Mal-effects of obstructive sleep apnea on the heart. Sleep Breath. 2012;16(3):717-22. doi: 10.1007/s11325-011-0566-1.
» https://doi.org/10.1007/s11325-011-0566-1 -
198Cicek D, Lakadamyali H, Yagbasan BD, Sapmaz I, Müderrisoglu H. Obstructive sleep apnoea and its association with left ventricular function and aortic root parameters in newly diagnosed, untreated patients: a prospective study. J Int Med Res. 2011;39(6):2228-38. doi: 10.1177/147323001103900619.
» https://doi.org/10.1177/147323001103900619 -
199Kim SH, Cho GY, Shin C, Lim HE, Kim YH, Song WH, et l. Impact of obstructive sleep apnea on left ventricular diastolic function. Am J Cardiol. 2008;101(11):1663-8. doi: 10.1016/j.amjcard.2008.01.056.
» https://doi.org/10.1016/j.amjcard.2008.01.056 -
200Fung JW, Li TS, Choy DK, Yip GW, Ko FW, Sanderson JE, et al. Severe obstructive sleep apnea is associated with left ventricular diastolic dysfunction. Chest. 2002;121(2):422-9. PMID: 11834652.
-
201Altekin RE, Yanikoglu A, Baktir AO, Karakas MS, Ozel D, Cilli A, et al. Assessment of subclinical left ventricular dysfunction in obstructive sleep apnea patients with speckle tracking echocardiography. Int J Cardiovasc Imaging. 2012;28(8):1917-30. doi: 10.1007/s10554-012-0026-4.
» https://doi.org/10.1007/s10554-012-0026-4 -
202Vitarelli A, D'Orazio S, Caranci F, Capotosto L, Rucos R, Iannucci G, et al. Left ventricular torsion abnormalities in patients with obstructive sleep apnea syndrome: an early sign of subclinical dysfunction. Int J Cardiol. 2013;165(3):512-8. doi: 10.1016/j.ijcard.2011.09.030.
» https://doi.org/10.1016/j.ijcard.2011.09.030 -
203Haruki N, Takeuchi M, Kanazawa Y, Tsubota N, Shintome R, Nakai H, et al. Continuous positive airway pressure ameliorates sleep-induced subclinical left ventricular systolic dysfunction: demonstration by two-dimensional speckle-tracking echocardiography. Eur J Echocardiogr. 2010;11(4):352-8. doi: 10.1093/ejechocard/jep215.
» https://doi.org/10.1093/ejechocard/jep215 -
204Butt M, Dwivedi G, Shantsila A, Khair OA, Lip GY. Left ventricular systolic and diastolic function in obstructive sleep apnea: impact of continuous positive airway pressure therapy. Circ Heart Fail 2012;5(2):226-33. doi: 10.1161/CIRCHEARTFAILURE.111.964106.
» https://doi.org/10.1161/CIRCHEARTFAILURE.111.964106 -
205Akar Bayram N, Ciftci B, Durmaz T, Keles T, Yeter E, Akcay M, et al. Effects of continuous positive airway pressure therapy on left ventricular function assessed by tissue Doppler imaging in patients with obstructive sleep apnoea syndrome. Eur J Echocardiogr. 2009;10(3):376-82. doi: 10.1093/ejechocard/jen257.
» https://doi.org/10.1093/ejechocard/jen257 -
206Arias MA, García-Río F, Alonso-Fernández A, Mediano O, Martínez I, Villamor J. Obstructive sleep apnea syndrome affects left ventricular diastolic function: effects of nasal continuous positive airway pressure in men. Circulation. 2005;112(3):375-83. doi: 10.1161/CIRCULATIONAHA.104.501841.
» https://doi.org/10.1161/CIRCULATIONAHA.104.501841 -
207Oliveira W, Campos O, Cintra F, Matos L, Vieira ML, Rollim B, et al. Impact of continuous positive airway pressure treatment on left atrial volume and function in patients with obstructive sleep apnoea assessed by real-time three-dimensional echocardiography. Heart. 2009;95(22):1872-8. doi: 10.1136/hrt.2009.173625.
» https://doi.org/10.1136/hrt.2009.173625 -
208Dimitri H, Ng M, Brooks AG, Kuklik P, Stiles MK, Lau DH, et al. Atrial remodeling in obstructive sleep apnea: implications for atrial fibrillation. Heart Rhythm. 2012;9(3):321-7. doi: 10.1016/j.hrthm.2011.10.017.
» https://doi.org/10.1016/j.hrthm.2011.10.017 -
209Yagmur J, Yetkin O, Cansel M, Acikgoz N, Ermis N, Karakus Y, et al. Assessment of atrial electromechanical delay and influential factors in patients with obstructive sleep apnea. Sleep Breath. 2012;16(1):83-8. doi: 10.1007/s11325-010-0477-6.
» https://doi.org/10.1007/s11325-010-0477-6 -
210Sanner BM, Konermann M, Sturm A, Muller HJ, Zidek W. Right ventricular dysfunction in patients with obstructive sleep apnoea syndrome. Eur Respir J. 1997;10(9):2079-83. PMID: 9311506.
-
211Dursunoglu N, Dursunoglu D, Kilic M. Impact of obstructive sleep apnea on right ventricular global function: sleep apnea and myocardial performance index. Respiration. 2005;72(3):278-84. doi: 10.1159/000085369.
» https://doi.org/10.1159/000085369 -
212Tugcu A, Yildirimturk O, Tayyareci Y, Demiroglu C, Aytekin S. Evaluation of subclinical right ventricular dysfunction in obstructive sleep apnea patients using velocity vector imaging. Circ J. 2010;74(2):312-9. PMID: 20009388.
-
213Oliveira W, Poyares D, Cintra F, Vieira ML, Fischer CH, Moises V, et al. Impact of continuous positive airway pressure treatment on right ventricle performance in patients with obstructive sleep apnoea, assessed by three-dimensional echocardiography. Sleep Med. 2012;13(5):510-6. doi: 10.1016/j.sleep.2011.12.010.
» https://doi.org/10.1016/j.sleep.2011.12.010 -
214Wang H, Parker JD, Newton GE, Floras JS, Mak S, Chiu KL, et al. Influence of obstructive sleep apnea on mortality in patients with heart failure. J Am Coll Cardiol. 2007;49(15):1625-31. doi: 10.1016/j.jacc.2006.12.046.
» https://doi.org/10.1016/j.jacc.2006.12.046 -
215Yoshinaga K, Burwash IG, Leech JA, Haddad H, Johnson CB, deKemp RA, et al. The effects of continuous positive airway pressure on myocardial energetics in patients with heart failure and obstructive sleep apnea. J Am Coll Cardiol. 2007;49(4):450-8. doi: 10.1016/j.jacc.2006.08.059.
» https://doi.org/10.1016/j.jacc.2006.08.059 -
216Hall AB, Ziadi MC, Leech JA, Chen SY, Burwash IG, Renaud J, et al. Effects of short-term continuous positive airway pressure on myocardial sympathetic nerve function and energetics in patients with heart failure and obstructive sleep apnea: a randomized study. Circulation. 2014;130(11):892-901. doi: 10.1161/CIRCULATIONAHA.113.005893.
» https://doi.org/10.1161/CIRCULATIONAHA.113.005893 -
217Maron BJ. Hypertrophic cardiomyopathy: a systematic review. JAMA. 2002;287(10):1308-20. PMID: 11886323.
-
218Zou Y, Song L, Wang Z, Ma A, Liu T, Gu H, et al. Prevalence of idiopathic hypertrophic cardiomyopathy in China: a population-based echocardiographic analysis of 8080 adults. Am J Med. 2004;116(1):14-8. PMID: 14706660.
-
219Maron BJ. Hypertrophic cardiomyopathy. Lancet. 1997;350(9071):127-33. doi: 10.1016/S0140-6736(97)01282-8. Erratum in: Lancet. 1997;350(9087):1330.
» https://doi.org/10.1016/S0140-6736(97)01282-8 -
220Gersh BJ, Maron BJ, Bonow RO, Dearani JA, Fifer MA, Link MS, et al; American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines; American Association for Thoracic Surgery; American Society of Echocardiography; American Society of Nuclear Cardiology; Heart Failure Society of America; Heart Rhythm Society; Society for Cardiovascular Angiography and Interventions; Society of Thoracic Surgeons. 2011 ACCF/AHA guideline for the diagnosis and treatment of hypertrophic cardiomyopathy: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. Circulation. 2011;124(24):e783-831. doi: 10.1161/CIR.0b013e318223e2bd.
» https://doi.org/10.1161/CIR.0b013e318223e2bd -
221Maron BJ, Seidman CE, Ackerman MJ, Towbin JA, Maron MS, Ommen SR, et al. How should hypertrophic cardiomyopathy be classified?: What's in a name? Dilemmas in nomenclature characterizing hypertrophic cardiomyopathy and left ventricular hypertrophy. Circ Cardiovasc Genet. 2009;2(1):81-5. doi: 10.1161/CIRCGENETICS.108.788703.
» https://doi.org/10.1161/CIRCGENETICS.108.788703 -
222Miller MA, Gomes JA, Fuster V. Risk stratification of sudden cardiac death in hypertrophic cardiomyopathy. Nat Clin Pract Cardiovasc Med. 2007;4(12):667-76. doi: 10.1038/ncpcardio1057.
» https://doi.org/10.1038/ncpcardio1057 -
223Banno K, Shiomi T, Sasanabe R, Otake K, Hasegawa R, Maekawa M, et al. Sleep-disordered breathing in patients with idiopathic cardiomyopathy. Circ J. 2004;68(4):338-42. PMID: 15056831.
-
224Pedrosa RP, Drager LF, Genta PR, Amaro AC, Antunes MO, Matsumoto AY, et al. Obstructive sleep apnea is common and independently associated with atrial fibrillation in patients with hypertrophic cardiomyopathy. Chest. 2010;137(5):1078-84. doi: 10.1378/chest.09-2335.
» https://doi.org/10.1378/chest.09-2335 -
225Konecny T, Brady PA, Orban M, Lin G, Pressman GS, Lehar F, et al. Interactions between sleep disordered breathing and atrial fibrillation in patients with hypertrophic cardiomyopathy. Am J Cardiol. 2010;105(11):1597-602. doi: 10.1016/j.amjcard.2010.01.023.
» https://doi.org/10.1016/j.amjcard.2010.01.023 -
226Eleid MF, Konecny T, Orban M, Sengupta PP, Somers VK, Parish JM, et al. High prevalence of abnormal nocturnal oximetry in patients with hypertrophic cardiomyopathy. J Am Coll Cardiol. 2009;54(19):1805-9. doi: 10.1016/j.jacc.2009.07.030.
» https://doi.org/10.1016/j.jacc.2009.07.030 -
227Prinz C, Bitter T, Oldenburg O, Horstkotte D, Faber L. Incidence of sleep-disordered breathing in patients with hypertrophic cardiomyopathy. Congest Heart Fail. 2011;17(1):19-24. doi: 10.1111/j.1751-7133.2010.00196.x.
» https://doi.org/10.1111/j.1751-7133.2010.00196.x -
228Pedrosa RP, Lima SG, Drager LF, Genta PR, Amaro AC, Antunes MO, et al. Sleep quality and quality of life in patients with hypertrophic cardiomyopathy. Cardiology. 2010;117(3):200-6. doi: 10.1159/000321718.
» https://doi.org/10.1159/000321718 -
229Nerbass FB, Pedrosa RP, Genta PR, Antunes MO, Arteaga-Fernández E, Drager LF, et al. Lack of reliable clinical predictors to identify obstructive sleep apnea in patients with hypertrophic cardiomyopathy. Clinics. 2013;68(7):992-6. doi: http://dx.doi.org/10.6061/clinics/2013(07)17
» http://dx.doi.org/10.6061/clinics/2013(07)17 -
230Limbruno U, Strata G, Zucchi R, Baglini R, Mengozzi G, Balbarini A, et al. Altered autonomic cardiac control in hypertrophic cardiomyopathy. Role of outflow tract obstruction and myocardial hypertrophy. Eur Heart J. 1998;19(1):146-53. PMID: 9503188.
-
231Sengupta PP, Sorajja D, Eleid MF, Somers VK, Ommen SR, Parish JM, et al. Hypertrophic obstructive cardiomyopathy and sleep-disordered breathing: an unfavorable combination. Nat Clin Pract Cardiovasc Med. 2009;6(1):14-5. doi: 10.1038/ncpcardio1401.
» https://doi.org/10.1038/ncpcardio1401 -
232Nistri S, Olivotto I, Betocchi S, Losi MA, Valsecchi G, Pinamonti B, et al. Prognostic significance of left atrial size in patients with hypertrophic cardiomyopathy (from the Italian Registry for Hypertrophic Cardiomyopathy). Am J Cardiol. 2006;98(7):960-5. doi: 10.1016/j.amjcard.2006.05.013.
» https://doi.org/10.1016/j.amjcard.2006.05.013 -
233Nerbass FB, Pedrosa RP, Danzi-Soares NJ, Drager LF, Arteaga-Fernández E, Lorenzi-Filho G. Obstructive sleep apnea and hypertrophic cardiomyopathy: A common and potential harmful combination. Sleep Med Rev. 2013;17(3):201-6. doi: 10.1016/j.smrv.2012.06.006.
» https://doi.org/10.1016/j.smrv.2012.06.006 -
234Geske JB, Sorajja P, Ommen SR, Nishimura RA. Left ventricular outflow tract gradient variability in hypertrophic cardiomyopathy. Clin Cardiol. 2009;32(7):397-402. doi: 10.1002/clc.20594.
» https://doi.org/10.1002/clc.20594 -
235Nerbass FB, Salemi VM, Pedrosa RP, Portilho NP, Ferreira-Filho JC, Moriya HT, et al. Acute effects of nasal CPAP in patients with hypertrophic cardiomyopathy. Chest. 2016;150(5):1050-8. doi: 10.1016/j.chest.2016.05.004.
» https://doi.org/10.1016/j.chest.2016.05.004 -
236Drager LF, Lopes HF, Maki-Nunes C, Trombetta IC, Toschi-Dias E, Alves MJ, et al. The impact of obstructive sleep apnea on metabolic and inflammatory markers in consecutive patients with metabolic syndrome. PLoSOne. 2010;5(8):e12065. doi: 10.1371/journal.pone.0012065.
» https://doi.org/10.1371/journal.pone.0012065 -
237Wilcox I, McNamara SG, Collins FL, Grunstein RR, Sullivan CE. "Syndrome Z": the interaction of sleepapnoea, vascular risk factors and heart disease. Thorax. 1998;53 Suppl 3:S25-8. PMID: 10193357.
-
238Li J, Thorne LN, Punjabi NM, Sun CK, Schwartz AR, Smith PL, et al. Intermittent hypoxia induces hyperlipidemia in lean mice. Circ Res. 2005;97(7):698-706. doi: 10.1161/01.RES.0000183879.60089.a9.
» https://doi.org/10.1161/01.RES.0000183879.60089.a9 -
239Li J, Grigoryev DN, Ye SQ, Thorne L, Schwartz AR, Smith PL et al. Chronic intermittent hypoxia upregulatesgenes of lipid biosynthesis in obese mice. J Appl Physiol (1985). 2005;99(5):1643-8. doi: 10.1152/japplphysiol.00522.2005.
» https://doi.org/10.1152/japplphysiol.00522.2005 -
240Savransky V, Jun J, Li J, Nanayakkara A, Fonti S, Moser AB, et al. Dyslipidemia and atherosclerosis induced by chronic intermittent hypoxia are attenuated by deficiency of stearoyl coenzyme A desaturase. Circ Res. 2008;103(10):1173-80. doi: 10.1161/CIRCRESAHA.108.178533.
» https://doi.org/10.1161/CIRCRESAHA.108.178533 -
241Drager LF, Li J, Shin MK, Reinke C, Aggarwal NR, Jun JC, et al. Intermittent hypoxia inhibits clearance of triglyceride-rich lipoproteins and inactivates adipose lipoprotein lipase in a mouse model of sleep apnoea. Eur Heart J. 2012;33(6):783-90. doi: 10.1093/eurheartj/ehr097.
» https://doi.org/10.1093/eurheartj/ehr097 -
242Drager LF, Yao Q, Hernandez KL, Shin MK, Bevans-Fonti S, Gay J, et al. Chronic Intermittent Hypoxia InducesAtherosclerosis via Activation of Adipose Angiopoietin-like 4. Am J Respir Crit Care Med. 2013;188(2):240-8. doi: 10.1164/rccm.201209-1688OC
» https://doi.org/10.1164/rccm.201209-1688OC -
243Drager LF, Jun J, Polotsky VY. Obstructive sleep apnea and dyslipidemia: implications foratherosclerosis. Curr Opin Endocrinol Diabetes Obes. 2010;17(2):161-5. doi: 10.1097/MED.0b013e3283373624. Erratum in: Curr Opin Endocrinol Diabetes Obes. 2010;17(4):394.
» https://doi.org/10.1097/MED.0b013e3283373624 -
244Togeiro SM, Carneiro G, Ribeiro Filho FF, Zanella MT, Santos-Silva R, Taddei JA, et al. Consequences of obstructive sleep apnea on metabolic profile: a population-based survey. Obesity (Silver Spring). 2013;21(4):847-51. doi: 10.1002/oby.20288.
» https://doi.org/10.1002/oby.20288 -
245Phillips CL, Yee BJ, Marshall NS, Liu PY, Sullivan DR, Grunstein RR. Continuous positive airway pressure reduces postprandial lipidemia in obstructive sleep apnea: a randomized, placebo-controlled crossover trial. Am J RespirCrit Care Med. 2011;184(3):355-61. doi: 10.1164/rccm.201102-0316OC.
» https://doi.org/10.1164/rccm.201102-0316OC -
246Punjabi NM, Shahar E, Redline S, Gottlieb DJ, Givelber R, Resnick HE. Sleep disordered breathing, glucose intolerance, and insulin resistance: The Sleep Heart Health Study. Am J Epidemiol. 2004;160(6):521-30. doi: 10.1093/aje/kwh261
» https://doi.org/10.1093/aje/kwh261 -
247Marshall NS, Wong KK, Phillips CL, Liu PY, Knuiman MW, Grunstein RR. Is sleep apnea an independent risk factor for prevalent and incident diabetes in the Busselton Health Study? J Clin Sleep Med. 2009;5(1):15-20. PMID: 19317376
-
248Reichmuth KJ, Austin D, Skatrud JB, Young T. Association of sleep apnea and type II diabetes: a population-based study. Am J Respir Crit Care Med. 2005;172(12):1590-5. doi: 10.1164/rccm.200504-637OC.
» https://doi.org/10.1164/rccm.200504-637OC -
249Drager LF, Togeiro SM, Polotsky VY, Lorenzi-Filho G. Obstructive sleep apnea: a cardiometabolic risk in obesity and the metabolic syndrome. J Am Coll Cardiol. 2013;62(7):569-76. doi: 10.1016/j.jacc.2013.05.045.
» https://doi.org/10.1016/j.jacc.2013.05.045 -
250Martínez-Ceron E, Fernández-Navarro I, Garcia-Rio F. Effects of continuous positive airway pressure treatment on glucose metabolism in patients with obstructive sleep apnea. Sleep Med Rev. 2016;25:121-30. doi: 10.1016/j.smrv.2015.03.002.
» https://doi.org/10.1016/j.smrv.2015.03.002 -
251Drager LF, Li J, Reinke C, Bevans-Fonti S, Jun JC, Polotsky VY. Intermittent hypoxia exacerbates metabolic effects of diet-induced obesity. Obesity (Silver Spring). 2011;19(11):2167-74. doi: 10.1038/oby.2011.240.
» https://doi.org/10.1038/oby.2011.240 -
252Murphy AM, Thomas A, Crinion SJ, Kent BD, Tambuwala MM, Fabre A, et al. Intermittent hypoxia in obstructive sleep apnoea mediates insulin resistance through adipose tissue inflammation. Eur Respir J. 2017;49(4). pii: 1601731. doi: 10.1183/13993003.01731-2016.
» https://doi.org/10.1183/13993003.01731-2016 -
253Poulain L, Thomas A, Rieusset J, Casteilla L, Levy P, Arnaud C, et al. Visceral white fat remodelling contributes to intermittent hypoxia-induced atherogenesis. Eur Respir J. 2014;43(2):513-22. doi: 10.1183/09031936.00019913.
» https://doi.org/10.1183/09031936.00019913 -
254Hoyos CM, Sullivan DR, Liu PY. Effect of CPAP on the metabolic syndrome: a randomised sham-controlled study. Thorax. 2013;68(6):588-9. doi: 10.1136/thoraxjnl-2012-203074.
» https://doi.org/10.1136/thoraxjnl-2012-203074 -
255Sivam S, Phillips CL, Trenell MI, Yee BJ, Liu PY, Wong KK, et al. Effects of 8 weeks of continuous positive airway pressure on abdominal adiposity in obstructive sleep apnoea. Eur Respir J. 2012;40(4):913-8. doi: 10.1183/09031936.00177011.
» https://doi.org/10.1183/09031936.00177011 -
256Drager LF, Brunoni AR, Jenner R, Lorenzi-Filho G, Benseñor IM, Lotufo PA. Effects of CPAP on body weight in patients with obstructive sleep apnoea: a meta-analysis of randomised trials. Thorax. 2015;70(3):258-64. doi: 10.1136/thoraxjnl-2014-205361.
» https://doi.org/10.1136/thoraxjnl-2014-205361 -
257Drager LF, Bortolotto LA, Maki-Nunes C, Trombetta IC, Alves MJ, Fraga RF, et al. The incremental role of obstructive sleep apnoea on markers of atherosclerosis in patients with metabolic syndrome. Atherosclerosis. 2010;208(2):490-5. doi: 10.1016/j.atherosclerosis.2009.08.016.
» https://doi.org/10.1016/j.atherosclerosis.2009.08.016 -
258Dorkova Z, Petrasova D, Molcanyiova A, Popovnakova M, Tkacova R. Effects of continuous positive airway pressure on cardiovascular risk profile in patients with severe obstructive sleep apnea and metabolic syndrome. Chest. 2008;134(4):686-692. doi: 10.1378/chest.08-0556.
» https://doi.org/10.1378/chest.08-0556 -
259Maki-Nunes C, Toschi-Dias E, Cepeda FX, Rondon MU, Alves MJ, Fraga RF, et al. Diet and exercise improve chemoreflex sensitivity in patients with metabolic syndrome and obstructive sleep apnea. Obesity (Silver Spring). 2015;23(8):1582-90. doi: 10.1002/oby.21126.
» https://doi.org/10.1002/oby.21126 -
260Drager LF, Polotsky VY, Lorenzi-Filho G. Obstructive sleep apnea: an emerging risk factor for atherosclerosis. Chest. 2011;140(2):534-42. doi: 10.1378/chest.10-2223.
» https://doi.org/10.1378/chest.10-2223 -
261Jelic S, Padeletti M, Kawut SM, Higgins C, Canfield SM, Onat D, et al. Inflammation, oxidative stress, and repair capacity of the vascular endothelium in obstructive sleep apnea. Circulation. 2008;117(17):2270-8. doi: 10.1161/CIRCULATIONAHA.107.741512.
» https://doi.org/10.1161/CIRCULATIONAHA.107.741512 -
262Shamsuzzaman AS, Winnicki M, Lanfranchi P, Wolk R, Kara T, Accurso V, et al. Elevated C-reactive protein in patients with obstructive sleep apnea. Circulation. 2002;105(21):2462-4. PMID: 12034649.
-
263Lavie L, Lavie P. Molecular mechanisms of cardiovascular disease in OSAHS: the oxidative stress link. Eur Respir J. 2009;33(6):1467-84. doi: 10.1183/09031936.00086608.
» https://doi.org/10.1183/09031936.00086608 -
264Carneiro G, Ribeiro Filho FF, Togeiro SM, Tufik S, Zanella MT. [Interactions between obstructive sleep apnea syndrome and insulin resistance]. Arq Bras Endocrinol Metabol. 2007;51(7):1035-40. doi: http://dx.doi.org/10.1590/S0004-27302007000700003
» http://dx.doi.org/10.1590/S0004-27302007000700003 -
265Friedlander AH, Yueh R, Littner MR. The prevalence of calcified carotid artery atheromas in patients with obstructive sleep apnea syndrome. J Oral Maxillofac Surg. 1998;56(8):950-4. PMID: 9710189.
-
266Friedlander AH, Friedlander IK, Yueh R, Littner MR. The prevalence of carotid atheromas seen on panoramic radiographs of patients with obstructive sleep apnea and their relation to risk factors for atherosclerosis. J Oral Maxillofac Surg. 1999;57(5):516-21. PMID: 10319824.
-
267Cilli A, Tatlicioglu T, Köktürk O. Nocturnal oxygen desaturation in coronary artery disease. Jpn Heart J. 1999;40(1):23-9. PMID: 10370394.
-
268Silvestrini M, Rizzato B, Placidi F, Baruffaldi R, Bianconi A, Diomedi M. Carotid artery wall thickness in patients with obstructive sleep apnea syndrome. Stroke. 2002;33(7):1782-5. PMID: 12105352.
-
269Nachtmann A, Stang A, Wang YM, Wondzinski E, Thilmann AF. Association of obstructive sleep apnea and stenotic artery disease in ischemic stroke patients. Atherosclerosis. 2003;169(2):301-7. PMID: 12921982.
-
270Hayashi M, Fujimoto K, Urushibata K, Uchikawa S, Imamura H, Kubo K. Nocturnal oxygen desaturation correlates with the severity of coronary atherosclerosis in coronary artery disease. Chest. 2003;124(3):936-41. PMID: 12970020.
-
271Suzuki T, Nakano H, Maekawa J, Okamoto Y, Ohnishi Y, Yamauchi M, et al. Obstructive sleep apnea and carotid-artery intima-media thickness. Sleep. 2004;27(1):129-33. PMID: 14998249.
-
272Schulz R, Seeger W, Fegbeutel C, Hüsken H, Bödeker RH, Tillmanns H, et al. Changes in extracranial arteries in obstructive sleep apnoea. Eur Respir J. 2005;25(1):69-74. doi: 10.1183/09031936.04.00030004.
» https://doi.org/10.1183/09031936.04.00030004 -
273Altin R, Ozdemir H, Mahmutyazicioglu K, Kart L, Uzun L, Ozer T, et al. Evaluation of carotid artery wall thickness with high-resolution sonography in obstructive sleep apnea syndrome. J Clin Ultrasound. 2005;33(2):80-6. doi: 10.1002/jcu.20093.
» https://doi.org/10.1002/jcu.20093 -
274Drager LF, Bortolotto LA, Lorenzi MC, Figueiredo AC, Krieger EM, Lorenzi-Filho G. Early signs of atherosclerosis in obstructive sleep apnea. Am J Respir Crit Care Med. 2005;172(5):613-8. doi: 10.1164/rccm.200503-340OC.
» https://doi.org/10.1164/rccm.200503-340OC -
275Minoguchi K, Yokoe T, Tazaki T, Minoguchi H, Tanaka A, Oda N, et al. Increased carotid intima-media thickness and serum inflammatory markers in obstructive sleep apnea.Am J Respir Crit Care Med. 2005;172(5):625-30. doi: 10.1164/rccm.200412-1652OC.
» https://doi.org/10.1164/rccm.200412-1652OC -
276Tian JL, Zhang Y, Wang Z, Cao L, Chen BY. [A study on non-invasive indexes of atherosclerosis in obstructive sleep apnea-hypopnea syndrome patients]. Zhonghua Jie He He Hu Xi Za Zhi. 2006;29(6):395-8. PMID: 17045022.
-
277Tanriverdi H, Evrengul H, Kara CO, Kuru O, Tanriverdi S, Ozkurt S, et al. Aortic stiffness, flow-mediated dilatation and carotid intima-media thickness in obstructive sleep apnea: non-invasive indicators of atherosclerosis. Respiration. 2006;73(6):741-50. doi: 10.1159/000093531.
» https://doi.org/10.1159/000093531 -
278Saletu M, Nosiska D, Kapfhammer G, Lalouschek W, Saletu B, Benesch T, et al. Structural and serum surrogate markers of cerebrovascular disease in obstructive sleep apnea (OSA): association of mild OSA with early atherosclerosis. J Neurol. 2006;253(6):746-52. doi: 10.1007/s00415-006-0110-6.
» https://doi.org/10.1007/s00415-006-0110-6 -
279Lu G, Xu ZW, Zhang YL, Yang ZJ, Zhang XL, Yin KS. Correlation among obstructive sleep apnea syndrome, coronary atherosclerosis and coronary heart disease.Chin Med J (Engl). 2007;120(18):1632-4. PMID: 17908485.
-
280Lu G, Xu ZW, Liu JN, Zhang YL, Yang ZJ, Zhang XL, et al. [A study on the association of obstructive sleep apnea hypopnea syndrome with coronary atherosclerosis and coronary heart disease]. Zhonghua Jie He He Hu Xi Za Zhi. 2007;30(3):178-81. PMID: 17572995.
-
281Szabóová E, Tomori Z, Donic V, Petrovicová J, Szabó P. Sleep apnoea inducing hypoxemia is associated with early signs of carotid atherosclerosis in males.Respir Physiol Neurobiol. 2007;155(2):121-7. doi: 10.1016/j.resp.2006.05.004.
» https://doi.org/10.1016/j.resp.2006.05.004 -
282Dziewas R, Ritter M, Usta N, Boentert M, Hor H, Dittrich R, et al. Atherosclerosis and obstructive sleep apnea in patients with ischemic stroke. Cerebrovasc Dis. 2007;24(1):122-6. doi: 10.1159/000103611.
» https://doi.org/10.1159/000103611 -
283Drager LF, Bortolotto LA, Figueiredo AC, Krieger EM, Lorenzi GF. Effects of continuous positive airway pressure on early signs of atherosclerosis in obstructive sleep apnea. Am J Respir Crit Care Med. 2007;176(7):706-12. doi: 10.1164/rccm.200703-500OC.
» https://doi.org/10.1164/rccm.200703-500OC -
284Wattanakit K, Boland L, Punjabi NM, Shahar E. Relation of sleep-disordered breathing to carotid plaque and intima-media thickness. Atherosclerosis. 2008;197(1):125-31. doi: 10.1016/j.atherosclerosis.2007.02.029.
» https://doi.org/10.1016/j.atherosclerosis.2007.02.029 -
285Lefebvre B, Pépin JL, Baguet JP, Tamisier R, Roustit M, Riedweg K, et al. Leukotriene B4: early mediator of atherosclerosis in obstructive sleep apnoea? Eur Respir J. 2008;32(1):113-20. doi: 10.1183/09031936.00137107.
» https://doi.org/10.1183/09031936.00137107 -
286Saletu M, Sauter C, Lalouschek W, Saletu B, Kapfhammer G, Benesch T, et al. Is excessive daytime sleepiness a predictor of carotid atherosclerosis in sleep apnea? Atherosclerosis. 2008;196(2):810-6. doi: 10.1016/j.atherosclerosis.2007.01.016.
» https://doi.org/10.1016/j.atherosclerosis.2007.01.016 -
287Protogerou AD, Laaban JP, Czernichow S, Kostopoulos C, Lekakis J, Safar ME, et al. Structural and functional arterial properties in patients with obstructive sleep apnoea syndrome and cardiovascular comorbidities. J Hum Hypertens. 2008;22(6):415-22. doi: 10.1038/sj.jhh.1002318.
» https://doi.org/10.1038/sj.jhh.1002318 -
288Drager LF, Bortolotto LA, Krieger EM, Lorenzi-Filho G. Additive effects of obstructive sleep apnea and hypertension on early markers of carotid atherosclerosis. Hypertension. 2009;53(1):64-9. doi: 10.1161/HYPERTENSIONAHA.108.119420.
» https://doi.org/10.1161/HYPERTENSIONAHA.108.119420 -
289Kong L, Guo XH. [The relation between obstructive sleep apnea hypopnea syndrome and the severity of coronary atherosclerosis in coronary artery disease]. Zhonghua Nei Ke Za Zhi. 2009;48(8):638-42. PMID: 19954054.
-
290Li C, Zhang XL, Liu H, Wang ZG, Yin KS. Association among plasma interleukin-18 levels, carotid intima- media thickness and severity of obstructive sleep apnea. Chin Med J (Engl). 2009;122(1):24-9. PMID: 19187612.
-
291Turmel J, Sériès F, Boulet LP, Poirier P, Tardif JC, Rodés-Cabeau J, et al. Relationship between atherosclerosis and the sleep apnea syndrome: an intravascular ultrasound study. Int J Cardiol. 2009;132(2):203-9. doi: 10.1016/j.ijcard.2007.11.063.
» https://doi.org/10.1016/j.ijcard.2007.11.063 -
292Kim SH, Cho GY, Baik I, Kim J, Kim SJ, Lee JB, et al. Association of coronary artery calcification with obstructive sleep apnea and obesity in middle-aged men. Nutr Metab Cardiovasc Dis. 2010;20(8):575-82. doi: 10.1016/j.numecd.2009.05.011.
» https://doi.org/10.1016/j.numecd.2009.05.011 -
293Monneret D, Pepin JL, Godin-Ribuot D, Ducros V, Baguet JP, Levy P, et al. Association of urinary 15-F2t-isoprostane level with oxygen desaturation and carotid intima-media thickness in nonobese sleep apnea patients. Free Radic Biol Med. 2010;48(4):619-25. doi: 10.1016/j.freeradbiomed.2009.12.008
» https://doi.org/10.1016/j.freeradbiomed.2009.12.008 -
294Tsuda H, Almeida FR, Tsuda T, Moritsuchi Y, Lowe AA. Cephalometric calcified carotid artery atheromas in patients with obstructive sleep apnea. Sleep Breath. 2010;14(4):365-70. doi: 10.1007/s11325-009-0324-9.
» https://doi.org/10.1007/s11325-009-0324-9 -
295Yun CH, Jung KH, Chu K, Kim SH, Ji KH, Park HK, et al. Increased circulating endothelial microparticles and carotid atherosclerosis in obstructive sleep apnea. J Clin Neurol. 2010;6(2):89-98. doi: 10.3988/jcn.2010.6.2.89.
» https://doi.org/10.3988/jcn.2010.6.2.89 -
296Steiropoulos P, Bogiatzi C, Archontogeorgis K, Nena E, Xanthoudaki M, Boglou P, et al. Is there evidence of early vascular disease in patients with obstructive sleep apnoea without known comorbidities? Preliminary findings. Open Cardiovasc Med J. 2013;7:61-8. doi: 10.2174/1874192401307010061.
» https://doi.org/10.2174/1874192401307010061 -
297Akyuz A, Oran M, Alpsoy S, Mutlu LC, Akkoyun DC, Guzel S, et al. Association between serum fetuin-A levels, carotid artery stiffness, and intima-media thickness in patients with normotensive obstructive sleep apnea syndrome. Angiology. 2014;65(7):607-13. doi: 10.1177/0003319713497421.
» https://doi.org/10.1177/0003319713497421 -
298Iannuzzi A, Licenziati MR, De Michele F, Verga MC, Santoriello C, Di Buono L, et al. C-reactive protein and carotid intima-media thickness in children with sleep disordered breathing. J Clin Sleep Med. 2013;9(5):493-8. doi: 10.5664/jcsm.2674.
» https://doi.org/10.5664/jcsm.2674 -
299Apaydin M, Ayik SO, Akhan G, Peker S, Uluc E. Carotid intima-media thickness increase in patients with habitual simple snoring and obstructive sleep apnea syndrome is associated with metabolic syndrome. J Clin Ultrasound. 2013;41(5):290-6. doi: 10.1002/jcu.22040.
» https://doi.org/10.1002/jcu.22040 -
300Kent BD, Garvey JF, Ryan S, Nolan G, Dodd JD, McNicholas WT. Severity of obstructive sleep apnoea predicts coronary artery plaque burden: a coronary computed tomographic angiography study. Eur Respir J. 2013;42(5):1263-70. doi: 10.1183/09031936.00094812.
» https://doi.org/10.1183/09031936.00094812 -
301Arik B, Inci MF, Gumus C, Varol K, Ege MR, Dogan OT, et al. Advanced age and apnea-hypopnea index predict subclinical atherosclerosis in patients with obstructive sleep apnea syndrome. Multidiscip Respir Med. 2013;8(1):9. doi: 10.1186/2049-6958-8-9.
» https://doi.org/10.1186/2049-6958-8-9 -
302Sforza E, Boissier C, Martin MS, Feasson S, Barthélémy JC, Roche F. Carotid artery atherosclerosis and sleep disordered breathing in healthy elderly subjects: the Synapse cohort. Sleep Med. 2013;14(1):66-70. doi: 10.1016/j.sleep.2012.08.016.
» https://doi.org/10.1016/j.sleep.2012.08.016 -
303Sharma S, Gebregziabher M, Parker AT, Abro JA, Armstrong AM, Schoepf UJ. Independent association between obstructive sleep apnea and noncalcified coronary plaque demonstrated by noninvasive coronary computed tomography angiography. Clin Cardiol. 2012;35(10):641-5. doi: 10.1002/clc.22057.
» https://doi.org/10.1002/clc.22057 -
304Tan TY, Liou CW, Friedman M, Lin HC, Chang HW, Lin MC. Factors associated with increased carotid intima-media thickness in obstructive sleep apnea/hypopnea syndrome. Neurologist. 2012;18(5):277-81. doi: 10.1097/NRL.0b013e3182675344.
» https://doi.org/10.1097/NRL.0b013e3182675344 -
305Stanke-Labesque F, Pépin JL, de Jouvencel T, Arnaud C, Baguet JP, Petri MH, et al. Leukotriene B4 pathway activation and atherosclerosis in obstructive sleep apnea. J Lipid Res. 2012;53(9):1944-51. doi: 10.1194/jlr.P022814.
» https://doi.org/10.1194/jlr.P022814 -
306Chang TI, Tanner JM, Harada ND, Garrett NR, Friedlander AH. Prevalence of calcified carotid artery atheromas on the panoramic images of patients with syndrome Z, coexisting obstructive sleep apnea, and metabolic syndrome. Oral Surg Oral Med Oral Pathol Oral Radiol. 2012;113(1):134-41. doi: 10.1016/j.tripleo.2011.07.039.
» https://doi.org/10.1016/j.tripleo.2011.07.039 -
307Kylintireas I, Craig S, Nethononda R, Kohler M, Francis J, Choudhury R, et al. Atherosclerosis and arterial stiffness in obstructive sleep apnea--a cardiovascular magnetic resonance study. Atherosclerosis. 2012;222(2):483-9. doi: 10.1016/j.atherosclerosis.2012.03.036.
» https://doi.org/10.1016/j.atherosclerosis.2012.03.036 -
308Ciccone MM, Scicchitano P, Mitacchione G, Zito A, Gesualdo M, Caputo P, et al. Is there a correlation between OSAS duration/severity and carotid intima-media thickness? Respir Med. 2012;106(5):740-6. doi: 10.1016/j.rmed.2011.12.016.
» https://doi.org/10.1016/j.rmed.2011.12.016 -
309Monneret D, Tamisier R, Ducros V, Garrel C, Levy P, Baguet JP, et al. The impact of obstructive sleep apnea on homocysteine and carotid remodeling in metabolic syndrome. Respir Physiol Neurobiol. 2012;180(2-3):298-304. doi: 10.1016/j.resp.2011.12.009.
» https://doi.org/10.1016/j.resp.2011.12.009 -
310Kepez A, Niksarlioglu EY, Hazirolan T, Hayran M, Kocabas U, Demir AU, et al. Evaluation of association between obstructive sleep apnea and coronary risk scores predicted by tomographic coronary calcium scoring in asymptomatic patients. Anadolu Kardiyol Derg. 2011;11(5):428-35. doi: 10.5152/akd.2011.106.
» https://doi.org/10.5152/akd.2011.106 -
311Weinreich G, Wessendorf TE, Erdmann T, Moebus S, Dragano N, Lehmann N, et al; Heinz Nixdorf Recall (HNR) study group. Association of obstructive sleep apnoea with subclinical coronary atherosclerosis. Atherosclerosis. 2013;231(2):191-7. doi: 10.1016/j.atherosclerosis.2013.09.011.
» https://doi.org/10.1016/j.atherosclerosis.2013.09.011 -
312Kwon Y, Duprez DA, Jacobs DR, Nagayoshi M, McClelland RL, Shahar E, et al. Obstructive sleep apnea and progression of coronary artery calcium: the multi-ethnic study of atherosclerosis study. J Am Heart Assoc. 2014;3(5):e001241. doi: 10.1161/JAHA.114.001241.
» https://doi.org/10.1161/JAHA.114.001241 -
313Gunnarsson SI, Peppard PE, Korcarz CE, Barnet JH, Aeschlimann SE, Hagen EW, et al. Obstructive sleep apnea is associated with future subclinical carotid artery disease: thirteen-year follow-up from the Wisconsin sleep cohort. Arterioscler Thromb Vasc Biol. 2014;34(10):2338-42. doi: 10.1161/ATVBAHA.114.303965.
» https://doi.org/10.1161/ATVBAHA.114.303965 -
314Rahangdale S, Yeh SY, Novack V, Stevenson K, Barnard MR, Furman MI, et al. The influence of intermittent hypoxemia on platelet activation in obese patients with obstructive sleep apnea. J Clin Sleep Med. 2011;7(2):172-8. PMID: 21509332.
-
315von Känel R, Dimsdale JE. Hemostatic alterations in patients with obstructive sleep apnea and the implications for cardiovascular disease. Chest. 2003;124(5):1956-67. PMID: 14605073.
-
316Hui DS, Ko FW, Fok JP, Chan MC, Li TS, Tomlinson B, et al. The effects of nasal continuous positive airway pressure on platelet activation in obstructive sleep apnea syndrome. Chest. 2004;125(5):1768-75. PMID: 15136389.
-
317von Känel R, Loredo JS, Ancoli-Israel S, Dimsdale JE. Association between sleep apnea severity and blood coagulability: treatment effects of nasal continuous positive airway pressure. Sleep Breath. 2006;10(3):139-46. doi: 10.1007/s11325-006-0060-3.
» https://doi.org/10.1007/s11325-006-0060-3 -
318Bradley TD, Floras JS. Obstructive sleep apnoea and its cardiovascular consequences. Lancet. 2009;373(9657):82-93. doi: 10.1016/S0140-6736(08)61622-0.
» https://doi.org/10.1016/S0140-6736(08)61622-0 -
319Franklin KA, Nilsson JB, Sahlin C, Naslund U. Sleep apnoea and nocturnal angina. Lancet. 1995;345(8957):1085-7. PMID: 7715342.
-
320Peled N, Abinader EG, Pillar G, Sharif D, Lavie P. Nocturnal ischemic events in patients with obstructive sleep apnea syndrome and ischemic heart disease: effects of continuous positive air pressure treatment. J Am Coll Cardiol. 1999;34(6):1744-9. PMID: 10577565.
-
321Hanly P, Sasson Z, Zuberi N, Lunn K. ST-segment depression during sleep in obstructive sleep apnea. Am J Cardiol. 1993;71(15):1341-5. PMID: 8498378.
-
322Philip P, Guilleminault C. ST segment abnormality, angina during sleep and obstructive sleep apnea. Sleep. 1993;16(6):558-9. PMID: 8235241.
-
323Araújo CM, Solimene MC, Grupi CJ, Genta PR, Lorenzi-Filho G, Da Luz PL. Evidence that the degree of obstructive sleep apnea may not increase myocardial ischemia and arrhythmias in patients with stable coronary artery disease. Clinics (Sao Paulo). 2009;64(3):223-30. doi: http://dx.doi.org/10.1590/S1807-59322009000300013
» http://dx.doi.org/10.1590/S1807-59322009000300013 -
324Gami AS, Svatikova A, Wolk R, Olson EJ, Duenwald CJ, Jaffe AS, et al. Cardiac troponin T in obstructive sleep apnea. Chest. 2004;125(6):2097-100. PMID: 15189927.
-
325Querejeta Roca G, Redline S, Punjabi N, Claggett B, Ballantyne CM, Solomon SD, et al. Sleep apnea is associated with subclinical myocardial injury in the community. The ARIC-SHHS study. Am J Respir Crit Care Med. 2013;188(12):1460-5. doi: 10.1164/rccm.201309-1572OC.
» https://doi.org/10.1164/rccm.201309-1572OC -
326Einvik G, Røsjø H, Randby A, Namtvedt SK, Hrubos-Strøm H, Brynildsen J, et al. Severity of obstructive sleep apnea is associated with cardiac troponin I concentrations in a community-based sample: data from the Akershus Sleep Apnea Project. Sleep. 2014;37(6):1111-6, 1116A-1116B. doi: 10.5665/sleep.3772.
» https://doi.org/10.5665/sleep.3772 -
327Geovanini GR, Pereira AC, Gowdak LH, Dourado LO, Poppi NT, Venturini G, et al. Obstructive sleep apnoea is associated with myocardial injury in patients with refractory angina. Heart. 2016;102(15):1193-9. doi: 10.1136/heartjnl-2015-309009.
» https://doi.org/10.1136/heartjnl-2015-309009 -
328Kuniyoshi FH, Garcia-Touchard A, Gami AS, Romero-Corral A, van der Walt C, Pusalavidyasagar S, et al. Day-night variation of acute myocardial infarction in obstructive sleep apnea. J Am Coll Cardiol. 2008;52(5):343-6. doi: 10.1016/j.jacc.2008.04.027.
» https://doi.org/10.1016/j.jacc.2008.04.027 -
329Gami AS, Howard DE, Olson EJ, Somers VK. Day-night pattern of sudden death in obstructive sleep apnea. N Engl J Med. 2005;352(12):1206-14. doi: 10.1056/NEJMoa041832.
» https://doi.org/10.1056/NEJMoa041832 -
330Campos-Rodriguez F, Martinez-Garcia MA, de la Cruz-Moron I, Almeida-Gonzalez C, Catalan-Serra P, Montserrat JM. Cardiovascular mortality in women with obstructive sleep apnea with or without continuous positive airway pressure treatment: a cohort study. Ann Intern Med. 2012;156(2):115-22. doi: 10.7326/0003-4819-156-2-201201170-00006.
» https://doi.org/10.7326/0003-4819-156-2-201201170-00006 -
331Valham F, Mooe T, Rabben T, Stenlund H, Wiklund U, Franklin KA. Increased risk of stroke in patients with coronary artery disease and sleep apnea: a 10-year follow-up. Circulation. 2008;118(9):955-60. doi: 10.1161/CIRCULATIONAHA.108.783290.
» https://doi.org/10.1161/CIRCULATIONAHA.108.783290 -
332Lee CH, Sethi R, Li R, Ho HH, Hein T, Jim MH, et al. Obstructive sleep apnea and cardiovascular events after percutaneous coronary intervention. Circulation. 2016;133(21):2008-17. doi: 10.1161/CIRCULATIONAHA.115.019392.
» https://doi.org/10.1161/CIRCULATIONAHA.115.019392 -
333Wu X, Lv S, Yu X, Yao L, Mokhlesi B, Wei Y. Treatment of OSA reduces the risk of repeat revascularization after percutaneous coronary intervention. Chest. 2015;147(3):708-18. doi: 10.1378/chest.14-1634.
» https://doi.org/10.1378/chest.14-1634 -
334Peker Y, Glantz H, Eulenburg C, Wegscheider K, Herlitz J, Thunström E. Effect of positive airway pressure on cardiovascular outcomes in coronary artery disease patients with nonsleepy obstructive sleep apnea. The RICCADSA Randomized Controlled Trial. Am J Respir Crit Care Med. 2016;194(5):613-20. doi: 10.1164/rccm.201601-0088OC.
» https://doi.org/10.1164/rccm.201601-0088OC -
335McEvoy RD, Antic NA, Heeley E, Luo Y, Ou Q, Zhang X, et al; SAVE Investigators and Coordinators. CPAP for prevention of cardiovascular events in obstructive sleep apnea. N Engl J Med. 2016;375(10):919-31. doi: 10.1056/NEJMoa1606599.
» https://doi.org/10.1056/NEJMoa1606599 -
336Bassetti C, Aldrich MS. Sleep apnoea in acute cerebrovascular diseases: final report on 128 patients. Sleep. 1999;22(2):217-23. PMID: 10201066.
-
337Somers VK, White DP, Amin R, Abraham WT, Costa F, Culebras A, et al; American Heart Association Council for High Blood Pressure Research Professional Education Committee, Council on Clinical Cardiology; American Heart Association Stroke Council; American Heart Association Council on Cardiovascular Nursing; American College of Cardiology Foundation. Sleep apnea and cardiovascular disease: an American Heart Association/American College of Cardiology Foundation Scientific Statement from the American Heart Association Council for High Blood Pressure Research Professional Education Committee, Council on Clinical Cardiology, Stroke Council, and Council on Cardiovascular Nursing. In collaboration with the National Heart, Lung, and Blood Institute National Center on Sleep Disorders Research (National Institutes of Health). Circulation. 2008;118(10):1080-111. doi: 10.1161/CIRCULATIONAHA.107.189375. Erratum in: Circulation. 2009;119(12):e380.
» https://doi.org/10.1161/CIRCULATIONAHA.107.189375 -
338Capampangan DJ, Wellik KE, Parish JM, Aguilar MI, Snyder CR, et al. Is obstructive sleep apnea an independent risk factor for stroke? A critically appraised topic. Neurologist. 2010;16(4):269-73. doi: 10.1097/NRL.0b013e3181e5a66c.
» https://doi.org/10.1097/NRL.0b013e3181e5a66c -
339Loke YK, Brown JW, Kwok CS, Niruban A, Myint PK. Association of obstructive sleep apnea with risk of serious cardiovascular events: a systematic review and meta-analysis. Circ Cardiovasc Qual Outcomes. 2012;5(5):720-8. doi: 10.1161/CIRCOUTCOMES.111.964783.
» https://doi.org/10.1161/CIRCOUTCOMES.111.964783 -
340Dong JY, Zhang YH, Qin LQ. Obstructive sleep apnea and cardiovascular risk: meta-analysis of prospective cohort studies. Atherosclerosis. 2013;229(2):489-95. doi: 10.1016/j.atherosclerosis.2013.04.026.
» https://doi.org/10.1016/j.atherosclerosis.2013.04.026 -
341Ryan CM, Bayley M, Green R, Murray BJ, Bradley TD. Influence of continuous positive airway pressure on outcomes of rehabilitation in stroke patients with obstructive sleep apnea. Stroke. 2011;42(4):1062-7. doi: 10.1161/STROKEAHA.110.597468.
» https://doi.org/10.1161/STROKEAHA.110.597468 -
342Martínez-García MA, Campos-Rodríguez F, Soler-Cataluña JJ, Catalán-Serra P, Román-Sánchez P, Montserrat JM. Increased incidence of nonfatal cardiovascular events in stroke patients with sleep apnoea: effect of CPAP treatment. Eur Respir J. 2012;39(4):906-12. doi: 10.1183/09031936.00011311.
» https://doi.org/10.1183/09031936.00011311 -
343Parra O, Sánchez-Armengol A, Bonnin M, Arboix A, Campos-Rodríguez F, Pérez-Ronchel J, et al. Early treatment of obstructive apnoea and stroke outcome: a randomised controlled trial. Eur Respir J. 2011;37(5):1128-36. doi: 10.1183/09031936.00034410.
» https://doi.org/10.1183/09031936.00034410 -
344Young T, Finn L, Peppard PE, Szklo-Coxe M, Austin D, Nieto FJ, et al. Sleep disordered breathing and mortality: eighteen-year follow-up of the Wisconsin sleep cohort. Sleep. 2008;31(8):1071-8. PMID: 18714778.
-
345Marshall NS, Wong KK, Liu PY, Cullen SR, Knuiman MW, Grunstein RR. Sleep apnea as an independent risk factor for all-cause mortality: the Busselton Health Study.Sleep. 2008;31(8):1079-85. PMID: 18714779.
-
346Punjabi NM, Caffo BS, Goodwin JL, Gottlieb DJ, Newman AB, O'Connor GT, et al. Sleep-disordered breathing and mortality: a prospective cohort study. PLoS Med. 2009;6(8):e1000132. doi: 10.1371/journal.pmed.1000132.
» https://doi.org/10.1371/journal.pmed.1000132 -
347Martínez-García MA, Soler-Cataluña JJ, Ejarque-Martínez L, Soriano Y, Román-Sánchez P, Illa FB, et al. Continuous positive airway pressure treatment reduces mortality in patients with ischemic stroke and obstructive sleep apnea: a 5-year follow-up study. Am J Respir Crit Care Med. 2009;180(1):36-41. doi: 10.1164/rccm.200808-1341OC.
» https://doi.org/10.1164/rccm.200808-1341OC -
348Martínez-García MA, Campos-Rodríguez F, Catalán-Serra P, Soler-Cataluña JJ, Almeida-Gonzalez C, De la Cruz Morón I, et al. Cardiovascular mortality in obstructive sleep apnea in the elderly: role of long-term continuous positive airway pressure treatment: a prospective observational study. Am J Respir Crit Care Med. 2012;186(9):909-16. doi: 10.1164/rccm.201203-0448OC.
» https://doi.org/10.1164/rccm.201203-0448OC -
349Ge X, Han F, Huang Y, Zhang Y, Yang T, Bai C, et al. Is obstructive sleep apnea associated with cardiovascular and all-cause mortality? PLoS One. 2013;8(7):e69432. doi: 10.1371/journal.pone.0069432.
» https://doi.org/10.1371/journal.pone.0069432 -
350Lavie P, Lavie L, Herer P. All-cause mortality in males with sleep apnoea syndrome: declining mortality rates with age. Eur Respir J. 2005;25(3):514-20. doi: 10.1183/09031936.05.00051504.
» https://doi.org/10.1183/09031936.05.00051504 -
351Marcus CL, Brooks LJ, Draper KA, Gozal D, Halbower AC, Jones J, et al; American Academy of Pediatrics. Diagnosis and management of childhood obstructive sleep apnea syndrome. Pediatrics. 2012;130(3):e714-55. doi: 10.1542/peds.2012-1672.
» https://doi.org/10.1542/peds.2012-1672 -
352Pack AI, Gislason T. Obstructive sleep apnea and cardiovascular disease: a perspective and future directions. Prog Cardiovasc Dis. 2009;51(5):434-51. doi: 10.1016/j.pcad.2009.01.002.
» https://doi.org/10.1016/j.pcad.2009.01.002 -
353Vlahandonis A, Walter LM, Horne RS. Does treatment of SDB in children improve cardiovascular outcome? Sleep Med Rev. 2013 ;17(1):75-85. doi: 10.1016/j.smrv.2012.04.004.
» https://doi.org/10.1016/j.smrv.2012.04.004 -
354Walter LM, Nixon GM, Davey MJ, Anderson V, Walker AM, Horne RS. Autonomic dysfunction in children with sleep disordered breathing. Sleep Breath. 2013;17(2):605-13. doi: 10.1007/s11325-012-0727-x.
» https://doi.org/10.1007/s11325-012-0727-x -
355Walter LM, Yiallourou SR, Vlahandonis A, Sands SA, Johnson CA, Nixon GM, et al. Impaired blood pressure control in children with obstructive sleep apnea. Sleep Med. 2013;14(9):858-66. doi: 10.1016/j.sleep.2013.01.015.
» https://doi.org/10.1016/j.sleep.2013.01.015 -
356Muzumdar HV, Sin S, Nikova M, Gates G, Kim D, Arens R. Changes in heart rate variability after adenotonsillectomy in children with obstructive sleep apnea. Chest. 2011;139(5):1050-9. doi: 10.1378/chest.10-1555.
» https://doi.org/10.1378/chest.10-1555 -
357O'Brien LM, Gozal D. Autonomic dysfunction in children with sleep-disordered breathing. Sleep. 2005;28(6):747-52. PMID: 16477962.
-
358Gozal D, Kheirandish-Gozal L, Serpero LD, Sans Capdevila O, Dayyat E. Obstructive sleep apnea and endothelial function in school-aged nonobese children: effect of adenotonsillectomy. Circulation. 2007;116(20):2307-14. doi: 10.1161/CIRCULATIONAHA.107.696823.
» https://doi.org/10.1161/CIRCULATIONAHA.107.696823 -
359Kheirandish-Gozal L, Capdevila OS, Tauman R, Gozal D. Plasma C-reactive protein in nonobese children with obstructive sleep apnea before and after adenotonsillectomy. J Clin Sleep Med. 2006;2(3):301-4. PMID: 17410279.
-
360Li AM, Chan MH, Yin J, So HK, Ng SK, Chan IH, et al. C-reactive protein in children with obstructive sleep apnea and the effects of treatment. Pediatr Pulmonol. 2008;43(1):34-40. doi: 10.1002/ppul.20732.
» https://doi.org/10.1002/ppul.20732 -
361Gozal D, Serpero LD, Kheirandish-Gozal L, Capdevila OS, Khalyfa A, Tauman R. Sleep measures and morning plasma TNF-alpha levels in children with sleep-disordered breathing. Sleep. 2010;33(3):319-25. PMID: 20337189.
-
362Gozal D, Serpero LD, Sans Capdevila O, Kheirandish-Gozal L. Systemic inflammation in non-obese children with obstructive sleep apnea. Sleep Med. 2008;9(3):254-9. doi: 10.1016/j.sleep.2007.04.013.
» https://doi.org/10.1016/j.sleep.2007.04.013 -
363Verhulst SL, Aerts L, Jacobs S, Schrauwen N, Haentjens D, Claes R, et al. Sleep-disordered breathing, obesity, and airway inflammation in children and adolescents. Chest 2008;134(6):1169-75. doi: 10.1378/chest.08-0535.
» https://doi.org/10.1378/chest.08-0535 -
364Chu L, Li Q. The evaluation of adenotonsillectomy on TNF-? and IL-6 levels in obese children with obstructive sleep apnea. Int J Pediatr Otorhinolaryngol. 2013;77(5):690-4. doi: 10.1016/j.ijporl.2013.01.019.
» https://doi.org/10.1016/j.ijporl.2013.01.019 -
365Gozal D, Capdevila OS, Kheirandish-Gozal L. Metabolic alterations and systemic inflammation in obstructive sleep apnea among nonobese and obese prepubertal children. Am J Respir Crit Care Med. 2008;177(10):1142-9. doi: 10.1164/rccm.200711-1670OC.
» https://doi.org/10.1164/rccm.200711-1670OC -
366Waters KA, Sitha S, O'brien LM, Bibby S, de Torres C, Vella S, et al. Follow-up on metabolic markers in children treated for obstructive sleep apnea. Am J Respir Crit Care Med. 2006;174(4):455-60. doi: 10.1164/rccm.200401-110OC.
» https://doi.org/10.1164/rccm.200401-110OC -
367O'Driscoll DM, Foster AM, Ng ML, Yang JS, Bashir F, Nixon GM, et al. Acute cardiovascular changes with obstructive events in children with sleep disordered breathing. Sleep. 2009;32(10):1265-71. PMID: 19848356.
-
368Enright PL, Goodwin JL, Sherrill DL, Quan JR, Quan SF; Tucson Children's Assessment of Sleep Apnea study. Blood pressure elevation associated with sleep-related breathing disorder in a community sample of white and Hispanic children: the Tucson Children's Assessment of Sleep Apnea study. Arch Pediatr Adolesc Med. 2003;157(9):901-4. doi: 10.1001/archpedi.157.9.901.
» https://doi.org/10.1001/archpedi.157.9.901 -
369Kwok KL, Ng DK, Cheung YF. BP and arterial distensibility in children with primary snoring. Chest. 2003;123(5):1561-6. PMID: 12740274.
-
370Li AM, Au CT, Ho C, Fok TF, Wing YK. Blood pressure is elevated in children with primary snoring. J Pediatr. 2009;155(3):362-8. doi: 10.1016/j.jpeds.2009.03.041.
» https://doi.org/10.1016/j.jpeds.2009.03.041 -
371Amin RS, Carroll JL, Jeffries JL, Grone C, Bean JA, Chini B, et al. Twenty-four-hour ambulatory blood pressure in children with sleep-disordered breathing. Am J Respir Crit Care Med. 2004;169(8):950-6. doi: 10.1164/rccm.200309-1305OC.
» https://doi.org/10.1164/rccm.200309-1305OC -
372Leung LC, Ng DK, Lau MW, Chan CH, Kwok KL, Chow PY, et al. Twenty-four-hour ambulatory BP in snoring children with obstructive sleep apnea syndrome. Chest. 2006;130(4):1009-17. doi: 10.1378/chest.130.4.1009.
» https://doi.org/10.1378/chest.130.4.1009 -
373Kang KT, Chiu SN, Weng WC, Lee PL, Hsu WC. comparisons of office and 24-hour ambulatory blood pressure monitoring in children with obstructive sleep apnea. J Pediatr. 2017 Mar;182:177-83. doi: 10.1016/j.jpeds.2016.11.032
» https://doi.org/10.1016/j.jpeds.2016.11.032 -
374Horne RS, Yang JS, Walter LM, Richardson HL, O'Driscoll DM, Foster AM, et al. Elevated blood pressure during sleep and wake in children with sleep-disordered breathing. Pediatrics. 2011;128(1):e85-92. doi: 10.1542/peds.2010-3431.
» https://doi.org/10.1542/peds.2010-3431 -
375Kwok KL, Ng DK, Chan CH. Cardiovascular changes in children with snoring and obstructive sleep apnoea. Ann Acad Med Singapore. 2008;37(8):715-21. PMID: 18797568.
-
376Nisbet LC, Yiallourou SR, Nixon GM, Biggs SN, Davey MJ, Trinder J, et al. Characterization of the acute pulse transit time response to obstructive apneas and hypopneas in preschool children with sleep-disordered breathing. Sleep Med. 2013;36(8):1219-26. doi: 10.5665/sleep.2890.
» https://doi.org/10.5665/sleep.2890 -
377Bao W, Threefoot SA, Srinivasan SR, Berenson GS. Essential hypertension predicted by tracking of elevated blood pressure from childhood to adulthood: the Bogalusa Heart Study. Am J Hypertens. 1995;8(7):657-65. doi: 10.1016/0895-7061(95)00116-7.
» https://doi.org/10.1016/0895-7061(95)00116-7 -
378Sun SS, Grave GD, Siervogel RM, Pickoff AA, Arslanian SS, Daniels SR. Systolic blood pressure in childhood predicts hypertension and metabolic syndrome later in life. Pediatrics. 2007;119(2):237-46. doi: 10.1542/peds.2006-2543.
» https://doi.org/10.1542/peds.2006-2543 -
379Archbold KH, Vasquez MM, Goodwin JL, Quan SF. Effects of sleep patterns and obesity on increases in blood pressure in a 5-year period: report from the Tucson Children's Assessment of Sleep Apnea Study. J Pediatr. 2012;161(1):26-30. doi: 10.1016/j.jpeds.2011.12.034.
» https://doi.org/10.1016/j.jpeds.2011.12.034 -
380Ng DK, Wong JC, Chan CH, Leung LC, Leung SY. Ambulatory blood pressure before and after adenotonsillectomy in children with obstructive sleep apnea. Sleep Med. 2010;11(7):721-5. doi: 10.1016/j.sleep.2009.10.007.
» https://doi.org/10.1016/j.sleep.2009.10.007 -
381Apostolidou MT, Alexopoulos EI, Damani E, Liakos N, Chaidas K, Boultadakis E, et al. Absence of blood pressure, metabolic, and inflammatory marker changes after adenotonsillectomy for sleep apnea in Greek children. Pediatr Pulmonol. 2008;43(6):550-60. doi: 10.1002/ppul.20808.
» https://doi.org/10.1002/ppul.20808 -
382Amin R, Anthony L, Somers V, Fenchel M, McConnell K, Jefferies J, et al. Growth velocity predicts recurrence of sleep-disordered breathing 1 year after adenotonsillectomy. Am J Respir Crit Care Med 2008;177(6):654-9. doi: 10.1164/rccm.200710-1610OC.
» https://doi.org/10.1164/rccm.200710-1610OC -
383Espinak-Sierra J, Vela-Bueno A, Luque-Otero M. Periodic leg movements in sleep in essential hypertension. Psychiatry Clin Neurosci. 1997;51(3):103-7. PMID: 9225372.
-
384Winkelman JW, Shahar E, Sharief I, Gottlieb DJ. Association of restless legs syndrome and cardiovascular disease in the Sleep Heart Health Study. Neurology. 2008;70(1):35-42. doi: 10.1212/01.wnl.0000287072.93277.c9.
» https://doi.org/10.1212/01.wnl.0000287072.93277.c9 -
385Hartzell K, Avis K, Lozano D, Feig D. Obstructive sleep apnea and periodic limb movement disorder in a population of children with hypertension and/or nocturnal nondipping blood pressures. J Am Soc Hypertens. 2016;10(2):101-7. doi: 10.1016/j.jash.2015.11.010.
» https://doi.org/10.1016/j.jash.2015.11.010 -
386Amin RS, Kimball TR, Bean JA, Jeffries JL, Willging JP, Cotton RT, et al. Left ventricular hypertrophy and abnormal ventricular geometry in children and adolescents with obstructive sleep apnea. Am J Respir Crit Care Med. 2002;165(10):1395-9. doi: 10.1164/rccm.2105118.
» https://doi.org/10.1164/rccm.2105118 -
387Amin RS, Kimball TR, Kalra M, Jeffries JL, Carroll JL, Bean JA, et al. Left ventricular function in children with sleep-disordered breathing. Am J Cardiol. 2005;95(6):801-4. doi: 10.1016/j.amjcard.2004.11.044.
» https://doi.org/10.1016/j.amjcard.2004.11.044 -
388Görür K, Döven O, Unal M, Akkus N, Ozcan C. Preoperative and postoperative cardiac and clinical findings of patients with adenotonsillar hypertrophy. Int J Pediatr Otorhinolaryngol. 2001;59(1):41-6. PMID: 11376817.
-
389Ugur MB, Dogan SM, Sogut A, Uzun L, Cinar F, Altin R, Aydin M. Effect of adenoidectomy and/or tonsillectomy on cardiac functions in children with obstructive sleep apnea. ORL J Otorhinolaryngol Relat Spec. 2008;70(3):202-8. doi: 10.1159/000124295.
» https://doi.org/10.1159/000124295 -
390Miman MC, Kirazli T, Ozyurek R. Doppler echocardiography in adenotonsillar hypertrophy. Int J Pediatr Otorhinolaryngol. 2000;54(1):21-6. PMID: 10960692.
-
391Ramakrishna S, Ingle VS, Patel S, Bhat P, Dada JE, Shah FA, et al. Reversible cardio-pulmonary changes due to adeno-tonsilar hypertrophy. Int J Pediatr Otorhinolaryngol. 2000;55(3):203-6. PMID: 11035178.
-
392Sofer S, Weinhouse E, Tal A, Wanderman KL, Margulis G, Leiberman A, et al. Cor pulmonale due to adenoidal or tonsillar hypertrophy or both in children. Noninvasive diagnosis and follow-up. Chest. 1988;93(1):119-22. PMID: 3335141.
-
393Switzer AJ, Hess DC, Nichols FT, Adams RJ. Pathophysiology and treatment of stroke in sickle-cell disease: present and future. Lancet Neurol. 2006;5(6):501-12. doi: 10.1016/S1474-4422(06)70469-0.
» https://doi.org/10.1016/S1474-4422(06)70469-0 -
394Kral MC, Brown RT, Nietert PJ, Abboud MR, Jackson SM, Hynd GW. Transcranial Doppler ultrasonography and neurocognitive functioning in children with sickle cell disease. Pediatrics. 2003;112(2):324-31. PMID: 12897282.
-
395Hill CM, Hogan AM, Onugha N, Harrison D, Cooper S, McGrigor VJ, et al. Increased cerebral blood flow velocity in children with mild sleep-disordered breathing: a possible association with abnormal neuropsychological function. Pediatrics. 2006;118(4):e1100-8. doi: 10.1542/peds.2006-0092.
» https://doi.org/10.1542/peds.2006-0092 -
396Kirkham FJ, Hewes DK, Prengler M, Wade A, Lane R, Evans JP. Nocturnal hypoxaemia and central-nervous-system events in sickle-cell disease. Lancet 2001;357(9269):1656-9. PMID: 11425370.
-
397Moreira GA. Respiratory repercussions of sickle cell anemia. J Bras Pneumol. 2007;33(3):18-20. doi: http://dx.doi.org/10.1590/S1806-37132007000300002
» http://dx.doi.org/10.1590/S1806-37132007000300002 -
398Bradley TD, Floras JS. Sleep apnea and heart failure: Part II: central sleep apnea. Circulation. 2003;107(13):1822-6. doi: 10.1161/01.CIR.0000061758.05044.64.
» https://doi.org/10.1161/01.CIR.0000061758.05044.64 -
399Naughton MT, Kee K. Sleep apnoea in heart failure: To treat or not to treat? Respirology. 2017;22(2):217-229. doi: 10.1111/resp.12964.
» https://doi.org/10.1111/resp.12964 -
400Lanfranchi PA, Braghiroli A, Bosimini E, Mazzuero G, Colombo R, Donner CF, et al. Prognostic value of nocturnal Cheyne-Stokes respiration in chronic heart failure. Circulation. 1999;99(11):1435-40. PMID: 10086966.
-
401Javaheri S, Parker TJ, Wexler L, Liming JD, Lindower P, Roselle GA. Effect of theophylline on sleep-disordered breathing in heart failure. N Engl J Med. 1996;335(8):562-7. doi: 10.1056/NEJM199608223350805.
» https://doi.org/10.1056/NEJM199608223350805 -
402Javaheri S. Acetazolamide improves central sleep apnea in heart failure: a double-blind, prospective study. Am J Respir Crit Care Med. 2006;173(2):234-7. doi: 10.1164/rccm.200507-1035OC.
» https://doi.org/10.1164/rccm.200507-1035OC -
403Fontana M, Emdin M, Giannoni A, Iudice G, Baruah R, Passino C. Effect of acetazolamide on chemosensitivity, Cheyne-Stokes respiration, and response to effort in patients with heart failure. Am J Cardiol. 2011;107(11):1675-80. doi: 10.1016/j.amjcard.2011.01.060.
» https://doi.org/10.1016/j.amjcard.2011.01.060 -
404Costanzo MR, Ponikowski P, Javaheri S, Augostini R, Goldberg L, Holcomb R, et al; remedé System Pivotal Trial Study Group. Transvenousneurostimulation for central sleep apnoea: a randomised controlled trial. Lancet. 2016;388(10048):974-82. doi: 10.1016/S0140-6736(16)30961-8.
» https://doi.org/10.1016/S0140-6736(16)30961-8 -
405Sinha AM, Skobel EC, Breithardt OA, Norra C, Markus KU, Breuer C, et al. Cardiac resynchronization therapy improves central sleep apnea and Cheyne-Stokes respiration in patients with chronic heart failure. J Am Coll Cardiol. 2004;44(1):68-71. doi: 10.1016/j.jacc.2004.03.040.
» https://doi.org/10.1016/j.jacc.2004.03.040 -
406Bradley TD, Logan AG, Kimoff RJ, Sériès F, Morrison D, Ferguson K, et al; CANPAP Investigators. Continuous positive airway pressure for central sleep apnea and heart failure. N Engl J Med. 2005;353(19):2025-33. doi: 10.1056/NEJMoa051001
» https://doi.org/10.1056/NEJMoa051001 -
407Arzt M, Floras JS, Logan AG, Kimoff RJ, Series F, Morrison D, et al; CANPAP Investigators. Suppression of central sleep apnea by continuous positive airway pressure and transplant-free survival in heart failure: a post hoc analysis of the Canadian Continuous Positive Airway Pressure for Patients with Central Sleep Apnea and Heart Failure Trial (CANPAP). Circulation. 2007;115(25):3173-80. doi: 10.1161/CIRCULATIONAHA.106.683482.
» https://doi.org/10.1161/CIRCULATIONAHA.106.683482 -
408Teschler H, Döhring J, Wang YM, Berthon-Jones M. Adaptive pressure support servo-ventilation: a novel treatment for Cheyne-Stokes respiration in heart failure. Am J Respir Crit Care Med. 2001;164(4):614-9. doi: 10.1164/ajrccm.164.4.9908114.
» https://doi.org/10.1164/ajrccm.164.4.9908114 -
409Javaheri S, Brown LK, Randerath WJ. Positive airway pressure therapy with adaptive servoventilation: part 1: operational algorithms. Chest. 2014;146(2):514-23. doi: 10.1378/chest.13-1776.
» https://doi.org/10.1378/chest.13-1776 -
410Arzt M, Wensel R, Montalvan S, Schichtl T, Schroll S, Budweiser S, et al. Effects of dynamic bilevel positive airway pressure support on central sleep apnea in men with heart failure. Chest. 2008;134(1):61-6. doi: 10.1378/chest.07-1620.
» https://doi.org/10.1378/chest.07-1620 -
411D'Elia E, Vanoli E, La Rovere MT, Fanfulla F, Maggioni A, Casali V, et al. Adaptive servo ventilation reduces central sleep apnea in chronic heart failure patients: beneficial effects on autonomic modulation of heart rate. J Cardiovasc Med (Hagerstown). 2013;14(4):296-300. doi: 10.2459/JCM.0b013e32835364b2.
» https://doi.org/10.2459/JCM.0b013e32835364b2 -
412Oldenburg O, Schmidt A, Lamp B, Bitter T, Muntean BG, Langer C, et al. Adaptive servoventilation improves cardiac function in patients with chronic heart failure and Cheyne-Stokes respiration. Eur J Heart Fail. 2008;10(6):581-6. doi: 10.1016/j.ejheart.2008.04.007.
» https://doi.org/10.1016/j.ejheart.2008.04.007 -
413Hastings PC, Vazir A, Meadows GE, Dayer M, Poole-Wilson PA, McIntyre HF, et al. Adaptive servo-ventilation in heart failure patients with sleep apnea: a real world study. Int J Cardiol. 2010;139(1):17-24. doi: 10.1016/j.ijcard.2008.08.022.
» https://doi.org/10.1016/j.ijcard.2008.08.022 -
414Cowie MR, Woehrle H, Wegscheider K, Angermann C, d'Ortho MP, Erdmann E, et al. Adaptive servo-ventilation for central sleep apnea in systolic heart failure. N Engl J Med. 2015;373(12):1095-105. doi: 10.1056/NEJMoa1506459.
» https://doi.org/10.1056/NEJMoa1506459 -
415Javaheri S, Brown LK, Randerath W, Khayat R. SERVE-HF: more questions than answers. Chest. 2016;149(4):900-4. doi: 10.1016/j.chest.2015.12.021.
» https://doi.org/10.1016/j.chest.2015.12.021 -
416Bradley TD, Floras JS; ADVENT-HF Investigators. The SERVE-HF Trial. Can Respir J. 2015;22(6):313. PMID: 26474274.
-
417O'Connor CM, Whellan DJ, Fiuzat M, Punjabi NM, Tasissa G, Anstrom KJ, et al. Cardiovascular outcomes with minute ventilation-targeted adaptive servo-ventilation therapy in heart failure: the CAT-HF Trial. J Am Coll Cardiol. 2017;69(12):1577-87. doi: 10.1016/j.jacc.2017.01.041.
» https://doi.org/10.1016/j.jacc.2017.01.041 -
418Lyons OD, Floras JS, Logan AG, Beanlands R, Cantolla JD, Fitzpatrick M, et al; ADVENT-HF Investigators. Design of the effect of adaptive servo-ventilation on survival and cardiovascular hospital admissions in patients with heart failure and sleep apnoea: the ADVENT-HF trial. Eur J Heart Fail. 2017;19(4):579-587. doi: 10.1002/ejhf.790.
» https://doi.org/10.1002/ejhf.790 -
419National Sleep Foundation [Internet]. [Accessed in 2016 Dec 10]. Available from: https://sleepfoundation.org/
» https://sleepfoundation.org/ -
420Taskar V, Hirshkowitz M. Health effects of sleep deprivation. Clin Pulm Med. 2003;10(1):47-52.
-
421Gangwisch JE. A review of evidence for the link between sleep duration and hypertension. Am J Hypertens. 2014;27(10):1235-42. doi: 10.1093/ajh/hpu071.
» https://doi.org/10.1093/ajh/hpu071 -
422Theorell-Haglöw J, Berglund L, Berne C, Lindberg E. Both habitual short sleepers and long sleepers are at greater risk of obesity: a population-based 10-year follow-up in women. Sleep Med. 2014;15(10):1204-11. doi: 10.1016/j.sleep.2014.02.014.
» https://doi.org/10.1016/j.sleep.2014.02.014 -
423Spiegel K, Leproult R, Cauter EV. Impact of sleep debt on metabolic and endocrine function. Lancet. 1999;354(9188):1435-9. doi: 10.1016/S0140-6736(99)01376-8.
» https://doi.org/10.1016/S0140-6736(99)01376-8 -
424Shan Z, Ma H, Xie M, Yan P, Guo Y, Bao W, et al. Sleep duration and risk of type 2 diabetes: a meta-analysis of prospective studies. Diabetes Care. 2015;38(3):529-37. doi: 10.2337/dc14-2073.
» https://doi.org/10.2337/dc14-2073 -
425King CR, Knutson KL, Rathouz PJ, Sidney S, Liu K, Lauderdale DS. Short sleep duration and incident coronary artery calcification. JAMA. 2008;300(24):2859-66. doi: 10.1001/jama.2008.867
» https://doi.org/10.1001/jama.2008.867 -
426Ayas NT, White DP, Manson JE, Stampfer MJ, Speizer FE, Malhotra A, et al. Aprospective study of sleep duration and coronary heart disease in women. Arch Intern Med. 2003;163(2):205-9. PMID: 12546611.
-
427Ikehara S, Iso H, Date C, Kikuchi S, Watanabe Y, Wada Y, et al. Association of sleep duration with mortality from cardiovascular disease and other causes for Japanese men and women: the JACC study. Sleep. 2009;32(3):295-301. PMID: 19294949.
-
428Cappuccio FP, Cooper D, D'Elia L, Strazzullo P, Miller MA. Sleep duration predicts cardiovascular outcomes: a systematic review and meta-analysis of prospective studies. Eur Heart J. 2011;32(12):1484-92. doi: 10.1093/eurheartj/ehr007.
» https://doi.org/10.1093/eurheartj/ehr007 -
429Méier-Ewert HK, Ridker PM, Rifai N, Regan MM, Price NJ, Dinges DF, et al. Effect of sleep loss on C-reative protein, an inflammatory marker of cardiovascular risk. J Am Coll Cardiol. 2004;43(4):678-83. doi: 10.1016/j.jacc.2003.07.050.
» https://doi.org/10.1016/j.jacc.2003.07.050 -
430Miller MA, Cappuccio FP. Biomarkers of cardiovascular risk in sleep-deprived people. J Hum Hypertens. 2013;27(10):583-8. doi: 10.1038/jhh.2013.27.
» https://doi.org/10.1038/jhh.2013.27 -
431American Psychiatric Association. Diagnostic and statistical manual of mental disorders. 5th ed. Arlington (VA); 2013.
-
432Ohayon MM, Reynolds CF 3rd. Epidemiological and clinical relevance of insomnia diagnosis algorithms according to the DSM-IV and the International Classification of Sleep Disorders (ICSD). Sleep Med. 2009;10(9):952-60. doi: 10.1016/j.sleep.2009.07.008. Erratum in: Sleep Med. 2010;11(2):227.
» https://doi.org/10.1016/j.sleep.2009.07.008 -
433Fernandez-Mendoza J, Calhoun SL, Bixler EO, Karataraki M, Liao D, Vela-Bueno A, et al. Sleep misperception and chronic insomnia in the general population: role of objective sleep duration and psychological profiles. Psychosom Med. 2011;73(1):88-97. doi: 10.1097/PSY.0b013e3181fe365a.
» https://doi.org/10.1097/PSY.0b013e3181fe365a -
434Fernandez-Mendoza J, Baker JH, Vgontzas AN, Gaines J, Liao D, Bixler EO. Insomnia symptoms with objective short sleep duration are associated with systemic inflammation in adolescents. Brain Behav Immun. 2017 Mar;61:110-6. doi: 10.1016/j.bbi.2016.12.026.
» https://doi.org/10.1016/j.bbi.2016.12.026 -
435Lin CL, Tsai YH, Yeh MC. The relationship between insomnia with short sleep duration is associated with hypercholesterolemia: a cross-sectional study. J Adv Nurs. 2016;72(2):339-47. doi: 10.1111/jan.12844.
» https://doi.org/10.1111/jan.12844 -
436Cespedes EM, Dudley KA, Sotres-Alvarez D, Zee PC, Daviglus ML, Shah NA, et al. Joint associations of insomnia and sleep duration with prevalent diabetes: the Hispanic Community Health Study/Study of Latinos (HCHS/SOL). J Diabetes. 2016;8(3):387-97. doi: 10.1111/1753-0407.12308.
» https://doi.org/10.1111/1753-0407.12308 -
437Bathgate CJ, Edinger JD, Wyatt JK, Krystal AD. Objective but not subjective short sleep duration associated with increased risk for hypertension in individuals with insomnia. Sleep. 2016;39(5):1037-45. doi: 10.5665/sleep.5748.
» https://doi.org/10.5665/sleep.5748 -
438Fernandez-Mendoza J, Vgontzas AN, Liao D, Shaffer ML, Vela-Bueno A, Basta M, et al. Insomnia with objective short sleep duration and incident hypertension: the Penn State Cohort. Hypertension. 2012;60(4):929-35. doi: 10.1161/HYPERTENSIONAHA.112.193268
» https://doi.org/10.1161/HYPERTENSIONAHA.112.193268 -
439Vgontzas AN, Fernandez-Mendoza J, Liao D, Bixler EO. Insomnia with objective short sleep duration: the most biologically severe phenotype of the disorder. Sleep Med Rev. 2013;17(4):241-54. doi: 10.1016/j.smrv.2012.09.005.
» https://doi.org/10.1016/j.smrv.2012.09.005 -
440Chien KL, Chen PC, Hsu HC, Su TC, Sung FC, Chen MF, et al. Habitual sleep duration and insomnia and the risk of cardiovascular events and all-cause death: report from a community-based cohort. Sleep. 2010;33(2):177-84. PMID: 20175401.
-
441Vgontzas AN, Liao D, Pejovic S, Calhoun S, Karataraki M, Basta M, et al. Insomnia with short sleep duration and mortality: the Penn State cohort. Sleep. 2010;33(9):1159-64. PMID: 20857861.
-
442Bathgate CJ, Edinger JD, Krystal AD. Insomnia patients with objective short sleep duration have a blunted response to cognitive behavioral therapy for insomnia. Sleep. 2017 Jan 1;40(1). doi: 10.1093/sleep/zsw012.
» https://doi.org/10.1093/sleep/zsw012 -
443Javaheri S, Redline S. Insomnia and risk of cardiovascular disease. Chest. 2017;152(2):435-44. doi: 10.1016/j.chest.2017.01.026.
» https://doi.org/10.1016/j.chest.2017.01.026 -
444Sofi F, Cesari F, Casini A, Macchi C, Abbate R, Gensini GF. Insomnia and risk of cardiovascular disease: a meta-analysis. Eur J Prev Cardiol. 2014;21(1):57-64. doi: 10.1177/2047487312460020.
» https://doi.org/10.1177/2047487312460020 -
445Li M, Zhang XW, Hou WS, Tang ZY. Insomnia and risk of cardiovascular disease: a meta-analysis of cohort studies. Int J Cardiol. 2014;176(3):1044-7. doi: 10.1016/j.ijcard.2014.07.284.
» https://doi.org/10.1016/j.ijcard.2014.07.284 -
446Parthasarathy S, Vasquez MM, Halonen M, Bootzin R, Quan SF, Martinez FD, et al. Persistent insomnia is associated with mortality risk. Am J Med. 2015;128(3):268-75. doi: 10.1016/j.amjmed.2014.10.015.
» https://doi.org/10.1016/j.amjmed.2014.10.015 -
447American Academy of Sleep Medicine. International classification of sleep disorders. diagnostic and coding manual. 2nd ed. Westchester, IL; 2005.
-
448Dauvilliers Y, Billiard M, Montplaisir J. Clinical aspects and pathophysiology of narcolepsy. Clin Neurophysiol. 2003;114(11):2000-17. PMID: 14580598.
-
449Plazzi G, Ferri R, Antelmi E, Bayard S, Franceschini C, Cosentino FI, et al. Restless legs syndrome is frequent in narcolepsy with cataplexy patients. Sleep. 2010;33(5):689-94. PMID: 20469811.
-
450Longstreth WT Jr, Koepsell TD, Ton TG, Hendrickson AF, van Belle G. The epidemiology of narcolepsy. Sleep. 2007;30(1):13-26. PMID: 17310860.
-
451Silber MH, Krahn LE, Olson EJ, Pankratz VS. The epidemiology of narcolepsy in Olmsted County, Minnesota: a population-based study. Sleep. 2002;25(2):197-202. PMID: 11902429.
-
452Sachs C, Kaijser L. Autonomic regulation of cardiopulmonary functions in sleep apnea syndrome and narcolepsy. Sleep. 1982;5(3):227-38. PMID: 6813932.
-
453Dauvilliers Y, Arnulf I, Mignot E. Narcolepsy with cataplexy. Lancet. 2007;369(9560):499-511. doi: 10.1016/S0140-6736(07)60237-2.
» https://doi.org/10.1016/S0140-6736(07)60237-2 -
454Nishino S. Clinical and neurobiological aspects of narcolepsy. Sleep Med. 2007;8(4):373-99. doi: 10.1016/j.sleep.2007.03.008.
» https://doi.org/10.1016/j.sleep.2007.03.008 -
455Silvani A, Grimaldi D, Barletta G, Bastianini S, Vandi S, Pierangeli G, et al. Cardiovascular variability as a function of sleep-wake behaviour in narcolepsy with cataplexy. J Sleep Res. 2013;22(2):178-84. doi: 10.1111/jsr.12007.
» https://doi.org/10.1111/jsr.12007 -
456Grimaldi D, Calandra-Buonaura G, Provini F, Agati P, Pierangeli G, Franceschini C, et al. Abnormal sleep-cardiovascular system interaction in narcolepsy with cataplexy: effects of hypocretin deficiency in humans. Sleep. 2012;35(4):519-28. doi: 10.5665/sleep.1738.
» https://doi.org/10.5665/sleep.1738 -
457Dauvilliers Y, Jaussent I, Krams B, Scholz S, Lado S, Levy P, et al. Non-dipping blood pressure profile in narcolepsy with cataplexy. PLoS One. 2012;7(6):e38977. doi: 10.1371/journal.pone.0038977.
» https://doi.org/10.1371/journal.pone.0038977 -
458Auger RR, Goodman SH, Silber MH, Krahn LE, Pankratz VS, Slocumb NL. Risks of high-dose stimulants in the treatment of disorders of excessive somnolence: a case-control study. Sleep. 2005;28(6):667-72. PMID: 16477952.
-
459Wallin M, Mahowald M. Blood pressure effects of long term stimulant use in disorders of hypersomnolence. J Sleep Res. 1998;7(3):209-15. PMID: 9785276.
-
460Allen RP, Picchietti D, Henning WA, Trenkwalder C, Walters AS, Montplaisi J; Restless Legs Syndrome Diagnosis and Epidemiology workshop at the National Institutes of Health; International Restless Legs Syndrome Study Group. Restless legs syndrome: diagnostic criteria, special considerations, and epidemiology. A report from the restless legs syndrome diagnosis and epidemiology workshop at the National Institutes of Health. Sleep Med. 2003;4(2):101-19. PMID: 14592341.
-
461Allen RP, Picchietti DL, Garcia-Borreguero D, Ondo WG, Walters AS, Winkelman JW, et al. Restless Legs Syndrome Willis-Ekbom disease diagnostic criteria: updated International Restless Legs Syndrome Study Group (IRLSSG) consensus criteria history, rationale, description, and significance. Sleep Medicine. 2014;15:800-73. doi: http//dx.doi.org/10.1016/j.sleep.2014.03.025
» http//dx.doi.org/10.1016/j.sleep.2014.03.025 -
462Szentkirályi A, Winter AC, Schürks M, Völzke H, Hoffmann W, E Buring J, et al. Restless legs syndrome and all-cause mortality in four prospective cohort studies. BMJ Open. 2012;2(6). pii: e001652. doi: 10.1136/bmjopen-2012-001652.
» https://doi.org/10.1136/bmjopen-2012-001652 -
463Berger K, Kurth T. RLS epidemiology?frequencies, risk factors and methods in population studies. Mov Disord. 2007;22 Suppl 18:S420-3. doi: 10.1002/mds.21589.
» https://doi.org/10.1002/mds.21589 -
464Rothdach AJ, Trenkwalder C, Haberstock J, Keil U, Berger K. Prevalence and risk factors of RLS in an elderly population: the MEMO study. Memory and Morbidity in Augsburg Elderly. Neurology. 2000;54(5):1064-8. PMID: 10720275.
-
465Berger K, Luedemann J, Trenkwalder C, John U, Kessler C. Sex and the risk of restless legs syndrome in the general population. Arch Intern Med. 2004;164(2):196-202. doi: 10.1001/archinte.164.2.196.
» https://doi.org/10.1001/archinte.164.2.196 -
466Ulfberg J, Nystrom B, Carter N, Edling C. Prevalence of restless legs syndrome among men aged 18 to 64 years: an association with somatic disease and neuropsychiatric symptoms. Mov Disord. 2001;16(6):1159-63. PMID: 11748753.
-
467Ohayon MM, Roth T. Prevalence of restless legs syndrome and periodic limb movement disorder in the general population. J Psychosom Res. 2002;53(1):547-54. PMID: 12127170.
-
468Winkelman JW, Finn L, Young T. Prevalence and correlates of restless legs syndrome symptoms in the Wisconsin Sleep Cohort. Sleep Med 2006;7(7):545-52. doi: 10.1016/j.sleep.2006.01.004.
» https://doi.org/10.1016/j.sleep.2006.01.004 -
469Batool-Anwar S, Malhotra A, Forman J, Winkelman J, Li Y, Gao X. Restless legs syndrome and hypertension in middle-aged women. Hypertension. 2011;58(5):791-6. doi: 10.1161/HYPERTENSIONAHA.111.174037.
» https://doi.org/10.1161/HYPERTENSIONAHA.111.174037 -
470Winter AC, Schürks M, Glynn RJ, Buring JE, Gaziano JE, Berger K, et al. Vascular risk factors, cardiovascular disease, and restless legs syndrome in women. Am J Med. 2013;126(3):220-7. doi: 10.1016/j.amjmed.2012.06.040.
» https://doi.org/10.1016/j.amjmed.2012.06.040 -
471Winter AC, Berger K, Glynn RJ, Buring JE, Gaziano JM, Schürks M, et al. Vascular risk factors, cardiovascular disease, and restless legs syndrome in men. Am J Med. 2013;126(3):228-35. doi: 10.1016/j.amjmed.2012.06.039.
» https://doi.org/10.1016/j.amjmed.2012.06.039 -
472Winter AC, Schürks M, Glynn RJ, Buring JE, Gaziano JM, Berger K, et al. Restless legs syndrome and risk of incident cardiovascular disease in women and men: prospective cohort study. BMJ Open. 2012;2(2):e000866. doi: 10.1136/bmjopen-2012-000866.
» https://doi.org/10.1136/bmjopen-2012-000866 -
473Li Y, Walters AS, Chiuve SE, Rimm EB, Winkelman JW, Gao X. Prospective study of restless legs syndrome and coronary heart disease among women. Circulation. 2012;126(14):1689-94. doi: 10.1161/CIRCULATIONAHA.112.112698.
» https://doi.org/10.1161/CIRCULATIONAHA.112.112698 -
474Mallon L, Broman JE, Hetta J. Restless legs symptoms with sleepiness in relation to mortality: 20-year follow-up study of a middle-aged Swedish population. Psychiatry Clin Neurosci. 2008;62(4):472-5. doi: 10.1111/j.1440-1819.2008.01825.x.
» https://doi.org/10.1111/j.1440-1819.2008.01825.x -
475Grunstein RR. Sleep-related breathing disorders. 5. nasal continuous positive airway pressure treatment for obstructive sleep apnoea. Thorax. 1995;50:1106-13. PMID: 7491563.
-
476Kribbs NB, Pack AI, Kline LR, Smith PL, Schwartz AR, Schubert NM, et al. Objective measurement of pattern of nasal CPAP use by patients with obstructive sleep apnea. Am Rev Respir Dis. 1993;147(4):887-95. doi: 10.1164/ajrccm/147.4.887.
» https://doi.org/10.1164/ajrccm/147.4.887 -
477Veasey SC, Guilleminault C, Strohl KP, Sanders MH, Ballard RD, Magalang UJ. Medical therapy for obstructive sleep apnea: a review by the Medical Therapy for Obstructive Sleep Apnea Task Force of the Standards of Practice Committee of the American Academy of Sleep Medicine. Sleep. 2006;29(8):1036-44. PMID: 16944672.
-
478Barnes M, Goldsworthy UR, Cary BA, Hill CJ. A diet and exercise program to improve clinical outcomes in patients with obstructive sleep apnea--a feasibility study. J Clin Sleep Med. 2009;5(5):409-15. PMID: 19961023.
-
479Norman JF, Von Essen SG, Fuchs RH, McElligott M. Exercise training effect on obstructive sleep apnoea syndrome. Sleep Res Online. 2000;3(3):121-9. PMID: 11382910.
-
480Tuomilehto HP, Seppä JM, Partinen MM, Peltonen M, Gylling H, Tuomilehto JO, et al; Kuopio Sleep Apnea Group. Lifestyle intervention with weight reduction: first-line treatment in mild obstructive sleep apnea. Am J Respir Crit Care Med. 2009;179(4):320-7. doi: 10.1164/rccm.200805-669OC.
» https://doi.org/10.1164/rccm.200805-669OC -
481Ueno LM, Drager LF, Rodrigues AC, Rondon MU, Braga AM, Mathias W Jr, et al. Effects of exercise training in patients with chronic heart failure and sleep apnea. Sleep. 2009;32(5):637-47. PMID: 19480231.
-
482Sengul YS, Ozalevli S, Oztura I, Itil O, Baklan B. The effect of exercise on obstructive sleep apnea: a randomized and controlled trial. Sleep Breath. 2009;15(1):49-56. doi: 10.1007/s11325-009-0311-1.
» https://doi.org/10.1007/s11325-009-0311-1 -
483Yamamoto U, Mohri M, Shimada K, Origuchi H, Miyata K, Ito K, et al. Six-month aerobic exercise training ameliorates central sleep apnea in patients with chronic heart failure. J Card Fail. 2007;13(10):825-9. doi: 10.1016/j.cardfail.2007.08.001.
» https://doi.org/10.1016/j.cardfail.2007.08.001 -
484Chirinos JA, Gurubhagavatula I, Teff K, Rader DJ, Wadden TA, Townsend R, et al. CPAP, weight loss, or both for obstructive sleep apnea. N Engl J Med. 2014;370(24):2265-75. doi: 10.1056/NEJMoa1306187.
» https://doi.org/10.1056/NEJMoa1306187 -
485Trakada G, Steiropoulos P, Zarogoulidis P, Nena E, Papanas N, Maltezos E, t al. A fatty meal aggravates apnea and increases sleep in patients with obstructive sleep apnea. Sleep Breath. 2014;18(1):53-8. doi: 10.1007/s11325-013-0847-y.
» https://doi.org/10.1007/s11325-013-0847-y -
486Cunali PA, Almeida FR, Santos CD, Valdrichi NY, Nascimento LS, Dal-Fabbro C, et al. Mandibular exercises improve mandibular advancement devide therapy for obstructive sleep apnea. Sleep Breath. 2011;15(4):717-27. doi: 10.1007/s11325-010-0428-2.
» https://doi.org/10.1007/s11325-010-0428-2 -
487Guimarães KC, Drager LF, Genta PR, Marcondes BF, Lorenzi-Filho G. Effects of oropharyngeal exercises on patients with moderate obstructive sleep apnea syndrome. Am J Respir Crit Care Med. 2009;179(10):962-6. doi: 10.1164/rccm.200806-981OC.
» https://doi.org/10.1164/rccm.200806-981OC -
488Ieto V, Kayamori F, Montes MI, Hirata RP, Gregório MG, Alencar AM, et al. Effects of oropharyngeal exercises on snoring: a randomized trial. Chest. 2015;148(3):683-91. doi: 10.1378/chest.14-2953
» https://doi.org/10.1378/chest.14-2953 -
489Diaferia G, Badke L, Santos-Silva R, Bommarito S, Tufik S, Bittencourt L. Effect of speech therapy as adjunct treatment to continuous positive airway pressure on the quality of life of patients with obstructive sleep apnea. Sleep Med. 2013;14(7):628-35. doi: 10.1016/j.sleep.2013.03.016.
» https://doi.org/10.1016/j.sleep.2013.03.016 -
490Diaféria G, Santos-Silva R, Truksinas E, Haddad FL, Santos R, Bommarito S, et al. Myofunctional therapy improves adherence to continuous positive airway pressure treatment. Sleep Breath. 2017;21(2):387-395. doi: 10.1007/s11325-016-1429-6.
» https://doi.org/10.1007/s11325-016-1429-6 -
491Weaver TE, Grunstein RR. Adherence to continuous positive airway pressure therapy: the challenge to effective treatment. Proc Am Thorac Soc. 2008;5(2):173-8. doi: 10.1513/pats.200708-119MG.
» https://doi.org/10.1513/pats.200708-119MG -
492Hoy CJ, Vennelle M, Kingshott RN, Engleman HM, Douglas NJ. Can intensive support improve continuous positive airway pressure use in patients with the sleep apnea/hypopnea syndrome? Am J Respir Crit Care Med. 1999;159(4 Pt 1):1096-100. doi: 10.1164/ajrccm.159.4.9808008.
» https://doi.org/10.1164/ajrccm.159.4.9808008 -
493Richards D, Bartlett DJ, Wong K, Malouff J, Grunstein RR. Increased adherence to CPAP with a group cognitive behavioral treatment intervention: a randomized trial. Sleep. 2007;30(5):635-40. PMID: 17552379.
-
494Almeida FR, Henrich N, Marra C, Lynd LD, Lowe AA, Tsuda H, et al. Patient preferences and experiences of CPAP and oral appliances for the treatment of obstructive sleep apnea: a qualitative analysis. Sleep Breath. 2013 May;17(2):659-66. doi: 10.1007/s11325-012-0739-6.
» https://doi.org/10.1007/s11325-012-0739-6 -
495Kushida CA, Morgenthaler TI, Littner MR, Alessi CA, Bailey D, Coleman J Jr, et al; American Academy of Sleep. Practice parameters for the treatment of snoring and Obstructive Sleep Apnea with oral appliances: an update for 2005. Sleep. 2006;29(2):240-3. PMID: 16494092.
-
496Almeida FR, Mulgrew A, Ayas N, Tsuda H, Lowe AA, Fox N, et al. Mandibular advancement splint as short-term alternative treatment in patients with obstructive sleep apnea already effectively treated with continuous positive airway pressure. J Clin Sleep Med. 2013;9(4):319-24. doi: 10.5664/jcsm.2576.
» https://doi.org/10.5664/jcsm.2576 -
497Fleetham J, Almeida FR. Oral appliances and appliances and surgical techniques for obstructive sleep apnea syndrome therapy. [Accessed in 2017 May 05]. Available from: http://neupsykey.com/oral-appliances-and-surgical-techniques-fr-obstructive-sleep-apnea-syndrome-therapy
» http://neupsykey.com/oral-appliances-and-surgical-techniques-fr-obstructive-sleep-apnea-syndrome-therapy -
498Gauthier L, Almeida F, Arcache JP, Ashton-McGregor C, Coté D, Driver HS, et al. Position paper by Canadian dental sleep medicine professionals on the role of different health care professionals in managing OSA and snoring with oral appliances. Can Respir J. 2012;19(5):307-9. PMID: 23061075.
-
499Almeida FR, Lowe AA. Principles of oral appliance therapy for the management of snoring and sleep disordered breathing. Oral Maxillofac Surg Clin North Am. 2009;21(4):413-20. doi: 10.1016/j.coms.2009.07.002.
» https://doi.org/10.1016/j.coms.2009.07.002 -
500Mehta A, Qian J, Petocz P, Darendeliler MA, Cistulli PA. A randomized, controlled study of a mandibular advancement splint for obstructive sleep apnea. Am J Respir Crit Care Med 2001;163(6):1457-61. doi: 10.1164/ajrccm.163.6.2004213.
» https://doi.org/10.1164/ajrccm.163.6.2004213 -
501Cunnington D, Junge M. Chronic insomnia: diagnosis and non-pharmacological management. BMJ. 2016;355:i5819. doi: 10.1136/bmj.i5819.
» https://doi.org/10.1136/bmj.i5819 -
502van Straten A, van der Zweerde T, Kleiboer A, Cuijpers P, Morin CM, Lancee J. Cognitive and behavioral therapies in the treatment of insomnia: A meta-analysis. Sleep Med Rev. 2017 Feb 9. pii: S1087-0792(17)30034-5. doi: 10.1016/j.smrv.2017.02.001. [Epub ahead of print].
» https://doi.org/10.1016/j.smrv.2017.02.001 -
503Trauer JM, Qian MY, Doyle JS, Rajaratnam SM, Cunnington D. Cognitive Behavioral Therapy for Chronic Insomnia: a systematic review and meta-analysis. Ann Intern Med. 2015;163(3):191-204. doi: 10.7326/M14-2841.
» https://doi.org/10.7326/M14-2841 -
504Zachariae R, Lyby MS, Ritterband LM, O'Toole MS. Efficacy of internet-delivered cognitive-behavioral therapy for insomnia - A systematic review and meta-analysis of randomized controlled trials. Sleep Med Rev. 2016 Dec;30:1-10. doi: 10.1016/j.smrv.2015.10.004.
» https://doi.org/10.1016/j.smrv.2015.10.004 -
505Drager LF, McEvoy RD, Barbe F, Lorenzi-Filho G, Redline S; INCOSACT Initiative (International Collaboration of Sleep Apnea Cardiovascular Trialists). Sleep Apnea and Cardiovascular Disease: Lessons From Recent Trials and Need for Team Science. Circulation. 2017;136(19):1840-1850. doi: 10.1161/CIRCULATIONAHA.117.029400.
» https://doi.org/10.1161/CIRCULATIONAHA.117.029400
Datas de Publicação
-
Publicação nesta coleção
Ago 2018


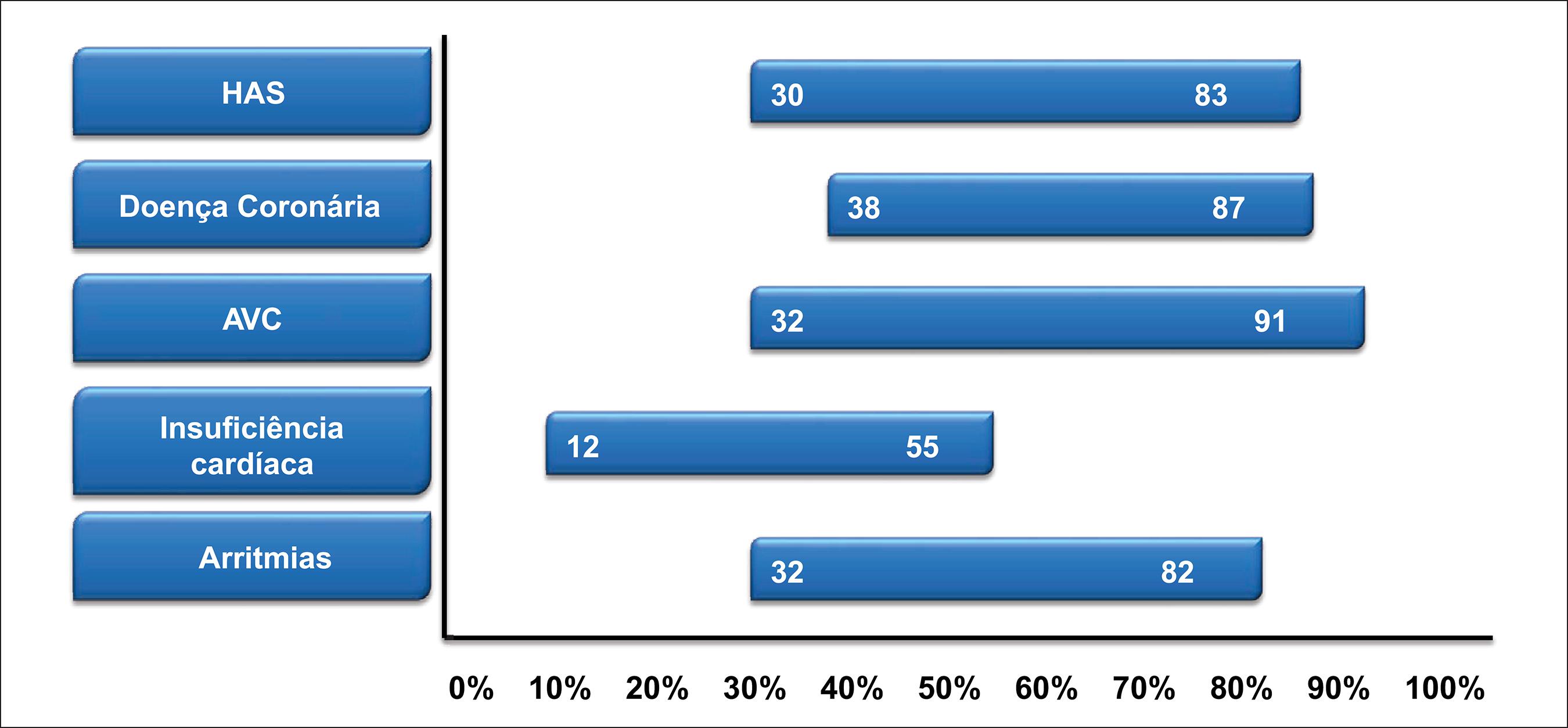 Fonte: Modificado de Javaheri et al.
Fonte: Modificado de Javaheri et al.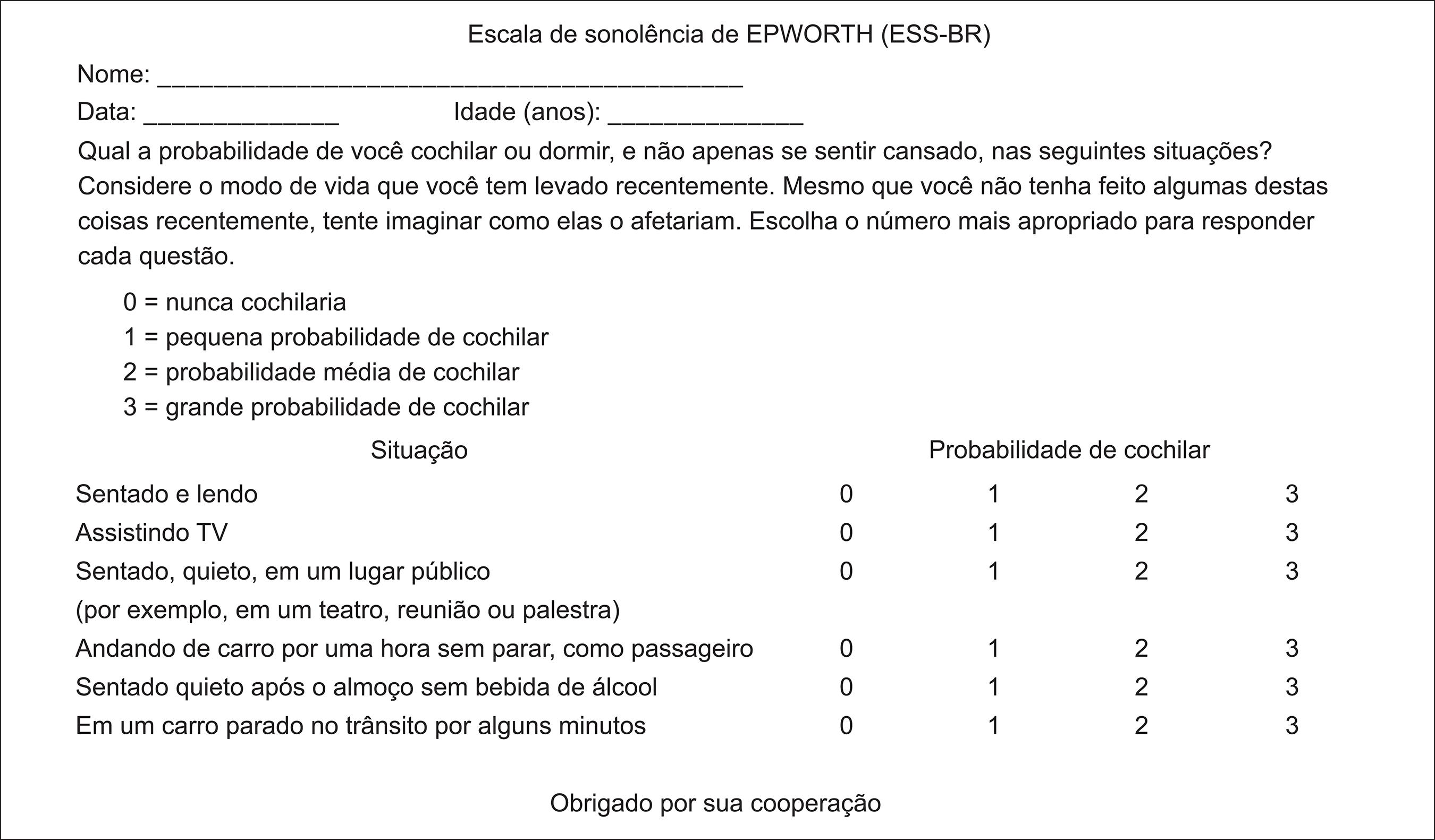 Fonte: Adaptado das Johns
Fonte: Adaptado das Johns Modificado de Javaheri et al.
Modificado de Javaheri et al.