Resumo
O miRNA (ou microRNA) constitui uma subclasse de RNAs não codificantes responsáveis pela regulação gênica pós-transcricional. Ele possui aproximadamente 22 nucleotídeos e regula a expressão gênica em plantas e animais ao nível pós-transcricional, pela clivagem de um mRNA alvo ou da repressão de sua tradução. Embora muitos processos e mecanismos ainda não estejam completamente elucidados, existe uma forte associação entre a expressão de miRNAs e diversas doenças que acometem o organismo. Os miRNAs são expressos no sistema cardiovascular, contudo o seu papel no desenvolvimento das doenças cardiovasculares (DCVs) ainda não está totalmente elucidado. Diante disso, realizou-se uma revisão não sistemática da literatura a fim de se discutir a relação entre os miRNAs e as DCVs. Nesta revisão, primeiramente é discutido o que são os miRNAs e a sua ação a nível celular. Após, é discutido o papel dos miRNAs como biomarcadores circulantes de DCVs e então o seu papel no remodelamento cardíaco e na aterosclerose. Apesar da complexidade e dos desafios, a identificação dos miRNAs desregulados nas DCVs é crucial, uma vez que possibilita uma melhor compressão dos mecanismos celulares e moleculares envolvidos, assim como auxilia o desenvolvimento de marcadores circulantes de diagnóstico e prognóstico mais acurados e de novas estratégias terapêuticas para os diferentes estágios da DCV.
Palavras-chave
Doenças Cardiovasculares/fisiopatologia; Doenças Cardiovasculares/diagnóstico; Doenças Cardiovasculares/genética; Biomarcadores/metabolismo; Remodelamento Cardíaco; Aterosclerose; Micro RNAs
Abstract
MiRNA (or microRNA) is a subclass of non-coding RNAs that is responsible for post-transcriptional gene regulation. It has approximately 22 nucleotides and regulates gene expression in plants and animals at the post-transcriptional level, by the cleavage of a target mRNA or by suppression of its translation. Although many of the processes and mechanisms have not yet been fully elucidated, there is a strong association between miRNA expression and several diseases. It is known that miRNAs are expressed in the cardiovascular system, but their role in cardiovascular diseases (CVDs) has not been clearly established. In this non-systematic review of the literature, we first present the definition of miRNAs and their action at the cellular level. Afterward, we discuss the role of miRNAs as circulating biomarkers of CVDs, and then their role in cardiac remodeling and atherosclerosis. Despite the complexity and challenges, it is crucial to identify deregulated miRNAs in CVDs, as it allows a better understanding of underlying cellular and molecular mechanisms and helps in the development of more accurate diagnostic and prognostic circulating biomarkers, and new therapeutic strategies for different stages of CVDs.
Keywords
Cardiovascular Diseases/physiopathology; Cardiovascular Diseases/diagnosis; Cardiovascular Diseases/genetics; Biomarkers/metabolism; Cardiac, Remodeling/genetics; Atherosclerosis; MicroRNAs
Introdução
A pesquisa científica tem buscado desvendar a fisiopatologia de diversas doenças para o desenvolvimento de novos caminhos terapêuticos. Nesse âmbito, o miRNA (ou microRNA) vem ganhando a atenção da comunidade científica como um possível alvo terapêutico. Desde que foram descobertos em 1993,11 Lee RC, Feinbaum RL, Ambros V. The C. elegans heterochronic gene lin-4 encodes small RNAs with antisense complementarity to lin-14. Cell. 1993;75(5):843-54. diversos miRNAs relacionados a processos biológicos como reguladores gênicos já foram catalogados. Estima-se que ainda haja diversos miRNAs desconhecidos, o que os torna uma das maiores classes de reguladores gênicos. Para dimensionar sua importância, estima-se que os miRNAs regulem cerca de 1/3 da expressão gênica em mamíferos.22 Mattick JS, Makunin IV. Non-coding RNA. Hum Mol Genet. 2006;15(spec1):R17-29.
Diversas pesquisas têm estabelecido uma relação do padrão de expressão de miRNAs com algumas doenças, embora muitos dos processos e mecanismos ainda não estejam completamente elucidados. No diabetes, por exemplo, estudos experimentais apontam a presença de miRNAs específicos nas ilhotas pancreáticas e sugerem que esses exerçam papel importante no controle da secreção da insulina.33 Poy MN, Eliasson L, Krutzfeldt J, Kuwajima S, Ma X, Macdonald PE, et al. A pancreatic islet-specific microRNA regulates insulin secretion. Nature. 2004;432(7014):226-30. A expressão de miRNAs também pode ser observada em diferentes tipos de tumores; em alguns casos eles atuam como supressores e em outros exercem papel oposto e com efeitos deletérios.44 Calin GA, Sevignani C, Dumitru CD, Hyslop T, Noch E, Yendamuri S, et al. Human microRNA genes are frequently located at fragile sites and genomic regions involved in cancers. Proc Natl Acad Sci U S A. 2004;101(9):2999-3004. Já se sabe hoje que os miRNAs são expressos no sistema cardiovascular; entretanto, este conhecimento ainda é insuficiente para um melhor entendimento sobre o seu papel no desenvolvimento das doenças cardiovasculares (DCVs).
Diante do exposto, realizou-se uma revisão não sistemática da literatura a fim de se organizar e discutir os principais estudos que investigam a relação dos miRNAs com a doença cardiovascular. A base de dados consultada foi o PubMed (www.ncbi.nlm.nih.gov/pubmed). Foram selecionados artigos originais realizados com humanos ou animais, redigidos na língua inglesa e utilizou-se como palavras-chave os descritores MeSH: microRNA AND Cardiovascular Diseases, miRNA AND Cardiovascular Diseases. Na presente revisão da literatura, primeiro apresentamos o que são os miRNAs e a sua ação a nível celular. Após, é discutido o papel dos miRNAs como biomarcadores circulantes e então o seu papel no remodelamento cardíaco e na aterosclerose.
Biologia dos miRNAs
Durante anos acreditava-se que as regiões não-codificantes do genoma eram “lixo genético”, pois não possuíam informação para a síntese de proteínas. Atualmente, sabe-se que a maior porção do transcriptoma produzido pelo genoma de eucariotos é composta por RNAs não-codificantes, que podem ser classificados em funcionais e reguladores. Entre os RNAs funcionais destacam-se o RNA transportador (tRNA), o RNA ribossomal (rRNA), o pequeno RNA nuclear (snRNA) e o pequeno RNA nucleolar (snoRNA). Dentre os RNAs reguladores destacam-se o miRNA, o pequeno RNA de interferência (siRNA), o piwiRNA (piRNA) e o longo RNA não-codificador (lncRNA).55 Zhou X, Zuo Z, Zhou F, Zhao W, Sakaguchi Y, Suzuki T, et al. Profiling sex-specific piRNAs in zebrafish. Genetics. 2010;186(4):1175-85.
Dessa ampla variedade de classes de RNAs não-codificantes, os miRNAs se tornaram alvo de grande interesse devido à associação observada entre a sua desregulação e o surgimento de alterações fenotípicas e patológicas.66 Chang TC, Mendell JT. MicroRNAs in vertebrate physiology and human disease. Annu Rev Genomics Hum Genet. 2007;8:215-39. Os miRNAs são definidos como pequenas moléculas endógenas de ácido ribonucleico (RNA) em cadeia simples, não codificantes, com aproximadamente 22 nucleotídeos (nt). Atuam como reguladores da expressão gênica em plantas e animais ao nível pós-transcricional, pela clivagem de um RNA mensageiro (RNAm) alvo ou da repressão de sua tradução.77 Bartel DP, Chen CZ. Micromanagers of gene expression: the potentially widespread influence of metazoan microRNAs. Nat Rev Genet. 2004;5(5):396-400.
O primeiro miRNA (lin-4) foi descrito em 1993 pelo grupo de Rosalind Lee, estando ele associado à regulação do desenvolvimento larval de Caenorhabditis elegans (C. elegans). Lin-4 regulava negativamente o nível da proteína LIN-14 (da primeira fase larvar), diminuindo sua expressão ao longo do tempo.11 Lee RC, Feinbaum RL, Ambros V. The C. elegans heterochronic gene lin-4 encodes small RNAs with antisense complementarity to lin-14. Cell. 1993;75(5):843-54.
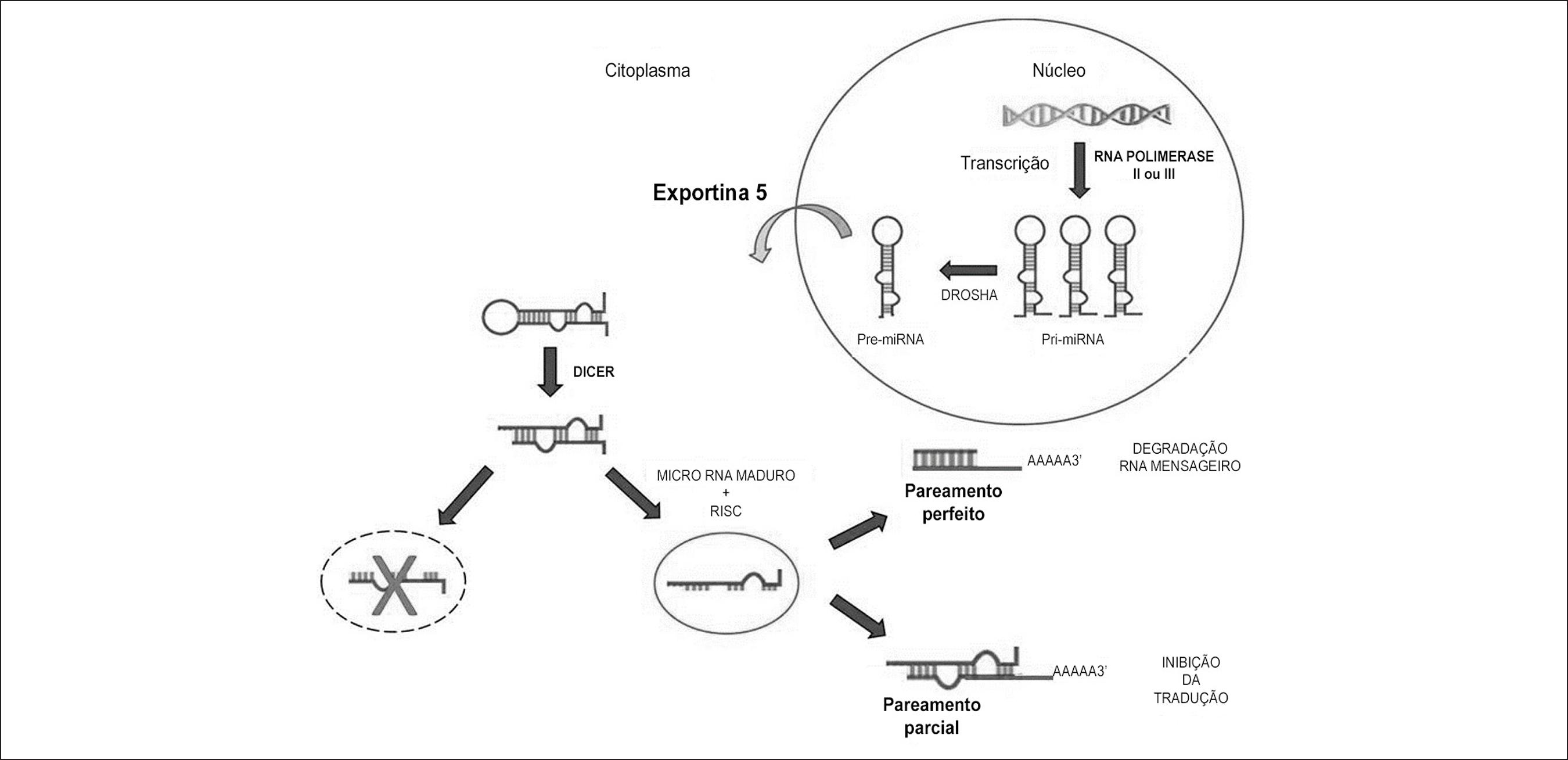
A biogênese de um miRNA começa com a síntese de um longo transcrito primário conhecido como pri-miRNA (~110pb) (Figura 1). Os pri-miRNAs são transcritos pelas RNAs polimerase II ou III88 Kim VN. MicroRNA biogenesis: coordinated cropping and dicing. Nat Rev Mol Cell Biol. 2005;6(5):376-85. e possuem uma estrutura de hairpin (“grampo de cabelo”), que é essencial para o reconhecimento das enzimas de processamento de miRNAs. No núcleo, o pri-miRNA é processado em pré-miRNA (~70pb) pela ação da enzima Drosha99 Han J, Lee Y, Yeom KH, Nam JW, Heo I, Rhee JK, et al. Molecular basis for the recognition of primary microRNAs by the Drosha-DGCR8 complex. Cell. 2006;125(5):887-901. que reconhece e cliva as extremidades de pequenas estruturas de RNA em forma de hairpin.1010 Lee Y, Han J, Yeom KH, Jin H, Kim VN. Drosha in primary microRNA processing. Cold Spring Harb Symp Quant Biol. 2006;71:51-7.
Síntese do miRNA e sua ação sobre o RNA mensageiro. O pri-miRNA em forma de grampo é sintetizado no núcleo e convertido a pre-miRNA pela ação da enzima Drosha, sendo então exportado do núcleo pela Exportina 5. No citoplasma, o pre-miRNA sofre ação da enzima DICER e a união do complexo de silenciamento induzido por RNA (RISC) à dupla fita de RNA (dsRNA) gera o miRNA maduro. O miRNA maduro se anela ao RNAm alvo, promovendo a sua degradação ou inibindo a sua tradução.
Após o processamento nuclear, cada pré-miRNA é exportado para o citoplasma através da proteína Exportina 5.1111 Yi R, Qin Y, Macara IG, Cullen BR. Exportin-5 mediates the nuclear export of pre-microRNAs and short hairpin RNAs. Genes Dev. 2003;17(24):3011-6. O pré-miRNA é reconhecido pela enzima Dicer que cliva a região do loop, resultando em uma molécula de dupla fita de RNA (dsRNA; ~22pb). Esse processo recruta proteínas da família argonauta (Ago) para formar o complexo de silenciamento induzido por RNA (RISC).1212 Kim VN, Han J, Siomi MC. Biogenesis of small RNAs in animals. Nat Rev Mol Cell Biol. 2009;10(2):126-39. O RISC se liga a uma das duas fitas do dsRNA para gerar o miRNA maduro (miR canônico ou miR-5p) que atua na regulação de um RNAm alvo.1313 Krützfeldt J, Poy MN, Stoffel M. Strategies to determine the biological function of microRNAs. Nat Genet. 2006;38 (Suppl):S14-9. A outra fita (miR* ou miR-3p) é degradada ou capaz de formar outro RISC e realizar a regulação de outro RNAm alvo.1414 Rand TA, Petersen S, Du F, Wang X. Argonaute2 cleaves the anti-guide strand of siRNA during RISC activation. Cell. 2005;123(4):621-9.
O pareamento perfeito entre o miRNA e a região 3' UTR do RNAm alvo promove a clivagem do RNAm e o seu posterior encaminhamento para os p-bodies (do inglês, mRNA processing bodies) para a sua consequente degradação.1515 Tang G, Reinhart BJ, Bartel DP, Zamore PD. A biochemical framework for RNA silencing in plants. Genes Dev. 2003;17(1):49-63. Por outro lado, o pareamento parcial entre o miRNA e a região 3’ UTR do mRNA promove inibição da tradução, o principal mecanismo de atuação dos miRNAs em mamíferos.1616 Zeng Y, Wagner EJ, Cullen BR. Both natural and designed micro RNAs can inhibit the expression of cognate mRNAs when expressed in human cells. Mol Cell. 2002;9(6):1327-33. Por meio desse pareamento, o miRNA tem a capacidade de inibir a tradução, interferindo diretamente com os fatores de iniciação da tradução ou perturbando a função da cauda poli-A.1717 Gebauer F, Hentze MW. Molecular mechanisms of translational control. Nat Rev Mol Cell Biol. 2004;5(10):827-35. A localização primária dos miRNAs é o citoplasma celular,88 Kim VN. MicroRNA biogenesis: coordinated cropping and dicing. Nat Rev Mol Cell Biol. 2005;6(5):376-85. embora alguns estudos confirmem o ingresso dessas moléculas no sistema circulatório, possivelmente devido ao processo de lise celular.1818 Zhang J, Zhao H, Gao Y, Zhang W. Secretory miRNAs as novel cancer biomarkers. Biochim Biophys Acta. 2012;1826(1):32-43.
Assim, os miRNAs também estão presentes na circulação sanguínea e diversos estudos mostram sua alta estabilidade no meio extracelular. A proteção dos miRNAs à degradação no meio extracelular seria devido à sua ligação a proteínas (p. ex., lipoproteínas) ou pelo seu encapsulamento em microvesículas e exossomas. Assim, os miRNAs podem ser detectados de forma confiável em amostras plasmáticas, sendo apontados como potenciais biomarcadores no diagnóstico das DCVs.1919 Muoio DM, Newgard CB. Mechanisms of disease: molecular and metabolic mechanisms of insulin resistance and beta-cell failure in type 2 diabetes. Nat Rev Mol Cell Biol. 2008;9(3):193-205. O fato dos miRNAs serem sequências pequenas e agirem sem a necessidade de pareamento completo faz com que um único miRNA possa ter como alvo dezenas de RNAm, assim como um único RNAm pode ser alvo de múltiplos miRNAs, gerando assim um grande poder regulatório da expressão genética.2020 van Rooij E, Liu N, Olson EN. MicroRNAs flex their muscles. Trends Genet. 2008;24(4):159-66.
miRNAs como biomarcadores circulantes
Estudos apontam que o nível circulante de miRNAs está alterado em algumas DCVs, despertando assim o interesse em seu uso como ferramenta de diagnóstico clínico e prognóstico, uma vez que os miRNAs possuem alta estabilidade na corrente sanguínea e são de fácil detecção. Os miRNAs poderiam ser utilizados, por exemplo, como biomarcadores da insuficiência cardíaca (IC), fibrilação atrial, infarto agudo do miocárdio (IAM) e aterosclerose, por meio de sua detecção no plasma sanguíneo (Figura 2).
Biomarcadores circulantes. Aqui são ilustrados alguns dos miRNAs encontrados no soro ou plasma sanguíneo que poderiam ser utilizados como biomarcadores de diagnóstico ou prognóstico de doenças cardiovasculares.
Já está bem estabelecido que a presença do miR-1 no sangue auxilia a identificação do IAM, mas sua utilização como biomarcador a longo-prazo não é recomendada, devido ao curto tempo no qual ele permanece na circulação sanguínea. Sua curta meia-vida resulta provavelmente de sua liberação direta no sangue a partir do tecido cardíaco necrótico de forma não encapsulada pelo exossoma.2121 Wang J, Huang W, Xu R, Nie Y, Cao X, Meng J, et al. MicroRNA-24 regulates cardiac fibrosis after myocardial infarction. J Cell Mol Med. 2012;16(9):2150-60. Quando há lesão cardíaca, miRNAs seriam liberados no sangue por meio de exossomos ou pela ruptura celular, podendo estar associados ou não a outras moléculas. Estas moléculas poderiam proteger os miRNAs contra a degradação, prolongando o seu tempo de permanência na circulação. Além disso, o aumento do fluxo sanguíneo, alteração do pH e a liberação de citocinas são fatores que também influenciam a meia-vida dos miRNAs circulantes. Por exemplo, foi verificado que o miR-1 maduro exogenamente adicionado ao soro é rapidamente degradado tantoin vitro quantoin vivo.2222 Cheng Y, Tan N, Yang J, Liu X, Cao X, He P, et al. A translational study of circulating cell-free microRNA-1 in acute myocardial infarction. Clin Sci (Lond). 2010;119(2):87-95. Uma limitação ao uso de miRNA circulantes é a falta de normalização de sua quantificação, quando comparado ao miRNA tecidual.2323 Rao PK, Toyama Y, Chiang HR, Gupta S, Bauer M, Medvid R, et al. Loss of cardiac microRNA-mediated regulation leads to dilated cardiomyopathy and heart failure. Circ Res. 2009;105(6):585-94. Contudo, apesar dessas limitações, o miR-1 apresenta alta sensibilidade na identificação do IAM no momento inicial desse evento adverso.
Diversos estudos relatam que o miR-499 possui acurácia diagnóstica superior a troponina T para o IAM.2424 Xin Y,Yang C, Han Z. Circulating miR-499 as a potential biomarker for acute myocardial infarction. Ann Transl Med. 2016;v.4.,2525 Xiao J, Shen B, Li J, Lv D, Zhao Y, Wang F, et al. Serum microRNA-499 and microRNA-208a as biomarkers of acute myocardial infarction. Int J Clin Exp Med. 2014;7(1):136-41 A vantagem do miR-499 é que ele pode ser detectado no sangue em menos de quatro horas após o IAM, enquanto a troponina só pode ser detectada mais tardiamente.2626 Chen X, Zhang L, Su T, Li H, Huang Q, Wu D, et al. Kinetics of plasma microRNA-499 expression in acute myocardial infarction. J Thorac Dis. 2015;7(5):890-6. Assim, miR-499 poderia aumentar a acurácia da troponina T no diagnóstico precoce do IAM. O estudo HUNT investigou 179 miRNAs em 212 indivíduos sadios com o objetivo de predizer IAM. Diversos miRNAs circulantes diferiram significativamente durante o período de acompanhamento entre indivíduos que posteriormente sofreram IAM e aqueles que permaneceram saudáveis. Após análise de regressão logística, foi observado que um conjunto de 5 miRNAs (miR-106a-5p, -424-5p, miR-144-3p, miR-660-5p e let-7g-5p) melhor prediziam o IAM, com 77% de acerto para ambos os gêneros.2727 Bye A, Røsjø H, Nauman J, Silva GJ, Follestad T, Omland T, et al. Circulating microRNAs predict future fatal myocardial infarction in healthy individuals - The HUNT study. J Mol Cell Cardiol. 2016 Aug;97:162-8. Jia et al.,2828 Jia K, Shi P, Han X, Chen T, Tang H, Wang J. Diagnostic value of miR-30d-5p and miR-125b-5p in acute myocardial infarction. Mol Med Rep. 2016;14(1):184-94. mostraram que os miR-30d-5p e -125b-5p também possuem valor diagnóstico para o IAM, quando avaliados em pacientes com síndrome coronariana aguda.2828 Jia K, Shi P, Han X, Chen T, Tang H, Wang J. Diagnostic value of miR-30d-5p and miR-125b-5p in acute myocardial infarction. Mol Med Rep. 2016;14(1):184-94. Em modelo animal de IAM cirúrgico, o miR-208a apresentou níveis circulantes elevados 4 horas e 24 horas após a indução do infarto.2525 Xiao J, Shen B, Li J, Lv D, Zhao Y, Wang F, et al. Serum microRNA-499 and microRNA-208a as biomarkers of acute myocardial infarction. Int J Clin Exp Med. 2014;7(1):136-41
Diversos estudos já foram realizados com o foco em se avaliar o valor prognóstico e/ou diagnóstico dos miRNAs na IC, assim como no tratamento da IC. Existem evidências de que os miRNAs desempenham um papel tanto no surgimento quanto na progressão da IC. Apesar do peptídeo natriurético cerebral (BNP) e do pró-peptídeo natriurético cerebral N-terminal (NT-proBNP) serem utilizados atualmente como padrão ouro no diagnóstico da IC, os miRNAs têm sido estudados exaustivamente como potenciais biomarcadores. Como exemplo, uma recente revisão sistemática com meta-análise mostrou que o miR-423-5p, associado ao peptídeo natriurético atrial (ANP), teria um potencial valor diagnóstico para a detecção da IC.2929 Yan H, Ma F, Zhang Y, Wang C, Qiu D, Zhou K, et al. miRNAs as biomarkers for diagnosis of heart failure: A systematic review and meta-analysis. Medicine (Baltimore). 2017;96(22):e6825. Na IC crônica, Cakmak et al.,3030 Cakmak HA, Coskunpinar E, Ikitimur B, Barman HA, Karadag B, Tiryakioglu NO. The prognostic value of circulating microRNAs in heart failure: preliminary results from a genome-wide expression study. J Cardiovasc Med (Hagerstown). 2015;16(6):431-7. mostraram que o miR-182 teria maior valor prognóstico para mortalidade cardiovascular, caracterizada pela morte súbita inexplicável, IC descompensada ou arritmia hemodinamicamente significativa, comparado ao NT-proBNP e a proteína C reativa (PCR) de alta sensibilidade pela análise da curva ROC em pacientes com IC compensado (NYHA II, n = 20) e descompensados (NYHA III, n = 22), comparado a controles saudáveis (n = 15).3030 Cakmak HA, Coskunpinar E, Ikitimur B, Barman HA, Karadag B, Tiryakioglu NO. The prognostic value of circulating microRNAs in heart failure: preliminary results from a genome-wide expression study. J Cardiovasc Med (Hagerstown). 2015;16(6):431-7. Um panorama mais completo dos miRNAs envolvidos na IC aguda e crônica pode ser visto na revisão recentemente publicada de Vegter e colaboradores.3131 Vegter EL, van der Meer P, de Windt LJ, Pinto YM, Voors AA. MicroRNAs in heart failure: from biomarker to target for therapy. Eur J Heart Fail. 2016;18(5):457-68.
Considerando os estudos em pacientes com fibrilação atrial (FA), já foi observado que pacientes com IC crônica estável com FA e fração de ejeção < 40% apresentam uma redução significativa dos níveis plasmáticos de miR-150 comparados aos seus controles saudáveis.3232 Lakschevitz F, Aboodi G, Tenenbaum H, Glogauer M. Diabetes and periodontal diseases: interplay and links. Curr Diabetes Rev. 2011;7(6):433-9. Harling et al.,3333 Harling L, Lambert J, Ashrafian H, Darzi A, Gooderham NJ, Athanasiou T. Elevated serum microRNA 483-5p levels may predict patients at risk of post-operative atrial fibrillation. Eur J Cardiothorac Surg. 2017;51(1):73-8. estudaram o plasma coletado no pré-operatório 24 horas antes de cirurgia de revascularização miocárdica, para avaliar a precisão diagnóstica do miRNA na fibrilação atrial pós-operatória. Nesta análise, os autores mostraram o miR483-5p como um potencial biomarcador da FA pós-operatória, com precisão preditiva global de 78%.3333 Harling L, Lambert J, Ashrafian H, Darzi A, Gooderham NJ, Athanasiou T. Elevated serum microRNA 483-5p levels may predict patients at risk of post-operative atrial fibrillation. Eur J Cardiothorac Surg. 2017;51(1):73-8. Os miR-23a e -26a também teriam a capacidade de prever a FA pós-operatória, uma vez que seus níveis estão reduzidos no período pós-operatório de pacientes submetidos à intervenção coronária arterial de by-pass.3434 Feldman A, Moreira DA, Gun C, Wang HL, Hirata MH, de Freitas Germano J, et al. Analysis of circulating miR-1, miR-23a, and miR-26a in atrial fibrillation patients undergoing coronary bypass artery grafting surgery. Ann Hum Genet. 2017;81(3):99-105. O nível circulante reduzido do miR-126 serviria como candidato a biomarcador do desenvolvimento, progressão e severidade da FA e da IC, de acordo com estudo realizado em pacientes com FA, IC ou associação de ambos.3535 Wei XJ, Han M, Yang FY, Wei GC, Liang ZG, Yao H, et al. Biological significance of miR-126 expression in atrial fibrillation and heart failure. Braz J Med Biol Res. 2015;48(11):983-9. Por fim, Gorem et al.,3636 Goren Y, Meiri E, Hogan C, Mitchell H, Lebanony D, Salman N, et al. Relation of reduced expression of MiR-150 in platelets to atrial fibrillation in patients with chronic systolic heart failure. Am J Cardiol. 2014;113(6):976-81. mostraram expressão reduzida do miR-150 nas plaquetas de pacientes com IC sistólica crônica associada à FA, comparado aos indivíduos sem FA, perfil também encontrado no soro desses pacientes.3636 Goren Y, Meiri E, Hogan C, Mitchell H, Lebanony D, Salman N, et al. Relation of reduced expression of MiR-150 in platelets to atrial fibrillation in patients with chronic systolic heart failure. Am J Cardiol. 2014;113(6):976-81.
Na doença vascular aterosclerótica, já foi observada a produção de corpos apoptóticos derivados de células endoteliais, os quais continham grande quantidade de miR-126 em seu interior e que eram, por sua vez, capazes de desencadear a produção de quimiocina CXCL12 nas células vasculares receptoras.3737 Zernecke A, Bidzhekov K, Noels H, Shagdarsuren E, Gan L, Denecke B, et al. Delivery of microRNA-126 by apoptotic bodies induces CXCL12-dependent vascular protection. Sci Signal. 2009;2(100): 81. O miR-212 circulante é sugerido por Jeong et al.,3838 Jeong HS, Kim JY, Lee SH, Hwang J, Shin JW, Song KS, et al. Synergy of circulating miR-212 with markers for cardiovascular risks to enhance estimation of atherosclerosis presence. PLoS One. 2017;12(5):e0177809. como um biomarcador da aterosclerose, visto que ele aumenta a predição da aterosclerose quando combinado a hemoglobina A1c, HDL e lipoproteína (a). Em pacientes com aterosclerose, foi visto uma associação entre o espessamento das túnicas intima-média da artéria carótida com níveis elevados do miR-29a circulante.3939 Liu CZ, Zhong Q, Huang YQ. Elevated plasma MiR-29a levels are associated with increased carotid intima-media thickness in atherosclerosis patients. Tohoku J Exp Med. 2017;241(3):183-8.
Remodelamento cardíaco
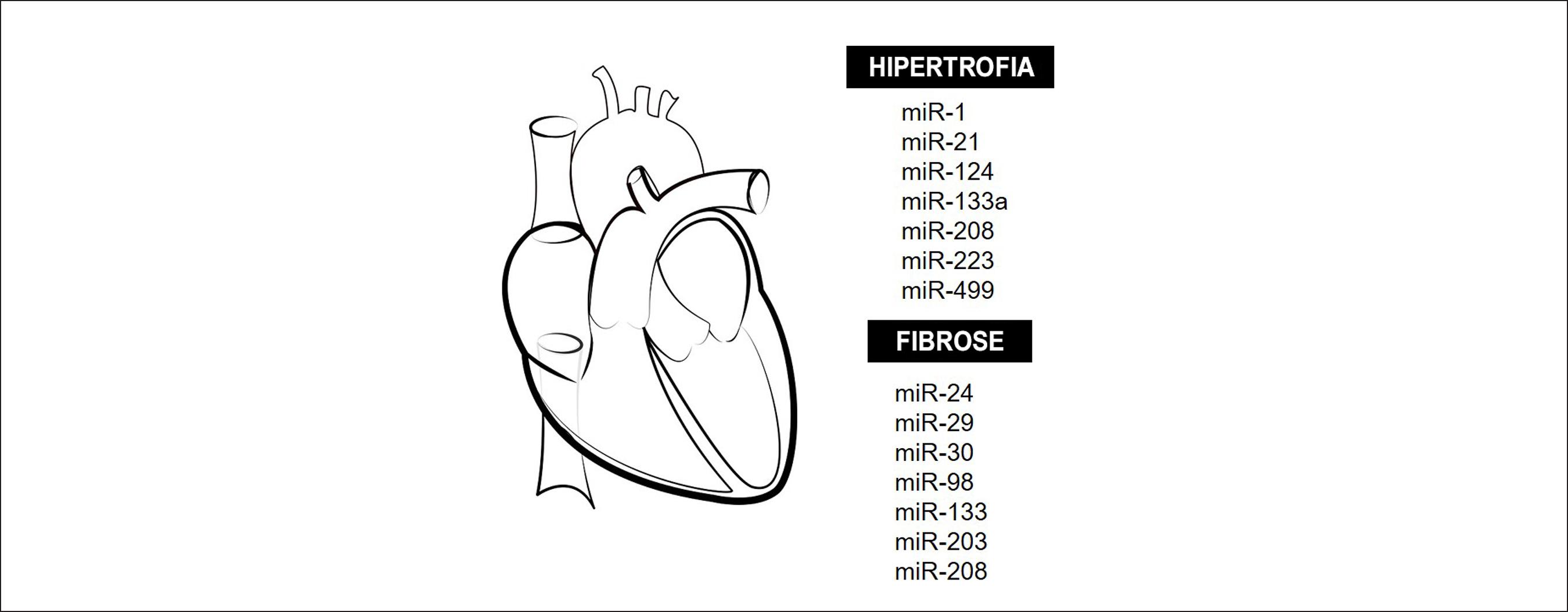
O remodelamento ventricular é um dos mecanismos envolvidos na progressão da IC e envolve a apoptose e hipertrofia de cardiomiócitos, fibrose intersticial decorrente da deposição de colágeno, e a rarefação vascular (Figura 3). Existem evidências de que os miRNAs desempenham um papel importante nesse remodelamento patológico, contudo ainda não se conhece todos os miRNAs envolvidos e alguns estudos apresentam divergências em seus resultados dependendo da doença em foco.
Remodelamento cardíaco e miRNAs. Principais miRNAs que modulam a hipertrofia cardíaca e a fibrose tecidual durante o remodelamento cardíaco adverso em diversas condições patológicas.
Uma vez que os miR-1, -133a, -208a/b e -499 são mais abundantes no coração em comparação a outros tecidos, acredita-se que eles sejam específicos desse tecido. Eles estão envolvidos na diferenciação dos precursores mesodérmicos e na transdiferenciação/reprogramação dos fibroblastos/miofibroblastos adultos em cardiomiócitos maduros, assim como mantêm a funcionalidade e a sobrevivência dos cardiomiócitos.4040 Piubelli C, Meraviglia V, Pompilio G, D'Alessandra Y, Colombo GI, Rossini A. microRNAs and Cardiac Cell Fate. Cells. 2014;3(3):802-23 Em condições patológicas, a desregulação dos miRNAs cardíacos pode levar à progressão da IC, associada a arritmia, hipóxia, isquemia, dilatação ventricular, fibrose e necrose tecidual.
Cardiomiócitos
O miR-1 é um dos mais abundantes miRNAs no tecido miocárdico, responsável pelo controle de diferentes aspectos do processo de diferenciação e proliferação dos cardiomiócitos. Em animais, o miR-1 estaria envolvido na proliferação e diferenciação das células cardíacas durante a cardiogênese.4141 Zhao Y, Samal E, Srivastava D. Serum response factor regulates a muscle-specific microRNA that targets Hand2 during cardiogenesis. Nature. 2005;436(7048):214-20. Por outro lado, o aumento da expressão do miR-1 leva à arritmia, visto que ele controla a condutância cardíaca e automaticidade pela modulação da expressão de proteínas envolvidas no manuseio do cálcio intracelular.4242 Carmean CM, Bobe AM, Yu JC, Volden PA, Brady MJ. Refeeding-induced brown adipose tissue glycogen hyper-accumulation in mice is mediated by insulin and catecholamines. PLoS One. 2013;8(7):e67807. O miR-21 é expresso predominantemente em fibroblastos cardíacos; o aumento de sua expressão promoveu indiretamente a hipertrofia cardíaca pela estimulação da MAP (Mitogen Activated Protein) quinase dos fibroblastos em modelo animal de IC,4343 Thum T, Gross C, Fiedler J, Fischer T, Kissler S, Bussen M, et al. MicroRNA-21 contributes to myocardial disease by stimulating MAP kinase signalling in fibroblasts. Nature. 2008;456(7224):980-4 embora haja evidências de que o aumento de sua expressão possui papel anti-hipertrófico em cardiomiócitos isolados.4444 Tatsuguchi M, Seok HY, Callis TE, Thomson JM, Chen JF, Newman M, et al. Expression of microRNAs is dynamically regulated during cardiomyocyte hypertrophy. J Mol Cell Cardiol. 2007;42(6):1137-41.
O silenciamento do miR-208 em modelo animal de IAM reduz a apoptose e atenua a hipertrofia e a fibrose cardíaca, refletindo em melhora da função cardíaca.4545 Tony H, Meng K, Wu B, Yu A, Zeng Q, Yu K, et al. MicroRNA-208a Dysregulates Apoptosis Genes Expression and Promotes Cardiomyocyte Apoptosis during Ischemia and Its Silencing Improves Cardiac Function after Myocardial Infarction. Mediators Inflamm. 2015;2015 Nov 25:479123. Existem evidências de que o miR-133a protege os cardiomiócitos neonatais de rato da hipertrofia. Entre os mecanismos envolvidos estão a modulação da concentração de cálcio intracelular e redução da expressão do RNA para o ANP e para a miosina de cadeia pesada do tipo beta (β-MHC).4646 Lee SY, Lee CY, Ham O, Moon JY, Lee J, Seo HH, et al. microRNA-133a attenuates cardiomyocyte hypertrophy by targeting PKCdelta and Gq. Mol Cell Biochem. 2018;439(1-2):105-15,4747 Wu Y, Wang YQ, Wang BX. [MicroRNA-133a attenuates isoproterenol-induced neonatal rat cardiomyocyte hypertrophy by downregulating L-type calcium channel alpha1C subunit gene expression.] Zhonghua Xin Xue Guan Bing Za Zhi. 2013;41(6):507-13. O miR-223 também é capaz de reduzir a concentração intracelular de cálcio, a contratilidade dos cardiomiócitos, e a fosforilação da troponina I (cTNI), mecanismos pelos quais este miRNA suprimiria a hipertrofia.4848 Wang YS, Zhou J, Hong K, Cheng XS, Li YG. MicroRNA-223 displays a protective role against cardiomyocyte hypertrophy by targeting cardiac troponin I-interacting kinase. Cell Physiol Biochem. 2015;35(4):1546-56.
O miR-124 estaria envolvido com a hipertrofia cardíaca, uma vez que sua expressão está aumentada em modelo de hipertrofia induzida pela angiotensina II em cardiomiócitos de ratos neonatais em cultura e a inibição de sua expressão suprime a hipertrofia induzida por angiotensina II.4949 Bao Q, Chen L, Li J, Zhao M, Wu S, Wu W, et al. Role of microRNA-124 in cardiomyocyte hypertrophy inducedby angiotensin II. Cell Mol Biol (Noisy-le-grand). 2017;63(4):23-27. Em camundongos, a indução da expressão do miR-499 especificamente no coração leva à hipertrofia celular e disfunção cardíaca devido à alteração da expressão de proteínas contráteis - MYH7B e actina alfa 1 do músculo esquelético (ACTA1).5050 Shieh JT, Huang Y, Gilmore J, Srivastava D. Elevated miR-499 levels blunt the cardiac stress response. PLoS One. 2011;6(5):e19481
Fibrose
O fator de crescimento do tecido conjuntivo (CTGF) é uma molécula considerada chave no processo fibrótico uma vez que ele induz a síntese da matriz extracelular (MEC). Duisters et al.,5151 Duisters RF, Tijsen AJ, Schroen B, Leenders JJ, Lentink V, van der Made I, et al. miR-133 and miR-30 regulate connective tissue growth factor: implications for a role of microRNAs in myocardial matrix remodeling. Circ Res. 2009;104(2):170-8, mostraram que os miR-133 e miR-30 regulam a expressão do CTGF.5151 Duisters RF, Tijsen AJ, Schroen B, Leenders JJ, Lentink V, van der Made I, et al. miR-133 and miR-30 regulate connective tissue growth factor: implications for a role of microRNAs in myocardial matrix remodeling. Circ Res. 2009;104(2):170-8, A expressão de CTGF é inversamente proporcional à expressão desses miRNAs em modelos de doença cardíaca em roedores (modelo genético com hiperativação do sistema renina-angiotensina-aldosterona, hipertrofia cardíaca e IC) e no remodelamento patológico do ventrículo esquerdo em humanos com estenose aórtica isolada submetidos à cirurgia de substituição valvar, cujas amostras foram coletadas por biópsia. Além disso, o aumento da expressão dos miR-133 e miR-30 reduz a expressão de CTGF, o que resulta em menor deposição de colágeno.5151 Duisters RF, Tijsen AJ, Schroen B, Leenders JJ, Lentink V, van der Made I, et al. miR-133 and miR-30 regulate connective tissue growth factor: implications for a role of microRNAs in myocardial matrix remodeling. Circ Res. 2009;104(2):170-8, Por outro lado, o miR-203 pode atuar com um fator fibrogênico, visto que a indução de sua expressão em cardiomiócitos de camundongo em cultura aumenta a produção de CTGF, fator de transformação do crescimento beta 1 (TGF-β1) e fibronectina.5252 He Q, Wang CM, Qin JY, Zhang YJ, Xia DS, Chen X, et al. Effect of miR-203 expression on myocardial fibrosis. Eur Rev Med Pharmacol Sci. 2017;21(4):837-42.
O miR-29 também parece desempenhar um papel importante no remodelamento da MEC em humanos com IC. Ele é expresso preferencialmente em fibroblastos, sendo encontrado no entorno de áreas infartadas. Ele estaria envolvido no processo de apoptose, principalmente no estágio final da IC, levando a redução da expressão de colágeno.5353 Lai KB, Sanderson JE, Izzat MB, Yu CM. Micro-RNA and mRNA myocardial tissue expression in biopsy specimen from patients with heart failure. Int J Cardiol. 2015 Nov 15;199:79-83. Em modelo animal de infarto, há redução da expressão do miR-24 e esse se correlaciona com o remodelamento da MEC. Quando a expressão do miR-24 é induzida por precursores sintéticos, há redução da fibrose, bem como da diferenciação e migração de fibroblastos cardíacos.2121 Wang J, Huang W, Xu R, Nie Y, Cao X, Meng J, et al. MicroRNA-24 regulates cardiac fibrosis after myocardial infarction. J Cell Mol Med. 2012;16(9):2150-60. O miR-98 atua de forma semelhante, visto que a indução de sua expressão em fibroblastos cardíacos humanos em cultura inibe a fibrose induzida pelo TGF-β1.5454 Cheng R, Dang R, Zhou Y, Ding M, Hua H. MicroRNA-98 inhibits TGF-beta1-induced differentiation and collagen production of cardiac fibroblasts by targeting TGFBR1. Hum Cell. 2017;30(3):192-200.
Perfil de expressão tecidual com base na doença
Ikeda et al.,5555 Ikeda S, Kong SW, Lu J, Bisping E, Zhang H, Allen PD, et al. Altered microRNA expression in human heart disease. Physiol Genomics. 2007;31(3):367-73. realizaram uma análise ampla da expressão de miRNAs de 67 amostras de miocárdio do ventrículo esquerdo de pacientes com cardiomiopatia isquêmica, cardiomiopatia dilatada e estenose aórtica. Eles detectaram expressão diferencial dependendo da condição, onde 13 miRNAs foram específicos para a estenose aórtica e 8 para as cardiomiopatias, sem sobreposição entre estes dois grupos.5555 Ikeda S, Kong SW, Lu J, Bisping E, Zhang H, Allen PD, et al. Altered microRNA expression in human heart disease. Physiol Genomics. 2007;31(3):367-73. Houve redução da expressão dos miR-1, -19a e -19b na cardiomiopatia dilatada e na estenose aórtica e aumento da expressão do miR-214, o qual está relacionado à hipertrofia cardíaca, mas sem alteração na expressão dos miRNAs-133 e -208.5555 Ikeda S, Kong SW, Lu J, Bisping E, Zhang H, Allen PD, et al. Altered microRNA expression in human heart disease. Physiol Genomics. 2007;31(3):367-73. Entretanto, Care et al.,5656 Carè A, Catalucci D, Felicetti F, Bonci D, Addario A, Gallo P, et al. MicroRNA-133 controls cardiac hypertrophy. Nat Med. 2007;13(5):613-8. mostraram expressão reduzida do miR-133 na cardiomiopatia hipertrófica e na dilatação atrial, e Yang et al.,5757 Yang B, Lin H, Xiao J, Lu Y, Luo X, Li B, et al. The muscle-specific microRNA miR-1 regulates cardiac arrhythmogenic potential by targeting GJA1 and KCNJ2. Nat Med. 2007;13(4):486-91. encontraram aumento da expressão do miR-1 na cardiomiopatia isquêmica.
Em estudo conduzido por Lai et al.,5353 Lai KB, Sanderson JE, Izzat MB, Yu CM. Micro-RNA and mRNA myocardial tissue expression in biopsy specimen from patients with heart failure. Int J Cardiol. 2015 Nov 15;199:79-83. a associação de diversos miRNAs com a IC foi investigada em amostras do ápice do ventrículo esquerdo obtidas por biópsia durante cirurgia cardíaca. O miocárdio desses pacientes apresentou aumento da expressão dos miR-1, -21, -23, -29, -130, -195 e -199, enquanto a expressão dos miR-30, -133 e -208 manteve-se inalterada. Esse perfil estava associado a maior expressão do mRNA para a caspase 3, colágenos tipo I e tipo III e TGF.5353 Lai KB, Sanderson JE, Izzat MB, Yu CM. Micro-RNA and mRNA myocardial tissue expression in biopsy specimen from patients with heart failure. Int J Cardiol. 2015 Nov 15;199:79-83.
Aterosclerose
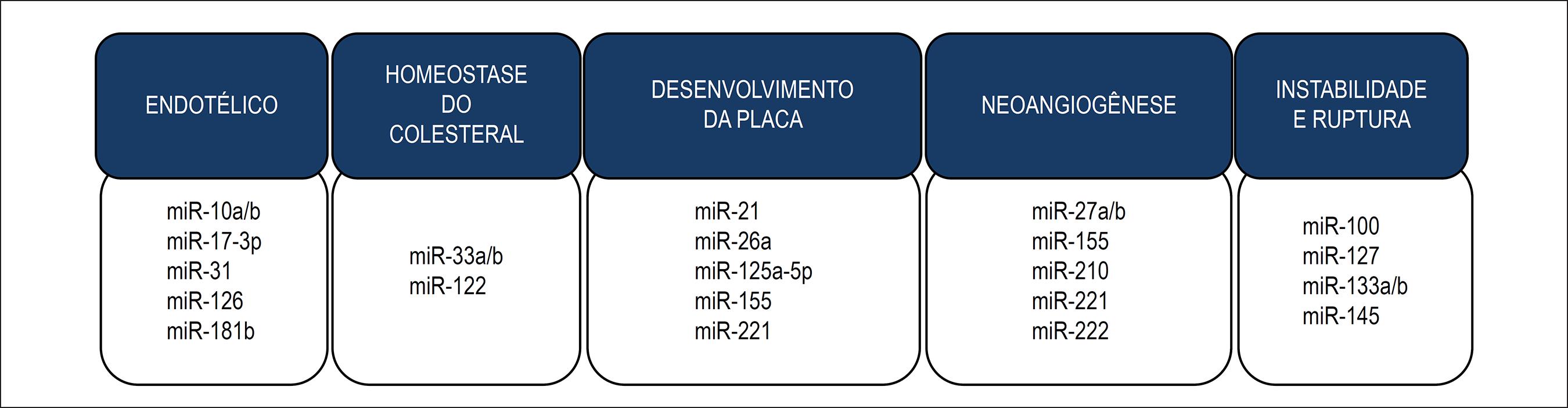
A aterosclerose é uma doença inflamatória crônica da parede arterial, que ocorre em resposta à lesão endotelial, principalmente em artérias elásticas de médio e grande calibre, artérias musculares e regiões onde há um distúrbio do fluxo sanguíneo laminar. Ela é considerada a principal responsável pela doença arterial coronariana, doença arterial carotídea, acidente vascular encefálico e doença vascular periférica.5858 Galkina E, Ley K. Immune and inflammatory mechanisms of atherosclerosis (*). Annu Rev Immunol. 2009;27:165-97. Existem diversas evidências de que os miRNAs estão envolvidos no desenvolvimento da aterosclerose, tanto em modelos experimentais quanto em humanos. Podemos separá-los em miRNAs envolvidos na disfunção endotelial, homeostase do colesterol, desenvolvimento da placa aterosclerótica, neoangiogênese e instabilidade e ruptura da placa, conforme ilustrado na Figura 4.
Aterosclerose e miRNAs. Desregulação da expressão de diversos miRNAs já foi encontrada nas diferentes etapas do desenvolvimento da aterosclerose. Aqui são ilustrados alguns miRNAs envolvidos na disfunção endotelial e inflamação, homeostase do colesterol, desenvolvimento da placa, neoangiogênese e instabilidade e ruptura da placa.
Endotélio
Em suínos, células endoteliais obtidas de regiões arteriais susceptíveis a aterosclerose (arco da aorta e bifurcação aorta abdominal-artéria renal) apresentaram expressão reduzida dos miR-10a e -10b. O miR-10a inibe alguns genes pró-inflamatório nas células endoteliais, incluindo a molécula de adesão celular vascular 1 (VCAM-1) e a E-selectina, assim como a via do NF-kB.5959 Fang Y, Shi C, Manduchi E, Civelek M, Davies PF. MicroRNA-10a regulation of proinflammatory phenotype in athero-susceptible endothelium in vivo and in vitro. Proc Natl Acad Sci U S A. 2010;107(30):13450-5. Em ratos, o miR-181b regula a ativação das células endoteliais e a resposta inflamatória vascular ao NF-kB diante de estímulos pró-inflamatórios.6060 Sun X, Icli B, Wara AK, Belkin N, He S, Kobzik L, et al. MicroRNA-181b regulates NF-?B-mediated vascular inflammation. J Clin Invest. 2012;122(6):1973-90. Em células endoteliais obtidas da veia umbilical humana (HUVEC), os miR-126, miR-31 e miR-17-3p também regulam a inflamação vascular pelo controle da expressão de moléculas de adesão celular (VCAM-1, molécula de adesão intercelular 1 [ICAM-1] e E-selectina).6161 Suárez Y, Wang C, Manes TD, Pober JS. Cutting edge: TNF-induced microRNAs regulate TNF-induced expression of E-selectin and intercellular adhesion molecule-1 on human endothelial cells: feedback control of inflammation. J Immunol. 2010;184(1):21-5.
Homeostase do colesterol
Os miR-33a e miR-33b regulam os genes SREBP2 e SREPB1, os quais são responsáveis pela regulação do colesterol e do metabolismo de ácidos graxo, tanto em células humanas quanto em camundongos.6262 Rayner KJ, Suárez Y, Dávalos A, Parathath S, Fitzgerald ML, Tamehiro N, et al. MiR-33 contributes to the regulation of cholesterol homeostasis. Science. 2010;328(5985):1570-3. A inibição do miR-33a resultou na regressão da aterosclerose em camundongos.6363 Rayner KJ, Sheedy FJ, Esau CC, Hussain FN, Temel RE, Parathath S, et al. Antagonism of miR-33 in mice promotes reverse cholesterol transport and regression of atherosclerosis. J Clin Invest. 2011;121(7):2921-31. A inibição do miR-122, que representa 80% dos miRNAs expressos pelo fígado, resultou em diminuição significativa dos níveis séricos de colesterol em camundongos e primatas não-humanos.6464 Elmén J, Lindow M, Schütz S, Lawrence M, Petri A, Obad S, et al. LNA-mediated microRNA silencing in non-human primates. Nature. 2008;452(7189):896-9.
Desenvolvimento da placa
O miR-155 é um importante regulador do sistema imunológico e demonstra estar envolvido na resposta inflamatória aguda. Ele modula o desenvolvimento da placa aterosclerótica, a captação de lipídeos e a resposta inflamatória de monócitos e macrófagos que leva à formação das células espumosas. Entre seus mecanismos de ação, ele atua como um regulador de feedback negativo na resposta inflamatória de macrófagos induzida pela LDL oxidada e inibe a liberação de citocinas inflamatórias pelos macrófagos como, por exemplo, as interleucina 6 (IL-6) e IL-8 e o fator de necrose tumoral alfa (TNF-α).6565 Huang RS, Hu GQ, Lin B, Lin ZY, Sun CC. MicroRNA-155 silencing enhances inflammatory response and lipid uptake in oxidized low-density lipoprotein-stimulated human THP-1 macrophages. J Investig Med. 2010;58(8):961-7.
Em monócitos de sangue periférico humano, o miR-125a-5p demonstrou papel importante na mediação da absorção de lipídios e diminuição da secreção de algumas citocinas inflamatórias (IL-2, IL-6, TNF-α e TGF-β) em macrófagos.6666 Chen T, Huang Z, Wang L, Wang Y, Wu F, Meng S, et al. MicroRNA-125a-5p partly regulates the inflammatory response, lipid uptake, and ORP9 expression in oxLDL-stimulated monocyte/macrophages. Cardiovasc Res. 2009;83(1):131-9. O LDL oxidado aumentou os níveis do miR-125a-5p, o qual regula a ORP-9 (um membro da família de proteínas ligantes de oxiesterol), reduzindo, assim, a expressão dos receptores scavengers SR (CD68) e LOX-1.6666 Chen T, Huang Z, Wang L, Wang Y, Wu F, Meng S, et al. MicroRNA-125a-5p partly regulates the inflammatory response, lipid uptake, and ORP9 expression in oxLDL-stimulated monocyte/macrophages. Cardiovasc Res. 2009;83(1):131-9. De forma semelhante, o miR-155 reduziu a captação de LDL oxidado diminuindo a expressão de CD36 e LOX-1.6565 Huang RS, Hu GQ, Lin B, Lin ZY, Sun CC. MicroRNA-155 silencing enhances inflammatory response and lipid uptake in oxidized low-density lipoprotein-stimulated human THP-1 macrophages. J Investig Med. 2010;58(8):961-7.
A evolução das estrias gordurosas para o ateroma fibroso (capsula fibrosa) é promovida, sobretudo, pela proliferação e migração das células musculares lisas vasculares (CMLV) para a camada intima do vaso. A proliferação e apoptose dessas células é regulada pelo TGF-β, que por sua vez é modulado negativamente pelo miR-26a (ou seja, a inibição do miR-26a promove a diferenciação das CMLVs) em soro humano.6767 Leeper NJ, Raiesdana A, Kojima Y, Chun HJ, Azuma J, Maegdefessel L, et al. MicroRNA-26a is a novel regulator of vascular smooth muscle cell function. J Cell Physiol. 2011;226(4):1035-43. Os miR-21 e miR-221 também modulam a proliferação das CMLVs, onde o miR-221 atua em resposta à sinalização do fator de crescimento derivado de plaquetas (PDGF). Além disso, a regulação negativa de p27Kip1 pelo miR-221 é crítica para a indução de proliferação celular mediada pelo PDGF, enquanto o c-Kit pode estar relacionado com a inibição da transcrição do gene contrátil específico de CMLVs, reduzindo a expressão de miocardina, um potente coativador nuclear específico das CMLVs.6868 Davis BN, Hilyard AC, Nguyen PH, Lagna G, Hata A.. Induction of microRNA-221 by platelet-derived growth factor signaling is critical for modulation of vascular smooth muscle phenotype. J Biol Chem. 2009;284(6):3728-38.
Neoangiogênese
Durante o desenvolvimento da placa aterosclerótica, os macrófagos ativados repletos de colesterol são responsáveis pela liberação de diversas citocinas, entre elas, citocinas que promovem a neoangiogênese. Entre os miRNAs envolvidos nesse processo estão o miR-221, -222, -155, -27a, -27b e -210. Em HUVEC, o miR-222/221 afeta a expressão do c-Kit,6969 Poliseno L, Tuccoli A, Mariani L, Evangelista M, Citti L, Woods K, et al. MicroRNAs modulate the angiogenic properties of HUVECs. Blood. 2006;108(9):3068-71 e o miR-222 está envolvido no remodelamento vascular mediado pela inflamação.7070 Dentelli P, Rosso A, Orso F, Olgasi C, Taverna D, Brizzi MF. microRNA-222 controls neovascularization by regulating signal transducer and activator of transcription 5A expression. Arterioscler Thromb Vasc Biol. 2010;30(8):1562-8. O miR-155 parece regular a expressão da óxido nítrico sintase endotelial (eNOS) e o relaxamento vascular dependente de endotélio.7171 Sun HX, Zeng DY, Li RT, Pang RP, Yang H, Hu YL, et al. Essential role of microRNA-155 in regulating endothelium-dependent vasorelaxation by targeting endothelial nitric oxide synthase. Hypertension. 2012;60(6):1407-14. Em modelo esferoide tridimensional, a expressão aumentada dos miR-27a/b estimula o brotamento vascular, mostrando, assim, sua ação pró-angiogênica, uma vez que esses miRNAs têm como alvo a semaforina 6A, um inibidor da angiogênese.7272 Urbich C, Kaluza D, Frömel T, Knau A, Bennewitz K, Boon RA, et al. MicroRNA-27a/b controls endothelial cell repulsion and angiogenesis by targeting semaphorin 6A. Blood. 2012;119(6):1607-16. Por fim, a expressão do miR-210 em HUVEC aumenta progressivamente em condições de hipóxia e a indução da sua expressão em condições de normóxia leva à formação de estruturas semelhantes a capilares em Matrigel guiada pelo VEGF.7373 Bonauer A, Carmona G, Iwasaki M, Mione M, Koyanagi M, Fischer A, et al. MicroRNA-92a controls angiogenesis and functional recovery of ischemic tissues in mice. Science. 2009;324(5935):1710-3.
Instabilidade e ruptura da placa
A instabilidade e ruptura da cápsula fibrosa da placa aterosclerótica depende do desequilíbrio entre a síntese e a degradação da MEC pelos fibroblastos. A ruptura da placa é o mecanismo mais importante para o surgimento do acidente vascular encefálico, IAM e morte súbita. A lise do colágeno ocorre por intermédio das enzimas metaloproteinases (MMPs), em especial as MMP-1, MMP-2, MMP-3 e MMP-9, que são liberadas principalmente por macrófagos ativados.7474 Cipollone F, Fazia M, Mezzetti A. Novel determinants of plaque instability. J Thromb Haemost. 2005;3(9):1962-75.
A MMP-9 é regulada pelos miR-133a/b, o qual também é capaz de modular a apoptose e a proliferação das CMLVs em modelos animais.7575 Torella D, Iaconetti C, Catalucci D, Ellison GM, Leone A, Waring CD, et al. MicroRNA-133 controls vascular smooth muscle cell phenotypic switch in vitro and vascular remodeling in vivo. Circ Res. 2011;109(8):880-93. Cipollone et al.7676 Cipollone F, Felicioni L, Sarzani R, Ucchino S, Spigonardo F, Mandolini C, et al. A unique microRNA signature associated with plaque instability in humans. Stroke. 2011;42(9):2556-63. investigaram, em humanos, a expressão de miRNAs e sua correlação com a instabilidade da placa aterosclerótica na artéria carótida interna. Foram avaliadas duas coortes independentes de placas ateroscleróticas coletadas em dois hospitais italianos (n = 15 e n = 38), de pacientes submetidos à endarterectomia carotídea para extracraniano de alto grau (> 70%) de estenose da artéria carótida interna. As placas foram subdivididas em grupos sintomático e assintomático de acordo com a presença ou ausência de AVE. Os autores observaram que, entre 41 miRNAs investigados, 5 miRNAs (miR-100, -127, -145, -133a e -133b) apresentaram expressão aumentada em placas sintomáticas (onde houve AVE) em comparação à placas assintomáticas.7676 Cipollone F, Felicioni L, Sarzani R, Ucchino S, Spigonardo F, Mandolini C, et al. A unique microRNA signature associated with plaque instability in humans. Stroke. 2011;42(9):2556-63. É importante ressaltar que a discrepância na expressão de miRNAs entre placas instáveis e estáveis não estava relacionada a diferenças em fatores de risco convencionais ou terapias concomitantes, pois essas variáveis estavam bem equilibradas entre os dois grupos. Ao incubar HUVEC com o miR-133a, houve redução da expressão da proteína alvo MMP-9, enquanto as células incubadas com miR-133a ou miR-145 apresentaram menor expressão de inibidor do ativador de plasminogênio 1 (PAI-1).7676 Cipollone F, Felicioni L, Sarzani R, Ucchino S, Spigonardo F, Mandolini C, et al. A unique microRNA signature associated with plaque instability in humans. Stroke. 2011;42(9):2556-63.
Conclusão
Apesar da complexidade e dos desafios, a identificação dos miRNAs desregulados é crucial, uma vez que possibilita uma melhor compressão dos mecanismos celulares e moleculares envolvidos nas DCVs. A pesquisa sobre miRNAs teciduais e circulantes poderá auxiliar no desenvolvimento de marcadores circulantes de diagnóstico e prognóstico mais acurados em comparação aos já utilizados, assim como novas estratégias terapêuticas para os diferentes estágios da DCV.
Apesar do avanço neste campo, ainda existem algumas limitações, por exemplo, no uso dos miRNAs circulantes como biomarcadores. Ainda não são conhecidos completamente os processos moleculares que regulam o empacotamento e a liberação de miRNAs extracelulares, quer por meio de mecanismos mediados por vesículas ou não. Além disso, a detecção dos miRNAs circulantes demanda alto custo técnico, o que limitaria, a princípio, o seu uso na rotina clínica laboratorial. Outro fator limitante é a onipresença dos miRNAs na circulação sanguínea, demandando, assim, investigações adicionais para determinar a sua origem tecidual.
-
Fontes de financiamentoO presente estudo foi financiado pela FAPERJ.
-
Vinculação acadêmicaEste artigo é parte de tese de Doutorado de Debora Cristina Pereira da Silva pelo Programa de Pós-graduação em Ciências Cardiovasculares da Universidade Federal Fluminense.
References
-
1Lee RC, Feinbaum RL, Ambros V. The C. elegans heterochronic gene lin-4 encodes small RNAs with antisense complementarity to lin-14. Cell. 1993;75(5):843-54.
-
2Mattick JS, Makunin IV. Non-coding RNA. Hum Mol Genet. 2006;15(spec1):R17-29.
-
3Poy MN, Eliasson L, Krutzfeldt J, Kuwajima S, Ma X, Macdonald PE, et al. A pancreatic islet-specific microRNA regulates insulin secretion. Nature. 2004;432(7014):226-30.
-
4Calin GA, Sevignani C, Dumitru CD, Hyslop T, Noch E, Yendamuri S, et al. Human microRNA genes are frequently located at fragile sites and genomic regions involved in cancers. Proc Natl Acad Sci U S A. 2004;101(9):2999-3004.
-
5Zhou X, Zuo Z, Zhou F, Zhao W, Sakaguchi Y, Suzuki T, et al. Profiling sex-specific piRNAs in zebrafish. Genetics. 2010;186(4):1175-85.
-
6Chang TC, Mendell JT. MicroRNAs in vertebrate physiology and human disease. Annu Rev Genomics Hum Genet. 2007;8:215-39.
-
7Bartel DP, Chen CZ. Micromanagers of gene expression: the potentially widespread influence of metazoan microRNAs. Nat Rev Genet. 2004;5(5):396-400.
-
8Kim VN. MicroRNA biogenesis: coordinated cropping and dicing. Nat Rev Mol Cell Biol. 2005;6(5):376-85.
-
9Han J, Lee Y, Yeom KH, Nam JW, Heo I, Rhee JK, et al. Molecular basis for the recognition of primary microRNAs by the Drosha-DGCR8 complex. Cell. 2006;125(5):887-901.
-
10Lee Y, Han J, Yeom KH, Jin H, Kim VN. Drosha in primary microRNA processing. Cold Spring Harb Symp Quant Biol. 2006;71:51-7.
-
11Yi R, Qin Y, Macara IG, Cullen BR. Exportin-5 mediates the nuclear export of pre-microRNAs and short hairpin RNAs. Genes Dev. 2003;17(24):3011-6.
-
12Kim VN, Han J, Siomi MC. Biogenesis of small RNAs in animals. Nat Rev Mol Cell Biol. 2009;10(2):126-39.
-
13Krützfeldt J, Poy MN, Stoffel M. Strategies to determine the biological function of microRNAs. Nat Genet. 2006;38 (Suppl):S14-9.
-
14Rand TA, Petersen S, Du F, Wang X. Argonaute2 cleaves the anti-guide strand of siRNA during RISC activation. Cell. 2005;123(4):621-9.
-
15Tang G, Reinhart BJ, Bartel DP, Zamore PD. A biochemical framework for RNA silencing in plants. Genes Dev. 2003;17(1):49-63.
-
16Zeng Y, Wagner EJ, Cullen BR. Both natural and designed micro RNAs can inhibit the expression of cognate mRNAs when expressed in human cells. Mol Cell. 2002;9(6):1327-33.
-
17Gebauer F, Hentze MW. Molecular mechanisms of translational control. Nat Rev Mol Cell Biol. 2004;5(10):827-35.
-
18Zhang J, Zhao H, Gao Y, Zhang W. Secretory miRNAs as novel cancer biomarkers. Biochim Biophys Acta. 2012;1826(1):32-43.
-
19Muoio DM, Newgard CB. Mechanisms of disease: molecular and metabolic mechanisms of insulin resistance and beta-cell failure in type 2 diabetes. Nat Rev Mol Cell Biol. 2008;9(3):193-205.
-
20van Rooij E, Liu N, Olson EN. MicroRNAs flex their muscles. Trends Genet. 2008;24(4):159-66.
-
21Wang J, Huang W, Xu R, Nie Y, Cao X, Meng J, et al. MicroRNA-24 regulates cardiac fibrosis after myocardial infarction. J Cell Mol Med. 2012;16(9):2150-60.
-
22Cheng Y, Tan N, Yang J, Liu X, Cao X, He P, et al. A translational study of circulating cell-free microRNA-1 in acute myocardial infarction. Clin Sci (Lond). 2010;119(2):87-95.
-
23Rao PK, Toyama Y, Chiang HR, Gupta S, Bauer M, Medvid R, et al. Loss of cardiac microRNA-mediated regulation leads to dilated cardiomyopathy and heart failure. Circ Res. 2009;105(6):585-94.
-
24Xin Y,Yang C, Han Z. Circulating miR-499 as a potential biomarker for acute myocardial infarction. Ann Transl Med. 2016;v.4.
-
25Xiao J, Shen B, Li J, Lv D, Zhao Y, Wang F, et al. Serum microRNA-499 and microRNA-208a as biomarkers of acute myocardial infarction. Int J Clin Exp Med. 2014;7(1):136-41
-
26Chen X, Zhang L, Su T, Li H, Huang Q, Wu D, et al. Kinetics of plasma microRNA-499 expression in acute myocardial infarction. J Thorac Dis. 2015;7(5):890-6.
-
27Bye A, Røsjø H, Nauman J, Silva GJ, Follestad T, Omland T, et al. Circulating microRNAs predict future fatal myocardial infarction in healthy individuals - The HUNT study. J Mol Cell Cardiol. 2016 Aug;97:162-8.
-
28Jia K, Shi P, Han X, Chen T, Tang H, Wang J. Diagnostic value of miR-30d-5p and miR-125b-5p in acute myocardial infarction. Mol Med Rep. 2016;14(1):184-94.
-
29Yan H, Ma F, Zhang Y, Wang C, Qiu D, Zhou K, et al. miRNAs as biomarkers for diagnosis of heart failure: A systematic review and meta-analysis. Medicine (Baltimore). 2017;96(22):e6825.
-
30Cakmak HA, Coskunpinar E, Ikitimur B, Barman HA, Karadag B, Tiryakioglu NO. The prognostic value of circulating microRNAs in heart failure: preliminary results from a genome-wide expression study. J Cardiovasc Med (Hagerstown). 2015;16(6):431-7.
-
31Vegter EL, van der Meer P, de Windt LJ, Pinto YM, Voors AA. MicroRNAs in heart failure: from biomarker to target for therapy. Eur J Heart Fail. 2016;18(5):457-68.
-
32Lakschevitz F, Aboodi G, Tenenbaum H, Glogauer M. Diabetes and periodontal diseases: interplay and links. Curr Diabetes Rev. 2011;7(6):433-9.
-
33Harling L, Lambert J, Ashrafian H, Darzi A, Gooderham NJ, Athanasiou T. Elevated serum microRNA 483-5p levels may predict patients at risk of post-operative atrial fibrillation. Eur J Cardiothorac Surg. 2017;51(1):73-8.
-
34Feldman A, Moreira DA, Gun C, Wang HL, Hirata MH, de Freitas Germano J, et al. Analysis of circulating miR-1, miR-23a, and miR-26a in atrial fibrillation patients undergoing coronary bypass artery grafting surgery. Ann Hum Genet. 2017;81(3):99-105.
-
35Wei XJ, Han M, Yang FY, Wei GC, Liang ZG, Yao H, et al. Biological significance of miR-126 expression in atrial fibrillation and heart failure. Braz J Med Biol Res. 2015;48(11):983-9.
-
36Goren Y, Meiri E, Hogan C, Mitchell H, Lebanony D, Salman N, et al. Relation of reduced expression of MiR-150 in platelets to atrial fibrillation in patients with chronic systolic heart failure. Am J Cardiol. 2014;113(6):976-81.
-
37Zernecke A, Bidzhekov K, Noels H, Shagdarsuren E, Gan L, Denecke B, et al. Delivery of microRNA-126 by apoptotic bodies induces CXCL12-dependent vascular protection. Sci Signal. 2009;2(100): 81.
-
38Jeong HS, Kim JY, Lee SH, Hwang J, Shin JW, Song KS, et al. Synergy of circulating miR-212 with markers for cardiovascular risks to enhance estimation of atherosclerosis presence. PLoS One. 2017;12(5):e0177809.
-
39Liu CZ, Zhong Q, Huang YQ. Elevated plasma MiR-29a levels are associated with increased carotid intima-media thickness in atherosclerosis patients. Tohoku J Exp Med. 2017;241(3):183-8.
-
40Piubelli C, Meraviglia V, Pompilio G, D'Alessandra Y, Colombo GI, Rossini A. microRNAs and Cardiac Cell Fate. Cells. 2014;3(3):802-23
-
41Zhao Y, Samal E, Srivastava D. Serum response factor regulates a muscle-specific microRNA that targets Hand2 during cardiogenesis. Nature. 2005;436(7048):214-20.
-
42Carmean CM, Bobe AM, Yu JC, Volden PA, Brady MJ. Refeeding-induced brown adipose tissue glycogen hyper-accumulation in mice is mediated by insulin and catecholamines. PLoS One. 2013;8(7):e67807.
-
43Thum T, Gross C, Fiedler J, Fischer T, Kissler S, Bussen M, et al. MicroRNA-21 contributes to myocardial disease by stimulating MAP kinase signalling in fibroblasts. Nature. 2008;456(7224):980-4
-
44Tatsuguchi M, Seok HY, Callis TE, Thomson JM, Chen JF, Newman M, et al. Expression of microRNAs is dynamically regulated during cardiomyocyte hypertrophy. J Mol Cell Cardiol. 2007;42(6):1137-41.
-
45Tony H, Meng K, Wu B, Yu A, Zeng Q, Yu K, et al. MicroRNA-208a Dysregulates Apoptosis Genes Expression and Promotes Cardiomyocyte Apoptosis during Ischemia and Its Silencing Improves Cardiac Function after Myocardial Infarction. Mediators Inflamm. 2015;2015 Nov 25:479123.
-
46Lee SY, Lee CY, Ham O, Moon JY, Lee J, Seo HH, et al. microRNA-133a attenuates cardiomyocyte hypertrophy by targeting PKCdelta and Gq. Mol Cell Biochem. 2018;439(1-2):105-15
-
47Wu Y, Wang YQ, Wang BX. [MicroRNA-133a attenuates isoproterenol-induced neonatal rat cardiomyocyte hypertrophy by downregulating L-type calcium channel alpha1C subunit gene expression.] Zhonghua Xin Xue Guan Bing Za Zhi. 2013;41(6):507-13.
-
48Wang YS, Zhou J, Hong K, Cheng XS, Li YG. MicroRNA-223 displays a protective role against cardiomyocyte hypertrophy by targeting cardiac troponin I-interacting kinase. Cell Physiol Biochem. 2015;35(4):1546-56.
-
49Bao Q, Chen L, Li J, Zhao M, Wu S, Wu W, et al. Role of microRNA-124 in cardiomyocyte hypertrophy inducedby angiotensin II. Cell Mol Biol (Noisy-le-grand). 2017;63(4):23-27.
-
50Shieh JT, Huang Y, Gilmore J, Srivastava D. Elevated miR-499 levels blunt the cardiac stress response. PLoS One. 2011;6(5):e19481
-
51Duisters RF, Tijsen AJ, Schroen B, Leenders JJ, Lentink V, van der Made I, et al. miR-133 and miR-30 regulate connective tissue growth factor: implications for a role of microRNAs in myocardial matrix remodeling. Circ Res. 2009;104(2):170-8,
-
52He Q, Wang CM, Qin JY, Zhang YJ, Xia DS, Chen X, et al. Effect of miR-203 expression on myocardial fibrosis. Eur Rev Med Pharmacol Sci. 2017;21(4):837-42.
-
53Lai KB, Sanderson JE, Izzat MB, Yu CM. Micro-RNA and mRNA myocardial tissue expression in biopsy specimen from patients with heart failure. Int J Cardiol. 2015 Nov 15;199:79-83.
-
54Cheng R, Dang R, Zhou Y, Ding M, Hua H. MicroRNA-98 inhibits TGF-beta1-induced differentiation and collagen production of cardiac fibroblasts by targeting TGFBR1. Hum Cell. 2017;30(3):192-200.
-
55Ikeda S, Kong SW, Lu J, Bisping E, Zhang H, Allen PD, et al. Altered microRNA expression in human heart disease. Physiol Genomics. 2007;31(3):367-73.
-
56Carè A, Catalucci D, Felicetti F, Bonci D, Addario A, Gallo P, et al. MicroRNA-133 controls cardiac hypertrophy. Nat Med. 2007;13(5):613-8.
-
57Yang B, Lin H, Xiao J, Lu Y, Luo X, Li B, et al. The muscle-specific microRNA miR-1 regulates cardiac arrhythmogenic potential by targeting GJA1 and KCNJ2. Nat Med. 2007;13(4):486-91.
-
58Galkina E, Ley K. Immune and inflammatory mechanisms of atherosclerosis (*). Annu Rev Immunol. 2009;27:165-97.
-
59Fang Y, Shi C, Manduchi E, Civelek M, Davies PF. MicroRNA-10a regulation of proinflammatory phenotype in athero-susceptible endothelium in vivo and in vitro. Proc Natl Acad Sci U S A. 2010;107(30):13450-5.
-
60Sun X, Icli B, Wara AK, Belkin N, He S, Kobzik L, et al. MicroRNA-181b regulates NF-?B-mediated vascular inflammation. J Clin Invest. 2012;122(6):1973-90.
-
61Suárez Y, Wang C, Manes TD, Pober JS. Cutting edge: TNF-induced microRNAs regulate TNF-induced expression of E-selectin and intercellular adhesion molecule-1 on human endothelial cells: feedback control of inflammation. J Immunol. 2010;184(1):21-5.
-
62Rayner KJ, Suárez Y, Dávalos A, Parathath S, Fitzgerald ML, Tamehiro N, et al. MiR-33 contributes to the regulation of cholesterol homeostasis. Science. 2010;328(5985):1570-3.
-
63Rayner KJ, Sheedy FJ, Esau CC, Hussain FN, Temel RE, Parathath S, et al. Antagonism of miR-33 in mice promotes reverse cholesterol transport and regression of atherosclerosis. J Clin Invest. 2011;121(7):2921-31.
-
64Elmén J, Lindow M, Schütz S, Lawrence M, Petri A, Obad S, et al. LNA-mediated microRNA silencing in non-human primates. Nature. 2008;452(7189):896-9.
-
65Huang RS, Hu GQ, Lin B, Lin ZY, Sun CC. MicroRNA-155 silencing enhances inflammatory response and lipid uptake in oxidized low-density lipoprotein-stimulated human THP-1 macrophages. J Investig Med. 2010;58(8):961-7.
-
66Chen T, Huang Z, Wang L, Wang Y, Wu F, Meng S, et al. MicroRNA-125a-5p partly regulates the inflammatory response, lipid uptake, and ORP9 expression in oxLDL-stimulated monocyte/macrophages. Cardiovasc Res. 2009;83(1):131-9.
-
67Leeper NJ, Raiesdana A, Kojima Y, Chun HJ, Azuma J, Maegdefessel L, et al. MicroRNA-26a is a novel regulator of vascular smooth muscle cell function. J Cell Physiol. 2011;226(4):1035-43.
-
68Davis BN, Hilyard AC, Nguyen PH, Lagna G, Hata A.. Induction of microRNA-221 by platelet-derived growth factor signaling is critical for modulation of vascular smooth muscle phenotype. J Biol Chem. 2009;284(6):3728-38.
-
69Poliseno L, Tuccoli A, Mariani L, Evangelista M, Citti L, Woods K, et al. MicroRNAs modulate the angiogenic properties of HUVECs. Blood. 2006;108(9):3068-71
-
70Dentelli P, Rosso A, Orso F, Olgasi C, Taverna D, Brizzi MF. microRNA-222 controls neovascularization by regulating signal transducer and activator of transcription 5A expression. Arterioscler Thromb Vasc Biol. 2010;30(8):1562-8.
-
71Sun HX, Zeng DY, Li RT, Pang RP, Yang H, Hu YL, et al. Essential role of microRNA-155 in regulating endothelium-dependent vasorelaxation by targeting endothelial nitric oxide synthase. Hypertension. 2012;60(6):1407-14.
-
72Urbich C, Kaluza D, Frömel T, Knau A, Bennewitz K, Boon RA, et al. MicroRNA-27a/b controls endothelial cell repulsion and angiogenesis by targeting semaphorin 6A. Blood. 2012;119(6):1607-16.
-
73Bonauer A, Carmona G, Iwasaki M, Mione M, Koyanagi M, Fischer A, et al. MicroRNA-92a controls angiogenesis and functional recovery of ischemic tissues in mice. Science. 2009;324(5935):1710-3.
-
74Cipollone F, Fazia M, Mezzetti A. Novel determinants of plaque instability. J Thromb Haemost. 2005;3(9):1962-75.
-
75Torella D, Iaconetti C, Catalucci D, Ellison GM, Leone A, Waring CD, et al. MicroRNA-133 controls vascular smooth muscle cell phenotypic switch in vitro and vascular remodeling in vivo. Circ Res. 2011;109(8):880-93.
-
76Cipollone F, Felicioni L, Sarzani R, Ucchino S, Spigonardo F, Mandolini C, et al. A unique microRNA signature associated with plaque instability in humans. Stroke. 2011;42(9):2556-63.
Datas de Publicação
-
Publicação nesta coleção
Nov 2018