RESUMO
Apresentamos listagem da entomofauna visitante de flores do estado de Mato Grosso do Sul (MS) com base na compilação de informações obtidas em 17 estudos, a maioria realizado em áreas de Cerrado (n = 11) e menos frequentemente no Pantanal (n = 6). Foram registrados 10 grupos de insetos, pertencentes a seis ordens, 80 famílias e 411 espécies. Maior riqueza foi amostrada para o Cerrado (307 spp.) que Pantanal (147 spp.), com somente 43 espécies (10,4%) em comum entre estes biomas. Anthophila foi o grupo mais rico (155 spp.), seguido por besouros (82), borboletas/mariposas (53) e vespas (45), que junto totalizaram 81,5% das espécies. Maior riqueza de abelhas está relacionada ao fato da maioria dos trabalhos enfocarem este grupo, além da especialização deste grupo na utilização de recursos florais. Surpreendente foi o segundo lugar ocupado por besouros em relação a outros visitantes mais “ativos” e “habituais”, como lepidópteros e moscas. Em MS os acervos e grupos de pesquisa com entomofauna antófila são restritos e/ou incipientes, sendo necessário fortalecimento dos mesmos através de parcerias, intercâmbios e formação de recursos humanos na área.
PALAVRAS-CHAVE
Biodiversidade de insetos; visitante floral; Programa BIOTA MS.
ABSTRACT
We present a checklist of the anthophilous entomofauna of Mato Grosso do Sul state (MS) based on information compiled from 17 studies, most of them achieved in Cerrado vegetation (n = 11) and less frequently in the Pantanal (n = 6). We recorded 10 groups of insects, belonging to six orders, 80 families and 411 species. Higher richness was sampled for Cerrado (307 spp.) compared to Pantanal (147 spp.), with only 43 species (10.4%) common to both biomes. Anthophila was the richest group (155 spp.), followed by beetles (82), butterflies/moths (53) and wasps (45), which totalized 81.5% of species. The highest richness of bees is related to the fact the most studies are concentrated in this group, besides the specialization of this group in utilization of floral resources. Surprising was the beetles occupying second place compared to others more “active” and “habitual” visitors, such as butterflies and flies. The entomofauna collections and research teams in MS are limited and/or incipient and they should be strenghtened through partnerships, exchange and capacity building in this biological group.
KEYWORDS
Insect biodiversity; floral visitor; BIOTA MS Program
A fauna antófila é constituída por diversos grupos de animais que visitam flores para buscar recursos alimentares (e.g. pólen, néctar, óleo, tecido floral, “sweet jelly”), materiais para a construção dos ninhos (óleo, resina) e/ou “perfumes” e podem também utilizar a flor como sítio de cópula, berçário e/ou dormitório (Simpson & Neff, 1981Simpson, B. B. & Neff, J. L. 1981. Floral rewards: alternatives to pollen and nectar. Annals of the Missouri Botanical Garden 68:301-322. ; Proctor et al., 1996Proctor, M.; Yeo, P. & Lack, A. 1996. The natural history of pollination. Portland, Timber Press. 487p.; Sazima et al., 2001Sazima, M.; Vogel, S.; Prado, A. L.; Oliveira, D. M.; Franz, G. & Sazima, I. 2001. The sweet jelly of Combretum lanceolatum flowers (Combretaceae): a cornucopia resource for bird pollinators in the Pantanal, western Brazil. Plant Systematics and Evolution 227:195-208.; Stehlmann & Semir, 2001Stehlmann, J. R. & Semir, J. 2001. Biologia reprodutiva de Calibrachoa elegans (Miers) (Solanaceae). Revista Brasileira de Botânica24:43-49. ; Dufaÿ & Anstett, 2003Dufaÿ, M. & Anstett, M. C. 2003. Conflicts between plants and pollinators that reproduce within inflorescences: evolutionary variations on a theme. Oikos 100:3-14.). Os visitantes florais são invertebrados (e.g. abelhas, moscas, besouros, vespas, borboletas, mariposas, grilos, baratas) e vertebrados (e.g. beija-flores, morcegos, lagartos) de várias Ordens (Faegri & van der Pijl, 1979Faegri, K. & van der Pijl, L. 1979. The principles of pollination ecology. London, Pergamon Press. 242p.; Proctor et al., 1996Proctor, M.; Yeo, P. & Lack, A. 1996. The natural history of pollination. Portland, Timber Press. 487p.; Nyhagen et al., 2001Nyhagen, D. F.; Kragelund, C.; Olesen, J. M. & Jones, C. G. 2001. Insular interactions between lizards and flowers: flower visitation by an endemic Mauritian gecko. Journal of Tropical Ecology 17:755-761.; Vlasáková et al., 2008Vlasáková, B.; Kalinová, B.; Gustafsson, M. H. G. & Teichert, H. 2008. Cockroaches as pollinators of Clusia aff. sellowiana (Clusiaceae) on inselbergs in French Guiana. Annals of Botany102:295-304.; Micheneau et al., 2010Micheneau, C.; Fournel, J.; Warren, B. H.; Hugel, S.; Gauvin-Bialecki, A.; Pailler, T.; Strasberg, D. & Chase, M. W. 2010. Orthoptera, a new order of pollinator. Annals of Botany 105:1-10.), com predomínio de insetos. A maioria dos insetos antófilos geralmente não é amostrada nos levantamentos faunísticos habituais, exceto pelas abelhas, que são essencialmente herbívoras e dependentes dos recursos florais.
A fauna antófila quando visita as flores, principalmente as abelhas (Anthophila), podem atuar como polinizadores. A polinização é serviço ambiental de grande relevância para a manutenção da integridade dos ecossistemas e para a sustentabilidade da agricultura, necessitando haver maior atenção no manejo agrícola e nas ações para a conservação dos polinizadores nativos. Por esta razão, o serviço ambiental prestado pelos polinizadores foi considerado uma das prioridades de estudo para o século XXI e em 2000 foi criado um programa que visa a conservação e o uso sustentado de polinizadores (ver Laroca & Orth, 2002Laroca, S. & Orth, A. I. 2002 Melissocoenology: historical perspective, method of sampling, and recommendations to the “Program of conservation and sustainable use of pollinators, with emphasis on bees” (ONU). In: Kevan, P. & Imperatriz Fonseca, V. L. eds. Pollinating bees. The conservation link between agriculture and nature. Brasília, Ministério do Meio Ambiente, p.217-225.), conhecido como “Iniciativa Internacional dos Polinizadores”. No Brasil a “Iniciativa Brasileira de Polinizadores” (IBP) foi legalmente instituída em 2005 com o objetivo de: (i) planejar e definir ações para a conscientização da importância da polinização, (ii) fornecer subsídios para a formulação de políticas públicas que favoreçam o manejo, conservação e uso sustentável de polinizadores na agricultura, (iii) disseminar os conhecimentos gerados através de livros e websites, (iv) incrementar a capacitação de pessoas envolvidas com o tema e (v) avançar nos conhecimentos sobre polinização e polinizadores (Imperatriz-Fonseca et al., 2007Imperatriz-Fonseca, V.; Saraiva, A. M. & Gonçalves, L. 2007. A iniciativa brasileira de polinizadores e os avanços para a compreensão do papel dos polinizadores como produtores de serviços ambientais. Bioscience Journal 23:100-106. ).
Tomando como foco a conservação de polinizadores, um dos resultados da IBP foi a publicação da Bibliografia Brasileira de Polinização e Polinizadores (MMA, 2006MMA - Ministério do Meio Ambiente. 2006. Disponível em: <Disponível em: http://www.mma.gov.br/estruturas/chm/_arquivos/lista_polinizadores.pdf
> . Acessado em: 08/08/2012.
http://www.mma.gov.br/estruturas/chm/_ar...
), levantamento detalhado da produção científica nacional sobre o tema. De acordo com este trabalho, o Pantanal aparece como o bioma com o menor número de estudos realizados. Considerando que o levantamento de espécies é o primeiro e essencial passo para avaliação do status de conservação, a falta dessa informação básica pode resultar em estratégias de conservação equivocadas, aumentando o risco de eventos irreversíveis de extinção de espécies.
Apresentamos a primeira listagem de visitantes florais de Mato Grosso do Sul (MS) com base na compilação de informações obtidas em estudos realizados no estado. Discutimos as principais lacunas e dificuldades existentes em termos de amostragem, o que certamente contribuirá para indicar áreas prioritárias para futuros estudos sobre o grupo, com consequente aumento do número de espécies registradas.
MATERIAL E MÉTODOS
O check list da entomofauna antófila foi elaborado a partir do levantamento bibliográfico sobre visitantes florais em periódicos científicos, boletins técnicos, livros, monografias de conclusão de curso, dissertações e teses, dentre outros. Foram considerados tanto trabalhos de levantamento como estudos de polinização. Os táxons não identificados até o nível específico foram inseridos à lista somente quando adicionavam nova família, tribo ou gênero. Os insetos foram organizados nos seguintes grupos: abelhas, besouros, borboletas/mariposas, formigas, hemípteros, moscas/mosquitos, vespas e outros. Os biomas foram classificados segundo IBGE (2004IBGE. 2004. Instituto Brasileiro de Geografia e Estatística. Disponível em: <Disponível em: www.ibge.gov.br
>. Acessado em 08/08/2012.
www.ibge.gov.br...
).
RESULTADOS E DISCUSSÃO
Lista das publicações e espécies para MS com comentários. Para o estado de MS foram registrados somente 17 estudos que trazem informações sobre visitantes florais, sendo sete artigos de periódicos, sete monografias/dissertações e três capítulos de livros. A maioria dos estudos (10) gerou dados para apenas um grupo de insetos, geralmente abelhas (Consolaro, 2002Consolaro, H. N. 2002. Levantamento das abelhas (Hymenoptera, Apoidea) do campus da Universidade Federal de Mato Grosso do Sul, Campo Grande, MS. Monografia de conclusão de curso. Campo Grande, Universidade Federal de Mato Grosso do Sul.; Rodrigues, 2002Rodrigues, L. C. 2002. Biologia da polinização de duas espécies de Bromelia (Bromeliaceae) em cerrado de Mato Grosso do Sul. Monografia de conclusão de curso. Campo Grande, Universidade Federal de Mato Grosso do Sul.; Oda, 2003Oda, F. H. 2003. Levantamento e o papel das abelhas nas flores de espécies vegetais em remanescente de cerrado em Campo Grande, MS. Monografia de conclusão de curso. Campo Grande, Universidade Federal de Mato Grosso do Sul.; Vieira et al., 2008Vieira, G. H. C.; Marchini, L. C.; Souza, B. A. & Moreti, A. C. C. C. 2008. Fontes florais usadas por abelhas (Hymenoptera, Apoidea) em área de Cerrado no município de Cassilândia, Mato Grosso do Sul, Brasil. Ciência e Agrotecnologia 32:1454-1460.; Oliveira et al., 2007Oliveira, M. I. B.; Polido, C. A.; Costa, L. C. & Fava, W. S. 2007. Sistema reprodutivo e polinização de Byrsonima intermedia A. Juss. (Malpighiaceae) em Mato Grosso do Sul, Brasil. Revista Brasileira de Biociências 5:756-758.; Maier, 2009Maier, J. E. 2009. Levantamento de abelhas e atuação na polinização de espécies vegetais em remanescente urbano de cerrado, Campo Grande, Mato Grosso do Sul. Monografia de conclusão de curso. Campo Grande, Universidade Federal de Mato Grosso do Sul.; Ferreira et al., 2010Ferreira, M. G.; Manente-Balestieri, F. C. D. & Balestieri, J. B. P. 2010. Pólen coletado por Scaptotrigona depilis (Moure) (Hymenoptera, Meliponini), na região de Dourados, Mato Grosso do Sul, Brasil. Revista Brasileira de Entomologia54(2):258-262.; Longo & Fischer, 2006Longo, J. M. & Fischer, E. 2006. Efeito da taxa de secreção de néctar sobre a polinização e a produção de sementes em flores de Passiflora speciosa Gardn. (Passifloraceae) no Pantanal. Revista Brasileira de Botânica29:481-488.; Vilas Boas, 2009Vilas Boas, J. C. 2009. Fenologia e biologia reprodutiva de Byrsonima intermedia A. Juss. e B. pachyphylla Griseb (Malpighiaceae) em remanescente de cerrado, Mato Grosso do Sul, Brasil. Dissertação de Mestrado. Campo Grande, Universidade Federal de Mato Grosso do Sul.; Aoki et al., 2012Aoki, C.; Teixeira-Gamarra, M. C.; Barônio, G. J.; Sigrist, M. R. & Laroca, S. 2012. Diversidade de abelhas (Hymenoptera: Apoidea) e recursos florais na RPPN Engenheiro Eliezer Batista, Pantanal de Mato Grosso do Sul. In: Rabelo, A. C. P.; Moreira, V. F.; Bertassoni, A. & Aoki, C. orgs. Descobrindo o Paraíso. Aspectos Biológicos da Reserva Particular do Patrimônio Natural Engenheiro Eliezer Batista. Rio de Janeiro, Instituto Homem Pantaneiro, p.82-111.). Outros incluíram também vespas (Boff, 2008Boff, S. 2008. Flora de capões e Hymenoptera (abelhas e vespas) visitantes de flores no pantanal do Miranda-Abobral. Dissertação de Mestrado. Campo Grande, Universidade Federal de Mato Grosso do Sul. ; Auko et al., 2012Auko, T. H.; Trad, B. M.; Silvestre, R. & Aoki, C.2012. Vespas Aculeata da Reserva Particular do Patrimônio Natural Engenheiro Eliezer Batista In: Rabelo, A. C. P.; Moreira, V. F.; Bertassoni, A.& Aoki, C.orgs. Descobrindo o Paraíso. Aspectos Biológicos da Reserva Particular do Patrimônio Natural Engenheiro Eliezer Batista. Rio de Janeiro, Instituto Homem Pantaneiro, p.240-261), besouros e/ou esfingídeos (Munin et al., 2008Munin, R. L.; Teixeira, R. C. & Sigrist, M. R.2008. Esfingofilia e sistema de reprodução de Bauhinia curvula Benth. (Leguminosae: Caesalpinioideae) em cerrado no Centro-Oeste brasileiro. Revista Brasileira de Botânica31:15-25.). Quatro estudos contemplaram grupos de animais que não são considerados “polinizadores habituais” (Aoki & Sigrist, 2006Aoki, C. & Sigrist, M. R. 2006. Inventário dos visitantes florais no Complexo Aporé-Sucuriú. In: Pagoto, T. C. S. & de Souza, P. R. orgs. Biodiversidade do Complexo Aporé-Sucuriú. Subsídios à conservação e ao manejo do Cerrado. Campo Grande, Editora da Universidade Federal de Mato Grosso do Sul, p.143-162.; Oliveira & Sigrist, 2008Oliveira, M. B. & Sigrist, M. R.2008. Fenologia reprodutiva, polinização e reprodução de Dipteryx alata Vogel (Leguminosae - Papilionoideae) em Mato Grosso do Sul, Brasil. Revista Brasileira de Botânica31:195-207. ; Fava et al., 2011Fava, W. S.; Sigrist, M. R. & Covre, W. S. 2011. Attalea phalerata and Bactris glaucescens (Arecaceae, Arecoideae): Phenology and pollination ecology in the Pantanal, Brazil. Flora 206:575-584.; Souza, 2012Souza, C. S. 2012. Fauna antófila diurna em formação chaquenha brasileira: composição e flora visitada. Monografia de conclusão de curso. Campo Grande, Universidade Federal de Mato Grosso do Sul.), sendo que apenas um investiga a fauna antófila como um todo (Aoki & Sigrist, 2006) (Tab. I).
Insetos visitantes de flores amostrados em vegetação de Cerrado e Pantanal, no Mato Grosso do Sul, Brasil e referência bibliográfica: 1, Consolaro (2002); 2, Rodrigues (2002); 3, Oda (2003); 4, Aoki & Sigrist (2006); 5, Oliveira et al. (2007); 6, Oliveira & Sigrist (2008); 7, Munin et al. (2008); 8, Vieira et al. (2008); 9, Maier (2009); 10, Vilas Boas (2009); 11, Ferreira et al. (2010); 12, Longo & Fischer (2006); 13, Boff (2008); 14, Fava et al . (2011); 15, Aoki et al . (2012); 16, Auko et al . (2012); 17, Souza (2012).
A maioria dos estudos foi realizada no Cerrado (n = 11) e menos frequentemente no Pantanal (n = 6) (Fig. 1). Não foram encontrados estudos em áreas de com vegetação de Mata Atlântica, bioma restrito à região sul do estado. Dentre os estudos em Cerrado, nove foram realizados em remanescentes florestais inseridos em área urbana no centro (Consolaro, 2002Consolaro, H. N. 2002. Levantamento das abelhas (Hymenoptera, Apoidea) do campus da Universidade Federal de Mato Grosso do Sul, Campo Grande, MS. Monografia de conclusão de curso. Campo Grande, Universidade Federal de Mato Grosso do Sul.; Rodrigues, 2002Rodrigues, L. C. 2002. Biologia da polinização de duas espécies de Bromelia (Bromeliaceae) em cerrado de Mato Grosso do Sul. Monografia de conclusão de curso. Campo Grande, Universidade Federal de Mato Grosso do Sul.; Oda, 2003Oda, F. H. 2003. Levantamento e o papel das abelhas nas flores de espécies vegetais em remanescente de cerrado em Campo Grande, MS. Monografia de conclusão de curso. Campo Grande, Universidade Federal de Mato Grosso do Sul.; Oliveira et al., 2007Oliveira, M. I. B.; Polido, C. A.; Costa, L. C. & Fava, W. S. 2007. Sistema reprodutivo e polinização de Byrsonima intermedia A. Juss. (Malpighiaceae) em Mato Grosso do Sul, Brasil. Revista Brasileira de Biociências 5:756-758.; Munin et al., 2008Munin, R. L.; Teixeira, R. C. & Sigrist, M. R.2008. Esfingofilia e sistema de reprodução de Bauhinia curvula Benth. (Leguminosae: Caesalpinioideae) em cerrado no Centro-Oeste brasileiro. Revista Brasileira de Botânica31:15-25.; Oliveira & Sigrist, 2008Oliveira, M. B. & Sigrist, M. R.2008. Fenologia reprodutiva, polinização e reprodução de Dipteryx alata Vogel (Leguminosae - Papilionoideae) em Mato Grosso do Sul, Brasil. Revista Brasileira de Botânica31:195-207. ; Maier, 2009Maier, J. E. 2009. Levantamento de abelhas e atuação na polinização de espécies vegetais em remanescente urbano de cerrado, Campo Grande, Mato Grosso do Sul. Monografia de conclusão de curso. Campo Grande, Universidade Federal de Mato Grosso do Sul.; Vilas Boas, 2009Vilas Boas, J. C. 2009. Fenologia e biologia reprodutiva de Byrsonima intermedia A. Juss. e B. pachyphylla Griseb (Malpighiaceae) em remanescente de cerrado, Mato Grosso do Sul, Brasil. Dissertação de Mestrado. Campo Grande, Universidade Federal de Mato Grosso do Sul.) ou mais ao sul do estado (Ferreira et al., 2010Ferreira, M. G.; Manente-Balestieri, F. C. D. & Balestieri, J. B. P. 2010. Pólen coletado por Scaptotrigona depilis (Moure) (Hymenoptera, Meliponini), na região de Dourados, Mato Grosso do Sul, Brasil. Revista Brasileira de Entomologia54(2):258-262.), com somente dois trabalhos realizados no nordeste de MS (Aoki & Sigrist, 2006Aoki, C. & Sigrist, M. R. 2006. Inventário dos visitantes florais no Complexo Aporé-Sucuriú. In: Pagoto, T. C. S. & de Souza, P. R. orgs. Biodiversidade do Complexo Aporé-Sucuriú. Subsídios à conservação e ao manejo do Cerrado. Campo Grande, Editora da Universidade Federal de Mato Grosso do Sul, p.143-162.; Vieira et al., 2008Vieira, G. H. C.; Marchini, L. C.; Souza, B. A. & Moreti, A. C. C. C. 2008. Fontes florais usadas por abelhas (Hymenoptera, Apoidea) em área de Cerrado no município de Cassilândia, Mato Grosso do Sul, Brasil. Ciência e Agrotecnologia 32:1454-1460.) (Fig. 1). No Pantanal, há estudos na planície (Longo & Fischer, 2006Longo, J. M. & Fischer, E. 2006. Efeito da taxa de secreção de néctar sobre a polinização e a produção de sementes em flores de Passiflora speciosa Gardn. (Passifloraceae) no Pantanal. Revista Brasileira de Botânica29:481-488.; Boff, 2008Boff, S. 2008. Flora de capões e Hymenoptera (abelhas e vespas) visitantes de flores no pantanal do Miranda-Abobral. Dissertação de Mestrado. Campo Grande, Universidade Federal de Mato Grosso do Sul. ; Fava et al., 2011Fava, W. S.; Sigrist, M. R. & Covre, W. S. 2011. Attalea phalerata and Bactris glaucescens (Arecaceae, Arecoideae): Phenology and pollination ecology in the Pantanal, Brazil. Flora 206:575-584.), incluindo um em formação chaquenha (Souza, 2012Souza, C. S. 2012. Fauna antófila diurna em formação chaquenha brasileira: composição e flora visitada. Monografia de conclusão de curso. Campo Grande, Universidade Federal de Mato Grosso do Sul.) e, mais raramente, no Planalto (Aoki et al., 2012Aoki, C.; Teixeira-Gamarra, M. C.; Barônio, G. J.; Sigrist, M. R. & Laroca, S. 2012. Diversidade de abelhas (Hymenoptera: Apoidea) e recursos florais na RPPN Engenheiro Eliezer Batista, Pantanal de Mato Grosso do Sul. In: Rabelo, A. C. P.; Moreira, V. F.; Bertassoni, A. & Aoki, C. orgs. Descobrindo o Paraíso. Aspectos Biológicos da Reserva Particular do Patrimônio Natural Engenheiro Eliezer Batista. Rio de Janeiro, Instituto Homem Pantaneiro, p.82-111.; Auko et al., 2012Auko, T. H.; Trad, B. M.; Silvestre, R. & Aoki, C.2012. Vespas Aculeata da Reserva Particular do Patrimônio Natural Engenheiro Eliezer Batista In: Rabelo, A. C. P.; Moreira, V. F.; Bertassoni, A.& Aoki, C.orgs. Descobrindo o Paraíso. Aspectos Biológicos da Reserva Particular do Patrimônio Natural Engenheiro Eliezer Batista. Rio de Janeiro, Instituto Homem Pantaneiro, p.240-261).
Mapa com a distribuição dos estudos sobre visitantes florais no estado do Mato Grosso do Sul (1, Consolaro, 2002; 2, Rodrigues, 2002; 3, Oda, 2003; 4. Aoki & Sigrist, 2006; 5. Oliveira et al., 2007; 6, Oliveira & Sigrist, 2008; 7, Munin et al., 2008; 8, Vieira et al., 2008; 9. Maier, 2009; 10, Vilas Boas, 2009; 11, Ferreira et al., 2010; 12. Longo & Fischer, 2006; 13, Boff, 2008; 14, Fava et al., 2011; 15, Aoki et al., 2012; 16, Auko et al., 2012; 17, Souza, 2012).
A compilação de dados revelou a ocorrência de dez grupos de insetos visitantes de flores, pertencentes a seis ordens, 80 famílias e que totalizaram 411 espécies (Tab. I). Contudo, ao menos mais 262 espécies ocorrem no estado (Fig. 2), mas permaneceram indeterminadas por conta de dificuldades taxonômicas, o que elevaria a riqueza para 673 espécies. Vespas e moscas estão entre os taxa com maior déficit na identificação. Maior riqueza foi amostrada para o Cerrado (307 spp.) que Pantanal (147 spp.), o que é razoável considerando o maior esforço amostral neste bioma, sendo registradas somente 43 espécies (10,4%) em comum entre os dois biomas.
Número mínimo de espécies não identificadas que constam em levantamentos realizados no Cerrado e Pantanal, Mato Grosso do Sul, Brasil.
Abelhas foi o grupo mais rico (155 spp.), seguido por besouros (82), borboletas/mariposas (53) e vespas (45), que junto totalizaram 81,5% das espécies (Fig. 3). Maior riqueza de abelhas está relacionada ao fato da maioria dos trabalhos enfocar este grupo, além da especialização deste grupo na utilização de recursos florais. Abelhas possuem cuidado parental e o néctar como principal fonte de carboidratos e o pólen de proteína para a nutrição da prole e adultos (Faegri & van der Pijl, 1979Faegri, K. & van der Pijl, L. 1979. The principles of pollination ecology. London, Pergamon Press. 242p.; Barbola et al., 2000Barbola, I. F.; Laroca, S.& Alemida, M. C. 2000. Utilização de recursos florais por abelhas silvestres (Hymenoptera, Apoidea) da Floresta Estadual do Passa Dois (Lapa, Paraná, Brasil). Revista Brasileira de Entomologia 44:9-19.). Surpreendente foi a segunda posição ocupada por besouros em relação a outros visitantes mais “ativos”, como lepidópteros e moscas.
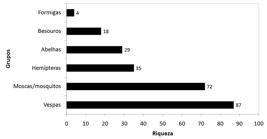
Riqueza de insetos amostrados em flores em estudos realizados em vegetação de Cerrado e Pantanal, Mato Grosso do Sul, Brasil.
Dentre os visitantes categorizados como “polinizadores não habituais”, destacaram-se hemípteros e formigas. Muitas espécies de percevejos são visitantes comuns e conspícuos, atraídos principalmente por néctar e tecidos florais, chegando muitas vezes a danificar o ovário (Faegri & van der Pijl, 1979Faegri, K. & van der Pijl, L. 1979. The principles of pollination ecology. London, Pergamon Press. 242p.). Por outro lado, formigas são comumente observadas em flores com néctar acessível e, raramente, são mencionadas sequer como visitantes florais, pois há o pressuposto que são polinizadores ineficientes ou, mais comumente, ladrões de néctar: são pequenas, desprovidas de asas, possuem corpo liso, que limpam frequentemente; bem como liberam secreções antibióticas que supostamente reduzem a viabilidade do pólen. Entretanto, formigas podem ser importantes polinizadores de espécies que crescem junto ao solo, em ambientes áridos ou desérticos ou em altitudes elevadas (Corlett, 2004Corlett, R. T. 2004. Flower visitors and pollination in the Oriental (Indomalayan) Region. Biological Reviews 79:497-532.).
Abelhas (Hymenoptera, Apoidea, Anthophila). As 155 espécies registradas pertencem a 68 gêneros e cinco famílias (Michener, 2000Michener, C. D. 2000. The bees of the world. Baltimore, Maryland, Johns Hopkins University Press. 992p.), sendo Apidae a mais rica (109 espécies), seguida por Halictidae (25), Megachilidae (14), Colletidae (4) e Andrenidae (3). A riqueza de abelhas amostrada até o momento em MS é pequena se comparada à estimada, por exemplo, para o estado de São Paulo (SP) (729 spp.) (Pedro & Camargo, 1999Pedro, S. R. M. & Camargo, J. M. F. 1999. Apoidea, Apiformes. In: Joly, C. A.; Bicudo, C. E. M.; Brandão, C. R. F. & Cancello, E. M. eds. Biodiversidade do Estado de São Paulo, Brasil. Síntese do conhecimento ao final do século XX. Invertebrados Terrestres. São Paulo, FAPESP. vol. 5, p.193-211.), onde são realizados levantamentos a mais de quatro décadas e onde ocorrem diversos grupos de pesquisas e acervos. Entretanto, trabalhos com coletas em sete localidades distintas no estado de SP (três na Mata Atlântica e quatro no cerrado), registraram total de 276 espécies e 88 gêneros, com Apidae como família mais representativa, mas com 105 espécies registradas em Cerrado, valor ligeiramente menor que neste estudo (126 spp.).
Centris (13 spp.), Augochloropsis, Trigona (9 spp. cada) e Epicharis (7 spp.) foram os gêneros mais representativos (Tab. I) e estão entre os oito gêneros mais ricos das savanas tropicais (exceto Trigona) (Pinheiro-Machado et al., 2002Pinheiro-Machado, C.; Santos, I. A.; Imperatriz-Fonseca, V. L.; Kleinert, A. M. P. & Silveira, F. A. 2002. Brazilian bee surveys: State of knowledge, conservation and sustainable use. In: Kevan, P. & Imperatriz Fonseca, V. L. eds. Pollinating bees. The conservation link between agriculture and nature., Brasília, Ministério do Meio Ambiente p. 115-129.). Apis melífera, exótica, foi a mais comum nos levantamentos, seguida pelas nativas Tetragonisca
angustula, Trigona spinipes, Paratrigona
lineata e Centris
varia. Exceto C. varia, as demais espécies são consideradas generalistas, pois geralmente visitam amplo espectro de plantas (Imperatriz-Fonseca et al., 2011Imperatriz-Fonseca, V. L.; Alves-dos-Santos, I.; Santos-Filho, P. S.; Engels, W.; Ramalho, M.; Wilms, W.; Aguilar, J. B. V.; Pinheiro-Machado, C. A.; Alves, D. A. & Kleinert, A. M. P. 2011. Checklist of bees and honey plants from São Paulo State, Brazil. Biota Neotropica 11(1a). Disponível em: <http://www.biotaneotropica.org.br/v11n1a/pt/abstract?article+bn0321101a2011>.
http://www.biotaneotropica.org.br/v11n1a...
).
Besouros (Coleoptera). Os 82 táxons de besouros com alguma identificação registrados para Mato Grosso do Sul estão relatados em apenas quatro estudos (Aoki & Sigrist, 2006Aoki, C. & Sigrist, M. R. 2006. Inventário dos visitantes florais no Complexo Aporé-Sucuriú. In: Pagoto, T. C. S. & de Souza, P. R. orgs. Biodiversidade do Complexo Aporé-Sucuriú. Subsídios à conservação e ao manejo do Cerrado. Campo Grande, Editora da Universidade Federal de Mato Grosso do Sul, p.143-162.; Munin et al., 2008Munin, R. L.; Teixeira, R. C. & Sigrist, M. R.2008. Esfingofilia e sistema de reprodução de Bauhinia curvula Benth. (Leguminosae: Caesalpinioideae) em cerrado no Centro-Oeste brasileiro. Revista Brasileira de Botânica31:15-25.; Fava et al., 2011Fava, W. S.; Sigrist, M. R. & Covre, W. S. 2011. Attalea phalerata and Bactris glaucescens (Arecaceae, Arecoideae): Phenology and pollination ecology in the Pantanal, Brazil. Flora 206:575-584.; Souza, 2012Souza, C. S. 2012. Fauna antófila diurna em formação chaquenha brasileira: composição e flora visitada. Monografia de conclusão de curso. Campo Grande, Universidade Federal de Mato Grosso do Sul.). Esta elevada riqueza de coleópteros mostra que flores são importantes sítios de coleta deste grupo de insetos. Dentre as 18 famílias registradas, Chrysomelidae foi a mais rica (20 espécies), seguida de Curculionidae (18) e Scarabaeidae (10). Representantes dessas famílias são comumente mencionadas como visitantes florais e/ou polinizadores de diversas famílias de Angiospermas (Gottsberger, 1999Gottsberger, G. 1999. Pollination and evolution in neotropical Annonaceae. Plant Species Biology 14:143-152.; Corlett, 2004Corlett, R. T. 2004. Flower visitors and pollination in the Oriental (Indomalayan) Region. Biological Reviews 79:497-532.; Lenzi et al., 2005Lenzi, M.; Orth, A. I. & Guerra, T. M. 2005. Ecologia da polinização de Momordica charantia L. (Cucurbitaceae), em Florianópolis, SC, Brasil. Revista Brasileira de Botânica 28:505-513.; Costa & Morais, 2008Costa, R. A. C. V. & Morais, A. B. B. 2008. Fenologia e visitantes florais de Erythrina crista-galli (Leguminosae: Faboideae) em Santa Maria, Rio Grande do Sul, Brasil. Biotemas 21(2):51-56.).
Borboletas/mariposas (Lepidoptera). As 53 espécies de lepidópteros registradas estão distribuídas em sete famílias, com destaque para Nymphalidae (16 espécies), Hesperiidae (16) e Lycaenidae (10), famílias com representantes de hábito diurno, período em que se concentrou a quase totalidade dos estudos realizados. No estado a amostragem de mariposas em flores praticamente inexiste, com duas espécies registradas em Bauhinia curvula por Munin et al. (2008Munin, R. L.; Teixeira, R. C. & Sigrist, M. R.2008. Esfingofilia e sistema de reprodução de Bauhinia curvula Benth. (Leguminosae: Caesalpinioideae) em cerrado no Centro-Oeste brasileiro. Revista Brasileira de Botânica31:15-25.).
Formigas (Hymenoptera, Formicidae). Somente dois estudos contribuíram para o conhecimento da fauna de formigas em flores (Aoki & Sigrist, 2006Aoki, C. & Sigrist, M. R. 2006. Inventário dos visitantes florais no Complexo Aporé-Sucuriú. In: Pagoto, T. C. S. & de Souza, P. R. orgs. Biodiversidade do Complexo Aporé-Sucuriú. Subsídios à conservação e ao manejo do Cerrado. Campo Grande, Editora da Universidade Federal de Mato Grosso do Sul, p.143-162.; Souza, 2012Souza, C. S. 2012. Fauna antófila diurna em formação chaquenha brasileira: composição e flora visitada. Monografia de conclusão de curso. Campo Grande, Universidade Federal de Mato Grosso do Sul.), resultando em listagem de 23 espécies distribuídas em seis subfamílias, com destaque para Myrmicinae (7 espécies), Formicinae (6) e Dolichoderinae (4). Apesar de ocuparem todos os extratos de um ambiente, muitos grupos de formigas mantêm relações estreitas com plantas, obtendo recursos como pólen e néctar floral e extrafloral e, na maioria das vezes, protegendo a planta hospedeira de outros herbívoros (Oliveira et al., 1987Oliveira, P. S.; Silva, A. F. & Martins, A. B.1987. Ant foraging on extrafloral nectaries of Qualea grandiflora (Vochysiacea) in Cerrado vegetation: ants a potential antiherbivore agent. Oecologia 74:228-230.).
Hemípteros (Hemiptera). Doze famílias foram listadas, e até o momento somente quatro, das 15 espécies registradas, foram identificadas. Representantes de Hemiptera são frequentemente amostrados em estudos que registram toda a fauna antófila, e geralmente visitam flores para comer partes florais, sendo o néctar de interesse secundário ou nulo (Faegri & van der Pijl, 1979Faegri, K. & van der Pijl, L. 1979. The principles of pollination ecology. London, Pergamon Press. 242p.).
Moscas/mosquitos (Diptera). Dentre as 34 espécies identificadas em algum nível taxonômico, foram registradas vinte famílias de moscas e mosquitos em visitas às flores, com destaque para Bombyliidae e Tachinidae em riqueza (5 spp. cada). No mundo, segundo Larson et al. (2001Larson, B. M. H.; Kevan, P. G. & Inouye, D. W. 2001. Flies and flowers: The taxonomic diversity of anthophiles and pollinators. The Canadian Entomologist 133(4):439-465.), Diptera corresponde à segunda ordem mais importante de insetos visitantes de flores, com pelo menos 71 famílias com representante antófilo.
Vespas (Hymenoptera, Apoidea, Aculeata). Treze famílias de vespas foram registradas em estudos de visitantes florais no estado, sendo que Vespidae foi majoritariamente a mais rica (26 spp.). Vespas são visitantes comuns em flores, embora algumas espécies sejam atraídas pela oportunidade de predar outros visitantes (Faegri & van der Pijl, 1979Faegri, K. & van der Pijl, L. 1979. The principles of pollination ecology. London, Pergamon Press. 242p.; Corlett, 2004Corlett, R. T. 2004. Flower visitors and pollination in the Oriental (Indomalayan) Region. Biological Reviews 79:497-532.).
Ordens diversas. Foram incluídos neste grupo representantes de Orthoptera (Acrididae) (grilos), Mantodea (louva-a-Deus) e Blattodae (Blattelidae e Blattidae) (baratas), que comumente são registrados em flores consumindo partes florais ou buscando alguma presa (Mantodea) e não atuando como polinizadores, com exceções (Nagamitsu & Inoue, 1997Nagamitsu, T. & Inoue, T. 1997. Cockroach pollination and breeding system of Uvaria elmeri (Annonaceae) in a lowland mixed-Dipterocarp forest in Sarawak. American Journal of Botany 84:208-213. ; Corlett, 2004Corlett, R. T. 2004. Flower visitors and pollination in the Oriental (Indomalayan) Region. Biological Reviews 79:497-532.; Vlasáková et al., 2008Vlasáková, B.; Kalinová, B.; Gustafsson, M. H. G. & Teichert, H. 2008. Cockroaches as pollinators of Clusia aff. sellowiana (Clusiaceae) on inselbergs in French Guiana. Annals of Botany102:295-304.; Micheneau et al., 2010Micheneau, C.; Fournel, J.; Warren, B. H.; Hugel, S.; Gauvin-Bialecki, A.; Pailler, T.; Strasberg, D. & Chase, M. W. 2010. Orthoptera, a new order of pollinator. Annals of Botany 105:1-10.).
Principais acervos e grupos de pesquisa. No MS há somente duas instituições que abrigam espécimes de insetos que visitam flores: a Universidade Federal de Mato Grosso do Sul (UFMS) com a Coleção Zoológica de Referência da UFMS (ZUFMS) e a Universidade Federal da Grande Dourados (UFGD), com o Museu de Biodiversidade da Faculdade de Ciências Biológicas e Ambientais (Mubio/UFGD). Temos apenas dois os grupos de pesquisas, ambos na UFMS, que trabalham direta ou indiretamente com insetos de visitantes de flores: (i) no campus Campo Grande, na linha de pesquisa “Conservação de Polinizadores” coordenado por Maria Rosângela Sigrist, (ii) no campus de Corumbá no grupo “Pesquisa em abelhas: biologia, diversidade e genética” coordenado por Aline Mackert dos Santos.
Principais dificuldades, lacunas de conhecimento e perspectivas para os próximos 10 anos. Para a maioria dos grupos amostrados (exceto abelhas, geralmente amostradas em flores) comparações foram limitadas por falta de dados e/ou estudos equivalentes no Brasil como um todo e não somente em MS. Dados sobre visitantes florais noturnos (e.g. besouros, mariposas, moscas) praticamente inexistem para o estado. Intercâmbio ou parceria entre profissionais que trabalham com levantamento de insetos em flores e taxonomistas destes grupos é incipiente, haja vista o elevado número de espécies na categoria de “indeterminado”. Este fato é agravado pela falta de taxonomistas para boa parte dos grupos amostrados, necessidade de revisões taxonômicas e de boas coleções de referência no estado.
A dificuldade de identificação de material biológico é uma limitação tanto com relação à determinação da riqueza de espécies em determinado bioma, estado ou país, como para a comparação e utilização dos dados de interações relatadas nos trabalhos. No Brasil, para quase todos os grupos de insetos há escassez de especialistas para a identificação das espécies, portanto, são necessários incentivos ou ações que promovam a formação de taxonomistas e a integração entre os taxonomistas existentes e os centros de pesquisa de regiões com carência deste tipo de profissional, principalmente nas regiões Centro-Oeste e Norte.
Perspectivas e necessidades. Fomento das coleções a partir de novos levantamentos, mas com o fortalecimento dos acervos e grupos de pesquisa através de parcerias entre pesquisadores do estado e do Brasil, bem como formação de recursos humanos nestas áreas. Pesquisas com enfoque nas redes de interação, no papel dos visitantes florais na polinização das espécies vegetais, estudos sobre o efeito da sazonalidade na diversidade de visitantes florais principalmente no Pantanal em que esta é muito marcada, estudo dos efeitos da inclusão de espécies exóticas (como Apis mellifera) sobre as nativas de polinizadores são necessários.
Agradecimentos.
CNPq, FUNDECT, Capes e Fundação Universidade Federal de Mato Grosso do Sul pelo apoio às nossas pesquisas; aos Drs. Ayr de Moura Bello, André V. L. Freitas, Carlos José Einicker Lamas, Gustavo Graciolli, Helcio Gil Santana e Rogério Silvestre, ao MSc. Manoel Fernando Demétrio e ao biólogo Daniel Máximo Corrêa de Alcântara pelo auxílio na identificação e/ou valiosos comentários sobre besouros, borboletas, hemípteros e moscas; Arnildo Pott revisou o abstract.
REFERÊNCIAS BIBLIOGRÁFICAS
- Aoki, C. & Sigrist, M. R. 2006. Inventário dos visitantes florais no Complexo Aporé-Sucuriú. In: Pagoto, T. C. S. & de Souza, P. R. orgs. Biodiversidade do Complexo Aporé-Sucuriú. Subsídios à conservação e ao manejo do Cerrado. Campo Grande, Editora da Universidade Federal de Mato Grosso do Sul, p.143-162.
- Aoki, C.; Teixeira-Gamarra, M. C.; Barônio, G. J.; Sigrist, M. R. & Laroca, S. 2012. Diversidade de abelhas (Hymenoptera: Apoidea) e recursos florais na RPPN Engenheiro Eliezer Batista, Pantanal de Mato Grosso do Sul. In: Rabelo, A. C. P.; Moreira, V. F.; Bertassoni, A. & Aoki, C. orgs. Descobrindo o Paraíso. Aspectos Biológicos da Reserva Particular do Patrimônio Natural Engenheiro Eliezer Batista. Rio de Janeiro, Instituto Homem Pantaneiro, p.82-111.
- Auko, T. H.; Trad, B. M.; Silvestre, R. & Aoki, C.2012. Vespas Aculeata da Reserva Particular do Patrimônio Natural Engenheiro Eliezer Batista In: Rabelo, A. C. P.; Moreira, V. F.; Bertassoni, A.& Aoki, C.orgs. Descobrindo o Paraíso. Aspectos Biológicos da Reserva Particular do Patrimônio Natural Engenheiro Eliezer Batista. Rio de Janeiro, Instituto Homem Pantaneiro, p.240-261
- Barbola, I. F.; Laroca, S.& Alemida, M. C. 2000. Utilização de recursos florais por abelhas silvestres (Hymenoptera, Apoidea) da Floresta Estadual do Passa Dois (Lapa, Paraná, Brasil). Revista Brasileira de Entomologia 44:9-19.
- Boff, S. 2008. Flora de capões e Hymenoptera (abelhas e vespas) visitantes de flores no pantanal do Miranda-Abobral. Dissertação de Mestrado. Campo Grande, Universidade Federal de Mato Grosso do Sul.
- Consolaro, H. N. 2002. Levantamento das abelhas (Hymenoptera, Apoidea) do campus da Universidade Federal de Mato Grosso do Sul, Campo Grande, MS. Monografia de conclusão de curso. Campo Grande, Universidade Federal de Mato Grosso do Sul.
- Corlett, R. T. 2004. Flower visitors and pollination in the Oriental (Indomalayan) Region. Biological Reviews 79:497-532.
- Costa, R. A. C. V. & Morais, A. B. B. 2008. Fenologia e visitantes florais de Erythrina crista-galli (Leguminosae: Faboideae) em Santa Maria, Rio Grande do Sul, Brasil. Biotemas 21(2):51-56.
- Dufaÿ, M. & Anstett, M. C. 2003. Conflicts between plants and pollinators that reproduce within inflorescences: evolutionary variations on a theme. Oikos 100:3-14.
- Faegri, K. & van der Pijl, L. 1979. The principles of pollination ecology. London, Pergamon Press. 242p.
- Fava, W. S.; Sigrist, M. R. & Covre, W. S. 2011. Attalea phalerata and Bactris glaucescens (Arecaceae, Arecoideae): Phenology and pollination ecology in the Pantanal, Brazil. Flora 206:575-584.
- Ferreira, M. G.; Manente-Balestieri, F. C. D. & Balestieri, J. B. P. 2010. Pólen coletado por Scaptotrigona depilis (Moure) (Hymenoptera, Meliponini), na região de Dourados, Mato Grosso do Sul, Brasil. Revista Brasileira de Entomologia54(2):258-262.
- Gottsberger, G. 1999. Pollination and evolution in neotropical Annonaceae. Plant Species Biology 14:143-152.
- IBGE. 2004. Instituto Brasileiro de Geografia e Estatística. Disponível em: <Disponível em: www.ibge.gov.br >. Acessado em 08/08/2012.
» www.ibge.gov.br - Imperatriz-Fonseca, V.; Saraiva, A. M. & Gonçalves, L. 2007. A iniciativa brasileira de polinizadores e os avanços para a compreensão do papel dos polinizadores como produtores de serviços ambientais. Bioscience Journal 23:100-106.
- Imperatriz-Fonseca, V. L.; Alves-dos-Santos, I.; Santos-Filho, P. S.; Engels, W.; Ramalho, M.; Wilms, W.; Aguilar, J. B. V.; Pinheiro-Machado, C. A.; Alves, D. A. & Kleinert, A. M. P. 2011. Checklist of bees and honey plants from São Paulo State, Brazil. Biota Neotropica 11(1a). Disponível em: <http://www.biotaneotropica.org.br/v11n1a/pt/abstract?article+bn0321101a2011>.
» http://www.biotaneotropica.org.br/v11n1a/pt/abstract?article+bn0321101a2011 - Laroca, S. & Orth, A. I. 2002 Melissocoenology: historical perspective, method of sampling, and recommendations to the “Program of conservation and sustainable use of pollinators, with emphasis on bees” (ONU). In: Kevan, P. & Imperatriz Fonseca, V. L. eds. Pollinating bees. The conservation link between agriculture and nature. Brasília, Ministério do Meio Ambiente, p.217-225.
- Larson, B. M. H.; Kevan, P. G. & Inouye, D. W. 2001. Flies and flowers: The taxonomic diversity of anthophiles and pollinators. The Canadian Entomologist 133(4):439-465.
- Lenzi, M.; Orth, A. I. & Guerra, T. M. 2005. Ecologia da polinização de Momordica charantia L. (Cucurbitaceae), em Florianópolis, SC, Brasil. Revista Brasileira de Botânica 28:505-513.
- Longo, J. M. & Fischer, E. 2006. Efeito da taxa de secreção de néctar sobre a polinização e a produção de sementes em flores de Passiflora speciosa Gardn. (Passifloraceae) no Pantanal. Revista Brasileira de Botânica29:481-488.
- Maier, J. E. 2009. Levantamento de abelhas e atuação na polinização de espécies vegetais em remanescente urbano de cerrado, Campo Grande, Mato Grosso do Sul. Monografia de conclusão de curso. Campo Grande, Universidade Federal de Mato Grosso do Sul.
- Micheneau, C.; Fournel, J.; Warren, B. H.; Hugel, S.; Gauvin-Bialecki, A.; Pailler, T.; Strasberg, D. & Chase, M. W. 2010. Orthoptera, a new order of pollinator. Annals of Botany 105:1-10.
- Michener, C. D. 2000. The bees of the world. Baltimore, Maryland, Johns Hopkins University Press. 992p.
- MMA - Ministério do Meio Ambiente. 2006. Disponível em: <Disponível em: http://www.mma.gov.br/estruturas/chm/_arquivos/lista_polinizadores.pdf > . Acessado em: 08/08/2012.
» http://www.mma.gov.br/estruturas/chm/_arquivos/lista_polinizadores.pdf - Munin, R. L.; Teixeira, R. C. & Sigrist, M. R.2008. Esfingofilia e sistema de reprodução de Bauhinia curvula Benth. (Leguminosae: Caesalpinioideae) em cerrado no Centro-Oeste brasileiro. Revista Brasileira de Botânica31:15-25.
- Nagamitsu, T. & Inoue, T. 1997. Cockroach pollination and breeding system of Uvaria elmeri (Annonaceae) in a lowland mixed-Dipterocarp forest in Sarawak. American Journal of Botany 84:208-213.
- Nyhagen, D. F.; Kragelund, C.; Olesen, J. M. & Jones, C. G. 2001. Insular interactions between lizards and flowers: flower visitation by an endemic Mauritian gecko. Journal of Tropical Ecology 17:755-761.
- Oda, F. H. 2003. Levantamento e o papel das abelhas nas flores de espécies vegetais em remanescente de cerrado em Campo Grande, MS. Monografia de conclusão de curso. Campo Grande, Universidade Federal de Mato Grosso do Sul.
- Oliveira, M. B. & Sigrist, M. R.2008. Fenologia reprodutiva, polinização e reprodução de Dipteryx alata Vogel (Leguminosae - Papilionoideae) em Mato Grosso do Sul, Brasil. Revista Brasileira de Botânica31:195-207.
- Oliveira, M. I. B.; Polido, C. A.; Costa, L. C. & Fava, W. S. 2007. Sistema reprodutivo e polinização de Byrsonima intermedia A. Juss. (Malpighiaceae) em Mato Grosso do Sul, Brasil. Revista Brasileira de Biociências 5:756-758.
- Oliveira, P. S.; Silva, A. F. & Martins, A. B.1987. Ant foraging on extrafloral nectaries of Qualea grandiflora (Vochysiacea) in Cerrado vegetation: ants a potential antiherbivore agent. Oecologia 74:228-230.
- Pedro, S. R. M. & Camargo, J. M. F. 1999. Apoidea, Apiformes. In: Joly, C. A.; Bicudo, C. E. M.; Brandão, C. R. F. & Cancello, E. M. eds. Biodiversidade do Estado de São Paulo, Brasil. Síntese do conhecimento ao final do século XX. Invertebrados Terrestres. São Paulo, FAPESP. vol. 5, p.193-211.
- Pinheiro-Machado, C.; Santos, I. A.; Imperatriz-Fonseca, V. L.; Kleinert, A. M. P. & Silveira, F. A. 2002. Brazilian bee surveys: State of knowledge, conservation and sustainable use. In: Kevan, P. & Imperatriz Fonseca, V. L. eds. Pollinating bees. The conservation link between agriculture and nature., Brasília, Ministério do Meio Ambiente p. 115-129.
- Proctor, M.; Yeo, P. & Lack, A. 1996. The natural history of pollination. Portland, Timber Press. 487p.
- Rodrigues, L. C. 2002. Biologia da polinização de duas espécies de Bromelia (Bromeliaceae) em cerrado de Mato Grosso do Sul. Monografia de conclusão de curso. Campo Grande, Universidade Federal de Mato Grosso do Sul.
- Sazima, M.; Vogel, S.; Prado, A. L.; Oliveira, D. M.; Franz, G. & Sazima, I. 2001. The sweet jelly of Combretum lanceolatum flowers (Combretaceae): a cornucopia resource for bird pollinators in the Pantanal, western Brazil. Plant Systematics and Evolution 227:195-208.
- Souza, C. S. 2012. Fauna antófila diurna em formação chaquenha brasileira: composição e flora visitada. Monografia de conclusão de curso. Campo Grande, Universidade Federal de Mato Grosso do Sul.
- Simpson, B. B. & Neff, J. L. 1981. Floral rewards: alternatives to pollen and nectar. Annals of the Missouri Botanical Garden 68:301-322.
- Stehlmann, J. R. & Semir, J. 2001. Biologia reprodutiva de Calibrachoa elegans (Miers) (Solanaceae). Revista Brasileira de Botânica24:43-49.
- Vieira, G. H. C.; Marchini, L. C.; Souza, B. A. & Moreti, A. C. C. C. 2008. Fontes florais usadas por abelhas (Hymenoptera, Apoidea) em área de Cerrado no município de Cassilândia, Mato Grosso do Sul, Brasil. Ciência e Agrotecnologia 32:1454-1460.
- Vilas Boas, J. C. 2009. Fenologia e biologia reprodutiva de Byrsonima intermedia A. Juss. e B. pachyphylla Griseb (Malpighiaceae) em remanescente de cerrado, Mato Grosso do Sul, Brasil. Dissertação de Mestrado. Campo Grande, Universidade Federal de Mato Grosso do Sul.
- Vlasáková, B.; Kalinová, B.; Gustafsson, M. H. G. & Teichert, H. 2008. Cockroaches as pollinators of Clusia aff. sellowiana (Clusiaceae) on inselbergs in French Guiana. Annals of Botany102:295-304.
Datas de Publicação
-
Publicação nesta coleção
2017
Histórico
-
Recebido
25 Nov 2016 -
Aceito
06 Fev 2017