Resumos
O principal objetivo deste estudo é identificar, na literatura, artigos sobre a ocorrência de contaminação das superfícies inanimadas e uma possível disseminação de bactérias resistentes no ambiente hospitalar. Realizou-se um levantamento bibliográfico de artigos publicados nas bases de dados LILACS, MEDLINE, Science Direct, SCOPUS e ISI Web of Knowledge, entre 2000 e 2008. Foram selecionados e analisados vinte e um artigos. Nos estudos analisados, realçou-se a presença de bactérias em monitores, grades de cama, mesas, torneiras, telefones, teclados de computador e outros objetos. Houve predominância de Staphylococcus aureus resistente à meticilina, Clostridium difficile, Acine-to-bacter baumannii e Enterococcus resistentes à vancomicina, sendo fator preditivo a ocupação prévia por pacientes colonizados por tais microrganismos. Verificou-se semelhança entre as cepas isoladas de pacientes colonizados e/ou infectados e as cepas do ambiente por tipificação molecular. Essas evidências reforçam a necessidade de conhecimento e controle de fontes de patógenos no ambiente hospitalar.
Infecção hospitalar; Contaminação; Farmacorresistência bacteriana
Se objetivó identificar en la literatura artículos sobre la ocurrencia de contaminación de superficies inanimadas y la posible diseminación de bacterias resistentes en el ambiente hospitalario. Se realizó una investigación bibliográfica en las bases de datos LLILACS, MEDLINE, Science Direct, SCOPUS e ISI Web of Knowledge acerca de artículos publicados entre 2000 y 2008. Fueron seleccionados veintiún artículos. En los estudios analizados, se puso de manifiesto la presencia de bacterias en monitores, barandas de camas, mesas, canillas, teléfonos, teclados de computadora y otras. Existió predominancia de Staphylococcus aureus resistente a la meticilina, Clostridium difficile, Acinetobacter baumannii y Enterococcus resistentes a la vancomicina, resultando como factor predictivo el uso previo por parte de pacientes colonizados por tales microorganismos. Se verificó semejanza en las cepas aisladas de pacientes colonizados y/o infectados y del ambiente por tipificación molecular. Esas evidencias refuerzan la necesidad de conocimiento y control de fuentes de patógenos en el ambiente hospitalario.
Infección hospitalaria; Contaminación; Farmacorresistencia bacteriana
The main objective of this study is to identify, in the literature, articles about the occurrence of contamination from inanimate surfaces and a possible dissemination of resistant bacteria in the hospital environment. A bibliographic survey was performed with articles published in the databases LILACS, MEDLINE, Science Direct, SCOPUS and ISI Web of Knowledge, between 2000 and 2008. Twenty-one articles were selected and analyzed. The analyzed studies highlighted the presence of bacteria on monitors, bed grids, tables, faucets, telephones, keyboards and other objects. There was a prevalence of Staphylococcus aureus resistant to methicillin, Clostridium difficile, Acinetobacter baumannii and Enterococcus resistant to vancomycin, being the predictive factor the previous occupation of patients colonized by these microorganisms. There was a similarity observed among the isolated strains of colonized and/or infected patients and the strains of the environment by molecular typification. These evidences reinforce the need for knowledge and control of the sources of pathogens in the hospital environment.
Cross infection; Contamination; Drug resistance, bacterial
ARTIGO DE REVISÃO
Superfícies do ambiente hospitalar como possíveis reservatórios de bactérias resistentes: uma revisão
Superficies inanimadas del ambiente hospitalario como posibles reservorios de bacterias resistentes: una revisión
Adriana Cristina de OliveiraI; Quésia Souza DamascenoII
IEnfermeira. Mestre. Doutora. Professora da Escola de Enfermagem da Universidade Federal de Minas Gerais. Belo Horizonte, MG, Brasil. acoliveira@ufmg.br
IIEnfermeira. Mestranda em Enfermagem pelo Programa de Pós-graduação da Escola de Enfermagem da Universidade Federal de Minas Gerais. Belo Horizonte, MG, Brasil. qdamasceno@yahoo.com.br
Correspondência Correspondência: Quésia Souza Damasceno Rua Paraíba, 100 - Morro das Bicas CEP 34400-000 - Raposos, MG, Brasil
RESUMO
O principal objetivo deste estudo é identificar, na literatura, artigos sobre a ocorrência de contaminação das superfícies inanimadas e uma possível disseminação de bactérias resistentes no ambiente hospitalar. Realizou-se um levantamento bibliográfico de artigos publicados nas bases de dados LILACS, MEDLINE, Science Direct, SCOPUS e ISI Web of Knowledge, entre 2000 e 2008. Foram selecionados e analisados vinte e um artigos. Nos estudos analisados, realçou-se a presença de bactérias em monitores, grades de cama, mesas, torneiras, telefones, teclados de computador e outros objetos. Houve predominância de Staphylococcus aureus resistente à meticilina, Clostridium difficile, Acine-to-bacter baumannii e Enterococcus resistentes à vancomicina, sendo fator preditivo a ocupação prévia por pacientes colonizados por tais microrganismos. Verificou-se semelhança entre as cepas isoladas de pacientes colonizados e/ou infectados e as cepas do ambiente por tipificação molecular. Essas evidências reforçam a necessidade de conhecimento e controle de fontes de patógenos no ambiente hospitalar.
Descritores: Infecção hospitalar. Contaminação. Farmacorresistência bacteriana
RESUMEN
Se objetivó identificar en la literatura artículos sobre la ocurrencia de contaminación de superficies inanimadas y la posible diseminación de bacterias resistentes en el ambiente hospitalario. Se realizó una investigación bibliográfica en las bases de datos LLILACS, MEDLINE, Science Direct, SCOPUS e ISI Web of Knowledge acerca de artículos publicados entre 2000 y 2008. Fueron seleccionados veintiún artículos. En los estudios analizados, se puso de manifiesto la presencia de bacterias en monitores, barandas de camas, mesas, canillas, teléfonos, teclados de computadora y otras. Existió predominancia de Staphylococcus aureus resistente a la meticilina, Clostridium difficile, Acinetobacter baumannii y Enterococcus resistentes a la vancomicina, resultando como factor predictivo el uso previo por parte de pacientes colonizados por tales microorganismos. Se verificó semejanza en las cepas aisladas de pacientes colonizados y/o infectados y del ambiente por tipificación molecular. Esas evidencias refuerzan la necesidad de conocimiento y control de fuentes de patógenos en el ambiente hospitalario.
Descriptores: Infección hospitalaria. Contaminación. Farmacorresistencia bacteriana.
INTRODUÇÃO
A disseminação de infecções relacionadas à assistência à saúde (IRAS) frequentemente advem da contaminação cruzada. A via mais comum de transferência de patógenos ocorre entre as mãos de profissionais de saúde e pacientes(1).
No entanto, o ambiente hospitalar pode contribuir para disseminação de patógenos. Geralmente o ambiente ocupado por pacientes colonizados e/ou infectados pode tornar-se contaminado(1). A presença de bactérias é comum em superfícies inanimadas e equipamentos(2).
Nos EUA identificou-se freqüente contaminação de superfícies por Enterococcus resistentes à vancomicina (VRE) e Staphylococcus aureus resistente à meticilina (MRSA). Embora os microrganismos sobrevivam no ambiente, não está claro o papel das superfícies na disseminação desses(3-4).
O esclarecimento do papel ambiental na aquisição das IRAS se destaca pela necessidade de estratégias mútiplas de controle da disseminação de bactérias resistentes aos antimicrobianos; problema mundial que eleva tempo de internação, custos e morbimortalidade(5). Portanto, torna-se relevante avaliar o papel do ambiente nas infecções para proposição de estratégias que reduzam a contaminação e a disseminação de patógenos(6).
Observa-se que a participação ambiental pode ser maior nas unidades de terapia intensiva (UTI) devido à gravidade e instabilidade do quadro clínico do paciente com necessidade de cuidados intensivos, somados a fatores como limpeza, desinfecção, estrutura física, quantidades de equipamentos e superfícies em determinadas unidades(7).
A disseminação das infecções associadas aos cuidados de saúde é complexa e multifatorial. Neste sentido, a abordagem do ambiente na disseminação de bactérias visa contribuir para melhor compreensão das recomendações de controle das IRAS, definição de políticas de controle e aproximação dos profissionais de saúde com o tema(8).
OBJETIVO
Objetivou-se identificar na literatura artigos sobre a ocorrência de contaminação das superfícies inanimadas e possível disseminação de bactérias resistentes no ambiente hospitalar.
MÉTODO
Realizou-se um levantamento bibliográfico em periódicos de língua inglesa de 2000 a 2008 nas bases de dados: Bibliografia Médica (MEDLINE), Literatura Latino-Americana e do Caribe em Ciências da Saúde (LILACS), Science Direct, SCOPUS (Database of research literature) e plataforma virtual de pesquisa Isi Web of Knowledge. Optou-se por trabalhos neste período por se tratar de um assunto ainda pouco estudado e que vem despertando atenção de pesquisadores. Utilizaram-se os descritores: cross infection, transmission, environment e bacterial drug resistance.
Os critérios de inclusão foram: artigos originais com identificação de contaminação de superfícies relacionados à infecção hospitalar e resistência bacteriana, em unidades de pacientes adultos, com aplicação de testes laboratoriais (bioquímico e/ou molecular) e estatísticos. Foram obtidos 348 artigos; foram excluídos aqueles não relacionados ao tema (327), sendo analisados 21 artigos.
RESULTADOS
Em situações endêmicas e de surto foi verificada a contaminação ambiental e transferência de bactérias entre paciente e ambiente (Quadro 1). Nesses estudos, as espécies bacterianas foram identificadas por testes bioquímicos (coloração de gram, coagulase, oxidase, piruvato e outros). O perfil dos isolados bacterianos foi verificado por teste de susceptibilidade aos antimicrobianos por disco de difusão ou determinação da concentração inibitória mínima (MIC) pelo E-teste(1-21).
A relação clonal dos isolados bacterianos foi frequentemente verificada por meio da eletroforese em campo pulsátil (PFGE); técnica de alto poder discriminatório, ampla aplicação às diversas espécies e que permite a comparação de similaridade entre cepas(17-21).
Nas observações endêmicas houve maior freqüência de MRSA e VRE com risco para aquisição de infecções por pacientes em ambiente contaminado. Nos surtos destacaram-se os gram negativos; P. aeruginosa e A. baumanni resistentes aos carbapenêmicos. A contaminação do ambiente por C. difficile foi observada em situação endêmica e de surto(1-14,16-18,20-21). Apesar do envolvimento ambiental em surtos, em alguns estudos, as culturas do ambiente foram negativas, ou se positivas, não houve similaridade de cepas, com possibilidade de outras fontes de disseminação(22-23).
Superfícies do ambiente hospitalar e espécies bacterianas recuperadas
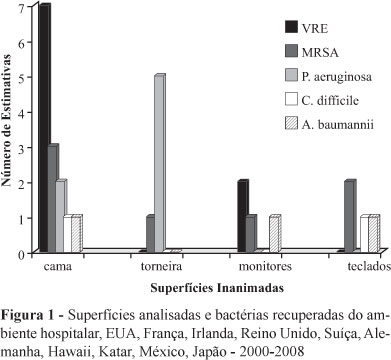
Analisou-se com freqüência: cama, torneira, monitor e computador (Figura1)(3-4,6-14).
Em superfícies da cama fora recuperadas VRE, P. aeruginosa, C.difficile, A. baumannii e MRSA, sendo o último mais freqüente, além de encontrado em maçanetas, cadeiras, assentos sanitários e mesa(1,3,7-11,14-16). Nas torneiras destacou-se P. aeruginosa; comum em locais úmidos(13).
Em um estudo em que o tempo de realização da limpeza foi aumentado em consonância com protocolo institucional, não houve recuperação bacteriana como antes detectada em telefones, torneiras e bomba de infusão(11). Todavia, há relato da persistência de VRE no ambiente devido à provável remoção incompleta do patógeno na limpeza(1). A recontaminação foi constatada após algumas semanas da troca de torneiras contaminadas, em surto por P. aeruginosa, pela possível formação de biofilme(13).
DISCUSSÃO
O ambiente hospitalar destacou-se como potencial reservatório de MRSA, VRE, P. aeruginosa, C. difficile e A. baumannii(1,8,10-13,16-21). A maior freqüência de contaminação nas UTI é coerente com a estrutura física, elevada quantidade de equipamentos e condições dos pacientes em cuidados intensivos, que tendem a apresentar mais fatores de risco e maiores taxas de infecção. Nesse ambiente, o risco de aquisição de MRSA e VRE pode ser reforçado na presença de pacientes colonizados ou se a permanência exceder uma média de 15 dias, conforme destacado pelo guideline sobre o gerenciamento de organismos multirresistentes nos estabelecimentos de saúde(9,24).
A contaminação de monitores e computadores corrobora a hipótese de que superfícies muito tocadas se tornam mais contaminadas(5,8). Tal premissa reforça a idéia de que muitas vezes os profissionais, após tocar um paciente, não se atêm à importância da higienização das mãos e retomam atividades sem se dar conta da possibilidade de disseminar microrganismos.
A similaridade das cepas, somada a outras evidências, permite considerações mais precisas sobre a origem de um surto de forma a favorecer a implementação de medidas eficazes de controle(2,17-21). Os testes moleculares constituem importante auxílio para verificação de similaridade de cepas. Todavia esses testes ainda são pouco acessíveis aos laboratórios hospitalares, devido a recursos econômicos limitados muitas vezes se fazendo inviáveis(4).
A circulação de clone único em surtos constitui evidência do envolvimento ambiental nas IRAS. Entretanto, a contaminação de superfícies pode diferir entre períodos endêmicos e de surtos(1). Durante surtos a contaminação ambiental pode ser mais elevada. Contudo, nas situações endêmicas também se registrou contaminação de superfícies com cepas similares às de pacientes e o ambiente contaminado como fator preditivo na aquisição de VRE e MRSA(1,8-9,11).
A contaminação de locais aparentemente limpos reforça a possibilidade da disseminação de patógenos, locais esses analisados como superficies limpas; sem aparente sujidade, fazendo com que muitas vezes sejam ignoradas medidas eficazes de limpeza. O trânsito de pessoas; equipe de saúde e visitantes, na unidade e, consequentemente, o contato com pacientes, objetos e superfícies diversas conferem possibilidades de disseminação de patógenos se não observadas às devidas precauções, com destaque para a higienização das mãos. Entretanto, outras vias podem contribuir na transferência de patógenos(22-23).
A transferência de MRSA e VRE de superfícies e equipamentos foi ressaltada no guideline de controle ambiental de infecção em serviços de saúde como provável via disseminadora. Com destaque da contaminação de superfícies por VRE mais elevada em áreas clínicas de pacientes colonizados em múltiplos sítios do corpo, com diarréia e falhas na técnica do uso de luvas pelos profissionais ou higienização do paciente, das mãos dos familiares e visitantes(24). A educação permanente dos profissionais e orientação dos pacientes, familiares e visitantes quanto às medidas de controle das IRA constituem importante aspecto para abordagem nos serviços de saúde.
A contaminação das superfícies poderia ser reduzida com a higienização das mãos antes e após contato com os pacientes e com essas. Todavia, a aderência a tal prática pelos profissionais tem sido frequentemente apontada com índices inferiores a 50%, nos estabelecimentos de saúde em geral(12,15). Diversos aspectos permeiam a aplicação efetiva das medidas de controle nas IRAS. Dentre esses tem sido observado, de acordo com o guideline sobre manejo de organismos multirresistentes nos estabelecimentos de saúde, que os profissionais são mais receptivos às medidas de controle quando os líderes participam conjuntamente(25).
O esclarecimento do papel das superfícies na disseminação das IRAS pode fornecer subsídios que favoreçam maior aderência às medidas de controle e revisão de políticas, além alertar para vias de disseminação ainda subestimadas.
A intensificação da limpeza de rotina minimiza a disseminação dos patógenos. A adequação do tempo, freqüência e cuidados específicos na limpeza de superfícies merecem maior atenção, pois a remoção de sujidades é relevante para redução de biofilmes. A disseminação dos patógenos pode ser prevenida pela aplicação de estratégias de engenharia e controle ambiental, ou seja, uma organização da unidade do paciente que favoreça a limpeza e demais cuidados(26).
CONSIDERAÇÕES FINAIS
A contaminação das superfícies ambientais das UTI, associada ao maior risco de aquisição de MRSA e VRE, foi frequente em situações endêmicas, enquanto nos surtos destacaram-se A. baumannii e P. aeruginosa resistentes ao carbapenêmicos. Nas duas situações observou-se a similaridade entre cepas encontradas em pacientes e aquelas isoladas das superfícies ambientais. Os métodos moleculares destacaram-se em análises da disseminação das IRAS.
As UTI merecem atenção especial devido ao seu aspecto físico que favorece a disseminação de patógenos somada à presença dos pacientes em cuidados intensivos com maior risco para aquisição de infecções. A organização do espaço físico entre leitos e equipamentos, assim como a aplicação de protocolos de limpeza dessas superfícies consoante as características do setor, somados à orientação do paciente, familiares e visitantes quanto à higienização das mãos e educação permanente dos profissionais podem reduzir a disseminação ambiental e aquisição de patógenos.
Diante das observações da disseminação de patógenos no ambiente hospitalar, faz-se necessário maior conhecimento, controle das fontes, vias disseminadoras e disponibilização de recursos que viabilizem as técnicas para identificação e comparação de patógenos, mais acuradas nos laboratórios hospitalares. Cabe ressaltar, ainda, a relevância de atentar para a qualidade da limpeza ambiental, métodos de execução, produtos, grau de conhecimento dos profissionais sobre a importância desses aspectos e relação com a redução da disseminação das IRAS.
Recebido: 20/01/2009
Aprovado: 27/11/2009
- 1. Drees M, Snydman DR, Schmid CH, Barefoot L, Hansjosten K, Vue PM, et al. Prior environmental contamination increases the risk of acquisition of vancomycin-resistant enterococci. Clin Infect Dis. 2008;46(5):678-85.
- 2. Kayabas U, Bayraktar M, Otlu B, Ugras M, Ersoy Y, Bayindir Y, et al. An outbreak of Pseudomonas aeruginosa because of inadequate disinfection procedures in a urology unite: A pulsed-field gel electrophoresis - based epidemiologic study. Am J Infect Control. 2008;36(1):33-8.
- 3. Hayden MK, Blom DW, Lyle EA, Moore CG, Weistein RA. Risk of hand or glove contamination after contact with vancomycin-resistant enterococcus or the colonized patients' environment. Infect Control Hosp Epidemiol. 2008;29(2):149-54.
- 4. Sexton T, Clark P, O'Neill E, Dillane T, Humphreys H. Environmental reservoirs of methicillin-resistant staphylococcus aureus in isolation rooms: correlation with patient isolates and implications for hospital hygiene. J Hosp Infect. 2006;62(2):187-94.
- 5. Hayden MK, Bonten MJM, Blom DW, Lyle EA, van de Vijver DAMC, Weinstein RA. Reduction in acquisition of of vancomycin-resistant enterococcus after enforcement of routine environmental cleaning measures. Clin Infect Dis. 2006;42(11):1552-60.
- 6. Eengelhart S, Krizek L, Glasmacher A, Fischnaller E, Marklein G, Exner M. Pseudomonas aeruginosa outbreak in a haematology-oncology unit associated with contaminated surface cleaning equipment. J Hosp Infect. 2002;52(1):93-8.
- 7. Huang SS, Datta R, Plat R. Risk of acquiring antibiotic-resistant bacteria from prior room occupants. Arch Intern Med. 2006;166(16):1945-51.
- 8. Lemmen SW, Häfner H, Zolldann D, Stanzel S, Lüttichen R. Distribution of multi-resistant gram-negative versus gram-positive bacteria in the hospital inanimate environment. J Hosp Infect. 2004;56(3):191-7.
- 9. Rogues A-M, Boulestreau H, Lashe´ras A, Boyer A, Gruson D, Merle C, et al. Contribution of tap water to patient colonisation with Pseudomonas aeruginosa in a medical intensive care unit. J Hosp Infect. 2007;67(1):72-8.
- 10. Hardy KJ, Oppenheim BA, Gossain S, Gao F, Hawkey PM. A study of relationship between environmental contamination with Methicillin-Resistant Staphylococcus Aureus (MRSA) and patients' acquisition of MRSA. Infect Control Hosp Epidemiol. 2006;27(2):127-32.
- 11. Martinez JA, Ruthazer R, Karen H, Barefoot L, Snydman DR. Role of environmental contamination as a risk factor for acquisition of vancomycin-resistant enterococci in patients treated in a medical intensive care unit. Arch Inter Med. 2003;163(16):1905-12.
- 12. Duckro AM, Blom DW, Lyle EA, Weisntein RA, Hayden MK. Transfer of vancomycin-resistant enterococci via healthy care worker hands. Arch Inter Med. 2005;165(3):302-7.
- 13. Petignat C, Francioli P, Nahimana N, Wenger A, Bille J, Schaller MD, et al. Exogenous source of pseudomonas aeruginosa in a intensive care unit patients: implementation of infection control and follow-up with molecular typing. Infect Control Hosp Epidemiol. 2006;27(9):953-7.
- 14. Bures S, Fishbain JT, Uyehara CFT, Parker JM, Berg BW. Computer keyboards and faucet handles as reservoirs of nosocomial pathogens in intensive care unit. Am J Infect Control. 2000;28(6):465-70.
- 15. Dubberke ER, Reske KA, Noble-Wang J, Thompson A, Killgore G, Mayfield J, et al. Prevalence of clostridium difficile environmental contamination and strain variability in multiple healthy care facilities. Am J Infect Control. 2007;35(5):315-8.
- 16. El Shafie SS, Alishaq M, Garcia ML. Investigation of an outbreak of multidrug-resistant Acinetobacter baumannii in trauma intensive care unit. J Hosp Infect. 2004;56(1):101-5.
- 17. Enoch DA, Summers C, Brown NM, Moore L, Gillham MI, Burnstein RM, et al. Investigation and management of an outbreak of multidrug-carbapenem-resistant acineto-bacter baumannii in Cambridge, UK. J Hosp Infect. 2008;70 (2):109-18.
- 18. Simor AE, Lee M, Vearncombe M, Jones-Paul L, Barry C, Gomez M, et al. An outbreak due to multirresistant Acinetobacter baumannii in a burn unit: risk factors for acquisition and management. Infect Control Hosp Epidemiol. 2002;23(5):261-7.
- 19. Kazakova SV, Ware K, Baughman B, Bilukha O, Paradis A, Sears S, et al. A hospital outbreak of diarrhea due to an emerging epidemic strain of Clostridium difficile. Arch Inter Med. 2006;166(22):2518-24.
- 20. Pena C, Dominguez MA, Pujol M, Verdaguer R, Gudiol F, Ariza J. An outbreak of carbapenem-resistant pseudomonas aeruginosa in a urology ward. Clin Microbiol Infect. 2003;9(9):938-43.
- 21. Deplano A, Denis O, Poirel L, Hocquet D, Nonhoff C, Byl B, et al. Molecular characterization of an epidemic clone of panantibiotic-resistant pseudomonas aeruginosa. J Clin Microbiol. 2005;43(3):1198-204.
- 22. Wybo I, Blommaert L, De Bier T, Soetens O, De Regt J, Lacor P, et al. Outbreak of multidrug-resistant Acinetobacter baumannii in a Belgian university hospital after transfer of patients from Greece. J Hosp Infect. 2007;67(4):374-80.
- 23. Comert FB, Kulah C, Aktas E, Ozlu N, Celebi G. First isolation of vancomycin-resistant enterococci and spread of a single clone in a university hospital in northswestern Turquey. Eur J Clin Microbiol Infect Dis. 2007;26(1):57-61.
- 24. Sehulster LM, Chinn RYW, Arduino MJ, Carpenter J, Donlan R, Ashford D, et al. Guidelines for environmental infection control in health-care facilities. Recommendations from Centers for Disease Control and Prevention (CDC) and the Healthcare Infection Control Practices Advisory Committee (HICPAC). Chicago, IL: American Society for Healthcare Engineering/American Hospital Association; 2004.
- 25. Siegel JD, Rhinehart E, Jackson M, Chiarello L, Healthcare Infection Control Practices Advisory Committee (HICPAC). Management of Multidrug-Resistant Organisms in Healthcare Settings, 2006. Atlanta, GA: Centers for Disease Control and Prevention; 2006.
- 26. Shulester L, Chinn RY. Guidelines for environmental infection control in healthcare facilities. Atlanta, GA: Centers for Disease Control and Prevention; 2003.
Correspondência:
Datas de Publicação
-
Publicação nesta coleção
15 Dez 2010 -
Data do Fascículo
Dez 2010
Histórico
-
Recebido
20 Jan 2009 -
Aceito
27 Nov 2009