Resumos
Anastrepha sororcula Zucchi, 1979, é uma das espécies de mosca-das-frutas mais disseminadas no País, sendo considerada a praga-chave que causa os maiores danos à produção de goiaba (Psidium guajava L., 1758) no Brasil. Em vista da importância desta espécie no complexo de pragas naturais da fruticultura brasileira e, em face à escassez de dados sobre sua biologia e comportamento, este trabalho teve por objetivo obter informações sobre a idade de maturação sexual de A. sororcula em laboratório e descrever seu comportamento reprodutivo. Os machos atingiram a maturidade sexual entre 7 e 18 dias após a emergência, com a maioria dos indivíduos tornando-se sexualmente maduros entre 10 e 13 dias de idade. Exibiram comportamento de sinalização às fêmeas, caracterizado pela distensão da região pleural do abdome, formando uma pequena bolsa de cada lado e, eversão de uma diminuta bolsa membranosa de cutícula retal que circunda a área anal. Durante este processo, os machos realizaram rápidos movimentos de vibração das asas, produzindo sinais audíveis. Uma gotícula foi liberada da região anal durante os movimentos de vibração alar. Após a atração das fêmeas, os machos realizaram uma série de movimentos elaborados de cortejo. As fêmeas alcançaram a maturação sexual entre 14 e 24 dias da emergência, com a maioria tornando-se sexualmente madura aos 19 dias de idade. A exibição diária das atividades sexuais foi confinada quase que exclusivamente ao período das 16:00-17:30h. A. sororcula apresentou um acentuado padrão de protandria.
Mosca-das-frutas; comportamento de acasalamento; maturação sexual; reprodução
Anastrepha sororcula Zucchi, 1979, is a fruit fly species that can be considered a key pest to the production of guava (Psidium guajava L., 1758), fruit tree which has a wide distribution in Brazil. In view of the importance of this species as a natural pest of Brazilian horticulture and, considering the lack of data about its biology and behavior, the aim of this paper is to obtain information about the age of sexual maturation of A. sororcula in the laboratory and to describe its reproductive behavior. The males reached sexual maturity between 7 and 18 days after emergence, with most of the individuals becoming sexually mature between 10 and 13 days of age. They exhibited signalling behavior to the females, characterized by the distension of the pleural area of the abdomen, forming a small pouch on each side, and by the protrusion of a tiny membranous pouch of rectal cuticle that surrounds the anal area. During this display, the males produced rapid movements of vibration of the wings, producing audible sounds. A droplet was liberated from the anal area during the vibration movements of the wings. After attracting the females, the males accomplished a series of elaborated movements of courtship behavior. The females reached sexual maturation between 14 and 24 days after emergence, with the majority becoming sexually mature at 19 days. The daily exhibition of sexual activities was confined almost exclusively to the period of 16:00-17:30h. A. sororcula presented a sharp protandry pattern.
Fruit fly; mating behavior; reproduction; sexual maturation
BIOLOGIA, ECOLOGIA E DIVERSIDADE
Comportamento sexual de Anastrepha sororcula Zucchi (Diptera, Tephritidae) em laboratório
Sexual behavior of Anastrepha sororcula Zucchi (Diptera, Tephritidae) in laboratory
Michelli C. N. Facholi-Bendassolli; Manoel A. Uchôa-Fernandes
Laboratório de Insetos Frugívoros, Programa de Pós-Graduação em Entomologia e Conservação da Biodiversidade, Universidade Federal da Grande Dourados (UFGD), Caixa Postal 241, Rodovia Dourados-Itahum, KM 12, 79804-970 Dourados-MS, Brasil. michelli@uems.br; uchoa@ceud.ufms.br
RESUMO
Anastrepha sororcula Zucchi, 1979, é uma das espécies de mosca-das-frutas mais disseminadas no País, sendo considerada a praga-chave que causa os maiores danos à produção de goiaba (Psidium guajava L., 1758) no Brasil. Em vista da importância desta espécie no complexo de pragas naturais da fruticultura brasileira e, em face à escassez de dados sobre sua biologia e comportamento, este trabalho teve por objetivo obter informações sobre a idade de maturação sexual de A. sororcula em laboratório e descrever seu comportamento reprodutivo. Os machos atingiram a maturidade sexual entre 7 e 18 dias após a emergência, com a maioria dos indivíduos tornando-se sexualmente maduros entre 10 e 13 dias de idade. Exibiram comportamento de sinalização às fêmeas, caracterizado pela distensão da região pleural do abdome, formando uma pequena bolsa de cada lado e, eversão de uma diminuta bolsa membranosa de cutícula retal que circunda a área anal. Durante este processo, os machos realizaram rápidos movimentos de vibração das asas, produzindo sinais audíveis. Uma gotícula foi liberada da região anal durante os movimentos de vibração alar. Após a atração das fêmeas, os machos realizaram uma série de movimentos elaborados de cortejo. As fêmeas alcançaram a maturação sexual entre 14 e 24 dias da emergência, com a maioria tornando-se sexualmente madura aos 19 dias de idade. A exibição diária das atividades sexuais foi confinada quase que exclusivamente ao período das 16:00-17:30h. A. sororcula apresentou um acentuado padrão de protandria.
Palavras-chave: Mosca-das-frutas; comportamento de acasalamento; maturação sexual; reprodução.
ABSTRACT
Anastrepha sororcula Zucchi, 1979, is a fruit fly species that can be considered a key pest to the production of guava (Psidium guajava L., 1758), fruit tree which has a wide distribution in Brazil. In view of the importance of this species as a natural pest of Brazilian horticulture and, considering the lack of data about its biology and behavior, the aim of this paper is to obtain information about the age of sexual maturation of A. sororcula in the laboratory and to describe its reproductive behavior. The males reached sexual maturity between 7 and 18 days after emergence, with most of the individuals becoming sexually mature between 10 and 13 days of age. They exhibited signalling behavior to the females, characterized by the distension of the pleural area of the abdomen, forming a small pouch on each side, and by the protrusion of a tiny membranous pouch of rectal cuticle that surrounds the anal area. During this display, the males produced rapid movements of vibration of the wings, producing audible sounds. A droplet was liberated from the anal area during the vibration movements of the wings. After attracting the females, the males accomplished a series of elaborated movements of courtship behavior. The females reached sexual maturation between 14 and 24 days after emergence, with the majority becoming sexually mature at 19 days. The daily exhibition of sexual activities was confined almost exclusively to the period of 16:00-17:30h. A. sororcula presented a sharp protandry pattern.
Keywords: Fruit fly; mating behavior; reproduction; sexual maturation.
O Brasil é considerado o maior produtor de frutos tropicais do mundo, exportando para vários países. No entanto, a fruticultura nacional enfrenta sérios problemas fitossanitários decorrentes da ação das moscas-das-frutas, que são limitantes à produção frutícola e motivo de restrições quarentenárias impostas pelos países importadores. Além disso, esses tefritídeos são responsáveis pelo uso de grandes quantidades de inseticidas químicos para seu controle (Duarte & Malavasi 2000; Vilela & Kovaleski 2000). Tais problemas motivaram a busca de novas tecnologias para o controle deste grupo de insetos-praga, principalmente, devido à nova tendência mundial da preferência por produtos de qualidade, mas isentos de resíduos de pesticidas, o que exige dos países exportadores menor número de pulverizações com agrotóxicos para a produção de frutas (Carvalho et al. 2000).
Estudos básicos de biologia e do comportamento das espécies neotropicais de moscas-das-frutas são importantes para a compreensão do ciclo de vida e das estratégias reprodutivas desses tefritídeos. Estas informações são fundamentais para dar suporte à implementação de técnicas de manejo integrado, principalmente as que incluem o monitoramento, a coleta massiva e a supressão populacional de insetos-praga por métodos biológicos e/ou que empregam infoquímicos.
Anastrepha sororcula Zucchi é amplamente disseminada no País e encontra-se entre as sete espécies de maior importância econômica no Brasil, atacando frutos de goiaba, jabuticaba e de outras Myrtaceae (Zucchi 1988, 2000). De acordo com Uchôa-Fernandes et al. (2002), no estado de Mato Grosso do Sul, A. sororcula é a espécie predominante em mirtáceas nativas e cultivadas. Entretanto, apesar de ser uma das pragas-chave da fruticultura, são escassos os estudos sobre seu comportamento reprodutivo.
Os objetivos deste trabalho foram obter informações sobre a idade de maturação sexual de machos e de fêmeas e estudar, em laboratório, o comportamento reprodutivo de A. sororcula, descrevendo cada etapa das atividades de corte e cópula, incluindo sua periodicidade e duração.
MATERIAL E MÉTODOS
Local do estudo. Os bioensaios foram conduzidos no período de outubro de 2003 a abril de 2004, no Laboratório de Insetos Frugívoros da Universidade Federal da Grande Dourados (UFGD), com fotofase de 12 horas (das 6 às 18h). A temperatura e umidade relativa ambiente foram registradas utilizando-se um termohigrômetro.
As observações foram realizadas diariamente, das 13:30 h às 18:30 horas, quando as moscas cessavam suas atividades. O período diário de registro das atividades comportamentais foi estabelecido conforme informações obtidas em Aluja et al. (2000) e bioensaios preliminares da atividade sexual exibida por A. sororcula no laboratório.
Obtenção dos insetos. Os insetos utilizados foram obtidos de frutos de goiaba (P. guajava) naturalmente infestados, coletados na região de Dourados-MS.
Os frutos foram mantidos em laboratório até a saída de todas as larvas para empupar, conforme metodologia descrita por Uchôa-Fernandes & Zucchi (1999). Os pupários foram acondicionados, até a emergência dos adultos, em potes de acrílico transparente (300ml) contendo areia estéril umedecida com água esterilizada. Os adultos recém-emergidos foram removidos das gaiolas de emergência, separados em casais (ao acaso), e mantidos em gaiolas de observação distintas, feitas com garrafas "PET" transparentes (25 cm altura X 10 cm de diâmetro) cobertas com tecido fino ("voil").
As moscas foram nutridas com água estéril e dieta artificial, composta por uma mistura de açúcar mascavo (100g), proteína hidrolisada (50ml), água esterilizada (100ml) e uma colher de sopa de mel (Salles 1992).
A identidade dos casais de A. sororcula foi confirmada após o término dos bioensaios, através do sacrifício das fêmeas, que foram fixadas em álcool 70% para exame do acúleo, uma vez que esta espécie pode ocorrer em simpatria com outras espécies crípticas.
Estudo da maturação sexual. Trinta casais virgens de A. sororcula, de mesma idade, foram individualizados em gaiolas de observação, conforme descrito anteriormente. Observações sistemáticas foram realizadas diariamente, visando registrar a data de início da exibição do comportamento reprodutivo, que caracteriza a maturidade sexual dos indivíduos. Foi considerado como indício de maturação sexual: a distensão das bolsas abdominais em machos e a ocorrência de acasalamento em fêmeas.
Estudo da atividade sexual. Para este bioensaio, foram utilizados vinte e um casais virgens de A. sororcula, cujos parceiros apresentavam a mesma idade. Diariamente, determinou-se a freqüência e a amplitude (duração) de exibição de atividade sexual, bem como as características comportamentais apresentadas pelos indivíduos. Os comportamentos sexuais dos machos e das fêmeas de A. sororcula foram registrados a intervalos regulares de 15 min., assumindo-se, assim, que os comportamentos da espécie durante os 15 min. precedentes seriam os mesmos exibidos no momento da observação.
Análise dos dados. Os dados sobre a idade de maturação sexual dos machos e das fêmeas de A. sororcula foram submetidos à análise de variância (ANOVA). As informações referentes ao período de ocorrência da atividade sexual foram analisadas pelo teste não-paramétrico de Mann-Whitney para comparar a variação na freqüência de chamamento em cada um dos períodos de observação, pois as variâncias não foram homogêneas e nem todos os dados das amostras aderiram à distribuição normal. Os dados sobre a amplitude (duração) da atividade sexual de chamamento foram submetidos à análise de variância (ANOVA) utilizando o teste de Tukey para comparação entre os dias de observação.
A correlação entre as variáveis ambientais e a amplitude (duração) do chamamento e da cópula foi verificada através da análise de correlação bivariada, calculando-se o índice de correlação de Pearson. Todas as análises foram feitas ao nível de significância de 5%.
RESULTADOS E DISCUSSÃO
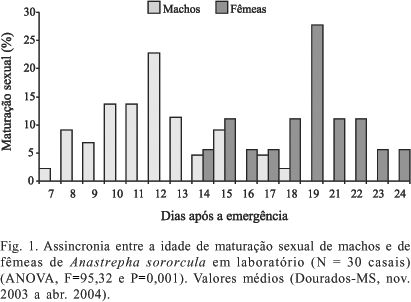
Maturação sexual. Os machos de A. sororcula atingiram a maturidade sexual entre 7 e 18 dias após a emergência, com a maioria dos indivíduos tornando-se sexualmente maduros entre 10 e 13 dias de emergidos (Fig. 1). Nesta idade, os machos distenderam pela primeira vez os pleuritos abdominais do 3° ao 5° segmentos, onde a parte distal das glândulas salivares, provavelmente associadas à produção de feromônios, está alojada. Isto caracterizou o início de atividade sexual dos machos (Fig. 2a). A característica morfológica de formação de bolsas abdominais pode ser utilizada como critério confiável para verificação da maturidade sexual em machos. Este aspecto também foi empregado com sucesso em estudo do dimorfismo sexual das glândulas salivares de A. suspensa (Loew, 1862), tendo sido verificada uma clara correlação entre o início do comportamento sexual, liberação de feromônio e o desenvolvimento das glândulas salivares naquela espécie (Nation 1989).
A idade média obtida para a maturação sexual dos machos de A. sororcula foi de 11,75 (Erro Padrão ± 2,54) dias após a emergência. As fêmeas de A. sororcula alcançaram à maturação sexual entre 14 e 24 dias da emergência, com a maioria tornando-se sexualmente madura aos 19 dias de idade (Fig. 1), quando acasalaram pela primeira vez. A idade média obtida para a maturação sexual das fêmeas de A. sororcula foi de 18,94 (±2,86) dias. Esses resultados diferiram daqueles registrados por Da Silva et al. (1985) que encontraram, em estudo com esta mesma espécie, em Ribeirão Preto-SP, idade média para o acasalamento de 24 dias. Este fato pode ser explicado, em parte, devido à preferência da fêmea pelo estado fisiológico do macho, como verificado por De Lima et al. (1994) para A. fraterculus, cujas fêmeas acasalam preferencialmente com machos que já haviam copulado.
Observou-se neste trabalho que a ocorrência de acasalamento para machos de A. sororcula não pode ser interpretada como indício de maturidade sexual, uma vez que os machos podem estar sexualmente maduros, mas não acasalarem, em decorrência da idade de maturação sexual da fêmea e/ou devido à preferência da fêmea por características individuais do macho, com base no seu sistema de escolha de parceiros sexuais. Aluja et al.(2000) apresentam possíveis fatores que conduzem ao sucesso reprodutivo dos machos nas espécies de Anastrepha, baseando-se em critérios provavelmente considerados pela fêmea para a escolha de seus parceiros sexuais, tais como: tamanho e condição fisiológica dos machos (virgem/acasalado). Da mesma forma, para fêmeas de A. sororcula, faz-se necessário que novas pesquisas sejam conduzidas para determinar qual é a característica que melhor determina sua idade de maturação sexual, uma vez que o acasalamento pode ser retardado em função de seu sistema de escolha de parceiros sexuais.
Foram encontradas diferenças significativas entre as idades de maturação sexual de machos e de fêmeas em A. sororcula (ANOVA, F= 95,32 e P<0,001). Os machos apresentaram desenvolvimento sexual mais rápido (Fig. 1), caracterizando uma protoandria na maturação sexual desta espécie.
Em muitos insetos, os machos completam o desenvolvimento sexual antes das fêmeas irmãs. Este processo de maturação que ocorre mais rápido no macho (protoandria) pode ser sexualmente selecionado (Sivinski & Calkins 1990). Nas espécies cuja emergência de ambos os sexos é sincronizada, os machos que emergem primeiro têm, potencialmente, maior oportunidade sexual. Em espécies com menor sincronia, o desenvolvimento pode refletir padrões dimórficos de necessidades nutricionais e de crescimento. Por exemplo, o tempo de desenvolvimento de fêmeas de certas espécies de besouros fengodídeos pode exceder o de machos irmãos por um ano ou mais (Sivinski & Calkins 1990). Exemplos do oposto, protoginia, são comparativamente raros e foram descritos somente para algumas espécies de Odonata (Aeshnidae), umas poucas espécies de abelhas megaquilídeas (Hymenoptera, Megachilidae), e a minoria das espécies de mosquitos (Diptera, Culicidae). Entre os tefritídeos, a protoginia ocorre em Rhagoletis completa Cresson, 1929 (Sivinski & Calkins 1990).
A assincronia entre a idade de maturação sexual em A. sororcula pode estar relacionada às necessidades nutricionais da espécie. Estas diferenças podem ser impostas pelo tempo de desenvolvimento entre os machos e as fêmeas durante a fase larval. Deste modo, já que as fêmeas necessitam de nutrientes que são facilmente obtidos através do forrageamento do adulto, elas podem gastar menos tempo como larva e mais tempo como adultos pré-reprodutivos. Assim, pode-se inferir que ao invés das fêmeas abreviarem o período larval, os machos poderiam ser selecionados por estenderem esta fase do ciclo de vida. Isso explicaria o dimorfismo temporal, particularmente, se o macho se tornaria maior com o tempo e assim melhoraria a capacidade de competir por parceiras (Sivinski & Burk 1989). Entretanto, o tempo gasto como juvenil simplesmente pode não se traduz em tamanho. Larvas que originarão fêmeas poderão ter um tempo de desenvolvimento mais curto e serem maiores que os machos co-específicos. As larvas que originarão machos poderiam estar acumulando recursos que lhes permitiriam encurtar o período de forrageamento do adulto, e assim, alcançarem a maturidade sexual mais cedo (Sivinski & Calkins 1990). Uma outra hipótese plausível é que esta diferença entre as idades de maturação sexual dos machos e das fêmeas de A. sororcula poderia se constituir em um importante mecanismo para evitar a ocorrência de endocruzamentos, uma vez que a maturação sexual mais cedo em machos, poderia agir diminuindo as chances de acasalamentos com suas irmãs, como destacado por Futuyma (1992).
O conhecimento científico sobre desenvolvimento larval dimórfico entre machos e fêmeas e, sobre essa assincronia no tempo de maturação sexual em A. sororcula, tem importantes implicações práticas para o manejo integrado desta espécie: larvas de machos poderiam ser empregadas na obtenção de adultos para a técnica do macho estéril; em programas de controle biológico com a liberação inundativa de parasitóides; já as larvas que originarão fêmeas, poderiam ser empregadas para a multiplicação desses entomófagos. Essa diferenciação temporal poderá ser útil, também, em pesquisas sobre a comunicação química intra-específica, facilitando a separação dos machos e das fêmeas para estudos do comportamento e de ecologia química. Pois, em pesquisas que envolvem feromônios sexuais, os machos e as fêmeas deverão ser mantidos em ambientes separados, de modo a evitar a acomodação sensorial aos fenômenos e o conseqüente mascaramento de respostas na atração entre os parceiros sexuais (Sivinski & Calkins 1990; Vilela & Della Lucia 2001). Portanto, este trabalho sugere a necessidade do desenvolvimento de pesquisas para verificar se em A. sororcula as fases juvenis para machos e fêmeas têm duração diferenciadas.
Comportamento sexual. Machos de A. sororcula sexualmente ativos sinalizaram às fêmeas predominantemente das paredes das gaiolas, em posição vertical ao piso. Estes, em determinado ponto na parede da gaiola, distendiam os pleuritos abdominais do 3° ao 5° segmentos, formando uma pequena bolsa de cada lado do abdome, e evertiam uma diminuta bolsa membranosa de cutícula retal que circunda a área anal (Fig.2a). Durante este processo, aqui denominado comportamento de chamamento, os machos geralmente realizaram rápidos movimentos de vibração das asas, executados em uma seqüência de pulsos de aproximadamente 1s, produzindo sinais sonoros audíveis e estereotipados, como evidenciado em outras espécies de Anastrepha (Landolt & Averill 1999). Uma gotícula, provavelmente de feromônio, era liberada da região anal durante os movimentos de vibração alar. Durante o período de maior atividade sexual, os machos repetidamente giravam o corpo em 360°, enquanto vibravam suas asas e tocavam várias vezes a membrana anal na parede da gaiola, na qual era deixada uma gota diminuta.
Os machos de A. sororcula permaneciam em atividade de sinalização até que a fêmea fosse atraída e se aproximasse. Caso a fêmea não se aproximasse, estes giravam o corpo assumindo uma nova direção ou moviam-se para outro ponto da gaiola, reiniciando o comportamento de chamamento. Quando houve atração, as fêmeas se aproximavam em vôo e pousavam a cerca de 5 cm dos machos, os quais iniciavam a exibição de uma série de movimentos elaborados de cortejo, aqui denominados comportamento de cortejo.
Em atividade de cortejo, os machos, logo após a aproximação das fêmeas, caminhavam frontal e lentamente em direção às fêmeas, realizando movimentos de rotação alternada das asas em um arco de cerca de 45°, perpendicularmente ao eixo do corpo. A cerca de 1 cm de distância das fêmeas, os machos paravam, e ambos (macho e fêmea), permaneciam imóveis frente a frente, por cerca de 3s (Fig.2b). Repentinamente o macho voava e pousava sobre o dorso da fêmea ou subia pela cabeça da parceira e a montava.
Na cópula, os machos posicionavam-se de forma retilínea sobre o corpo das fêmeas, de modo que, quando vistos de cima, pareciam um único indivíduo (Fig.2c). Os machos dispunham suas pernas anteriores na região do cérvix ou da propleura das parceiras, com as pernas medianas na região pleural do abdome e as posteriores entrelaçando-se ao redor da bainha do ovipositor, de modo a elevá-lo para que o acúleo fosse protraído e assim pudesse ocorrer o acoplamento das genitálias (Fig.2d). Durante este comportamento, aqui denominado comportamento pré-copulatório, os machos apresentavam vibração intensa e ininterrupta das asas, produzindo um som audível (devido à alta velocidade da vibração alar) que durava aproximadamente 60s, cessando quando a cópula se iniciava, ou seja, a partir do momento em que o edeago era inserido no ovipositor. Comportamento semelhante foi registrado por Da Silva et al. (1985) para A. obliqua (Macquart,1835), A. pseudoparallela (Loew, 1873) e para a espécie aqui estudada, corroborando as observações obtidas neste trabalho. Da mesma forma, Dickens et al. (1982) observaram, em A.ludens (Loew, 1873), posicionamento do macho sobre a fêmea muito semelhante ao descrito para A. sororcula nesta pesquisa.
Em muitas das tentativas de cópula, as fêmeas rejeitavam os machos, abaixando seu ovipositor para que não houvesse introdução da genitália masculina, e movimentando as asas, de forma que o parceiro era impelido a afastar-se. Quando o macho era rejeitado, ele então reiniciava o chamamento (Fig.2a). Quando a fêmea aceitava o parceiro, permitia que ele levantasse seu ovipositor para o acoplamento das genitálias; iniciando-se a cópula propriamente dita. No decorrer desta, o macho, regularmente, realizava movimentos de aproximação do seu corpo (região ventral do tórax) sobre o da fêmea (região dorsal do tórax). O casal permanecia estacionário durante toda a cópula (Fig.2e), movimentando-se somente quando perturbado ou após o desacoplamento das genitálias ao final do acasalamento.
O processo de separação das genitálias iniciava-se com a fêmea movimentando suas pernas posteriores ao longo do ovipositor, provavelmente na tentativa de soltá-lo do macho, que o segurava. A fêmea, ainda, movimentava as asas, fazendo com que o macho se afastasse. O macho, então, desmontava da fêmea e os dois, em posição diametralmente oposta, caminhavam lentamente para o desacoplamento das genitálias (Fig.2f). Após a separação, a fêmea iniciava a limpeza do ovipositor com suas pernas posteriores, e o macho iniciava a limpeza do edeago (Fig.2g). De Lima & Howse (1997) observaram comportamento pós-copulatório semelhante para A. fraterculus (Wiedemann, 1830).
Através desse estudo sobre o comportamento sexual de A. sororcula, foi evidenciado o comportamento de chamamento, no qual, provavelmente, ocorre a liberação de feromônio sexual para atrair a fêmea para o acasalamento. Ocorreu também a exibição de um ritual complexo de cortejamento após o macho e a fêmea entrarem em contato.
O comportamento pré-copulatório observado para A. sororcula apresentou muitas semelhanças com aqueles já descritos para outras espécies deste gênero, como: A. bistrigata Bezzi, 1919, A. fraterculus, A. ludens, A. obliqua, A. serpentina (Wiedemann, 1830) e A. suspensa. Os machos dessas espécies também apresentaram comportamento caracterizado pela distensão dos pleuritos abdominais e eversão da bolsa anal, associada à vibração das asas, bem como a liberação de uma gotícula da região anal (Morgante et al. 1983; Da Silva et al. 1985; Robacker & Hart 1985; Nation 1989; De Lima & Howse 1997). Além disso, o comportamento de A. sororcula aqui apresentado, corrobora com as informações publicadas por Da Silva et al. (1985) para esta mesma espécie, que observaram os mesmos processos de sinalização e cortejamento exibidos pelos machos.
Periodicidade e Duração das Atividades Sexuais. Os machos de A. sororcula apresentaram atividade sexual mais concentrada ao final do período vespertino (Fig. 3). O início do chamamento ocorre por volta das 13:30 h, aumentando linearmente após esse horário e atingindo o pico de atividade às 17:30h. O comportamento sexual praticamente cessa ao redor das 18:30h. Esses resultados corroboram com aqueles apresentados em Aluja et al. (2000), que indicaram, para esta mesma espécie, um período de atividade semelhante, entre 16-19h.
Foram encontradas diferenças estatisticamente significativas entre as horas do dia em que ocorre a atividade de chamamento em A. sororcula (Mann-Whitney, P < 0,05). Os machos apresentaram tendência de chamamento expressivamente maior entre 16:00 e 17:30 h, havendo, neste horário, aumento significativo na freqüência do comportamento de chamamento. Antes ou após esse período, foi exibida pouca ou nenhuma atividade sexual. O início da cópula também ocorre nesse intervalo, provavelmente porque a freqüência da atividade sexual é mais intensa.
O ritmo diário de chamamento exibido por machos é muito diferente entre as espécies de Anastrepha. Seu início varia do amanhecer ao anoitecer, dependendo da espécie (Aluja et al. 2000). O fato do comportamento de chamamento e o início da cópula estarem confinados quase que exclusivamente ao período entre 16:00h e 17:30h, pode ser muito importante na manutenção do isolamento reprodutivo entre as diferentes espécies de um mesmo gênero, principalmente quando estas utilizam simultaneamente o mesmo hospedeiro. Esse é o caso de A. sororcula, A. fraterculus, A. turpiniae Stone, 1942 e A. zenildae Zucchi, 1979, espécies crípticas que podem compartilhar o mesmo recurso, frutos de goiaba. Por serem espécies morfologicamente semelhantes, elas apresentam mecanismos pré-zigóticos bem caracterizados, com diferenças comportamentais marcantes que influenciam no reconhecimento específico, como os diferentes períodos de atividade sexual (Malavasi et al. 1983; Dos Santos et al. 2001).
Verificou-se, portanto, uma tendência para maior atividade sexual de A. sororcula ao final do período vespertino. Resultados semelhantes foram encontrados por Kuba et al.(1984). Aqueles autores observaram que para machos de Bactrocera curcubitae (Coquillett, 1899), quando a intensidade luminosa diminui a um valor crítico, eles agregam-se sobre as folhas da planta hospedeira e vibram as asas, emitindo feromônio sexual. Em Bactrocera (Dacinae, tefritídeos mais primitivos), os machos atraem as fêmeas receptivas e saltam sobre as que se aproximam, tentando a cópula. Estudos sobre o comportamento de acasalamento de Bactrocera dorsalis (Hendel, 1912) evidenciaram que, próximo ao início do crepúsculo, as fêmeas e os machos ficam excitados, produzindo um som em forma de zumbido e em seguida ocorre a cópula (Sivinski et al. 2000).
Em estudos do comportamento sexual de A. ludens e de A. suspensa, não foi constatada cópula até poucos minutos antes do pôr-do-sol (Sivinski et al. 2000). Aluja et al (2000) mencionaram que, em experimentos realizados para testar o efeito do fotoperíodo no acasalamento de A. ludens, foi observado que aquela espécie pode ter o início do acasalamento induzido pela luminosidade em horários diferentes do seu padrão normal de atividade.
Os insetos, como outros organismos, geralmente restringem suas atividades a certos períodos do dia ou da noite, respondendo a um ritmo circadiano que determina os momentos em que estas atividades ocorrerão (Saunders 1982). Um grande número de trabalhos relatam vários exemplos de espécies de insetos nas quais a liberação e a resposta aos feromônios são evidentes em uma certa hora do dia ou da noite. Segundo Saunders (1982), as atividades rítmicas estão sob a influência de vários componentes endógenos e exógenos. Assim, estas atividades, embora controladas por fatores endógenos, são continuamente afetadas pelos efeitos diretos dos fatores ambientais cíclicos, como temperatura, umidade relativa do ar e luminosidade; particularmente pelas trocas bruscas na intensidade de luz.
A análise da influência exercida pelas variáveis ambientais: temperatura e umidade relativa do ar sobre a duração da atividade sexual de chamamento de A. sororcula, não constatou correlação significativa entre estas (Pearson, r = 0,35, P > 0,05 e r = - 0,116; P > 0,05, respectivamente). A amplitude de temperatura e da umidade relativa do ar, verificadas durante o período experimental foi baixa. Essa pequena variação explica, provavelmente, a ausência de correlação entre esses dois fatores climáticos e a duração do comportamento de chamamento, como constatado pela análise de correlação.
A duração média diária da atividade de chamamento entre os machos de A. sororcula foi de 2,3 (±0.99) horas. A duração média diária da atividade de chamamento foi significativamente influenciada pela idade do macho, sendo os maiores períodos de chamamento observados quando os machos encontravam-se entre o 18º e 22º dias da emergência (Tukey, P<0,05) (Fig. 4). Esses resultados constituem uma informação importante para o desenvolvimento de pesquisa aplicada, uma vez que apresentam a melhor idade para o emprego de machos vivos de A. sororcula como atrativo em armadilhas de feromônio, para a extração de glândulas ou coleta de odores em olfatômetro, visando comprovar ou refutar a existência de feromônio sexual nesta espécie.
A duração média da atividade de cópula de A. sororcula foi de 56,3 (±20,41) min. Esses resultados estão de acordo com os obtidos por Da Silva et al. (1985), que encontraram, para esta mesma espécie, média de 58 min. para o acasalamento. Aluja et al. (2000) apresentam, para A. sororcula, tempo médio de cópula de 50 min. Entre as espécies de Anastrepha, o tempo médio de acasalamento varia entre 24,3 (±1,5) min. para A. bistrigata a 350 (± 60) min. para A. hamata (Loew, 1873). Cópulas que se estendem além do necessário para a transferência de espermatozóides em espécies filogeneticamente próximas, freqüentemente são interpretadas como um mecanismo de evitar a competição intra-específica por parceiras já inseminadas (Sivinski et al. 2000). Em várias espécies de Diptera, os machos fornecem recursos que são incorporados aos tecidos somáticos e aos ovários das fêmeas. Em Musca domestica L., 1758, todos os espermatozóides são transferidos nos primeiros 10-15 minutos, mas o período de cópula geralmente atinge 1h (Sivinski et al. 2000). Alguns autores acreditam que um tempo extra de cópula é necessário para que os machos transfiram substâncias químicas, juntamente com o fluido seminal, diminuindo a receptividade das fêmeas para futuros acasalamentos (Chen et al. 1988; Kuba & Itô 1993).
Agradecimentos. Ao Dr. Honório Roberto dos Santos (DCA, UFGD), pelo auxílio prestado; ao Dr. Odival Faccenda (PROPP, UEMS) pelas análises estatísticas e sugestões; a CAPES pela concessão da bolsa de estudo ao primeiro autor e à Fundação de Apoio ao Desenvolvimento do Ensino, Ciência e Tecnologia do Estado de Mato Grosso do Sul (FUNDECT) pelo aporte financeiro ao projeto "Biodiversidade de insetos frugívoros, seus hospedeiros e inimigos naturais no Brasil Central" (Edital 01/2002, Processo No.41/100126/2003).
Recebido em 22/11/2005; aceito em 20/06/2006
- Aluja, M.; J. Piñero; I. Jácome; F. Díaz-Fleischer & J. Sivinski. 2000. Behavior of flies in the genus Anastrepha (Trypetinae: Toxotrypanini), p. 375401. In: M. Aluja & A. L. Norrbom (eds.). Fruit flies (Tephritidae): phylogeny and evolution of behavior. New York, CRC Press, 944p.
- Carvalho, R. da S.; A. S. Nascimento & W. J. R. Matrangolo. 2000. Controle biológico, p. 113117. In: A. Malavasi & R. A. Zucchi (eds.). Moscas-das-frutas de importância econômica no Brasil: conhecimento básico e aplicado. Ribeirão Preto, Holos, 327p.
- Chen, P. S.; E. Stumm-Zollinger; T. Aigaki; M. Balmer; M. Bienz & P. Böhlen. 1988. A male accessory gland peptide that regulates reproductive behavior of female D. melanogaster Cell 54: 291298.
- Da Silva, M. T.; Y. J. Polloni & S. Bressan. 1985. Mating behavior of some fruit flies of the genus Anastrepha Schiner, 1868 (Diptera, Tephritidae) in the laboratory. Revista Brasileira de Entomologia 29: 155164.
- De Lima, I. S. & P. E. Howse 1997. Diurnal activity maturation of the South American fruit fly (Diptera: Tephritidae) in the laboratory. Anais da Sociedade Entomológica do Brasil 26: 299308.
- De Lima, L. S.; P. E. Howse & L. A. B. Salles. 1994. Reproductive behavior of the South American fruit fly Anastrepha fraterculus (Diptera: Tephritidae): laboratory and field studies. Physiological Entomology 19: 271277.
- Dickens, J. C.; E. Solis & W. G. Hart. 1982. Sexual development and mating behavior of the Mexican fruit fly, Anastrepha ludens (Loew). Southwestern Entomologist 7: 915.
- Dos Santos, P.; K. Uramoto & S. R. Martioli. 2001. Experimental hybridization among Anastrepha species (Diptera: Tephritidae): production and morphological characterization of F1 hybrids. Annals of the Entomological Society of America 94: 717725.
- Duarte, A. L. & A. Malavasi. 2000. Tratamentos quarentenários, p. 187192. In: A. Malavasi & R. A. Zucchi (eds.). Moscas-das-frutas de importância econômica no Brasil: conhecimento básico e aplicado. Ribeirão Preto, Holos, 327p.
- Futuyma, D. J. 1992. Biologia Evolutiva 2. ed. Sociedade Brasileira de Genética-CNPq. Ribeirão Preto. 631p.
- Kuba, H. & Y. Itô. 1993. Remating inhibition in the melon fly, Bactrocera (=Dacus) curcubitae (Diptera: Tephritidae): copulation with spermless males inhibits female remating. Journal Of Ethology 11: 2328.
- Kuba, H.; J. Koyama & R. J. Prokopy. 1984. Mating behavior of wild melon flies, Dacus curcubitae Coquillet (Diptera: Tephritidae) in a field cage: distribution and behavior of flies. Applied Entomology and Zoology 19: 367373.
- Landolt, P. J. & A. L. Averill. 1999. Fruit flies, p. 325. In: J. Hardie & A. K. Minks (eds.). Pheromones of non-lepidopteran insects associated agricultural plants. Portland, CABI Publishing, 466p.
- Malavasi A.; J. S. Morgante & R. J. Prokopy. 1983. Distribution and activities of Anastrepha fraterculus (Diptera: Tephritidae) flies on host and nonhost trees. Annals of the Entomological Society of America 76: 286292.
- Morgante, J. S.; A. Malavasi & R. J. Prokopy. 1983. Mating behavior of wild Anastrepha fraterculus (Diptera: Tephritidae) on a caged host tree. Florida Entomologist 66: 234241.
- Nation, J. L. 1989. The role of pheromones in the mating system of Anastrepha fruit flies, p. 189205. In: A. Robinson & S. Hooper (eds.). World crop pests, fruit flies: their biology, natural enemies and control. Amsterdam, Elsevier, V.3A. 327p.
- Robacker, D. C. & W. G. Hart. 1985. Courtship and territoriality of laboratory reared Mexican fruit flies, Anastrepha ludens (Diptera Tephritidae), in cages containing host and nonhost trees. Annals of the Entomological Society of America 78: 488494.
- Salles, L. A. B. 1992. Metodologia de criação de Anastrepha fraterculus (Wied., 1830) (Diptera: Tephritidae) em dieta artificial em laboratório. Anais da Sociedade Entomológica do Brasil 21: 479486.
- Saunders, D. S. 1982. Insect Clocks. Oxford, Pergamon Press, 409p.
- Sivinski, J. M. & T. Burk. 1989. Reproductive and mating behavior, p.343351. In: A. S. Robinson & G. Hooper (eds.). Fruit flies - biology, natural enemies and control. Amsterdam, Elsevier, 447p.
- Sivinski, J. M. & C. O. Calkins. 1990. Sexually dimorphic developmental rates in the Caribbean fruit fly (Anastrepha suspensa (Loew)). Environmental Entomology 19: 14911495.
- Sivinski, J.; M. Aluja; G. Dodson; A. Freidberg; D. Headrick; K. Kaneshiro & P. Landolt. 2000. Topics in the evolution of sexual behavior in the Tephritidae, p. 751786. In: M. Aluja & A. L. Norrbom (eds.). Fruit flies (Tephritidae): phylogeny and evolution of behavior. New York, CRC Press, 944p.
- Uchôa-Fernandes, M. A. & R. A. Zucchi. 1999. Metodología de colecta de Tephritidae y Lonchaeidae frugívoros (Diptera: Tephritoidea) y sus parasitoides (Hymenoptera). Anais da Sociedade Entomológica do Brasil 28: 601610.
- Uchôa-Fernandes, M. A.; I. de Oliveira; R. M. S. Molina & R. A. Zucchi. 2002. Species diversity of frugivorous flies (Diptera: Tephritoidea) from hosts in the cerrado of the state of Mato Grosso do Sul, Brazil. Neotropical Entomology 31: 515524.
- Vilela, E. F. & T. M. C. Della Lucia. 2001. Feromônios de Insetos:biologia, química e emprego no manejo de pragas. 2ed. Ribeirão Preto, Holos, 206 p.
- Vilela, E. F. & A. Kovaleski. 2000. Feromônios, p. 99102. In: A. Malavasi & R. A. Zucchi (eds.). Moscas-das-frutas de importância econômica no Brasil: conhecimento básico e aplicado. Ribeirão Preto, Holos, 327 p.
- Zucchi, R. A. 1988. Moscas-das-frutas (Dip., Tephritidae) no Brasil: taxonomia, distribuição geográfica e hospedeiros, p. 110. In: H.M.L Souza (coord.). Moscas-das-frutas no Brasil. Campinas, Fundação Cargill, 114p.
- Zucchi, R. A. 2000. Taxonomia, p. 1324. In : A. Malavasi & R. A. Zucchi (eds.). Moscas-das-frutas de importância econômica no Brasil: conhecimento básico e aplicado. Ribeirão Preto, Holos-FAPESP, 327 p.
Datas de Publicação
-
Publicação nesta coleção
27 Out 2006 -
Data do Fascículo
Set 2006
Histórico
-
Recebido
22 Nov 2005 -
Aceito
20 Jun 2006