Resumos
O aumento da disponibilidade de P na camada superficial do solo no sistema plantio direto pode resultar em maior transformação de P inorgânico em frações orgânicas de P de diferentes labilidades. Este trabalho teve como objetivo determinar as frações preferenciais de acumulação de P pela adição de doses de fosfato solúvel ao solo no sistema plantio direto. Após cinco anos e meio da instalação do experimento em um Latossolo Vermelho distroférrico típico argiloso, coletaram-se amostras da camada de 0-10 cm de tratamentos com diferentes doses acumuladas de fosfato solúvel: 0, 130, 180, 260, 360, 540 e 720, 980 e 1.240 kg ha-1 P2O5, aplicadas no inverno e, ou, no verão ao longo do tempo. Determinaram-se o P orgânico, inorgânico, total microbiano e seis frações inorgânicas e três orgânicas de P, em extração seqüencial com labilidade decrescente. As modificações observadas no P total, com a adição de fosfato ficaram restritas às frações inorgânicas. A fração moderadamente lábil foi o maior dreno do P adicionado. A contribuição das frações mais lábeis de P aumentou numa relação direta com as doses aplicadas. As frações orgânicas lábeis e moderadamente lábeis de P foram constituintes tão importantes como as respectivas frações inorgânicas, especialmente nas baixas adições de fosfato.
P orgânico; P geoquímico; labilidade
Increased phosphorus availability in the top soil layer of no-tillage systems can lead to a higher transformation from inorganic into organic phosphorus fractions of different labilities. The preferential phosphorus accumulation forms and fractions under the application of soluble phosphate rates in a no-tillage system were determined. During five and a half years, the following accumulated P2O5 rates: 0, 130, 180, 260, 360, 540, 720, 980, and 1.240 kg ha-1 of P2O5, were applied in the winter and/or summer, whereupon samples of the 0-10 cm layer of a clayey Rhodic Hapludox (Oxisol) were collected. Total, organic, inorganic, and microbial phosphorus, as well as six inorganic and three organic phosphorus fractions were determined in a decreasing lability sequence. The observed alterations in the total phosphorus content under phosphate addition were restricted to the inorganic fractions. The moderately labile fraction was the major sink for the applied phosphorus. The importance of labile phosphorus fractions increased in direct relation to the phosphate application rates. Labile and moderately labile organic phosphorus fractions in the soil were as important as the respective inorganic fractions, especially under low phosphate application rates.
biological P; geochemical P; lability
SEÇÃO IV - FERTILIDADE DO SOLO E NUTRIÇÃO DE PLANTAS
Frações de fósforo acumuladas em Latossolo argiloso pela aplicação de fosfato no sistema plantio direto1 1 Parte da Tese de Mestrado do primeiro autor, apresentada à Universidade Federal do Rio Grande do Sul UFRGS para a obtenção do título de Mestre em Ciência do Solo.
Phosphorus accumulation fractions in a clayey oxisol in relation to phosphate doses under no-tillage
E. ConteI; I. AnghinoniII; D. S. RheinheimerIII
IEngenheiro-Agrônomo, Universidade Federal do Rio Grande do Sul UFRGS. Caixa Postal 776, CEP 90001-970 Porto Alegre (RS). E-mail: e.d.conte@zipmail.com.br
IIProfessor do Departamento de Solos, UFRGS. Bolsista CNPq. E-mail: ibanghi@ufrgs.br
IIIProfessor do Departamento de Solos, Universidade Federal de Santa Maria UFSM. Caixa Postal 221, CEP 97105-900 Santa Maria (RS). Bolsista CNPq. E-mail: danilo@ccr.ufsm.br
RESUMO
O aumento da disponibilidade de P na camada superficial do solo no sistema plantio direto pode resultar em maior transformação de P inorgânico em frações orgânicas de P de diferentes labilidades. Este trabalho teve como objetivo determinar as frações preferenciais de acumulação de P pela adição de doses de fosfato solúvel ao solo no sistema plantio direto. Após cinco anos e meio da instalação do experimento em um Latossolo Vermelho distroférrico típico argiloso, coletaram-se amostras da camada de 0-10 cm de tratamentos com diferentes doses acumuladas de fosfato solúvel: 0, 130, 180, 260, 360, 540 e 720, 980 e 1.240 kg ha-1 P2O5, aplicadas no inverno e, ou, no verão ao longo do tempo. Determinaram-se o P orgânico, inorgânico, total microbiano e seis frações inorgânicas e três orgânicas de P, em extração seqüencial com labilidade decrescente. As modificações observadas no P total, com a adição de fosfato ficaram restritas às frações inorgânicas. A fração moderadamente lábil foi o maior dreno do P adicionado. A contribuição das frações mais lábeis de P aumentou numa relação direta com as doses aplicadas. As frações orgânicas lábeis e moderadamente lábeis de P foram constituintes tão importantes como as respectivas frações inorgânicas, especialmente nas baixas adições de fosfato.
Termos de indexação: P orgânico, P geoquímico, labilidade.
SUMMARY
Increased phosphorus availability in the top soil layer of no-tillage systems can lead to a higher transformation from inorganic into organic phosphorus fractions of different labilities. The preferential phosphorus accumulation forms and fractions under the application of soluble phosphate rates in a no-tillage system were determined. During five and a half years, the following accumulated P2O5 rates: 0, 130, 180, 260, 360, 540, 720, 980, and 1.240 kg ha-1 of P2O5, were applied in the winter and/or summer, whereupon samples of the 0-10 cm layer of a clayey Rhodic Hapludox (Oxisol) were collected. Total, organic, inorganic, and microbial phosphorus, as well as six inorganic and three organic phosphorus fractions were determined in a decreasing lability sequence. The observed alterations in the total phosphorus content under phosphate addition were restricted to the inorganic fractions. The moderately labile fraction was the major sink for the applied phosphorus. The importance of labile phosphorus fractions increased in direct relation to the phosphate application rates. Labile and moderately labile organic phosphorus fractions in the soil were as important as the respective inorganic fractions, especially under low phosphate application rates.
Index terms: biological P, geochemical P, lability.
INTRODUÇÃO
A maioria dos solos de regiões tropicais e subtropicais, graças ao seu avançado intemperismo, apresenta maior eletropositividade e adsorção aniônica, como a de fosfatos. O solo compete com a planta pelo P adicionado, caracterizando-se, neste caso, como um dreno (Novais et al., 1998). Esses solos respondem a grandes adições de fertilizantes fosfatados, aumentando a produção vegetal, com reflexos econômicos acentuados. No entanto, as quantidades adicionadas devem ser econômica e ecologicamente corretas, para que, no futuro, não venham a causar problemas ambientais, tal como a eutroficação dos sistemas aquáticos superficiais.
Por outro lado, com o avanço do intemperismo, o P inorgânico (Pi) vai-se tornando mais intensamente adsorvido aos óxidos de Fe e Al, ao mesmo tempo que aumenta a participação do P orgânico (Po) no total de P no solo (Cross & Schlesinger, 1995). O Po pode representar uma fonte potencial de P às plantas por meio da biociclagem (Tiessen et al., 1984). O estudo da biogeoquímica do P deve envolver todas as etapas do seu ciclo para que se possa melhorar a biociclagem, aumentar a eficiência da adubação fosfatada e prevenir problemas ambientais causados pelo excesso de P no solo.
O uso e o manejo do solo altera a dinâmica do P, principalmente naqueles mais arenosos, com maior resiliência (Rheinheimer, 2000). O sistema plantio direto (SPD) tem sido rapidamente incorporado à exploração agrícola do País e tem sido uma importante alternativa para reduzir os riscos de degradação ambiental, sem alterar a produtividade das culturas. Neste sistema, os fertilizantes fosfatados são adicionados na superfície, sem revolvimento do solo, o que, aliado à deposição dos resíduos vegetais também na superfície, favorece sua ciclagem nessa camada do solo, diminuindo as perdas de P e determinando seu acúmulo na camada superficial (Muzilli, 1983). Nesta camada, sua sorção é menor (Guertal et al., 1991), causada pela saturação dos sítios de adsorção e pela diminuição da energia de ligação do fosfato com os colóides do solo, propiciando aumento do P em formas mais lábeis.
O fracionamento do P tem sido útil para detectar a ação antrópica na sua dinâmica nos solos. Em solos tropicais, as maiores proporções de P têm sido encontradas em extrações com NaOH (Araújo & Salcedo, 1997; Rheinheimer & Anghinoni, 2001), estando relacionadas com óxidos de ferro e alumínio, caulinita e matéria orgânica. Quando se adicionam altas doses de fosfatos, têm-se observado aumentos nas frações inorgânicas lábeis (extraídas com resina e NaHCO3), moderadamente lábeis (extraídas com NaOH) e, em algumas situações, também nas frações com baixa labilidade (Beck & Sanchez, 1994; Maroko et al., 1999). Os aumentos seguem os compartimentos preexistentes, dependendo sua distribuição da qualidade e da quantidade dos sítios de adsorção no solo (Rheinheimer, 2000). De acordo com Araújo & Salcedo (1997), as alterações preferenciais nas frações de P ocorrem nas formas inorgânicas.
Uma interpretação alternativa em relação às frações de P apresentadas foi proposta por Cross & Chlesinger (1995). Nessa proposta, são considerados dois compartimentos: o biológico (Po extraído por NaHCO3 + NaOH + ultra-som) e o geoquímico (Pi extraído pelos mesmos extratores + P residual). Essa separação foi mais sensível, segundo os autores, na detecção das transformações que ocorrem com o P na formação do solo. Ela pode também ser útil no estabelecimento da importância dessas formas de P como resultado da interferência antrópica nos sistemas, como o manejo do solo, a adição de fertilizantes minerais e a rotação de culturas.
O aumento na disponibilidade de P na superfície do solo no sistema plantio direto (SPD) pode resultar em maior transformação do Pi em Po. No entanto, em solos argilosos com altos teores de óxidos de ferro, pode ocorrer pouca modificação nos teores de Po (Rheinheimer, 2000) e de matéria orgânica (Bayer, 1996), mesmo com a adoção do SPD por vários anos, quando comparados a solos mais arenosos. O pequeno acúmulo do P ocorre como conseqüência da maior quantidade de sítios de adsorção, o que confere a característica de menor resiliência nos solos mais argilosos em relação aos mais arenosos (Seybold et al., 1999).
O presente trabalho teve como objetivo determinar as formas preferenciais de acumulação do P proveniente da adição de doses de fosfato solúvel em Latossolo Vermelho distroférrico sob plantio direto por cinco anos e meio.
MATERIAL E MÉTODOS
Foram utilizadas amostras de solo do experimento "Calibração de doses de fósforo em sistema plantio direto", conduzido pela Cooperativa Tritícola Santo Ângelo (COTRISA Santo Ângelo, RS) em convênio com a Fundação Centro de Experimentação e Pesquisa Fecotrigo (FUNDACEP), Cruz Alta (RS). O experimento foi instalado no inverno de 1994 em uma área que vinha sendo cultivada há longo tempo em preparo convencional, seguida de cultivo por três anos no SPD, num Latossolo Vermelho distroférrico típico argiloso (613 g kg-1 de argila), com 105 g kg-1 de óxidos de ferro (ditionito-citrato-bicarbonato). A correção da acidez do solo foi efetuada para elevar o pH do solo a 6,0 (CFS RS/SC, 1995) por ocasião da instalado do SPD.
Os tratamentos consistiram de um fatorial (5 x 5), com aplicação de 0, 30, 60, 90 e 120 kg ha-1 de P2O5 (superfosfato triplo) anualmente em faixas nas culturas de inverno, em uma direção, e de 0, 1/3, 2/3, 3/3 e 4/3 das doses recomendadas para as culturas de verão (CFS RS/SC, 1995), também em faixa, em direção perpendicular à anterior. Os 25 tratamentos foram arranjados em blocos ao acaso com parcelas subdivididas em faixa nas duas direções, com três repetições. Cultivaram-se: aveia forrageira (Avena strigosa), em 1994; soja (Glycine max), em 1994/95; nabo forrageiro (Rhaphanus raphanistrum), em 1995; milho (Zea mays), em 1995/96; aveia forrageira + nabo forrageiro, em 1996; milho, em 1996/97; aveia forrageira, em 1997; soja, em 1997/98; aveia forrageira + nabo forrageiro, em 1998; milho, em 1998/99; trigo (Triticum vulgare), em 1999, e soja, em 1999/00.
As adubações com N (uréia) e K (cloreto de potássio) foram as mesmas para todos os tratamentos em cada instalação das diferentes culturas e consistiram nas recomendações da CFS RS/SC (1995). Amostras de solo foram coletadas em janeiro de 2000 em nove das 25 parcelas com vistas em obter uma ampla faixa da adição acumulada de P.
Os tratamentos selecionados foram: doses de 0, 30, 60, 90 e 120 kg ha-1 de P2O5 aplicadas anualmente no inverno sem adubação de manutenção no verão; adubação de 1/3 e 2/3 da recomendação para as culturas de verão sobre 0 kg ha-1 no inverno e adubação de 2/3 e 4/3 da recomendação para as culturas de verão sobre 120 kg ha-1 de P2O5 no inverno. Isso representou, nos cinco anos e meio de cultivo, doses acumuladas de 0, 130, 180, 260, 360, 540, 720, 980 e 1.240 kg ha-1 de P2O5 (Quadro 1).
As amostras de solo foram retiradas na camada de 0-10 cm, em cada um dos três blocos, e foram compostas de quatro monólitos (subamostras) de solo (5 × 20 × 10 cm: espessura × largura × profundidade), coletados em minitrincheiras. O solo foi seco ao ar, peneirado em malha de 1 mm e acondicionado em potes plásticos.
O P total (Pt) foi determinado após extração com H2SO4 + H2O2 a quente (Rheinheimer, 2000) e o Po pelo método de ignição (Olsen & Sommer, 1982). O Pi foi obtido pela diferença entre o Pt e o Po. O teor de P microbiano (Pm) foi determinado após incubação do solo por 40 dias na temperatura de 25 oC, conforme Hedley et al. (1982). Este procedimento contempla a extração do Pi disponível por resina antes do processo fumigação-extração com NaHCO3 (Brookes et al., 1982)e ajuste na capacidade de adsorção de P pelo solo.
O P foi separado em seis frações inorgânicas e três orgânicas, numa extração seqüencial caracterizada pela labilidade decrescente, segundo método de Hedley et al. (1982), com modificações propostas por Condron et al. (1985).
Amostras de 1,500 g foram submetidas aos diferentes extratores da seguinte forma: inicialmente, foi extraído o P com resina trocadora de ânions em membranas (AR 103 QDP 434), saturadas com HCO3- 0,5 mol L-1 (P-resina), conforme Bissani et al. (2002); em seqüência, na mesma amostra, foi adicionado NaHCO3 0,5 mol L-1, extraindo-se o P inorgânico (Pi-NaHCO3) quimissorvido com baixa energia e o Po lábil (Po-NaHCO3); após, foi extraído o P solúvel em NaOH 0,1 mol L-1, quimissorvido com média energia (Pi NaOH 0,1 mol L-1) e o Po moderadamente lábil (Po NaOH 0,1 mol L-1); então, o P de fosfatos de cálcio e fortemente adsorvido foi extraído com HCl 1,0 mol L-1 (Pi-HCl); em seguida, adicionou-se NaOH 0,5 mol L-1, extraindo-se o P inorgânico quimissorvido com alta energia (Pi NaOH 0,5 mol L-1) e orgânico não-lábil (Po NaOH 0,5 mol L-1); e, finalmente, extraiu-se o P residual (P-res), por meio da digestão com H2SO4 + H2O2 + MgCl2 saturado (Brookes & Polson, 1982).
Todas as extrações foram realizadas em temperatura ambiente de 25 ºC com 16 h de duração. Alíquotas dos extratos alcalinos foram digeridas, conforme Rheinheimer (2000), para a obtenção do Pt de cada extração. O teor de Pi nos extratos alcalinos foi determinado pelo método de Dick & Tabatabai (1977), enquanto o de Pi, nos extratos ácidos e no digerido, pelo método de Murphy & Riley (1962). O teor de Po dos extratores alcalinos foi obtido pela diferença entre o teor de P depois e antes da digestão. O teor de carbono orgânico total (COT) foi determinado pelo método da combustão úmida, segundo Tedesco et al. (1995).
O P geoquímico foi considerado, de acordo com Cross & Schlesinger (1995), como a soma das frações inorgânicas de P (P-resina, Pi-NaHCO3, Pi-NaOH, Pi-HCl e P-residual), e o P biológico, como a soma das frações orgânicas de P (Po-NaHCO3, Po-NaOH e Pm).
Foi efetuada a análise da variância (P < 0,05), para verificar os efeitos dos tratamentos no acúmulo de P nas diferentes frações no solo. No caso de significância na análise da variância, foi aplicado o teste Tukey (P < 0,05), para discriminar a diferença entre mais de duas médias. Os valores das frações de fósforo foram relacionados com as doses de fosfato por meio de regressão (P < 0,05).
RESULTADOS E DISCUSSÃO
Fósforo total e orgânico
A adição anual de fósforo por cinco anos e meio resultou em aumento de 336 mg kg-1 no Pt do solo, na maior dose de fosfato aplicada (Quadro 2). Este aumento, considerando as doses de P2O5 aplicadas, foi quadrático (Quadro 2).
Os teores de Pi variaram de 545 mg kg-1, no tratamento sem adição, a 894 mg kg-1, no tratamento com a maior dose acumulada de P (Figura 1 e Quadro 1). Assim, à medida que aumentou a quantidade adicionada, aumentaram também os valores de Pi, com ajuste quadrático dos dados. Como os valores de Po diminuíram com as doses de fosfato adicionadas em quantitativos termos (Figura 1) e relativos (Quadro 2), os incrementos de Pt ocorreram exclusivamente na fração inorgânica, com os quais se correlacionaram de forma significativa (r = 0,84, P<0,05). Esses resultados concordam com os verificados por Araújo & Salcedo (1997), cuja adição de fosfato ao solo alterou preferencialmente as frações inorgânicas de P, como também verificado por Schmidt et al. (1996), em solos argilosos e com altas quantidades de óxidos de ferro e alumínio, como é o solo deste estudo.
A diminuição do Po com a adição de doses de P foi linear (Figura 1), de forma que sua participação no Pt decresceu de 29 %, no tratamento sem adição de fosfato, para 18 %, com a maior dose de P (Quadro 2). O aumento da quantidade de resíduos adicionados ao solo, considerando as doses de fosfato utilizadas, não foi suficiente para aumentar os teores de Po. Isto está em concordância com a inexistência de efeito no teor de carbono orgânico total (Quadro 2). Aumentos na fração orgânica, em decorrência do manejo do solo, foram somente observados em solos arenosos do sul do Brasil, tanto por Bayer (1996), para C orgânico, como por Rheinheimer (2000), para P orgânico.
Frações de fósforo
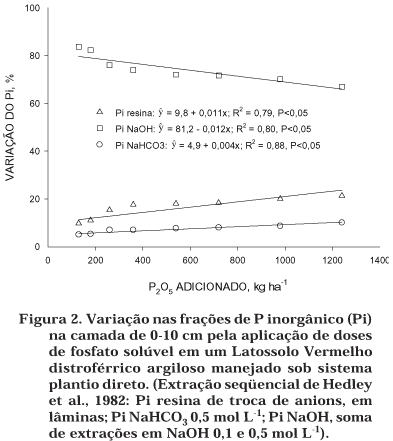
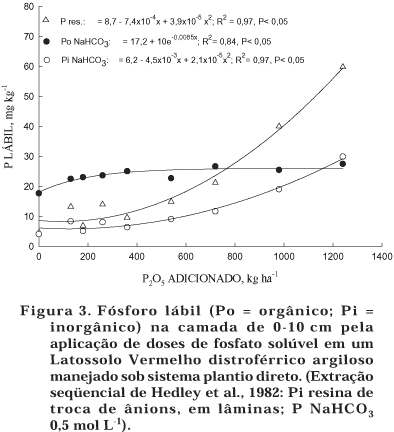
Embora a fração inorgânica lábil (Pi-resina + Pi-NaHCO3)tenha aumentado com as doses de P (Figuras 2 e 3), esse aumento representa apenas uma pequena parte (em torno de 22 % - Figura 2) do aumento dessa fração de Pi. Tanto o P-resina como o Pi-NaHCO3 aumentaram de forma quadrática com a adição do fertilizante fosfatado ao solo (Figura 3). A fração orgânica de P extraída com bicarbonato ficou em torno de 24 mg kg-1, enquanto o encontrado na fração inorgânica foi de somente 11 mg kg-1 (Quadro 3). Foi necessária a adição de 1.240 kg ha-1 de P2O5, para que o valor de Pi-NaHCO3 se equivalesse ao de Po-NaHCO3 (Figura 3). Esta fração foi pouco afetada pela adição do fertilizante fosfatado ao solo. A fração lábil, embora muito importante para o suprimento de P às plantas, representou uma fração muito pequena (55 mg kg-1 = 6 %) do total de P no solo (Quadro 3).
A fração Pi-NaOH 0,1 mol L-1 representou a maior parte do Pi acumulado no solo pela adição de P (Figura 4 e Quadro 3). Acúmulos foram também observados na fração Pi-NaOH 0,5 mol L-1 que, no entanto, apresentou um menor aumento no solo devido à adição de P (Figura 4). A soma das duas extrações com NaOH (fração moderadamente lábil) representou entre 65 e 80 % das variações do Pi do solo (Figura 2), por ser esta fração associada aos óxidos de Fe e Al. Acúmulos de P fração inorgânica moderadamente lábil, resultantes da adição de adubo fosfatado, têm sido relatados por outros pesquisadores (Magid et al., 1996; Schmidt et al., 1996; Friesen et al., 1997). Segundo Sadler & Stewart (1977), essa é a principal forma de acumulação do P dos fertilizantes em solos ácidos, especialmente nos solos com teores elevados de Fe e Al extraídos por ditionito, chegando, como no trabalho de Araújo & Salcedo (1977), a 50 % do total.
No entanto, as frações orgânicas de P extraídas com NaOH não foram alteradas pela adição de doses de fosfato (Figura 4). Mesmo assim, o Po-NaOH 0,1 mol L-1 foi a fração predominante (Figura 4) do Po extraível, com 148 mg kg-1 contra 121 mg kg-1 de Pi-NaOH 0,1 mol L-1, na média (Quadro 3). A fração orgânica moderadamente lábil (Po-NaOH) foi similar à respectiva fração inorgânica (Pi NaOH) (Quadro 3), embora os valores elevados de Pi-NaOH 0,1 mol L-1 obtidos pela adição de 980 kg ha-1 ou mais de P2O5 (Figura 4), demonstrando, a exemplo de Lindo et al. (1996), que essa fração também pode atuar como fonte de P. Os valores de Po encontrados nas extrações com NaHCO3 e NaOH 0,1 mol L-1 (Quadro 3) evidenciaram a importância do Po como fonte de P às plantas, principalmente em solos intemperizados e, ou, em sistemas com baixas adições de fertilizantes fosfatados (Walker & Syers, 1976; Tiessen et al., 1984).
Portanto, sistemas de produção que minimizem as perdas de Po do solo com o cultivo podem ser importantes para a manutenção da disponibilidade de P, garantindo a sua sustentabilidade. O P moderadamente lábil (Pi + Po) representa uma fração importante (398/904 = 44 %) do P total do solo (Quadro 3).
O P extraído com HCl constituiu uma pequena fração (29/904 = 3 % - Quadro 3) de P no solo e aumentou (função linear) com a quantidade de P adicionada, variando de 18,9 a 52,3 mg kg-1 (Figura 5). Esta fração, composta pelo Pi contido nos fosfatos de cálcio e fortemente adsorvido, é considerada pouco lábil (Tiessen et al., 1984). O aumento nessa fração com a adição de P pode ser atribuído à saturação superficial dos sítios de adsorção.
A fração residual mostrou-se elevada, em média, 422 mg kg-1, e não foi afetada pela adição do fertilizante fosfatado (Figura 5). Essa fração representa o P fortemente retido em minerais como hematita, goetita e gibsita (Smeck, 1985) e formas estáveis de Po.
Somente frações inorgânicas aumentaram com a adição de doses do fosfato ao solo. Isto indica que o P, adicionado via fertilizante, acumula-se nas formas inorgânicas preexistentes do solo. No entanto, a intensidade relativa das acumulações, tendo como base o tratamento sem adição de P, variou para cada fração do Pi (Figura 2). As frações mais lábeis, P-resina e Pi-NaHCO3, aumentaram sua importância relativa no acúmulo de P no solo à medida que a quantidade de fosfato adicionada aumentou. A variação das duas frações apresentou um aumento linear (P < 0,05). Por outro lado, a variação da soma das extrações sucessivas com NaOH decresceu, também de forma linear (P < 0,05), com o aumento da adição de P. Portanto, à medida que se adiciona P ao solo, aumenta a importância das frações mais lábeis, o que indica um processo de saturação dos sítios de adsorção.
Segundo Cross & Schlesinger (1995), o P do solo pode ser dividido em dois grandes compartimentos:geoquímico e biológico. Este representou somente em torno de 1/3 do compartimento geoquímico (Quadro 3). Enquanto o biológico não foi afetado, o geoquímico aumentou de forma quadrática ( = 720 + 0,035x + 0,000015x2; R2 = 0,95; P < 0,05) com as doses de fosfato aplicadas. Assim, a adição de fosfato solúvel em solos com altos teores de argila e óxidos de Fe e Al resultou em maior contribuição ao compartimento geoquímico, que predomina sobre o biológico. Todavia, a importância do Po no suprimento de P para as plantas pode ser alta, principalmente em sistemas com baixa adição de fertilizantes, que é evidenciada pelo fato de ser o conteúdo de Po no maior compartimento (moderadamente lábil) similar ao do Pi (Quadro 3).
= 720 + 0,035x + 0,000015x2; R2 = 0,95; P < 0,05) com as doses de fosfato aplicadas. Assim, a adição de fosfato solúvel em solos com altos teores de argila e óxidos de Fe e Al resultou em maior contribuição ao compartimento geoquímico, que predomina sobre o biológico. Todavia, a importância do Po no suprimento de P para as plantas pode ser alta, principalmente em sistemas com baixa adição de fertilizantes, que é evidenciada pelo fato de ser o conteúdo de Po no maior compartimento (moderadamente lábil) similar ao do Pi (Quadro 3).
CONCLUSÕES
1. O P orgânico diminuiu pela adição de fosfato solúvel e o aumento no teor total de P no solo, decorrente dessa adição, ocorreu no P inorgânico.
2. A fração de P inorgânico moderadamente lábil foi o maior dreno do P adicionado ao solo.
3. À medida que aumentou a quantidade de fosfato adicionada, aumentou a participação de frações mais lábeis de P inorgânico no teor total.
4. Da fração pouco lábil de P, inicialmente elevada no solo, somente a formada de fosfatos de cálcio e fortemente adsorvida aumentou com a adição de fosfato.
AGRADECIMENTOS
Ao pesquisador João Becker, da Cooperativa Tritícola de Santo Angelo COTRISA, pela atenção e concessão da área experimental para este trabalho.
LITERATURA CITADA
Financiado pelo CNPq e FINEP/PRONEX.
Recebido para publicação em outubro de 2001 e aprovado em junho de 2003.
- ARAÚJO, M.S.B. & SALCEDO, I.H. Formas preferenciais de acumulação de fósforo em solos cultivados com cana-de-açúcar na região Nordeste. R. Bras. Ci. Solo, 21:643-650, 1997.
- BAYER, C. Dinâmica da matéria orgânica em sistemas de manejo de solos. Porto Alegre, Universidade Federal do Rio Grande do Sul, 1996. 240p. (Tese de Doutorado)
- BECK, M.A. & SANCHEZ, P.A. Soil phosphorus fraction dynamics during 18 years of cultivation on a Typic Paleudult. Soil Sci. Soc. Am. J., 58:1424-1431, 1994.
- BISSANI, C.A.; TEDESCO, M.J.; CAMARGO, F.A.O.; MIOLA, G.L. & GIANELLO, C. Anion-exchange resins and iron oxide impregnated filter paper as plant available phosphorus indicator in soils. Comm. Soil Sci. Plant Anal., 33:1119-1129, 2002.
- BROOKES, P.C.; POWLSON, D.S. & JEKILSON, D.S. Measurement of microbial biomass phosphorus in soil. Soil Biol. Biochem., 14:319-329, 1982.
- COMISSÃO DE FERTILIDADE DO SOLO - CFS RS/SC. Recomendações de adubação e de calagem para os estados do Rio Grande do Sul e Santa Catarina. Passo Fundo, Sociedade Brasileira de Ciência do Solo, 1995. 224p.
- CONDRON, L.M.; GOH, K.M. & NEWMAN, R.H. Nature and distribution of soil phosphorus as revealed by sequential extraction method followed by 31P nuclear magnetic resonance analysis. J. Soil Sci., 36:199-207, 1985.
- CROSS, A.F. & SCHLESINGER, W.H. A literature review and evaluation of the Hedley fractionation: Applications to the biogeochemical cycle of soil phosphorus in natural ecosystems. Geoderma, 64:197-214, 1995.
- DICK, W.A. & TABATABAI, M.A. Determination of orthophosphate in aqueous solutions containing labile organic and inorganic phosphorus compounds. J. Environ. Qual., 6:82-85, 1977.
- FRIESEN, D.K.; RAO, I.M.; THOMAS, R.J.; OBERSON, A. & SANZ, J.I. Phosphorus acquisition and cycling in crop and pasture systems in low fertility tropical soils. Plant Soil, 196:289-294, 1997.
- GUERTAL, E.A.; ECKERT, D.J.; TRAINA, S.J. & LOGAN, T.J. Differential phosphorus retention in soil profiles under no-till crop production. Soil Sci. Soc. Am. J., 55:410-413, 1991.
- HEDLEY, M.J.; STEWART, J.W.B. & CHAUHAN, B.S. Changes in inorganic and organic soil phosphorus fractions induced by cultivation practices and by laboratory incubations. Method to measure microbial phosphate in soils. Soil Sci. Soc. Am. J., 46:970-976, 1982.
- LINDO, P.V.; TAYLOR, R.W.; ADRIANO, D.C. & SHUFORD, J.W. Fractionation of residual phosphorus in a highly weathered sludge-treated soil: organic phosphorus. Comm. Soil Sci. Plant Anal., 26:2639-2653, 1996.
- MAGID, J.; TIESSEN, H. & CONDRON, L.M. Dynamics of organic phosphorus in soils under natural and agricultural ecosystems. In: PICCOLO, A., ed. Humic substances in terrestrial ecosystems. Amsterdan, Elsevier, 1996. p.429-466.
- MAROKO, J.B.; BURESH, R.J. & SMITHSON, P.C. Soil phosphorus fractions in unfertilized fallow-maize systems on two tropical soils. Soil Sci. Soc. Am. J., 63:320-326, 1999.
- MURPHY, J. & RILEY, J.P. A modified single solution method for the determination of phosphate in natural waters. Anal. Chimica Acta, 27:31-36, 1962.
- MUZILLI, O. Influência do sistema plantio direto, comparado ao convencional, sobre a fertilidade da camada arável do solo. R. Bras. Ci. Solo, 7:95-100, 1983.
- NOVAIS, R.F.; SMYTH, T.J. & BARROS, N.F. A natureza não tem palito de fósforo! B. Inf. SBCS, 23:24-26, 1998.
- OLSEN, S.R. & SOMMER, L.E. Phosphorus. In: PAGE, A.L.; MILLER, R.H. & KEENEY, Q.R., eds. Methods of soil analysis, Part 2. Chemical and microbiological properties. 2.ed. Madison, American Society of Agronomy, 1982. p.403-430. (Agronomy Monograph, 9)
- RHEINHEIMER, D.S. Dinâmica do fósforo em sistemas de manejo de solos. Porto Alegre, Universidade Federal do Rio Grande do Sul, 2000. 210p. (Tese de Doutorado)
- RHEINHEIMER, D.S. & ANGHINONI, I. Distribuição do fósforo inorgânico em sistemas de manejo de solo. Pesq. Agropec. Bras., 36:151-160, 2001.
- SADLER, J.M. & STEWART, J.W.B. Labile residual fertilizer phosphorus in chernozemic soils. I. Solubility and quantity/intensity studies. Can. J. Soil Sci, 57:65-73, 1977.
- SEYBOLD, C.A.; HERRICK, J.E. & BREJDA, J.J. Soil resilience: A fundamental component of soil quality. Soil Sci., 16:224-234, 1999.
- SCHMIDT, J.P.; BUOL, S.W. & KAMPRATH, E.J. Soil phosphorus dynamics during seventeen years of continuous cultivation: fractionation analyses. Soil Sci. Soc. Am. J., 60:1168-1172, 1996.
- SMECK, N.E. Phosphorus dynamics in soil and landscapes. Geoderma, 36:185-199, 1985.
- TEDESCO, M.J.; GIANELLO, C.; BISSANI, C.A.;BOHNEN, H. & VOLKWEISS, S.J. Análises de solo, plantas e outros materiais, 2.ed. Porto Alegre, Universidade Federal do Rio Grande do Sul, 1995. 174p. (Boletim Técnico, 5)
- TIESSEN, H.; STEWART, W.B. & COLE, C.V. Pathways of phosphorus transformations in soils of differing pedogenesis. Soil Sci. Soc. Am. J., 48:853-858, 1984.
- WALKER, T.W. & SYERS, J.K. The fate of phosphorus during pedogenesis. Geoderma, 15:1-19, 1976.
Datas de Publicação
-
Publicação nesta coleção
05 Jan 2004 -
Data do Fascículo
Out 2003
Histórico
-
Recebido
Out 2001 -
Aceito
Jun 2003