Resumos
Realizou-se um experimento em casa de vegetação para avaliar a atuação do enxofre (S) inoculado com Acidithiobacillus na disponibilidade de fósforo (P) de fosfato natural (FN), em diferentes modos de aplicação do fertilizante, em um Espodossolo Ferrocárbico Órtico, do tabuleiro costeiro da Zona da Mata de Pernambuco, cultivado com jacatupé (Pachyrhizus erosus). As plantas foram inoculadas com rizóbio (NFB 747 e NFB 748) e adicionado tratamento-controle sem inoculação com rizóbio. Os tratamentos com P foram: (1) FN revestindo o enxofre inoculado com Acidithiobacillus (FN S*), (2) FN revestido com S e com Acidithiobacillus (S* FN), (3) mistura FN com S e com Acidithiobacillus (FN + S*), (4) mistura FN com S e sem Acidithiobacillus (FN + S), (5) superfosfato triplo (ST) e (6) sem aplicação de fósforo (P0). Os tratamentos foram aplicados: (a) na superfície, (b) em sulco 10 cm abaixo da semente, e (c) em sulco 10 cm abaixo e ao lado da semente. A biomassa nodular foi maior no tratamento (FN + S*) com melhor efeito quando aplicado ao lado e abaixo das sementes. O (FN + S*) também aumentou a altura das plantas, a biomassa da parte aérea e das túberas e o N total da parte aérea, especialmente quando aplicado 10 cm abaixo das sementes. O P total da parte aérea foi mais elevado com (S* FN) aplicado 10 cm abaixo das sementes. Os melhores teores de P no solo foram obtidos com (FN + S*) e (S* FN), com efeito mais evidente quando aplicados 10 cm abaixo das sementes.
biofertilizantes; fosfato reativo; Gafsa; localização do fertilizante
A greenhouse experiment was carried out to evaluate the effect of sulphur (S) inoculated with Acidithiobacillus on phosphorus (P) availability from natural phosphate (NP) using different fertilizer application methods on yam bean (Pachyrhizus erosus) grown in a "Tableland Forest" soil (Podzol Hydromorphic dystrophic) of the "Zona da Mata" in the State of Pernambuco, Brazil. Plants were inoculated with rhizobia strains (NFN 747 and NFB 748) and control treatments added without rhizobia inoculation. The P treatments were: (1) NP pelleted with S inoculated with Acidithiobacillus (NP S*); (2) S with Acidithiobacillus pelleted with NP (S* NP); (3) NP and S mixture inoculated with Acidithiobacillus (S* + NP); (4) NP and S mixture without Acidithiobacillus (NP + S); (5) triple superphosphate (TS) fertilization and (6) control treatment without phosphorus application (P0). The fertilizers were applied: a) on the surface; b) in the plant furrow 10 cm below the seeds; c) in the furrow 10 cm below and beside the seeds. Nodule dry matter was higher with (NP + S*), and best results were obtained when fertilizers were applied beside and above seeds. The treatment (FN + S*) increased plant height, dry biomass of nodules, tubers, and shoots, and the total N uptake, especially when applied 10 cm below seeds. Total P uptake was highest with (S* NP) applied 10 cm below seeds. The available soil P was highest in the treatments (NP + S*) and (NP + S) with most evident results when applied 10 cm below seeds.
biofertilizers; reactive phosphate; Gafsa; fertilizer placement
SEÇÃO III - BIOLOGIA DO SOLO
Atuação de Acidithiobacillus na solubilização de fosfato natural em solo de tabuleiro cultivado com jacatupé (Pachyrhizus erosus)
Effect of Acidithiobacillus on solubilization of natural phosphate in a coastal tableland soil under yam bean (Pachyrhizus erosus) crop
N. P. StamfordI; A. M. M. F. MouraII; K. S. SantosII; P. R. SantosIII
IProfessor Titular do Departamento de Agronomia, Universidade Federal Rural de Pernambuco UFRPE. Rua Dom Manoel de Medeiros s/n, Casa Forte, CEP 52061-060 Recife (PE). Bolsista do CNPq. E. mail: newtonps@fastmodem.com.br
IIMestranda em Agronomia, Ciência do Solo, UFRPE. E-mail: kassiasantos@bol.com.br
IIIGraduanda em Agronomia da UFRPE, Bolsista do PIBIC. E-mail: mandacaru@bol.com.br
RESUMO
Realizou-se um experimento em casa de vegetação para avaliar a atuação do enxofre (S) inoculado com Acidithiobacillus na disponibilidade de fósforo (P) de fosfato natural (FN), em diferentes modos de aplicação do fertilizante, em um Espodossolo Ferrocárbico Órtico, do tabuleiro costeiro da Zona da Mata de Pernambuco, cultivado com jacatupé (Pachyrhizus erosus). As plantas foram inoculadas com rizóbio (NFB 747 e NFB 748) e adicionado tratamento-controle sem inoculação com rizóbio. Os tratamentos com P foram: (1) FN revestindo o enxofre inoculado com Acidithiobacillus (FN S*), (2) FN revestido com S e com Acidithiobacillus (S* FN), (3) mistura FN com S e com Acidithiobacillus (FN + S*), (4) mistura FN com S e sem Acidithiobacillus (FN + S), (5) superfosfato triplo (ST) e (6) sem aplicação de fósforo (P0). Os tratamentos foram aplicados: (a) na superfície, (b) em sulco 10 cm abaixo da semente, e (c) em sulco 10 cm abaixo e ao lado da semente. A biomassa nodular foi maior no tratamento (FN + S*) com melhor efeito quando aplicado ao lado e abaixo das sementes. O (FN + S*) também aumentou a altura das plantas, a biomassa da parte aérea e das túberas e o N total da parte aérea, especialmente quando aplicado 10 cm abaixo das sementes. O P total da parte aérea foi mais elevado com (S* FN) aplicado 10 cm abaixo das sementes. Os melhores teores de P no solo foram obtidos com (FN + S*) e (S* FN), com efeito mais evidente quando aplicados 10 cm abaixo das sementes.
Termos de indexação: biofertilizantes, fosfato reativo, Gafsa, localização do fertilizante.
SUMMARY
A greenhouse experiment was carried out to evaluate the effect of sulphur (S) inoculated with Acidithiobacillus on phosphorus (P) availability from natural phosphate (NP) using different fertilizer application methods on yam bean (Pachyrhizus erosus) grown in a "Tableland Forest" soil (Podzol Hydromorphic dystrophic) of the "Zona da Mata" in the State of Pernambuco, Brazil. Plants were inoculated with rhizobia strains (NFN 747 and NFB 748) and control treatments added without rhizobia inoculation. The P treatments were: (1) NP pelleted with S inoculated with Acidithiobacillus (NP S*); (2) S with Acidithiobacillus pelleted with NP (S* NP); (3) NP and S mixture inoculated with Acidithiobacillus (S* + NP); (4) NP and S mixture without Acidithiobacillus (NP + S); (5) triple superphosphate (TS) fertilization and (6) control treatment without phosphorus application (P0). The fertilizers were applied: a) on the surface; b) in the plant furrow 10 cm below the seeds; c) in the furrow 10 cm below and beside the seeds. Nodule dry matter was higher with (NP + S*), and best results were obtained when fertilizers were applied beside and above seeds. The treatment (FN + S*) increased plant height, dry biomass of nodules, tubers, and shoots, and the total N uptake, especially when applied 10 cm below seeds. Total P uptake was highest with (S* NP) applied 10 cm below seeds. The available soil P was highest in the treatments (NP + S*) and (NP + S) with most evident results when applied 10 cm below seeds.
Index terms: biofertilizers, reactive phosphate, Gafsa, fertilizer placement.
INTRODUÇÃO
O jacatupé (Pachyrhizus erosus L. Urban) é uma leguminosa originária da região amazônica e do México, produtora de túberas ricas em amido (60 t ha-1) e de grãos (4 t ha-1) com elevado teor em óleo e proteína, apresentando aminograma similar ao da soja (Sales et al., 1990), e portanto, com potencial na alimentação humana e animal, bem como para uso como adubo verde (Sorensen, 1996). Trata-se de uma leguminosa com características de rusticidade, com bom desenvolvimento em solos de baixa fertilidade, arenosos e argilosos. Trabalhos para obtenção de cultivares para condições específicas, tais como: resistência à estiagem prolongada e à salinidade, acidez, alta temperatura, dentre outras, ainda não foram desenvolvidos.
Desde o início da década de 1990, a eficiência da inoculação com rizóbio e a resposta à fertilização por jacatupé vêm sendo pesquisadas na Universidade Federal Rural de Pernambuco pelo Núcleo de Fixação Biológica do N2 nos Trópicos. A inoculação do jacatupé com estirpes de rizóbio mostra-se bastante efetiva, sendo o N proveniente da fixação biológica suficiente para suprir todo o N necessário para produção satisfatória, especialmente em solos com baixo nível de rizóbio nativo (Cruz et al., 1997).
Para uma eficiente fixação do N2, faz-se necessária a aplicação de nutrientes, sendo especialmente importante a adição de P, considerando as várias funções exercidas por este nutriente no processo simbiótico, particularmente na nodulação, na atividade da nitrogenase e na acumulação de N na planta, como comprovado por Cruz et al. (1997), utilizando fertilizantes fosfatados solúveis e reativos na cultura do jacatupé.
A matéria-prima básica para a fabricação de fertilizantes fosfatados é a rocha fosfática, sendo mais comum o uso de apatitas. Trata-se de um recurso natural não-renovável e que não tem sucedâneo para as plantas, havendo necessidade de estabelecer estratégias para o uso eficiente e econômico das rochas fosfáticas (Goedert & Sousa, 1986).
Para a produção de fertilizantes solúveis, ocorre apreciável consumo de energia, e, no processamento com ácido sulfúrico ou ácido fosfórico, é necessária mão-de-obra especializada. Também, deve ser levado em consideração que o uso de fertilizantes é importante para o desenvolvimento e produção das culturas, e os altos custos dos produtos solúveis contribuem diretamente para reduzir a sua aplicação por agricultores de baixa renda (Sanchez, 2002).
Fontes minerais não ocorrem na natureza em forma diretamente disponível para as plantas e devem ser modificadas por processos físicos, químicos ou biológicos para serem fontes efetivas de nutrientes para as culturas (Straatem van, 2002). A utilização direta de fosfatos naturais é muito restrita; por causa da baixa reatividade, os fosfatos são usados em forma de pó ou em misturas com os fertilizantes solúveis, visando ao aproveitamento, graças à sua lenta solubilização no solo (Oliveira et al., 1977).
O uso de microrganismos com maior habilidade em solubilizar fosfatos de rocha vem recebendo a atenção dos pesquisadores, principalmente pela possibilidade de seu emprego em programas de interação com microrganismos fixadores de N2 (Nahas, 1999). A fixação biológica do N2 deverá apresentar interação com bactérias solubilizadoras de fosfatos, principalmente do gênero Acidithiobacillus, que são capazes de produzir H2SO4 (Garcia Júnior, 1992), que podem atuar, com intensidade, na disponibilidade de P de fosfatos naturais. Espécies de Acidithiobacillus ocorrem naturalmente nos solos agrícolas; entretanto, alguns poucos trabalhos realizados sem a adição da bactéria específica mostraram que a sua atuação na solubilidade de fosfatos naturais é lenta e com resultados bastante variáveis. Por outro lado, a adição da bactéria em concentração conhecida e aplicada diretamente no S deverá promover ação mais rápida e eficiente, favorecendo o processo simbiótico e o desenvolvimentos das plantas (Santos, 2002).
Alguns fatores podem influenciar a efetividade de fosfatos naturais aplicados no solo, tais como: mineralogia do fosfato natural, reatividade do fosfato, tamanho do grão e área superficial, atributos físicos e químicos do solo, especialmente pH, capacidade do solo na manutenção de umidade, estado nutricional da planta, principalmente quanto a Ca e P, capacidade de fixação de P do solo, espécie cultivada e seu requerimento nutricional, práticas de manejo, incluindo método e tempo de aplicação, e calagem do solo (Straatem van, 2002).
O ácido sulfúrico produzido na reação microbiológica pode atuar no fosfato natural disponibilizando P, bem como no solo, promovendo redução no pH (Stamford et al., 2002). Assim, faz-se necessário avaliar a atuação do S inoculado com Acidithiobacillus na disponibilidade de fosfato natural, bem como verificar o efeito da localização do P aplicado em relação à semente (Stamford et al., 1990).
Neste sentido, a presente pesquisa objetivou avaliar a atuação do S inoculado com Acidithiobacillus na nodulação, no desenvolvimento e acumulação de N e P por jacatupé e na solubilização de fosfato natural em um solo com baixo teor de P disponível. Procurou-se observar a interação dos produtos usados para adição de P com as estirpes de rizóbio, bem como verificar a melhor forma de aplicação do fosfato natural (Gafsa) com adição de S inoculado com Acidithiobacillus.
MATERIAIS E MÉTODOS
Realizou-se um experimento em casa de vegetação com um solo de tabuleiro costeiro da Zona da Mata de Pernambuco, com baixo teor de P disponível, em vasos de polietileno com capacidade para 5 L. O experimento foi efetuado em esquema fatorial (6 x 3), no delineamento em blocos ao acaso, sendo seis tratamentos com P e três modos de aplicação do fertilizante em relação às sementes, com três repetições.
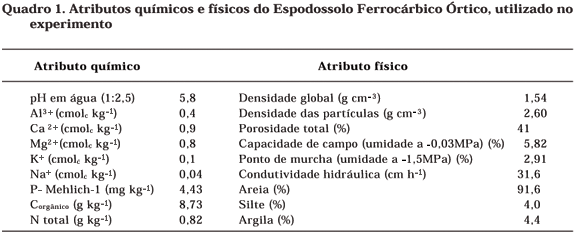
O solo utilizado foi classificado como Espodossolo Ferrocárbico Órtico (textura arenosa), de acordo com o Sistema Brasileiro de Classificação de Solos (EMBRAPA, 1999). Foram coletadas amostras na camada arável (0-20 cm), na Estação Experimental da Empresa Pernambucana de Pesquisas Agropecuária IPA, Itapirema (PE). Os resultados da análise de alguns atributos químicos e físicos encontram-se no quadro 1.
Usou-se o fosfato natural de Gafsa (FN), com os seguintes tratamentos: (1) FN revestindo o enxofre inoculado com Acidithiobacillus (FN S*); (2) FN revestido pelo enxofre inoculado com Acidithiobacillus (S* FN); (3) Mistura de FN com enxofre inoculado com Acidithiobacillus (FN + S*); (4) Mistura de FN com enxofre sem Acidithiobacillus (FN + S); (5) Adubação com superfosfato triplo (ST), e (6) Tratamento sem fertilização fosfatada (P0). Os tratamentos foram aplicados: (a) na superfície, (b) em sulco 10 cm abaixo da semente, e (c) em sulco 10 cm abaixo e ao lado da semente, da forma descrita por Stamford et al. (1990).
De acordo com o tratamento, o revestimento foi feito em pérolas de isopor, usando cola solúvel em água como adesivo. Imediatamente após a secagem da primeira camada, adicionou-se o material para revestir, empregando-se o mesmo adesivo. Em todos os tratamentos fosfatados, usou-se a dose equivalente a 100 kg ha-1 de P, quantidade máxima recomendada para jacatupé em solo de tabuleiro (Stamford et al., 1999). O S foi adicionado na dose equivalente a 300 kg ha-1 de S (enxofre elementar), com base nos resultados obtidos por Stamford et al. (2002).
Na inoculação com rizóbio, usou-se a mistura das estirpes NFB 747 e NFB 748, selecionadas para jacatupé em ensaios prévios, em condições de acidez e temperatura elevadas (Stamford et al., 1995). O inoculante foi preparado em meio YM (Vincent, 1970), usando-se erlenmeyers mantidos em agitação (100 gpm, durante cinco dias). Aplicou-se 1 mL da cultura por planta. Foram adicionados dois tratamentos sem inoculante (com superfosfato triplo e sem P), com três repetições, para fins comparativos.
A bactéria Acidithiobacillus foi cultivada em meio específico 9K (Garcia Júnior, 1991), em erlenmeyers de 125 mL, colocados em agitador rotativo a 150 gpm, por cinco dias, a 28-30 ºC. Na inoculação do S elementar, usou-se 1 mL g-1. Para evitar acidificação do solo por efeito do ácido sulfúrico produzido na reação microbiológica do Acidithiobacillus com o S, realizou-se a calagem usando calcário comercial (Megaó), com PRNT equivalente a 95 %, com incubação durante 30 dias. O pH, após o período de incubação, estabilizou-se em 6,2 (média de seis repetições).
Em virtude da significativa influência da umidade na disponibilidade e distribuição de P nas plantas, como comprovado por Ruiz et al. (1990), foi realizada irrigação duas vezes por dia, (início da manhã e final da tarde), mantendo-se a umidade próxima à capacidade de campo durante o cultivo por 90 dias após a emergência (DAE).
Com a finalidade de evitar deficiência de K e micronutrientes mais Ca, S e Mg, foi feita uma adubação básica com KCl, na dose equivalente a 100 kg ha-1, e, para micronutrientes, adicionou-se a solução de Norris (1964) para leguminosas (2 mL kg-1 de solo). O KCl foi aplicado da mesma forma da fertilização com P (na superfície, 10 cm abaixo da semente, e 10 cm abaixo e ao lado da semente).
Após a colheita, de cada vaso foi retirada uma amostra de 20 g de solo, para determinação do pH e do P extraído por Mehlich-1 (EMBRAPA, 1997), por ser este o método utilizado para determinação de P no solo na maioria dos laboratórios no Brasil. Nas plantas, determinaram-se: altura, biomassa seca dos nódulos, da parte aérea e das túberas, N total acumulado na parte aérea (Kjeldhal semimicro) em autoanalisador (Kjeltec 1030) e P total na planta, de acordo com Malavolta et al. (1989). Procedeu-se à análise de variância, utilizando o Programa Sanest (Zonta, 1982), e as médias foram comparadas pelo teste de Tukey a 5 %.
RESULTADOS E DISCUSSÃO
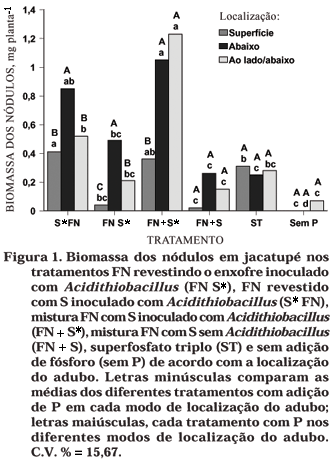
Na nodulação (biomassa seca dos nódulos), foram observados os melhores resultados, quando usado o fosfato natural em mistura com o S inoculado com Acidithiobacillus (FN + S*) e com fosfato natural revestido com S inoculado com Acidithiobacillus (S* FN) (Figura 1). Para os tratamentos (S* FN) e (FN S*), os efeitos foram mais evidenciados com a aplicação do biofertilizante abaixo das sementes. Nas plantas não inoculadas com rizóbio e sem adição de P, não houve formação de nódulos (Quadro 2), enquanto, no tratamento sem P e sem adição de rizóbio, foram formados poucos nódulos (Figura 1). Os resultados obtidos na nodulação evidenciam que, no solo usado, não ocorre rizóbio específico para jacatupé, sendo importante a inoculação com estirpes de rizóbio efetivos.
O crescimento do jacatupé, avaliado pela altura, biomassa da parte aérea e das túberas, é apresentado nas figuras 2 a 4. De maneira geral, observa-se que houve efeito dos tratamentos com adição de P e dos modos de aplicação. Os melhores resultados foram obtidos com aplicação de fosfato natural em mistura com S inoculado com Acidithiobacillus (FN + S*), seguido do tratamento com fosfato natural revestido com o S inoculado com Acidithiobacillus (S* FN), e com fosfato natural revestindo o S inoculado com Acidithiobacillus (FN S*), quando aplicados 10 cm abaixo das sementes e 10 cm abaixo e ao lado das sementes.
A maior produção de biomassa seca da parte aérea foi obtida com a mistura fosfato natural e S inoculado com Acidithiobacillus (FN + S*), especialmente quando aplicado abaixo e ao lado das sementes (Figura 3). Stamford et al. (1990), avaliando o efeito de modos de aplicação de P e K (fertilizantes solúveis) na cultura do caupi, em solo ácido (Latossolo Vermelho-Amarelo distrófico) do estado de Pernambuco, e Klepker & Anghinoni (1995), trabalhando com milho fertilizado com fosfato solúvel, também verificaram melhor resposta na produção de matéria seca, quando realizada a aplicação dos fertilizantes abaixo das sementes. Neste modo de localização do fertilizante, os resultados obtidos com adição de fosfato natural (FN) com S inoculado com Acidithiobacillus (S*) foram superiores aos do superfosfato triplo (ST) e do fosfato natural com S sem inoculação com Acidithiobacillus (FN + S). Ernani et al. (2001) relataram que, na presença de calcário (pH 5,7), não houve diferença entre os modos de aplicação de fosfatos, sendo obtidos os melhores rendimentos de milho com fontes solúveis, comparando com o fosfato natural de Arad.
O fosfato natural em mistura (FN + S*) ou revestido pelo S inoculado com Acidithiobacillus (S* FN) provavelmente promoveu maior reação da bactéria oxidante do S, resultando em maior quantidade de H2SO4, dependendo da maior aeração e umidade (Garcia Júnior, 1992). Por outro lado, no tratamento com o fosfato natural revestindo o S (FN S*), a reação microbiológica deve ter sido dificultada pela existência da camada com fosfato natural promovendo redução na aeração e na umidade, tendo em vista o uso de cola no revestimento do S com o fosfato natural.
Na biomassa das túberas (Figura 4), houve efeito da adição de P; entretanto, verificou-se maior resposta com S inoculado com Acidithiobacillus revestindo o fosfato natural (S* FN), quando aplicado na superfície, diferindo (P < 0,05) das demais fontes. A mistura do fosfato natural com S inoculado com Acidithiobacillus (FN + S*), o fosfato natural revestido pelo S com Acidithiobacillus (FN S*) e o superfosfato triplo (ST) também mostraram os melhores resultados, quando aplicados 10 cm abaixo ou abaixo e ao lado das sementes. As menores produções nos tratamentos com aplicação de fosfato natural revestido pelo S inoculado com Acidithiobacillus (FN S*) devem ter sido por efeito do revestimento do S pelo fosfato natural, por reduzir a atuação da bactéria na produção de ácido sulfúrico. Por outro lado, deve ser considerado que as túberas ainda estavam pouco desenvolvidas e, portanto, os resultados observados neste período podem sofrer modificações.
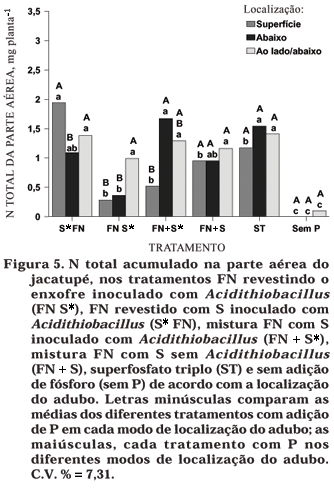
No N total acumulado (Figura 5), os melhores resultados foram obtidos quando usados os tratamentos com fosfato natural em mistura com S inoculado com Acidithiobacillus (FN + S*) com aplicação abaixo e, abaixo e ao lado das sementes e para o S inoculado com Acidithiobacillus revestindo o fosfato natural (S* FN), quando aplicado o fertilizante abaixo da semente. É provável que, nesses tratamentos, tenha ocorrido maior produção de H2SO4, tendo em vista o efeito da aeração e da umidade, decorrente do contato direto com o solo.
Para P total acumulado, o melhor resultado foi obtido com o tratamento com S inoculado com Acidithiobacillus revestindo o fosfato natural (S* FN) aplicado 10 cm abaixo da semente. O superfosfato triplo (ST) e o fosfato natural em mistura com S inoculado com Acidithiobacillus (FN + S*) também mostraram resposta do tratamento com P, sem efeito do modo de aplicação do tratamento.
Lombardi (1981) também verificou efeito do fosfato Alvorada com adição de S inoculado com Acidithiobacillus na acumulação de P total e no desenvolvimento do capim-colonião. As bactérias nativas do solo promoveram atuação tão efetiva quanto o tratamento com adição de Acidithiobacillus; entretanto, no experimento desenvolvido por esse pesquisador, os coeficientes de variação obtidos no experimento foram bastante elevados. Santos (2002) também observou efeito positivo do fosfato natural com adição de S inoculado com Acidithiobacillus no P total acumulado na parte aérea e no desenvolvimento de sabiá (Mimosa caesalpiniaefolia), obtendo resultados superiores aos do fertilizante solúvel (superfosfato triplo) e aos do tratamento com adição de fosfato natural e S sem inoculação com Acidithiobacillus.
A disponibilidade de P no solo foi determinada pela extração pelo método de Mehlich-1, após os noventa dias de cultivo (Figura 7). De maneira geral, observou-se efeito (P < 0,05) dos tratamentos com aplicação de P, em comparação com o tratamento sem fertilização (sem P). O P no solo foi mais elevado no tratamento com fosfato natural em mistura com o S inoculado com Acidithiobacillus (FN + S*) aplicado 10 cm abaixo da semente. É interessante observar que esse tratamento esteve entre os melhores resultados para todos os tratamentos com adição de P.
Notou-se que Acidithiobacillus do solo, ao final do período de cultivo, passou a atuar no S aplicado, tendo em vista que, no tratamento com adição de enxofre sem inoculação com Acidithiobacillus, houve boa disponibilidade de P, superior à aplicação de superfosfato triplo que apresentou menores valores de P disponível (Mehlich). Para o tratamento com fosfato natural com S inoculado com Acidithiobacillus (FN + S*) e (S*FN), provavelmente deverá ocorrer maior efeito residual, tendo em vista que esses tratamentos apresentaram elevados valores de P disponível no solo, após o primeiro cultivo com jacatupé.
Santos (2002), usando o mesmo solo do presente trabalho, verificou que o fosfato natural inoculado com Acidithiobacillus aumentou o P disponível do solo avaliado por Mehlich-1, Mehlich-3 e Bray-1 e promoveu maior desenvolvimento de sabiá (M. caesalpiniaefolia).
Verificou-se variação de pH 6,2 para pH 4,8 de acordo com os tratamentos com adição de fósforo com maior efeito, quando se usou a mistura fosfato natural e enxofre inoculado com Acidithiobacillus (FN + S*) e sem inoculação com Acidithiobacillus (FN + S) (Figura 8). Santos (2000) utilizou tratamentos com fosfato natural revestindo o S com Acidithiobacillus e, neste caso, não observou efeito de acidificação do solo, tendo em vista que o ácido sulfúrico produzido provavelmente atuou mais internamente disponibilizando P do fosfato natural sem promover redução no pH do solo.
O pH do solo foi afetado pelos tratamentos fosfatados, sem prejuízo no desenvolvimento das plantas. Estes resultados são concordantes com os obtidos por Ernani et al. (2001), quando aplicaram calcário em solo ácido e com baixo teor de P. É possível que a redução do pH observada nos tratamentos com adição de S inoculado com Acidithiobacillus possa ter influenciado a maior disponibilidade de P (Mehlich-1) e acidificação do solo. He et al. (1996) consideraram o efeito da acidez como fator de grande importância na solubilidade de fosfatos naturais. Stamford et al. (2002), usando S inoculado com Acidithiobacillus na recuperação de solos salinos sódicos, observaram que a produção de H2SO4 continua a ocorrer até o consumo total do S adicionado, chegando a promover a acidificação do solo com redução do pH inicial 8,2 para pH 4,5 com adição de 1,8 t ha-1 de S.
Os resultados evidenciam a possibilidade do uso de biofertilizante produzido a partir de fosfato natural com adição de S inoculado com Acidithiobacillus como fonte alternativa de substituição a fertilizantes fosfatados solúveis, encontrando apoio na recomendação de Raij (1986), que considerou possível o uso de fontes alternativas de P quando obtidos rendimentos mínimos de 80 a 90 % do apresentado pela fonte solúvel.
CONCLUSÕES
1. Jacatupé, cultivado em solo com baixo teor de P disponível, requer aplicação de inoculante com rizóbio eficiente, para promover bom crescimento da cultura.
2. O fosfato natural em mistura (FN + S*) ou revestido pelo S inoculado com Acidithiobacillus (FN S*) incrementa o crescimento e a acumulação de N na parte aérea, com maior efeito quando aplicado abaixo das sementes.
3. Os melhores resultados na acumulação de P na parte aérea do jacatupé foram obtidos com fosfato natural revestido com S inoculado com Acidithiobacillus, com maior evidencia quando aplicado 10 cm abaixo da semente.
4. O fosfato natural em mistura com S inoculado com Acidithiobacillus aumenta a disponibilidade de P e reduz o pH do solo.
AGRADECIMENTOS
Os autores agradecem ao Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq), pelas bolsas concedidas, e à FACEPE (Fundação de Apoio à Ciência e Tecnologia do Estado de Pernambuco), pelo auxílio para a realização da pesquisa.
LITERATURA CITADA
Recebido para publicação em junho de 2002 e aprovado em novembro de 2003.
- CRUZ, G.N.; STAMFORD, N.P.; SILVA, J.A.A. & CHAMBER-PEREZ, C. Effects of inoculation with Bradyrhizobium and urea application on N2 fixation and growth of yam bean. Trop. Grassl., 33:23-27, 1997.
- EMPRESA BRASILEIRA DE PESQUISA AGROPECUÁRIA - EMBRAPA. Centro Nacional de Pesquisa de Solos. Brasília, Sistema Brasileiro de Classificação dos Solos, 1999. 412p.
- EMPRESA BRASILEIRA DE PESQUISA AGROPECUÁRIA - EMBRAPA. Centro Nacional de Pesquisa de Solos. Manual de métodos de análise de solo. 2ª ed. Rio de Janeiro, 1997. 212p.
- ERNANI, P.R.; STECKLING, C. & BAYER, C. Características químicas de solo e rendimento de massa seca de milho em função do método de aplicação de fosfatos, em dois níveis de acidez. R. Bras. Ci. Solo, 25:939-946, 2001.
- GARCIA JÚNIOR, O. Isolation and characterization of Acidithiobacillus thiooxidans ands Acidithiobacillus ferrooxidans from mineral mines. R. Bras. Microbiol., 20:1-6, 1991.
- GARCIA JÚNIOR, O. O enxofre e suas transformações microbianas. In: CARDOSO, E.; SAITO, M.T. & NEVES, M.C.P., eds. Microbiologia do solo. Campinas, Sociedade Brasileira de Ciência do Solo, 1992. p.243-255.
- GOEDERT, W.J. & SOUSA, D.M.G. Avaliação preliminar de fosfato com acidulação parcial. R. Bras. Ci. Solo, 10:75-80, 1986.
- HE, Z.L.; BALIGAR, V.C.; MARTENS, D.C.; RITCHEY, K.D. & KEMPER, W.D. Factors affecting phosphate rock dissolution in acid soil amended with liming materials and cellulose. Soil Sci. Soc. Am. J., 60:1596-1601, 1996.
- KLEPKER, D. & ANGHINONI, I. Crescimento radicular e aéreo do milho em vasos, em função do nível de fósforo no solo e da localização do adubo fosfatado. R. Bras. Ci. Solo, 19:403-408, 1995.
- LOMBARDI, M.L.C.O. Dissolução de três fosfatos naturais através da atividade microbiológica do enxofre. Piracicaba, Escola Superior de Agricultura "Luiz de Queiroz". 1981. 62p. (Tese de Mestrado)
- MALAVOLTA, E.; VITTI, G.C. & OLIVEIRA, S.A. Avaliação do estado nutricional das plantas. Principios e aplicação. Piracicaba, Associação Brasileira para Pesquisa da Potassa e do Fosfato. 1989. 201p.
- NAHAS, E. Solubilização microbiana de fosfatos e de outros elementos. In: SIQUEIRA, J.O.; MOREIRA, F.M.S.; LOPES, A.S.; GUILHERME, L.R.G.; FAQUIN, V.; FURTINI NETO, A.E. & CARVALHO, J.G., eds. Interrelação fertilidade, biologia do solo e nutrição de plantas. Lavras, Universidade Federal de Lavras, 1999. p.467-486.
- NORRIS, D.A. Techniques used in works with Rhizobium In: Some concepts and methods in sub-tropical pasture research. Camberra, Commonwealth Bureau and Field Crops, 1964. p.196-198.
- OLIVEIRA, M.C.C.; LOPES, E.S.; SILVA, M.T.R. & NAGAI, R. Influência de oxidação microbiológica do enxofre na solubilização de apatita de Araxá. R. Bras. Ci. Solo, 1:24-28, 1977.
- RAIJ, B. van. Condições mínimas de eficiência para fosfatos alternativos ao superfosfato. R. Bras. Ci. Solo, 10:235-239, 1986.
- RUIZ, H.A.; FERNANDES, B.; NOVAIS, R.F. & ALVAREZ V., V.H. Teor, acúmulo e distribuição de fósforo em plantas de soja em relação ao conteúdo de água do solo. R. Bras. Ci. Solo, 14:181-185, 1990.
- SALES, A.M.; BALDINI, V.S.S. & CUNHA, M.F. Perfil eletroforético e composição de aminoácidos de sementes de jacatupé (Pachyrrhizus tuberosus, Spreg). Ci. Tecnol. Alimen., 10:87-108,1990.
- SANCHEZ, P.A. Soil fertility and hunger in Africa. Science, 295:2019-2020, 2002.
- SANTOS, K.S. Atuação de fosfato natural com adição de enxofre com Acidithiobacillus na solubilização de fósforo e no desenvolvimento de sabiá (Mimosa caesalpiniaefolia) em solo de tabuleiro. Recife, Universidade Federal Rural de Pernambuco, 2002. 68p. (Tese de Mestrado)
- SORENSEN, M. Yam Bean.: Promoting the conservation and use of underutilized and neglected crops, 2., Rome, International Plant Genetic Resource Institute, 1996. 141p.
- STAMFORD, N.P.; MEDEIROS, R. & MESQUITA, J.C.P. Avaliação de estirpes de Bradyrhizobium para jacatupé em regime de temperatura elevada. R. Bras. Ci. Solo, 9:45-54, 1995.
- STAMFORD, N.P.; SANTOS, C.E.R.; MEDEIROS, R. & FREITAS, A.D.S. Efeito da fertilização com fósforo, potássio e magnésio, em jacatupé infectado com rizóbio em um Latossolo álico. Pesq. Agropec. Bras., 34:1831-1838, 1999.
- STAMFORD, N.P.; SANTOS, D.R. & LOPES, A.J.R. Rendimento e teor de nutrientes por cultivares de caupi em Latossolo Vermelho-Amarelo com diferentes modos de aplicação do fertilizante R. Bras. Ci. Solo, 14:57-61, 1990.
- STAMFORD, N.P.; SILVA, J.A.; FREITAS, A.D.S. & ARAÚJO FILHO, J.T. Effect of sulphur inoculated with Acidithiobacillus in a saline soil grown with leucena and mimosa tree legumes. Biores. Technol., 81:53-59, 2002.
- STRAATEM, P. van. Rocks for crops: Agrominerals of sub-Saharan Africa. Nairobi, ICRAF, 2002. 338p.
- VINCENT, J.M. A manual for the practical study of root-nodule bacteria. Oxford, 1970. 164p.
- ZONTA, E.P.; MACHADO, A.A. & SILVEIRA JÚNIOR, P. Sistema de análise estatística para microcomputadores (SANEST). Pelotas, Universidade Federal de Pelotas, 1982. 151p.
Datas de Publicação
-
Publicação nesta coleção
21 Jun 2004 -
Data do Fascículo
Fev 2004
Histórico
-
Aceito
Nov 2003 -
Recebido
Jun 2002