Resumos
A presença de ligantes orgânicos na rizosfera tem importante papel no processo de solubilização de metais pesados em solos tratados com lodo de esgoto. Ácidos orgânicos de baixo peso molecular exsudados por raízes e, ou, liberados por microrganismos são considerados agentes mobilizadores desses metais. No presente estudo, determinou-se a cinética de solubilização de Cu, Cr, Ni e Zn em solos tratados com lodo de esgoto, utilizando solução com mistura de quatro ácidos orgânicos (acético, cítrico, lático e oxálico) preparada para obter concentração final de 0,05 e 0,10 mol L-1. A extração foi feita segundo o método de "batch". A solução 0,10 mol L-1 de ácidos orgânicos extraiu maiores quantidades de Cu, Cr, Ni e Zn do que a solução 0,05 mol L¹. A cinética de solubilização apresentou duas fases: uma inicial, com rápida liberação dos metais, seguida de outra mais lenta, tendendo ao equilíbrio. As constantes de velocidade de solubilização mais altas foram observadas para Ni e Zn, seguidos de Cu e Cr. Os valores para o reservatório lábil variaram entre 2 e 15 % do total de cada metal pesado estudado. A porcentagem que este reservatório representou, em relação ao total, obedeceu à ordem: Zn > Cu <FONT FACE=Symbol>@</FONT> Ni > Cr.
biossólido; Cr; Cu; Ni; Zn; fitodisponibilidade
The presence of organic ligands in the rhizosphere plays an important role in heavy metal solubilization in soils treated with sewage sludge. Low molecular weight organic acids exuded by roots and/or released by microorganisms are considered mobilizing agents of these metals. The present study determined Cd, Cu, Cr, Ni, and Zn solubilization kinetics in sewage sludge-treated soils using a mixture of four organic acids (acetic, citric, lactic, and oxalic) in 0.05 and 0.10 mol L-1 solutions. Based on the batch extraction method the 0.10 mol L-1 solution extracted greater quantities of Cu, Cr, Ni and Zn. Two phases of solubilization kinetics were observed: an initial one of fast metal release, followed by a slower one tending to equilibrium. The highest velocity constants were observed for Ni and Zn, followed by Cu and Cr. The values calculated for the labile pool varied from 2 to 15% of the total content of each metal under study. The percentage of this metal pool in relation to the total content followed the order: Zn > Cu <FONT FACE=Symbol>@</FONT> Ni > Cr.
biosolids; Cr; Cu; Ni; Zn; phytoavailability
SEÇÃO IX - POLUIÇÃO DO SOLO E QUALIDADE AMBIENTAL
Cinética de solubilização de metais pesados por ácidos orgânicos em solos tratados com lodo de esgoto1 1 Parte da Tese de Doutorado do primeiro autor.
Kinetics of heavy metal solubilization by organic acids in sludge-treated soils
Adriana Marlene Moreno PiresI; Maria Emília MattiazzoII
IPesquisadora da Embrapa Meio Ambiente. Caixa Postal 69, CEP 13820-000 Jaguariúna (SP). E-mail: adriana@cnpma.embrapa.br
IIProfessora Aposentada do Departamento de Ciências Exatas, Escola Superior de Agricultura "Luiz de Queiroz" ESALQ/USP. Caixa Postal 9, CEP 13418-900 Piracicaba (SP). E-mail: mila@biossolidos.com.br
RESUMO
A presença de ligantes orgânicos na rizosfera tem importante papel no processo de solubilização de metais pesados em solos tratados com lodo de esgoto. Ácidos orgânicos de baixo peso molecular exsudados por raízes e, ou, liberados por microrganismos são considerados agentes mobilizadores desses metais. No presente estudo, determinou-se a cinética de solubilização de Cu, Cr, Ni e Zn em solos tratados com lodo de esgoto, utilizando solução com mistura de quatro ácidos orgânicos (acético, cítrico, lático e oxálico) preparada para obter concentração final de 0,05 e 0,10 mol L-1. A extração foi feita segundo o método de "batch". A solução 0,10 mol L-1 de ácidos orgânicos extraiu maiores quantidades de Cu, Cr, Ni e Zn do que a solução 0,05 mol L1. A cinética de solubilização apresentou duas fases: uma inicial, com rápida liberação dos metais, seguida de outra mais lenta, tendendo ao equilíbrio. As constantes de velocidade de solubilização mais altas foram observadas para Ni e Zn, seguidos de Cu e Cr. Os valores para o reservatório lábil variaram entre 2 e 15 % do total de cada metal pesado estudado. A porcentagem que este reservatório representou, em relação ao total, obedeceu à ordem: Zn > Cu @ Ni > Cr.
Termos de indexação: biossólido, Cr, Cu, Ni, Zn, fitodisponibilidade.
SUMMARY
The presence of organic ligands in the rhizosphere plays an important role in heavy metal solubilization in soils treated with sewage sludge. Low molecular weight organic acids exuded by roots and/or released by microorganisms are considered mobilizing agents of these metals. The present study determined Cd, Cu, Cr, Ni, and Zn solubilization kinetics in sewage sludge-treated soils using a mixture of four organic acids (acetic, citric, lactic, and oxalic) in 0.05 and 0.10 mol L-1 solutions. Based on the batch extraction method the 0.10 mol L-1 solution extracted greater quantities of Cu, Cr, Ni and Zn. Two phases of solubilization kinetics were observed: an initial one of fast metal release, followed by a slower one tending to equilibrium. The highest velocity constants were observed for Ni and Zn, followed by Cu and Cr. The values calculated for the labile pool varied from 2 to 15% of the total content of each metal under study. The percentage of this metal pool in relation to the total content followed the order: Zn > Cu @ Ni > Cr.
Index terms: biosolids, Cr, Cu, Ni, Zn, phytoavailability.
INTRODUÇÃO
No Brasil, a aplicação de lodo de esgoto nos solos ainda não foi amplamente difundida, e vários estudos comprovaram a eficácia do uso agrícola desse resíduo (Silva et al., 2002; Oliveira, 1995; Melo et al., 1994; Berton et al., 1989). Entretanto, a possível presença de poluentes, como metais pesados, patógenos e compostos orgânicos persistentes, é um fator que pode provocar impactos ambientais negativos (Chaney & Ryan, 1993). As principais preocupações em relação à adição de metais pesados aos solos são: entrada destes na cadeia alimentar, redução da produtividade agrícola devido a efeitos fitotóxicos, acúmulo no solo, alteração da atividade microbiana e contaminação de recursos hídricos. Os processos que conduzem à solubilização dos metais no solo são os mais importantes em relação à disponibilidade e mobilidade desses elementos (Camargo et al., 2001).
Plantas e microrganismos podem provocar, direta e, ou, indiretamente, alterações físicas, químicas e biológicas na rizosfera. Nesta região, em relação ao solo como um todo, são encontradas maiores concentrações de compostos orgânicos, como aminoácidos, açúcares, ácidos orgânicos, lipídeos, proteínas e enzimas, devido à exsudação das raízes e à intensa atividade microbiana (Ali et al., 2000). Esses compostos estão diretamente relacionados com os processos de acidificação, complexação, precipitação e oxirredução que ocorrem na rizosfera, influenciando a solubilidade e a absorção de metais pesados pelas plantas, a dinâmica da atividade microbiana e o desenvolvimento da raiz. Os ácidos orgânicos de baixo peso molecular como oxálico, lático, succínico, entre outros são efetivos na solubilização de metais ligados a frações minerais pouco solúveis do solo, por formarem complexos estáveis com os íons metálicos (Alloway, 1995; Marschner, 1995; Krishnamurti et al., 1997; Chen et al., 2003). O nível de complexação é dependente do número e proximidade dos grupos carboxílicos do ácido orgânico envolvido, do pH do solo e da concentração e do tipo de metal em questão.
A adsorção dos metais pesados em minerais do solo pode ser aumentada ou diminuída na presença de ligantes orgânicos. Alta concentração de ligantes, como os ácidos orgânicos, em relação à concentração de metais catiônicos, como os metais pesados, tende a diminuir a adsorção desses metais devido à competição entre a complexação e a superfície do mineral. Quando essa relação se aproxima de 1, pode ocorrer aumento na adsorção, possivelmente pela formação de complexos envolvendo o ligante, o metal e a superfície adsorvente do solo, denominados complexos ternários (McBride, 1994).
Mench & Martin (1991) observaram que Cd, Cu, Fe, Mn, Ni e Zn presentes no solo foram solubilizados por exsudatos de raiz de Nicotiana tabacum L., N. rustica L. e Zea mays L. Os exsudatos eram compostos por açúcares, aminoácidos, proteínas e ácidos orgânicos, sendo as quantidades de cada componente diferentes para as três espécies vegetais. Qin et al. (2004) avaliaram o efeito de ácidos orgânicos de baixo peso molecular, em comparação com sais inorgânicos (CaCl2 e NaNO3), no tempo de residência e na dessorção de Cu, Cd e Pb de solos e concluíram que os ligantes orgânicos tiveram papel dominante na dessorção dos metais. Krishnamurti et al. (1997) concluíram que o Cd do solo é mobilizado por ácidos orgânicos de baixo peso molecular (acético, cítrico, oxálico, fumárico e succínico), que são normalmente encontrados na rizosfera. Para a mesma concentração de ácido, a liberação de Cd obedeceu à seguinte ordem: fumárico > cítrico > oxálico > acético > succínico. Os resultados para a cinética de solubilização foram concordantes com as quantidades de Cd solubilizadas pelos ácidos. Koo (2001) avaliou a cinética de solubilização de Cd, Cr, Cu, Ni, Pb e Zn em solos (Typic Haploxeralf e Typic Hapludox) tratados com lodo de esgoto, na presença de ácidos orgânicos (acético, butírico, glutárico, lático, maleico, oxálico, propiônico, pirúvico, succínico, tartático e valérico), e a absorção dos metais por plantas (milho, aveia, alfafa e soja) cultivadas nesses solos. Foi constatada semelhança no comportamento dos processos de solubilização e de absorção, sendo ambos explicados pelo mesmo modelo matemático de primeira ordem (Yx = a . (1e-bx)).
O presente estudo teve como objetivo determinar a cinética de solubilização de metais pesados em diferentes solos tratados com lodo de esgoto, na presença de ácidos orgânicos comumente encontrados na rizosfera.
MATERIAL E MÉTODOS
Amostras de solo
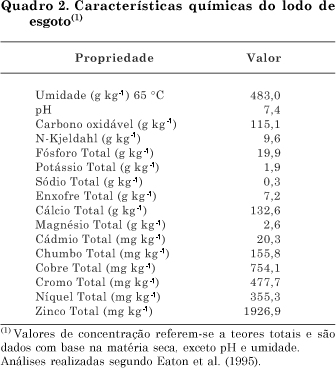
As avaliações do presente estudo foram feitas em amostras provenientes de um experimento a céu aberto montado no Departamento de Ciências Exatas, Setor de Química Ambiental da ESALQ/USP (Anjos, 1999; Bertoncini, 2002). Amostras de um Latossolo Vermelho distrófico (LVd) e um Latossolo Vermelho-Amarelo distrófico (LVAd), coletados na região de Piracicaba-SP, foram acondicionadas em caixas de amianto de 0,5 m3; o preenchimento das caixas em profundidade (3060 cm) foi feito com solo coletado na camada de 3060 cm e em superfície (030 cm) com solo da camada de 030 cm, seco ao ar e peneirado (malha de 2 mm). No quadro 1 são apresentadas características granulométricas e teores totais de óxidos de Al, de Fe e de Si de amostras da camada superficial dos solos (LVd e LVAd) utilizadas na instalação do experimento (Anjos, 1999). Estas amostras foram tratadas ou não com lodo de esgoto na quantidade total correspondente a 388 Mg ha-1 (base seca), incorporada nos primeiros 20 cm de solo, parcelada em cinco vezes (bimestral), seguida de plantio e colheita de milho e repouso. Em cada caixa, instalou-se um sistema de drenagem que possibilitava a coleta de lixiviados após as chuvas. O lodo de esgoto (Quadro 2) foi proveniente da Estação de Tratamentos de Esgotos de Barueri-SP, sendo resultante de tratamento biológico com adição de cloreto férrico e cal para auxiliar na prensagem. Utilizou-se o delineamento de blocos ao acaso, com quatro tratamentos: LVd e LVAd (testemunhas), LVd + LE e LVAd + LE (solos tratados com lodo de esgoto), e quatro repetições, sendo cada parcela composta por uma caixa. As amostras de solo utilizadas neste estudo foram coletadas 17 meses após o início do experimento, sendo retiradas da camada de 00,25 m de profundidade dos tratamentos em que o lodo de esgoto foi adicionado (LVd + LE e LVAd + LE). Algumas características químicas, incluindo teores totais de Cr, Cu, Ni, Pb e Zn (espectrometria de absorção atômica em extrato de digestão em microonda com HNO3, HCl e HF) (Quadro 3), foram determinadas por ocasião da amostragem (Bertoncini, 2000).
Composição e concentração da solução de ácidos orgânicos
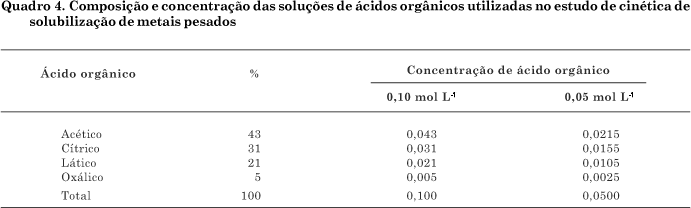
A composição da solução de ácidos orgânicos utilizada no estudo de cinética de liberação dos metais pesados (Quadro 4) foi baseada nas porcentagens médias obtidas por Pires (2003) ao estudar a rizosfera de diferentes espécies vegetais (braquiária, cana-de-açúcar, eucalipto e milho) cultivadas em areia tratada com lodo de esgoto, a saber: 43 % acético; 31 % cítrico; 21 % lático e 5 % oxálico, do total determinado. Para definição da concentração final da solução dos ácidos, foram realizados testes preliminares de extração de metais pesados com soluções que apresentavam concentração final variando entre 0,01 e 0,20 mol L-1. Os melhores resultados foram obtidos com o uso das soluções 0,10 mol L-1 e 0,05 mol L-1 de ácidos orgânicos preparadas com água deionizada e 0,4 % de clorofórmio, para inibir a atividade microbiana.
Experimento de cinética
O método de "batch", ou em batelada, é utilizado para avaliar o equilíbrio de distribuição de um soluto entre o sorvente e a solução do solo (Lavorenti et al., 2003), consistindo em agitar por um período de tempo predeterminado uma determinada quantidade de sorvente e solução e, ao término da agitação, analisar a concentração do soluto em solução. No presente estudo, utilizou-se o método de "batch", de acordo com a seguinte marcha analítica, para determinar a cinética da reação de solubilização dos metais Cd, Cu, Cr, Ni, Pb e Zn: adicionaram-se 25 mL de solução de ácidos orgânicos a uma amostra de 5 g de TFSA, agitou-se por 15 min (agitador horizontal Innova 2.1002.500 rpm), centrifugou-se (centrífuga Sorvall RC 5c Plus 10.000 rpm e 24 °C), filtrou-se (filtro de papel Whatman nº 1) e reservou-se o extrato para a quantificação dos metais. Os demais tempos testados foram: 30 min, 1, 2, 6, 8, 12, 24 e 36 h. A concentração de metais pesados em cada tempo é resultado da soma do teor de metal pesado encontrado no extrato do tempo em questão com o dos tempos anteriores. Todas as determinações foram feitas em duplicata para as quatro repetições.
Durante todo o experimento, manteve-se o pH da suspensão em 4,8, utilizando-se solução 1 mol L-1 de HCl ou NaOH, tendo em vista o pH observado na rizosfera, especificamente nas regiões mais próximas das raízes (1 mm), onde ocorre a absorção de nutrientes (Youssef & Chino, 1989). A quantificação de Cd, Cr, Cu, Ni, Pb e Zn foi feita por espectrofotometria de emissão atômica por indução de plasma (ICP-AES).
Os resultados obtidos foram ajustados por meio do programa Curve Expert 1.3 - ao seguinte modelo de cinética de primeira ordem:
Mt = M x (1-e-kt)
em que Mt = concentração do metal na solução no tempo "t"; M = concentração passível de ser removida pela concentração de ácidos orgânicos testada (reservatório lábil); e k = constante de velocidade da reação de solubilização, também referida como taxa de solubilização.
A constante M encontrada pelo modelo foi denominada reservatório lábil, ou seja, quantidade passível de ser absorvida pelas plantas. Entretanto, é importante destacar que o valor encontrado representa a quantidade máxima de cada metal pesado que pode ser solubilizada pela concentração de ácidos orgânicos na solução. Dessa maneira, o valor de M não representa o total de metais pesados que poderão ser solubilizados nesse solo agrícola tratado com lodo de esgoto, pois, neste estudo, foi avaliado o efeito de uma concentração fixa de ácidos orgânicos considerando o tempo e não se sabe quais são as variações da concentração desses ácidos na rizosfera considerando diferentes estádios de desenvolvimento, espécie vegetal, tipo de solo, tempo, atividade microbiana, dentre outros fatores de variação.
A solubilização dos metais pesados originários do lodo de esgoto na presença de ácidos orgânicos foi avaliada pela comparação dos valores de k e M obtidos, bem como da porcentagem que este reservatório lábil (M) representa em relação ao total de cada metal pesado presente no solo por ocasião da amostragem.
RESULTADOS E DISCUSSÃO
Os teores de Cd e Pb nos extratos apresentaram valores abaixo do limite de detecção do método analítico utilizado, impossibilitando a modelagem.
As quantidades de metais removidas foram superiores quando foi usada a solução 0,10 mol L-1 (Quadros 5 e 6). O processo de solubilização obedeceu à mesma tendência para todos os metais estudados, isto é, quando as amostras foram equilibradas com a solução de ácidos orgânicos, observou-se inicialmente liberação rápida dos metais em solução sob forma livre ou complexada (Quadros 5 e 6). As quantidades de Zn solubilizadas nas primeiras duas horas corresponderam, aproximadamente, a 8090 % do total dissolvido. Para Cu, Cr e Ni foram necessárias entre seis e oito horas para solubilizar quantidades correspondentes a estas mesmas porcentagens. Após esse período, a solubilização observada foi lenta, com as quantidades removidas tendendo a um valor constante, o que caracteriza o estado de equilíbrio.
Esses resultados sugerem que a solubilização dos metais Cu, Cr, Ni e Zn ocorre em duas etapas: uma mais rápida, na qual são solubilizadas as formas mais lábeis (por exemplo, as adsorvidas eletrostaticamente), além de se considerarem as quantidades de metais já solúveis; e uma mais lenta, em que menores quantidades do metal são solubilizadas, provavelmente provenientes de sítios de adsorção específica e, ou, ligadas a materiais orgânicos insolúveis. Dessa forma, os vários reservatórios de metais pesados do solo explicam o fato de a cinética de solubilização ter apresentado fases distintas. Sposito (1981) afirma que as reações de troca iônica podem ocorrer em segundos, enquanto reações de sorção/dessorção podem levar horas, dias, meses ou até anos para atingirem o equilíbrio.
Os maiores valores para a constante de velocidade da reação de solubilização (k) (Quadro 7) foram obtidos para Zn e Ni, seguidos de Cu e Cr. Isso era esperado, uma vez que os íons metálicos Cu2+ e Cr3+ tendem a formar fortes complexos de esfera interna (Guilherme, 2002), tornando estes elementos menos móveis e, conseqüentemente, dificultando a solubilização. A alteração na concentração da solução de ácidos orgânicos não resultou em diferenças nos valores de k.
Mesmo apresentando maiores teores totais de metais pesados (Quadro 3), a concentração passível de remoção (M calculado a partir da equação de cinética de primeira ordem) no LVd foi menor (Quadro 7), provavelmente por este apresentar maior teor de argila e de óxidos de ferro (Quadro 1), o que representa um diferencial em termos de cargas e retenção de metais no solo em relação ao LVAd. Portanto, esse resultado era esperado, visto que solos com maior teor de argila apresentam maior potencial de troca catiônica e presença de óxidos de Fe e de Al, mediante aumento do pH, resultam em maior adsorção de metais pesados (Alloway, 1995; Hayes & Traina, 1998).
A porcentagem de metais pesados passíveis de serem solubilizados pela concentração de ácidos orgânicos utilizada (M), em relação ao total presente no solo (Quadro 3), foi de até 15 % (Quadro 8). As porcentagens obtidas para cada metal pesado estudado obedeceram à seguinte ordem: Zn > Cu @ Ni > Cr. Logan & Chaney (1984) afirmam que o Ni geralmente apresenta-se mais disponível que o Cr e Cu, pois estes tendem a formar complexos insolúveis com a matéria orgânica, e menos disponível que Zn, o que está de acordo com o resultado encontrado. Chang (2003) diz que, enquanto a absorção de Cr, Cu e Ni por plantas cultivadas em solos tratados com lodo de esgoto parece não ser afetada pelos elevados teores solúveis de metais pesados no solo, os teores de Cd e Zn nos tecidos vegetais aumentam com o incremento da concentração no solo.
Neste estudo, os ácidos orgânicos foram adicionados ao solo uma única vez, numa concentração maior do que a geralmente encontrada na solução da rizosfera. Além disso, tentou-se evitar que ocorresse a degradação desses ácidos ao longo do tempo (uso de clorofórmio). Nesse caso, a concentração de ácidos orgânicos na solução foi de acordo com as reações de complexação, precipitação e adsorção/dessorção com a fase sólida do solo. Portanto, o equilíbrio foi atingido numa situação diferente daquela que ocorre no solo, onde esses ácidos podem ser lixiviados, degradados por microrganismos ou liberados constantemente na solução por plantas, microrganismos ou como resultado da degradação da matéria orgânica (Jones, 1998; Ryan et al., 2001). Mesmo com as diferenças entre as condições estudadas e as que ocorrem no campo, o resultado demonstra a importância dos ácidos orgânicos de baixo peso molecular na disponibilização de metais pesados presentes no solo.
Maior atenção tem sido dada à influência de cátions inorgânicos, como Na+ e Ca2+, na dessorção de metais pesados de diferentes frações do solo; entretanto, as informações sobre a influência dos ácidos orgânicos de baixo peso molecular nessa dessorção ainda são muito limitadas (Naidu & Harter, 1998). O resultado do presente estudo indica que, nas condições experimentais utilizadas, de 2 a 15 % do teor total de cada metal pesado em estudo poderia ser solubilizado e, conseqüentemente, fitodisponibilizado. Tem-se, portanto, mais um indicativo da importância desses ácidos na dessorção dos metais e da necessidade de que mais estudos sejam realizados para entender detalhadamente as reações que ocorrem entre os metais pesados, os constituintes do solo e esses ligantes orgânicos naturalmente presentes na rizosfera, assim como a influência dessas reações no tempo de residência dos metais no solo.
CONCLUSÕES
1. O aumento da concentração de ácidos orgânicos na solução extratora resultou no aumento da concentração de metais pesados em solução, demonstrando que a solubilização é dependente do teor de ácidos orgânicos.
2. A cinética de solubilização dos metais pesados apresentou duas fases distintas: uma inicial, de liberação rápida dos metais em solução, seguida de uma fase com liberação mais lenta, tendendo ao equilíbrio. Isso indica que as diferentes formas de metais presentes no solo mostram comportamento diferenciado em relação ao processo de solubilização.
3. Maiores valores para a constante de velocidade da reação de solubilização foram obtidos para Zn e Ni, seguidos de Cu e Cr, indicando que metais com tendência a serem adsorvidos especificamente apresentam menor velocidade de solubilização.
4. A quantidade de metais pesados passível de ser solubilizada pela concentração de ácidos orgânicos utilizada (M) variou de 2 a 15 % do total de cada metal pesado estudado, obedecendo à seguinte ordem: Zn > Cu @ Ni > Cr.
LITERATURA CITADA
Recebido para publicação em fevereiro de 2003 e aprovado em janeiro de 2007.
Trabalho financiado pela FAPESP.
- ALI, I.A.; KAFKAFI, U.; YAMAGUCHI, I.; SUGIMOTO, Y. & INANAGA, S. Growth, transpiration, root-born cytokinins and gibberelins, and nutrient compositional changes in sesame exposed to low root zone temperature under different ratios of nitrate: ammonium supply. J. Plant Nut., 23:123-140, 2000.
- ALLOWAY, B.J. Heavy metals in soils. 2.ed. Glasgow, Blackie A&P, 1995. 368p.
- ANJOS, A.R.M. Lixiviação de espécies químicas em Latossolos sucessivamente tratados com biossólido e disponibilidade de metais pesados para plantas de milho. Piracicaba, Escola Superior de Agricultura "Luiz de Queiroz", 1999. 191p. (Tese de Doutorado)
- BERTON, R.S.; CAMARGO, O.A. & VALADARES, J.M.A.S. Absorção de nutrientes pelo milho em resposta à adição de lodo de esgoto a cinco solos paulistas. R. Bras. Ci. Solo, 13:187-192, 1989.
- BERTONCINI, E.I. Comportamento de Cd, Cr, Cu, Ni e Zn em Latossolos sucessivamente tratados com biossólido: extração sequencial, fitodisponibilidade e caracterização de substâncias húmicas. Piracicaba, Escola Superior de Agricultura "Luiz de Queiroz", 2002. 195p. (Tese de Dotutorado)
- CAMARGO, O.A.; ALLEONI, L.R.F. & CASAGRANDE, J.C. Reações dos micronutrientes e elementos tóxicos no solo. In: FERREIRA, M.E., ed. Micronutrientes e elementos tóxicos na agricultura. Jaboticabal, CNPQ; FAPESP; POTAFOS, 2001. 599p.
- CAMARGO, O.A.; MONIZ, A.C.; JORGE, J.A. & VALVADARES, J.M.A.S. Métodos de análise química, mineralógica e física de solos do Instituto Agronômico. Campinas, Instituto Agronômico, 1986. 94p. (Boletim Técnico, 106)
- CHANEY, R.L. & RYAN, A.J. Toxic metals and toxic organic pollutants in MSW-composts. In: HOITINK, H.A. & KEENER, H.M., eds. Research results on phyto-availability, bioavailability, fate, etc. Worthington, Renaissance, 1993.
- CHANG, A.C. Soil sustainability of long term cropland application of municipal wastewater and sewage sludge. In: CONGRESSO BRASILEIRO DE CIÊNCIA DO SOLO, 29., Ribeirão Preto, 2003. Anais. Ribeirão Preto, SBCS/UNESP, 2003. CD-ROM
- CHEN, Y.X.; LIN, Q.; LUO, Y.M.; HE, Y.F.; ZHEN, S.J.; YU, Y.L.; TIAN, G.M. & WONG, M.H. The role of citric acid on the phytoremediation of heavy metal contaminated soil. Chemosphere, 50:807-811, 2003.
- GUILHERME, L.R.G.; MARQUES, J.J.; PIERANGELI, M.A.P.; ZULIANI, D.Q. & CAMPOS, M.L. Elementos-traço em solos, sedimentos e águas. In: SIMPÓSIO NACIONAL SOBRE RECUPERAÇÃO DE ÁREAS DEGRADADAS, 5., Belo Horizonte, 2002. Palestras. Belo Horizonte, SOBRADE/UFLA, 2002. p.30-55.
- HAYNES, K.F.& TRAINA, S.J. Metal speciation and its significance in ecosystem health. In: HUANG, P.M., ed. Soil chemistry and ecosystem health. Madison, Soil Science Society of America, 1998. p. 45-84.
- JONES, D.L. Organic acids in the rhizosphere-a critical review. Plant Soil, 205:25-44, 1998.
- KOO, B.J. Assessing bioavailability of metals in biosolid treated soils: root exudates and their effects on solubility of metals. Riverside, University of California, 2001. 261p. (Tese de Doutorado)
- KRISHNAMURTI, G.S.R.; CIESLINSKI, G.; HUANG, P.M. & van REES, K.C.J. Kinetics of cadmium release from soils as influenced by organic acids: implication in cadmium availability. J. Environ.. Qual., 26:271-277, 1997.
- LAVORENTI, A.; PRATA, F. & REGITANO, J. Comportamento de pesticidas em solos brasileiros. In: CURI, N.; MARQUES, J.J.; GUILHERME, G.L.R.; LIMA, J.M.; LOPES, A.S. & AVAREZ V., V.H., eds. Tópicos em ciência do solo. Viçosa, MG, Sociedade Brasileira de Ciência do Solo. 2003.v.3 p.335-400.
- LOGAN, T.J. & CHANEY, R.L. Metals. In: PAGE, A.L.; GEASON, T.L.; SMITH, J.E.; ISKANDAR, J.K. & SOMMERS, L.E., eds. Utilization of municipal wastewater and sludge on land. Riverside, University of California, 1984. p. 235-326.
- MARSCHNER, H. Mineral nutrition of higher plants. London, Academic Press, 1995. 889p.
- McBRIDE, M.B. Environmental chemistry of soils. New York, Oxford University Press, 1994. 406p.
- MELO, W.J.; MARQUES, M.O.; SANTIAGO, G.; CHELLI, R.A. & LEITE, S.A.S. Efeito de doses crescentes de lodo de esgoto sobre frações de matéria orgânica e CTC de um latossolo cultivado com cana-de-açúcar. R. Bras. Ci. Solo, 18:449-455, 1994.
- MENCH, M. & MARTIN, M. Mobilization of cadmium and other metals from two soils by root exudates of Zea mays L., Nicotiana tobaccum L., and Nicotiana rustica L. Plant Soil, 132:187-196, 1991.
- NAIDU, R. & HARTER, R.D. Effect of different organic ligands on cadmium sorption by and extractability from soil. Soil Sci. Soc. Am. J., 62:644-650, 1998.
- OLIVEIRA, F.C. Comportamento de metais pesados e formas nitrogenadas em solos tratados com lodo de esgoto. Piracicaba, Escola Superior de Agricultura "Luiz de Queiroz" 1995. 91 p. (Tese de Mestrado).
- PIRES, A.M.M. Ácidos Orgânicos da rizosfera:aspectos qualitativos e quantitativos e fitodisponibilidade de metais pesados originários de biossólidos. Piracicaba, Escola Superior de Agricultura "Luiz de Queiroz", 2003. 94p. (Tese de Dotutorado).
- QIN, F.; SHAN, X. & WEI, B. Effects of low-molecular-weight organic acids and residence time on desorption of Cu, Cd and Pb from soils. Chemosphere, 57:253-263, 2004.
- RAIJ, B. van & QUAGGIO, J.A. Métodos de análise química de solo para fins de fertilidade. Campinas, Instituto Agronômico , 1983. 31p. (Boletim Técnico, 81)
- RYAN, P.R.; DELHAIZE, E. & JONES, D.L. Function and mechanism of organic anion exudation from plant roots. Ann. Rev. Plant Physiol. Plant Molec. Biol., 52:527-560, 2001.
- SILVA, J.E.; RESCK, D.V.S.& SHARMA, R.D. Alternativa agronômica para o biossólido produzido no Distrito Federal. I-Efeito na produção de milho e na adição de metais pesados em Latossolo no cerrado. R. Bras. Ci. Solo,26:487-495, 2002.
- SPOSITO, G. Trace metals in contaminated waters. Environ. Sci. Technol., 15:396-403, 1981.
- YOUSSEF, R.A. & CHINO, M. Root-induced changes in the rhizosphere of plants. Soil Sci. Plant Nut., 35:461-468, 1989.
Datas de Publicação
-
Publicação nesta coleção
07 Maio 2007 -
Data do Fascículo
Fev 2007
Histórico
-
Recebido
Fev 2003 -
Aceito
Jan 2007