Resumos
Os ácidos orgânicos podem ser adsorvidos aos coloides do solo, favorecendo maior disponibilidade de P às plantas. Por meio de isotermas, avaliou-se a influência de ácido fúlvico (AF) sobre a adsorção de P na fração argila de dois Latossolos Vermelhos (LVdf e LVd), caulinita natural pouco cristalizada (KGa2), goethita (Gt) e hematita (Hm) sintéticas. As isotermas de adsorção de P ajustadas pelo modelo de Langmuir na presença de AF foram adequadas somente para a região de baixa concentração de P. De maneira geral, a presença de AF incubado nas frações argila estudadas foi capaz de reduzir a adsorção de P. Na fração argila do LVdf, a adsorção de P em baixas e altas concentrações desse nutriente teve pequena influência da sequência de incubação de P com AF, enquanto para a fração argila do LVd as sequências de incubação com P e AF influenciaram a adsorção de P. A redução da adsorção de P sobre a fração argila da KGa2 em baixas concentrações de P nas isotermas não dependeu da sequência de incubação de P e AF, e sim da presença do AF. Na região de altas concentrações de P, a sequência de incubação de P e AF influenciou a adsorção desse elemento. A adsorção de P sobre Gt foi dependente da sequência de incubação com AF, e a incubação prévia do AF promoveu redução da adsorção de P. A sequência de incubação do P e AF na Hm influenciou a adsorção de P quando em baixas e altas concentrações nas isotermas. Os menores valores de adsorção de P ocorreram com a incubação de P juntamente ao AF ou incubação de AF precedida da do P.
isoterma; fosfato; Langmuir
Organic acids can be adsorbed onto soil colloids, increasing the P availability to plants. Isotherms were used to evaluate the influence of fulvic acid (FA) on P adsorption in the clay fraction of two Rhodic Ferralsols (LVdf) and (LVd), poor crystallized natural kaolinite (KGa2), synthetic goethite (Gt) and hematite (Hm). The P adsorption isotherms adjusted to the Langmuir model in the presence of FA were suitable only for the region of low P concentration. In general, the presence of FA incubated in the studied clay fractions was able to reduce P adsorption. In the clay fraction of LVdf, P adsorption at low and high P concentrations were little influenced by the P sequence of incubation with FA. In the clay fraction of the LVd, however, the sequences of incubation with P and FA affected phosphorus adsorption. The reduction of P adsorption to the clay fraction of KGa2 at low P concentrations had no dependence on the incubation sequence of P and FA, but rather on the presence of FA. In the region of high P concentrations the incubation sequence of P and FA influenced P adsorption. P adsorption to Gt depended on the incubation sequence with FA, and previous incubation of FA reduced P adsorption. The incubation sequence of P and FA in Hm influenced P adsorption at low and high concentrations in the isotherms. The values of P adsorption were lowest under P incubation with FA or FA incubation preceded by P.
isotherm; phosphate; Langmuir
SEÇÃO II - QUÍMICA E MINERALOGIA DO SOLO
Adsorção de fósforo em frações argila na presença de ácido fúlvico(1 (1 ) Parte da Tese de Doutorado do primeiro autor apresentada à Universidade Federal da Grande Dourados - UFGD. )
Phosphorus adsorption by clay fractions in the presence of fulvic acid
Raphael Maia Aveiro CessaI; Antonio Carlos Tadeu VitorinoII; Luisella CeliIII; José Oscar NovelinoIII; Elisabetta BarberisIV
IDoutorando em Agronomia pela Universidade Federal da Grande Dourados - UFGD. Rodovia MS 270, km 12, Caixa Postal 533, CEP 79804-970 Dourados (MS). E-mail: raphaelcessa@hotmail.com
IIProfessor da Faculdade de Ciências Agrárias, UFGD. E-mail: vitorino@ufgd.edu.br, jnovel@ufgd.edu.br
IIIProfessora da Facoltà di Agrária, Dipartimento di Valorizzazione e Protezione delle Risorse Agroforestali/Universitá di Torino. Via Leonardo da Vinci 44, Grugliasco (TO), 10095. E-mail: luisella.celi@unito.it, elisabetta.barberis@unito.it
RESUMO
Os ácidos orgânicos podem ser adsorvidos aos coloides do solo, favorecendo maior disponibilidade de P às plantas. Por meio de isotermas, avaliou-se a influência de ácido fúlvico (AF) sobre a adsorção de P na fração argila de dois Latossolos Vermelhos (LVdf e LVd), caulinita natural pouco cristalizada (KGa2), goethita (Gt) e hematita (Hm) sintéticas. As isotermas de adsorção de P ajustadas pelo modelo de Langmuir na presença de AF foram adequadas somente para a região de baixa concentração de P. De maneira geral, a presença de AF incubado nas frações argila estudadas foi capaz de reduzir a adsorção de P. Na fração argila do LVdf, a adsorção de P em baixas e altas concentrações desse nutriente teve pequena influência da sequência de incubação de P com AF, enquanto para a fração argila do LVd as sequências de incubação com P e AF influenciaram a adsorção de P. A redução da adsorção de P sobre a fração argila da KGa2 em baixas concentrações de P nas isotermas não dependeu da sequência de incubação de P e AF, e sim da presença do AF. Na região de altas concentrações de P, a sequência de incubação de P e AF influenciou a adsorção desse elemento. A adsorção de P sobre Gt foi dependente da sequência de incubação com AF, e a incubação prévia do AF promoveu redução da adsorção de P. A sequência de incubação do P e AF na Hm influenciou a adsorção de P quando em baixas e altas concentrações nas isotermas. Os menores valores de adsorção de P ocorreram com a incubação de P juntamente ao AF ou incubação de AF precedida da do P.
Temos de indexação: isoterma, fosfato, Langmuir.
SUMMARY
Organic acids can be adsorbed onto soil colloids, increasing the P availability to plants. Isotherms were used to evaluate the influence of fulvic acid (FA) on P adsorption in the clay fraction of two Rhodic Ferralsols (LVdf) and (LVd), poor crystallized natural kaolinite (KGa2), synthetic goethite (Gt) and hematite (Hm). The P adsorption isotherms adjusted to the Langmuir model in the presence of FA were suitable only for the region of low P concentration. In general, the presence of FA incubated in the studied clay fractions was able to reduce P adsorption. In the clay fraction of LVdf, P adsorption at low and high P concentrations were little influenced by the P sequence of incubation with FA. In the clay fraction of the LVd, however, the sequences of incubation with P and FA affected phosphorus adsorption. The reduction of P adsorption to the clay fraction of KGa2 at low P concentrations had no dependence on the incubation sequence of P and FA, but rather on the presence of FA. In the region of high P concentrations the incubation sequence of P and FA influenced P adsorption. P adsorption to Gt depended on the incubation sequence with FA, and previous incubation of FA reduced P adsorption. The incubation sequence of P and FA in Hm influenced P adsorption at low and high concentrations in the isotherms. The values of P adsorption were lowest under P incubation with FA or FA incubation preceded by P.
Index terms: isotherm, phosphate, Langmuir.
INTRODUÇÃO
A adsorção de ânions sobre a superfície mineral dos solos e suas interações com vários íons orgânicos (Andrade et al., 2003) e inorgânicos (Sposito, 1989) têm grande impacto sobre a disponibilidade e mobilidade de nutrientes e contaminantes (Moreira & Dourado, 2007).
Os ácidos orgânicos podem ser adsorvidos aos coloides do solo com grande energia, formando complexos organometálicos com Fe e Al e, assim, competir com o P pelos sítios de adsorção de cargas, favorecendo sua maior disponibilidade às plantas (Haynes, 1984; Sposito, 1989; Pavinato & Rosolem, 2008). É preciso considerar que o efeito da matéria orgânica do solo, bem como dos ácidos orgânicos fornecidos por ela sobre o bloqueio dos sítios de adsorção, é transitório (Afif et al., 1995), mas pode ser vantajoso quando se considera a época de aplicação de fosfato.
A capacidade dos ácidos orgânicos em competir com P vai depender das suas concentrações e formas (macromoléculas ou polimerizadas), pH, força iônica da solução e, principalmente, da sua persistência no solo (Ghosh & Schnitzer 1980; Haynes, 1984; Stevenson, 1986; Sposito, 1989; Kirk, 1999; Rauen et al., 2002).
Lopez Hernandez et al. (1986) puderam constatar redução da adsorção de P sobre a superfície de partículas minerais devido à capacidade dos ácidos húmicos, málicos e oxálicos em competir com o P pelos sítios de adsorção de carga. Guppy et al. (2005) relatam que entre os ácidos orgânicos mais ativos à disponibilização de P estão: cítrico, oxálico, glucôncio, lático e málico. Ácidos húmicos e fúlvicos, compostos mais estáveis e de longa persistência na fração orgânica do solo, também podem competir pelos sítios de adsorção. No entanto, a adsorção dos ácidos orgânicos e consequentemente a redução da adsorção de P não dependem apenas da eficiência dos grupos carboxílicos, mas também da capacidade de esses ácidos complexarem Fe e Al livres em solução, os quais poderiam formar precipitados com P. Além disso, a redução da adsorção de P é mais importante quando a incubação é realizada simultânea ou primeiramente com ácidos orgânicos.
O ácido fúlvico (AF) é a substância húmica (SH) com maior acidez total, sendo solúvel em todas as faixas de pH (Vermeer & Koopal, 1998). Dessa forma, durante a solubilização do AF, os prótons contidos nos seus grupamentos carboxílicos serão dissociados, gerando carga negativa na extremidade (COO-) responsável pela adsorção do AF à superfície dos minerais (Parfitt et al., 1977) durante o processo de competição por sítios de carga com P.
O presente trabalho teve por objetivo quantificar a adsorção de P na presença de ácido fúlvico (AF) na fração argila de dois Latossolos Vermelhos, caulinita natural pouco cristalinizada, goethita e hematita sintéticas.
MATERIAL E MÉTODOS
O estudo foi realizado no Dipartimento di Valorizzazione e Protezione delle Risorse Agroforestali (DI.VA.PRA), localizado na Facoltà Agrária da Università di Torino, Itália. As frações argila dos solos foram provenientes de dois Latossolos Vermelhos do Estado de Mato Grosso do Sul - Brasil, sendo um distroférrico (LVdf) de textura muito argilosa (71 % de argila) e outro distrófico (LVd) de textura média (18 % de argila), coletadas na profundidade de 20 a 40 cm, localizados às margens da rodovia estadual MS-270 (Dourados - Itahum) nos km 11 e 38, respectivamente. A vegetação de cobertura do LVdf era composta predominantemente pela espécie Brachiaria decumbens e o LVd encontrava-se sob vegetação natural de Cerrado. Esses solos não haviam recebido qualquer tipo de adubação há pelo menos 30 anos.
O ácido fúlvico (AF) utilizado foi obtido no DI.VA.PRA e extraído de um Organossolo. O peso molecular aparente de 60 % das partículas que o compõem encontra-se entre 30.000 e 10.000 Da, e 40 % entre 10.000 e 1.000 Da. Os valores em percentagem do AF para C (49,2), N (4,50), H (4,23), S (0,84), O (41,3) e cinzas (2,67) foram obtidos pelo aparelho analisador elementar (CE Instruments, NA2100 Protein), além das relações C/N (12,7), H/C (1,02) e O/C (0,63). As quantidades de acidez total, grupamento carboxílico (-COOH) e hidroxílico (-OH) foram, respectivamente, de 1.386, 686 e 700 cmolc kg-1. O teor de Pi determinado por digestão sulfoperclórica foi de 0,034 %.
Para construção das isotermas de adsorção de AF nas matrizes sintéticas de Hm e Gt, foram preparadas soluções de AF nas concentrações de 0, 15, 25, 35, 45, 60, 80 e 100 mg L-1 em KCl a 0,001 mol L-1 a pH 5,5. Para caulinita natural (KGa2) e para as frações argila extraídas dos Latossolos Vermelhos distroférrico (LVdf) e distrófico (LVd), as concentrações das soluções de AF foram de 0, 15, 20, 25, 50, 100, 150 e 200 mg L-1 em KCl a 0,001 mol L-1 a pH 5,5. Essas soluções eram adicionadas em 5 mL das suspensões de argila preparadas com 24 h de antecedência, por meio da agitação magnética em solução KCl a 0,001 mol L-1 a pH 5,5. A concentração das argilas nas suspensões foi determinada usando-se por base os valores de superfície específica obtidos previamente (Cessa et al., 2009). Para isso, pesou-se uma quantidade de argila suficiente para obter uma suspensão contendo 10 m2 do material de argila. Essas suspensões de argila eram transferidas para tubos plásticos, que, juntamente com as soluções de AF, eram fechados, e foram agitadas verticalmente por 24 h; posteriormente, esse material foi centrifugado a 3.000 rpm durante 15 min. O sobrenadante obtido foi separado e filtrado com auxílio de seringa em malha de 0,2 µm. As leituras para determinação da concentração de AF nos sobrenadantes não diluídos das amostras foram realizadas em espectrofotômetro, no comprimento de onda de 465 nm.
Para construção das isotermas de adsorção de P na presença de AF, foram realizadas incubações de P e AF em conjunto nas suspensões de argila, alterando-se a sequência de suas aplicações. A dose fixa de AF utilizada para todos os materiais foi de 3,21 x 10-5 mg L-1, obtida a partir de uma solução de 200 mg L-1 de AF estabelecida em função da capacidade máxima de adsorção entre os materiais estudados, determinada em ensaios prévios. Foram preparadas soluções de P a 10, 100 e 1.000 mg L-1 em KCl 0,01 mol L-1 a pH 5,5. Posteriormente, em oito tubos plásticos de 10,0 mL foram adicionadas alíquotas da solução de AF em 5,0 mL de suspensões de argila, permitindo as concentrações finais de 0,0; 2,0; 5,0; 10,0; 20,0; 30,0; 40,0 e 50,0 mg L-1 de P para a construção das isotermas de adsorção de P sobre Hm e Gt sintéticas e para as frações argila extraídas dos solos, e de 0,0; 1,0; 2,0; 4,0; 8,0; 10,0; 15,0; e 20,0 mg L-1 de P para a construção das isotermas de adsorção sobre caulinita natural (Kga2). Em seguida, os tubos foram fechados, agitados verticalmente por 24 h e centrifugados a 3.000 rpm por 15 min. Os sobrenadantes obtidos foram filtrados em filtro de 0,2 µm e diluídos, e as leituras para determinação da concentração de P, procedidas em espectrofotômetro no comprimento de onda de 725 nm (Braga & Defelipo, 1974).
As sequências de aplicação de P e AF em cada suspensão de argila foram: P-AF (P e AF incubados juntos), P/AF (primeiro P e depois AF) e AF/P (primeiro AF depois P). Cada intervalo de incubação foi de 24 h.
RESULTADOS E DISCUSSÃO
As isotermas de adsorção de ácido fúlvico (AF) sobre os materiais das diferentes frações argila adequaram-se ao modelo de Langmuir (Quadro 1).
Em geral, para as isotermas de adsorção de P foram observados dois platôs, sendo o primeiro relacionado às baixas concentrações de P (primeira região da isoterma) e o segundo às altas concentrações de P. Dessa forma, para a primeira região das isotermas, considerando-se os quatro primeiros pontos, foi possível por meio do modelo de Langmuir calcular os valores de máxima adsorção de P (Pmax em µmol m-2) (Quadro 2).
No trabalho de Celi et al. (2000), também foram observados dois platôs nas isotermas de adsorção de P sobre goethita. Segundo esses autores, isso ocorreu por uma questão relacionada às formas de ligação do P sobre a superfície do mineral. Com base nos resultados dos testes de espectroscopia de infravermelho e em análises químicas de recuperação de P, os autores sugeriram, para a primeira região da isoterma, que tal elemento estaria ligado à superfície da goethita de forma binuclear bidentada. Para a segunda região da isoterma, a ligação estabelecida pelo P na superfície da goethita seria do tipo binuclear monodentada.
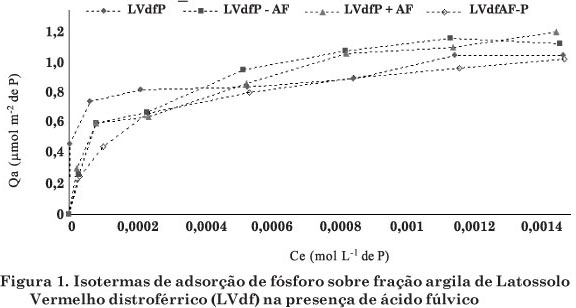
Os valores de Pmax para LVdf determinados na região de baixa concentração de P nas isotermas (Quadro 2) foram próximos. Essa tendência também foi observada na região de altas concentrações de P nas isotermas (Figura 1).
Para LVd, o valor de Pmax na região de baixa concentração de P nas isotermas (Quadro 2) foi maior com a sua incubação isolada, seguido da sua incubação precedida do AF (P-AF). Quanto à sequência de incubação P+AF e AF-P, os valores de Pmax foram próximos e menores do que os observados para incubação de P e P-AF. Possivelmente, os valores de Pmax nesse caso foram influenciados pela presença de AF e pela sua sequência de incubação com P.
Na região das isotermas com alta concentração de P os valores de Pmax foram decrescentes para as sequências de incubação P, P-AF, P+AF e AF-P (Figura 2), sendo a sequência de incubação entre P e AF capaz de influenciar os valores de Pmax.
Para KGa2, o valor de Pmax na região de baixa concentração de P nas isotermas (Quadro 2) foi maior com a sua incubação isolada, seguido da sua incubação juntamente com AF (P+AF) e P incubado após incubação com AF (AF-P). Assim, a redução do valor de Pmax sobre a fração argila da KGa2 não dependeu da sequência de incubação de P e AF, e sim da presença do AF.
Na região de altas concentrações de P nas isotermas para KGa2 (Figura 3), pode-se observar que a sequência de incubação de P e AF influencia a Pmax; para redução desse valor, é importante que o AF seja incubado nas sequências P+AF ou AF-P.
Os valores de Pmax para Gt determinados na região de baixa concentração de P nas isotermas (Quadro 2) foram próximos para sequência de incubação P, P-AF e P+AF e maiores do que os observados para a sequência de incubação AF-P (Quadro 2). Essa tendência também foi observada na região de altas concentrações de P nas isotermas (Figura 4). Pode-se notar, nesse material, que para haver redução da Pmax é preciso que o AF seja incubado primeiro.
Para Hm, na região das isotermas com baixa concentração de P os valores de Pmax foram decrescentes para as sequências de incubação P, P-AF, P+AF e AF-P (Quadro 2), sendo a sequência de incubação entre P e AF capaz de influenciar os valores de Pmax. Na região das isotermas com altas concentrações de P, os valores de Pmax foram próximos para incubação isolada de P e P-AF. Esses valores foram maiores do que os observados para as sequências de incubação P+AF e AF-P, os quais foram próximos entre si (Figura 5). Com isso, pode-se notar que a sequência de incubação de P e AF influenciaram a Pmax; para redução desse valor, é importante que o AF seja incubado nas sequências P+AF ou AF-P.
Andrade et al. (2003) observaram alterações nos valores de adsorção do P quando o elemento foi incubado em diferentes ordens com os ácidos cítrico, oxálico, salicílico e húmico. Em diversos trabalhos, Lopez Hernandez et al. (1986), Morelli & Bortoluzzi (1992) e Violante & Gianfreda (1993) relatam que a incubação do P posterior à de ácidos orgânicos acarreta redução da sua adsorção, uma vez que o ácido orgânico pode ter ocupado maior número de sítios de adsorção no período avaliado.
A variação nas respostas de adsorção de P referentes às sequências de incubação com AF entre os materiais estudados está relacionada à afinidade do elemento em adsorver-se à superfície das partículas dos minerais, que por sua vez têm variações na composição química e nos tipos e quantidades de grupamentos químicos presentes.
Em solos contendo óxidos de Fe e de Al e caulinita a interação do P com o grupo funcional ligado aos cátions (em geral, Fe-OH e Al-OH e grupamento aluminol) nas superfícies das partículas ocorre pelo compartilhamento eletrônico e, portanto, apresenta diferentes graus de energia de ligação (Barrow et al., 1998; Barrow, 1983,1999; Berwanger et al., 2008). Assim, quando presentes na superfície, a existência dos grupamentos OH dependerá do pH e da força iônica da solução (Stumm, 1992), bem como do tipo de ligação em coordenação dos grupamentos protonados com o metal na superfície do mineral (Rakovan et al., 1999).
Hingston et al. (1978) postularam que o mecanismo de ligação para adsorção específica de diversos ânions inorgânicos sobre goethita ocorreu pelo deslocamento de OH ligadas com Fe e Al por coordenação simples. Mclaughlin et al. (1981) observaram, entre sistemas mineralógicos sintéticos formados por goethita, hematita, caulinita e caulinita contendo Fe precipitado em superfície, que a goethita foi o material que mais adsorveu P. Para esse acontecimento caberia a explicação de Fontes & Weed (1996), os quais relatam que a goethita, por ter maior densidade de OH em coordenação simples em uma de suas faces cristalográficas (100), proporcionou maior afinidade de ligação com íons de fosfato (Atkinson et al., 1974; Parfitt et al., 1976), sendo isso também observado para hematita em menor intensidade.
De acordo com o que foi postulado anteriormente, a proximidade dos valores de Pmax em diferentes sequências de incubação de P e AF nos materiais de argila LVdf deve estar relacionada à presença de Gt nesse material (Cessa et al., 2009) e, consequentemente, com os grupamentos Fe-OH (OH em coordenação simples) nas superfícies das suas partículas. Sobre Gt, também foi observada pouca resposta às sequências de incubação de P e AF sobre os valores de Pmax.
CONCLUSÕES
1. As isotermas de adsorção de P ajustadas pelo modelo de Langmuir na presença de AF foram adequadas somente para a região de baixa concentração de P.
2. De maneira geral, a presença de AF incubado nas frações argila estudadas foi capaz de reduzir a adsorção de P.
3. A adsorção de P em baixas e altas concentrações de P, sobre a fração argila do Latossolo Vermelho distroférrico (LVdf), foi pouco influenciada pela sequência de incubação de P com AF, enquanto para a fração argila do Latossolo Vermelho distrófico (LVd) as sequências de incubação com P e AF influenciaram a adsorção de P.
4. A redução da adsorção de P sobre a fração argila da KGa2 em baixas concentrações de P nas isotermas não dependeu da sequência de incubação de P e AF, e sim da presença do AF. Na região de altas concentrações de P, a sequência de incubação de P e AF influenciou a adsorção de P.
5. A adsorção de P sobre Gt foi dependente da sequência de incubação com AF; para haver redução da adsorção de P, foi necessário que o AF fosse incubado primeiro.
6. A sequência de incubação do P e AF na Hm influenciou a adsorção de P quando em baixas e altas concentrações nas isotermas. Os menores valores ocorreram com a incubação de P juntamente ao AF ou incubação de AF precedida da do P.
LITERATURA CITADA
Recebido para publicação em maio de 2009 e aprovado em agosto de 2010.
- ATKINSON, R.J.; PARFITT, R.L. & SMART, R.St.C. Infrared study of phosphate adsorption on goethite. J. Chem. Soc. Faraday Trans., 70:1472-1479, 1974.
- AFIF, E.; BARRÓN, V. & TORRENT, J. Organic matter delay but does not prevent phosphate sorption by cerrado soils from Brazil. Soil Sci., 159:207-211, 1995.
- ANDRADE, F.V.; MENDONÇA, E.S.; ALVAREZ V., V.H. & NOVAIS, R.F. Adição de ácido orgânicos e húmicos em Latossolos e adsorção de fosfato. R. Bras. Ci. Solo, 27:1003-1011, 2003.
- BARROW, N.J. A mechanistic model for describing the sorption and desorption of phosphate by soil. J. Soil Sci., 34:733-750, 1983.
- BARROW, N.J.; BOLLAND, M.D.A. & ALLEN, D.G. Effect of addition of superphosphate on sorption of phosphate. Austr. J. Soil Res., 36:359-372, 1998.
- BARROW, N.J. The fours laws of soil chemistry: The leer lecture 1998. Austr. J. Soil Res., 37:787-829, 1999.
- BERWANGER, A.L.; CERETTA, C.A. & SANTOS, D.R. Alterações no teor de fósforo no solo com aplicação de dejetos líquidos de suínos. R. Bras. Ci. Solo, 32:2525-2532, 2008.
- BRAGA, J. M. & DEFELIPO, B.V. Determinação espectrofotométrica de fósforo em extratos de solo e material vegetal. R. Ceres, 21:73-85, 1974.
- CELI, L.; BARBERIS, E. & MARSAN, F. A. Sorption of phosphate on goethite at high concentration. Soil Sci., 165:657-664, 2000.
- CESSA, R.M.A.C.; CELI, L.; VITORINO, A.C.T.; NOVELINO, J.O. & BARBERIS, E. Área superficial específica, porosidade da fração argila e adsorção de fósforo em dois Latossolos Vermelhos. R. Bras. Ci. Solo, 33:1153-1162, 2009.
- FONTES, M.P.F. & WEED, S.B. Phosphate adsorption by clays from Brazilian Oxisols: Relationships with specifc surface area and mineralogy. Geoderma, 72:37-51, 1996.
- GHOSH, C.H. & SCHNITZER, M. Macromolecular structures of humic substances. Soil Sci. Soc. Am. Proc., 129:266-276, 1980.
- GUPPY, C.N.; MENZIES, N.W.; MOODY, P.W. & BLAMEY, F.P.C. Competitive sorption reactions between phosphorus and organic matter in soil: A review. Austr. J. Soil Res., 43:189-202, 2005.
- HAYNES, R.J. Lime and phosphate in the soil plant system. Adv. Agron., 37:249-315, 1984.
- HINGSTON, F.J.; POSNER, A.M. & QUIRK, J.P. Anion adsorption by gibbsita and goethite. 1. The role of the proton in determining the adsorption envelopes. J. Soil Sci., 23:177-192, 1972.
- KIRK, G.J.D. A model of phosphate solubilization by organic anion excretion from plant roots. Europ. J. Soil Sci., 50:369-378, 1999.
- LOPEZ HERNANDEZ, D.; SIEGERT, G. & RODRIGUEZ, J.V. Competitive adsorption of phosphate with malate and oxalate by tropical soil. Soil Sci. Soc. Am. J., 57:1460-1462, 1986.
- McLAUGHLIN, J.R.; RYDEN, J.C. & SYERS, J.K. Sorption of inorganic phosphate by iron and aluminium - containing components. J. Soil Sci., 32:365-377, 1981.
- MOREIRA, C.A. & DOURADO, J.C. Monitoramento da atenuação natural de pluma de contaminação pelo método de radar de penetração no solo. R. Bras. Geof., 25:389-398, 2007.
- MORELLI, M. & BORTOLUZZI, G. Efeito do humato e do poligalactoronato na sorção de fósforo pelo solo. R. Bras. Ci. Solo, 16:373-377, 1992.
- PARFITT, R.L.; RUSSELL, J.D. & FARMER, V.C. Confirmation of the surface structures of goethite (á-FeOOH) and phosphated goethite. J. Chem. Soc. Faraday Trans., 72:1082-1087, 1976.
- PARFITT, R.L.; FRASER, A.R. & FARMER, V.C. Adsorption on hydrous oxides. III. Fulvic acid and humic acid on goethite, gibbsite and imogolite. J. Soil Sci., 28:289-296, 1977.
- PAVINATO, P.S. & ROSOLEM, C.A. Disponibilidade de nutrientes no solo - Decomposição e liberação de compostos orgânicos de resíduos vegetais. R. Bras. Ci. Solo, 32:911-920, 2008.
- RAKOVAN, J.; BECKER, U. & HOCHELLA, M.F. Aspects of goethite surface microtopography, structure, chemistry, and reactivity. Am. Miner., 84:884-894, 1999.
- RAUEN, T.G.; DEBACHER, N.A. & SIERRA, M.M.S. Tensoativos de ácidos húmicos de procedências distintas. Química Nova, 25:909-913, 2002.
- SPOSITO, G. The chemistry of soils. New York, Oxford University, 1989. 277p.
- STEVENSON, F.J. Cycles of carbon, nitrogen, phosphorus, sulphur and micronutrients. New York, John Wiley & Sons, 1986. 380p.
- STUMM, W. Chemistry on the solid-water interface. New York, J. Wiley, 1992. 428p.
- VERMEER, A.W.P. & KOOPAL, L.K. Adsorption of humic acids to mineral particles. 2. Polydispersity effects with polyelectrolyte adsorption. Langmuir, 14:4210-4216, 1998.
- VIOLANTE, A. & GIANFREDA, L. Competition in adsorption between phosphate and oxalate on aluminium hydroxide montmorillonite complex. Soil Sci. Soc. Am. J., 57:1235-1241, 1993.
Datas de Publicação
-
Publicação nesta coleção
16 Dez 2010 -
Data do Fascículo
Out 2010
Histórico
-
Aceito
Ago 2010 -
Recebido
Maio 2009