RESUMO
A mesofauna edáfica compreende organismos de dimensões entre 100 μm e 2 mm, sendo importante avaliar os métodos utilizados para sua caracterização. Os objetivos deste trabalho foram definir o período de tempo de permanência do material de solo no extrator Berlese-Tüllgren para a captura dos organismos da mesofauna e determinar o tempo mínimo de extração para a correta utilização dos índices de Shannon, Simpson, Pielou e Margalef, empregados na avaliação da diversidade, dominância e equabilidade das comunidades da mesofauna. O estudo foi conduzido no Departamento de Solos do Instituto de Agronomia da Universidade Federal Rural do Rio de Janeiro, Seropédica, Rio de Janeiro, em terreno altamente antropizado. Foram instaladas parcelas experimentais com os seguintes tratamentos: feijão-de-porco (Canavalia ensiformis), mucuna-preta (Mucuna aterrima), feijão-bravo-do-Ceará (Canavalia brasiliensis), guandu (Cajanus cajan) e vegetação espontânea, em delineamento de quadrado latino. Em cada uma das unidades experimentais, foram coletadas amostras formadas por serapilheira e material de solo, nos primeiros 5 cm da camada superficial do solo realizada um dia antes do plantio das leguminosas (outubro) e, posteriormente, por ocasião do corte da parte aérea das plantas (março). As amostras foram submetidas a uma bateria de extratores do tipo Berlese-Tüllgren, por um período de 15 dias, realizando-se a contagem diária dos organismos. A partir da contagem e identificação em nível de grupo (Ordem/Família) dos organismos capturados, foram determinados os índices de Margalef, Simpson, Shannon e Pielou, bem como verificou-se a correlação por ordem de Kendall entre os valores obtidos dia a dia até o 8º dia de extração, usando-se o índice de Shannon como referência. Concluiu-se que é possível a redução do tempo de permanência das amostras de material de solo nos funis Berlese-Tüllgren, não sendo recomendável a adoção de período de tempo inferior a seis dias para se determinar a composição da mesofauna edáfica ou para se obterem dados mais consistentes e confiáveis para se avaliarem os índices de diversidade, quando se utiliza esse procedimento.
método de Berlese-Tüllgren; índice de Shannon; índice de Simpson; índice de Pielou; ecologia do solo
ABSTRACT
Soil mesofauna consists of organisms that measure from 0.100 μm to 2 mm, being important to evaluate methods employed for its characterization. The objectives of this study were to define how long the soil material must remain in the Berlese-Tüllgren extraction device to capture organisms of the mesofauna and determine the minimum extraction time for correct use of the Shannon, Simpson, Pielou, and Margalef indices used to evaluate the diversity, dominance, and richness of the mesofauna communities. The study was conducted at the Department of Soil Science at the Institute of Agronomy of the Universidade Federal Rural do Rio de Janeiro, Seropédica, Rio de Janeiro, Brazil, in highly anthropic land. Experimental plots were set up with the following treatments: jack bean (Canavalia ensiformis), velvet bean (Mucuna aterrima), Ceará bravo bean (Canavalia brasiliensis), pigeon pea (Cajanus cajan), and spontaneous vegetation in a Latin square design. Samples were collected from each of the experimental units, made up of plant litter and soil material in the first 5 cm of topsoil the day before planting legumes (October), and, subsequently, at the time of cutting plant shoots (March). The samples were subjected to a battery of the Berlese-Tüllgren type funnels for a period of 15 days, performing a daily count of organisms. From the count and group-level identification (Order/Family) of the captured organisms, the Margalef, Simpson, Shannon, and Pielou indices were determined and verified by Kendall rank correlation between the values obtained from one day to the next until the 8th day of extraction, using the Shannon index as a reference. From the study, it may be concluded that it is possible to reduce the time the material samples remain in the Berlese-Tüllgren funnels, but adoption of a time less than six days is not recommended to determine the composition of the soil mesofauna or to obtain more consistent and reliable data for evaluating diversity indices when using this procedure.
Berlese-Tüllgren method; Shannon index; Simpson index; Pielou index; soil ecology
INTRODUÇÃO
A mesofauna edáfica compreende organismos de dimensões entre 100 μm e 2 mm, que são constituídos pelos grupos Acari, Aranea, Chilopoda, Collembola, Diplopoda, Diplura, Diptera, Enchytraeidae, Hymenoptera, Isoptera, Mollusca, Protura e Symphyla, podendo incluir também pequenos indivíduos da ordem Coleoptera (Rossi et al., 2009Rossi CQ, Nobre CP, Coelho CP, Benazzi ESS, Rodrigues K, Correia MEF. Efeito de diferentes coberturas vegetais sobre a mesofauna edáfica em manejo agroecológico. R Bras Agroecol. 2009;4:1326-30.; Morais et al., 2013Morais JW, Oliveira, FL, Braga RF, Korasaki V. Mesofauna. In: Moreira FMS, Cares JE, Zanetti R, Stürmer SL, editores. O ecossistema solo: componentes, relações ecológicas e efeitos na produção vegetal. Lavras: Universidade Federal de Lavras; 2013. p.183-200.). As ordens Acari e Collembola são as mais numerosas, constituindo 72 a 97 % da população total de artrópodes da fauna do solo (Lins et al., 2007Lins V, Santos H, Gonçalves MC. The effect of the glyphosate, 2,4-D, atrazine e nicosulfuron herbicides upon the edaphic collembola (Arthropoda: Ellipura) in a no tillage system. Neotrop Entomol. 2007;36:261-7.). De acordo com Assad (1997)Assad MLL. Fauna do solo. In: Vargas MAT, Hungria M, editores. Biologia dos solos dos Cerrados. Planaltina: Embrapa Soja; 1997. p.363-443., a mesofauna edáfica é importante como catalisadora na atividade microbiana de decomposição da matéria orgânica, na desagregação mecânica do material vegetal em decomposição, na formação e manutenção da estrutura do solo. Além disso, esses invertebrados destacam-se pela sua contribuição significativa na regulação das populações microbianas, fragmentação de resíduos vegetais e predação de outros invertebrados (Antonini et al., 2003Antonini Y, Colli G, Accacio G, Constantino R, Franceschinelli E, Laps R, Scariot A, Vieira M, Wiederhecker H. Fragmentação dos ecossistemas e a biodiversidade brasileira: uma síntese. In: Rambaldi D, Oliveira D, editores. Fragmentação de ecossistemas: causas, efeitos sobre a biodiversidade e recomendações de políticas públicas. Brasília, DF: Ministério do Meio Ambiente; 2003. p.317-24.).
O procedimento para estudo dos organismos consiste em sua captura, identificação e quantificação dos componentes da comunidade em questão. Atualmente, são encontrados trabalhos que utilizam diferentes métodos, adotados segundo o arbítrio dos pesquisadores, levando em conta principalmente os objetivos do estudo e a praticidade dos procedimentos. O mais tradicional dos métodos é o que utiliza a retirada de material de solo, e a posterior extração dos organismos seja por catação, flotação ou emprego de funis (Sandler et al., 2010Sandler R, Falco LB, Ciocco C, Luca R, Coviella CE. Eficiencia del embudo Berlese-Tullgren para extracción de artrópodos edáficos en suelos arguidoles típicos de la Provincia de Buenos Aires. Ci Suelo (Argentina). 2010;28:1-7.).
Os métodos de funil, com base naqueles descritos por Antonio Berlese (Pass e Szucsich, 2011Pass G, Szucsich NU. 100 years of research on the Protura: many secrets still retained. Soil Organ. 2011;83:309-34..) e modificados por Tüllgren em 1918 (Sandler et al, 2010Sandler R, Falco LB, Ciocco C, Luca R, Coviella CE. Eficiencia del embudo Berlese-Tullgren para extracción de artrópodos edáficos en suelos arguidoles típicos de la Provincia de Buenos Aires. Ci Suelo (Argentina). 2010;28:1-7.), são simples para extrair animais em boas condições para identificação (Edwards e Fletcher, 1970Edwards CA, Fletcher KE Assessment of terrestrial invertebrate populations. In: Phillipson J, editor. Methods of study in soil ecology. Paris: Unesco, 1970. p.57-66.), apesar de se encontrar grande variabilidade na sua aplicação. Assim, ainda que o tempo-padrão seja de 15 dias de permanência da amostra no extrator, há trabalhos com o tempo de extração em 48 h (Ferreira e Marques, 1998Ferreira R, Marques M. A fauna de artrópodes de serapilheira de áreas de monocultura com Eucalyptus sp. e mata secundária heterogênea. An Soc Entomol Bras. 1998;27:95-403.;Krolow, 2009Krolow DRV. Estudo da macro e mesofauna do solo em um sistema de produção de base ecológica [tese]. Pelotas: Universidade Federal de Pelotas; 2009.; Ogedegbe e Egwuonwu, 2014Ogedegbe ABO, Egwuonwu IC. Biodiversity of soil Arthropods in Nigerian Institute for Oil Palm Research (NIFOR), Nigeria. J Appl Sci Environ Manage. 2014;18 377-86.), 72 h (Mineiro e Moraes, 2001Mineiro JC, Moraes GJ. Gamasida (Arachnida: Acari) Edáficos de Piracicaba, Estado de São Paulo. Neotrop Entomol. 2001;30:379-85.), quatro dias (Souto et al., 2008Souto PC, Souto JS, Miranda JP, Santos RV, Alves AR. Comunidade microbiana e mesofauna edáficas em solo sob caatinga no Semiárido da Paraíba. R Bras Ci Solo. 2008;32:151-60.), sete dias (Vieira, 2008Vieira MP. Mesofauna edáfica e a taxa de decomposição da resteva de três sucessões de cultura em sistema plantio direto [tese]. Dourados; Universidade Federal de Dourados; 2008.; Rossi et al., 2009Rossi CQ, Nobre CP, Coelho CP, Benazzi ESS, Rodrigues K, Correia MEF. Efeito de diferentes coberturas vegetais sobre a mesofauna edáfica em manejo agroecológico. R Bras Agroecol. 2009;4:1326-30.;Barros et al., 2010Barros Y, Melo V, Sautter K, Buschle B, Oliveira E, Azevedo J, Souza L, Kummer L. Indicadores de qualidade de solos de área de mineração e metalurgia de chumbo. II - Mesofauna e plantas. R Bras Ci Solo. 2010;34:1413-26.; São José et al., 2013São José JBS, Rieff G, Sá ELS. Mesofauna edáfica e atividade microbiana em diferentes sistemas de manejo do solo na cultura do tabaco. Curr Agric Sci Technol. 2013;19:56-66.) e 10 dias (Villatoro, 2004Villatoro MAA. Matéria orgânica e indicadores biológicos da qualidade do solo na cultura de café sob manejo agroflorestal e orgânico [tese]. Seropédica: Universidade Federal Rural do Rio de Janeiro; 2004.; Sandler et al., 2010Sandler R, Falco LB, Ciocco C, Luca R, Coviella CE. Eficiencia del embudo Berlese-Tullgren para extracción de artrópodos edáficos en suelos arguidoles típicos de la Provincia de Buenos Aires. Ci Suelo (Argentina). 2010;28:1-7.).
A captura por meio do uso de armadilhas de queda (pitfall) tem sido usada amplamente em razão da sua praticidade, e os procedimentos têm recebido adaptações variadas. Conforme expôs Woodcock (2005)Woodcock BA. Pitfall trapping in ecological studies. In: Leather SR, editor. Insect sampling in forest ecosystems. Victoria, Australia: Blackwell Science; 2005. p.37-57., esse método, simples e de baixo custo, foi inicialmente concebido por Hertz em, 1927, e utilizado por Barber, em 1931. Originalmente desenvolvido como técnica qualitativa, foi, posteriormente, reconhecido o potencial do método para a amostragem quantitativa da população epígea de invertebrados (Woodcock, 2005Woodcock BA. Pitfall trapping in ecological studies. In: Leather SR, editor. Insect sampling in forest ecosystems. Victoria, Australia: Blackwell Science; 2005. p.37-57.).
A armadilha de Tretzel e suas variações como a tipo Provid são técnicas em que se instalam recipientes de plástico enterrados no solo de maneira que suas bordas fiquem niveladas com a superfície do terreno (Antonioli et al., 2006). Os recipientes contêm solução aquosa com composição determinada pelo pesquisador (formol, álcool, detergente), visando à morte e conservação dos organismos capturados. Por suas características, são capturados os animais que constituem a fauna epígea, tanto da macro como da mesofauna. O tempo de permanência das armadilhas não é uniforme: a proposição mais frequente é a de sete dias (Antoniolli et al., 2006Antoniolli Z, Conceição P, Böck V, Port O, Silva D, Silva R. Método alternativo para estudar a fauna do solo. Ci Flor. 2006;16:407-17.; Krolow, 2009Krolow DRV. Estudo da macro e mesofauna do solo em um sistema de produção de base ecológica [tese]. Pelotas: Universidade Federal de Pelotas; 2009.; Silva et al., 2012Silva RF, Scheid DL, Corassa GM, Bertollo GM, Kuss CC, Lamego FP. Influência da aplicação de herbicidas pré-emergentes na fauna do solo em sistema convencional de plantio de cana-de-açúcar. R Biotemas. 2012;25:227-38., 2014Silva RF, Bertollo GM, Corassa GM, Cocco LB, Steffen RB, Basso CJ. Doses de dejeto líquido de suínos na comunidade da fauna edáfica em sistema plantio direto e cultivo mínimo. Ci Rural. 2014;44:418-24.; Nunes et al., 2012Nunes LPL, Silva DIB, Araújo ASF, Leite LFC, Correia MEF. Caracterização da fauna edáfica em sistemas de manejo para produção de forragens no Estado do Piauí1. R Ci Agron. 2012;43:30-7.; Cezar, 2013Cezar RM. Parâmetros biológicos de solos em sistemas agroflorestais multiestrata sucessional e regeneração natural [dissertação]. Curitiba: Universidade Federal do Paraná; 2013.; Brito et al., 2014Brito M, Tsujigushi B, Gomes S, Silva R, Otsubo A, Mercante FM. Atributos microbiológicos e fauna invertebrada epigeica do solo em cultivo de milho consorciado com leguminosas. Cad Agroecol. 2014;9:1-12.), mas há relatos com coletas em um dia (Araújo et al, 2010Araújo C, Nomelini QS, Pereira J, Liporacci H, Kataguiri V. Comparação da abundância de invertebrados de solo por meio da estimação intervalar encontrados em diferentes ambientes na cidade de Ituiutaba - MG. Biosci J. 2010;26:817-23.), dois dias (Ogedegbe e Egwuonwu, 2014Ogedegbe ABO, Egwuonwu IC. Biodiversity of soil Arthropods in Nigerian Institute for Oil Palm Research (NIFOR), Nigeria. J Appl Sci Environ Manage. 2014;18 377-86.), três dias (Baretta et al., 2008Baretta D, Ferreira CS, Souza J, Cardoso EJBN. Colêmbolos (Hexapoda: Collembola) como bioindicadores de qualidade do solo em áreas comAraucaria angustifolia. R Bras Ci Solo.2008;32:2693-9. Número especial.), quatro dias (Rovedder et al., 2004Rovedder AP, Antoniolli ZI, Spagnollo E, Venturini SF. Fauna edáfica em solo suscetível à arenização na região sudoeste do Rio Grande do Sul. R Ci Agrovet. 2004;3: 87-96.) e permanência das armadilhas por 21 dias, com retirada do material biológico a cada sete dias (Cristofolini, 2011Cristofolini J. Fauna edáfica como indicador da recuperação ambiental em três áreas distintas às margens do rio Itajaí-Açu, Apiúna, SC [dissertação]. Blumenau: Universidade Regional de Blumenau; 2011.). Aquino et al. (2006)Aquino AM, Aguiar-Menezes E, Queiróz J. Recomendações para coleta de artrópodes terrestres por armadilhas de queda (Pitfall Traps). Seropédica: Embrapa Agrobiologia; 2006. (Circular Técnica, 18).expuseram os cuidados para uso das armadilhas de queda.
Os resultados têm sido interpretados com o emprego de índices como os de Shannon-Weaver, Simpson, Pielou, entre outros, visando caracterizar riqueza, abundância, dominância, equabilidade e qualidade do solo (Araújo e Monteiro, 2007Araújo A, Monteiro R. Indicadores biológicos de qualidade do solo. Biosci J. 2007;23:66-75.; Baretta et al., 2008Baretta D, Ferreira CS, Souza J, Cardoso EJBN. Colêmbolos (Hexapoda: Collembola) como bioindicadores de qualidade do solo em áreas comAraucaria angustifolia. R Bras Ci Solo.2008;32:2693-9. Número especial.; Estevam, 2011Estevam R. Uso de atributos físicos, químicos, biológicos e bioquímicos para a indicação e predição de degradação em solo de Tabuleiro Costeiro [dissertação]. Cruz das Almas: Universidade Federal do Recôncavo da Bahia; 2011.; Silva et al., 2014Silva RF, Bertollo GM, Corassa GM, Cocco LB, Steffen RB, Basso CJ. Doses de dejeto líquido de suínos na comunidade da fauna edáfica em sistema plantio direto e cultivo mínimo. Ci Rural. 2014;44:418-24.; Martínez-Falcón et al., 2015Martínez-Falcón AP, Moreno CE, Pavón NP. Litter fauna communities and litter decomposition in a selectively logged and an unmanaged pine-oak forest in Mexico. Bosque. 2015;36: 81-93.).
Em razão da ampla adoção do método Berlese, um dos objetivos deste trabalho foi definir o período de tempo de permanência do material de solo no extrator Berlese-Tüllgren para a captura de organismos da mesofauna. Adicionalmente, determinar o tempo mínimo de extração para a correta utilização dos índices de Shannon, Simpson e Pielou,usualmente empregados na avaliação da diversidade, dominância e equabilidade das comunidades dos componentes da mesofauna edáfica.
MATERIAL E MÉTODOS
O estudo foi conduzido em uma área experimental do Departamento de Solos do Instituto de Agronomia da Universidade Federal Rural do Rio de Janeiro, situada no km 7 da BR 465, no município de Seropédica, Rio de Janeiro. O preparo inicial do terreno foi realizado por meio de aração e gradagem. O solo dessa área, originalmente Argissolo Vermelho-Amarelo, foi altamente antropizado por causa de o terreno ter sido destinado anteriormente a outras atividades. Foram instaladas parcelas experimentais com os seguintes tratamentos: feijão-de-porco (Canavalia ensiformis), mucuna-preta (Mucuna aterrima), feijão-bravo-do-Ceará (Canavalia brasiliensis), guandu (Cajanus cajan) e vegetação espontânea. O delineamento utilizado foi o quadrado latino com cinco tratamentos, com emprego de parcelas com dimensões de 3 × 5 m. A vegetação predominante no local antes da instalação do experimento era formada, predominantemente, pelas espécies Hemarthria altíssima, Panicum maximum e Sorghum halepense. Em cada uma das unidades experimentais, foi coletada amostra formada por serapilheira e material de solo, nos primeiros 5 cm da camada superficial do solo, com a utilização de cilindro metálico com 0,15 m de diâmetro. A primeira coleta foi realizada um dia antes do plantio das leguminosas (outubro), com o objetivo de quantificar os organismos da mesofauna, caracterizando-se previamente a comunidade em cada parcela. Posteriormente, por ocasião do corte da parte aérea das plantas (março), foi feita nova amostragem, também em cada uma das parcelas experimentais, adotando-se o mesmo método já descrito.
Após a coleta, as amostras foram submetidas a uma bateria de extratores do tipo Berlese-Tüllgren, por um período de 15 dias, realizando-se a contagem diária dos organismos, a fim de se obter o tempo necessário para completa extração.
A partir da contagem e identificação em nível de grupo (Ordem/Família) dos organismos capturados, foram calculados, conforme Barros (2007)Barros RSM. Medidas de diversidade biológica. Juiz de Fora: Universidade Federal de Juiz de Fora; 2007., os seguintes índices de biodiversidade: índice de riqueza de Margalef, dado por I = [(S - 1)]/ln N, em que I é a diversidade; S, o número de espécies presente; e N, o número total de indivíduos encontrados na amostra; índice de Simpson, forma de dominância dada por D = Σ (ni/N)2, sendo ni = número de indivíduos do grupo “i” e N = somatório da densidade de todos os grupos; índice de Diversidade de Shannon (H = -ΣPi lnPi), em quePi é a proporção do grupo i no total da amostra; e índice de equabilidade de Pielou definido por: J = H/ln S, em que H corresponde ao índice de Shannon e S é o número total de grupos na comunidade. A riqueza dos grupos taxonômicos foi indicada pelo número de grupos presentes no tratamento.
Para determinar o tempo de extração adequado para o uso dos índices de diversidade, foi calculada a correlação por ordem de Kendall entre os valores obtidos dia a dia até o 8º dia de extração, usando-se o índice de Shannon como referência.
RESULTADOS E DISCUSSÃO
Os totais de organismos capturados em cada ocasião de coleta estão apresentados nosquadros 1 e 2. Além da grande diferença na quantidade total de organismos encontrados na segunda coleta, nela constatou-se a presença de Protura, larva de Diptera, Orthoptera e Trichoptera, não detectados na primeira coleta. As diferenças em quantidade e riqueza de grupos taxonômicos podem ser atribuídas a efeitos de preparo inicial do terreno, com distúrbios que interferiram na comunidade da mesofauna; à resiliência de organismos e adição de matéria orgânica decorrente da cobertura vegetal nas parcelas. As razões das diferenças detectadas entre as ocasiões das coletas não estão abordadas neste trabalho, em virtude de o seu escopo estar centralizado na variação da quantidade de espécimes capturados em cada dia.
Número de indivíduos capturados por grupo de organismos e total coletados dia a dia, na primeira avaliação
Número de indivíduos capturados por grupo de organismos e total coletados dia a dia, na segunda avaliação
Considerando o conjunto dos espécimes, a maioria dos organismos foi capturada até o 8º dia da extração (Figura 1). Ao se fazer o exame de cada grupo de organismos, os espécimes de Acari, Formicideae, Simphyla, Diptera, Chilopoda, Isoptera, Isopoda, Diplopoda, Protura e larvas de Coleoptera e Diptera tiveram mais de 95 % de seus representantes capturados até o 5º dia de extração, nas duas épocas avaliadas. Collembola diferiu ligeiramente dos demais, superando 95 % no 4º dia em março e alcançando 96 % no 6º dia em outubro. Os organismos que demandaram mais tempo para sua completa extração foram Thysanoptera e Coleoptera.
Variação diária do índice de Simpson (D), em razão da quantidade de organismos capturados, discriminada por época de avaliação: em outubro, um dia antes do plantio das leguminosas; e, em março, por ocasião do corte da parte aérea das plantas.
As diferenças na taxa de captura dos distintos organismos podem ser atribuídas aos hábitos particulares de cada grupo, incluindo-se sua mobilidade e resistência às condições adversas provocadas pelo sistema de captura.
Os dados obtidos merecem a ressalva de os organismos não terem sido identificados taxonomicamente em nível de espécie e restringem-se às condições experimentais prevalentes no local. Contudo, a consistência dos dados sugere que é possível a redução do tempo de permanência das amostras de material de solo nos funis Berlese-Tüllgren, dependendo dos objetivos. Entretanto, para a maioria dos organismos, esses dados indicam não ser recomendada a adoção de período de tempo inferior a seis dias para avaliar a composição da mesofauna edáfica, quando se utiliza a sistemática de processamento das amostras com o funil Berlese-Tüllgren.
A seleção do método a ser empregado deve considerar suas vantagens, sua praticidade, o tipo de organismo avaliado e a limitação de cada técnica. Entre as limitações do método que utiliza os funis de Berlese-Tüllgren figuram a possibilidade de fuga de organismos durante a coleta das amostras, a localização do ponto de amostragem e a não detecção de formas imaturas e de baixa mobilidade, o que pode levar a distorções na avaliação (Sandler et al., 2010Sandler R, Falco LB, Ciocco C, Luca R, Coviella CE. Eficiencia del embudo Berlese-Tullgren para extracción de artrópodos edáficos en suelos arguidoles típicos de la Provincia de Buenos Aires. Ci Suelo (Argentina). 2010;28:1-7.). O emprego de monólitos de terra e posterior flotação não separam organismos vivos dos já mortos, mas permite obter as formas imaturas e as de restrita mobilidade. As armadilhas de queda capturam os organismos com alta atividade na superfície do terreno e não avalia os demais.
Comparando o método de armadilha de queda com o extrator Berlese-Tüllgren, Ogedegbe e Egwuonwu (2014)Ogedegbe ABO, Egwuonwu IC. Biodiversity of soil Arthropods in Nigerian Institute for Oil Palm Research (NIFOR), Nigeria. J Appl Sci Environ Manage. 2014;18 377-86. verificaram que o primeiro permitiu número mais reduzido de espécimes capturados nos dois locais estudados. Nesse estudo, deve ser considerado que o uso de tempo reduzido (48 h, nos dois métodos) para captura dos organismos restringe o alcance dessa conclusão. Na avaliação feita por Krolow (2009)Krolow DRV. Estudo da macro e mesofauna do solo em um sistema de produção de base ecológica [tese]. Pelotas: Universidade Federal de Pelotas; 2009., tanto a armadilha de Tretzel quanto os funis de Berlese-Tüllgren dão resultados satisfatórios. Na mesma linha de investigação, Quemer e Bruckner (2010)Quemer P, Bruckner A. Combining pitfall traps and soil samples to collect Collembola for site scale biodiversity assessments. Appl Soil Ecol. 2010;45:293-7. concluíram que a combinação dos dois procedimentos leva a um resultado mais adequado, especialmente para a avaliação da população de colêmbolos.
Em trabalho projetado para a verificação de método alternativo ao da armadilha de Tretzel, Antoniolli et al. (2006)Antoniolli Z, Conceição P, Böck V, Port O, Silva D, Silva R. Método alternativo para estudar a fauna do solo. Ci Flor. 2006;16:407-17. detectaram que os grupos predominantes foram Acarina, Collembola e Himenoptera em todas as áreas, correspondendo a 20,75 % (496 indivíduos), 47,49 % (1.135 indivíduos) e 17,87 % (427 indivíduos), respectivamente, perfazendo juntos 86,11 % do total de organismos coletados pelo método Tretzel modificado. Para o método Provid, dos indivíduos coletados, 10,74 % (345 indivíduos) pertenciam ao grupo Acarina; 35,56 % (1.142 indivíduos) ao grupo Collembola; e 42,4 % (1.362 indivíduos) ao grupo Himenoptera, sendo esses três grupos equivalentes a 88,72 % do total de indivíduos coletados por esse método. Estudando a ocorrência de colêmbolos em florestas deAraucaria angustifolia, Baretta et al. (2008)Baretta D, Ferreira CS, Souza J, Cardoso EJBN. Colêmbolos (Hexapoda: Collembola) como bioindicadores de qualidade do solo em áreas comAraucaria angustifolia. R Bras Ci Solo.2008;32:2693-9. Número especial. constataram que as áreas apresentaram grande variabilidade em termos da distribuição da abundância e diversidade de famílias de colêmbolos. Esses autores consideraram que, para trabalhos de avaliação da diversidade de Collembola, além da utilização de armadilhas, sejam também utilizados métodos de amostragens complementares, como a coleta de solo e extração com funil de Berlese-Tüllgren, visando à extração de maior diversidade de famílias.
No que tange à distribuição de grupos edáficos, em alguns sistemas naturais e modificados da Amazônia Central foi registrado que os grupos Acari, Collembola e Formicideae foram dominantes, com abundâncias relativas máximas de 87, 29 e 6 %, respectivamente (Antony, 1997Antony LMK. Abundância e distribuição da fauna vertical do solo de ecossistemas amazônicos naturais e modificados. In: Anais do 26º Congresso Brasileiro de Ciência do Solo; 1997; Rio de Janeiro [CD-ROM]. Rio de Janeiro; Sociedade Brasileira de Ciência do Solo; 1997.).
Considerando a forma de manejo – plantio direto ou cultivo mínimo – as ordens Collembola e Acarina foram as mais abundantes, representando, respectivamente, 61,7 e 29,2 % do total de indivíduos no cultivo mínimo; e 77,7 e 12 %, no plantio direto (Silva et al., 2014Silva RF, Bertollo GM, Corassa GM, Cocco LB, Steffen RB, Basso CJ. Doses de dejeto líquido de suínos na comunidade da fauna edáfica em sistema plantio direto e cultivo mínimo. Ci Rural. 2014;44:418-24.).
Dentre os insetos sociais, destacam-se Isoptera e Hymenoptera; a maior parte dos indivíduos Hymenoptera (aproximadamente 99 %) é da família Formicideae. Pellens (1996)Pellens R. A comunidade de macroartrópodos edáficos deAcacia mangium Wild, Eucalyptus grandisHill, Coffea robusta Linden e de floresta primária [dissertação]. Rio de Janeiro: Universidade Federal do Rio de Janeiro; 1996. afirmou que, independentemente de qualquer problema metodológico, as formigas e as térmitas não apenas estão presentes em todos os sítios de estudo como também representam fração importante da comunidade de macroartrópodes edáficos.
É consistente a constatação de serem Acari, Collembola e Formicideae os organismos mais frequentes nos diversos ambientes pesquisados, com a abundância maior de um ou outro grupo oscilando em razão das características próprias de cada área pesquisada. Essa situação foi também verificada neste estudo.
Diante do exposto, pode-se inferir que nenhum dos métodos, isoladamente, permite a detecção de todos os espécimes e as espécies de organismos.
Os índices de diversidade, como era de se esperar, apresentaram variação compatível com as diferenças apresentadas no que concerne à quantidade de espécimes capturados a cada dia da avaliação.
A variação dos valores calculados para os diversos índices e relacionada com a comparação entre as épocas (outubro e março) de coleta das amostras de material do solo está apresentada nas figuras 1, 2, 3 e4. Ao se considerarem os dados referentes à primeira coleta (outubro), deve ser ressaltado que nessa ocasião a amostragem foi feita antes da instalação dos tratamentos. Assim, pode se admitir que as diferenças entre as parcelas estivessem condicionadas pela variabilidade espacial da área, e o conjunto dos dados pode ser entendido como reflexo de uma comunidade. Nesse pressuposto, as oscilações dos diversos índices são menores do que as verificadas na avaliação realizada com as amostras coletadas em março do ano seguinte, onde os efeitos dos tratamentos levaram às diferenças mais marcantes.
Variação diária do índice de Shannon (H’), por causa da quantidade de organismos capturados, discriminada por época de avaliação: em outubro, um dia antes do plantio das leguminosas; e, em março, por ocasião do corte da parte aérea das plantas.
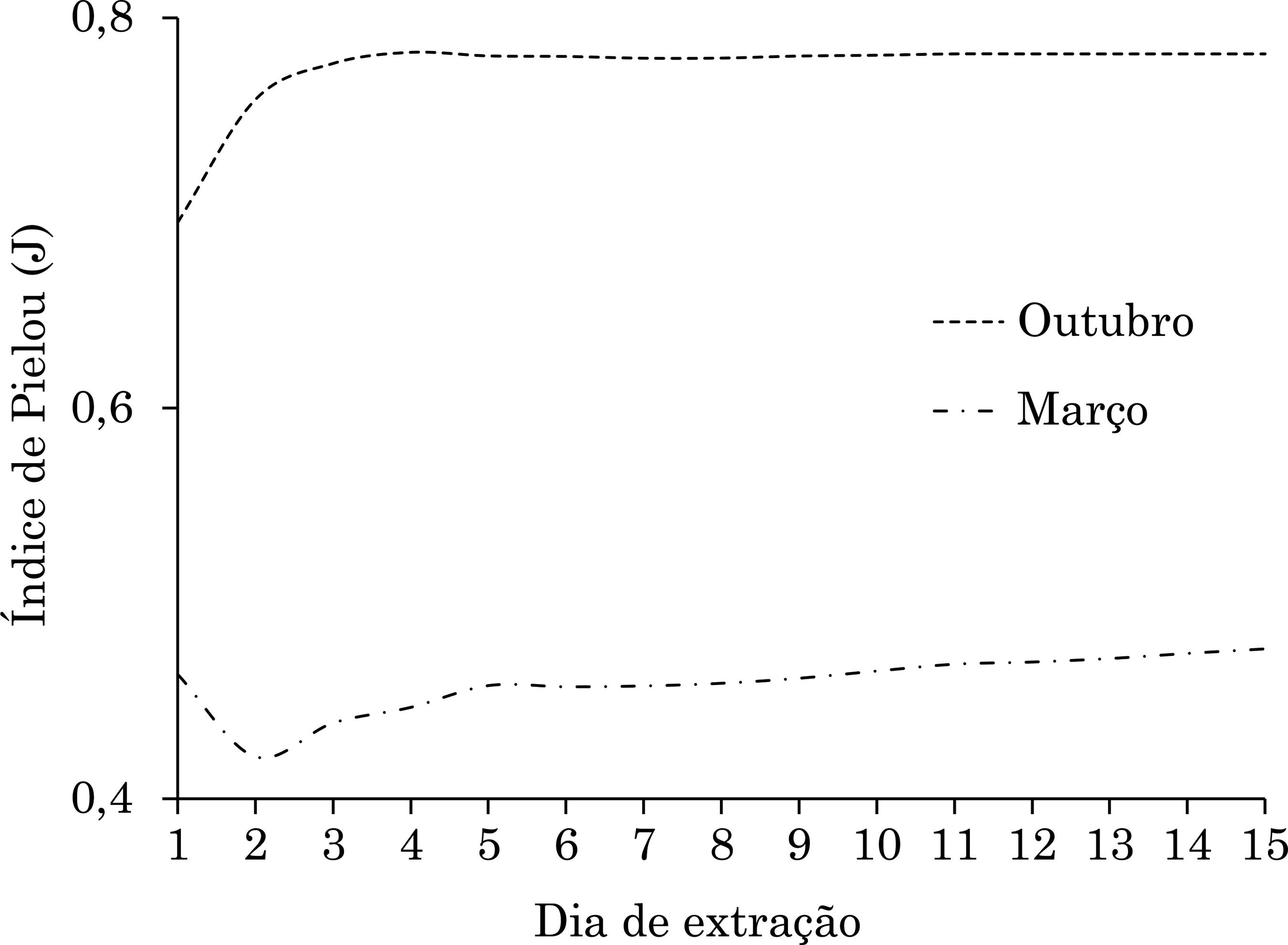
Variação diária do índice de Pielou (J), em razão da quantidade de organismos capturados, discriminada por época de avaliação: em outubro, um dia antes do plantio das leguminosas; e, em março, por ocasião do corte da parteaérea das plantas.
Variação diária do índice de Margalef (I), por causa da quantidade de organismos capturados, discriminada por época de avaliação: em outubro, um dia antes do plantio das leguminosas; e, em março, por ocasião do corte da parte aérea das plantas.
A utilização de período de tempo inferior a quatro dias, para avaliar os índices de diversidade em uma comunidade menos heterogênea, não permite inferências adequadas sobre a diversidade ecológica da mesofauna edáfica (Figuras 1, 2, 3 e 4).
Quando são apreciados os efeitos dos tratamentos (Figuras 5, 6 e 7), há mudança no que concerne ao tempo mínimo para obter índices confiáveis. Os efeitos de cada tratamento induzem a modificação da interpretação feita quando os dados são agrupados. Isso pode ser atribuído às variações de riqueza, à abundância e diversidade próprias de cada comunidade influenciada pelas condições geradas pela adoção de revestimento vegetal diferente. No quadro 3, estão apresentadas as quantidades totais de organismos capturados e discriminados por tratamento e a riqueza de grupo. Na figura 8, visualiza-se a variação diária da quantidade de organismos capturados, também contemplada por tratamentos.
Variação diária do índice de Simpson (D), em razão da quantidade de organismos capturados, discriminada por tratamentos [feijão-de-porco (Canavalia ensiformis), mucuna-preta (Mucuna aterrima), feijão-bravo-do-Ceará (Canavalia brasiliensis), guandu (Cajanus cajan) e vegetação espontânea], referente à segunda coleta.
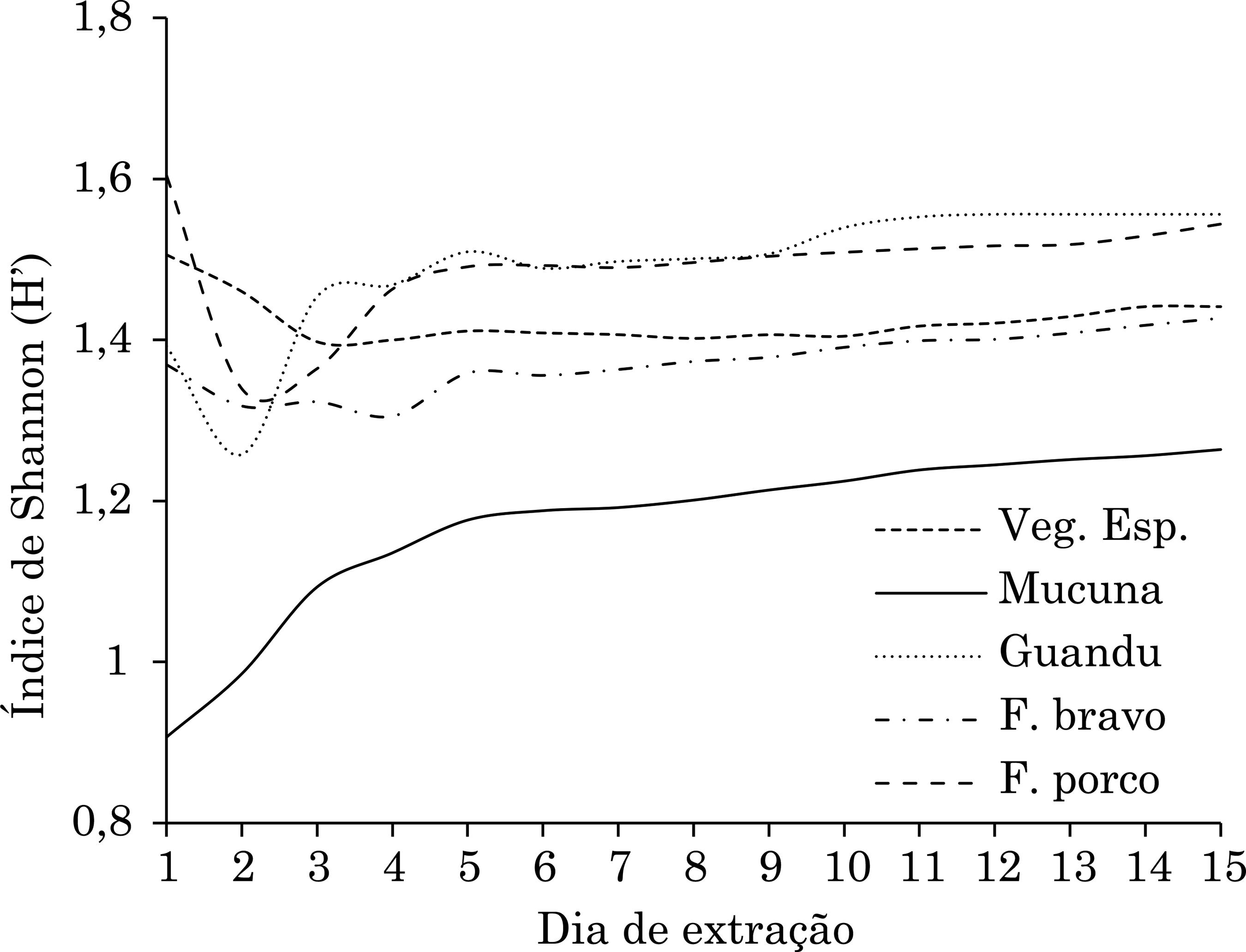
Variação diária do índice de Shannon (H’), por causa da quantidade de organismos capturados, discriminada por tratamentos [feijão-de-porco (Canavalia ensiformis), mucuna-preta (Mucuna aterrima), feijão-bravo-do-Ceará (Canavalia brasiliensis), guandu (Cajanus cajan) e vegetação espontânea], referente à segunda coleta.
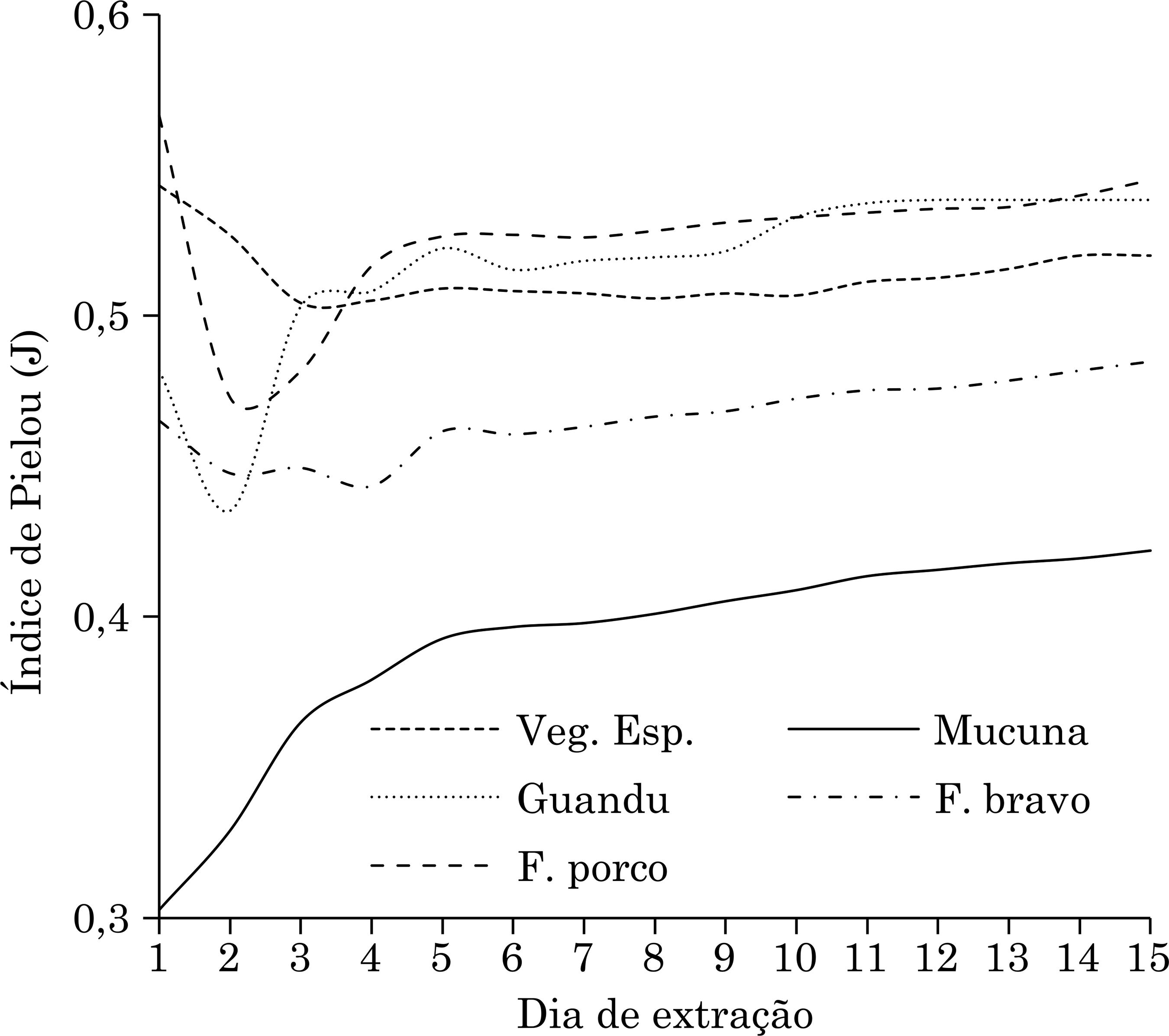
Variação diária do índice de Pielou (J), em razão da quantidade de organismos capturados, discriminada por tratamentos [feijão-de-porco (Canavalia ensiformis), mucuna-preta (Mucuna aterrima), feijão-bravo-do-Ceará (Canavalia brasiliensis), guandu (Cajanus cajan) e vegetação espontânea], referente à segunda coleta.
Variação diária da quantidade de organismos capturados, discriminada por tratamentos [feijão-de-porco (Canavalia ensiformis), mucuna-preta (Mucuna aterrima), feijão-bravo-do-Ceará (Canavalia brasiliensis), guandu (Cajanus cajan) e vegetação espontânea], referente à segunda coleta.
Para confirmar o tempo mínimo de permanência no funil de Berlese-Tüllgren adequado para inferências mais consistentes tanto no que concerne à quantidade de organismos capturados e quanto para a avaliação dos índices de diversidade, foi calculada a correlação por ordem de Kendall, cujos resultados estão apresentados no quadro 4. A correlação por ordem de Kendall é um teste estatístico de associação entre duas variáveis mensuradas em nível ordinal (postos). Utilizaram-se o índice de Shannon como referência para a tomada de decisão e os dados referentes à avaliação do 8º dia de extração da 2ª coleta, quando já estavam estabilizados os valores calculados, visando dar mais simplicidade nessa avaliação. Os resultados apresentados sugerem que, para o número total de organismos, sem considerar Ordem/Família, são necessários quatro dias de permanência no extrator de Berlese-Tüllgren, enquanto a interpretação mais apropriada do índice de Shannon se dá a partir do 6º dia.
Coeficientes de correlação por ordem de Kendall, determinados para o índice de Shannon, e número total de organismos capturados, acumulado dia a dia, referentes à segunda coleta
CONCLUSÕES
Em ambiente menos heterogêneo, a utilização de período de tempo de captura dos organismos inferior a quatro dias para avaliar os índices de diversidade não permite inferências adequadas sobre a diversidade ecológica da mesofauna edáfica.
Em ambiente mais heterogêneo, o tempo mínimo de permanência no funil de Berlese-Tüllgren adequado para obter dados mais consistentes e confiáveis para avaliar os índices de diversidade é de pelo menos seis dias.
REFERÊNCIAS
- Antonini Y, Colli G, Accacio G, Constantino R, Franceschinelli E, Laps R, Scariot A, Vieira M, Wiederhecker H. Fragmentação dos ecossistemas e a biodiversidade brasileira: uma síntese. In: Rambaldi D, Oliveira D, editores. Fragmentação de ecossistemas: causas, efeitos sobre a biodiversidade e recomendações de políticas públicas. Brasília, DF: Ministério do Meio Ambiente; 2003. p.317-24.
- Antoniolli Z, Conceição P, Böck V, Port O, Silva D, Silva R. Método alternativo para estudar a fauna do solo. Ci Flor. 2006;16:407-17.
- Antony LMK. Abundância e distribuição da fauna vertical do solo de ecossistemas amazônicos naturais e modificados. In: Anais do 26º Congresso Brasileiro de Ciência do Solo; 1997; Rio de Janeiro [CD-ROM]. Rio de Janeiro; Sociedade Brasileira de Ciência do Solo; 1997.
- Aquino AM, Aguiar-Menezes E, Queiróz J. Recomendações para coleta de artrópodes terrestres por armadilhas de queda (Pitfall Traps). Seropédica: Embrapa Agrobiologia; 2006. (Circular Técnica, 18).
- Araújo A, Monteiro R. Indicadores biológicos de qualidade do solo. Biosci J. 2007;23:66-75.
- Araújo C, Nomelini QS, Pereira J, Liporacci H, Kataguiri V. Comparação da abundância de invertebrados de solo por meio da estimação intervalar encontrados em diferentes ambientes na cidade de Ituiutaba - MG. Biosci J. 2010;26:817-23.
- Assad MLL. Fauna do solo. In: Vargas MAT, Hungria M, editores. Biologia dos solos dos Cerrados. Planaltina: Embrapa Soja; 1997. p.363-443.
- Baretta D, Ferreira CS, Souza J, Cardoso EJBN. Colêmbolos (Hexapoda: Collembola) como bioindicadores de qualidade do solo em áreas comAraucaria angustifolia R Bras Ci Solo.2008;32:2693-9. Número especial.
- Barros RSM. Medidas de diversidade biológica. Juiz de Fora: Universidade Federal de Juiz de Fora; 2007.
- Barros Y, Melo V, Sautter K, Buschle B, Oliveira E, Azevedo J, Souza L, Kummer L. Indicadores de qualidade de solos de área de mineração e metalurgia de chumbo. II - Mesofauna e plantas. R Bras Ci Solo. 2010;34:1413-26.
- Brito M, Tsujigushi B, Gomes S, Silva R, Otsubo A, Mercante FM. Atributos microbiológicos e fauna invertebrada epigeica do solo em cultivo de milho consorciado com leguminosas. Cad Agroecol. 2014;9:1-12.
- Cezar RM. Parâmetros biológicos de solos em sistemas agroflorestais multiestrata sucessional e regeneração natural [dissertação]. Curitiba: Universidade Federal do Paraná; 2013.
- Cristofolini J. Fauna edáfica como indicador da recuperação ambiental em três áreas distintas às margens do rio Itajaí-Açu, Apiúna, SC [dissertação]. Blumenau: Universidade Regional de Blumenau; 2011.
- Edwards CA, Fletcher KE Assessment of terrestrial invertebrate populations. In: Phillipson J, editor. Methods of study in soil ecology. Paris: Unesco, 1970. p.57-66.
- Estevam R. Uso de atributos físicos, químicos, biológicos e bioquímicos para a indicação e predição de degradação em solo de Tabuleiro Costeiro [dissertação]. Cruz das Almas: Universidade Federal do Recôncavo da Bahia; 2011.
- Ferreira R, Marques M. A fauna de artrópodes de serapilheira de áreas de monocultura com Eucalyptus sp e mata secundária heterogênea. An Soc Entomol Bras. 1998;27:95-403.
- Krolow DRV. Estudo da macro e mesofauna do solo em um sistema de produção de base ecológica [tese]. Pelotas: Universidade Federal de Pelotas; 2009.
- Lins V, Santos H, Gonçalves MC. The effect of the glyphosate, 2,4-D, atrazine e nicosulfuron herbicides upon the edaphic collembola (Arthropoda: Ellipura) in a no tillage system. Neotrop Entomol. 2007;36:261-7.
- Martínez-Falcón AP, Moreno CE, Pavón NP. Litter fauna communities and litter decomposition in a selectively logged and an unmanaged pine-oak forest in Mexico. Bosque. 2015;36: 81-93.
- Mineiro JC, Moraes GJ. Gamasida (Arachnida: Acari) Edáficos de Piracicaba, Estado de São Paulo. Neotrop Entomol. 2001;30:379-85.
- Morais JW, Oliveira, FL, Braga RF, Korasaki V. Mesofauna. In: Moreira FMS, Cares JE, Zanetti R, Stürmer SL, editores. O ecossistema solo: componentes, relações ecológicas e efeitos na produção vegetal. Lavras: Universidade Federal de Lavras; 2013. p.183-200.
- Nunes LPL, Silva DIB, Araújo ASF, Leite LFC, Correia MEF. Caracterização da fauna edáfica em sistemas de manejo para produção de forragens no Estado do Piauí1. R Ci Agron. 2012;43:30-7.
- Ogedegbe ABO, Egwuonwu IC. Biodiversity of soil Arthropods in Nigerian Institute for Oil Palm Research (NIFOR), Nigeria. J Appl Sci Environ Manage. 2014;18 377-86.
- Pass G, Szucsich NU. 100 years of research on the Protura: many secrets still retained. Soil Organ. 2011;83:309-34.
- Pellens R. A comunidade de macroartrópodos edáficos deAcacia mangium Wild, Eucalyptus grandisHill, Coffea robusta Linden e de floresta primária [dissertação]. Rio de Janeiro: Universidade Federal do Rio de Janeiro; 1996.
- Quemer P, Bruckner A. Combining pitfall traps and soil samples to collect Collembola for site scale biodiversity assessments. Appl Soil Ecol. 2010;45:293-7.
- Rossi CQ, Nobre CP, Coelho CP, Benazzi ESS, Rodrigues K, Correia MEF. Efeito de diferentes coberturas vegetais sobre a mesofauna edáfica em manejo agroecológico. R Bras Agroecol. 2009;4:1326-30.
- Rovedder AP, Antoniolli ZI, Spagnollo E, Venturini SF. Fauna edáfica em solo suscetível à arenização na região sudoeste do Rio Grande do Sul. R Ci Agrovet. 2004;3: 87-96.
- Sandler R, Falco LB, Ciocco C, Luca R, Coviella CE. Eficiencia del embudo Berlese-Tullgren para extracción de artrópodos edáficos en suelos arguidoles típicos de la Provincia de Buenos Aires. Ci Suelo (Argentina). 2010;28:1-7.
- São José JBS, Rieff G, Sá ELS. Mesofauna edáfica e atividade microbiana em diferentes sistemas de manejo do solo na cultura do tabaco. Curr Agric Sci Technol. 2013;19:56-66.
- Silva RF, Bertollo GM, Corassa GM, Cocco LB, Steffen RB, Basso CJ. Doses de dejeto líquido de suínos na comunidade da fauna edáfica em sistema plantio direto e cultivo mínimo. Ci Rural. 2014;44:418-24.
- Silva RF, Scheid DL, Corassa GM, Bertollo GM, Kuss CC, Lamego FP. Influência da aplicação de herbicidas pré-emergentes na fauna do solo em sistema convencional de plantio de cana-de-açúcar. R Biotemas. 2012;25:227-38.
- Souto PC, Souto JS, Miranda JP, Santos RV, Alves AR. Comunidade microbiana e mesofauna edáficas em solo sob caatinga no Semiárido da Paraíba. R Bras Ci Solo. 2008;32:151-60.
- Vieira MP. Mesofauna edáfica e a taxa de decomposição da resteva de três sucessões de cultura em sistema plantio direto [tese]. Dourados; Universidade Federal de Dourados; 2008.
- Villatoro MAA. Matéria orgânica e indicadores biológicos da qualidade do solo na cultura de café sob manejo agroflorestal e orgânico [tese]. Seropédica: Universidade Federal Rural do Rio de Janeiro; 2004.
- Woodcock BA. Pitfall trapping in ecological studies. In: Leather SR, editor. Insect sampling in forest ecosystems. Victoria, Australia: Blackwell Science; 2005. p.37-57.
Datas de Publicação
-
Publicação nesta coleção
Sep-Oct 2015
Histórico
-
Recebido
21 Fev 2015 -
Aceito
24 Jun 2015