Resumos
O objetivo deste trabalho foi avaliar o padrão espacial da variabilidade genética entre plantas, dentro de três populações naturais de barueiro (Dipteryx alata Vogel), pela genotipagem por RAPD e técnicas de autocorrelação espacial. Os cinco iniciadores RAPD permitiram a codificação de 45 locos, utilizados nas análises de diversidade, estrutura e distribuição espacial da variabilidade genética entre populações. As populações apresentaram diversidade genética (Hs) com valor médio 0,314. Verificou-se que 12% da variação total se encontra entre as populações, o que indica que estas mantêm um considerável nível de variabilidade genética. Foi observada tendência de autocorrelação espacial positiva nas primeiras classes de distâncias, nas três populações, o que indica a formação de grupos de vizinhança com estruturação familiar, dentro das populações de barueiro. Entretanto, o tamanho desses grupos de vizinhança varia entre as populações; isso mostra que outros processos ecológicos influenciaram a distribuição espacial da variabilidade genética. As populações naturais de barueiro apresentam consideráveis níveis de diversidade genética, com base nos 45 locos RAPD avaliados.
autocorrelação espacial; baru; conservação; estrutura familiar; fluxo gênico; RAPD
The aim of this paper was to evaluate the spatial pattern of the genetic variability among plants, within local populations of "barueiro" (Dipteryx alata Vogel), using RAPD markers and spatial autocorrelation analyses. The five RAPD primers used allowed the coding of 45 loci used for standard analyses of diversity, structure and spatial distribution of genetic variability within each local population. These populations showed considerable amount of genetic diversity, with an average Hs of 0.314. From the total genetic variation 12% occur among the three local populations studied, indicating that each of these contains a significant amount of variation. Within each population, this variability is structured with significant and positive spatial autocorrelation in the first three distance classes, suggesting the existence of neighbor groups of genetically similar individuals. The size of these neighbor groups, however, varies among local populations; this shows that other ecological components affected the spatial structure of genetic diversity. Natural populations of "barueiro" present considerable levels of genetic diversity, based on 45 RAPD loci analysed.
spatial autocorrelation; baru; conservation; familiar structure; genetic flow; RAPD
GENÉTICA
Distribuição espacial da variabilidade genética intrapopulacional de Dipteryx alata
Spatial distribution of intrapopulational genetic variability in Dipteryx alata
Thannya Nascimento SoaresI; Lázaro José ChavesI; Mariana Pires de Campos TellesII; José Alexandre Felizola Diniz-FilhoII; Lucileide Vilela ResendeIII
IUniversidade Federal de Goiás (UFG), Escola de Agronomia e Engenharia de Alimentos, Programa de PósGraduação em Agronomia, Campus Samambaia, Caixa Postal 131, CEP 74001-970 Goiânia, GO. E-mail: tnsoares@gmail.com, lchaves@agro.ufg.br
IIUFG, Instituto de Ciências Biológicas, Departamento de Biologia Geral, Campus Samambaia. E-mail: mpctelles@pq.cnpq.br, diniz@icb.ufg.br
IIISystema Naturae Consultoria Ambiental Ltda. Rua 58, nº 217, Jardim Goiás, CEP 74810-250 Goiânia, GO. E-mail: lvilelar@gmail.com
RESUMO
O objetivo deste trabalho foi avaliar o padrão espacial da variabilidade genética entre plantas, dentro de três populações naturais de barueiro (Dipteryx alata Vogel), pela genotipagem por RAPD e técnicas de autocorrelação espacial. Os cinco iniciadores RAPD permitiram a codificação de 45 locos, utilizados nas análises de diversidade, estrutura e distribuição espacial da variabilidade genética entre populações. As populações apresentaram diversidade genética (Hs) com valor médio 0,314. Verificou-se que 12% da variação total se encontra entre as populações, o que indica que estas mantêm um considerável nível de variabilidade genética. Foi observada tendência de autocorrelação espacial positiva nas primeiras classes de distâncias, nas três populações, o que indica a formação de grupos de vizinhança com estruturação familiar, dentro das populações de barueiro. Entretanto, o tamanho desses grupos de vizinhança varia entre as populações; isso mostra que outros processos ecológicos influenciaram a distribuição espacial da variabilidade genética. As populações naturais de barueiro apresentam consideráveis níveis de diversidade genética, com base nos 45 locos RAPD avaliados.
Termos para indexação: autocorrelação espacial, baru, conservação, estrutura familiar, fluxo gênico, RAPD.
ABSTRACT
The aim of this paper was to evaluate the spatial pattern of the genetic variability among plants, within local populations of "barueiro" (Dipteryx alata Vogel), using RAPD markers and spatial autocorrelation analyses. The five RAPD primers used allowed the coding of 45 loci used for standard analyses of diversity, structure and spatial distribution of genetic variability within each local population. These populations showed considerable amount of genetic diversity, with an average Hs of 0.314. From the total genetic variation 12% occur among the three local populations studied, indicating that each of these contains a significant amount of variation. Within each population, this variability is structured with significant and positive spatial autocorrelation in the first three distance classes, suggesting the existence of neighbor groups of genetically similar individuals. The size of these neighbor groups, however, varies among local populations; this shows that other ecological components affected the spatial structure of genetic diversity. Natural populations of "barueiro" present considerable levels of genetic diversity, based on 45 RAPD loci analysed.
Index terms: spatial autocorrelation, baru, conservation, familiar structure, genetic flow, RAPD.
Introdução
A distribuição espacial das plantas, dentro de uma população, pode ser considerada um dos fatores que influenciam o sistema de acasalamento que, com a dispersão de pólen e sementes, pode desempenhar grande efeito na estrutura espacial da variabilidade genética. Além disso, a estrutura genética espacial também é influenciada por processos microevolutivos e demográficos em curto e longo prazos (Epperson, 2003). Estrutura e processo podem estar intrinsecamente ligados e associados à influência de fatores ecológicos que afetam a reprodução, a dispersão e o tamanho do grupo de vizinhança, tornando-se particularmente importantes nesta determinação (Loveless & Hamrick, 1984).
Os mesmos fatores que levam ao isolamento por distância, entre populações de plantas, são também responsáveis pela subdivisão genética dentro das populações. A subdivisão genética local, ou estruturação em parentesco, resulta de um agrupamento espacial de indivíduos, que estão mais intimamente relacionados do que seria esperado em genótipos que estão distribuídos aleatoriamente (Heywood, 1991). Espécies de plantas com baixas densidades e bancos de semente discretos, desenvolvem estrutura genética espacial positiva em pequenas escalas, ou seja, as plantas mais próximas espacialmente são mais similares geneticamente do que o esperado pelo acaso. Em contraste, espécies com sobreposição de banco de sementes, alta taxa de fecundação cruzada, estabelecimento raro das plântulas e recrutamento distante da planta mãe devem apresentar pouca estruturação genética intrapopulacional (Cavers et al., 2005).
As técnicas moleculares tornaram possível distinguir a estrutura genética, dentro e entre populações, e têm auxiliado no esclarecimento dos padrões de fluxo gênico, dispersão e seleção (Cavers et al., 2005). Aliadas às técnicas de autocorrelação espacial, elas possibilitaram o aprimoramento dos métodos de análise e permitiram a estimativa do fluxo gênico aparente dentro de populações, com base na estrutura genética espacial entre plantas (Epperson, 2003; Fenster et al., 2003; Vekemans & Hardy, 2004; Diniz-Filho et al., 2008). Por meio desses métodos, a estrutura genética que tradicionalmente era avaliada apenas em grandes escalas espaciais, entre populações, passou também a ser feita em escala local (Degen, 2001b; Hardy, 2003).
O marcador RAPD é uma alternativa rápida, barata e eficiente para este tipo de análise, tanto por ser baseado em PCR, quanto por fornecer um padrão de informação genética multiloco, principalmente sobre espécies para as quais não estão disponíveis marcadores espécie-específicos (Degen et al., 2001a; Zucchi et al., 2005; Telles & Soares, 2007).
O Cerrado possui grande diversidade de plantas, entre as quais muitas apresentam grandes possibilidades de exploração, cujo maior potencial é sua utilidade na alimentação. O barueiro (Dipteryx alata Vogel) faz parte do grupo de espécies nativas usadas pela população regional como fonte complementar de renda familiar, pela exploração extrativista de seu fruto, o baru. É uma das espécies frutíferas nativas mais promissoras para cultivo, em razão do seu uso múltiplo, alta taxa de germinação de sementes e de estabelecimento de mudas. Em longo prazo, o uso do barueiro nas áreas a serem recuperadas como reservas legais e de proteção ambiental, margens de rios e córregos favorecerá a sua conservação e a manutenção de outras espécies associadas (Sano et al., 2004). Como a exploração se dá por extrativismo, e são ainda insuficientes as informações sobre a biologia e manejo do barueiro, é indispensável a realização de estudos que contribuam para direcionar estratégias mais eficientes para sua domesticação, conservação e uso sustentável (Silva et al., 1997). O barueiro também apresenta grande importância ecológica e é classificado como espécie-chave do Cerrado, pois seu fruto amadurece na seca e alimenta várias espécies da fauna dessa região, inclusive o gado (Sano et al., 2004).
O objetivo deste trabalho foi avaliar o padrão espacial da variabilidade genética entre plantas, dentro de três populações naturais de D. alata, pela genotipagem por meio de RAPD e técnicas de autocorrelação espacial.
Material e Métodos
As populações utilizadas neste trabalho fazem parte de um conjunto de dez populações, de um estudo prévio realizado por Soares et al. (2008). Para o presente trabalho, foram analisadas três populações, para as quais existe informação do posicionamento geográfico de cada planta, no total de 90 indivíduos. A primeira população, constituída de 32 plantas, encontra-se no Estado de São Paulo, no Município de Icém (população 1), em área com ambientes de pastagem e faixa de domínio de estrada. Em razão da grande distância entre as plantas, a área ocupada por esta população é ampla, com distâncias de até 8 km entre plantas. A segunda população, localizada no Estado de Minas Gerais, no Município de Monte Alegre, possui 31 plantas, que se encontram muito próximas umas das outras, em ambiente de cerradão, constituído de pequena área de coleta com aproximadamente 0,5 km de extensão. A terceira população foi amostrada em Luziânia, GO, em área mista entre pastagem e cerrado degradado, com extensão de aproximadamente 1 km, onde foram coletadas 27 plantas.
Das plantas de cada população, foram coletadas folhas - as mais jovens possível - que foram acondicionadas em sacos de papel pardo identificados com o número da planta e sua população de origem. Posteriormente, as amostras foram acondicionadas em caixas de isopor com gelo, para o transporte até o laboratório. Cada uma das plantas coletadas foi georreferenciada por aparelho GPS.
O trabalho foi realizado no Laboratório de Genética e Biodiversidade, da Universidade Católica de Goiás, em Goiânia, GO. O DNA foi extraído a partir de tecido foliar, conforme o protocolo de extração de DNA, para análises com RAPD descrito por Ferreira & Grattapaglia (1998). Este protocolo consiste em minipreparações de DNA, diretamente em microtubos, a partir de alguns miligramas (aproximadamente 150) de tecido vegetal, e utiliza o CBTA (cátion de brometo de hexadecil trimetil amônia), como detergente do tampão de extração. Após a extração, o DNA total foi quantificado, por comparação, com o perfil de bandas do marcador de peso molecular da Invitrogen; realizou-se, assim, a quantificação (em nanogramas por microlitro) do DNA de cada planta. Em seguida, foi realizada a diluição do DNA, para a concentração de trabalho de aproximadamente 2,5 ng µL-1.
Para a amplificação, foram utilizados cinco iniciadores (OPC-19, OPP-19, OPP-15, OPP-07 e OPP-08), previamente selecionados por Soares et al. (2008). A montagem das reações para a amplificação dos fragmentos de DNA, via PCR, foi realizada, inicialmente, com alíquotas de 3 µL do DNA colocados em microplacas para PCR. Em seguida, foram adicionados 10 µL de um coquetel com: 0,91 ng µL-1 de iniciador; 0,23 mol mL-1 de d'NTP; 1,17 X de tampão da enzima; 1,77 mol mL-1 de cloreto de magnésio (MgCl2); 0,05 U da enzima Taq polimerase; e 5,5 µL de água milliQ, para completar o volume final de 13 µL.
O programa para a amplificação dos fragmentos de DNA via PCR, no termociclador, apresenta os seguintes passos, com os tempos e temperaturas respectivos: 1º) desnaturação do DNA a 96ºC por 3 min; 2º) a 92°C por 1 min; 3º) anelamento do iniciador a 37ºC por 1 min; 4º) extensão da molécula pela enzima Taq polimerase a 72°C por 1 min; 5º) 40 ciclos do 2º ao 4º passo; 6º) extensão de 3 min a 72°C, para finalizar os produtos amplificados; 7º) programa completo. Para as amplificações, foram adotadas medidas de padronização para garantir a boa qualidade dos dados, principalmente no que diz respeito à reprodutibilidade das bandas. Todas as amplificações para um determinado iniciador foram realizadas no mesmo termociclador, com todas as plantas, o que minimizou possíveis problemas com relação à mudança nas condições de amplificação, que pode ocorrer entre diferentes termocicladores. Além disso, foi utilizado um programa de termociclagem com temperatura de anelamento mais alta (37°C) do que o comumente recomendado para RAPD, o que melhorou a estabilidade do pareamento do iniciador à região-alvo.
O produto amplificado foi submetido à eletroforese horizontal com gel de agarose 1,4%, imerso em tampão para eletroforese TBE à concentração de 1 X. Foram adicionados dois pentes em alturas diferentes no gel, que proporcionaram eletroforese "multiplex". Cada pente permite a formação de 49 poços. A cada 23 amostras, foi aplicada uma alíquota do marcador 100 pares de base, da Pharmacia Biotech, para auxiliar na codificação e obtenção dos genótipos nos géis.
A obtenção dos genótipos foi realizada tendo-se atribuído 1 para a presença e 0 para a ausência da banda no loco. Somente os locos cujas bandas estavam mais nítidas no gel foram utilizados, o que facilitou a distinção entre os locos de um gel para outro. Além disso, foram escolhidos somente os locos que se encontravam entre 1.600 e 300 pb, tendo sido respeitada uma determinada altura dos locos nos géis. Desta codificação, foi elaborada uma matriz de dados binários, utilizada para as análises genético-populacionais.
A diversidade genética foi avaliada, inicialmente, pelo nível de polimorfismo dos locos para os cinco iniciadores RAPD utilizados, tendo-se considerado todas as populações e cada uma separadamente, pela estimativa do número e proporção de locos (ou bandas) polimórficos. Nessa análise, o polimorfismo foi considerado a partir do critério pelo qual a freqüência da banda mais freqüente do loco é inferior a 99%. Em seguida, a diversidade genética, para cada população, foi avaliada por uma abordagem bayesiana, proposta por Holsinger (1999).
A distribuição da variabilidade genética dentro e entre as populações também foi avaliada pelo método bayesiano (Holsinger, 1999). As análises de diversidade e estrutura foram realizadas no programa Hickory versão 1.0 (Holsinger, 2003), que permite estimar o valor de θB por meio de quatro modelos diferentes. O utilizado no presente estudo foi o que assume o valor de , equivalente ao índice de fixação intrapopulacional de Weir & Cockerham (1984), igual a zero, isso porque este modelo se mostrou adequado para a estimativa de estrutura genética em populações de D. alata, com utilização do mesmo conjunto de dados (45 locos RAPD) (Soares et al., 2008).
As informações genéticas e geográficas (coordenadas geográficas em graus decimais) de cada planta, das três populações, foram utilizadas para estimar um índice de agregação (R) intrapopulacional e para as análises de estrutura espacial da variabilidade genética, em escala local (intrapopulacional), que foram realizadas no SGS versão 1.0 (Degen et al., 2001b). Esse índice de agregação, baseado no índice R, estimado para diferentes classes de distância geográfica, permite a inferência do padrão de distribuição espacial das árvores, em cada uma das populações. Os valores de R indicam: <1, distribuição agregada; 1, distribuição aleatória; e >1, associam-se à distribuição regular (Degen, 2000; Degen et al., 2001a; Hardesty et al., 2005).
As estimativas são realizadas entre os pares de pontos (árvores), ao longo das classes de distância espacial. Sugere-se que as análises sejam repetidas com diferentes intervalos na classe de distância, pois estas possuem a mesma amplitude, e, assim, se pode verificar sua influência nos resultados (Degen, 2000). No presente estudo, esse procedimento foi adotado para a escolha do número adequado de classes que aperfeiçoasse o número de pares de pontos por classe. Assim, procurou-se manter um número próximo a 30 pares de plantas por classe de distância (Degen, 2000), para garantir maior robustez estatística.
Para dados de marcadores dominantes, calcula-se a distância genética média (distância de Tanimoto) entre as plantas, dentro de cada uma das classes de distância espacial (Degen, 2000). Pelo fato de esta análise basear-se nas distâncias genéticas entre os indivíduos, a relação entre a distância genética média e cada classe de distância geográfica é medida por um gráfico denominado de distograma (Degen, 2000). A significância, em relação aos desvios da distribuição espacial aleatória, para cada classe, é obtida por um procedimento de permutação de Monte Carlo. A partir das permutações, com base em um limite de significância préestabelecido, é construído um intervalo de confiança para os parâmetros estimados (Degen et al., 2001b). No presente estudo, foram realizadas 1.000 permutações e foi considerado o limite de confiança de 95%.
Resultados e Discussão
Os cinco iniciadores RAPD, nas três populações de barueiro, permitiram a codificação de 45 locos, dos quais, em média, 26 foram polimórficos (58%), tendo-se considerado o critério de polimorfismo de 99%. O número de locos polimórficos em cada população foi 33, 24 e 22% em Icém, SP, Monte Alegre de Minas, MG, e Luziânia, GO, respectivamente. As populações apresentaram uma considerável diversidade genética (Hs), com valor médio de 0,314 (Tabela 1). Os níveis de diversidade genética detectados são relevantes para a conservação in situ do barueiro, pois possibilitam a ocorrência de novas recombinações genotípicas, o que mantém o potencial evolutivo da espécie (Reed & Frankham, 2003).
A análise de estruturação da variabilidade genética revelou que 12% da variação total se encontram entre as populações. Logo, 88% da variação total estão no componente intrapopulacional. O valor de θB estimado nestas três populações foi próximo ao encontrado (0,15) para as dez populações analisadas por Soares et al. (2008), o que indica que, embora o número de populações analisadas seja pequeno, estas mantêm um considerável nível de variabilidade genética que as distingue.
Os valores do índice de agregação foram 0,150, 0,545 e 0,424, nas populações 1, 2 e 3, respectivamente. Todos os valores são menores do que 1, o que indica que a espécie exibe um padrão espacial dos indivíduos de forma agregada (mesmo com a variação na extensão de amostragem de cada população). Esse padrão de agregação pode ser visualizado pela distribuição espacial das árvores nas populações (Figuras 1 A, 2 A e 3 A). De fato, é muito comum encontrar-se grande quantidade de plântulas ao redor de uma árvore adulta, e a literatura documenta que o barueiro tem distribuição irregular e forma, eventualmente, grandes agrupamentos homogêneos (Ribeiro et al., 2000; Sano et al., 2004). O valor mais baixo de agregação, na população 1, é conseqüência da maior extensão espacial ocupada por esta população.
Embora este estudo tenha sido realizado com o tamanho amostral de indivíduos e locos menores do que os sugeridos na literatura (cerca de 150 indivíduos por população e 100 marcas) (Cavers et al., 2005), foi possível detectar um padrão de estrutura genética espacial intrapopulacional, que mostrou tendência de relação positiva entre distância genética e geográfica, nas primeiras classes de distâncias (autocorrelação espacial positiva).
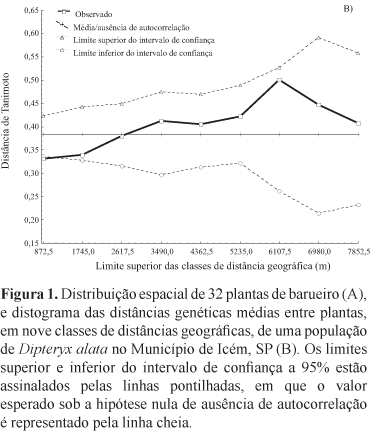
Na população de Icém as duas primeiras classes de distâncias, cujos limites superiores foram 872 e 1.745 m, apresentaram estrutura com relação positiva e significativa entre distância genética e geográfica, com valores médios de distância genética de Tanimoto de 0,33 e 0,34, respectivamente. As demais classes de distância não apresentaram valores significativos (Figura 1 B). Assim, pode-se considerar que existe a formação de uma estruturação em parentesco e que o tamanho do grupo de vizinhança, nessa população, ocupa área com diâmetro de cerca de 1.800 m.
A população de Monte Alegre de Minas exibiu um padrão espacial de estruturação em parentesco semelhante ao encontrado para a população de Icém, e mostrou autocorrelação positiva e significativa na primeira classe de distância (limite superior 40 m), cuja distância genética de Tanimoto foi de 0,21 (Figura 2 B). Entretanto, é importante lembrar que as árvores nessa população se encontravam mais agregadas, e que a área total da população é bem menor, de modo que o tamanho do grupo de vizinhança nessa população foi menor, com diâmetro de cerca de 40 m.
Diferentemente das populações de Icém e Monte Alegre de Minas, não foram encontrados valores significativos de estruturação genética espacial entre as plantas dentro da população de Luziânia (Figura 3 B). Os valores médios de distância de Tanimoto foram sempre próximos ao valor que indicava a ausência de estrutura espacial (distância de Tanimoto igual a 0,36), o que indica aleatoriedade na distribuição da variabilidade genética. Entretanto, essa estruturação suave pode ter sido decorrente do menor tamanho amostral utilizado no presente estudo (27 plantas), de modo que uma nova análise, com maior número de indivíduos e locos, deve ser realizada no sentido de se esclarecer o padrão espacial da variabilidade genética nessa população.
Ao se analisarem os resultados de estrutura genética espacial, nas populações de Icém e Monte Alegre de Minas, percebe-se que os grupos de vizinhança gerados em relação a essas populações apresentaram muita diferença de escala geográfica, o que tem conseqüência direta para a indicação do esquema de coleta de germoplasma com o objetivo de amostrar a maior quantidade de variabilidade genética, com a menor pseudo-replicação possível (Diniz-Filho & Telles, 2002). Portanto, se o objetivo for coletar indivíduos em grupos de vizinhança diferentes e maximizar a representatividade da variabilidade genética, deve-se respeitar a distância mínima de 1.800 m em Icém, mas apenas 40 m em Monte Alegre de Minas.
Esta diferença, provavelmente, deve estar relacionada à diversificação das características do ambiente, em cada população, o que inclui o fato de as duas apresentarem níveis variados de antropização. Essas características podem afetar a densidade dos indivíduos nas populações e, conseqüentemente, a estruturação espacial da variabilidade genética intrapopulacional. Uma hipótese a ser considerada é a de que na população de Icém, que se encontra em áreas cujo ambiente natural já está mais descaracterizado (com pastagens ou lavouras), a dispersão por animais, que alcança distâncias maiores, estaria sobrepondo os efeitos da dispersão por barocoria, já que as novas plântulas teriam muito menos chances de persistirem próximas à árvore mãe.
A densidade diferenciada nas populações pode ser uma das explicações para os padrões observados. Vekemans & Hardy (2004) compararam a estrutura espacial interna de populações (de diferentes espécies), com diferentes níveis de densidade, e verificaram que a estrutura genética espacial foi consistente e significativamente maior em populações com baixa densidade. De acordo com esses autores, a densidade populacional tem papel importante na determinação da estrutura genética espacial intrapopulacional, pois ela está associada à maneira como se dá a dispersão de pólen e de sementes dentro da população. De fato, Loveless & Hamrick (1984) esclareceram que a dispersão do pólen por animais é mais suscetível à densidade populacional, ou seja, em populações com alta densidade, o fluxo do pólen é restrito, o que aumenta a subdivisão. Portanto, pode-se concluir que populações com baixa densidade terão um efeito de autocorrelação em maiores distâncias e em mais de uma classe de distância geográfica.
A literatura mostra que os valores de densidade do barueiro são suscetíveis ao seu local de ocorrência; por exemplo, em áreas de cerrado denso ou matas, a densidade é maior do que no cerrado no sentido restrito. Em relação à mata semidecídua, foram relatadas densidades de 7 a 88 indivíduos por hectare, e no caso de cerrado denso e mata estacional, acima de 23 indivíduos adultos por hectare (Salis & Crispim, 2006). Em áreas de cerrado com murundus, foi observado um alto valor de densidade, de 143 indivíduos por hectare (Sano et al., 2004), e no cerrado sentido restrito, cerca de 5 indivíduos adultos por hectare (Felfili et al., 2002). Esses dados mostram como os fatores ambientais e ecológicos podem influenciar a estrutura das diferentes populações de uma mesma espécie, de modo que devem ser levados em conta, no momento de se sugerirem estratégias de coleta de germoplasma da espécie, seja para fins de conservação ou uso em um programa de melhoramento.
Os resultados deste estudo corroboram a hipótese de formação de grupos de vizinhança com estruturação familiar, dentro das populações de D. alata, como indicado por Sano et al. (1999), que observaram árvores de barueiro que apresentaram grupos distintos quanto às características de fruto e semente. Esta estruturação pode ser explicada tanto pelo tipo de dispersão barocórica - em que as sementes caem próximas às plantas mãe e germinam (e, ocasionalmente, as plântulas se desenvolvem no local) -, quanto pela dispersão por morcego, que possibilita que vários frutos de uma mesma árvore sejam levados para uma determinada área, onde o animal se alimenta e deixa as sementes nesse local.
Conclusões
1. As populações naturais de barueiro (Dipteryx alata) apresentam consideráveis níveis de diversidade genética, com base nos 45 locos RAPD analisados.
2. A variabilidade genética encontra-se estruturada entre as populações (12,4%).
3. A estrutura genética espacial intrapopulacional indica que a espécie tende a apresentar estruturação em parentesco e forma grupos de vizinhança, em diferentes escalas geográficas.
4. Existe relação entre a agregação das árvores dentro das populações e o tamanho da área do grupo de vizinhança, obtido a partir dos dados genéticos.
5. A coleta de sementes de árvores de D. alata muito próximas, considerando a densidade populacional, afeta a representatividade genética da amostra, pois leva à obtenção de um tamanho amostral efetivo inadequado para a conservação ou uso do germoplasma.
Agradecimentos
Ao Conselho Nacional de Desenvolvimento Científico e Tecnológico, pelo apoio financeiro e por concessão de bolsa; à equipe do Laboratório de Genética e Biodiversidade da Universidade Católica de Goiás, pelo apoio durante a coleta de dados moleculares; à Pró-Reitoria de Pós-Graduação e Pesquisa da Universidade Católica de Goiás, pelo apoio financeiro e logístico.
Recebido em 9 de abril de 2008 e aprovado em 19 de agosto de 2008
- CAVERS, S.; DEGEN, B.; CARON, H.; LEMES, M.R.; MARGIS, R.; SALGUEIRO, F.; LOWE, A.J. Optimal sampling strategy for estimation of spatial genetic structure in tree populations. Heredity, v.95, p.281-289, 2005.
- DEGEN, B. SGS: spatial genetic software: computer program and user's manual. 2000. Disponível em: <http://kourou.cirad.fr/genetique/software.html>. Acesso em: 14 mar. 2008.
- DEGEN, B.; CARON, H.; BANDOU, E.; MAGGIA, L.; CHEVALLIER, M.H.L.; LEVEAU, A.; KREMER, A. Finescale spatial genetic structure of eight tropical tree species as analysed by RAPDs. Heredity, v.87, p.497-507, 2001a.
- DEGEN, B.; PETIT, R.; KREMER, A. SGS: spatial genetic software: a computer program for analysis of spatial genetic and phenotypic structures of individuals and populations. Journal of Heredity, v.92, p.447-448, 2001b.
- DINIZ-FILHO, J.A.F.; TELLES, M.P. de C. Spatial autocorrelation analysis and the identification of operational units for conservation in continuous populations. Conservation Biology, v.16, p.924-935, 2002.
- DINIZ-FILHO, J.A.F.; TELLES, M.P. de C.; BONATTO, S.L.; EIZIRIK E.; FREITAS, T.R.O. de; MARCO, P. de; SANTOS, F.R.; SOLE-CAVA, A.; SOARES, T.N. Mapping the evolutionary twilight zone: molecular markers, populations and geography. Journal of Biogeography, v.35, p.753-763, 2008.
- EPPERSON, B.K. Geographical genetics New Jersey: Princeton University Press, 2003. 356p. (Monographs in Population Biology, 38).
- FELFILI, J.M.; NOGUEIRA, P.E.; SILVA JÚNIOR, M.C. da; MARIMON, B.S.; DELITTI, W.B.C. Composição florística e fitossociologia do cerrado sentido restrito no Município de Água Boa, MT. Acta Botanica Brasilica, v.16, p.103-112, 2002.
- FENSTER, C.B.; VEKEMANS, X.; HARDY, O.J. Quantifying gene flow from spatial genetic structure data in a metapopulation of Chamaecrista fasciculata (Leguminosae). Evolution, v.57, p.995-1007, 2003.
- FERREIRA, M.E.; Grattapaglia, D. Introdução ao uso de marcadores moleculares em análise genética 3.ed. Brasília: Embrapa Recursos Genéticos e Biotecnologia, 1998. 220p. (Embrapa Recursos Genéticos e Biotecnologia. Documentos, 20).
- HARDESTY, B.D.; DICK, C.W.; KREMER, A.; HUBBELL, S.; BERMINGHAM, E. Spatial genetic structure of Simarouba amara Aubl. (Simaroubaceae), a dioecious, animal-dispersed Neotropical tree, on Barro Colorado Island, Panama. Heredity, v.95, p.290-297, 2005.
- HARDY, O.J. Estimation of pairwise relatedness between individuals and characterization of isolation-by-distance processes using dominant genetic markers. Molecular Ecology, v.12, p.1577-1588, 2003.
- HEYWOOD, J.S. Spatial analysis of genetic variation in plant populations. Annual Review of Ecology and Systematics, v.22, p.335-355, 1991.
- HOLSINGER, K.E. Analysis of genetic diversity in geographically structured populations: a Bayesian perspective. Hereditas, v.130, p.245-255, 1999.
- HOLSINGER, K.E.; LEWIS, P.O. Hickory: software for analysis of population genetic data v.1.0. Storrs: University of Connecticut, 2003. Disponível em: <http://darwin.eeb.uconn.edu/hickory>. Acesso em: 14 mar. 2008.
- LOVELESS, M.D.; HAMRICK, J.L. Ecological determinants of genetic structure in plant populations. Annual Review of Ecology and Systematics, v.15, p.65-95, 1984.
- REED, D.H.; FRANKHAM, R. Correlation between fitness and genetic diversity. Conservation Biology, v.17, p.230-237, 2003.
- RIBEIRO, J.F.; SANO, S.M.; BRITO, M.A.; FONSECA, C.E.L. Baru (Dipteryx alata Vog.). Jaboticabal: Funep, 2000. 41p. (Série Frutas Nativas, 10).
- SALIS, S.M.; CRISPIM, S.M.A. Densidades de árvores listadas como ameaçadas de extinção na Bacia do Alto Paraguai Corumbá: Embrapa Pantanal, 2006. 6p. (Embrapa Pantanal. Comunicado Técnico, 54).
- SANO, S.M.; RIBEIRO, J.F.; BRITO, M.A. de. Baru: biologia e uso. Planaltina: Embrapa Cerrados, 2004. 52p. (Embrapa Cerrados. Documentos, 116).
- SANO, S.M.; VIVALDI, L.J.; SPEHAR, C.R. Diversidade morfológica de frutos e sementes de baru (Dipteryx alata Vog.). Pesquisa Agropecuária Brasileira, v.34, p.513-518, 1999.
- SILVA, J.A. da; SILVA, D.B. da; JUNQUEIRA, N.T.V.; ANDRADE, L.R.M. de. Coleta de sementes, produção de mudas e plantio de espécies frutíferas nativas dos cerrados: informações exploratórias. Planaltina: Embrapa-CPAC, 1997. 23p. (Embrapa-CPAC. Documentos, 44).
- SOARES, T.N.; CHAVES, L.J.; TELLES, M.P. de C.; RESENDE, L.V.; DINIZ-FILHO, J.A.F. Landscape conservation genetics of Dipteryx alata (baru tree: Fabaceae) from Cerrado region of Central Brazil. Genetica, v.132, p.9-19, 2008.
- TELLES, M.P.C.; SOARES, T.N. DNA fingerprinting no estudo de populações de plantas do Cerrado. In: PEREIRA, A.M.S. (Org.). Recursos genéticos e conservação de plantas medicinais do Cerrado Ribeirão Preto: Legis Summa, 2007. p.109-145.
- VEKEMANS, X.; HARDY, O.J. New insights from fine-scale spatial genetic structure analyses in plant population. Molecular Ecology, v.13, p.921-935, 2004.
- WEIR, B.S.; COCKERHAM, C.C. Estimating F-statistics for the analysis of population structure. Evolution, v.38, p.1358-1370, 1984.
- ZUCCHI, M.; PINHEIRO J.B.; CHAVES, L.J.; COELHO, A.S.G.; COUTO, M.A.; MORAIS, L.K. de; VENCOVSKY, R. Genetic structure and gene flow of Eugenia dysenterica natural populations. Pesquisa Agropecuária Brasileira, v.40, p.975-980, 2005.
Datas de Publicação
-
Publicação nesta coleção
08 Out 2008 -
Data do Fascículo
Set 2008
Histórico
-
Aceito
19 Ago 2008 -
Recebido
09 Abr 2008