Resumos
As frutas nativas do cerrado têm despertado ultimamente interesse crescente, devido às suas propriedades nutricionais e funcionais aliadas ao potencial para agregar valor e conservar a biodiversidade deste bioma. Muitos compostos fenólicos apresentam capacidade antioxidante de neutralizar a atividade de radicais livres gerados no organismo, que estão associados a diversas doenças crônico-degenerativas. O objetivo deste trabalho foi avaliar a eficiência de três soluções extratoras (acetona a 70 %, etanol a 95 % e metanol a 99,8 %) e determinar os teores de compostos fenólicos em 10 espécies de frutas nativas do cerrado, utilizando o método de Folin-Ciocalteou para compostos fenólicos totais e o método da vanilina para taninos condensados. A acetona a 70 % mostrou-se como o melhor solvente extrator de compostos fenólicos totais e taninos condensados em frutos de Pouteria gardneriana, Eugenia dysenterica, E. klostzchiana, E. punicifolia, Plinia edulis, Campomanesia sp., fenólicos totais de Brosimium gaudichaudii e taninos condensados de Jaracatia spinosa. O etanol a 95 % foi mais eficiente na extração de fenólicos totais de Jaracatia spinosa e taninos condensados de Brosimium gaudichaudii; o metanol a 99,8 % foi mais eficiente na extração de taninos condensados de Eugenia dysenterica. Os teores de compostos fenólicos totais variaram entre 90 e 327 mg de ácido gálico equivalente por 100g de polpa para as espécies E. dysenterica e E. punicifolia, respectivamente. Os teores de taninos condensados variaram entre 4 e 291 mg de catequina equivalente por 100 g de polpa para as espécies E. dysenterica e E. calcyna, respectivamente. As espécies de frutas do cerrado, avaliadas neste estudo, podem ser consideradas boas fontes de compostos fenólicos totais, sendo que a natureza específica dos diferentes tipos deve ser avaliada em estudos futuros.
Anacardium spp; Eugenia spp; Brosimium gaudichaudii; Campomanesia sp; Pouteria gardneriana; Plinia edulis; Jaracatia spinosa
The native fruits from Brazilian savanna are arousing increasing interest due to their nutritional and functional properties combined with the potential to add value and conserve the biodiversity of this biome. Many phenolic compounds have antioxidant capacity to neutralize free radicals generated in the body that are associated with many chronic degenerative diseases. The objective of this study was to evaluate the efficiency of three extraction solutions (acetone 70%, ethanol 95% and methanol 99.8 %) and determining the levels of phenolic compounds in 10 species of native fruits from Brazilian savanna, using the Folin-Ciocalteu method for total phenolic compounds and vanillin method for condensed tannins. Acetone 70 % proved to be the best solvent extractor for total phenolics and condensed tannins in fruits of Pouteria gardneriana, Eugenia dysenterica, E. klostzchiana, E. punicifolia, Plinia edulis, Campomanesia sp. and for total phenolics in Brosimium gaudichaudii and for condensed tannins in Jaracatia spinosa. The ethanol 95 % was more efficient in the extraction of total phenolics of Jaracatia spinosa and condensed tannins of Brosimium gaudichaudii. The methanol 99.8 % was more efficient in the extraction of condensed tannins of Eugenia dysenterica. The contents of phenolic compounds ranged between 90 and 327 mg of gallic acid equivalent per 100 g of pulp for the species of E. dysenterica and E. punicifolia respectively. The levels of condensed tannins ranged between 4 and 291 mg of catechin equivalent per 100 g of pulp for the species of E. dysenterica and E. calcyna respectively. Evaluated species of fruit from Brazilian savanna can be considered good sources of total phenolic compounds, although the specific nature of different types should be evaluated in future studies.
Anacardium spp; Eugenia spp; Brosimium gaudichaudii; Campomanesia sp; Pouteria gard neriana; Plinia edulis; Jaracatia spinosa
PROCESSAMENTO
Compostos fenólicos totais e taninos condensados em frutas nativas do cerrado1 1 (Trabalho 206-10).
Total phenolics and condensed tannins in native fruits from Brazilian savanna
Wesley Silveira RochaI; Renata Miranda LopesI; Dijalma Barbosa da SilvaII; Roberto Fontes VieiraII; Joseane Padilha da SilvaII; Tânia da Silveira Agostini-CostaII
IBiólogos/ bolsistas do Programa Biodiversidade Brasil-Itália - Embrapa Recursos Genéticos e Biotecnologia, Brasília- DF. e-mail: biosrocha@yahoo.com.br; rm.lopes@yahoo.com.br
IIPesquisadores/ Embrapa Recursos Genéticos e Biotecnologia, Parque Estação Biológica, PqEB, W5 Norte, final, CEP: 70770-900, Brasília-DF. E-mails: dijalma@cenargen.embrapa.br; rfvieira@cenargen.embrapa.br; joseane@cenargen.embrapa.br; tania@cenargen.embrapa.br
RESUMO
As frutas nativas do cerrado têm despertado ultimamente interesse crescente, devido às suas propriedades nutricionais e funcionais aliadas ao potencial para agregar valor e conservar a biodiversidade deste bioma. Muitos compostos fenólicos apresentam capacidade antioxidante de neutralizar a atividade de radicais livres gerados no organismo, que estão associados a diversas doenças crônico-degenerativas. O objetivo deste trabalho foi avaliar a eficiência de três soluções extratoras (acetona a 70 %, etanol a 95 % e metanol a 99,8 %) e determinar os teores de compostos fenólicos em 10 espécies de frutas nativas do cerrado, utilizando o método de Folin-Ciocalteou para compostos fenólicos totais e o método da vanilina para taninos condensados. A acetona a 70 % mostrou-se como o melhor solvente extrator de compostos fenólicos totais e taninos condensados em frutos de Pouteria gardneriana, Eugenia dysenterica, E. klostzchiana, E. punicifolia, Plinia edulis, Campomanesia sp., fenólicos totais de Brosimium gaudichaudii e taninos condensados de Jaracatia spinosa. O etanol a 95 % foi mais eficiente na extração de fenólicos totais de Jaracatia spinosa e taninos condensados de Brosimium gaudichaudii; o metanol a 99,8 % foi mais eficiente na extração de taninos condensados de Eugenia dysenterica. Os teores de compostos fenólicos totais variaram entre 90 e 327 mg de ácido gálico equivalente por 100g de polpa para as espécies E. dysenterica e E. punicifolia, respectivamente. Os teores de taninos condensados variaram entre 4 e 291 mg de catequina equivalente por 100 g de polpa para as espécies E. dysenterica e E. calcyna, respectivamente. As espécies de frutas do cerrado, avaliadas neste estudo, podem ser consideradas boas fontes de compostos fenólicos totais, sendo que a natureza específica dos diferentes tipos deve ser avaliada em estudos futuros.
Termos para indexação:Anacardium spp., Eugenia spp., Brosimium gaudichaudii, Campomanesia sp., Pouteria gardneriana, Plinia edulis, Jaracatia spinosa .
ABSTRACT
The native fruits from Brazilian savanna are arousing increasing interest due to their nutritional and functional properties combined with the potential to add value and conserve the biodiversity of this biome. Many phenolic compounds have antioxidant capacity to neutralize free radicals generated in the body that are associated with many chronic degenerative diseases. The objective of this study was to evaluate the efficiency of three extraction solutions (acetone 70%, ethanol 95% and methanol 99.8 %) and determining the levels of phenolic compounds in 10 species of native fruits from Brazilian savanna, using the Folin-Ciocalteu method for total phenolic compounds and vanillin method for condensed tannins. Acetone 70 % proved to be the best solvent extractor for total phenolics and condensed tannins in fruits of Pouteria gardneriana, Eugenia dysenterica, E. klostzchiana, E. punicifolia, Plinia edulis, Campomanesia sp. and for total phenolics in Brosimium gaudichaudii and for condensed tannins in Jaracatia spinosa. The ethanol 95 % was more efficient in the extraction of total phenolics of Jaracatia spinosa and condensed tannins of Brosimium gaudichaudii. The methanol 99.8 % was more efficient in the extraction of condensed tannins of Eugenia dysenterica. The contents of phenolic compounds ranged between 90 and 327 mg of gallic acid equivalent per 100 g of pulp for the species of E. dysenterica and E. punicifolia respectively. The levels of condensed tannins ranged between 4 and 291 mg of catechin equivalent per 100 g of pulp for the species of E. dysenterica and E. calcyna respectively. Evaluated species of fruit from Brazilian savanna can be considered good sources of total phenolic compounds, although the specific nature of different types should be evaluated in future studies.
Index terms:Anacardium spp., Eugenia spp., Brosimium gaudichaudii, Campomanesia sp., Pouteria gard neriana, Plinia edulis, Jaracatia spinosa.
INTRODUÇÃO
A flora do Cerrado possui diversas espécies frutíferas com grande potencial de utilização agrícola, que são tradicionalmente utilizadas pela população local através do consumo in natura ou processadas na forma de sucos, licores, sorvetes, geleias e doces (SILVA et al.,2008). O aumento do consumo de frutas deu- se principalmente em razão de elas apresentarem propriedades funcionais, atribuídas à presença de substâncias bioativas que, mesmo em pequenas quantidades, podem apresentar efeitos fisiológicos adicionais, por meio de sua ação antioxidante (LIMA et al., 2002 e 2004; MELO et al., 2008).
Os compostos fenólicos presentes nas plantas estão relacionados, principalmente, com a proteção, conferindo alta resistência a microrganismos e pragas. Nos alimentos, estes compostos podem influenciar o valor nutricional e a qualidade sensorial, conferindo atributos como cor, textura, amargor e adstringência. Na maioria dos vegetais, os compostos fenólicos constituem os antioxidantes mais abundantes (EVERETTE et al., 2010). Em função da elevada atividade antioxidante que possuem, uma variedade de compostos fenólicos desempenha um papel importante nos processos de inibição do risco das doenças cardiovasculares e podem atuar sobre o estresse oxidativo, relacionado com diversas patologias crônico-degenerativas, como o diabetes, o câncer e processos inflamatórios. Entretanto, quando em concentração muito elevada ou em composição inadequada, estes compostos podem conferir características indesejáveis, como o escurecimento enzimático de frutas e a interação com proteínas, carboidratos e minerais (IMEH; KHOKHAR 2002).
Os compostos fenólicos são definidos como substâncias que possuem um anel aromático com um ou mais substituintes hidroxílicos, incluindo seus grupos funcionais. Estão amplamente distribuídos no reino vegetal, englobando desde moléculas simples até outras com alto grau de polimerização (SOARES et al.,2008). Além de moléculas mais simples como os ácidos fenólicos e os flavonoides, os taninos são encontrados em muitas frutas, sendo caracterizados como compostos fenólicos de alto peso molecular, que precipitam proteínas, incluindo proteínas salivares da cavidade oral. Essas propriedades são fundamentais para explicar o papel dos taninos na proteção vegetal contra patógenos e na detenção de herbívoros que se alimentam destas plantas. Esses compostos são divididos em dois grupos, de acordo com seu tipo estrutural: taninos hidrolisáveis e taninos condensados ou proantocianidinas. Considerando a grande diversidade química de compostos fenólicos distribuídos na natureza, diferentes solventes são empregados no processo de extração e diferentes metodologias analíticas são empregadas no processo de quantificação destes compostos (EFRAIM et al., 2006).
O método de Folin-Ciocalteou é empregado com o objetivo de detectar todas as classes de compostos poli-hidroxifenólicos. Como o reagente Folin-Ciocalteou reage com alguns compostos não fenólicos que também apresentam atividade antioxidante e apresenta elevada correlação com métodos usados para avaliar atividade antioxidante, alguns autores sugerem que este método seja empregado para determinar capacidade antioxidante total (EVERETTE et al., 2010). Já o método da vanilina é empregado com o objetivo de detectar uma classe mais limitada de compostos fenólicos que apresentam uma ligação simples na posição 2,3 e grupos hidroxila em posições alternadas no anel A, embora possa detectar tanto flavonoides monoméricos quanto poliméricos. Neste método, tanto as leucoantocianidinas (catequinas) quanto as proantocianidinas (taninos condensados) reagem com a vanilina na presença de HCl para produzir um produto de condensação vermelho, que é detectado espectrofotometricamente (AGOSTINI-COSTA et al.,2003).
Os compostos fenólicos têm sido bastante avaliados em frutas de clima temperado, como maçã (321-474 mg.100g-1 ), pera (271-408 mg.100g-1), kiwi (274,4 mg.100g-1), e ameixa (471,4 mg.100g-1) (IMEH; KHOKHAR, 2002); uva (117,1 mg.100g-1), amora (118,1 mg.100g-1), morango (132,1 mg.100g-1), e em outras frutas de clima tropical, como manga (544,9 mg.100g-1), açaí (136,8 mg.100g-1), goiaba (83,0 mg.100g-1), graviola (84,3 mg.100g-1), maracujá (20,0 mg.100g-1) (KUSKOSKI et al. ,2006) e coquinho-azedo (78-166 mg.100g-1) (FARIA et al. ,2008). Entretanto, pouco se conhece sobre o conteúdo e a composição de compostos fenólicos em frutas nativas do cerrado. Desse modo, este trabalho teve como objetivo avaliar a eficiência do solvente extrator e quantificar os teores de compostos fenólicos totais e de taninos condensados, empregando, respectivamente, os métodos de Folin-Ciocalteou e da vanilina em diferentes espécies de frutas nativas do cerrado.
MATERIAL E MÉTODOS
Material vegetal. Os frutos in natura utilizados para as análises químicas foram obtidos entre outubro de 2008 e fevereiro de 2009, sendo provenientes de doze espécies: três espécies do gênero Anacardium (A. occidentale conhecido como caju cultivado, A. nanum ou cajuí-do-cerrado; e A. othonianum ou caju-de-árvore-do-cerrado), quatro espécies do gênero Eugenia (E. dysenterica ou cagaita, E. klostzchiana ou pera-do-cerrado; E. punicifolia e E. calcyna, que são duas espécies de pitanga-do-cerrado); Brosimium gaudichaudii ou mama-cadela; Campomanesia sp. ou gabiroba; Pouteria gardneriana ou guapeva; Plinia edulis ou Cambucá e Jaracatia spinosa ou Jaracatiá. Como a cagaita geralmente é processada verde, os frutos foram coletados e analisados nos dois estádios de maturação (verde e maduro), conforme tradição de consumo; as demais frutas foram coletadas e analisadas maduras, no ponto apropriado para o consumo. Os frutos foram procedentes dos Estados de Goiás, Bahia e Distrito Federal; aqueles coletados nos Estados da Bahia e Goiás foram acondicionados em isopor com gelo e transportados diretamente ao Laboratório de Química de Produtos Naturais da Embrapa Recursos Genéticos e Biotecnologia, onde foram realizados triagem, limpeza e acondicionamento em freezer a -20ºC, até o momento das análises.
Reagentes e equipamentos. O reagente de Folin-Ciocalteou foi adquirido da Fluka e diluído 1:10, antes da reação. O reagente da vanilina foi preparado antes da reação com vanilina (Vetec), ácido clorídrico concentrado (Merck) e metanol (Vetec) 4:56:83 (p/v/v). Os padrões de ácido gálico, catequina e ácido tânico foram obtidos da Sigma e diluídos em água destilada para a obtenção das curvas de calibração.
Para a leitura da absorbância, foi empregado um espectrofotômetro de varredura espectral Lambda 25 da Perkin Elmer.
Obtenção do extrato. Os frutos foram cortados em pequenos pedaços, e a polpa com casca foi triturada em multiprocessador doméstico e passada por uma peneira, garantindo a homogeneidade da amostra. Foram avaliados três solventes distintos para extração a frio de compostos fenólicos nas diferentes amostras de tecidos vegetais: acetona a 70 %, etanol a 95 % e metanol, conforme Agostini-Costa et al. (2003). Para cada solvente testado, foram pesados dois gramas da polpa fresca homogeneizada em erlemeyer de 50 ml, aos quais foram adicionados 25 ml de solvente, em quintuplicata. A extração dos compostos fenólicos foi feita com proteção da luz à temperatura ambiente (25ºC) por 3 h.
Os extratos etanólico e metanólico foram filtrados em lã de vidro diretamente para balões volumétricos de 25 ml; o volume foi completado com água destilada. Os extratos obtidos com acetona a 70 % foram evaporados a vácuo (40 ºC), prevenindo a interferência da acetona nas reações da vanilina; o resíduo aquoso foi transferido quantitativamente do balão de evaporação para o balão volumétrico de 25 ml, e o volume foi completado com água destilada. Para cada solvente avaliado, foram realizados os brancos da amostra, que seguiram os procedimentos descritos acima, sem adição de amostra.
Compostos fenólicos totais. Os compostos fenólicos totais foram determinados empregando-se o método espectrofotométrico de Folin-Ciocalteau (XU; CHANG , 2009). Alíquotas de 1 ml de extrato foram transferidas para balões de 10 ml, contendo 5 ml de água destilada. Foram adicionados 1 ml de carbonato de sódio a 25 % e 1 ml do reagente Fólin-Ciocalteou, completando o volume com água destilada. Após 30 minutos, foi determinada a absorbância a 760 nm em espectrofotômetro. O teor de compostos fenólicos totais de cada extrato foi quantificado por curvas de calibração externa, e os resultados foram expressos em mg de ácido gálico equivalente (AGE) e em mg de ácido tânico equivalente (ATE) por 100 g de polpa.
Taninos condensados. Foram determinados pela reação da vanilina, conforme método de Broadhurst e Jones (1978), adaptado por Agostini-Costa et al. (1999). Visando a manter a estabilidade da reação, os tubos de ensaio de 25 ml (com tampa de rosca e teflon) foram cobertos com papel-alumínio. Adicionaram-se 5 ml de vanilina, reagente recém- preparado, em cada tubo de ensaio (em quintuplicata); em seguida, os tubos foram pre-aquecidos em banho-maria a 30 ºC por 30 min. Após essa etapa, foi adicionado 1 ml de extrato em cada tubo e agitado em vórtex por 30 seg. A reação foi mantida a 30º C por 20 minutos; a leitura da absorbância foi realizada a 510 nm, dentro de um prazo máximo de 1 hora. O mesmo procedimento foi feito para o branco e para os padrões. A quantificação foi feita por meio de curva de calibração externa, empregando-se a catequina como padrão. Os resultados foram expressos em mg de catequina equivalente (CAE) por 100 g de polpa. A proporção entre compostos fenólicos totais (CFT) e taninos condensados (TC) foi obtida por CFT/TC.
Análise estatística. Para comparar a eficiência dos diferentes solventes na extração dos compostos fenólicos, foi utilizado um modelo linear do efeito dos tratamentos, seguido de um teste de comparações múltiplas de Tukey. Para os frutos procedentes de mais de um acesso, foi feita a análise de variância, seguida de teste de Tukey, para as comparações múltiplas, com nível de significância de 5 %.
RESULTADOS E DISCUSSÃO
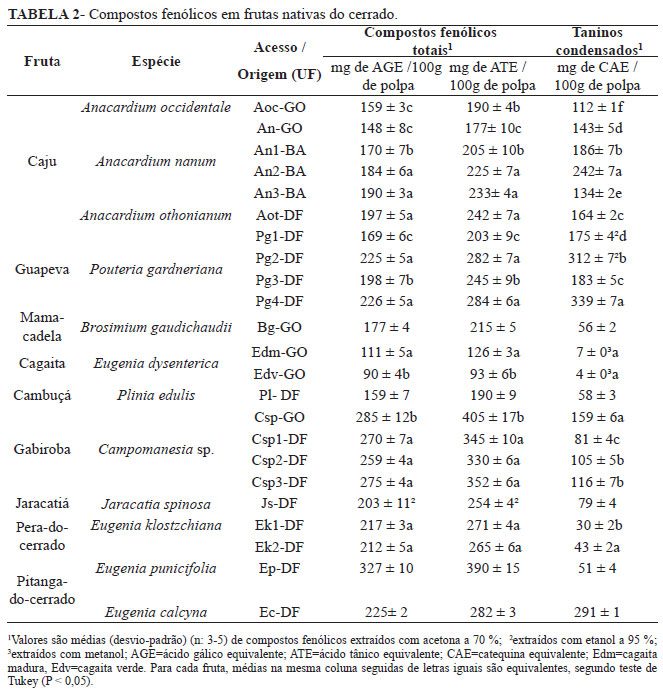
De acordo com a Tabela 1, a acetona a 70 % foi o melhor solvente extrator de compostos fenólicos para a maioria das frutas analisadas, fornecendo teores significativamente mais elevados e melhor precisão de resultados em relação aos demais solventes avaliados; exceção para a extração de fenólicos totais em jaracatiá com etanol a 95 % e extração de taninos condensados em Guapeva com etanol a 95 % e em cagaita com metanol. Os resultados finais obtidos com o solvente de eleição (Tabela 2) indicam que as frutas nativas do cerrado avaliadas neste estudo são boas fontes de compostos fenólicos (90 a 327 mg de AGE.100g-1 de polpa) se comparadas com a polpa de outras frutas normalmente consumidas, tais como maracujá, abacaxi e cupuaçu (20,0 a 21,7 mg de AGE.100g-1), goiaba (83 mg de AGE.100g-1) uva e açaí (117,1 a 136,8 mg de AGE.100g-1), morango (203-223 ATE.100g-1), amora-preta (241,7 AGE.100g-1), ou manga (544,9 mg de AGE.100g-1) (KUSKOSKI et al., 2006; FERREIRA et al., 2010). Canuto et al. 2010 encontraram teores de compostos fenólicos totais entre 0,3 e 3,5 mmol.L-1 de AGE em frutas da Amazônia, sendo que algumas polpas, como a de acerola (3,5 mmol.L-1 de AGE) e a de açaí (2,5 mmol.L-1 de AGE) apresentaram elevado potencial antioxidante associado.
Os pedúnculos ou pseudofrutos das espécies de cajueiros nativos do Cerrado (A. nanum e A. othonianum) apresentaram teores de compostos fenólicos e taninos condensados (134-242 mg de CAE.100g-1 de polpa) significativamente mais elevados do que o A. occidentale (112 mg de CAE.100g-1 de polpa); entretanto, os teores encontrados para todas estas espécies estão de acordo com variações da literatura (85-285 mg de CAE.100g-1 de polpa) para diferentes acessos do banco de germoplasma de A. occidentale (AGOSTINI-COSTA et al., 2003). Canuto et al. 2010 encontraram 0,6 mmol.L-1 de AGE em pedúnculos de caju da Amazônia. Para as espécies do gênero Anacardium analisadas neste trabalho, a relação entre compostos fenólicos totais e taninos condensados (CFT/TC) variou entre 0,8 e 1,4, indicando que os compostos fenólicos se encontram predominantemente na forma de taninos condensados que, provavelmente, estão associados à adstringência dos frutos. Além do caju, a guapeva (P. gardneriana) e uma das espécies de pitanga-do-cerrado (E. calcyna) apresentaram relação CFT/TC variando entre 0,7 e 1,1, também indicando predominância de taninos condensados. Diferentes acessos de P. gardneriana apresentaram diferença significativa entre os teores de compostos fenólicos.
Ao contrário da E. calcyna, as outras três espécies do gênero Eugenia avaliadas apresentaram menores concentrações de taninos condensados em relação aos teores de fenólicos totais (E. dysenterica CFT/TC entre 15,9 e 22,5; E. punicifolia CFT/TC igual a 6,4; e E. klostzchiana CFT/TC entre 4,9 e 7,2), indicando a provável presença de compostos fenólicos simples, como os ácidos fenólicos, ou taninos hidrolisáveis. A pitanga-do-cerrado Eugenia punicifolia apresentou elevadas concentrações de compostos fenólicos totais (327 ± 10 mg de AGE.100g-1 de polpa ou 390 ± 15 mg de ATE.100g-1 de polpa) e baixos teores de taninos condensados (51 ± 3 mg de CAE.100g-1 de polpa). Não foram encontrados resultados na literatura sobre o teor de compostos fenólicos nas espécies nativas de pitanga; entretanto, a pitanga comercial vermelha e roxa (E. uniflora) apresentou teores de compostos fenólicos totais entre 252 e 325 mg CAE.100g-1 (LIMA et al., 2002) muito próximos aos encontrados para as pitangas nativas avaliadas neste trabalho. Os frutos de cagaita (E. dysenterica) apresentaram os menores teores de taninos condensados, entre as espécies avaliadas neste estudo (4 a 7 mg CAE / 100g polpa). Já a pera-do-cerrado (Eugenia klostzchiana) apresentou 212 a 217 mg AGE.100g-1 polpa, enquanto a pera cultivada (Pyrus comunis) avaliada por Imeh e Khokhar (2002) apresentou 271 a 408 mg AGE.100g-1 polpa.
A gabiroba (Campomanesia sp.) que, assim como o gênero Eugenia, também pertence à família Myrtaceae, apresentou elevados teores de compostos fenólicos totais e menores teores de taninos condensados (relação CFT/TC entre 1,8 e 3,3), sendo que, entre os quatro acessos analisados, apenas um apresentou diferença significativa dos demais. Os frutos de mama-cadela (B. gaudichaudii) apresentaram relação CFT/TC 3,2. Estas duas espécies,provavelmente, apresentam uma relação mais equilibrada entre taninos condensados e outros compostos fenólicos de estrutura mais simples.
Os compostos fenólicos geralmente estão associados ao mecanismo de adaptação e resistência da planta ao meio ambiente. Estudos futuros devem identificar o tipo de composto fenólico presente em cada espécie, já que os mesmos podem influenciar no sabor, nas características tecnológicas, como escurecimento ou precipitação durante o processamento, assim como no potencial nutricional e funcional destas frutas.
CONCLUSÃO
Para a maioria das frutas analisadas, a acetona a 70 % apresenta melhor eficiência de extração de compostos fenólicos totais e de taninos condensados; o etanol a 95% é eficiente para o jaracatiá e a guapeva; e o metanol, para a cagaita. As frutas de espécies nativas do cerrado, analisadas pela primeira vez neste estudo, apresentam elevados teores de compostos fenólicos totais e de taninos condensados, sendo que os taninos condensados predominam nas espécies do gênero Anacardium, P. gardneriana e E. calcyna. Nas demais espécies da família Myrtaceae avaliadas e em Brosimium gaudichaudii, os elevados teores de compostos fenólicos totais associados às menores proporções de taninos condensados indicam a provável ocorrência de compostos fenólicos de estrutura mais simples, como os ácidos fenólicos, ou taninos hidrolisáveis.
AGRADECIMENTOS
À Embrapa e ao Programa Biodiversidade Brasil Itália - PBBI, pelo financiamento da pesquisa.
Recebido em: 07-10-2010.
Aceito para publicação em: 18-08-2011.
O trabalho foi financiado pelo Programa Biodiversidade Brasil-Itália - PBBI e Embrapa
- AGOSTINI-COSTA, T. S.; GARRUTI, D. S.; LIMA, L.; FREIRE, S.; ABREU, F. A. P.; FEITOSA, T. Avaliação de metodologias para determinação de taninos no suco de caju. Boletim CEPPA, Curitiba, v. 17, n. 2, p. 167-176, 1999.
- AGOSTINI-COSTA, T. S.; LIMA, A.; LIMA, M. V. Determinação de taninos em pedúnculo de caju: método da vanilina versus método do butanol ácido. Química Nova, São Paulo, v. 26, n. 5, p. 763-765, 2003.
- BROADHURST, R. B.; JONES, W. T. Analysis of condensed tannins using acidified vanillin. Journal of the Science of Food and Agriculture, Baffins Lane Chichester, v. 29, n.9, p. 788-794, 1978.
- CANUTO, G.A.B; XAVIER, A.A.O; NEVES, L.C.; BENASSI, M.T. Caracterização físico-química de polpas de frutos da Amazônia e sua correlação com a atividade antirradical livre. Revista Brasileira de Fruticultura, Jaboticabal, v. 32, p. 1.196-1.205, 2010.
- EFRAIM, P.; TUCCI, M. L.; PEZOA-GÁRCIA, N. H.; HADDAD, R.; EBERLIN, M. N. Teores de compostos fenólicos de sementes de cacaueiro de diferentes genótipos. Brazilian Journal of Food Technology, Campinas, v. 9, n. 4, p. 229-236, 2006.
- EVERETTE, J. D.; BRYANT, Q. M.; GREEN, A. M.; ABBEY, Y. A.; WANGILA, G. W.; WALKER, R. B. Thorough study of reactivity of various compound classes toward the Folin-Ciocalteou reagent. Journal of Agricultural and Food Chemistry, Washington, v. 58, p. 8.139-8.144, 2010.
- FARIA, J. P.; ALMEIDA, F. SILVA, L. C. R.; VIEIRA, R. F.; AGOSTINI, T. S. Caracterização da polpa do coquinho-azedo (Butia capitata var capitata). Revista Brasileira de Fruticultura, Jaboticabal, v. 30, n. 3, p. 827-829, 2008.
- FERREIRA, D. S.; ROSSO, V. V.; MERCADANTE, A. Z. Compostos bioativos presentes em amora-preta (Rubus spp.). Revista Brasileira de Fruticultura, Jaboticabal, v. 32, p. 664-674, 2010.
- IMEH. U.; KHOKHAR. S. Distribution of Conjugated and Free Phenols in Fruits: Antioxidant Activity and Cultivar Variations. Journal of Agricultural and Food Chemistry, Washington, v. 50, p. 6.301-6.306, 2002.
- KUSKOSKI. E. M.; ASUERO. A. G.; MORALES. M. T.; FETT, R. Frutos tropicais silvestres e polpas de frutas congeladas: atividade antioxidante, polifenóis e antocianinas. Ciência Rural, Santa Maria, v. 36, n. 4, p. 1.283-1.287, 2006.
- LIMA, V. L. A. G. de; MÉLO, E. A.; LIMA, D. E. S. Fenólicos e carotenoides totais em pitanga. Scientia Agricola, São Paulo, v. 59, n. 3, p. 447-450, 2002.
- LIMA, V. L. A. G. de; MÉLO, E. A.; MACIEL, M. I. S.; SILVA, G. S. B.; LIMA, D. E. S. Fenólicos totais e atividade antioxidante do extrato aquoso de broto de feijão-mungo (Vigna radiata L.). Revista de Nutrição, Campinas, v. 17, n. 1, p. 53-57, 2004.
- MELO, E. A.; MACIEL, M. I. S.; LIMA, V. L. A. G.; NASCIMENTO, R. J. Capacidade antioxidante de frutas. Brazilian Journal of Pharmaceutical Sciences, São Paulo, v. 44, n. 2, 2008.
- SILVA, M. R.; LACERDA, D. B. C. L.; SANTOS, G. G.; MARTINS, D. M. O. Caracterização química de frutos nativos do cerrado. Ciência Rural, Santa Maria, v. 38, n. 6, p. 1.790-1.793, 2008.
- SOARES, M.; WELTER, L.; KUSKOSKI, E. M.; GONZAGA, L.; FETT, R. Compostos Fenólicos e atividade antioxidante da casca de uvas Niágara e Isabel. Revista Brasileira de Fruticultura, Jaboticabal, v, 30, n. 1, p. 59-64, 2008.
- XU, B.; CHANG, S. K. C. Total phenolic, phenolic Acid, anthocyanin, flavan-3-ol, and flavonol profiles and antioxidant properties of pinto and black beans (Phaseolus vulgaris L.) as affected by thermal processing. Journal of Agricultural and Food Chemistry, Washington, v. 57, p. 4754-4764, 2009.
Datas de Publicação
-
Publicação nesta coleção
30 Jan 2012 -
Data do Fascículo
Dez 2011
Histórico
-
Recebido
07 Out 2010 -
Aceito
18 Ago 2011