Resumos
O lulo é um fruto tropical e exótico, originário dos Andes, tem cor laranja quando maduro, e é uma baga globosa, assemelha- se a um tomate, o epicarpo é grosso e coriáceo, sua polpa é verde-clara, pegajosa, ácida e suculenta, contendo muitas sementes. Objetivou-se acompanhar as características físicas, químicas e fisiológicas ocorridas durante o desenvolvimento do fruto de lulo, da antese ao amadurecimento completo, em Viçosa-MG. Os frutos apresentaram um padrão de crescimento sigmoidal simples em resposta à variação do tempo. O desenvolvimento do fruto foi dividido em três fases. A primeira foi até os 7,39 dias após a antese (DAA), sendo caracterizada pela alta taxa respiratória, provavelmente devido à intensa multiplicação celular, e o pericarpo apresentava coloração verde-clara. A segunda fase estendeu-se a partir dos 7,39 até os 57,63 DAA, sendo caracterizada pelas taxas máximas das características estudadas. A taxa respiratória cresceu até 45 DAA, mantendo-se estável até os 52 DAA. A última fase estendeu-se a partir dos 57,63 DAA até os 95,00 DAA. Essa fase foi caracterizada pela estabilização nas dimensões e no acúmulo de massa fresca. Nesse período, ocorreu a ascensão climatérica (dos 52 aos 59 DAA). O climatério respiratório ocorreu aos 66 DAA, com pico de produção de CO2 de 110,99 mg de CO2 kg-1h-1. O pós-climatério ocorreu dos 73 aos 95 DAA, quando houve aumento no teor de sólidos solúveis e queda da acidez titulável e vitamina C da polpa. Nessa fase, o pericarpo dos frutos apresentava-se com coloração alaranjada.
análise de crescimento; ponto de colheita; fruto exótico
The lulo is a tropical and exotic fruit, originating in the Andes is orange when ripe, and is a globose berry, resembling a tomato, the epicarp is thick and leathery, its pulp is light green, sticky, sour and juicy, containing many seeds. The objective of this study was to monitor the physical, chemical and physiological characteristic changes occurring during lulo fruit development, from anthesis to the full plant maturation. The fruits were harvested in the orchard of the Federal University of Viçosa and the analysis performed in the Laboratory of Fruits Analysis, from the Plant Science Department. The reproductive cycle of lulo lasted 95 days. Fruits development was divided into three phases. The first phase was up to 7.39 days after anthesis (DAA), being characterized by high respiratory rates, probably due to the intense cell multiplication and the pericarp showed light green color. The second phase occurred from 7.39 DAA to 57,63 DAA, being characterized by maximum rates of increase in dimensions of the fresh and dry fruit, the pericarp developed an intense green color and respiratory rates increased until 45 DAA and remained stable until 52 DAA. The third and final development phase occurred from 57.63 DAA to 95.00 DAA, the last day of evaluations. This phase was characterized by dimensions stabilization and accumulation of fresh mass. In this period, the climacteric rise (from 52 to 59 DAA) occurred. The respiratory climacteric occurred at 66 DAA, with peak production of CO2 of 110,99 mg CO2 kg-1 h-1. The post-climacteric was between 73 and 95 DAA, when soluble solids increased and acidity and vitamin C from the pulp decreased. At this stage, the pericarp of the fruits showed orange coloration.
growth analysis; point of harvest; exotic fruit
FITOTECNIA CROP PRODUCTION
Desenvolvimento dos frutos de lulo (Solanum quitoense LAM), em Viçosa-MG1 1 (Trabalho 150-12).
Lulo (Solanum quitoense LAM) fruits development in Viçosa - MG
Pedro Henrique Monteiro MatarazzoI; Dalmo Lopes de SiqueiraII; Luiz Carlos Chamhum SalomaoII; Danielle Fabíola Pereira da SilvaIII; Paulo Roberto CeconIV
IEng. Agr., Mestre. Universidade Federal de Viçosa, Departamento de Fitotecnia. Av. Peter Henry Rolfs, s/n, 36570-000 Viçosa-MG. pedro.matarazzo@yahoo.com.br (endereço para correspondência)
IIEngennheiro Agrônomo, Doutor. Universidade Federal de Viçosa, Departamento de Fitotecnia. Av. Peter Henry Rolfs, s/n, 36570-000 Viçosa-MG. siqueira@ufv.br; lsalomao@ufv.br
IIIEngennheira Agrônoma, Pós-Doutoranda. Universidade Federal de Viçosa, Departamento de Fitotecnia. Av. Peter Henry Rolfs, s/n, 36570-000 Viçosa-MG. danieele@ufv.br
IVEng.Agr., Doutor. Universidade Federal de Viçosa, Departamento de Informática, Universidade Federal de Viçosa, Av. P.H. Rolfs, s/nº, 36570-000, Viçosa-MG, Brasil.cecon@ufv.br
RESUMO
O lulo é um fruto tropical e exótico, originário dos Andes, tem cor laranja quando maduro, e é uma baga globosa, assemelha- se a um tomate, o epicarpo é grosso e coriáceo, sua polpa é verde-clara, pegajosa, ácida e suculenta, contendo muitas sementes. Objetivou-se acompanhar as características físicas, químicas e fisiológicas ocorridas durante o desenvolvimento do fruto de lulo, da antese ao amadurecimento completo, em Viçosa-MG. Os frutos apresentaram um padrão de crescimento sigmoidal simples em resposta à variação do tempo. O desenvolvimento do fruto foi dividido em três fases. A primeira foi até os 7,39 dias após a antese (DAA), sendo caracterizada pela alta taxa respiratória, provavelmente devido à intensa multiplicação celular, e o pericarpo apresentava coloração verde-clara. A segunda fase estendeu-se a partir dos 7,39 até os 57,63 DAA, sendo caracterizada pelas taxas máximas das características estudadas. A taxa respiratória cresceu até 45 DAA, mantendo-se estável até os 52 DAA. A última fase estendeu-se a partir dos 57,63 DAA até os 95,00 DAA. Essa fase foi caracterizada pela estabilização nas dimensões e no acúmulo de massa fresca. Nesse período, ocorreu a ascensão climatérica (dos 52 aos 59 DAA). O climatério respiratório ocorreu aos 66 DAA, com pico de produção de CO2 de 110,99 mg de CO2 kg-1h-1. O pós-climatério ocorreu dos 73 aos 95 DAA, quando houve aumento no teor de sólidos solúveis e queda da acidez titulável e vitamina C da polpa. Nessa fase, o pericarpo dos frutos apresentava-se com coloração alaranjada.
Termos Para indexação: análise de crescimento, ponto de colheita, fruto exótico.
ABSTRACT
The lulo is a tropical and exotic fruit, originating in the Andes is orange when ripe, and is a globose berry, resembling a tomato, the epicarp is thick and leathery, its pulp is light green, sticky, sour and juicy, containing many seeds. The objective of this study was to monitor the physical, chemical and physiological characteristic changes occurring during lulo fruit development, from anthesis to the full plant maturation. The fruits were harvested in the orchard of the Federal University of Viçosa and the analysis performed in the Laboratory of Fruits Analysis, from the Plant Science Department. The reproductive cycle of lulo lasted 95 days. Fruits development was divided into three phases. The first phase was up to 7.39 days after anthesis (DAA), being characterized by high respiratory rates, probably due to the intense cell multiplication and the pericarp showed light green color. The second phase occurred from 7.39 DAA to 57,63 DAA, being characterized by maximum rates of increase in dimensions of the fresh and dry fruit, the pericarp developed an intense green color and respiratory rates increased until 45 DAA and remained stable until 52 DAA. The third and final development phase occurred from 57.63 DAA to 95.00 DAA, the last day of evaluations. This phase was characterized by dimensions stabilization and accumulation of fresh mass. In this period, the climacteric rise (from 52 to 59 DAA) occurred. The respiratory climacteric occurred at 66 DAA, with peak production of CO2 of 110,99 mg CO2 kg-1 h-1. The post-climacteric was between 73 and 95 DAA, when soluble solids increased and acidity and vitamin C from the pulp decreased. At this stage, the pericarp of the fruits showed orange coloration.
Index terms: growth analysis, point of harvest, exotic fruit.
INTRODUÇÃO
O fruto do lulo, de cor laranja quando maduro, é uma baga globosa, medindo entre 4,0 e 6,5 cm de diâmetro equatorial, coberto de pelos curtos que caem facilmente quando friccionados. Internamente, possui epicarpo grosso e coriáceo, polpa verde-clara, pegajosa, ácida e suculenta, contendo muitas sementes (HUYSKENS et al., 2001). A acidez dificulta o consumo in natura, entretanto é desejável para a produção de suco, pois permite diluições, obtendo-se maior rendimento. Segundo Álvares et al. (2004), as mudanças físicas e físico-químicas que ocorrem durante o desenvolvimento e maturação dos frutos são usadas como critérios para determinar padrões de maturidade, ponto de colheita e qualidade em vários frutos. Durante o desenvolvimento, o fruto passa por diversas etapas ou estádios com características bem definidas, cuja avaliação é importante para o entendimento das alterações que ocorrem durante o ciclo de desenvolvimento (ÁLVARES et al., 2004).
Em geral, o período da antese à colheita dos frutos pode variar devido a diferentes fatores, como condições climáticas, variedades e época do ano. Esses fatores interferem diretamente no desenvolvimento da planta e, consequentemente, no desenvolvimento fisiológico do fruto (CAVICHIOLI et al., 2006).
A avaliação do desenvolvimento de frutos, em geral, é baseada na evolução dos atributos físicos, tais como comprimento, diâmetro, volume, massas frescas e secas, associados à avaliação de alterações nas características físico-químicas medidas a intervalos regulares durante o ciclo (ÁLVARES et al., 2004). O conhecimento das fases do desenvolvimento de frutos é essencial para auxiliar na determinação de práticas culturais, podendo revelar períodos críticos no desenvolvimento dos frutos que possibilitem sua produção com qualidade, como também a colheita na época correta (SALOMÃO et al., 2006).
Apesar da importância de se conhecer o desenvolvimento dos frutos, na literatura, não foram encontradas informações disponíveis sobre a curva de crescimento de frutos de lulo.
Desta forma, o objetivo deste trabalho foi determinar a curva de desenvolvimento dos frutos de lulo, em Viçosa-MG.
MATERIAL E MÉTODOS
Os frutos foram coletados no Pomar Experimental da Universidade Federal de Viçosa, localizado no município de Viçosa, Minas Gerais, que se encontra a 651 metros de altitude, na latitude sul 20°45'20'' e longitude oeste 42°52'40'', sendo o clima tipo Cwa, mesotérmico úmido com verões chuvosos e invernos secos.
O trabalho foi realizado no período de 27 de outubro de 2009 a 02 de fevereiro de 2010. Durante o período, a temperatura média do ar variou de 21 a 23,5 °C. A umidade relativa média foi de 85,2%,e a precipitação pluvial total foi de 702,4 mm de chuva.
Os frutos utilizados foram colhidos de 18 plantas de lulo (Solanum quiotense Lam. Var. septentrionale), com cerca de doze meses de idade, em plena produção. Foram marcados cachos com todos os botões florais fechados, com o objetivo de utilizar frutos com aproximadamente a mesma idade cronológica e fisiológica. A primeira coleta dos frutos ocorreu 10 dias após a antese, e a última, aos 95 dias após a antese, quando os frutos apresentavam completo amadurecimento na planta. As análises foram realizadas semanalmente, totalizando 13 coletas.
Os frutos foram colhidos ao acaso, num total de oito por período de amostragem (semanal), no período da manhã, sendo organizados em quatro repetições de dois frutos cada. Foram avaliados o comprimento (mm), diâmetro equatorial (mm) e volume do fruto (cm3), espessura (mm) e ângulo hue do pericarpo (ºh), massas frescas do fruto, polpa e pericarpo (g), massas secas do pericarpo e da polpa (g), teor de sólidos solúveis (ºBrix), teor de vitamina C (mg ácido ascórbico/100g suco), acidez titulável (% ác. cítrico). Para análise de carotenoides da polpa, foram pesados aproximadamente 2,0 g, que foram triturados em cadinho com areia lavada, acetona a 80% e 10 mg de CaCO3. O extrato cetônico foi filtrado em papel de filtro, e o volume, completado para 25 mL. Suas absorbâncias foram determinadas a 470 nm, e os níveis de carotenoides, determinados segundo as equações de Lichtenthaler (1987), em µg/mL de extrato. Os resultados foram expressos em µg/mL de suco). A produção de CO2 foi obtida por cromatografia gasosa, e os resultados, expressos em mg de CO2 kg-1 de fruto h-1.
O delineamento experimental foi o inteiramente casualizado, com os tratamentos correspondendo aos dias de amostragem e quatro repetições, sendo dois frutos por unidade experimental. Os dados obtidos em função do tempo foram submetidos à análise de variância e de regressão. Para algumas características, utilizaram-se modelos de regressões não lineares sigmoidais, com três e quatro parâmetros. A escolha dos modelos não lineares foi baseada no coeficiente de determinação e no potencial para explicar o fenômeno biológico.
Os pontos de inflexão das curvas ajustadas corresponderam aos momentos em que ocorreram as taxas máximas de acúmulo da característica em análise. Os pontos de curvatura mínima (PCmín) e máxima (PCmáx) nos modelos sigmoidais, com três parâmetros, foram calculados conforme método citado por Laviola et al. (2012), utilizando os parâmetros das equações não lineares.
O PCmín indica o momento na curva de acúmulo em que se iniciam ganhos significativos no acúmulo da característica em análise. Já o PCmáx indica o momento em que o acúmulo da característica em análise começa a se estabilizar. O programa estatístico utilizado foi o SIGMAPLOT, versão 11.0.
RESULTADOS E DISCUSSÃO
Nas condições de Viçosa, o fruto do lulo foi colhido 95 dias após a antese, período muito curto quando comparado ao de 156 a 164 dias observado por Santacruz (2004) em Honduras. É provável que as condições climáticas de Viçosa, principalmente a temperatura média do ar (22,2 ºC), tenha reduzido o ciclo reprodutivo. Já o maior ciclo reprodutivo no trabalho de Santacruz (2004), provavelmente, ocorreu devido ao sistema de cultivo, que ocorreu em casa de vegetação, em vasos de 19 L, com espaçamentos entre os vasos de 0,35 m.
As medidas dos comprimentos (Figura 1A), diâmetros equatoriais (Figura 1B) e volumes (Figura 1C) dos frutos ajustaram-se ao modelo sigmoidal simples, em resposta à variação do tempo.
FIGURA 1 - Valores observados e estimados do comprimento (A), diâmetro (B) e volume (C) de frutos de lulo durante o desenvolvimento, em função do tempo (DAA). A linha com traços e pontos (― ∙∙ ―) indica o ponto de curvatura máxima, e a tracejada (― ―), a derivada primeira da curva de crescimento. Viçosa-MG.
Foi registrado o ponto de curvatura mínima para o comprimento, aos -13,64 dias, indicando que o início dos ganhos expressivos no comprimento do fruto ocorreu 13,64 dias antes da abertura floral (Figura 1A). Em trabalho realizado paralelamente ao do desenvolvimento do fruto nas mesmas plantas (dados não mostrados), foi observado o desenvolvimento do botão floral, nas mesmas plantas e épocas estudadas, o qual variou de 22 a 25 dias. Esses dados mostram, portanto, que mesmo antes da antese, o ovário já estava presente, sendo que os ganhos expressivos no comprimento ocorreram durante esse período (13,64 dias antes da abertura floral).
A taxa máxima do comprimento ocorreu aos 16,96 DAA, com ganho diário de 0,91 mm. O comprimento começou a estabilizar-se aos 47,57 DAA (ponto de curvatura máxima), correspondendo a 88,09% do acúmulo máximo. O comprimento máximo atingido pelo fruto foi de 55,81 mm.
De forma semelhante ao comprimento, o início de ganhos expressivos no diâmetro iniciou-se aos 2,58 DDA antes da abertura floral (Figura 1B). A taxa de crescimento máxima do diâmetro ocorreu aos 19,84 DAA, com ganho diário de 0,69 mm. A partir de 42,26 DAA, o diâmetro começou a se estabilizar, correspondendo a 88,08% do acúmulo máximo. O diâmetro equatorial máximo atingido pelo fruto foi de 55,25 mm.
O início dos ganhos expressivos no volume do fruto ocorreu aos 14,81 DAA (Figura 1C). A taxa de crescimento máxima do volume ocorreu aos 39,09 DAA, com ganho diário de 2,02 cm3/dia. A partir de 63,37 DAA, o volume começou a se estabilizar, correspondendo a 88,08% do acúmulo máximo. O volume máximo atingido pelo fruto foi de 97,79 cm3.
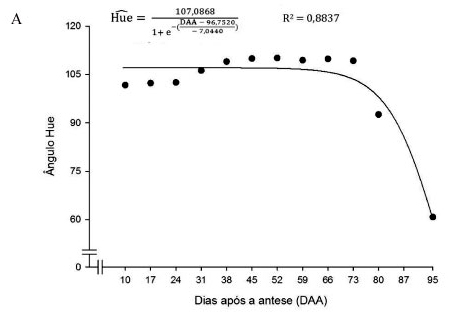
A intensificação da cor verde do pericarpo do fruto, medida pelo ângulo hue (°h), ocorreu até os 31 DAA (Figura 2A). Segundo Soares et al. (2011), a variação da cor verde- clara brilhante para o verde-escuro opaco ocorre devido à degradação da clorofila. A coloração dos frutos, a partir dos 31 DAA até os 66 DAA, correspondeu a um valor médio de ângulo hue de 109,6°, equivalendo à cor verde-escura do pericarpo. A coloração do pericarpo é fator determinante na compra da fruta pelo consumidor, que associa a cor do pericarpo ao paladar (SILVA et al., 2011b). A coloração verde do pericarpo, que gradualmente se extingue com o desenvolvimento do fruto, é resultado da degradação da clorofila presente no pericarpo e à síntese e ou manifestação dos pigmentos carotenoides (MEDEIROS et al., 2011). No caso do lulo, essa mudança começou a ocorrer a partir dos 66 DAA, até o ângulo hue atingir 60,8°, aos 95 dias após a antese, como pode ser visto na Figura 2A.
FIGURA 2 - Estimativa da A: evolução do ângulo hue (°h) do pericarpo e B: valores observados e estimados da espessura do pericarpo (mm) ao longo do desenvolvimento do fruto de lulo, em função do tempo (DAA). Viçosa-MG.
A espessura do pericarpo ajustou-se ao padrão de desenvolvimento sigmoidal simples, em resposta à variação do tempo, havendo acréscimo da espessura durante o desenvolvimento do fruto (Figura 2B). A partir de 68,25 DAA, a espessura do fruto começou a se estabilizar, correspondendo a 88,09% da espessura máxima atingida pelo pericarpo (3,08 mm aos 95 DAA).
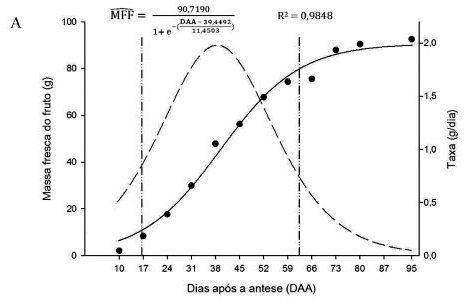
Semelhantemente às dimensões, o acúmulo das massas frescas do fruto (Figura 3A), polpa e pericarpo (Figura 4A) ajustaram-se a um padrão de desenvolvimento sigmoidal simples, em resposta à variação do tempo.
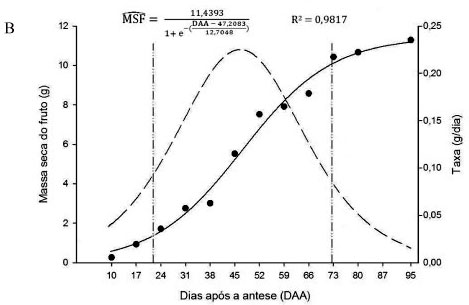
FIGURA 3 - Valores observados e estimados da massa fresca (A) e massa seca (B) do fruto de lulo durante o desenvolvimento, em função do tempo (DAA). As linhas com traços e pontos (― ∙∙ ―) indicam os ponto de curvatura mínima e máxima, e a tracejada (― ―), a derivada primeira da curva de crescimento. Viçosa-MG.
- Valores observados e estimados da massa fresca (A) e seca (B) do pericarpo (- - -) e da polpa ( ― ) do fruto de lulo durante o desenvolvimento, em função do tempo (DAA). Viçosa-MG.
O início dos ganhos expressivos na massa do fruto ocorreu aos 17 DAA (Figura 3A). A taxa de crescimento máxima ocorreu aos 39 DAA, com ganho diário de 1,96 g/dia. A partir de 62 DAA, a massa do fruto começou a se estabilizar, correspondendo a 88% da massa fresca máxima atingida (91 g aos 95 DAA). Para o lulo, não se recomenda colher os frutos logo após o começo da estabilização da massa fresca total, que ocorreu aos 62 DAA, pois não apresentam teores de sólidos solúveis (Figura 7A) e acidez titulável (Figura 7B) adequados para o consumo. Do 66° DAA em diante, foi possível separar a polpa do pericarpo; ainda neste dia, a massa do pericarpo representava 77% da massa total do fruto, e foi decrescendo até atingir 72% na última análise, aos 95 DAA.
FIGURA 5 - Valores observados e estimados de A:teor de sólidos solúveis (A) da polpa (°Brix), B: acidez titulável da polpa (% de ácido citrico) do fruto de lulo durante o desenvolvimento, em função do tempo (DAA). Viçosa-MG.
FIGURA 6 - Valores observados e estimados de A: vitamina C da polpa (mg/100g de massa fresca da polpa) e B: teor de carotenoides da polpa (mg/100g de polpa) do fruto de lulo durante o desenvolvimento do fruto, em função do tempo (DAA). Viçosa-MG.
- Produção de CO2 (mg CO2 kg-1 h-1) durante o desenvolvimento do fruto de lulo, ao longo do tempo (DAA). Viçosa, MG-2010.
O acúmulo de massa seca do fruto (Figura 3B) ajustou-se ao padrão de desenvolvimento sigmoidal simples em resposta à variação do tempo, semelhantemente ao que ocorreu com as dimensões e com o acúmulo de massa fresca do fruto.
O início de ganhos expressivos no acúmulo de massa seca dos frutos ocorreu aos 21,80 DAA. A taxa de crescimento máxima ocorreu aos 47,21 DAA, com ganho diário de 0,223 g/dia, a partir de 72,62 DAA, e a massa do fruto começou a se estabilizar, correspondendo a 88,08% da massa seca máxima atingida (11,44 g aos 95 DAA).
Aos 66 DAA, a polpa era o componente responsável pela maior quantidade de massa seca no fruto (Figura 3B), representando 56,50%. Mas esse padrão logo se inverteu, e aos 95 DAA, o pericarpo representava 69,52% da massa seca total do fruto.
O teor de sólidos solúveis da polpa ajustou-se ao modelo sigmoidal simples, havendo acréscimo durante o desenvolvimento do fruto (Figura 7A). A evolução do conteúdo de açúcares nos frutos durante o desenvolvimento é resultado da translocação de assimilados resultantes da fixação fotossintética de carbono, reduzindo o ácido 3-fosfoglicérico em gliceraldeído 3-fosfato, seguido de sua redução à glicose nos drenos da planta (JOAS et al., 2012).
Aos 95 DAA, o teor de sólidos solúveis foi de 9,98 °Brix, quase 80% superior ao valor que estava quatro semanas antes, aos 66 DAA (5,59 °Brix). A partir de 92,54 DAA, o teor de sólidos solúveis começou a se estabilizar.
Segundo Franco et al. (2002), os frutos de lulo destinados à agroindústria devem apresentar, no mínimo, 9 °Brix e, para venda in natura, devem possuir mais de 50% do pericarpo alaranjado. Aos 73 DAA, os frutos apresentavam aproximadamente metade do pericarpo alaranjado, e a polpa, 7,24 °Brix. A partir dos 85,47 DAA, os frutos estavam aptos a serem colhidos para uso na agroindústria, pois apresentavam mais de 9 °Brix.
Ocorreu redução na acidez titutável com o decorrer do desenvolvimento do fruto (Figura 5B). Aos 66 DAA, o teor de ácido cítrico foi de 2,76%, decrescendo até 1,92%, aos 95 DAA. Este resultado justifica-se porque, ao passo que a fruta amadurece, o teor de açúcar vai aumentando e, paralelamente, ocorre degradação de ácidos orgânicos, que são utilizados como substrato no processo respiratório. Comportamento similar foi encontrado por outros autores, como Argenta et al. (1995), determinando padrões de maturação e índices de colheita de maçãs, e por Gouveia et al. (2003), estudando a maturação de frutos de goiaba.
O teor de vitamina C decresceu, segundo modelo sigmoidal simples, ao longo do desenvolvimento (Figura 6A), decrescendo até aos 90 DAA, quando se estabilizou até a última análise. O teor de vitamina C, na maioria dos frutos, tende a diminuir durante o processo de maturação. Silva et al. (2012) atribuem este decréscimo à atuação da enzima denominada ácido ascórbico oxidase (ascorbato oxidase), sendo que a atividade enzimática nos frutos maduros é maior que nos verdes, fato que pode explicar as perdas encontradas no decorrer da maturação.
Os frutos são classificados quanto aos teores de ácido ascórbico, da seguinte forma (FRANCO, 2002): fontes elevadas (100 a 300 mg/100g); fontes médias (50 a 100 mg/100g); fontes baixas (25 a 50 mg/100g) e fontes muito baixas, quando menores que 25 mg/100g de polpa. Os frutos de lulo do presente trabalho apresentaram, aos 63;73; 80; 87; 90 e 95 DAA, teores de ácido ascórbico de 2,86; 2,56; 2,36; 2,16; 2,07 e 1,92 mg/100g de polpa. Portanto, segundo a classificação apresentada, os frutos de lulo são classificados como de fonte muito baixa de vitamina C.
As médias dos teores de carotenoides ajustaram-se a um padrão de desenvolvimento sigmoidal simples em resposta à variação do tempo (Figura 6B).
Observa-se, ao longo do desenvolvimento dos frutos, incremento no teor de carotenoides, partindo de 2,33 mg/100g da massa fresca da polpa aos 66 DAA para 5,16 mg/100g aos 95 DAA.
Os teores de carotenoides totais aumentam durante o amadurecimento de diversos frutos, momento em que a carotenogênese é intensificada (LIMA et al., 2002), a exemplo da manga (SILVA et al., 2011a). Segundo Huyskens et al. (2001), o principal carotenoide encontrado no fruto de lulo é o β-caroteno.
A atividade respiratória nos primeiros 10 dias de desenvolvimento do fruto foi intensa (Figura 7). A alta atividade respiratória durante o período inicial de desenvolvimento pode estar relacionada à maior energia despendida devido à intensa divisão celular. Em geral, os tecidos jovens que apresentam células em crescimento ativo possuem taxas de respiração mais elevadas que os tecidos com células mais velhas ou maduras, fato que não tem relação com o padrão climatérico ou não climatérico do fruto (JOAS et al., 2012).
A taxa de produção de CO2 decresceu de 1.206,35 mg CO2 kg-1 h-1, aos 10 DAA, para 447,04 mg CO2 kg-1 h-1 aos 17 DAA (Figura 7). Essa queda brusca na atividade respiratória, provavelmente, ocorreu porque a multiplicação celular diminuiu com o passar do tempo. Dos 17 aos 45 DAA, a produção de CO2 continuou em queda, porém um pouco mais suave, passando de 447,05 mg CO2 kg-1 h-1 para 58,06 mg CO2 kg-1 h-1. Dos 45 aos 52 DAA, a produção do CO2 manteve-se estável, com média de 57,08 mg CO2 kg-1 h-1. Dos 52 aos 59 DAA, houve um aumento da produção de CO2 caracterizado como ascensão climatérica, até atingir o pico aos 66 DAA, com produção de 110,99 mg CO2 kg-1 h-1. Pode-se observar que eventos importantes ocorreram simultaneamente ao pico climatérico, como o ponto de curvatura máxima para a massa fresca do fruto (Figura 3A) e o volume do fruto (Figura 1C). No último dia de análise, aos 95 DAA, a produção de CO2 foi de 13,05 mg CO2 kg-1h-1.
A partir dos 66 DAA, após o climatério respiratório, observa-se que o teor de vitamina C (Figura 6A) e a acidez titulável (Figura 5B) da polpa diminuem com o passar do desenvolvimento, e o teor de sólidos solúveis (Figura 5A) aumenta. Segundo Joas et al. (2012), esse decréscimo ocorre porque os ácidos orgânicos estão sendo largamente utilizados como substratos no processo respiratório ou na sua transformação em açúcares, levando a um aumento no teor de sólidos solúveis.
Durante o desenvolvimento do fruto de lulo, foram identificadas três fases, delimitadas pelos PCmín e PCmáx das equações de ajuste sigmoidal simples das características físicas referentes ao fruto inteiro (Tabela 1). Segundo Alvares et al. (2004), nesse modelo, a primeira fase é, predominantemente, de intensa divisão celular, a segunda fase, de expansão rápida e a terceira fase, de maturação. Nota-se também que os PCmín e PCmáx variaram de acordo com a característica. Portanto, embora seja possível estabelecer as fases do desenvolvimento para cada uma das características avaliadas, optou-se por utilizar suas médias para a delimitação do intervalo de tempo de cada fase.
- Pontos de curvatura mínima e máxima e taxas de crescimento máximas, em função do DAA, para as características físicas avaliadas durante o desenvolvimento do fruto de lulo, nas condições de Viçosa-MG.
A primeira fase do desenvolvimento do fruto variou de -13,64 (comprimento) a 21,80 DAA (massa seca do fruto), com média de 7,39 DAA (Tabela 1). Essa fase é caracterizada pela alta taxa respiratória (Figura 9), provavelmente devido à intensa multiplicação celular, sendo que a maior parte dos assimilados que chega ao fruto é convertida em energia e esqueletos de carbono para a formação de novas células, restringindo o acúmulo de reservas (JOAS et al., 2012). Ainda nesta fase, o fruto apresenta o pericarpo com coloração verde-clara (Figura 4), e os incrementos no comprimento, diâmetro, volume e da massa do fruto são muito pequenos.
A segunda fase do desenvolvimento do fruto estendeu-se a partir dos 7,39 DAA até 57,63 DAA (Tabela 1), com o final da fase variando de 47,57 DAA para o comprimento, 42,26 DAA para o diâmetro equatorial, 63,37 DAA para o volume, 62,35 DAA para a massa fresca do fruto e 72,62 DAA para a massa seca do fruto. Nesta fase, registraram-se as taxas máximas de incremento das dimensões e da massa do fruto. A taxa respiratória decresceu dos 10 aos 45 DAA, e manteve-se estável por mais uma semana (52 DAA), e o pericarpo desenvolveu cor verde intensa (109 °h) (Figura 4). De acordo com Joas et al. (2012), durante o alongamento celular, polímeros de parede são constantemente sintetizados, ao mesmo tempo em que a parede preexistente se expande. Durante essa fase, houve grande incremento no comprimento, no diâmetro equatorial, no volume e no acúmulo de massa fresca, e não foi possível separar a polpa do pericarpo.
A terceira e última fase do desenvolvimento estendeu-se a partir dos 57,63 DAA até os 95,00 DAA (Tabela 1), último dia de avaliação. Nessa fase, houve tendência à estabilização nas dimensões e no acúmulo de massa fresca e seca do fruto. Nesse período, ocorreu a ascensão climatérica (de 52 a 59 DAA), o climatério respiratório (66 DAA), com pico de produção de CO2 de 110,99 CO2 kg-1 h-1 e o pós-climatério (dos 73 aos 95 DAA). Essa é a fase de amadurecimento do fruto, quando há aumento no teor de sólidos solúveis na polpa (Figura 10) e, concomitantemente, queda da acidez titulável (Figura 11) e vitamina C da polpa (Figura 12), o que é comum nos frutos em seu estágio final de amadurecimento e senescência, quando os ácidos orgânicos começam a ser utilizados como substrato para o processo de respiração. Paralelamente, o pericarpo desenvolveu coloração alaranjada (Figura 4) gradativamente, característica da espécie. Nessa terceira fase, devido à mudança na textura do fruto, foi possível separar a polpa do pericarpo (a partir dos 66 DAA), estando o fruto apto para ser consumido.
CONCLUSÕES
1-O ciclo do desenvolvimento do fruto de lulo em Viçosa estende-se por 95 dias.
2-O padrão de desenvolvimento do fruto ajusta-se ao modelo sigmoidal simples, com três estágios de crescimento, de 0 a 7,39 dias após a antese (DAA), de 7,39 até 57,63 DAA e de 57,63 a 95,00 DAA.
3-O climatérico respiratório do fruto ligado à planta é atingido aos 66 DAA, com pico de produção de CO2 de 110,99 mg de CO2 kg-1 h-1.
4-Para consumo in natura, o fruto de lulo pode ser colhido a partir dos 73 DAA, pois apresenta mais de 50% do pericarpo alaranjado.
5-Para uso na agroindústria, o fruto de lulo pode ser colhido a partir dos 85,47 DAA, pois apresenta mais de 9º Brix.
Recebido em: 15-05-2012.
Aceito para publicação em: 24-01-2013.
- ÁLVARES, V. S.; BRAGA, L. R.; MAIA, V. M.; SALOMÃO, L. C. C.; BRUCKNER, C. H.; RUIZ, G. A. C. Desenvolvimento do pêssego 'Rei da Conserva' em Viçosa-MG. Revista Ceres, Viçosa, MG, v.52, n. 294, 2004.
- ARGENTA, L.C; BENDER, R.J; KREUS, C.L.; MONDARDO, M. Padrões de maturação índices de colheita de maçãs cvs. Gala, Golden Delicious e Fuji. Pesquisa Agropecuária Brasileira, Brasília, v. 30, n. 10, p. 1259- 1166, 1995.
- CAVICHIOLI, J. C.; RUGGIERO, C.; VOLPE, C. A.; PAULO, E. M.; FAGUNDES, J. L.; KASAI, F. S. Florescimento e frutificação do maracujazeiro-amarelo submetido à iluminação artificial, irrigação e sombreamento. Revista Brasileira de Fruticultura, Jaboticabal, v.28, n.1, p.92-96, 2006.
- FRANCO, G.; BERNAL, J.; GIRALDO, M. J.; TAMAYO, P J.; CASTAÑO , O.; TAMAYO, A.; GALLEGO, J. L.; BOTERO, M. J.; RODRIGUEZ, J. E.; GUEVARA, N. J.; MORALES, J. E.; LONDOÑO, M.; RÍOS, G.; RODRÍGUEZ, J. L.; CARDONA, J. H.; ZULETA, J.; CASTAÑO, J.; RAMÍREZ, M. C. El cultivo del lulo Colômbia: CORPOICA, 2002. 103 p.
- GOUVEIA, J. P. G.; ALMEIDA, F. A. C.; MEDEIROS, B. G. S.; RIBEIRO, C. F. A.; SILVA, M. M. Maturação da goiaba (Psidium guajava l.) mediante parâmetros físico-químicos. Revista Brasileira de Produtos Agroindustriais, Campina Grande, n.1, p.85-94, 2003.
- HUYSKENS, K. S.; PRONO-WIDAYAT, H.; SCHREINER, M.; PETERS, P. Effect of surface coating and film packaging on the keeping quality of solanaceous crops (Solanum muricatum Ait., Solanum quitoense Lam.). Acta Horticulturae, The Hague, v.553, p.621 - 625, 2001.
- JOAS, J.; VULCAIN, E.; DESVIGNES, C.; MORALES, E.; LÉCHAUDEL, M. Physiological age at harvest regulates the variability in postharvest ripening, sensory and nutritional characteristics of mango (Mangifera indica L.) cv. Coghshall due to growing conditions. Journal of the Science of Food and Agriculture, London, v. 92, n. 6, p. 1282-1290, 2012.
- LAVIOLA, B. G.; ALVES, A. A.; GURGEL, F. L.; ROSADO, T. B. ; ROCHA, R. B. ; ALBRECHT, J. C. Estimates of genetic parameters for Physic nut traits based in the germplasm two years evaluation. Ciência Rural, Santa Maria, v. 42, p. 1-7, 2012.
- LICHTENTHALER, H. K. Chlorophylls and carotenoids: Pigments of photosynthetic biomembranes. Methods in Enzymology, New York, v. 148, p. 349-382, 1987.
- LIMA, V. L. A. G.; MELO, E. A., LIMA, D. E. Fenólicos e carotenóides totais em pitanga. Scientia Agricola, Piracicaba, v.59, n.3, p.447-450. 2002.
- MEDEIROS, E. A. A.; SOARES, N. de F. F.; POLITO, T. de O. S.; SOUSA, M. M. de; SILVA, D. F. P. da. Sachês antimicrobianos em pós-colheita de manga. Revista Brasileira de Fruticultura, Jaboticabal, v. 33, p. 363-370, 2011.
- SALOMÃO, L. C. C.; SIQUEIRA, D. L. DE; PEREIRA, M. E. C. Desenvolvimento do fruto da lichieira (Litchi chinensis Sonn.) 'Bengal'. Revista Brasileira de Fruticultura, Jaboticabal, v. 28, n.1, p. 11-13, 2006.
- SANTACRUZ, M. A. Estudio fenológico y reproductivo de la naranjilla (Solanum quitoense Lam), peach tomato (Solanum sessiliflorum Dunal) y uchuva (Physalis peruviana Lam). 2004. 67 f. Tese (Mestrado em Ciencia y Producción Agropecuaria) - El Zamorano, Honduras, 2004.
- SILVA, D. F. P. da; SALOMÃO, L. C. C.; CABRINI, E. C.; ALVES, R. R.; STRUIVING, T. B. Prevenção do escurecimento do pericarpo de lichia através do uso de ácidos e filmes. Revista Brasileira de Fruticultura, Jaboticabal, v. 33, p. 519-527, 2011b.
- SILVA, D. F. P. da; SALOMÃO, L. C. C.; CECON, P. R.; SIQUEIRA, D. L.; ROCHA, A. Anticipation of 'Ubá' mango ripening with preharvest ethephon application. Ciência Rural, Santa Maria, v. 41, p. 63-69, 2011a.
- SILVA, D. F. P. DA; SALOMÃO, L. C. C.; SIQUEIRA, D. L.; CECON, P. R.; STRUIVING, T. B. Amadurecimento de manga 'Ubá'com etileno e carbureto de cálcio na pós-colheita. Ciência Rural, Santa Maria, v. 42, p. 213-220, 2012.
- SOARES, N. DE F. F.; SILVA, D. F. P.; CAMILLOTO, G. P.; OLIVEIRA, C. P.; PINHEIRO, N. M.; MEDEIROS, E. A. A. Antimicrobial edible coating in postharvest conservation of guava. Revista Brasileira de Fruticultura, Jaboticabal, v. 33, p. 281-289, 2011.
Datas de Publicação
-
Publicação nesta coleção
27 Maio 2013 -
Data do Fascículo
Mar 2013
Histórico
-
Recebido
15 Maio 2012 -
Aceito
24 Jan 2013