Resumo
Chromium and copper-doped hematites were prepared with the aim of studying the synergistic effect of these dopants on the textural and on the catalytic properties of the iron oxides towards the high temperature shift reaction. It was found that the most active catalysts were those with the highest amount of copper. They had the Fe(II)/Fe(III) ratio near the stoichiometric value of magnetite, the highest surface areas under the reactional atmosphere and the greatest tendency to produce the active form; they also were poorly crystalline solids. The best performance was shown by the catalyst with Fe/Cu=10, heated at 300ºC. It can thus be concluded that copper acts both as textural and structural promoter in these catalysts.
iron oxides; copper-doped catalysts; chromium-doped catalysts
iron oxides; copper-doped catalysts; chromium-doped catalysts
ARTIGO
Propriedades texturais e catalíticas de óxidos de ferro contendo cromo e cobre
Instituto de Química - Universidade Federal da Bahia - Campus Universitário de Ondina - 40.170-280 - Salvador - BA
Recebido em 12/6/97; aceito em 8/10/97
Textural and catalytic properties of chromium and copper-doped iron oxides. Chromium and copper-doped hematites were prepared with the aim of studying the synergistic effect of these dopants on the textural and on the catalytic properties of the iron oxides towards the high temperature shift reaction. It was found that the most active catalysts were those with the highest amount of copper. They had the Fe(II)/Fe(III) ratio near the stoichiometric value of magnetite, the highest surface areas under the reactional atmosphere and the greatest tendency to produce the active form; they also were poorly crystalline solids. The best performance was shown by the catalyst with Fe/Cu=10, heated at 300oC. It can thus be concluded that copper acts both as textural and structural promoter in these catalysts.
Keywords: iron oxides; copper-doped catalysts; chromium-doped catalysts.
INTRODUÇÃO
Os catalisadores a base de óxidos de ferro são usados em diversos processos industriais, tais como a síntese de amônia, conversão do monóxido a dióxido de carbono a altas temperaturas1, desidrogenação do etilbenzeno a estireno, amoxidação do propeno a acrilonitrila e desidrogenação oxidativa de buteno a butadieno2,3.
Na conversão do monóxido a dióxido de carbono:
os óxidos de ferro catalisam a reação na faixa de 350 a 400oC, sob condições cinéticas favoráveis. Esta etapa, conhecida como reação de HTS (High Temperature Shift), é seguida de um outro estágio (reação de LTS, Low Temperature Shift), conduzido a cerca de 200oC, em atendimento aos requisitos termodinâmicos. A ocorrência dos dois processos se justifica pela necessidade de se alcançar conversões comercialmente aceitáveis1.
Essa reação é uma etapa importante em diversos processos industriais, principalmente na síntese de amônia e na produção de hidrogênio para a liquefação do carvão, hidrotratamento de frações pesadas do petróleo, além do uso direto como combustível4.
Os catalisadores usados no estágio conduzido a altas temperaturas são comercializados, em sua maioria, na forma de hematita (a-Fe2O3), mas em alguns casos podem ser encontrados como maghemita (g-Fe2O3) ou goethita, a-FeOOH5. Esses materiais devem ser reduzidos, para formar a fase ativa, magnetita (Fe3O4). A natureza do estado precursor influencia o grau de sinterização do sólido durante o processo de redução.
Usualmente, óxidos de cromo (Cr2O3 ou CrO) são incorporados ao sólido para aumentar a área específica e evitar a sinterização tanto durante a redução como ao longo da vida útil do catalisador6,7. A interação desses óxidos com a hematita, durante a calcinação, foi estudada a várias temperaturas, visando elucidar as propriedades físico-químicas do sistema6. Observou-se que os óxidos de cromo formam soluções sólidas com a magnetita, sendo dispersos através da massa do óxido de ferro evitando, desta forma, a sinterização durante a redução8. Diversos estudos5,9 demonstraram que, em materiais com teores de cromo superiores a 14% (m/m), a espécie Cr+3 livre recobre a superfície do óxido de ferro, levando à perda de atividade catalítica. Os catalisadores comerciais típicos apresentam óxido de cromo na faixa de 8-10% (m/m)9.
Na maioria das plantas industriais, o processo de redução do catalisador de HTS ocorre in situ, utilizando-se o gás de processo, constituído por monóxido e dióxido de carbono, nitrogênio, argônio, hidrogênio e vapor d'água1,10. As relações CO/CO2 e H2/H2O são parâmetros importantes para determinar o equilíbrio entre a hematita e magnetita. A produção deste último óxido deve ser favorecida, enquanto deve-se evitar a formação de ferro metálico, pois este catalisa a reação entre o monóxido de carbono e o hidrogênio para formar metano, ou o desproporcionamento do CO para formar carbono1:
A reação de metanação, por ser altamente exotérmica, leva ao aumento da temperatura da superfície, podendo causar danos ao catalisador. Por outro lado, o carbono depositado no desproporcionamento do CO leva ao bloqueio dos sítios ativos1.
As propriedades e desempenho dos catalisadores industriais, assim como os processos de redução, são alterados pela adição de promotores. Além do cromo, encontram-se na literatura8, estudos envolvendo catalisadores dopados com Ni+2, Cu+2, Mg+2, Co+2, Al+3, Mn+2, Li+, Na+, K+, Ba+2 e Si+4. Entre eles, o cobre foi considerado o mais promissor, pois aumenta a atividade da magnetita em relação à reação de HTS11. Este metal é encontrado na última geração de catalisadores industriais dessa reação que, por essa razão, apresentam melhor desempenho quando comparados aos sistemas tradicionais. Pode-se, usando-se esses materiais, diminuir a temperatura de reação de 370oC a valores próximos a 330oC, e a relação vapor/gás pode ser inferior àquela usada industrialmente (0,6), mantendo-se ainda a seletividade. Entretanto, apesar da importância comercial desses catalisadores, não existe, em literatura aberta, um estudo sistemático sobre a influência do cobre nas características e no desempenho desses sistemas. Além disso, os estudos relacionados à preparação desses materiais também ainda são incipientes.
Neste trabalho foram preparados catalisadores a base de óxidos de ferro, contendo cromo e cobre, através do processo sol-gel, visando estudar o efeito sinérgico desses metais nas propriedades texturais e catalíticas dos materiais, relacionando as características do catalisador com o seu desempenho. Os sólidos obtidos foram caracterizados por análise química, difratometria de raios X, medidas de área superficial e de porosidade, calorimetria exploratória diferencial e termogravimetria. As amostras foram avaliadas em teste microcatalítico, em relação à reação de HTS e os resultados de atividade catalítica foram comparados com aquele obtido com o catalisador comercial.
PARTE EXPERIMENTAL
Os catalisadores foram produzidos por decomposição térmica dos hidróxidos mistos de ferro, cromo e cobre, seguindo um planejamento fatorial de duas variáveis em dois níveis: (i) razão molar Fe/Cu = 10 ou 55; (ii) temperatura de calcinação de 300 ou 600oC. Em todas as amostras, a relação Fe/Cr=10 foi mantida constante. Todos os materiais foram preparados a partir de soluções 1 M de nitrato férrico, obtidas dissolvendo-se 0,25 mol (101g) de Fe(NO3)3.9H2O em água, e soluções aquosas de 0,1M de nitrato de cromo (III), obtidas a partir de 0,025 mol (10g) de Cr(NO3)3.9H2O. Na síntese dos materiais com relação Fe/Cu = 55, partiu-se de soluções 0,02M de nitrato de cobre, contendo 0,005 mol (1,21g) de Cu(NO3)2.3H2O. Na obtenção dos sólidos com relacão molar Fe/Cu = 10, foram usadas soluções 0,1 M de nitrato de cobre (II), a partir de 6,02g de Cu(NO3)2.3H2O. Na preparação dos precursores, as soluções dos nitratos de ferro, cromo e cobre foram misturadas. A esse sistema, adicionou-se uma solução 6M de hidróxido de potássio, à temperatura ambiente e sob agitação magnética. O pH final foi ajustado para 10. O sistema foi agitado por meia hora e depois centrifugado. O gel obtido foi lavado seis vezes com água, a 60oC, para retirar o potássio e nitrato provenientes do material de partida e do agente precipitante. Após a lavagem, o gel foi seco a 120oC, até se obter uma massa constante. O material foi moído e passado em uma peneira de 200 mesh. Em seguida, as amostras foram calcinadas ao ar, nas temperaturas de 300 e 600oC, por 2 h.
A determinação do teor de ferro nas amostras foi feita através do método espectrofotométrico de complexação do íon Fe+3 com ácido tioglicólico12, utilizando-se um espectrofotômetro Colleman, modelo 295E e comprimento de onda de 535 nm. Na análise de cromo, os catalisadores foram fundidos com uma mistura de ácido bórico e carbonato de potássio e dissolvidos em ácido clorídrico. Após a adição de solução de permanganato de potássio, destruiu-se o excesso de permanganato por ebulição em presença de ácido clorídrico, e adicionou-se sulfato ferroso amoniacal, seguido de ácido fosfórico. O excesso de sulfato ferroso amoniacal foi titulado por retorno, com solução padrão de dicromato de potássio, utilizando-se difenilaminassulfonato de bário como indicador13. Os teores de cobre e potássio foram determinados por absorção atômica, em um aparelho Perkin Elmer, modelo 403, utilizando-se-se uma lâmpada de cátodo oco e comprimento de onda de 683 nm e 766,5 nm respectivamente.
Na obtenção dos difratogramas de raios X foi usado um equipamento Phillips, modelo 1130, com radiação CuKa , gerada a 30 KV, 20 mA e filtro de níquel. Na medida das áreas superficiais, foram usadas duas condições de ativação das amostras: (i) sob vácuo, a 150oC, por 6h; (ii) sob fluxo (100 ml/min) de uma mistura redutora, a 350oC, por 2h. No primeiro caso, utilizou-se um instrumento Micrometics, modelo Digisorb 2600. No outro, foi usado um aparelho da CG Instrumentos Científicos, modelo CG-2000, e uma mistura 50% H2/N2, com composição próxima à do gás de processo, usado na reação de HTS.
As curvas de calorimetria exploratória diferencial foram obtidas em duas condições diferentes: (i) sob fluxo de nitrogênio; (ii) sob fluxo de uma mistura 50% H2/N2, ambos a 100 ml/min. O aquecimento foi feito desde a temperatura ambiente até 600oC, a uma velocidade de 10 graus/min. As análises termogravimétricas foram efetuadas nas duas condições descritas. Em todos os casos, utilizou-se um aparelho Du Pont, modelo 9900. As medidas de porosidade foram conduzidas em um porosímetro de mercúrio Micrometrics, modelo Auto Pore II 9220.
A atividade catalítica dos sólidos foi avaliada em relação à reação de HTS, em teste microcatalítico (Figura 1) operando à pressão atmosférica e 370oC, usando-se uma relação vapor/gás de processo igual a 0,6 na mistura gasosa de alimentação do reator. Além das amostras preparadas, utilizou-se também um catalisador comercial, para fins de comparação. Foi usado um reator de leito fixo, construído em aço inox, com diâmetro interno de 3/16". A temperatura do reator foi medida através de um termopar centrado no leito catalítico, formado por aproximadamente 0,1g do catalisador. A mistura gasosa (40ml/min) foi passada por um saturador contendo água à temperatura de 76oC e, em seguida, alimentada ao reator. Os efluentes da reação foram analisados por um cromatógrafo CG-35, em linha com o reator. Na determinação dos teores de CO e CO2 foram utilizadas colunas empacotadas com peneira molecular 13X e porapak-Q respectivamente, e um detetor de condutividade térmica. Usou-se hidrogênio como gás de arraste (30 ml/min). Após os testes catalíticos, determinou- se a razão Fe(II)/Fe(III) nos catalisadores, para avaliar a estabilidade da fase ativa (magnetita) sob as condições da reação.
Os teores de Fe(II) foram determinados dissolvendo-se as amostras numa solução de ácido clorídrico 18%,sob refluxo e em atmosfera de dióxido de carbono, seguida da titulação com dicromato de potássio, usando difenilaminasulfonato de bário como indicador12. Os teores de ferro total foram obtidos como descrito anteriormente e os de Fe(III) foram calculados por diferença.
RESULTADOS E DISCUSSÃO
Os resultados de análise química indicaram que as condições de precipitação foram favoráveis à formação dos compostos de ferro e cromo. Isto pode ser evidenciado pelos valores da razão Fe/Cr dos sólidos obtidos, apresentados na tabela 1, que diferem pouco daqueles da solução de partida. O mesmo acontece com os materiais com elevados teores de cobre. Por outro lado, as amostras com Fe/Cu=55, na solução de partida, apresentaram uma diminuição nesta relação. Este comportamento pode ser explicado considerando-se a adsorção do íon cobre, pelas partículas coloidais de hidróxido de ferro14. Nas condições do experimento, dificilmente se formaria hidróxido de cobre, pois a presença dos íons amônio leva à formação do complexo [Cu(NH3)4(H2O) 2]2+, solúvel em água. Isto se deve à alta labilidade do composto [Cu(H2O)6]2+, presente em soluções aquosas de sais de cobre, característica da configuração d9, facilitando a troca das moléculas de água. A substituição posterior de ligantes é difícil, em virtude da maior distância entre o íon Cu+2 e o quinto e sexto ligantes, como resultado do efeito Jahn Teller. Devido a esse fenômeno, se forma um complexo quadrado planar tetramina, com as demais posições permanecendo ocupadas por moléculas do solvente. Dessa forma, o complexo [Cu(NH3)6]2+ só se forma em amoníaco líquido, enquanto o hidróxido de cobre só é produzido em soluções diluídas de amônia sem excesso15-17. A razão Fe/K variou consideravelmente entre os materiais com Fe/Cu=10 e 55, e em relação ao material de partida (Fe/K= 0,2), observando-se que, em presença de maior quantidade de cobre, há uma menor retenção do potássio proveniente do agente precipitante. .
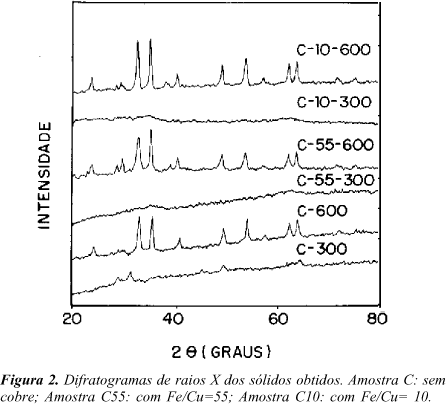
Nos difratogramas de raios X das amostras obtidas (Figura 2), observa-se o padrão da hematita, em todos os sólidos cristalinos18. Os materiais calcinados a 300oC permaneceram não-cristalinos, havendo uma cristalização incipiente apenas na amostra sem cobre. Não se notou um efeito significativo da presença e do teor de cobre, sobre a cristalinidade dos sólidos.
A figura 3 mostra os resultados dos experimentos de análise térmica, conduzidos em atmosfera inerte e usando-se amostras dos precursores dos catalisadores (hidróxidos ou óxidos de ferro hidratados). Neste caso, pode-se acompanhar as transformações térmicas decorrentes da formação da hematita (forma comercial do catalisador de HTS). Observa-se a presença de efeitos endotérmicos,em temperaturas inferiores a 300oC, que são atribuídos à perda de água adsorvida e de desidratação19; isto concorda com a curva termogravimétrica, que mostra uma perda de massa nesta região. A partir de 300oC, as curvas térmicas apresentam diferentes perfis: no caso da amostra C10, nota-se um pico a 490oC devido à formação da hematita19 enquanto que, na curva térmica da amostra C-55, há um efeito endotérmico a 571oC, provavelmente associado à ocorrência simultânea de formação da hematita (exotérmica) e à perda de água de hidratação remanescente (endotérmica). A forma do pico sugere que o segundo processo superou o primeiro, resultando num efeito endotérmico. Isto é confirmado pela curva termogravimétrica, que mostra uma perda de massa nessa região, correspondente ao processo de desidratação, apenas no caso da amostras C-55. Esses resultados estão coerentes com os difratogramas obtidos, que mostram a formação de hematita em temperaturas superiores a 300oC.
As curvas térmicas dos catalisadores, obtidos em atmosfera redutora (50% H2/N2), apresentam picos característicos da redução da hematita (a-Fe2O3) a magnetita (Fe3O4) e da formação de ferro métalico. De acordo com informações da literatura20, a redução do óxido férrico ocorre em duas etapas consecutivas:
com a etapa I (exotérmica) ocorrendo a cerca de 300oC e a etapa II (endotérmica) em temperaturas mais altas; a posição dos picos, nas curvas térmicas, pode ser alterada pela presença de dopantes. Portanto, os picos observados na região de 150 a 260oC, nos termogramas dos sólidos, podem ser atribuídos à formação da magnetita, enquanto aqueles observados a cerca de 400oC são provavelmente devido à produção de ferro metálico.
As temperaturas iniciais de formação da magnetita (Tm) e do ferro metálico (Tf) são apresentadas na tabela 2. Nota-se que, em todos os casos, os valores de Tm diminuem com o aumento do teor de cobre nas amostras. Os sólidos isentos de cobre apresentam temperaturas mais elevadas, o que está em concordância com dados da literatura20:estudando o efeito de dopantes na redução da hematita, notou-se que este óxido isento de dopantes apresentou Tm=310oC, enquanto que o óxido férrico dopado com cromo mostrou Tm=275oC e o mesmo óxido dopado com cobre (isento de cromo) apresentou Tm= 210oC.
Observou-se a formação do ferro metálico em temperaturas superiores a 340oC, exceto no caso da amostra C, calcinada a 300oC, em que esse fenômeno não ocorreu na faixa de temperatura utilizada nos experimentos. O aumento do teor de cobre levou a um aumento dessa temperatura, indicando que a presença do metal dificulta a formação do ferro metálico estabilizando, portanto, a fase ativa. A temperatura de calcinação também influencia esse processo, notando-se que a magnetita é tanto mais estável, quanto menor for o seu valor.
Os resultados das áreas superficiais das amostras estão indicados na tabela 3. Esses valores foram obtidos após a ativação das amostras em atmosfera inerte (N2,100ml/min, por 2h a 150oC) e sob fluxo de uma mistura 50% H2/N2 (100 ml/min) por 2h, a 350oC. Na última situação, obtém-se resultados de área em condições semelhantes às da reação de HTS. Em ambos os casos, a área varia com o teor de cobre: em atmosfera inerte, essa variação é irregular mas, sob condições redutoras,a presença do cobre favorece a formação de sólidos com áreas mais elevadas. Os valores obtidos em atmosfera redutora, foram menores que aqueles medidos sob fluxo de gás inerte, com os materiais calcinados a 300oC, indicando que ocorre uma diminuição da área, durante a redução desses catalisadores. As áreas dos materiais, aquecidos a 600oC, não variaram de modo regular devido à redução. Relacionando estes resultados com aqueles obtidos por difratometria de raios X, observa-se que, no caso das amostras calcinadas a 600oC, se obtém magnetita bem cristalizada a partir da hematita. Nos sólidos obtidos a 300oC a redução da hematita ocorre a partir de uma forma não-cristalina aos raios X, provavelmente uma mistura de óxidos e hidróxidos de ferro. No processo de redução a partir da goethita, ocorrem as seguintes etapas21:
Uma vez que as fases presentes, nos sólidos calcinados a 300oC, podem ser constituídas por óxidos e hidróxidos de ferro, estas etapas podem estar ocorrendo simultaneamente com a desidratação, sendo as principais responsáveis pela sinterização; entretanto, nos sólidos calcinados a 600oC provavelmente ocorre apenas a etapa de redução, observando-se uma diminuição menor da área. Isto pode explicar a diferença na área superficial entre os materiais obtidos nas diferentes temperaturas e ativados em condições distintas.
As medidas de porosidade mostraram que os materiais são macroporosos, com mais de 70% dos poros com diâmetros superiores a 50nm. Os resultados são mostrados na tabela 4. Nota-se que o aumento do teor de cobre favorece a produção de sólidos mesoporosos a 300oC, enquanto que, a temperaturas mais altas, ocorre o inverso, com formação predominante de catalisadores macroporosos.
Com exceção da amostra C-10, calcinada a 300oC, os sólidos apresentaram cerca de 20% dos poros com diâmetros na faixa de 10 a 50 nm, que é próxima àquela sugerida por Datta e colaboradores22, como sendo a mais adequada para a reação de HTS. Esses pesquisadores, em estudos do efeito da porosidade na atividade catalítica para essa reação, concluíram que um aumento no tamanho de poros na faixa de 14,5 a 30nm contribui para um aumento na atividade catalítica, e que poros com diâmetros superiores a esse valor não têm efeito significativo sobre a atividade. Entretanto, esses resultados não foram confirmados por outros pesquisadores, não existindo na literatura um consenso sobre o efeito da porosidade na atividade dos óxidos de ferro, em relação à reação de HTS.
Todos os sólidos obtidos foram ativos, em relação à reação de HTS e os valores de atividade, correspondentes ao estado estacionário, estão indicados na tabela 5. Constatou-se que a presença de cobre leva à formação de catalisadores mais ativos, sendo o de melhor desempenho aquele com razão Fe/Cu=10 e calcinado a 300oC, que apresentou atividade próxima à do catalisador comercial. Esse sólido mostrou maior facilidade para formar magnetita, como foi detectado pelos resultados de análise térmica e o mais alto valor de área superficial sob condições redutoras. A partir da tabela, pode-se concluir que baixas temperaturas de calcinação e relações Fe/Cu favorecem a formação de catalisadores mais ativos.
Os resultados também mostraram que a seletividade aumentou com a diminuição da temperatura de calcinação, o que pode ser relacionado à menor tendência dos catalisadores, calcinados a baixas temperaturas, para produzir ferro metálico, como mostram os resultados de análise térmica, obtidos sob condições redutoras. Isto significa que, nestes casos, a magnetita é estável em atmosfera reacional. O efeito do teor do cobre variou em função da temperatura de calcinação: nas amostras calcinadas a 600oC, o aumento da concentração desse metal (e diminuição do teor de potássio) levou à produção de catalisadores mais seletivos, o que pode estar relacionado à atividade do cobre para a reação de HTS. É conhecido4 que esse metal é mais ativo que o ferro, nessa reação, sendo o seu uso limitado a baixas temperaturas (inferiores a 200oC) devido a problemas de sinterização. Entretanto é provável que, nas amostras estudadas, esse fenômeno seja dificultado pelo óxido de ferro, que funcionaria como suporte, atuando como espaçador do cobre e dificultando a sinterização. O baixo valor de seletividade da amostra C-55, calcinada a 600oC, pode ser associado à instabilidade da magnetita, com formação de ferro metálico, como mostram os valores da razão Fe(II)/Fe(III) e os resultados de análise térmica, obtidos sob condições redutoras, respectivamente. Por outro lado, a amostra C-10, calcinada a 600oC, apresentou pouca tendência para produzir ferro metálico e mostrou uma relação Fe(II)/Fe(III) próxima ao valor estequiométrico da magnetita. A 300oC, o aumento do teor de cobre leva a uma diminuição da seletividade, o que pode estar relacionado à porosidade da amostra C-10, calcinada nesta temperatura, que apresenta apenas 2% dos poros na faixa de tamanho considerada como a mais adequada para a reação de HTS22. A amostra C-55, calcinada a 300oC, por outro lado, possui características semelhantes, mas apresenta 18% dos poros na faixa indicada.
A razão Fe(II)/FeIII), medida após os testes variou em função da presença e do teor de cobre nos sólidos: as amostras com quantidades mais elevadas desse metal apresentaram valores próximos ou superiores ao valor estequiométrico da magnetita (0,5). Isto indica que a magnetita é a fase estável sob as condições da reação.
A tabela 6 mostra a atividade catalítica por área superficial dos catalisadores, medida em atmosfera redutora. Esses resultados indicam que a presença e o aumento no teor de cobre, nos materiais, aumentam a atividade por área do catalisador. A combinação desse efeito com o da temperatura de calcinação eleva a atividade do catalisador com Fe/Cu=10 para 1,36 mol.m2.h-1.
Com relação ao efeito dos promotores sobre a cinética da reação de HTS, observou-se que estes podem afetar a velocidade da reação de diversas maneiras. Bohlbro10, por exemplo, encontrou que a presença de hidróxido de sódio altera a forma matemática da lei de velocidade, levando a um aumento no expoente da concentração de monóxido de carbono e tornando negativo o expoente do termo da concentração da água. Entretanto, não existe estudo cinético de catalisadores de HTS contendo cobre, em literatura aberta.
De modo geral, muitas expressões têm sido propostas para descrever a cinética da reação de HTS sobre catalisadores industriais; existem, todavia, muitas discordâncias não só sobre a forma da lei de velocidade, mas também dos valores das constantes cinéticas ou de energias de ativação9. Esta diversidade se deve às variações de composição da superfície dos sólidos, presença de impurezas, condições não-isotérmicas e difusão superficial1,10.
No presente trabalho, observou-se que a presença e o aumento do teor de cobre aumentam a atividade dos catalisadores à base de ferro e cromo, sugerindo que o mesmo aumenta a velocidade da reação; por outro lado, altos teores de cobre estão sempre associados a baixos teores de potássio, não sendo possível inferir sobre o efeito deste último sobre a velocidade, sem o estudo sistemático da influência dessas variáveis sobre a cinética da reação.
A partir desses resultados verifica-se que os catalisadores mais ativos foram aqueles com maiores teores de cobre, que apresentaram as seguintes características: baixa cristalização, áreas superficiais mais elevadas sob as condições da reação, razão Fe(II)/Fe(III) próxima ao valor estequiométrico da magnetita e maior tendência a formar a fase ativa. A atividade catalítica por área aumentou com o teor de cobre e com a temperatura de calcinação. Esses resultados mostram que, nesses catalisadores, o cobre atua como promotor textural e estrutural.
CONCLUSÕES
Aquecendo-se hidróxidos mistos de ferro, cobre e cromo, à temperatura de 600oC, formam-se hematitas cristalinas, sendo a cristalinidade independente da relação Fe/Cu; o aquecimento a 300oC não conduz à cristalização dos sólidos, que ocorre a 500oC. Esses materiais são macroporosos e possuem áreas superficiais entre 8 e 160 m2.g-1, sendo seu valor dependente da temperatura de calcinação e do teor de cobre.
Nas condições da reação de HTS, esses sólidos são reduzidos a magnetita, cujas áreas são tanto maiores quanto menores forem a temperatura de calcinação e a razão Fe/Cu. A presença de cobre facilita a formação desse óxido e esse efeito é acentuado pelo aumento do teor do metal e da temperatura. As atividades desses catalisadores também variaram no mesmo sentido; por outro lado, a seletividade aumentou com a presença de cobre e com a diminuição da temperatura de calcinação. Os valores de atividade catalítica por área indicaram que o cobre atua também como promotor estrutural.
Os sólidos com Fe/Cu= 10 apresentaram atividade catalítica próxima e seletividade mais alta, em relação ao comercial; entre eles a amostra calcinada a 300oC apresentou o melhor desempenho.
A partir desses resultados, concluiu-se que o papel do cobre em aumentar a atividade desses catalisadores está relacionado com as modificações texturais (baixa cristalização, áreas elevadas sob as condições da reação) e estruturais, como a razão Fe(II)/Fe(III) próxima ao valor estequiométrico da magnetita e maior tendência em formar a magnetita.
AGRADECIMENTOS
MOGS e EBQ agradecem à CAPES e ao CNPq pelas bolsas concedidas. Os autores agradecem ao CNPq e à FINEP, pelo apoio financeiro e à Oxiteno Química S.A. e ao Instituto de Química da Unicamp pela caracterização dos catalisadores.
18. Powder Diffraction File, Joint Comitee on Powder Diffraction Standards, card 13-534.
- 1. Campbell, J. S.; Craven, P.; Young, P. W.; Catalyst Handbook; Wolfe Scientific Books ; London, 1970; p. 97.
- 2. Kung, H. Hand Kung, M. C.; Advances in Catalysis 1985, 13, 159.
- 3. Lee, E. H.; Catal. Rev. - Sci Eng. 1973, 8, 285.
- 4. Newsome E.; David S.; Catal. Rev. - Sci Eng. 1980, 21, 275.
- 5. Kundu, M. L.; Segupta, A. C.; Maiti, G. C.; Sen, B.; Ghosh, S. K.; Kuznetsov, V. I.; Kustova, G. N.; Yurchenco, E. N.; J. Catal. 1988, 112, 375.
- 6. Maitti, G.; Ghosh, S. K.; Indian J. Chem. 1985, 24A, 513.
- 7. Rangel, M. C.; Sassaki, R. M.; Galembeck, F.; Catal. Lett. 1995, 33, 237.
- 8. Dry, M. E.; Plessis, J. A. K.; Leuritz, G.; J. Catal. 1966, 6, 194.
- 9. Chinchen R. H. L.; Spencer M. S.; Appl. Catal. 1984, 12, 69.
- 10. Bohlbro, H.; J. Catal. 1964, 3, 207.
- 11. Idakiév, V.; Mihajlova, D.; Kunev B.; Andreev A.; React. Kinet. Catal. Lett. 1988, 33, 119.
- 12. Vogel, A.; Denney, R. C.; Jeffery, G. H.; Medham, J.; Análise Inorgânica Quantitativa; Editora Guanabara Koogan S. A.; Rio de Janeiro, 1984; p. 268.
- 13. Bennett, H.; Reed R. H., Chemical Methods of Silicates Analysis A Handbook Academic Press Inc. London, 1971, 129.
- 14. Kolthoff, I. M.; Moskovitz, B. J.; Anal. Chem. 1937, 41, 629.
- 15. Cotton, F. A.; Wilkinson, G.; Química Inorganica Avanzada; Editorial Limusa S. A.; México, 1986; p. 933.
- 16. Basolo, F.; Johnson, R.; Química de los Compuestos de Coordinación; Editorial Reverté S. A.; Barcelona, 1980; p. 82, 144.
- 17. Livage, J.; Henry, M.; Sanchez, C.; Prog. Solid State Chem. 1988, 4, 259.
- 19. Fischer, W. R.; Shwertmann, V.; Clays Clay Miner. 1975, 23, 33.
- 20. Shimokawabe, M.; Fiuruichi R.; Ishii, T.; Thermochim. Acta 1979, 28, 287.
- 21. Seshan, K; Anatharaman, M. R.; Venkatseh R.; Shashimohan, K. V.; Chakrabarty, K.; Bulletin of Material Science 1981, 3, 201.
- 22. Datta, K. P.; Gupta, K. P.; Sen, B.; Procedings of the 4th Natl. Symposium on Catalysis 1978, 4, 226.
Datas de Publicação
-
Publicação nesta coleção
05 Nov 2002 -
Data do Fascículo
Jul 1998
Histórico
-
Recebido
12 Jun 1997 -
Aceito
08 Out 1997