Resumo
This review presents a brief account concerning the production, characterization and evolution of the knowledge in the area of diamond and boron-doped diamond films. The most important methods used for the growth of these films, such as chemical vapor deposition and high pressure/high temperature systems, as well as the several kinds of reactors which can be employed are reviewed. However, larger emphasis is given to the CVD method. Morphological, structural and electric properties of these films, as well as their role in the performance of voltammetric electrodes for electrochemistry and electroanalytical chemistry are also discussed.
CVD boron-doped diamond growth; diamond electrodes; electrochemistry
CVD boron-doped diamond growth; diamond electrodes; electrochemistry
DIVULGAÇÃO
Filmes de diamante CVD dopado com boro. Parte I . Histórico, produção e caracterização
Boron-doped CVD diamond films. Part I. History, production and characterization
Rita de Cássia Mendes de BarrosI; Mauro Celso RibeiroI; Paulo Teng An-SumodjoI; Murilo Sérgio da Silva Julião I,# * e-mail: shps@iq.usp.br ; Sílvia Helena Pires SerranoI,* # Endereço permanente: Centro de Ciências Exatas e Tecnologia, Universidade Estadual Vale do Acaraú, Av. da Universidade, 850, 62040-470 Sobral - CE. ; Neidenêi Gomes FerreiraII
IInstituto de Química, Universidade de São Paulo, Av. Prof. Lineu Prestes, 748, 05508-900 São Paulo - SP
IIDivisão de Materiais, Centro Técnico Aeroespacial, Praça Mal. Eduardo Gomes, 50, 12228-901 São José dos Campos - SP
ABSTRACT
This review presents a brief account concerning the production, characterization and evolution of the knowledge in the area of diamond and boron-doped diamond films. The most important methods used for the growth of these films, such as chemical vapor deposition and high pressure/high temperature systems, as well as the several kinds of reactors which can be employed are reviewed. However, larger emphasis is given to the CVD method. Morphological, structural and electric properties of these films, as well as their role in the performance of voltammetric electrodes for electrochemistry and electroanalytical chemistry are also discussed.
Keywords: CVD boron-doped diamond growth; diamond electrodes; electrochemistry.
INTRODUÇÃO
Um breve histórico
Os dois métodos básicos para a síntese de diamante são a deposição química a partir da fase vapor (do inglês "chemical vapor deposition", sigla CVD) e o crescimento a alta-pressão/alta-temperatura (do inglês "high-pressure/high-temperature", sigla HPHT), sendo este último o que mais se assemelha ao processo de formação do diamante natural. Ambos os métodos foram desenvolvidos quase ao mesmo tempo, na década de 50. O primeiro relato de produção de diamante pelo homem, por qualquer método, mas especificamente pelo método a baixas pressões (CVD), é creditado a William Eversole, da Union Carbide, em 19521. O processo HPHT foi desenvolvido pela General Electric a partir de 19551. Inicialmente os processos de deposição se restringiam ao crescimento unicamente de grãos, sobre grãos pré-existentes de diamante ou a partir de material à base de carbono que não o diamante1. Com o desenvolvimento e entendimento cada vez maior das técnicas de crescimento, passou-se então a produzir filmes de diamante, sobre os mais variados tipos de substratos2-4.
Há diferenças marcantes quanto aos parâmetros de crescimento utilizados em cada processo. O método HPHT necessita de temperaturas iguais ou maiores a 1 670 K e de pressões altíssimas, da ordem de 5 x 109 Pa, enquanto o método CVD trabalha a temperaturas da ordem de 1 270 K e pressões subatmosféricas, da ordem de 1 000 a 10 000 Pa1.
O empenho na proposição e estudo dos métodos para síntese de filmes de diamante deu-se, nos últimos anos, devido ao interesse no uso deste material nas mais variadas áreas, graças ao seu conjunto ímpar de propriedades, em comparação a outros materiais utilizados pela indústria em geral. Algumas destas propriedades, comparadas às de outros materiais, estão relacionadas na Tabela 1. A intenção foi propor e aprimorar métodos que pudessem ser principalmente econômicos e de grande versatilidade, o que resultou no grande desenvolvimento do processo CVD. As aplicações dos filmes de diamante foram então facilitadas pelo crescimento a baixas pressões (método CVD), em condições de produção em série. Atualmente, este método de crescimento de filmes de diamante é uma técnica muito difundida, por ser econômica, permitir o crescimento dos filmes em vários substratos de diferentes tamanhos e formatos, e utilizar reatores de construção e manuseio simplificados.
Assim, o diamante sintético passou a ter aplicações industriais de grande importância, em diversos setores, tais como: i) mecânico, devido à sua alta dureza, condutividade térmica e força de flexão; ii) eletrônico, opto-eletrônico, óptico e espacial, devido à sua alta condutividade térmica, baixa constante dielétrica, alta temperatura de operação, bom isolamento elétrico e boa transparência óptica; iii) médico, devido à inércia química e baixo coeficiente de fricção; iv) eletroquímico, devido ao seu caráter semicondutor quando dopado, alta resistência química, ampla janela de potencial de trabalho e baixa corrente de fundo1,8. Todas estas propriedades são em muitos casos inigualáveis, principalmente por se apresentarem em conjunto, num único material.
A Figura 1 apresenta as morfologias de crescimento, típicas de cada tipo de diamante considerado.
O diamante natural tem, em geral, grãos de formato octaédrico, enquanto o diamante CVD apresenta dois planos preferenciais de crescimento de grãos, um em formato cúbico e outro em formato octaédrico, como pode ser visto na Figura 1c. O diamante HPHT apresenta grãos com cantos não definidos. É importante notar que várias das propriedades do diamante, como condutividade térmica, resistência elétrica, não variam com a orientação dos grãos9.
Filmes de diamante CVD
O método CVD baseia-se na deposição de um filme de diamante sobre diferentes tipos de substratos, inclusive o próprio diamante, sob condições termodinamicamente metaestáveis, a partir da ativação de uma fase gasosa introduzida em um reator. Os reagentes gasosos utilizados são metano altamente diluído em hidrogênio. No entanto, podem ser empregadas outras substâncias orgânicas como fonte de carbono, ou juntamente com o metano, tais como metanol, acetona, etanol. Pequenas frações de oxigênio, ou ainda compostos halogenados, também podem ser usados com o objetivo de aumentar a taxa de crescimento e/ou aumentar a qualidade final dos filmes crescidos10-14. O processo também pode praticamente dispensar o emprego de hidrogênio, partindo apenas de uma fonte de carbono (por exemplo, metano, C60), diluída em grande quantidade de argônio15. Desta forma, obtém-se filmes nanocristalinos de diamante CVD.
De maneira geral, a ativação química dos gases acontece como indicado na Figura 2.
Os gases são injetados no reator, na etapa representada pela região 1. Em seguida, passam pela região de ativação, região 2, onde são formados, inicialmente, hidrogênio atômico e, logo em seguida, o radical metila, o qual é considerado o principal precursor do crescimento de diamante CVD (Zhou et al.15 consideram que um dímero de C2 se incorpore ao carbono superficial, sendo então a espécie precursora neste tipo de mecanismo). Outros radicais também são formados, mas têm participação secundária no processo. O hidrogênio atômico e o radical metila são, então, as principais espécies reativas envolvidas no crescimento de diamante. Por difusão, passando à região 3, o hidrogênio atômico e o radical metila chegam ao substrato, o qual é colocado a uma distância previamente definida da região de ativação. Desta forma, terá início o processo de nucleação, com posterior coalescência e crescimento dos grãos do filme de diamante policristalino, sobre o substrato empregado. Os grãos de diamante do filme começam a crescer a partir de uma camada intermediária de carbeto, originada pela reação entre o substrato e o radical metila, ou a partir de outros grãos de diamante previamente depositados sobre o substrato, antes do crescimento, pelo método da semeadura. Neste caso, igualmente haverá formação de uma camada intermediária de carbeto, antes do início do crescimento propriamente dito e este processo é chamado de incorporação. No entanto, se o substrato for o próprio diamante, poderá ocorrer o crescimento de um cristal único, e não de um filme.
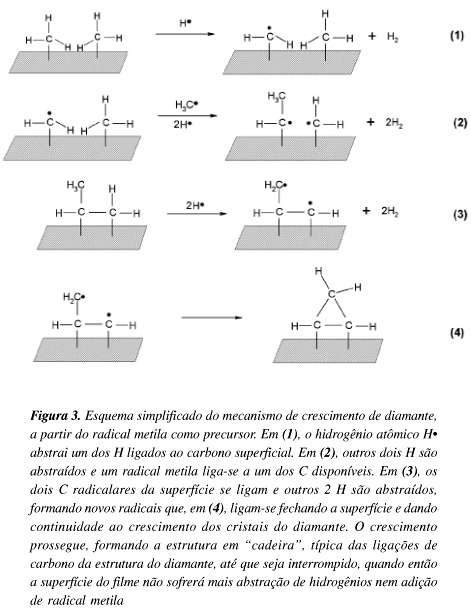
De forma esquemática, a Figura 3 apresenta o mecanismo proposto para o crescimento do filme de diamante, a partir do radical metila como precursor e com o hidrogênio atômico promovendo a abstração de outros átomos de hidrogênio ligados ao carbono da superfície, conforme a reação (1) abaixo16 (Cd = carbono da superfície do diamante):
Assim, a ativação dos gases é necessária para que se atinjam taxas de crescimento apreciáveis. O tipo de ativação da fase gasosa define a espécie de reator utilizado. Pode-se citar, por exemplo, os reatores com ativação por filamento quente de tungstênio (térmica), por plasma de microondas, por plasma de rádio-frequência, por chama de oxi-acetileno, dentre outros. Na Figura 4 são mostrados dois tipos de reatores, assistidos por filamento quente e por plasma de microondas.
Há variações na construção dos diferentes reatores, mas não no fundamento do processo de deposição. No reator assistido por filamento quente de tungstênio mostrado na Figura 4, os gases são injetados pela parte superior da câmara de reação, que está sob vácuo e possui sistema de refrigeração. O substrato é posicionado de modo que fique a uma distância adequada da região de ativação. Esta distância e as temperaturas do filamento e do substrato são previamente estabelecidas e controladas ao longo dos experimentos, de acordo com as necessidades. No reator assistido por plasma de microondas da Figura 4, os gases entram na câmara de quartzo pela parte inferior do sistema, o qual encontra-se sob vácuo e possui igualmente sistema de refrigeração. Um magnetron situado no topo do reator gera o plasma, o qual fica posicionado na região do substrato. O processo em ambos os reatores dar-se-á como mostrado na Figura 2. Obtém-se deste modo os filmes de diamante, a partir de diferentes condições e taxas variáveis de crescimento, mas com características morfológicas e qualidade parecidas, para os vários tipos de reatores.
A Tabela 2 apresenta diferentes parâmetros de crescimento, para cada tipo de reator citado.
Os fatores que determinam a escolha do reator são os custos envolvidos na sua aquisição ou a disponibilidade de material para sua montagem em laboratório. Por esta razão, se o objetivo é desenvolver pesquisa no campo de produção e caracterização dos filmes, o reator mais acessível é aquele assistido por filamento quente, justamente por empregar peças simples e ser de fácil montagem. Uma micrografia com morfologia típica de um filme de diamante CVD é mostrada na Figura 5, onde se nota a presença de grãos cúbicos ou octaédricos, característicos dos planos preferenciais de crescimento.
FILMES DE DIAMANTE CVD DOPADO COM BORO
Os filmes policristalinos crescidos pelo método CVD podem conter, em sua rede cristalina, uma certa quantidade de impurezas provenientes de gases não totalmente eliminados do reator pelo vácuo, ou dos materiais usados no reator (filamento, porta-substrato, tubo de quartzo), mas também podem ser formadas ligações sp2 entre os próprios átomos de carbono 16. A superfície do diamante é terminada em hidrogênio, ou seja, a superfície crescida tem uma camada terminal de átomos de hidrogênio, em estágios diferentes de estruturação superficial. A evolução desta estruturação superficial, para um dos planos de crescimento, está representada na Figura 6. Observa-se a passagem de uma estrutura com alta energia superficial, portanto menos estável (a), na forma de di-hidreto (2 átomos de hidrogênio ligados ao mesmo átomo de carbono, com alta energia estérica), à forma mais estável (c), a de mono-hidreto, com menor energia superficial, na qual apenas 1 átomo de hidrogênio está ligado a cada átomo de carbono, em toda a extensão da estrutura cristalina18.
O diamante natural é um material isolante (com exceção do tipo IIb, que contém boro em sua estrutura), com resistividade da ordem de 1016Wcm. Os filmes de diamante terminados em hidrogênio, como aqueles da Figura 6, ou o próprio diamante natural tratado em plasma de hidrogênio, têm sua resistividade reduzida para algo em torno de 106Wcm 5, mas do ponto de vista de obtenção de materiais semicondutores, este valor de resistividade ainda é muito alto.
Com a intenção de se crescer filmes com características semicondutoras, e sabendo de antemão que o diamante natural tipo IIb é um semicondutor tipo p que contém boro, Poferl et al.19, em 1973, foram os primeiros a crescer diamante dopado com boro a baixas pressões, a partir da mistura B2H6/CH4, usando grãos de diamante natural como substrato. Apesar do grande passo dado para obtenção de diamante dopado, as taxas de crescimento foram ainda muito baixas, da ordem de 4 x 10-5 µmh-1, em comparação com o que se consegue atualmente, da ordem de 100 µmh-1.
Aproximadamente uma década depois, vislumbrou-se a possibilidade de aplicação do diamante dopado, principalmente com boro, no campo dos semicondutores e, em 1986, Fujimori et al.20 cresceram filme policristalino dopado com boro sobre substrato de silício, pelo processo CVD e, como já haviam feito Poferl et al.19, também obtiveram cristais únicos crescidos sobre diamante, usando reator assistido por plasma de microondas. As grandes contribuições dadas por estes autores foram o aumento na taxa de crescimento para 2,5 x 10-4 µmh-1, além da determinação da resistividade elétrica como função da concentração de boro usado como dopante. Como os valores de resistividade foram menores que 0,01 Wcm, os autores sugeriram que o boro age como um dopante mais efetivo quando incorporado durante a deposição da fase gasosa, no processo CVD, do que quando inserido no filme já crescido pelo processo de implantação iônica, ou mesmo durante a deposição a alta pressão (HPHT).
No Brasil, esta área de pesquisa começou a ser divulgada e difundida por meio do trabalho pioneiro de Ferreira et al.21, do Grupo de Diamantes e Materiais Relacionados, do Instituto Nacional de Pesquisas Espaciais (INPE), em São José dos Campos/SP. Os autores cresceram filmes de diamante dopado com boro sobre silício, em reator assistido por filamento quente. Os filmes e eletrodos foram caracterizados quanto à morfologia, nível de dopagem e qualidade do diamante, usando técnicas como microscopia eletrônica de varredura e espectroscopia Raman; quanto às propriedades elétricas, através de gráficos Mott-Schottky e análises fotoeletroquímicas, que ajudam no entendimento do processo elétrico na interface semicondutor/eletrólito e quanto ao comportamento voltamétrico, na tentativa de correlacionar as propriedades anteriores ao comportamento eletroquímico dos eletrodos. A experiência e criatividade deste grupo de pesquisa têm possibilitado interações profícuas com pesquisadores das áreas de eletroquímica e eletroanalítica. Neste sentido, os trabalhos em colaboração recentemente desenvolvidos22,23, demonstram um caminho aberto para a utilização de eletrodos de filme de diamante em áreas tradicionais e interdisciplinares da ciência, com conseqüente formação de recursos humanos e avanço tecnológico.
Eletrodos de diamante CVD dopado com boro
O estabelecimento do método de dopagem de filmes de diamante CVD descortinou uma ampla faixa de possibilidades de aplicação destes filmes semicondutores, em diferentes áreas da ciência24-30. Uma das aplicações que mais despertou interesse a partir dos anos 90, foi a fabricação de eletrodos para uso em aplicações eletroquímicas.
Diferentes parâmetros devem ser considerados no desenvolvimento de eletrodos e estes envolvem a escolha da mistura gasosa, substrato, método de crescimento, estabelecimento do contato elétrico e montagem final do eletrodo. Para o crescimento de filmes de diamante dopado ou não com boro, vários substratos podem ser utilizados, mas deve-se levar em conta a semelhança entre o parâmetro de rede e/ou o coeficiente de dilatação térmica dos dois materiais, para facilitar o crescimento de um filme aderente e de qualidade. O substrato também deve ser resistente à temperatura de operação do reator. É importante também considerar o tipo de aplicação futura dos filmes ou a disponibilidade de materiais. Alguns dos substratos mais usados são silício21,29,31-44, tungstênio32,35,45-50, molibdênio49,51-55, titânio35,56,57, grafite27,35,58,59, carbono vítreo3,27, liga Ti6Al4V60, irídio61, nióbio62. Diferentes formatos e tamanhos são empregados e dentre os mais comuns e de menor tamanho estão os materiais planos27,34,37,52,60, fios48,50, tecidos4,63, ou mesmo substratos esféricos23. Substratos com área grande podem também ser usados, em geral no formato plano64.
Quanto ao dopante, diferentes compostos podem ser usados e injetados no reator simultaneamente com hidrogênio e metano (exceto no caso do emprego de disco sólido, o qual é posicionado dentro do reator, em geral abaixo do substrato, antes de se iniciar o processo). Os dopantes mais empregados são o boro e seus derivados, cada qual com características próprias, tais como B2H6, que não contém carbono ou oxigênio na molécula, o que evita a inclusão de elementos extras no reator, é facilmente encontrado e possibilita controle de concentração de boro, mas é altamente tóxico, explosivo e reativo20,25,65; trimetilborato, que não é tóxico, mas deve ser diluído em acetona ou metanol para ser usado, o que implica em fonte adicional de carbono e oxigênio66-68; B2O3, o mais comum deles, que tem grande disponibilidade, mas também deve ser solubilizado em acetona ou metanol21-23,40,46,63,69,70, ou pode ser usado como disco sólido71. Outros elementos usados como dopante são enxofre66,72-75, nitrogênio76-78, fósforo74,75,79, lítio63,80.
Outro método também utilizado para dopagem de filmes de diamante é a implantação iônica com diferentes dopantes, após a etapa de crescimento20,73,81-83. No entanto, a eficiência de dopagem deste processo é menor, em função da maior quantidade de impurezas e danos estruturais inseridos nos filmes.
Após o crescimento dos filmes de diamante dopado, um dos parâmetros mais importantes na montagem de eletrodos é o estabelecimento do contato elétrico, normalmente ôhmico (contato entre um metal e um semicondutor), o qual deve apresentar resistência mínima84. Alguns dos contatos mais usados são os de índio/gálio29,84, gálio85, subcamada de titânio84,86, pasta de prata21-23,30,63,84, ouro ou Au/Ta87,88, metalização em camadas84,88-90.
Igualmente importante é o isolamento de todas as partes do eletrodo que não devem entrar em contato com a solução de medida. O filme deve ter sua borda totalmente vedada, em geral com borracha de silicone, ou deve ser embutido em um material inerte adequado, para que somente a superfície do diamante dopado fique exposta à solução, de modo que ela não se infiltre por eventuais orifícios e alcance o material usado como suporte22,23. Uma das dificuldades enfrentadas nesta etapa é conseguir um isolamento perfeito do filme pelo maior período possível, pois muitas vezes a solução utilizada pode promover o descolamento do material usado para a vedação.
CARACTERIZAÇÃO MORFOLÓGICA, ESTRUTURAL E ELÉTRICA DE FILMES E ELETRODOS DE DIAMANTE CVD
O diamante dopado tem uma resistividade semelhante ao carbono vítreo, mas um pouco maior que outros materiais de carbono usados na fabricação de eletrodos, Tabela 3. No entanto, as aplicações dos filmes de diamante em eletroanálise estão muito relacionadas às várias propriedades físicas que os mesmos exibem. Algumas dessas aplicações já podem ser empregadas por exemplo, pela exigente indústria de dispositivos eletrônicos. Até pouco tempo atrás o principal empecilho para o uso do diamante em larga escala era o fator econômico, pois o processo de crescimento dos filmes era muito caro quando comparado a outros materiais alternativos. Entretanto, a utilização de reatores de alta potência tornou-se mais comum e, pela primeira vez, no ano de 2000, foi possível produzir um pequeno pedaço de diamante, cerca de 0,2 g, por menos de US$ 1,091. Isto viabilizou economicamente o uso de diamante e permitiu que os pesquisadores explorassem seu amplo conjunto de propriedades para uma grande variedade de aplicações92-95.
Algumas empresas fabricam eletrodos de diamante, por diversos métodos e empregando diferentes condições e substratos para obtenção dos filmes, Tabela 4.
É importante ressaltar que as informações sobre os parâmetros de crescimento, ou as análises morfológicas, não se encontram disponíveis para possíveis compradores e que muitas vezes resultados experimentais, obtidos em um certo laboratório, não são reproduzidos em outro, principalmente devido a eventuais diferenças nos parâmetros experimentais utilizados durante o processo de crescimento dos filmes. Uma vez que estes dados e, em geral, também os dados de caracterização, são mantidos como segredos industriais pelas empresas, a utilização de eletrodos comerciais acaba por impedir o estabelecimento de correlação entre os resultados experimentais obtidos e os parâmetros de crescimento empregados.
Muitas técnicas podem ser usadas para a caracterização morfológica e estrutural dos filmes de diamante dopado, individualmente ou em conjunto com outras. Cada técnica contempla um tipo específico de análise98 e as mais comuns são:
-
Microscopia Eletrônica de Varredura ("scanning electron microscopy", SEM), utilizada para investigar topografia e morfologia superficiais;
-
Microscopia Eletrônica de Transmissão ("transmission electron microscopy", TEM), possui maior resolução que a técnica SEM e é usada para análises de morfologia e estrutura dos filmes, detectando defeitos da rede;
-
Microscopia de Força Atômica ("atomic force microscopy", AFM), usada para avaliar morfologia superficial;
-
Microscopia de Varredura por Tunelamento ("scanning tunneling microscopy", STM), produz imagens de alta resolução da morfologia superficial dos filmes, em escala atômica, sendo também usada para estudar propriedades eletrônicas locais;
-
Espectroscopia Eletrônica Auger ("Auger electron spectroscopy", AES), utilizada na determinação da composição química superficial e interfacial, e na análise de traços de elementos;
-
Espectroscopia Raman, investiga a microestrutura dos filmes, identificando a presença de ligações sp2 em seu interior, fornecendo dados para estudo de estresse intrínseco, causado pela incorporação do agente dopante na rede cristalina do diamante;
-
Difração de Raio-X ("X-ray diffraction", XRD), usada para investigar a orientação cristalina, composição e estrutura dos filmes;
-
Espectroscopia de Fotoelétrons Excitados por Raio-X ("X-ray photoelectron spectroscopy", XPS), permite a determinação da composição e estrutura dos filmes na região próxima à superfície;
-
Espectrometria de Massa de Íon Secundário ("Secondary ion mass spectrometry", SIMS), permite a determinação quantitativa do agente dopante e sua distribuição espacial na região próxima à superfície dos filmes.
Outros métodos também são empregados nas caracterizações, mas com menor frequência, como: i) Difração de Elétrons Refletidos de Alta Energia ("Reflection high energy electron diffraction", RHEED; ou "Reflection electron diffraction", RED), usada para determinação de parâmetros de rede; ii) Espectroscopia de Perda Eletrônica de Baixa Energia ("Low-energy electron loss spectroscopy", LEELS), utilizada para avaliação da composição de ligações de carbono nos filmes; iii) Análise por Reação Nuclear ("Nuclear reaction analysis", NRA), permite a detecção e medida de elementos de baixo número atômico (como boro ou flúor) nos filmes, ou em amostras isotopicamente marcadas, como óxidos; iv) Análise de Detecção da Retração Elástica ("Elastic recoil detection analysis", ERDA), permite a medida da incorporação de átomos de agente dopante (baixo número atômico, como boro) nos filmes e tem maior eficiência que o método dos gráficos Mott-Schottky, porque detecta boro total e não apenas os transportadores de carga.
Dentre os trabalhos que utilizaram estas técnicas na caracterização de filmes e eletrodos, podem ser citados aqueles que empregaram SEM7,21,29,33-35,40,43,45,47-49,53,54,57-59,64,99-110 , AFM31,48,49,58,99,102,103,111, TEM103,110, SAM31, espectroscopia Raman7,21,31,33,35,38,40,43,45,47,48,50,57,58,64,99 -106,110-113, XPS29,36,43,45,69,102,113, XRD40,48,57,99-101,103,104,114, SIMS29,33,35,48,64, NRA103,104, RHEED20, LEELS20 e ERDA114. A caracterização das propriedades morfológicas, estruturais e composição dos filmes de diamante ocorreu concomitantemente com as aplicações iniciais, quase que exclusivamente dedicadas à determinação de propriedades elétricas e/ou fotoeletroquímicas20,24,71,115,116 , mas sem a intenção de utilização de filmes para construção de eletrodos destinados à aplicação em eletroquímica. Fujimori et al.20 foram os primeiros autores a efetuar uma caracterização detalhada de filmes de diamante semicondutor, dopado com boro por processo CVD, utilizando diborano como fonte de boro. Contribuíram com dados de análises de SEM, TEM, SIMS, RHEED e LEELS, estabelecendo a existência de correlação entre a resistividade elétrica dos filmes e a razão B/C no gás reagente. Por SIMS determinaram a concentração de boro nos filmes, como sendo da ordem de 1020 cm-3. Coube a Pleskov et al.24 estudarem, pela primeira vez, o comportamento fotoeletroquímico de um filme de diamante semicondutor usado como eletrodo, na presença de solução aquosa de eletrólito. Os autores demonstraram que as propriedades semicondutoras do diamante influenciavam o comportamento fotoeletroquímico de eletrodos e que, de modo similar, as características superficiais, impostas por pré-tratamento eletroquímico ou composição da solução (por exemplo, pH) influenciavam o comportamento eletroquímico dos mesmos. Posteriormente, Mort et al.25 comprovaram, empregando análises SIMS e Raman, que o aumento de condutividade dos filmes era resultado da dopagem com átomos de boro, e não da presença de qualquer fase grafítica no filme.
A partir de então, os trabalhos se intensificaram no sentido de avaliar as características gerais de filmes ou eletrodos de diamante dopado. Análises SEM, RHEED e Raman foram utilizadas por Okano et al.115 para analisar a estrutura dos filmes e demonstrar a existência de relação linear entre a resistividade e a razão B/C, enquanto a análise SIMS foi utilizada para determinar o teor de boro. A influência da concentração de boro no gás reagente está diretamente relacionada à cristalinidade dos filmes e foi estudada por Fujimori et al.116 usando as técnicas SIMS e RED. Os estudos prosseguiram, passando por Ramesham et al.71, Patel et al.117 até que, em 1993, Swain e Ramesham26 realizaram o primeiro trabalho sobre avaliação do comportamento eletroquímico de eletrodos de diamante dopado com boro, com emprego de voltametria cíclica e diferentes meios aquosos.
A espectroscopia Raman foi utilizada por Zhang et al.110 para demonstrar que o pico típico da estrutura do diamante diminui de intensidade e desloca-se para energias menores, à medida que a resistividade do filme diminui. Apesar disto estruturas cristalinas, com constantes de rede similares àquelas do diamante natural, foram identificadas usando a técnica TEM. Carbeto de boro não foi detectado nos filmes, nem outras fases de carbono, porém análises por SEM detectaram a presença de defeitos em toda a extensão dos filmes. Espectroscopia Raman e XRD foram utilizadas por Ferreira et al.101 para estudar o estresse residual e a qualidade cristalina de filmes de diamante dopado com boro e os resultados demonstraram que esta diminuiu de 99 a 75% com o aumento do nível de dopagem. Espectroscopia XPS foi utilizada por Chen et al.102 para a detecção de mudanças na composição superficial dos filmes, a qual foi caracterizada como um processo de oxigenação, responsável pelo aumento do sobrepotencial de reações eletródicas devido à diminuição da condutividade superficial com perda simultânea de sítios redox cineticamente ativos. Esta mesma técnica foi utilizada por Granger e Swain69 para demonstrar que eletrodos de filmes de diamante dopado com boro e submetidos à polarização anódica apresentam um aumento de 10 vezes na razão atômica superficial O/C, o que diminui a cinética de transferência de carga do par [Fe(CN)6]3-/[Fe(CN)6 ]4- , caracterizada por um aumento no valor de DEp para o par reversível. A espectroscopia XPS foi ainda utilizada por Goeting et al.45,58 para demonstrar que a superfície dos eletrodos de diamante é significativamente modificada por tratamentos eletroquímicos. Os autores verificaram por AFM e SEM que é possível nuclear e depositar, não homogeneamente, chumbo metálico sobre o filme de diamante e demonstraram que o depósito ocorre em áreas superficiais ativas, independente dos contornos de grão. A microscopia AFM foi utilizada por Granger e Swain69 para determinar a rugosidade superficial, que parece ser independente do tempo de crescimento. Esta técnica foi também utilizada por Silva et al.99 para estudar a dimensão fractal de filmes de diamante dopado. A difração de raios-X (XRD) de luz síncroton e a análise ERDA114 foram importantes para que estes autores identificassem a incorporação e o aumento do conteúdo de carbeto de tungstênio, proveniente do filamento do reator, em filmes de diamante dopado com boro, em função do aumento do conteúdo de óxido de boro no gás. A análise por XPS, detectou apenas um sinal fraco de carbeto de boro, enquanto a análise ERDA detectou a presença de oxigênio nos filmes. É, portanto, importante, que se faça uma avaliação da influência de contaminações como a de carbeto de boro nas características eletroquímicas dos eletrodos.
O trabalho de Pleskov et al.24 descrevendo o comportamento fotoeletroquímico de filmes de diamante acabou por mostrar que os filmes de diamante não são tão eletroquimicamente inertes assim quanto se pensava, e que as propriedades superficiais podem ser sensivelmente alteradas via pré-tratamento superficial. A partir deste trabalho muito esforço tem sido direcionado para a caracterização do comportamento eletroquímico118,119, em função de alterações impostas à sua superfície, via recozimento em vácuo26,52,120, plasmas de H252,69,121,122, O236,122-125, ou via tratamentos anódicos e catódicos26,52,69,107,122-127. O tratamento de filmes de diamante através da intercalação de lítio63,111,128, bombardeamento com íons de argônio129 e plasmas de halogêneos107,130 tem sido igualmente descrito. Trabalhos de caráter mais fundamental, visando elucidar alguns fenômenos relacionados à alteração superficial do eletrodo tais como condutividade superficial e intervalo de estabilidade em solvente52,130-136, além do mecanismo de geração eletroquímica de gases (H2, O3, Cl2)40,137-140, têm igualmente sido descritos.
Desde que os eletrodos de filmes de diamantes apresentam propriedades importantes tais como ampla janela de potencial de trabalho141 e baixa corrente de fundo, é evidente que a possibilidade de construir Eletrodos de Filmes de Diamante Quimicamente Modificados (EFDQM) é um aspecto bastante atrativo, principalmente do ponto de vista da Química Eletroanalítica. Para tanto, o conhecimento das conseqüências do pré-tratamento eletroquímico superficial de eletrodos de filme de diamante, dopado ou não, sobre as eventuais aplicações eletroquímicas dos mesmos é um ponto fundamental. Sob esse aspecto, o trabalho de Yagi et al.142 foi extremamente importante, principalmente por demonstrar que se pode oxidar a superfície de filmes de diamante por meio de pré-tratamento anódico ou por plasma de oxigênio, porém a superfície só é eletroquimicamente recuperada, quando a oxidação superficial também foi obtida via eletroquímica. Os resultados experimentais foram interpretados admitindo-se que o tratamento por plasma de oxigênio além de retirar a camada sub-superficial condutiva de hidrogênio26,52,125,143, altera a estrutura local do filme, dificultando a inserção de hidrogênio na camada sub-superficial. Por outro lado, o tratamento anódico, apesar de também oxidar a superfície, não exerceria efeito tão intenso na camada sub-superficial do diamante. Atenção deve ser dada ao fato de que oxidações anódicas e tratamentos por plasma de oxigênio aumentam a relação O/C na superfície do filme36,123, tornando mais lenta a cinética de transferência de carga de alguns pares redox, como por exemplo [Fe(CN)6]3-/4- e [IrCl6]2-/3-69,107,122. A reversibilidade da reação de transferência de carga para estas espécies aumenta com o abaixamento do pH, indicativo de que grupos carboxila, negativamente carregados podem estar presentes na superfície do filme, diminuindo a reversibilidade da reação de transferência eletrônica por exclusão de carga69.
A possibilidade de introduzir espécies oxigenadas, ou ainda outras espécies, na superfície dos filmes de diamante, seja de modo temporário ou definitivo, que possam implementar alguma seletividade às reações de transferência de carga, ou ainda servir como âncora para imobilização superficial de espécies biológicas é uma possibilidade que deve ser explorada, visando o desenvolvimento de novos EFDQM e Biossensores.
CONSIDERAÇÕES FINAIS
O método CVD de crescimento de filmes de diamante, bem como as diferentes técnicas utilizadas na caracterização estrutural, morfológica, química e elétrica de novos materiais são ferramentas poderosas para o desenvolvimento e a aplicação de eletrodos, dopados ou não, por permitirem estabelecer correlações entre as propriedades eletroquímicas dos mesmos e os parâmetros de crescimento, ou ainda, mudanças superficiais causadas por diversos tipos de pré-tratamentos, sejam estes eletroquímicos ou não. Será através destas correlações que, nos próximos anos, poderemos medir o impacto da aplicação deste tipo de material nos mais variados ramos da ciência. Sob este aspecto, a existência de um grupo de pesquisa no Brasil, nesta área, interagindo com pesquisadores dos mais diversos campos da ciência, é de fundamental importância para o avanço nas áreas tecnológicas de desenvolvimento e aplicação destes filmes.
Diversos artigos de revisão abordando o assunto foram publicados em língua inglesa93,144-150, de modo que esta revisão não tem a pretensão de esgotar o assunto, mas apenas fornecer uma abordagem didática, que sirva de estímulo para que outros profissionais se interessem pelo tema. As aplicações de eletrodos de filmes de diamante no campo da Eletroquímica e Eletroanalítica serão revisadas na Parte II deste trabalho, a ser submetida futuramente a este mesmo periódico.
AGRADECIMENTOS
Os autores agradecem o suporte financeiro do CNPq e da FAPESP, e ao Dr. V. J. Trava-Airoldi, do LAS/INPE São José dos Campos, por disponibilizar o laboratório para crescimento dos filmes.
6. Davidson, J. L. Em ref. 1, p. 356.
7. Ravi, K. V. Em ref. 1, pp. 538 e 553.
9. van Enckevort, W. J. P. Em ref. 1, p. 311.
17. Moustakas, T. D. Em ref. 1, cap. 6.
18. Spear, K. E.; Frenklach, M. Em ref. 1, p. 252.
Recebido em 14/6/04; publicado na web em 12/11/04
- 1. Angus, J. C. Em Synthetic diamond: emerging CVD science and technology; Spear, K. E.; Dismukes, J. P., eds.; John Wiley & Sons: New York, 1994, cap.2.
- 2. Celii, F. G.; Butler, J. E.; Annu. Rev. Phys. Chem. 1991, 42, 643.
- 3. DeClements, R.; Hirsche, B. L.; Granger, M. C.; Xu, J.; Swain, G. M.; J. Electrochem. Soc. 1996, 143, L150.
- 4. Ferreira, N. G.; Silva, L. L. G.; Corat, E. J.; Diamond Relat. Mater. 2002, 11, 657.
-
5chemfinder.cambridgesoft.com/result.asp, acessada em Julho 2004.
- 8. Swain, G. M.; J. Electrochem. Soc. 1994, 141, 3382.
- 10. Bachmann, P. K.; Hagemann, H.-J.; Lade, H.; Leers, D.; Picht, F.; Wiechert, D. U.; Wilson, H.; Mater. Res. Soc. Symp. Proc. 1994, 339, 267.
- 11. Ferreira, N. G.; Corat, E. J.; Trava-Airoldi, V. J.; Leite, N. F.; Del Bosco, E.; Diamond Relat. Mater. 1998, 7, 81.
- 12. Mendes de Barros, R. C.; Corat, E. J.; Trava-Airoldi, V. J.; Ferreira, N. G.; Lemos, V.; Leite, N. F.; Iha, K.; Braz. J. Phys. 1997, 27/A, 142.
- 13. Corat, E. J.; Ferreira, N. G.; Trava-Airoldi, V. J.; Leite, N. F.; Lemos, V.; Mendes de Barros, R. C.; Iha, K.; Diamond Relat. Mater. 1997, 6, 1172.
- 14. Mendes de Barros, R. C.; Corat, E. J.; Ferreira, N. G.; Trava-Airoldi, V. J.; Leite, N. F.; Iha, K.; Diamond Relat. Mater. 1997, 6, 490.
- 15. Zhou, D.; Gruen, D. M.; Qin, L. C.; McCauley, T. C.; Krauss, A. R.; J. Appl. Phys. 1998, 84, 1981.
- 16. Goodwin, D. G.; Butler, J. E. Em Handbook of industrial diamond and diamond films; Prelas, M.; Popovici, G.; Bigelow, L. K.; eds.; Marcel Dekker Inc.: New York, 1997.
- 19. Poferl, D. J.; Gardner, N. C.; Angus, J. C.; J. Appl. Phys. 1973, 44, 1428.
- 20. Fujimori, N.; Imai, T.; Doi, A.; Vacuum 1986, 36, 99.
- 21. Ferreira, N. G.; Silva, L. L. G.; Corat, E. J.; Trava-Airoldi, V. J.; Iha, K.; Braz. J. Phys. 1999, 29, 760.
- 22. Julião, M. S. S.; Almeida, E. C.; La Scalea, M. A.; Ferreira, N. G.; Compton, R. G.; Serrano, S. H. P.; Electroanalysis, no prelo.
- 23. Mendes de Barros, R. C.; Azevedo, A. F.; Corat, E. J.; Ferreira, N. G.; Sumodjo, P. T. A.; Serrano, S. H. P.; submetido ao 207th Meeting of the Electrochemical Society, May 15-20, Canadá, a ser publicado nos anais do congresso, 2005.
- 24. Pleskov, Y. V.; Sakharova, A. Y.; Krotova, M. D.; Bouilov, L. L.; Spitsyn, B. V.; J. Electroanal. Chem. 1987, 228, 19.
- 25. Mort, J.; Kuhman, D.; Machonkin, M.; Morgan, M.; Jansen, F.; Okumura, K.; LeGrice, Y. M.; Nemanich, R. J.; Appl. Phys. Lett. 1989, 55, 1121.
- 26. Swain, G. M.; Ramesham, R.; Anal. Chem. 1993, 65, 345.
- 27. Ramesham, R.; Askew, R. F.; Rose, M. F.; Loo, B. H.; J. Electrochem. Soc. 1993, 140, 3018.
- 28. Swain, G.M.; Adv. Mater. 1994, 6, 388.
- 29. Reuben, C.; Galun, E.; Cohen, H.; Tenne, R.; Kalish, R.; Muraki, Y.; Hashimoto, K.; Fujishima, A.; Butler, J. M.; Lévy-Clément, C.; J. Electroanal. Chem. 1995, 396, 233.
- 30. Zhu, J. Z.; Yang, S. Z.; Zhu, P. L.; Zhang, X. K.; Zhang, G. X.; Xu, C. F.; Fan, H. Z.; Fresenius J. Anal. Chem. 1995, 352, 389.
- 31. Li, L. F.; Totir, D. A.; Vinokur, N.; Miller, B.; Chottiner, G.; Evans, E. A.; Angus, J. C.; Scherson, D. A.; J. Electrochem. Soc. 1998, 145, L85.
- 32. Bouamrane, F.; Tadjeddine, A.; Tenne, R.; Butler, J. E.; Kalish, R.; Levy-Clement, C.; J. Phys. Chem. B 1998, 102, 134.
- 33. Vinokur, N.; Miller, B.; Avyigal, Y.; Kalish, R.; J. Electrochem. Soc. 1996, 143, L238.
- 34. Awada, H.; Strojek, J. W.; Swain, G. M.; J. Electrochem. Soc. 1995, 142, L42.
- 35. Fryda, M.; Herrmann, D.; Schäfer, L.; Klages, C. P.; Perret, A.; Hänni, W.; Comninellis, C.; Gandini, D.; New Diamond Front. Carbon Technol. 1999, 9, 229.
- 36. Yagi, I.; Notsu, H.; Kondo, T.; Tryk, D. A.; Fujishima, A.; J. Electroanal. Chem. 1999, 473, 173.
- 37. Ferro, S.; De Battisti, A.; Phys. Chem. Chem. Phys. 2002, 4, 1915.
- 38. Shin, D. C.; Sarada, B. V.; Tryk, D. A.; Fujishima, A.; Anal. Chem. 2003, 75, 530.
- 39. Martin, H. B.; Morrison, P. W.; Electrochem. Solid State Lett. 2001, 4, E17.
- 40. Katsuki, N.; Takahashi, E.; Toyoda, M.; Kurosu, T.; Iida, M.; Wakita, S.; Nishiki, Y.; Shimamune, T.; J. Electrochem. Soc. 1998, 145, 2358.
- 41. Katsuki, N.; Wakita, S.; Nishiki, Y.; Shimamune, T.; Akiba, Y.; Iida, M.; Jpn. J. Appl. Phys., Part 2 1997, 36, L260.
- 42. Alehashem, S.; Chambers, F.; Strojek, J. W.; Swain, G. M.; Ramesham, R.; Anal. Chem. 1995, 67, 2812.
- 43. Terashima, C.; Rao, T. N.; Sarada, B. V.; Spataru, N.; Fujishima, A.; J. Electroanal. Chem. 2003, 544, 65.
- 44. Troupe, C. E.; Drummond, I. C.; Graham, C.; Grice, J.; John, P.; Wilson, J. I. B.; Jubber, M. G.; Morrison, N. A.; Diamond Relat. Mater. 1998, 7, 575.
- 45. Goeting, C. H.; Marken, F.; Gutierrez-Sosa, A.; Compton, R. G.; Foord, J. S.; New Diamond Front. Carbon Technol. 1999, 9, 207.
- 46. Sarada, B. V.; Rao, T. N.; Tryk, D. A.; Fujishima, A.; J. Electrochem. Soc. 1999, 146, 1469.
- 47. Glesener, J. W.; Natishan, P. M.; O'Grady, W. E.; Aiken, J.; Morrish, A. A.; Mater. Lett. 1998, 37, 138.
- 48. Martin, H. B.; Argoitia, A.; Landau, U.; Anderson, A. B.; Angus, J. C.; J. Electrochem. Soc. 1996, 143, L133.
- 49. Zak, J. K.; Butler, J. E.; Swain, G. M.; Anal. Chem. 2001, 73, 908.
- 50. Cooper, J. B.; Pang, S.; Albin, S.; Zheng, J. L.; Johnson, R. M.; Anal. Chem. 1998, 70, 464.
- 51. Ramesham, R.; Sens. Mater. 1998, 10, 461.
- 52. Ramesham, R.; Thin Solid Films 1998, 315, 222.
- 53. Ramesham, R.; Sens. Actuators, B 1998, 50, 131.
- 54. Ramesham, R.; Sens. Mater. 1998, 10, 275.
- 55. Ramesham, R.; Rose, M. F.; Thin Solid Films 1997, 300, 144.
- 56. Beck, F.; Krohn, H.; Kaiser, W.; Fryda, M.; Klages, C. P.; Schäfer, L.; Electrochim. Acta 1998, 44, 525.
- 57. Fisher, V.; Gandini, D.; Laufer, S.; Blank, E.; Comninellis, C.; Electrochim. Acta 1998, 44, 521.
- 58. Goeting, C. H.; Jones, F.; Foord, J. S.; Eklund, J. C.; Marken, F.; Compton, R. G.; Chalker, P. R.; Johnston, C.; J. Electroanal. Chem. 1998, 442, 207.
- 59. Ramesham, R.; Thin Solid Films 1999, 339, 82.
- 60. Diniz, A. V.; Ferreira, N. G.; Corat, E. J.; Trava-Airoldi, V. J.; Diamond Relat. Mater. 2003, 12, 577.
- 61. Kusakabe, K.; Sobana, A.; Sotowa, K.; Imato, T.; Tsubota, T.; Diamond Relat. Mater. 2003, 12, 1396.
- 62. Becker, D.; Juttner, K.; J. Appl. Electrochem. 2003, 33, 959.
- 63. Ferreira, N. G.; Mendonça, L. L.; Trava-Airoldi, V. J.; Rosolen, J. M.; Diamond Relat. Mater. 2003, 12, 596.
- 64. Tröster, I.; Fryda, M.; Herrmann, D.; Schäfer, L.; Hänni, W.; Perret, A.; Blaschke, M.; Kraft, A.; Stadelmann, M.; Diamond Relat. Mater. 2002, 11, 640.
- 65. Bouamrane, F.; Tadjeddine, A.; Butler, J. E.; Tenne, R.; Lévy-Clément, C.; J. Electroanal. Chem. 1996, 405, 95.
- 66. Kusakabe, K.; Sobana, A.; Taniguchi, H.; Sotowa, K. I.; Tsubota, T.; J. Chem. Eng. Jpn. 2002, 35, 996.
- 67. Pleskov, Y. V.; Evstefeeva, Y. E.; Krotova, M. D.; Elkin, V. V.; Mazin, V. M.; Mishuk, V. Y.; Varnin, V. P.; Teremetskaya, I. G.; J. Electroanal. Chem. 1998, 455, 139.
- 68. Chen, S.-H.; Chen, S.-L.; Tsai, M.-H.; Shyn, J. J.; Chen, C.-F.; J. Electrochem. Soc. 1995, 142, L223.
- 69. Granger, M. C.; Swain, G. M.; J. Electrochem. Soc. 1999, 146, 4551.
- 70. Ramesham, R.; Rose, M. F.; J. Mater. Sci. Lett. 1997, 16, 799.
- 71. Ramesham, R.; Roppel, T.; Ellis, C.; Loo, B. H.; J. Electrochem. Soc. 1991, 138, 2981.
- 72. Rong-Bin, L.; Xiao-Jun, H.; He-Sheng, S.; Xian-Chang, H.; J. Mater. Sci. 2004, 39, 1135.
- 73. Kalish, R.; Uzan-Saguy, C.; New Diamond Front. Carbon Technol. 2004, 14, 109.
- 74. Gheeraert, E.; Casanova, N.; Tajani, A.; Deneuville, A.; Bustarret, E.; Garrido, J. A.; Nebel, C. E.; Stutzmann, M.; Diamond Relat. Mater. 2002, 11, 289.
- 75. Wang, L. G.; Zunger, A.; Phys. Rev. B: Condens. Matter Mater. Phys. 2002, 66, Art. No. 161202.
- 76. Ristein, J.; Riedel, M.; Stammler, M.; Mantel, B. F.; Ley, L.; Diamond Relat. Mater. 2002, 11, 359.
- 77. Musale, D. V.; Sainkar, S. R.; Kshirsagar, S. T.; Diamond Relat. Mater. 2002, 11, 75.
- 78. Perng, K.; Liu, K. S.; Lin, I. N.; Diamond Relat. Mater. 2000, 9, 358.
- 79. Teraji, T.; Katagiri, M.; Koizumi, S.; Ito, T.; Kanda, H.; Jpn. J. Appl. Phys., Part 2 2003, 42, L882.
- 80. Sternschulte, H.; Schreck, M.; Stritzker, B.; Bergmaier, A.; Dollinger, G.; Phys. Stat. Sol. A-Appl. Res. 1999, 174, 65.
- 81. Kalish, R.; Uzan-Saguy, C.; Walker, R.; Prawer, S.; J. Appl. Phys. 2003, 94, 3923.
- 82. Prins, J. F.; Semicond. Sci. Technol. 2003, 18, S27.
- 83. Prins, J. F.; Mater. Sci. Rep. 1992, 7, 271.
- 84. Latto, M. N.; PhD Thesis, chapter 2, p. 39, University of Bristol, 2001. Obtida em www.chm.bris.ac.uh/pt/diamond/mattthesis/title.htm, acessada em Novembro 2003.
- 85. Teraji, T.; Koizumi, S.; Kanda, H.; Appl. Phys. Lett. 2000, 76, 1303.
- 86. Alexander, M. S.; Latto, M. N.; May, P. W.; Riley, D. J.; Pastor-Moreno, G.; Diamond Relat. Mater. 2003, 12, 1460.
- 87. Zhen, C. M.; Wang, Y. Y.; He, S. H.; Guo, Q. F.; Yan, Z. J.; Pu, Y. J.; Opt. Mater. 2003, 23, 117.
- 88. Zhen, C. M.; Wang, Y. Y.; Guo, Q. F.; Zhao, M.; He, Z. W.; Guo, Y. P.; Diamond Relat. Mater. 2002, 11, 1709.
- 89. Werner, M.; Dorsch, O.; Baerwind, H. U.; Obermeier, E.; Johnston, C.; Chalker, P. R.; Romani, S.; IEEE Transac. Electron Dev. 1995, 42, 1344.
- 90. Werner, M.; Job, R.; Denisenko, A.; Zaitsev, A.; Fahrner, W. R.; Johnston, C.; Chalker, P. R.; BuckleyGolder, I. M.; Diamond Relat. Mater. 1996, 5, 723.
- 91. May, P. W.; Philos. Trans R. Soc. Lond. A 2000, 358, 473.
- 92. Sarada, B. V.; Rao, T. N.; Tryk, D. A.; Fujishima, A.; New Diamond Front. Carbon Technol. 1999, 9, 365.
- 93. Pleskov, Y. V.; Russ. J. Electrochem. 2002, 38, 1275.
- 94. Wu, J. L.; Zhu, J. Z.; Shan, L.; Cheng, N. Y.; Anal. Chim. Acta 1996, 333, 125.
- 95. Strojek, J. W.; Granger, M. C.; Swain, G. M.; Dallas, T.; Holtz, M. W.; Anal. Chem. 1996, 68, 2031.
- 96. Brett, C. M. A.; Brett, A. M. O.; Electrochemistry: principles, methods and applications; Oxford University Press: Oxford, 1993, p. 131.
- 97. www.csem.ch; www.windsor-ltd.co.uk; www.ist.fraunhofer.de; www.cypresssystems.com; www.magnetochemie.com, acessadas em Fevereiro 2004; e comunicações pessoais com as empresas.
- 98. Sibilia, J. P., ed.; A guide to materials characterization and chemical analysis; VCH: New York, 1988.
- 99. Silva, L. L. G.; Ferreira, N. G.; Dotto, M. E. R.; Kleinke, M. U.; Appl. Surf. Sci. 2001, 181, 327.
- 100. Ferreira, N. G.; Abramof, E.; Corat, E. J.; Leite, N. F.; Trava-Airoldi, V. J.; Diamond Relat. Mater. 2001, 10, 750.
- 101. Ferreira, N. G.; Abramof, E.; Corat, E. J.; Trava-Airoldi, V. J.; Carbon 2003, 41, 1301.
- 102. Chen, Q. Y.; Granger, M. C.; Lister, T. E.; Swain, G. M.; J. Electrochem. Soc. 1997, 144, 3806.
- 103. Show, Y.; Witek, M. A.; Sonthalia, P.; Swain, G. M.; Chem. Mater. 2003, 15, 879.
- 104. Shaw, J.; Jones, A. N.; Monk, P. M. S.; Rego, C. A.; Diamond Relat. Mater. 2002, 11, 1690.
- 105. Granger, M. C.; Witek, M.; Xu, J. S.; Wang, J.; Hupert, M.; Hanks, A.; Koppang, M. D.; Butler, J. E.; Lucaze, G.; Mermoux, M.; Strojek, J. W.; Swain, G. M.; Anal. Chem. 2000, 72, 3793.
- 106. Nakabayashi, S.; Tryk, D. A.; Fujishima, A.; Ohta, N.; Chem. Phys. Lett. 1999, 300, 409.
- 107. Martin, H. B.; Argoitia, A.; Angus, J. C.; Landau, U.; J. Electrochem. Soc. 1999, 146, 2959.
- 108. Popa, E.; Notsu, H.; Miwa, T.; Tryk, D. A.; Fujishima, A.; Electrochem. Solid State Lett. 1999, 2, 49.
- 109. Saterlay, A. J.; Agra-Gutierrez, C.; Taylor, M. P.; Marken, F.; Compton, R. G.; Electroanalysis 1999, 11, 1083.
- 110. Zhang, R. J.; Lee, S. T.; Lam, Y. W.; Diamond Relat. Mater. 1996, 5, 1288.
- 111. Li, L. F.; Totir, D.; Miller, B.; Chottiner, G.; Argoitia, A.; Angus, J. C.; Scherson, D.; J. Am. Chem. Soc. 1997, 119, 7875.
- 112. Levy-Clement, C.; Zenia, F.; Ndao, N. A.; Deneuville, A.; New Diamond Front. Carbon Technol. 1999, 9, 189.
- 113. Kuo, T. C.; McCreery, R. L.; Swain, G. M.; Electrochem. Solid State Lett. 1999, 2, 288.
- 114. Silva, L. L. G.; Franco, M. K.; Yokaichiya, F.; Ferreira, N. G.; Corat, E. J.; Diamond Relat. Mater. 2002, 11, 153.
- 115. Okano, K.; Naruki, H.; Akiba, Y.; Kurosu, T.; Iida, M.; Hirose, Y.; Nakamura, T.; Jpn. J. Appl. Phys. 1989, 28, 1066.
- 116. Fujimori, N.; Nakahata, H.; Imai, T.; Jpn. J. Appl. Phys. 1990, 29, 824.
- 117. Patel, K.; Hashimoto, K.; Fujishima, A.; J. Photochem. Photobiol., A. 1992, 65, 419.
- 118. Silva, L. L. G.; Corat, E. J.; Iha, K.; Sumodjo, P. T. A.; Resumos do 200th Meeting of the Electrochemical Society, San Francisco, Estados Unidos, 2001.
- 119. Ribeiro, M. C.; Ribeiro, E. F.; Sumodjo, P. T. A.; Silva, L. L. G.; Corat, E. J. Em: Diamond Materials VII; Swain, G. M.; Ando, T.; Angus, J. C.; Brown, W. D.; Davidson, J. L.; Gicquel, A.; Kang, W. P.; Spitsyn B. V., eds.; PV 2001-25, The Electrochemical Society, Pennington, 2002, pp. 24-33.
- 120. Pleskov, Y. V.; Krotova, M. D.; Ralchenko, V. G.; Khomich, A. V.; Khmelnitskiy, R. A.; Electrochim. Acta 2003, 49, 41.
- 121. Tachiki, M.; Fukuda, T.; Sugata, K.; Seo, H.; Umezawa, H.; Kawarada, H.; Appl. Surf. Sci. 2000, 159, 578.
- 122. Goeting, C. H.; Marken, F.; Sosa, A.; Compton, R. G.; Foord, J. S.; Diamond Relat. Mater. 2000, 9, 390.
- 123. Notsu, H.; Yagi, I.; Tatsuma, T.; Tryk, D. A.; Fujishima, A.; Electrochem. Solid-State Lett. 1999, 2, 522.
- 124. Notsu, H.; Yagi, I.; Tatsuma, T.; Tryk, D. A.; Fujishima, A.; J. Electroanal. Chem. 2000, 492, 31.
- 125. Notsu, H.; Fukazawa, T.; Tatsuma, T.; Tryk, D. A.; Fujishima A.; Electrochem. Solid-State Lett. 2001, 4, H1.
- 126. Fujishima, A.; Rao, T. N.; Popa, E.; Sarada, B. V.; Yagi, I.; Tryk, D. A.; J. Electroanal. Chem. 1999, 473, 179.
- 127. Ohta, N.; Nakabayashi, S.; Fujishima, A.; Chem. Lett. 1999, 1147.
- 128. Roy, S. C.; Bruce, P. G.; J. Electroanal. Chem. 1996, 415, 33.
- 129. Sato, R.; Kondo, T.; Shimizu, K.; Honda, K.; Shibayama, Y.; Shirahama, K.; Fujishima, A.; Einaga, Y.; Chem. Lett. 2003, 973.
- 130. Ferro, S.; De Battisti, A.; Anal. Chem. 2003, 75, 7040.
- 131. Yoshihara, S.; Shinozaki, K.; Shirakashi, T.; Hashimoto, K.; Tryk, D. A.; Fujishima, A.; Electrochim. Acta 1999, 44, 2711.
- 132. Yoshihara, S.; Shinozaki, K.; Zenbayashi, T.; Morino, S.; Shirakashi, T.; Hashimoto, K.; Tryk, D. A.; Fujishima, A.; Electrochim. Acta 2000, 45, 3375.
- 133. Ristein, J.; Maier, F.; Riedel, M.; Stammler, M.; Ley, L.; Diamond Relat. Mater. 2001, 10, 416.
- 134. Looi, H. J.; Pang, L.; Molloy, A.; Jones, F.; Foord, J. S.; Jackman, R.; Diamond Relat. Mater. 1998, 7, 550.
- 135. Denisenko, A.; Aleksov, A.; Kohn, E.; Diamond Relat. Mater. 2001, 10, 667.
- 136. Bergmaier, A.; Dollinger, G.; Aleksov, A.; Gluche, P.; Kohn, E.; Surf. Sci. Lett. 2001, 481, L433.
- 137. Yagi, I.; Ogai, K.; Kondo, T.; Fujishima, A.; Ueda, K.; Uosaki, K.; Chem. Lett. 2003, 32, 1050.
- 138. Suffredini, H. B.; Machado, S.; Avaca, L. A.; J. Braz. Chem. Soc. 2004, 15, 16.
- 139. Silva, L. M.; Santana, M.; Boodts, J.; Quim. Nova 2003, 26, 880.
- 140. Ferro, S.; De Battisti, A.; Duo, I.; Comninellis, C.; Hänni, W.; Perret, A.; J. Electrochem. Soc. 2000, 147, 2614.
- 141. Silva, L. L. G.; Corat, E. J.; Sumodjo, P. T. A. Em: Diamond Materials VIII; Swain, G. M., ed.; The Electrochemical Society: Pennington, 2004, no prelo.
- 142. Yagi, I.; Tsunozaki, K.; Tryk, D. A.; Fujishima, A.; Electrochem. Solid-State Lett. 1999, 2, 457.
- 143. Nishikawa, O.; Maeda, K.; Ohtani, Y.; Watanabe, M.; Tanaka, K.; Sekine, T.; Iwatsuki, M.; Aoki, S.; Itoh, J.; Yamanaka, K.; Appl. Surf. Sci. 1999, 146, 398.
- 144. Xu, J. S.; Granger, M. C.; Chen, Q. Y.; Strojek, J. W.; Lister, T. E.; Swain, G. M.; Anal. Chem. 1997, 69, A591.
- 145. Tenne, R.; Levy-Clement, C.; Isr. J. Chem. 1998, 38, 57.
- 146. Swain, G. M.; Anderson, A. B.; Angus, J. C.; MRS Bull. 1998, 23, 56.
- 147. Angus, J. C.; Martin, H. B.; Landau, U.; Evstefeeva, Y. E.; Miller, B.; Vinokur, N.; New Diamond Front. Carbon Technol. 1999, 9, 175.
- 148. Pleskov, Y. V.; Uspekhi Khimii 1999, 68, 416.
- 149. Pleskov, Y. V.; Anal. Chem. 2000, 55, 1045.
- 150. Hupert, M.; Muck, A.; Wang, J.; Stotter, J.; Cvackova, Z.; Haymond, S.; Show, Y.; Swain, G. M.; Diamond Relat. Mater. 2003, 12, 1940.
Datas de Publicação
-
Publicação nesta coleção
04 Maio 2005 -
Data do Fascículo
Mar 2005
Histórico
-
Aceito
12 Nov 2004 -
Recebido
14 Jun 2004