Resumos
Onze fungicidas foram analisados in vitro e seus efeitos testados em campo para o controle de Colletotrichum acutatum, agente da flor-preta do morangueiro (Fragaria X ananassa). Os tratamentos (campo) foram (dosagens de i.a/100 l): iprodione (75 ml), benomil (100 g), tebuconazole (50 ml), tiofanato metílico (70 g), prochloraz (100 ml), propiconazole (50 ml), mancozeb (200 g), folpet (270 g), sulfato de cobre (200 g) e chlorotalonil (200 g), em pulverizações semanais (protetores) e quinzenais (sistêmicos). Foram avaliados a produção de frutos e o número de flores com sintoma de queima. Nos testes de fungitoxicidade in vitro, estudou-se o crescimento micelial, a germinação de conídios e a formação de apressórios. Nos testes in vitro foram utilizadas as concentrações de 1 e 10 ppm de i.a. para todos os fungicidas e posteriormente testadas as concentrações de 0,01, 0,1 e 1 ppm para os mais eficientes, e 10, 50 e 100 ppm para os menos eficazes. Os que resultaram em maior inibição micelial em baixas concentrações foram prochloraz e tebuconazole e os que menos inibiram o crescimento micelial foram sulfato de cobre, clorotalonil e folpet. Para inibir a germinação conidial mostraram-se mais eficientes chlorotalonil, tebuconazole, prochloraz e benomil, e para inibir a formação de apressórios, chlorotalonil e benomil. Os resultados de campo diferiram parcialmente dos testes in vitro: prochloraz e sulfato de cobre apresentaram os menores percentuais de flores doentes (53-55%), enquanto benomil apresentou 100% de ataque. Embora prochloraz, seguido de iprodione, folpet e mancozeb tenham resultado em maiores produções, nenhum fungicida controlou a doença satisfatoriamente.
Fragaria X ananassa; controle químico
Eleven fungicides were tested in the field, and their effects on Colletotrichum acutatum, the agent of strawberry (Fragaria X ananassa) flower blight,, were examined in vitro. Treatments and doses tested in the field per 100 l of water were iprodione (75 ml), benomyl (100 g), tebuconazole (50 ml), methyl thiofanate (70g), prochloraz (100 ml), propiconazole (50 ml), mancozeb (200 g), folpet (270 g), copper sulfate (200 g) and chlorothalonil (200 g), sprayed weekly (protectants) or bi-weekly (systemic). Fruit yield and number of blighted flowers were computed. For the in vitro fungitoxicity tests, the rate of mycelial growth rate of conidial germination and appressorium formation were studied in fungicide dilutions. In vitro tests were conducted with 1 and 10 ppm, and subsequently at 0.01, 0.1 and 1 ppm for the most efficient products and at 10, 50 and 100 ppm, for the least efficient a.i. The fungicides that resulted in least mycelial growth at the lowest concentrations were prochloraz and tebuconazole, and the ones that least inhibited mycelial growth the was copper sulfate, chlorothalonil and folpet. Most efficient products for inhibition of conidial germination were chlorothalonil, tebuconazole, prochloraz and benomyl. Most efficient products for inhibition of appressorium formation were chlorothalonil and benomyl. Field results were partially different from in vitro results: prochloraz and copper sulfate had the lowest percentages of blighted flowers (53-55%), whereas benomyl had 100% blighted flowers. Although prochloraz, followed by iprodione, folpet and mancozeb resulted in larger fruit yields, no product alone provided sufficient control of strawberry flower blight.
a16v26n3
EFEITO DE FUNGICIDAS EM Colletotrichum acutatum E CONTROLE DA ANTRACNOSE DO MORANGUEIRO
RAFAELA M. KOSOSKI1, CLEBER FURLANETTO2, CELSO K. TOMITA1 & ADALBERTO C. CAFÉ FILHO1
1Departamento de Fitopatologia,Universidade de Brasília, CEP 70910-900, Brasília, DF, e-mail: cafefilh@unb.br ; 2Universidade Estadual do Oeste do Paraná, UNIOESTE, Cx. Postal 91, CEP 85960-000, Marechal Cândido Rondon, PR
(Aceito para publicação em 10/07/2001)
Autor para correspondência: Adalberto C. Café Filho
RESUMO
Onze fungicidas foram analisados in vitro e seus efeitos testados em campo para o controle de Colletotrichum acutatum, agente da flor-preta do morangueiro (Fragaria X ananassa). Os tratamentos (campo) foram (dosagens de i.a/100 l): iprodione (75 ml), benomil (100 g), tebuconazole (50 ml), tiofanato metílico (70 g), prochloraz (100 ml), propiconazole (50 ml), mancozeb (200 g), folpet (270 g), sulfato de cobre (200 g) e chlorotalonil (200 g), em pulverizações semanais (protetores) e quinzenais (sistêmicos). Foram avaliados a produção de frutos e o número de flores com sintoma de queima. Nos testes de fungitoxicidade in vitro, estudou-se o crescimento micelial, a germinação de conídios e a formação de apressórios. Nos testes in vitro foram utilizadas as concentrações de 1 e 10 ppm de i.a. para todos os fungicidas e posteriormente testadas as concentrações de 0,01, 0,1 e 1 ppm para os mais eficientes, e 10, 50 e 100 ppm para os menos eficazes. Os que resultaram em maior inibição micelial em baixas concentrações foram prochloraz e tebuconazole e os que menos inibiram o crescimento micelial foram sulfato de cobre, clorotalonil e folpet. Para inibir a germinação conidial mostraram-se mais eficientes chlorotalonil, tebuconazole, prochloraz e benomil, e para inibir a formação de apressórios, chlorotalonil e benomil. Os resultados de campo diferiram parcialmente dos testes in vitro: prochloraz e sulfato de cobre apresentaram os menores percentuais de flores doentes (53-55%), enquanto benomil apresentou 100% de ataque. Embora prochloraz, seguido de iprodione, folpet e mancozeb tenham resultado em maiores produções, nenhum fungicida controlou a doença satisfatoriamente.
Palavras-chave: Fragaria X ananassa, controle químico.
ABSTRACT
Effect of fungicides on Colletotrichum acutatum and field control of strawberry flower blight
Eleven fungicides were tested in the field, and their effects on Colletotrichum acutatum, the agent of strawberry (Fragaria X ananassa) flower blight,, were examined in vitro. Treatments and doses tested in the field per 100 l of water were iprodione (75 ml), benomyl (100 g), tebuconazole (50 ml), methyl thiofanate (70g), prochloraz (100 ml), propiconazole (50 ml), mancozeb (200 g), folpet (270 g), copper sulfate (200 g) and chlorothalonil (200 g), sprayed weekly (protectants) or bi-weekly (systemic). Fruit yield and number of blighted flowers were computed. For the in vitro fungitoxicity tests, the rate of mycelial growth rate of conidial germination and appressorium formation were studied in fungicide dilutions. In vitro tests were conducted with 1 and 10 ppm, and subsequently at 0.01, 0.1 and 1 ppm for the most efficient products and at 10, 50 and 100 ppm, for the least efficient a.i. The fungicides that resulted in least mycelial growth at the lowest concentrations were prochloraz and tebuconazole, and the ones that least inhibited mycelial growth the was copper sulfate, chlorothalonil and folpet. Most efficient products for inhibition of conidial germination were chlorothalonil, tebuconazole, prochloraz and benomyl. Most efficient products for inhibition of appressorium formation were chlorothalonil and benomyl. Field results were partially different from in vitro results: prochloraz and copper sulfate had the lowest percentages of blighted flowers (53-55%), whereas benomyl had 100% blighted flowers. Although prochloraz, followed by iprodione, folpet and mancozeb resulted in larger fruit yields, no product alone provided sufficient control of strawberry flower blight.
Dentre os patógenos que limitam o cultivo do morangueiro (Fragaria X ananassa Duch.) destaca-se Colletotrichum acutatum Simmonds, principal agente causal do complexo antracnose do morangueiro no Brasil. A doença manifesta-se principalmente pelo sintoma denominado flor-preta e encontra-se disseminada nas principais regiões produtoras (Furlanetto et al., 1996b). Além das flores, o fungo também afeta frutos e folhas (Tanaka et al., 1994 e 1996).
A capacidade do patógeno em causar infecções latentes dificulta a visualização de sintomas, principalmente em folhas e hastes, durante a produção de mudas (Tanaka et al., 1996). A dificuldade por parte dos produtores em identificar sintomas em mudas, aliada à carência de cultivares com um bom nível de resistência, favorece a introdução da doença em novas áreas, quando as mudas atuam como inóculo primário. Uma vez iniciada a doença, o inóculo secundário é responsável pela infecção de flores e frutos, principalmente via água de chuva ou de irrigação, podendo ocasionar prejuízos significativos.
O método mais utilizado no controle das doenças do morangueiro tem sido o químico, seja para o complexo da antracnose ou para as demais doenças da cultura (e.g.: Furlanetto et al., 1999). As informações recentes relativas ao controle químico da antracnose restringem-se a registros de testes de campo em congressos científicos (Domingues et al., 1997, 1998; Furlanetto et al., 1996a; Sinigaglia, 1996; Smith, 1987). Além disso, não obstante a larga utilização de fungicidas, verifica-se que a maioria dos produtos utilizados se mostram pouco eficientes no controle da flor-preta em campo, são aplicados de maneira inadequada, e nenhum está registrado para o morango no Brasil.
O objetivo deste trabalho foi testar a eficiência de campo e o efeito in vitro de produtos que vêm sendo utilizados para o controle da flor-preta do morangueiro. Foram selecionados fungicidas de diferentes grupos químicos, de ação protetora ou sistêmica, recomendados para o controle de fungos coelomicetos, ao qual pertence o gênero Colletotrichum. Para subsidiar a utilização das diversas alternativas químicas em um manejo integrado da doença, os efeitos dos produtos no crescimento micelial, germinação de conídios e formação de apressórios de C. acutatum foram examinados separadamente in vitro (Kososki et al., 1997, 1998).
Testes de fungitoxicidade in vitro
Crescimento micelial: Para o crescimento micelial, os ensaios foram conduzidos em incubadora biológica a 25 oC e fotoperíodo de 12 h a partir da inoculação em BDA de discos de micélio de 7 mm de diâmetro. Foi utilizado o isolado de C. acutatum UnB-9, originário do DF, cuja identidade e patogenicidade haviam sido comprovadas (Barros et al., 1997). Os seguintes ingredientes ativos (i.a.) foram testados: iprodione; benomil; tebuconazole; tiofanato metílico; prochloraz; propiconazole; mancozeb; folpet; sulfato de cobre; chlorotalonil. Os i.a. foram dissolvidos em acetona a 1% antes de serem incorporados em BDA à 45 oC. O delineamento experimental foi inteiramente casualisado com cinco repetições. Nos primeiros ensaios, benomil foi considerado o tratamento-padrão devido à sua larga utilização na cultura do morangueiro. Nos demais ensaios, foram incluídas duas testemunhas (BDA e BDA + 1% de acetona). O crescimento micelial foi avaliado com régua milimetrada oito dias após a inoculação em meio de cultura e as áreas de micélio foram calculadas pelo diâmetro médio de cada repetição (pd2/4).
Germinação de conídios e formação de apressórios: Para a avaliação da germinação de conídios e da formação de apressórios utilizou-se incubadora biológica a 25 oC no escuro. Dimetilsulfóxido (DMSO) a 1% foi o solvente usado para todos os fungicidas, incluindo-se como testemunhas DMSO 1% e água destilada. O delineamento experimental foi inteiramente casualisado com três repetições, dez tratamentos fungicidas e duas testemunhas. Os experimentos foram executados em lâminas escavadas, e em cada lâmina, contendo 30 ml de suspensão de 2 x 105 conídios/ml juntamente com cada i.a. A suspensão de esporos foi obtida de colônias em BDA com sete a dez dias de crescimento. As leituras de germinação de conídios e formação de apressórios foram realizadas 24 h após a incubação da suspensão de conídios, com a interrupção do processo através da adição de azul-de-algodão. Foram calculadas as percentagens de conídios germinados e de conídios que formaram apressórios. Consideraram-se como germinados os conídios com tubo germinativo maior que o próprio comprimento.
Separação por etapas dos ensaios segundo a concentração dos i.a. Tanto para crescimento micelial, quanto para germinação de conídios e formação de apressórios, as avaliações foram executadas em séries de três ensaios: (a) concentrações intermediárias: o primeiro ensaio incluiu todos os 10 i.a. a 1 e 10 ppm para crescimento micelial e a 1 ppm para germinação de conídios e formação de apressórios; (b) baixas concentrações: no segundo ensaio foram testados os melhores tratamentos do primeiro ensaio em 0,01, 01 e 1 ppm e as testemunhas BDA e BDA + acetona a 1% ou água destilada e DMSO a 1%; (c) altas concentrações: no terceiro ensaio, foram incluídos os i.a. menos eficientes no primeiro ensaio nas concentrações de 10, 50 e 100 ppm e as testemunhas pertinentes. Cada ensaio foi repetido duas vezes.
Os dados obtidos foram transformados para arco seno raíz de x + 1/2 e submetidos à análise de variância e as médias dos tratamentos comparadas pelo teste Tukey a 5%.
Ensaio de campo
Mudas de morango, obtidas de cultivo de meristemas (In Vitro Biotecnologia de Plantas Ltda), foram instaladas em área produtora em Brazlândia, DF. O ensaio constou de 11 tratamentos e quatro repetições em blocos ao acaso, com 12 plantas por parcela, sendo a parcela útil constituída pelas quatro plantas centrais. Os tratamentos e dosagens de i.a./100 l de água foram: iprodione, 75 ml (protetor); benomil, 100 g (sistêmico); tebuconazole, 50 ml (sistêmico); tiofanato metílico, 70 g (sistêmico); prochloraz, 100 ml (translaminar); propiconazole, 50 ml (sistêmico); mancozeb, 200 g (protetor); folpet, 270 g (protetor); sulfato de cobre, 200 g (protetor); chlorotalonil, 200 g (protetor); e Testemunha pulverizada com água. As aplicações iniciaram-se logo após o transplantio com pulverizador costal de 20 l e bico de vazão cônica, sendo semanais para fungicidas protetores e quinzenais para os sistêmicos. Por ocasião da primeira e segunda floradas, as plantas foram inoculadas com uma suspensão de 106 conídios/ml do isolado de C. acutatum UnB-9. Foram avaliados o peso de frutos em colheitas semanais e o número de flores com sintomas da doença ao longo do ciclo da cultura. Os resultados foram submetidos a análise de variância e as médias comparadas pelo teste Tukey a 5%.
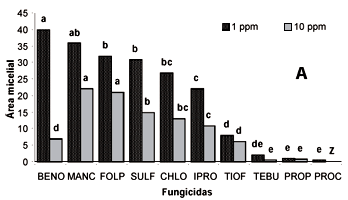
Para a inibição do crescimento micelial, os fungicidas mais eficientes em concentrações intermediárias (1 e 10 ppm) foram prochloraz, propiconazole e tebuconazole (Figura 1A). Neste ensaio, benomil não foi eficiente a 1 ppm, mostrando-se eficiente apenas a 10 ppm. O segundo ensaio, realizado com os fungicidas de melhor desempenho a 1 e 10 ppm, mostrou que prochloraz foi o fungicida mais eficiente para inibir o crescimento micelial em baixas concentrações (0,1 e 0,01 ppm, Figura 1B). Os fungicidas mancozeb, benomil, iprodione, tiofanato metílico, folpet, sulfato de cobre e chlorotalonil foram testados no 3º ensaio em altas concentrações (50 e 100 ppm). Neste ensaio mancozeb, benomil, iprodione e tiofanato metílico destacaram-se dos demais, reduzindo crescimento micelial de C. acutatum (Figura 1C).
A eficiência comparativa de prochloraz em baixas concentrações sobre o crescimento micelial de C. acutatum foi demonstrada anteriormente por Freeman et al. (1997). Os resultados apresentados aqui confirmam a eficiência deste i.a. em baixas concentrações (< 1 ppm), principalmente quando comparado a fungicidas protetores como o folpet e o mancozeb. Propiconazole e tebuconazole também foram consistentemente eficientes para a redução do crescimento micelial de C. acutatum a 1 ppm. A eficiência de propiconazole em reduzir o crescimento micelial in vitro também já havia sido demostrada por Freeman et al. (1997). A avaliação do terceiro ensaio permitiu diferenciar o efeito dos fungicidas sistêmicos e protetores. Os sistêmicos benomil, iprodione e tiofanato metílico apresentaram áreas menores de crescimento que os protetores folpet, sulfato de cobre e chlorotalonil. Entretanto, mancozeb (protetor) foi bastante eficiente em reduzir o crescimento micelial a 50 e 100 ppm.
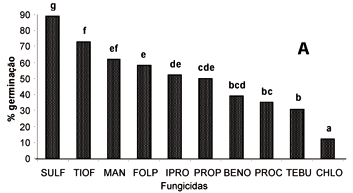
Os efeitos dos i.a sobre as taxas de germinação de conídios e de formação de apressórios foram diferentes dos observados para crescimento micelial, refletindo os diferentes processos biológicos mensurados a partir destas variáveis. Com relação à inibição da germinação, o fungicida com melhor desempenho na concentração de 1 ppm foi o chlorotalonil (Figura 2A). Neste tratamento apenas 12% dos conídios germinaram, inferior a todos os demais (p<0,05). Tebuconazole, prochloraz, benomil, propiconazole e iprodione apresentaram taxas de germinação entre 31 e 52%, e também foram testados em baixas concentrações. Entretanto, nenhum tratamento foi eficiente a 0,01 ppm ou 0,1 ppm (resultados não apresentados). A 0,1 ppm prochloraz apresentou a menor taxa de germinação de conídios (42%), enquanto chlorotalonil não foi eficiente nestas concentrações. No terceiro ensaio (altas concentrações: 10, 50 e 100 ppm), mancozeb e folpet foram os que mais inibiram a germinação de conídios, com apenas 1-2% de conídios germinados (dados não apresentados).
O efeito dos fungicidas sobre a formação de apressórios não diferenciou os tratamentos nitidamente a 1 ppm, embora benomil tenha apresentado os menores índices (Figura 2B).
O ensaio com baixas concentrações foi realizado com benomil, chlorotalonil, iprodione, tebuconazole, propiconazole e prochloraz. A 0,01 ppm chlorotalonil, benomil e prochloraz foram os mais eficientes, com 2,5, 2,5 e 17 % de apressórios, respectivamente (dados não apresentados). A 0,1 ppm chlorotalonil destacou-se de todos os demais, com a menor percentagem de formação de apressórios. No ensaio realizado com as concentrações de 10, 50 e 100 ppm, mancozeb e folpet apresentaram o melhor desempenho.
A produção de frutos por parcela útil (Figura 3A) destaca o tratamento prochloraz (p<0,05). Com relação à incidência de flores doentes, as parcelas pulverizadas com prochloraz e sulfato de cobre apresentaram menor número de flores doentes que os tratamentos com benomil e a testemunha (Figura 3B). Em relação ao total de flores presentes, prochloraz e sulfato de cobre apresentaram 53-55% de flores doentes por ocasião da colheita, enquanto benomil e a testemunha apresentaram 85-100% de ataque.
Trabalhos recentes destacam a eficiência de prochloraz em reduzir a porcentagem de flores doentes em campo, aplicado isoladamente ou em combinação com outros fungicidas (Domingues et al., 1997, 1998; Freeman et al., 1997; Sinigaglia, 1996). A baixa eficiência de benomil em campo confirma trabalhos anteriores que mostraram pouca eficiência deste benzimidazol para o controle da doença (Delp & Milholland, 1980; Gullino et al., 1985). Sabe-se que o uso contínuo de benzimidazois pode levar à formação de estirpes resistentes de Colletotrichum sp. De fato, o isolado utilizado neste experimento é proveniente de área de cultivo com uso intensivo de fungicidas e pode representar uma estirpe resistente ao benomil. O bom desempenho do sulfato de cobre no campo, apesar da menor eficiência in vitro, sugere um efeito indireto do fungicida sobre o morangueiro, possivelmente induzindo um aumento do nível de resistência à doença. Com efeito, a falta de correspondência completa entre os resultados in vitro e de campo explica-se porque cada ensaio in vitro visou a análise separada das propriedades dos i.a. em diferentes processos fisiológicos de C. acutatum, enquanto que em campo, foram medidos todos os efeitos dos agroquímicos no processo doença, incluindo prováveis efeitos na planta e em outros microorganismos.
Aplicações fungicidas, especialmente de prochloraz, garantiram maior produção de frutos e menor ocorrência da doença em flores (Figuras 3A, B). Entretanto, de modo geral, a incidência da doença em todos os tratamentos foi muito alta, mostrando que o controle químico, isoladamente, pode não ser um método eficiente para o manejo da flor-preta e indicando a necessidade de investigação de outras estratégias de controle da antracnose do morangueiro. Finalmente, é necessário notar que estudos complementares de resíduos são necessários antes do registro de qualquer produto para a cultura do morango.
AGRADECIMENTOS
C. Furlanetto agradece concessão de bolsa RHAE/CNPq junto à In Vitro Biotecnologia de Plantas Ltda. A Juvenil Cares, pela revisão final do manuscrito.
- BARROS, T., FURLANETTO, C. & CAFÉ FILHO., A.C. Caracterização de isolados de Colletotrichum de morango no Distrito Federal. Fitopatologia Brasileira 22:250. 1997. (Resumo).
- DELP, B. & MILHOLLAND, R.D. Control of strawberry anthracnose with captafol. Plant Disease 64:1013-1015. 1980.
- DOMINGUES, R.J., TOFOLI, J.G. & OLIVEIRA, S.H.F. Avaliação de fungicidas no controle da flor preta (Colletotrichum acutatum) da cultura do morango. Summa Phytopathologica 23:66.1997. (Resumo).
- DOMINGUES, R.J., OLIVEIRA, S.H.F, TOFOLI, J.G. & GARCIA, J.R. Controle químico da flor preta (Colletotrichum acutatum) do morangueiro com azoxystrobin. Summa Phytopathologica 24:72.1998. (Resumo).
- FREEMAN, S., NIZANI, F., DOTAN, S., EVEN,S. & SANDO, T. Control of Colletotrichum acutatum in strawberry under laboratory, greenhouse and field conditions. Plant Disease 81:749-752. 1997.
- FURLANETTO C., CAFÉ FILHO, A.C., TOMITA, C.K. & CAVALCANTI, M.H. Eficiência de fungicidas e de um composto líquido bioativo no controle da flor preta do morangueiro no Distrito Federal. Fitopatologia Brasileira 21:399. 1996a. (Resumo).
- FURLANETTO, C., CAFÉ FILHO, A.C., TOMITA, C.K. & CAVALCANTI, M.H. Doenças do morangueiro e aspectos da produção no Distrito Federal. Horticultura Brasileira 14:218-220. 1996b.
- FURLANETTO, C., TOMITA, C.K. & CAFÉ FILHO, A.C. Efeito da época de aplicação de fungicida no controle da mancha de Mycosphaerella do morangueiro. Horticultura Brasileira 17:231-233. 1999.
- GULLINO, M.L.; ROMANO, M.L. & GARIBALDI, A. Identification and response to fungicides of Colletotrichum gloeosporioides, incitant of strawberry black rot in Italy. Plant Disease 69:608-609. 1985.
- KOSOSKI, R.M., FURLANETTO, C. & CAFÉ FILHO, A.C. Efeito de fungicidas sobre o crescimento micelial de Colletotrichum acutatum, agente da flor preta do morangueiro. Fitopatologia Brasileira 22:273.1997. (Resumo).
- KOSOSKI, R.M., FURLANETTO, C. & CAFÉ FILHO, A.C. Efeito de fungicidas sobre a germinação de conídios e formação de apressório de Colletotrichum acutatum Fitopatologia Brasileira 23:251.1998. (Resumo).
- SINIGAGLIA, C. Efeito de fungicidas no controle da antracnose do morangueiro. Summa Phytopathologica 22:63.1996. (Resumo).
- SMITH, B.J. Greenhouse evaluation of fungicides for control of strawberry antracnose crown-rot. Phytopathology 77:643. 1987. (Resumo).
- TANAKA, M.A.S., PASSOS, F.A. & ITO, M.F. Incidência da cultivar e do estádio fenológico do fruto de morangueiro sobre o desenvolvimento de lesões causadas por Colletotrichum spp. Summa Phytopathologica 20:160-163. 1994.
- TANAKA, M.A.S., PASSOS, F.A. & BETTI, J.A. Mancha irregular da folha do morangueiro, causada por Colletotrichum acutatum, no Brasil. Fitopatologia Brasileira 21:486-488. 1996.
Datas de Publicação
-
Publicação nesta coleção
27 Nov 2001 -
Data do Fascículo
Set 2001
Histórico
-
Aceito
10 Jul 2001