Resumos
Neste trabalho, usando o processo de coacervação, foi estudado o sistema NaPO3/AgNO3/H2O. Determinou-se o domínio de coacervação a partir de diferentes concentrações de NaPO3 e AgNO3 e a influência do pH na estabilização do coacervato foi determinada. Os coacervatos obtidos em pH ~ 5 apresentam maior região de estabilidade.
coacervato; vidros e fosfatos
In this work, using coacervation process, the influence of the pH in the stability of the coacervates of the NaPO3/AgNO3/H2O system was studied. The coacervate domain was established using different concentrations of NaPO3 and AgNO3 and the influence of the pH in the stability of the coacervate was putfoward. The coacervates obtained at pH ~ 5 present highest stability.
coacervate; glasses and phosphates
Influência do pH na estabilidade dos coacervatos de prata como precursores vítreos
Influence of the pH in the stability of the silver coacervate by vitreous precursors
Bianca Montanari; Pierre Vast; Marco Antonio Utrera Martines; Sidney José Lima Ribeiro; Younes Messaddeq
Departamento de Química Geral e Inorgânica - Instituto de Química - UNESP - 14801-970 - Araraquara - SP - Brasil
RESUMO
Neste trabalho, usando o processo de coacervação, foi estudado o sistema NaPO3/AgNO3/H2O. Determinou-se o domínio de coacervação a partir de diferentes concentrações de NaPO3 e AgNO3 e a influência do pH na estabilização do coacervato foi determinada. Os coacervatos obtidos em pH ~ 5 apresentam maior região de estabilidade.
Palavras-chave:coacervato, vidros e fosfatos
ABSTRACT
In this work, using coacervation process, the influence of the pH in the stability of the coacervates of the NaPO3/AgNO3/H2O system was studied. The coacervate domain was established using different concentrations of NaPO3 and AgNO3 and the influence of the pH in the stability of the coacervate was putfoward. The coacervates obtained at pH ~ 5 present highest stability.
Keywords: coacervate, glasses and phosphates
Introdução
Vidros contendo partículas de prata têm sido estudados durante vários anos. Uma propriedade óptica que chama a atenção no âmbito de seu potencial à aplicações, no campo de materiais de interesse tecnológico, é a propriedade fotocrômica. Diversos processos foram usados para o controle do tamanho de partículas de prata, seja por radiação X ou por radiação na faixa espectral de UV. Recentemente, vários estudos têm empregado novos processos de preparação no intuito de obter um melhor controle do tamanho de partículas. Como exemplo, a microencapsulação de partículas insolúveis[11,1] ou líquidos imiscíveis[8], a fim de controlar sua reatividade. Rota coloidal de preparação destes materiais permite controlar o tamanho e a forma das partículas. Como os fosfatos monoméricos não se condensam em solução aquosa, o processo de coacervação de polifosfatos é proposto como método de obtenção de vidros de fosfatos a partir de solução aquosa. A obtenção de precursores vítreos a partir de coacervatos de polifosfatos vem sendo estudada por Vast et al[13]. Coacervação é bastante empregada nas indústrias agro-químicas[2] e alimentícia, cosmética[10] e sobretudo farmacêutica[12,3]. No entanto, esta técnica é pouca empregada em química inorgânica, mas é muito promissora para preparação de vidros, pois envolve temperatura de tratamento térmico baixa e leva a boa homogeneidade.
Para os polifosfatos, os coacervatos podem ser obtidos pela adição de etanol e cloreto de magnésio ou cálcio às soluções do sal de Graham[13].
A característica importante dos coacervatos de polifosfatos, para este trabalho, reside na potencialidade do método para obtenção, homogeneização e controle do tamanho de partículas em vidros[6].
No presente trabalho, foi estudado o sistema NaPO3/AgNO3/H2O. O domínio de coacervação foi determinado e a influência do pH na estabilidade dos coacervatos foi estabelecida.
Material
Neste trabalho foram utilizados os seguintes materiais:
-
Bureta graduada de 10 mL;
-
Béqueres de 50 e 100 mL;
-
Agitador magnético;
-
Luvas cirúrgicas (proteção contra soluções de prata utilizadas);
-
Balões volumétricos de 25, 50, 100 e 250 mL para preparo de soluções;
-
Soluções dos seguintes sais: polifosfato de sódio (sal de Graham) e nitrato de prata.
Métodos
Determinação do domínio de estabilidade:
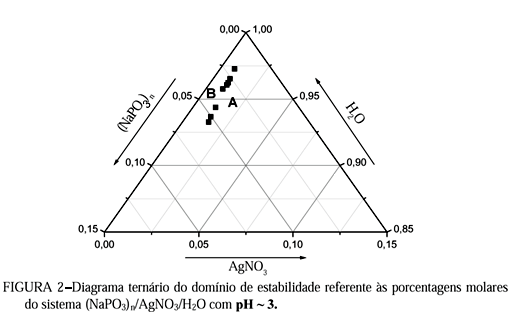
Na determinação do domínio de estabilidade, utilizamos a seguinte metodologia: a solução de nitrato de prata foi adicionada, gota à gota, a um volume de 25 ml de solução de polifosfato de sódio (sal de Graham) sob constante agitação utilizando-se um agitador magnético e temperatura constante (22°C), até a formação inicial do coacervato. (Figura 1).
Influência do pH:
Ajustou-se o pH das soluções de partida de polifosfato de sódio (pH ~3 e 5) com ácido nítrico concentrado.
Resultados
Influência do pH
Partindo de uma solução aquosa, de polifosfato de sódio 4 mol/L e nitrato de prata 2 mol/L, a pH ~ 12, observou-se a formação de um precipitado de coloração amarela, estável. Este precipitado formado é o ortofosfato de prata (AgPO3) que apresenta uma constante de solubilidade, Kps = 8,89.10-17[9] , ou seja pK = 12,05. O ortofosfato de prata é solúvel em ácidos[9]. Quando se ajusta a mesma solução, em pH ~ 6, também resulta na formação de ortofosfato de prata. Observa-se que em pH ~ 5, ou inferior, formam-se coacervatos. Então, no intuito de determinar o domínio de estabilidade desses coacervatos construiu-se o limite de coacervação, partindo de uma solução de polifosfato em pH ~ 3 e 5.
Formação do coacervato com a adição da solução de AgNO3
Com o auxílio de uma bureta graduada de 10mL, adicionou-se, gota à gota, a solução de AgNO3 à solução de (NaPO3)n, sob agitação constante (agitador magnético). Rapidamente inicia-se a formação de um precipitado branco. Então, depois de um certo tempo, a formação e a estabilização do coacervato puderam ser observadas devido à propriedade do polifosfato de formar complexos solúveis relativamente estáveis entre metal e fosfato[13].
Características dos coacervatos
Os coacervatos obtidos a partir do sistema a pH ~ 3 são transparentes e os obtidos a partir do sistema a pH ~ 5 também são transparentes, mas observa-se a formação de um precipitado branco, tornando-se um sistema constituído por 3 fases: sobrenadante (fase menos densa), coacervato (fase intermediária) e precipitado (fase mais densa). Isso se deve à parcial estabilidade dos íons Ag+ adicionados. O precipitado branco formado em pH ~ 5 é estável.
Domínio de estabilidade - (NaPO3)n /AgNO3 /H2O
Foram feitos vários ensaios, controlando-se temperatura (22°C). Fez-se uma média dos valores obtidos para um melhor resultado.
A adição da solução de AgNO3 é feita lentamente, sob agitação constante, pois primeiramente, observa-se a formação de um precipitado branco que, após um longo período de tempo, resulta na formação do coacervato.
Através dos volumes gastos de solução de nitrato de prata, calculou-se as porcentagens molares dos componentes envolvidos nos sistemas (Tabelas 1 e 2).
® Solução de polifosfato: pH ~ 3
Com os valores das porcentagens molares dos componentes, Tabela 1, construiu-se o diagrama ternário do domínio de estabilidade, Figura 2, referente ao sistema (NaPO3)n/AgNO3/H2O pH ~3.
Na região B, tem-se um sistema monofásico (sol) e na região A, tem-se a formação do coacervato.
® Solução de polifosfato: pH ~ 5
Não foi necessário o ajuste do pH, pois as soluções de polifosfato de sódio têm pH ~5.
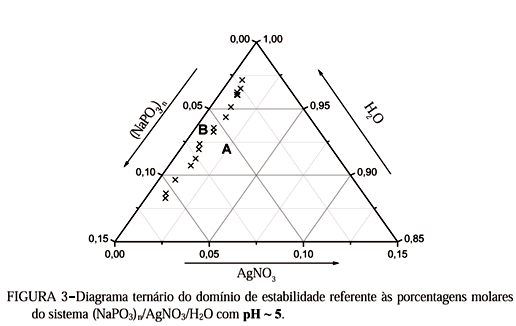
Com os valores das porcentagens molares dos componentes, Tabela 2, construiu-se o diagrama ternário do domínio de estabilidade, Figura 3, referente ao sistema (NaPO3)n/AgNO3/H2O pH ~ 5.
Na região B, tem-se um sistema monofásico (sol) e na região A, tem-se a formação do coacervato.
Para maior visualização, construiu-se o diagrama ternário a seguir com os resultados obtidos.
Discussão
Neste trabalho, numa primeira etapa, foram estabelecidas as condições termoquímicas dos coacervatos. Em seguida, foi estudado o efeito do pH na estabilização do domínio de coacervação. Sabendo que o pH influi na densidade de carga no meio coloidal da natureza orgânica contendo grupos ionizáveis. No caso de macromoléculas de origem mineral, o pH tem efeito na modificação de grupos terminais das moléculas. No caso específico dos polifosfatos estes apresentam dois hidrogênios ionizáveis. O primeiro corresponde aos ácidos fortes que são os grupos médios e o segundo aos ácidos fracos que são os grupos terminais. Isto explica a formação de coacervatos à base de fosfatos apenas em meio ácido[4,5], enquanto que em meio básico resulta na géis.
No nosso caso, os sistemas (NaPO3)n/AgNO3/H2O em pH ~ 3, observa-se um menor limite de coacervação (Figura 4), não possibilitando a formação de coacervatos de prata a partir de soluções muito concentradas de polifosfato de sódio (6 e 8 mol/L). À medida que o pH aumenta até 5, isto é, acompanhado por um aumento na viscosidade, permitindo assim, a estabilização do coacervato de prata, conseqüentemente, um precipitado branco é formado. Podemos pensar que neste caso temos um aumento da densidade de carga relacionado com a evolução de pH, levando à formação de cadeias mais longas.
A partir dos dados obtidos pode-se observar o efeito de pH na estabilização de coacervatos. Em todos os sistemas, os coacervatos podem ser obtidos somente a pH < 6.
A estabilização das condições de coacervação é muito importante, pois pode levar a preparação de vidros com tamanho controlado de partículas de prata[14]. Outro ponto importante dos coacervatos de prata é a utilização dos mesmos para revestimento de materiais metálicos operando na faixa de temperatura de 400 à 500°C[7,13,14].
Conclusão
Foi mostrado a influência do pH na estabilização dos coacervatos no sistema (NaPO3)n/AgNO3/H2O. Foi verificado que os coacervatos em pH ~ 5 são os precursores mais adequados pois apresentam maior região de estabilidade. Este estudo é muito promissor para a obtenção de partículas de prata com tamanho bem controlado.
Agradecimentos
Os autores agradecem à FAPESP pelo apoio financeiro ao projeto e B. Montanari agradece à bolsa concedida pela FAPESP.
12 MORTADA, S.A.M. J. Pharm. Sci., v.3, n.1, p.1-5, 1989. Apud GOMEZ, F. Gestion dun procédé de vitrification de métaux à partir de coacervates de polyphosphates. Compiegne, 1998. 239p. Tese (Doutorado) Université de Technologie de Compiegne.
Recebido em 04.01.2002
Aceito em 19.03.2002
- 1 ARSHADY, R. Microspheres and Microcapsules, a survey of manufacturing techniques.2. Coacervation. Polym. Eng.Sci, v.30, p.905-914, 1990.
- 2 BUNGENBERG de Jong, H.G.; KRUYST, H.R. Proc. Kon. Ned. Akad. Wetensch, v.32, p.849, 1929. Apud GOMEZ, F.; Gestion dun procédé de vitrification de métaux à partir de coacervates de polyphosphates. Compiegne, 1998. 239p. Tese (Doutorado) Université de Technologie de Compiegne.
- 3 CHUKWA, A.; AGRWAL, S.P.; ADIKWU, M.U.; S.T.P. Pharma Sciences, v.1, n.2, p.117-120, 1991. Apud GOMEZ, F.; Gestion dun procédé de vitrification de métaux à partir de coacervates de polyphosphates. Compiegne, 1998. 239p. Tese (Doutorado) Université de Technologie de Compiegne.
- 4 DEFOONTAINES, B.; DEFFONTAINES-FOUREZ, M.; VAST, P. Silicates industriels, 1994, LIX (3-4), 145-155.
- 5 DRAOUI, M. Aplication du procédé sol-gel â verre à lobtention de matériaux phosphates utilisables en génie biomédical. Spectrochimie Inorganique, 1975. 27p. Tese (Doutorado) Université des Sciences et Techniques de Lille.
- 6 FILHO, F.A.D. Preparação e caracterização de vidros e filmes a base de fosfatos dopados com Eu3+ e Er3+ via coacervação. Araraquara, Tese de Doutorado sob orientação do Prof. Dr. Sidney J.L. Ribeiro (em andamento) Instituto de Química de Araraquara/ UNESP.
- 7 GOMEZ, F. Gestion dun procédé de vitrification de métaux à partir de coacervates de polyphosphates. Compiegne, 1998. 239p. Tese (Doutorado) Université de Technologie de Compiegne.
- 8 GREEN, B.K.; SCHLEICHER, L. Oil containing microscopic capsules and method of making them. US Patent, 2800 457, 1957 07 23. Apud GOMEZ, F.; Gestion dun procédé de vitrification de métaux à partir de coacervates de polyphosphates Compiegne, 1998. 239p. Tese (Doutorado) Université de Technologie de Compiegne.
- 9 LIDE, D.R. HANDBOOK of Chemistry and Physics, 80st edition, 1999.
- 10 MAGILL, M. Cosmet. Toiletries, v.105, n.6, p.59-62, 1990. Apud GOMEZ, F.; Gestion dun procédé de vitrification de métaux à partir de coacervates de polyphosphates. Compiegne, 1998. 239p. Tese (Doutorado) Université de Technologie de Compiegne.
- 11 MISTRY. Coacervation Process, European Patent, 9300 533, 16 mar. 1993. Apud GOMEZ, F. Gestion dun procédé de vitrification de métaux à partir de coacervates de polyphosphates. Compiegne, 1998. 239p. Tese (Doutorado) Université de Technologie de Compiegne.
- 13 VAST, P.; BARBIEUX, F.; GOMEZ, F. Les verres de phosphates: une methode originale de préparation à finalité industrielle. Verre, v.2, n.3, p.3-10, 1996.
- 14 WILLOT, G. Les verres de phosphates de zinc et dargent : une solution puor lémaillage des métaux à température inférieure à 500°C Compiegne, 1999. 39p. Dissertação (Mestrado) Université de Technologie de Compiegne.
Datas de Publicação
-
Publicação nesta coleção
28 Abr 2003 -
Data do Fascículo
2002
Histórico
-
Recebido
04 Jan 2002 -
Aceito
19 Mar 2002