Resumos
Objetivos: analisar os efeitos da betametasona sobre o binômio materno-fetal da rata albina. Métodos: utilizamos 60 ratas albinas prenhes divididas ao acaso em três grupos numericamente iguais. As ratas do grupo I foram tratadas com betametasona na dose de 1 mg/kg de peso em 0,5 ml de água destilada, por via intramuscular no 11º, 12º, 18º e 19º dia de prenhez; as do grupo II receberam 0,5 ml de água destilada, por via intramuscular no 11º, 12º, 18º e 19º dia de prenhez, e as do grupo III não receberam qualquer fármaco ou veículo. O ganho de peso das matrizes foi avaliado nos dias 0, 7, 14 e 20 de prenhez, sendo que no 20º dia todos os animais foram sacrificados por decapitação. Foram quantificados o número de implantações, de reabsorções, de fetos, de placentas, de malformações maiores, de mortalidade materna e fetal, assim como o peso dos fetos e das placentas. Resultados: nossos resultados revelaram que as matrizes tratadas com betametasona apresentaram menor ganho de peso. Quanto aos fetos e as placentas do grupo tratado, observamos que os pesos foram inferiores aos dos outros grupos. A média de peso dos fetos foi de 3,20 g contra 3,75 g no grupo controle. A média de peso das placentas foi de 0,36 g no grupo tratado com betametasona contra 0,48 g no grupo controle. Todas estas diferenças foram estatisticamente significantes. Conclusões: a betametasona apresenta efeito negativo sobre o ganho de peso das matrizes, fetos e placentas, quando administrada de forma repetitiva a partir da segunda metade da prenhez.
Corticóides; Síndrome do desconforto respiratório; Prematuridade
Purpose: to analyze the effect of betamethasone on the pregnancy of rats. Methods: thirty pregnant rats were divided into three groups of ten animals each. Group I -- the animals received betamethasone IM (1 mg/kg body weight, in 0.5 ml distilled water) on the 11th, 12th, 18th and 19th day of pregnancy. Group II -- the rats received distilled water (0.5 ml) IM on the 11th, 12th, 18th and 19th day of pregnancy. Group III - the rats did not receive any drug or vehicle. The animals were weighed on days 0, 7, 14 and on the 20th of pregnancy, and on the last day of weighing, the animals were sacrificed. The number of implantations, resorptions, fetuses, placentas, malformations, maternal and fetal mortality as well as the weight of the fetuses and placentas were obtained and analyzed. Results: our results show that the rats treated with betamethasone gained significantly less weight. Their fetuses had an average weight of 3.2 g compared with 3.75 g in the control group. The results regarding placental weight were 0.36 g vs 0.48 g, respectively. All these differences were statistically significant. Conclusions: betamethasone had a negative effect on the gain of weight of matrices, fetuses and placentas when administered repeatedly and continuousy after the second half of pregnancy.
Corticosteroids; Respiratory distress syndrome; Prematurity
Trabalhos Originais
Efeitos da Betametasona sobre os Fetos e Placentas da Rata Albina.
Effects of Betamethasone on the Fetuses and Placentas of Female Albino Rats.
Eduardo de Souza, Manuel J. Simões, Luiz Camano, Luiz Kulay Júnior
RESUMO
Objetivos: analisar os efeitos da betametasona sobre o binômio materno-fetal da rata albina.
Métodos: utilizamos 60 ratas albinas prenhes divididas ao acaso em três grupos numericamente iguais. As ratas do grupo I foram tratadas com betametasona na dose de 1 mg/kg de peso em 0,5 ml de água destilada, por via intramuscular no 11o, 12o, 18o e 19o dia de prenhez; as do grupo II receberam 0,5 ml de água destilada, por via intramuscular no 11o, 12o, 18o e 19o dia de prenhez, e as do grupo III não receberam qualquer fármaco ou veículo. O ganho de peso das matrizes foi avaliado nos dias 0, 7, 14 e 20 de prenhez, sendo que no 20o dia todos os animais foram sacrificados por decapitação. Foram quantificados o número de implantações, de reabsorções, de fetos, de placentas, de malformações maiores, de mortalidade materna e fetal, assim como o peso dos fetos e das placentas.
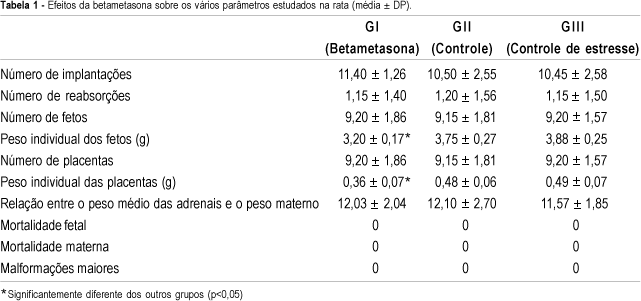
Resultados: nossos resultados revelaram que as matrizes tratadas com betametasona apresentaram menor ganho de peso. Quanto aos fetos e as placentas do grupo tratado, observamos que os pesos foram inferiores aos dos outros grupos. A média de peso dos fetos foi de 3,20 g contra 3,75 g no grupo controle. A média de peso das placentas foi de 0,36 g no grupo tratado com betametasona contra 0,48 g no grupo controle. Todas estas diferenças foram estatisticamente significantes.
Conclusões: a betametasona apresenta efeito negativo sobre o ganho de peso das matrizes, fetos e placentas, quando administrada de forma repetitiva a partir da segunda metade da prenhez.
PALAVRAS-CHAVE: Corticóides. Síndrome do desconforto respiratório. Prematuridade.
Introdução
A corticoterapia materna tem sido utilizada em gestantes com risco de parto prematuro, para promover a aceleração da maturidade pulmonar fetal. Coube a Liggins1 relatar observação preliminar da ação do hormônio adenocorticotrófico na aceleração da maturidade pulmonar de crias prematuras de ovelhas. Posteriormente, Liggins e Howie2, realizando estudo randômico duplo-cego em humanos, observaram que a betametasona e a cortisona reduziram não só a incidência da síndrome de desconforto respiratório (SDR), como também a mortalidade neonatal. Tais fatos foram bem evidentes, quando a ministração dos fármacos ocorreu entre 24 horas e sete dias antes do parto e em grávidas com idade gestacional inferior a 33 semanas. O Collaborative Group on Antenatal Steroid Therapy3 e Crowley et al.4 trabalhando com grupos maiores, porém usando a mesma metodologia de Liggins e Howie2, quantificaram em 50% a diminuição da SDR e apontaram que os melhores resultados sempre coincidiam com a ultimação do parto entre a 30a e a 34a semana da gestação.
Vencida a fase inicial em que o benefício sobrepujou o custo, as investigações prosseguiram. No que diz respeito à idade gestacional, foi comprovado sucesso, já a partir da 24a semana, tanto para acelerar a maturidade pulmonar3,5-7, quanto para reduzir a incidência de hemorragia intra e periventriculares do concepto4,5,7,8. Com relação à associação de medicamentos há autores que prescrevem o uso concomitante de corticóides e tocolíticos9 ou surfactante exógeno8, a fim de diminuir a morbimortalidade neonatal. Na vigência da rotura prematura de membranas, porém, as opiniões continuam bastante controvertidas4,10.
Baseado na literatura e nos achados de Crowley11, fruto de intensa pesquisa realizada entre 1972-1994, os National Institutes of Health dos Estados Unidos reconheceram os efeitos positivos da corticoterapia materna em recém-nascidos prematuros com 24-33 semanas de vida intra-uterina, recomendando o seu uso independentemente do sexo fetal, da disponibilidade de surfactante e de tocolíticos12.
Embora os trabalhos venham demonstrando que no humano os efeitos da betametasona são benéficos, no campo da experimentação animal foram mostrados efeitos adversos, como: redução da circunferência do pólo cefálico, do peso das supra-renais e do timo, assim como o aumento do peso do fígado13,14.
Diante de tais evidências, considerando a importância e os múltiplos aspectos da corticoterapia na prematuridade, apreciamos a ação da betametasona sobre o número de implantações, de reabsorções, de fetos, de placentas, de malformações maiores, de mortalidade materna e fetal, assim como o peso dos fetos, das placentas e das matrizes durante a prenhez da rata.
Material e Métodos
Utilizamos para a presente pesquisa ratas albinas (Rattus norvegicus albinus, Rodentia, Mammalia), da linhagem EPM-1 Wistar, oriundas do Biotério Central da Universidade Federal de São Paulo/Escola Paulista de Medicina, adultas, virgens, com aproximadamente 90 dias de idade, sob regime de alimentação normal (ração Purina Labina) e água ad libitum.
Todos os animais foram mantidos em gaiolas de poliuretano medindo 45 x 30 x 15 cm de comprimento, largura e altura respectivamente, contendo cinco ratas cada. A temperatura ambiente era de aproximadamente 22ºC. A iluminação era artificial com uso de lâmpadas fluorescentes (modelo Luz do Dia) de 400 watts, sendo o período de luz das 7:00 às 19:00 horas. As fêmeas foram acasaladas na proporção de duas para cada macho por um período de 12 horas, durante o fotoperíodo escuro. O início da prenhez foi determinado pelo encontro de espermatozóides na vagina da rata. Este foi considerado o dia zero da prenhez.
Sessenta ratas com teste de prenhez positivo foram distribuídas aleatoriamente em três grupos numericamente iguais, a saber: grupo I (GI) - 20 ratas tratadas com 1 mg/kg de peso corporal de betametasona em 0,5 ml de água destilada, por via intramuscular (IM), no 11o, 12o, 18o e 19o dia de prenhez (grupo experimental); grupo II (GII) - 20 ratas que receberam 0,5 ml de água destilada, IM, no 11o, 12o, 18o e 19o dia de prenhez (grupo controle), e grupo III (GIII) - 20 ratas que não receberam qualquer fármaco ou veículo do fármaco (grupo controle de estresse). Todas as injeções foram aplicadas entre 9:00 e 10:00 horas. Os animais foram mantidos em número de cinco por gaiola, tendo sido pesados individualmente nos dias zero, 7, 14 e 20 de prenhez, entre 8:00 e 9:00 horas.
As matrizes foram decapitadas em guilhotina entre 9:00 e 10:00 horas do 20o dia de prenhez. O tempo decorrido entre a retirada da rata da gaiola e sua decapitação foi sempre inferior a 30 segundos. De imediato os animais foram submetidos a laparotomia com incisão xifopúbica longitudinal mediana, expondo os órgãos internos. Rapidamente os cornos uterinos foram abertos para extração dos fetos, das placentas, contagem dos sítios de implantação e de reabsorção. As crias e as placentas foram pesadas separadamente em balança eletrônica de precisão (Gehaka-BG 1000).
Para a análise dos dados, foram realizadas análises paramétricas e não-paramétricas, sendo o nível de rejeição para a hipótese de nulidade fixado em 0,05 ou 5%. Múltiplas comparações foram feitas pelo teste de Kruskal-Wallis e análise de variância.
Resultados
Os nossos resultados estão expressos na Figura 1 e na Tabela 1. A Figura 1 ilustra o ganho de peso materno durante a gestação. A análise estatística revelou que as ratas tratadas com betametasona (GI) dia exibiram, a partir do 14o dia, ganho de peso significantemente menor, quando comparadas com as dos grupos controles (GII e GIII). A Tabela 1 mostra que houve redução significante dos pesos individuais dos fetos e das placentas no grupo tratado (GI) quando comparado aos demais (GII e GIII). Outros parâmetros analisados, como o número de implantações, de reabsorções, de fetos, de placentas, de malformações maiores, de mortalidade materna e fetal, não apresentaram diferenças estatisticamente significantes.
Discussão
Embora a corticoterapia materna venha sendo utilizada com sucesso para acelerar a maturidade pulmonar fetal há cerca de 30 anos, alguns aspectos ainda não estão bem esclarecidos. Assim, o objetivo do presente estudo foi expor o concepto da rata a betametasona, em dose dez vezes maior do que a recomendada para a gestante, com a finalidade de apreciar os efeitos das doses repetitivas.
Inicialmente podemos dizer que nas ratas tratadas (GI) não foram encontrados sinais da síndrome de Cushing iatrogênica, descrita com freqüência nas gestantes15; as matrizes, pelo contrário, tiveram menor ganho de peso, estatisticamente significante quando comparado com os dois grupos controles (GII e GIII). Para perfazer o intervalo de sete dias entre as duas aplicações, iniciamos o tratamento a partir da segunda metade da prenhez; na rata este intervalo de tempo corresponde ao final do período embriogênico e todo o período fetal16. Não foram anotadas, porém, entre as crias do grupo I fenda palatina ou lábio leporino13; é preciso dizer que no 10o dia já se completou a penetração do mesoderma nos sulcos e já houve integração tecidual entre o processo nasal medial e o ramo maxilar, sendo, portanto, o término da formação tanto do palato quanto dos lábios17.
O peso dos fetos e das placentas dos animais tratados com betametasona foi estatisticamente menor quando comparado àqueles dos grupos controles. A literatura refere que a betametasona, consideradas doses semelhantes por nós ministradas, pode determinar menor ganho de peso dos fetos e de alguns de seus órgãos, como coração, fígado, pulmões e cérebro17,18, resultando em retardo de crescimento19.
Ora, sabemos que os glicocorticóides têm ação bastante ampla e variada. Reduzem a captação e utilização da glicose, determinando hiperglicemia e indução das enzimas da neoglicogênese; conseqüentemente, ocorre lipólise e catabolismo protéico20. Promovem também a diminuição da proliferação de capilares e restringem o aporte de leucócitos e fibroblastos reduzindo a síntese de colágeno20. Não bastasse isso, ainda estimulam a proteína ativadora do fator de transcrição (AP1) envolvida com vários genes, inclusive da colagenase21. Deve ser referido ademais que os hormônios deste grupo têm efeito depressor sobre o DNA, inibindo sua síntese e divisão celular20,22. A par desta multiplicidade de ações não é difícil justificar o baixo peso das crias e das placentas no termo da prenhez, como também, o pouco ganho de peso das matrizes do grupo I aferido a partir do 14º dia de prenhez.
Votando ao exercício diário da clínica é preciso lembrar que, embora seja difícil extrapolar os nossos resultados - a redução do ganho de peso das matrizes, como também dos fetos e das placentas - para o gênero humano, fica a recomendação do uso cauteloso do corticóide antenatal, principalmente quando for repetitivo.
SUMMARY
Purpose: to analyze the effect of betamethasone on the pregnancy of rats.
Methods: thirty pregnant rats were divided into three groups of ten animals each. Group I ¾ the animals received betamethasone IM (1 mg/kg body weight, in 0.5 ml distilled water) on the 11th, 12th, 18th and 19th day of pregnancy. Group II ¾ the rats received distilled water (0.5 ml) IM on the 11th, 12th, 18th and 19th day of pregnancy. Group III - the rats did not receive any drug or vehicle. The animals were weighed on days 0, 7, 14 and on the 20th of pregnancy, and on the last day of weighing, the animals were sacrificed. The number of implantations, resorptions, fetuses, placentas, malformations, maternal and fetal mortality as well as the weight of the fetuses and placentas were obtained and analyzed.
Results: our results show that the rats treated with betamethasone gained significantly less weight. Their fetuses had an average weight of 3.2 g compared with 3.75 g in the control group. The results regarding placental weight were 0.36 g vs 0.48 g, respectively. All these differences were statistically significant.
Conclusions: betamethasone had a negative effect on the gain of weight of matrices, fetuses and placentas when administered repeatedly and continuousy after the second half of pregnancy.
KEY WORDS: Corticosteroids. Respiratory distress syndrome. Prematurity.
Referências
Disciplina de Obstetrícia - Departamento de Tocoginecologia da Universidade Federal de São Paulo/Escola Paulista de Medicina, São Paulo.
Correspondência:
Luiz Kulay Júnior
Hospital São Paulo, Disciplina de Obstetrícia
Rua Napoleão de Barros, 715; 8º andar
04024-002 ¾ São Paulo ¾ SP ¾ Brasil
- 1. Liggins GC. Premature delivery of foetal lambs infused with glucocorticoids. J Endocrinol 1969; 45:515-23.
- 2. Liggins GC, Howie RN. A controlled trial of antepartum glucocorticoid treatment for prevention of the respiratory distress syndrome in premature infants. Pediatrics 1972; 50:515-25.
- 3. Effect of antenatal dexamethasone therapy on the prevention of respiratory distress syndrome. Am J Obstet Gynecol. 1981; 141:276-87.
- 4. Crowley P, Chalmers I, Keirse MJ. The effects of corticosteroid administration before preterm delivery: an overview of the evidence from controlled trials. Br J Obstet Gynaecol 1990; 97:11-25.
- 5. Gunkel JH, Mitchell BR. Observational evidence for the efficacy of antenatal steroids from randomized studies of surfactant replacement. Am J Obstet Gynecol 1995; 173:281-5.
- 6. Horbar JD. Antenatal corticosteroid treatment and neonatal outcomes for infants 501 to 1500 gm in the Vermont-Oxford Trials Network. Am J Obstet Gynecol 1995; 173: 275-81.
- 7. Shankaran S, Bauer CR, Bain R, Wright LL, Zaxhary J. Relationship between antenatal steroid administration and grades III and IV intracranial hemorrhage in low birth weight infants. The NICHD Neonatal Research Network. Am J Obstet Gynecol 1995; 173:305-12.
- 8. Farrell EE, Silver RK, Kimberlin LV, Wolf ES, Dusik JM. Impact of antenatal dexamethasone administration on respiratory distress syndrome in surfactant-treated infants. Am J Obstet Gynecol 1989; 161:628-33.
- 9. Piper JM, Atkinson MW, Mitchel EF Jr, Cliver SP, Snowden M, Wilson SC. Improved outcomes for very low birth weight infants associated with the use of combined maternal corticosteroids and tocolytics. J Reprod Med 1996; 41:692-8.
- 10.Ohlsson A. Treatments of preterm premature rupture of the membranes: a meta-analysis. Am J Obstet Gynecol 1989; 160:890-906.
- 11.Crowley PA. Antenatal corticosteroid therapy: a meta-analysis of the randomized trials. 1972 to 1994. Am J Obstet Gynecol 1995; 173:322-35.
- 12.National Institutes of Health. The effect of antenatal steroids for fetal maturation on perinatal outcomes. Consensus Statement 1994; 212: 1-24.
- 13.Johnson JW, Mitzner W, London WT, Palmer AE, Scott R. Betamethasone and the rhesus fetus: multisystemic effects. Am J Obstet Gynecol 1979; 133:677-84.
- 14.Taeusch HW Jr. Glucocorticoid prophylaxis for respiratory distress syndrome: a review of potential toxicity. J Pediatr 1975; 87:617-23.
- 15.Baxter JD, Rousseau G. Glucocorticoid hormone action. Monographs on endocrinology. Berlin: Springer Verlag; 1979. v.2.
- 16.Stockard CR. The influence of the alcohol and other anesthetics on embryonic development. Am J Anat 1910; 10:369-92.
- 17.Stark RB. The pathogenesis of harelip and cleft palate. Plast Reconstr Surg 1954; 13: 20-5.
- 18.Carlos RQ, Seidler FJ, Slotkin TA. Fetal dexamethasone exposure alters macromolecular characteristics of rat brain development: a critical period for regionally selective alterations? Teratology 1992; 46:45-59.
- 19.Schimmer BP, Palmer KL. Hormônio adrenocorticotrófico; esteróides adrenocorticais e seus análogos sintéticos; inibidores da síntese e das ações dos hormônios adrenocorticais. In: Hardman JG, Limbird LE, editores Goodman & Gilman As Bases Farmacológicas da Terapêutica. 9a ed. Rio de Janeiro: McGraw Hill; 1996. p. 1095.
- 20.Rang HP, Dale MM, Ritter M. Pharmacology. 3a ed. Edhinburgh: Churchill Livingstone; 1995. p.438-42.
- 21.Barnes PJ, Adcok I. Anti-inflammatory actions of steroids: molecular mechanism Trends Pharmacol Sci. 1993; 14:436-41.
- 22.Slotkin TA, Seidler FJ, Kavlock RJ, Bartolome JV. Fetal dexamethasone exposure impairs cellular development in neonatal rat heart and kidney: effects on DNA and protein in whole tissues. Teratology 1991; 43:301-6.
Datas de Publicação
-
Publicação nesta coleção
25 Jun 2003 -
Data do Fascículo
Mar 2001