Resumos
A interpretação das alterações encontradas na necropsia é uma etapa importante para o sucesso do diagnóstico final. Este trabalho tem como objetivo descrever e ilustrar os aspectos anatômicos, não lesões, artefatos, lesões sem significado clínico e alterações post mortem encontradas em suínos domésticos e selvagens. Além disso, também se recomenda técnicas de colheita de tecidos para o diagnóstico de doenças que acometem essa espécie. Os principais aspectos anatômicos e não lesões descritos são fímbrias linguais, quadrilátero esofágico, toro pilórico e demarcação do padrão lobular do fígado (sistema gastrintestinal); tonsilas do palato mole, tecido linfoide associado ao estômago, placas de Peyer do intestino delgado e dobras da margem do baço (sistema hematopoiético); mediastino proeminente do testículo e aréolas da placenta (sistema reprodutor); atelectasia pulmonar e apêndice decidual (feto); e glândulas carpais (sistema tegumentar). Os artefatos de eutanásia abordados são petéquias na superfície do pulmão e rim, falsa anemia por sangria, hemorragia subdural por concussão cerebral, pseudo-infartos do baço e aspecto cerebriforme do intestino delgado. As lesões de pouco significado clínico descritas são cistos renais, linfonodos com pigmento de ferro, papilomas e hemangiomas no escroto, ossos no mesentério e hiperemia da mucosa gástrica. As alterações post mortem comumente encontradas são livor mortis, músculos pálidos, pseudomelanose e líquido serosanguinolento nas cavidades torácica e abdominal em fetos.
Necropsia; não lesões; macroscopia; suíno; javali; Sus scrofa
The interpretation of the changes observed at necropsy is an important step for the success of the final diagnosis. This article aims to describe and illustrate the anatomical structures, non-lesions, artifacts, lesions without clinical significance and postmortem changes observed in domestic and wild pigs. Moreover, the article also recommends collection techniques of organs or structures for the diagnosis of diseases affecting this species. The main anatomical structures and non-lesions described are marginal lingual papillae, pars oesophagea of the stomach, torus pyloricus, and well demarcated lobular pattern of the liver (gastrointestinal system); tonsils of the soft palate, gastric lymphoid tissue, Peyer's patches of the small intestine, marginal folds of the spleen (hematopoietic system); prominent mediastinum testis and placental areolae (reproductive system); pulmonary atelectasis and periople (fetus); and carpal glands (integumentary system). The discussed artifacts related to euthanasia are petechiae on the surface of the lung and kidney, false anemia due to exsanguination, subdural hemorrhage due to cerebral concussion, pseudoinfarcts of the spleen, and cerebriform appearance of the small intestine. Lesions without clinical significance described are renal cysts, lymph nodes with iron pigment, papillomas and hemangiomas on the scrotum, osseous metaplasia in the mesentery, and hyperemia of the gastric mucosa. Commonly found postmortem changes are livor mortis, pale muscles, pseudomelanosis, and serosanguinous fluid in the thoracic and abdominal cavities of fetuses.
Necropsy; non-lesions; gross pathology; swine; wild boar; Sus scrofa
ANIMAIS DE PRODUÇÃO
Nem tudo que parece ser, é lesão: aspectos anatômicos, não lesões, artefatos, lesões sem significado clínico e alterações post mortem encontrados na necropsia de suínos domésticos e selvagens (Sus scrofa)
Not everything is an important lesion: anatomical structures, non-lesions, artifacts, lesions without clinical significance, and postmortem findings in domestic and feral pigs (Sus scrofa)
Raquel R. RechI,* * Autor para correspondência: raquel.rech@embrapa.br ou keka_rrr@yahoo.com.br ; Marcia C. da SilvaII; Ingeborg M. LangohrIII; Mariana G. MarquesI; Caroline A. PescadorIV; Gustavo S. SilvaIV; Maurício C. DutraV; Juliana S. BrumVI; Beatris KramerI; Luiz C. BordinI; Virginia S. SilvaI
IEmbrapa Suínos e Aves, BR-153 Km 110, Vila Tamanduá, Concórdia, SC 89700-000, Brasil
IICentro de Diagnóstico de Sanidade Animal (CEDISA), BR-153 Km 110, Concórdia, SC 89700-000
IIIDepartment of Pathobiological Sciences, School of Veterinary Medicine, Louisiana State University, 1909 Skip Bertman Drive, Baton Rouge, LA 70803, USA
IVLaboratório de Patologia Veterinária, Universidade Federal do Mato Grosso, Av. Fernando Corrêa da Costa 2367, Coxipó, Cuiabá, MT 78069-900, Brasil
VPrograma de Pós-Graduação em Epidemiologia Experimental, Departamento de Medicina Veterinária Preventiva e Saúde Animal, Av. Prof. Orlando Marques de Paiva 87, Cidade Universitária, São Paulo, SP 05508-270, Brasil
VIPrograma de Pós-Graduação em Medicina Veterinária, área de concentração em Patologia Veterinária, Centro de Ciências Rurais, Universidade Federal de Santa Maria, Camobi, Santa Maria, RS 97105-900, Brasil
RESUMO
A interpretação das alterações encontradas na necropsia é uma etapa importante para o sucesso do diagnóstico final. Este trabalho tem como objetivo descrever e ilustrar os aspectos anatômicos, não lesões, artefatos, lesões sem significado clínico e alterações post mortem encontradas em suínos domésticos e selvagens. Além disso, também se recomenda técnicas de colheita de tecidos para o diagnóstico de doenças que acometem essa espécie. Os principais aspectos anatômicos e não lesões descritos são fímbrias linguais, quadrilátero esofágico, toro pilórico e demarcação do padrão lobular do fígado (sistema gastrintestinal); tonsilas do palato mole, tecido linfoide associado ao estômago, placas de Peyer do intestino delgado e dobras da margem do baço (sistema hematopoiético); mediastino proeminente do testículo e aréolas da placenta (sistema reprodutor); atelectasia pulmonar e apêndice decidual (feto); e glândulas carpais (sistema tegumentar). Os artefatos de eutanásia abordados são petéquias na superfície do pulmão e rim, falsa anemia por sangria, hemorragia subdural por concussão cerebral, pseudo-infartos do baço e aspecto cerebriforme do intestino delgado. As lesões de pouco significado clínico descritas são cistos renais, linfonodos com pigmento de ferro, papilomas e hemangiomas no escroto, ossos no mesentério e hiperemia da mucosa gástrica. As alterações post mortem comumente encontradas são livor mortis, músculos pálidos, pseudomelanose e líquido serosanguinolento nas cavidades torácica e abdominal em fetos.
Termos de indexação: Necropsia, não lesões, macroscopia, suíno, javali, Sus scrofa.
ABSTRACT
The interpretation of the changes observed at necropsy is an important step for the success of the final diagnosis. This article aims to describe and illustrate the anatomical structures, non-lesions, artifacts, lesions without clinical significance and postmortem changes observed in domestic and wild pigs. Moreover, the article also recommends collection techniques of organs or structures for the diagnosis of diseases affecting this species. The main anatomical structures and non-lesions described are marginal lingual papillae, pars oesophagea of the stomach, torus pyloricus, and well demarcated lobular pattern of the liver (gastrointestinal system); tonsils of the soft palate, gastric lymphoid tissue, Peyer's patches of the small intestine, marginal folds of the spleen (hematopoietic system); prominent mediastinum testis and placental areolae (reproductive system); pulmonary atelectasis and periople (fetus); and carpal glands (integumentary system). The discussed artifacts related to euthanasia are petechiae on the surface of the lung and kidney, false anemia due to exsanguination, subdural hemorrhage due to cerebral concussion, pseudoinfarcts of the spleen, and cerebriform appearance of the small intestine. Lesions without clinical significance described are renal cysts, lymph nodes with iron pigment, papillomas and hemangiomas on the scrotum, osseous metaplasia in the mesentery, and hyperemia of the gastric mucosa. Commonly found postmortem changes are livor mortis, pale muscles, pseudomelanosis, and serosanguinous fluid in the thoracic and abdominal cavities of fetuses.
Index terms: Necropsy, non-lesions, gross pathology, swine, wild boar, Sus scrofa.
INTRODUÇÃO
Uma necropsia bem realizada fornece informações importantes sobre as doenças. Em doenças de rebanho, essas informações podem direcionar as medidas terapêuticas e profiláticas para o seu controle e erradicação. Além de realizar a necropsia sistemática, ou seja, seguir uma técnica de necropsia estabelecida para examinar todos os órgãos, o reconhecimento das alterações, a descrição e a possível interpretação das lesões são os pontos mais relevantes desta técnica. A interpretação das lesões macroscópicas é determinante para a escolha do material a ser enviado para o exame laboratorial e está diretamente relacionada ao sucesso do diagnóstico.
Uma das primeiras perguntas quando examinamos os órgãos é: isto é normal ou anormal? Dentro desse propósito, cada espécie tem suas particularidades anatômicas e devem ser reconhecidas pelo médico veterinário durante a necropsia. Além disso, alterações post mortem podem mascarar ou serem confundidas com lesões. Algumas lesões encontradas durante a necropsia podem ser causadas pelo método de eutanásia ou não ter correlação com o quadro clínico, ou seja, com o real problema a ser solucionado. Dr. John King, um patologista com mais de 50 anos de experiência, diz em seu livro de necropsia: "Nós geralmente alertamos os principiantes que a maioria das coisas vistas na necropsia se enquadra em uma das seguintes categorias: normal, artefato, alterações post mortem, lesões parasitárias e, por último, lesões importantes. Portanto, três das cinco alterações encontradas na necropsia geralmente não têm grande significado" (King et al. 2005).
Os objetivos deste trabalho são (1) familiarizar os médicos veterinários que realizam a necropsia com as particularidades anatômicas dos suínos (Sus scrofa), (2) auxiliar na localização de estruturas anatômicas durante a necropsia, caso seja necessária a sua colheita para diagnóstico, e (3) descrever as principais lesões sem significado clínico e alterações post mortem.
ASPECTOS ANATÔMICOS E NÃO LESÕES
Neste tópico serão abordados os aspectos anatômicos, a localização de algumas estruturas anatômicas e as não lesões, que são estruturas normais pouco conhecidas ou semelhantes a lesões, mas que ocasionalmente são interpretadas como tal. A descrição dessas estruturas será feita por sistemas.
Sistema gastrintestinal
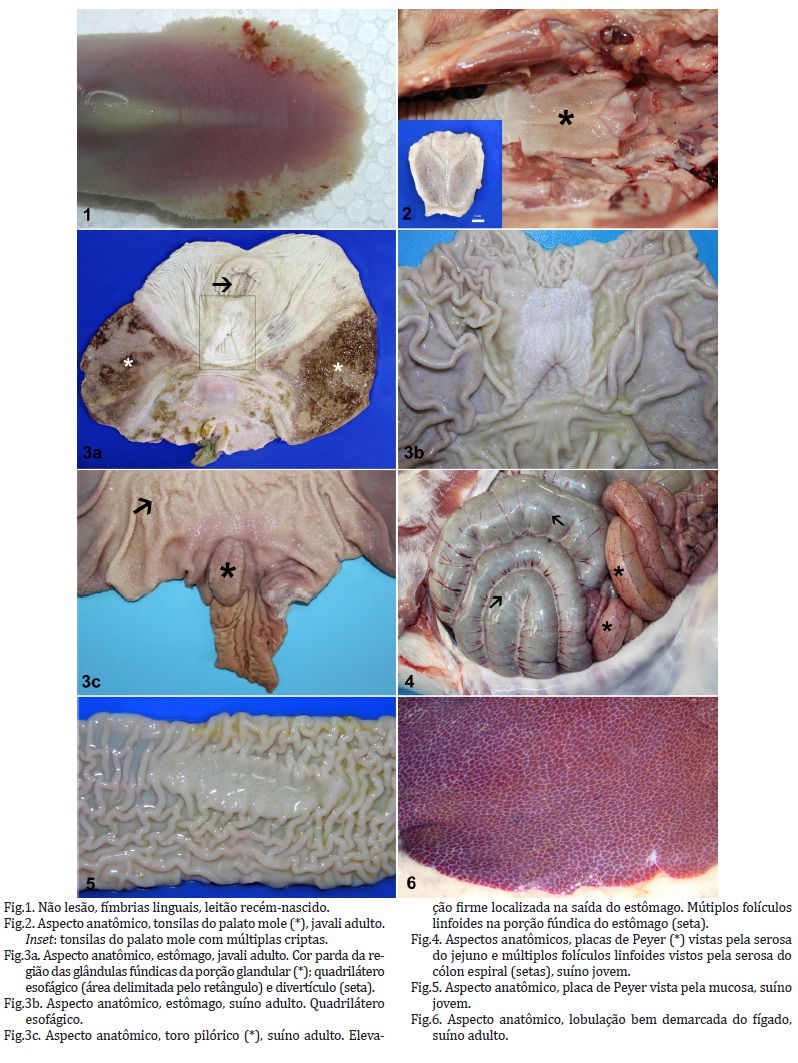
As fímbrias linguais são estruturas papilíferas salientes localizadas bilateralmente nas margens do terço proximal da língua de leitões recém-nascidos (Fig.1) (King et al. 2005). Essas fímbrias têm a função de auxiliar na sucção do leite durante a primeira semana de vida do leitão (Schneider et al. 1996) e depois desaparecem devido à fricção da língua na teta da porca. As fímbrias linguais podem ser erroneamente interpretadas como lesões de candidíase oral. Em caso de dúvida, a diferenciação é feita facilmente pelo exame histopatológico.
As tonsilas do palato mole são estruturas bilaterais ovaladas e achatadas que se localizam na porção caudal do palato mole (Fig.2). As tonsilas do palato mole fazem parte do tecido linfoide associado à mucosa (MALT - mucosa-associated lymphoid tissue) (Casteleyn et al. 2011). Na superfície das tonsilas há múltiplas reentrâncias que formam as criptas (inset Fig.2). O exame das tonsilas é necessário, pois na sua superfície é possível observar múltiplos pontos de necrose (tonsilite necrosante) na doença de Aujeszky (Sims & Glastonbury 1996) e na peste suína clássica (Fernández & White 2010). Esses pontos de necrose devem ser macroscopicamente diferenciados de abscessos, que são levemente elevados, em menor número e considerados lesão incidental (Sims & Glastonbury 1996).
O estômago dos suínos tem algumas estruturas peculiares. A região das glândulas fúndicas da mucosa é parda, em comparação às outras regiões que são claras (Fig.3a) (Getty 1981). A extremidade esquerda do estômago próxima ao cárdia apresenta um saco cego cônico denominado divertículo (Fig.3a) (Getty 1981). O quadrilátero esofágico ou pars oesophagea é a porção aglandular do estômago, composto por epitélio estratificado queratinizado e localizado próximo ao cárdia (Fig.3b). Essa área é suscetível à paraqueratose, erosões e úlceras. O toro pilórico ou torus pyloricus é uma elevação firme na superfície da porção pilórica em formato de castanha-do-pará (Fig.3c), que auxilia na regulação da abertura e fechamento do orifício pilórico (Bal & Ghoshal 1972). Devido ao seu formato, o toro pilórico pode ser erroneamente interpretado como neoplasma (leiomioma). Além disso, há múltiplos folículos linfoides no estômago dos suínos, observados como pequenos pontos levemente salientes na mucosa, localizados próximo ao quadrilátero esofágico e na parte fúndica da porção glandular (Fig.3c).
As placas de Peyer são agregados linfoides ovais ou em forma de cinta, localizadas no jejuno e íleo (Figs.4 e 5). Essas estruturas podem ser observadas tanto pela serosa quanto pela mucosa e são maiores e mais numerosas no íleo (Rothköter et al. 1990). Para manter as placas de Peyer inteiras para a observação macroscópica e exame histopatológico, deve-se abrir o intestino delgado pela borda mesentérica (Fig.5). A seleção de um segmento do intestino delgado com placas de Peyer é importante para o diagnóstico em casos de circovirose (Corrêa et al. 2006). Como as placas de Peyer podem ser observadas tanto no jejuno como no íleo, a diferenciação microscópica entre os três segmentos do intestino delgado pode ser um desafio para o patologista. Dessa forma, recomenda-se colher uma estrutura adjacente ao segmento de intestino delgado selecionado para exame, a fim de permitir a identificação correta do segmento sob o microscópio. Assim, aconselha-se colher o duodeno ligado a um fragmento de pâncreas, o íleo ligado ao linfonodo ileocólico e o jejuno separadamente.
Múltiplos agregados linfoides, observados macroscopicamente como focos circulares brancacentos com 4-6 mm de diâmetro, podem ser vistos no ceco e cólon de suínos (Fig.4), tanto pela serosa, quanto pela mucosa (King et al. 2005).
O fígado dos suínos tem a lobulação bem demarcada (Fig.6), diferentemente das outras espécies. Essa demarcação ocorre porque cada lóbulo é circundado por tecido conjuntivo, sendo mais proeminente em animais mais velhos e menos evidente em leitões jovens. Em função dessa característica, o fígado dos suínos é um pouco mais firme que o das outras espécies domésticas (Frappier 2006).
Sistema hematopoiético
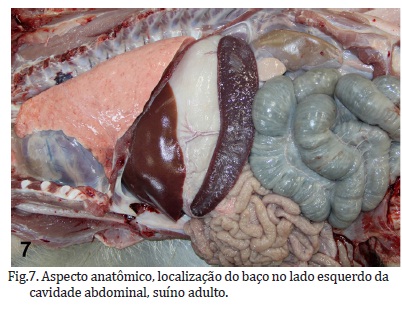
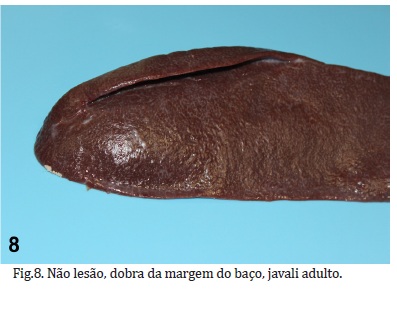
Além das tonsilas do palato mole (Fig.2), folículos linfoides do estômago (Fig.3c), ceco e cólon (Fig.4) e placas de Peyer (Fig.4 e 5), que são todos tecidos linfoides associados à mucosa (MALT), os outros órgãos linfoides dos suínos são baço, linfonodos e timo. O timo em fetos e suínos jovens se estende caudalmente desde a origem do músculo digástrico, ao longo das artérias carótidas em ambos os lados do pescoço até a entrada do tórax onde os lados direito e esquerdo parecem se fundir (ver Fig.34) e involui completamente após um ano de idade (Getty 1981). O baço é alongado e localiza-se dorsoventralmente no lado esquerdo da cavidade abdominal. Para visualizá-lo durante a abertura da cavidade abdominal, sugere-se realizar a necropsia de suínos em decúbito lateral direito (Fig.7), já que macroscopicamente o baço pode apresentar lesões visíveis em doenças importantes, como infartos na peste suína clássica, salmonelose, erisipela (Sims & Glastonbury 1996) e circovirose (Corrêa et al. 2006) e esplenomegalia acentuada na peste suína africana (Fernández & White 2010), esta última erradicada do Brasil desde 1984 (Tokarnia et al. 2004). Uma não lesão encontrada no baço são as dobras ou pregas das margens (Fig.8), que podem estar aderidas à cápsula. O baço deve sempre ser analisado microscopicamente em suínos porque a ausência de lesões macroscópicas não necessariamente significa ausência de lesões microscópicas (Sims & Glastonbury 1996).
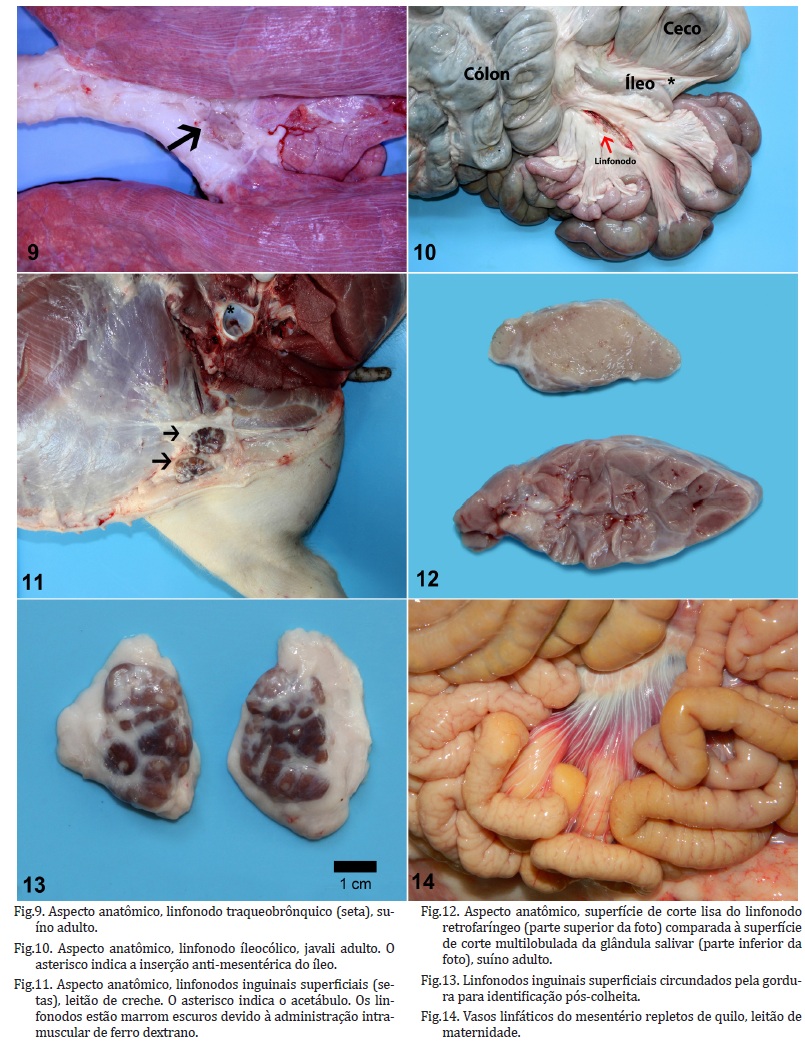
Os principais linfonodos dos suínos que devem ser consistemente analisados durante a necropsia são os retrofaríngeos, traqueobrônquicos e mediastínicos, mesentéricos e inguinais superficiais. Durante a necropsia é necessário localizar os principais linfonodos (Figs.9-11), bem como diferenciá-los de estruturas adjacentes. Um exemplo é a confusão que se faz entre os linfonodos retrofaríngeos laterais e as glândulas salivares parótidas, pois ambos se localizam na porção caudal do arco da mandíbula. Para evitar essa confusão deve-se observar a superfície de corte de ambas as estruturas (Fig.12).
Independente da localização, todos os linfonodos apresentam morfologia idêntica ao exame microscópico. Assim, para auxiliar na identificação pelo patologista, recomenda-se colher os linfonodos com estruturas adjacentes. Para isso, os linfonodos mesentéricos devem ser colhidos junto com uma porção dos vasos do mesentério adjacente. Os linfonodos retrofaríngeos devem ter um fragmento da glândula salivar ou do músculo esquelético adjacente. Os linfonodos traqueobrônquicos e mediastínicos devem ser colhidos com um fragmento de traqueia ou brônquio adjacente. O linfonodo inguinal superficial deve ser colhido com a gordura que o circunda (Fig.13).
A análise sistemática dos linfonodos e a observação da superfície de corte permite suspeitar de doenças como a circovirose e a micobacteriose, com aumento de volume dos linfonodos (Corrêa et al. 2006) e formação de concreções cáseo-calcárias (Sims & Glastonbury 1996), respectivamente. Ainda, hemorragia é observada em casos de peste suína clássica e peste suína africana (Fernandez & White 2010, Gabriel et al. 2011).
Sempre que possível, convém colher linfonodos inteiros para exame histopatológico, pois o sentido em que o linfonodo é seccionado pode interferir na observação microscópica pelo patologista. Recomenda-se cortar os linfonodos longitudinalmente, evitando cortes tangenciais que podem prejudicar a visualização dos folículos linfoides durante o exame microscópico (Sims & Glastonbury 1996). É oportuno salientar que microscopicamente os linfonodos dos suínos têm a arquitetura invertida: o córtex é central e a medula é periférica.
Os vasos linfáticos do mesentério podem ficar brancacentos e proeminentes em leitões após a ingestão de leite (Fig.14). O aspecto brancacento dos vasos linfáticos do mesentério se deve à presença de quilo por causa da absorção de gordura (Sims & Glastonbury 1996). Essa alteração fisiológica não deve ser confundida com a linfangiectasia e linfangite observada na circovirose. Nesses casos, a linfangiectasia é acompanhada de linfadenomegalia e edema do mesentério (Langohr et al. 2010).
Sistema musculo-esquelético
Fossas sinoviais são depressões normais da superfície articular de ossos longos, especialmente na extremidade distal da escápula, úmero, rádio e carpo intermédio e na extremidade proximal do rádio. Quando presentes, geralmente são bilaterais e simétricas e localizadas nas áreas côncavas do osso que não suportam peso. Fossas sinoviais estão ausentes em leitões neonatos e aparecem em suínos após 5-6 meses de idade (Doige & Horowitz 1975). Essas depressões não devem ser confundidas com lesões de osteocondrose dissecans.
Sistema nervoso
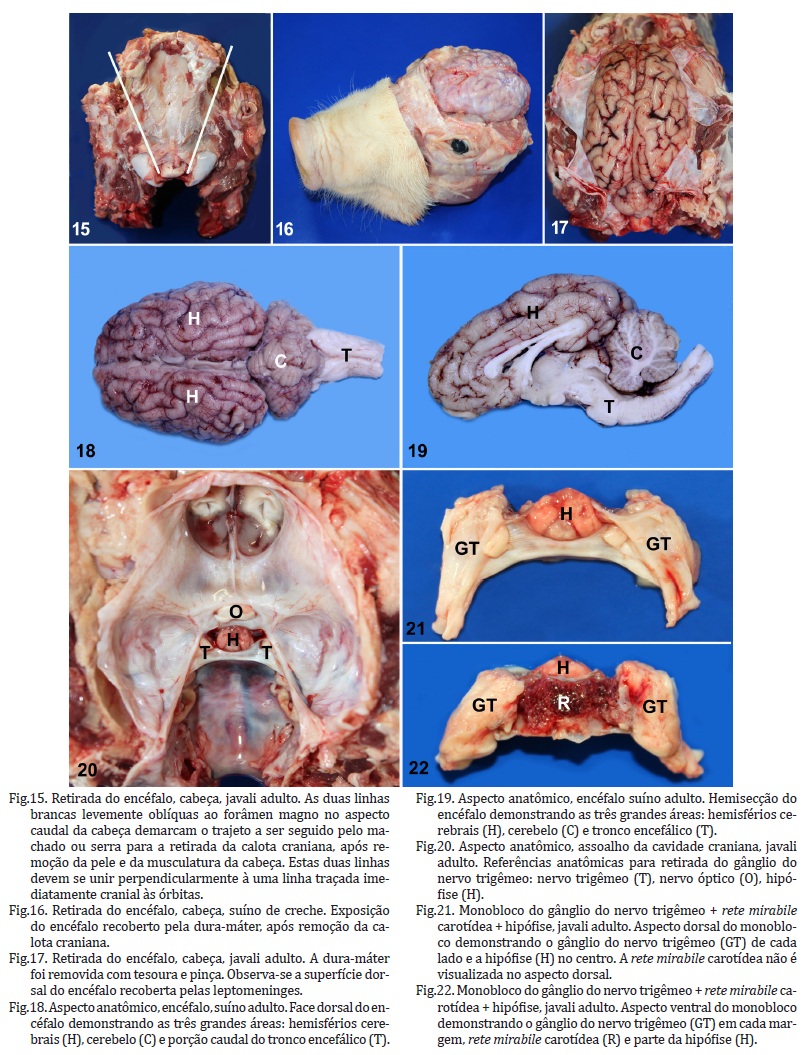
Um dos maiores desafios para os médicos veterinários é a retirada do encéfalo íntegro da cavidade craniana, assim como a remoção da medula espinhal e a localização e remoção do par de gânglios do nervo trigêmeo e gânglios sacrais. Como a maioria das doenças neurológicas em suínos não apresenta lesão macroscópica, a remoção e o envio dessas estruturas para o laboratório é essencial para o diagnóstico. Para retirar o encéfalo é necessário desarticular a cabeça, desfazendo a articulação atlanto-occipital. Após dissecar a pele e remover os músculos da cabeça, deve-se serrar ou cortar os ossos da cavidade craniana (Fig.15 e 16) com o auxílio de uma serra ou machado. Após cortar a dura-máter com uma tesoura (Fig.17) (preferencialmente limpa e desinfetada), este é o momento apropriado para a colheita de amostras com suabes, especialmente se há suspeita de meningite bacteriana, geralmente causadas por Streptococcus suis ou Haemophilus parasuis (Summers et al. 1995). Recomenda-se passar o suabe não somente na superfície do telencéfalo (entre os hemisférios), mas também na base do encéfalo (tronco encefálico), pois o exsudato se acumula em maior quantidade na porção ventral do encéfalo (Summers et al. 1995) e as chances de isolar a bactéria do exsudato são maiores.
Após a retirada do encéfalo da cavidade craniana deve-se localizar as três grandes áreas anatômicas: telencéfalo ou hemisférios cerebrais, tronco encefálico e cerebelo (Fig.18 e 19). O reconhecimento dessas áreas é importante para localizar lesões no sistema nervoso central. Para o envio ao laboratório, geralmente se faz um corte longitudinal no encéfalo e se envia uma metade em formol tamponado a 10% para exame histopatológico (Fig.19) e a outra metade sob refrigeração para exames microbiológicos. Se a integridade do encéfalo for necessária para observar lesões bilaterais simétricas no exame histopatológico, especialmente na base do encéfalo (tálamo e tronco encefálico) (Oliveira et al. 2005, Casteignau et al. 2006), recomenda-se colher um quadrante cranial do telencéfalo sob refrigeração e colocar o restante do encéfalo em formol.
Com o encéfalo fora do crânio, é possível observar a localização do par de gânglios do nervo trigêmeo (ou de Gasser) no assoalho da cavidade craniana, de cada lado da hipófise (Fig.20). A colheita deste gânglio é importante porque é o local de latência do vírus de Aujeszky em suínos domésticos (Romero et al. 2003). A colheita do par de gânglios pode ser feita com bisturi ou com a ponta da faca (Fig.21 e 22). Um gânglio conectado com a hipófise deve ser acondicionado em formol a 10% para exame histopatológico e o outro refrigerado para exame virológico.
A colheita da medula espinhal é pouco comum na rotina de necropsia, mas deve ser feita sobretudo quando há suspeita de infecção por teschovirus suíno (Salles et al. 2011) e intoxicação por selênio (Casteignau et al. 2006). Para retirar a medula espinhal, deve-se remover a musculatura que circunda a coluna vertebral e cortar os processos espinhosos dorsais com um alicate de corte, serra ou machadinha. Após a exposição da porção dorsal da medula espinhal, deve-se segurar a dura-máter com uma pinça, elevar a medula espinhal dorsocaudalmente e cortar as raízes nervosas com tesoura. Dessa forma, a medula espinhal se desprende da coluna vertebral. Para examinar o parênquima da medula, deve-se fazer alguns cortes transversais nos segmentos cervical, torácico e lombar. Sempre que possível, a medula espinhal deve ser enviada inteira para melhor localização das lesões pelo patologista. Se optar por enviar diferentes segmentos da medula espinhal, estes devem ser identificados. Isso pode ser feito enviando os diferentes segmentos em frascos separados ou anotando com lápis em papel toalha cada segmento da medula, enrolando-a nos vários papeis identificados e imergindo-a em formol juntamente com os outros órgãos.
A colheita dos gânglios sacrais é laboriosa, pois envolve a retirada da cauda equina na porção lombossacral da medula espinhal. O exame dos gânglios sacrais é importante porque é o local de latência do vírus de Aujeszky em javalis, já que a transmissão do vírus nesses animais ocorre de forma venérea (Romero et al. 2003).
Sistema reprodutor feminino
Uma das etapas da investigação de causas de falhas reprodutivas consiste no exame do aparelho genital. Assim, o exame macroscópico dos ovários é fundamental para determinar se a fêmea estava ciclando e qual era o estágio do ciclo estral dela.
A identificação da fase do ciclo estral pode ser determinada pela presença de corpos lúteos e folículos no ovário. O ciclo estral na porca varia de 17 a 25 dias e apresenta uma fase lútea e uma fase folicular. Após a ovulação, considerado o primeiro dia do ciclo, ocorre o início da fase lútea. Os folículos que ovularam (4-5 mm) são preenchidos por sangue, formando o corpo hemorrágico (Fig.46), que é vermelho e apresenta uma pequena protuberância chamada estigma, onde ocorreu a ovulação (Senger 2003). As células tornam-se luteinizadas, formando o corpo lúteo (CL) e produzem progesterona (P4), que tem influência negativa sobre o crescimento de folículos, pois impede a secreção do hormônio folículo estimulante (FSH) e do hormônio luteinizante (LH), inibindo a secreção do hormônio liberador de gonadotrofinas (GnRH).
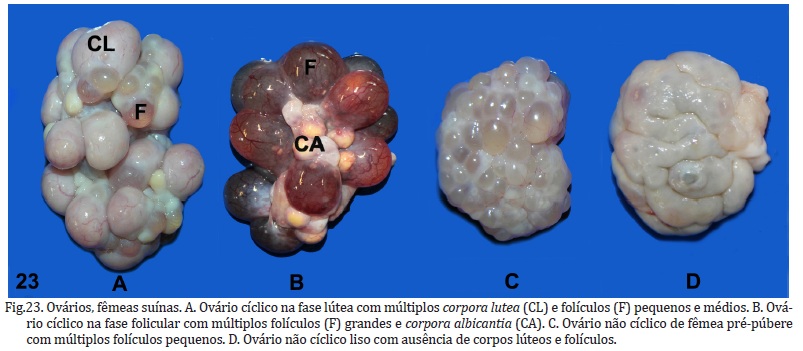
No início da fase lútea, imediatamente após a ovulação, as concentrações periféricas de P4 são mínimas e as concentrações de inibina e estrógeno diminuem, pois com a ovulação não existem mais folículos grandes (≥7 mm) no ovário. Assim, cessa a inibição à liberação de FSH. As maiores concentrações periféricas de FSH nos dias 1 e 2 após a ovulação induzem o início do desenvolvimento sincronizado de uma onda folicular e aumento do número de folículos de pequeno (<3 mm) e médio (3-6,9 mm) porte no ovário (Knox 2005). Posteriormente, a produção de inibina por estes folículos em crescimento reduz as concentrações periféricas de FSH (Soede et al. 2011). Nessa fase do ciclo, portanto, o ovário apresentará CL funcionais e folículos pequenos e médios (Fig.23a), sendo considerada a fase lútea do ciclo. Pelos dias 5 e 6 pós-ovulação, cada CL atinge a maturidade com 9-11 mm de diâmetro e a cavidade é completamente preenchida por células luteinizadas.
Em torno de 12 - 14 dias do ciclo estral, se a fêmea não está gestante, a prostaglandina F2α é liberada pelo útero e faz com que ocorra a regressão do CL (luteólise), formando o corpus albicans. Com isso, os níveis de P4 caem rapidamente e seu controle inibitório sobre o crescimento dos folículos é removido. O FSH promove o aumento do número de folículos que alcançam porte médio ou grande (recrutamento). O LH é necessário para o crescimento destes folículos ao tamanho pré-ovulatório (seleção) e posterior ovulação (Soede et al. 2011). Enquanto os folículos se desenvolvem, eles produzem estradiol, que aumenta de forma constante durante os últimos estágios do ciclo estral. Nessa fase podem ser observados CL não funcionais que regrediram (corpora albicantia) e folículos grandes com diâmetro médio de 7-8 mm (Fig.23b), sendo esta considerada a fase folicular do ciclo estral. Quando as concentrações de estradiol atingem um nível alto o suficiente, o pico pré-ovulatório de LH ocorre e segue a ovulação dos folículos grandes (Cardenas & Pope 2001). O estradiol também é responsável pelos sinais de cio como vulva inchada e hiperêmica, postura imóvel e orelhas eretas.
Fêmeas ciclando são aquelas que apresentam CLs ou corpora albicantia no ovário (Fig.23a,b). Fêmeas pré-púberes, consideradas não cíclicas, apresentam folículos de tamanhos pequenos e médios e ausência de CL (Fig.23c). Também são fêmeas não cíclicas as que apresentam ovários lisos e firmes (ausência de folículos e CL) (Fig.23d).
Sistema reprodutor masculino
O escroto do suíno está localizado imediatamente ventral ao ânus, de forma não pendular, o que leva essa espécie a ser mais suscetível do que outras às perturbações da espermatogênese durante a estação quente do ano (Youngquest & Threlfall 2007).
O testículo esquerdo é usualmente maior que o direito, com cerca de 0,5 cm de diâmetro de diferença entre eles (Clark et al. 2003) (Fig.24). O mediastino do testículo de suínos é proeminente (Fig.25), formado por tecido conjuntivo e pela rete testis. O denso tecido conjuntivo no mediastino previne o colapso da rete testis, facilitando o transporte dos espermatozoides (Senger 2003). O parênquima testicular é cinza a marrom-avermelhado (Fig.25) e escurece com o avançar da idade devido à pigmentação das células de Leydig (Sims & Glastonbury 1996).
A cauda do epidídimo é palpável e se localiza dorsalmente no escroto. Ao exame macroscópico é possível observar claramente o aumento de calibre dos túbulos na porção distal da cauda do epidídimo (Fig.26), sendo esta porção epididimária um importante reservatório de espermatozoides para o momento da ejaculação.
Os suínos possuem as seguintes glândulas sexuais acessórias: um par de vesículas seminais, próstata e um par de glândulas bulbouretrais (Fig.27). As glândulas vesiculares ou vesículas seminais são grandes, lobuladas e responsáveis pelo grande volume do ejaculado. A próstata é a menor de todas as glândulas anexas e está localizada ventrocaudalmente às glândulas vesiculares. As glândulas bulbouretrais são grandes e alongadas, situam-se na entrada pélvica interna e são responsáveis pela produção da fração gel característica do sêmen suíno (Youngquest & Threlfall 2007).
Feto e placenta
As falhas reprodutivas relacionadas ao abortamento em fêmeas suínas são comuns nas criações modernas, podendo ser de causa infecciosa (responsável por 30 a 40% dos casos) e não infecciosa (Maldonado et al. 2005). Parte do diagnóstico dessas falhas está diretamente relacionada à acurácia do exame macroscópico do feto, membranas fetais, placenta e útero (Fig.28 e 29) e na correta submissão de material ao laboratório.
As membranas fetais são compostas por âmnio, alantoide e córion. O córion é a contribuição fetal da placenta. A placenta, por sua vez, é um órgão transitório endócrino formado durante a gestação, composto por um componente fetal (o corioalantoide) e um componente materno derivado de modificações do endométrio uterino (Senger 2003). A placenta dos suínos é classificada como epiteliocorial difusa, de acordo com o número de camadas da placenta e a distribuição das vilosidades coriônicas, respectivamente. Isso quer dizer que o epitélio dos lados materno e fetal está intacto (epiteliocorial) e que a maior parte do saco coriônico está uniformemente unida ao endométrio por pregas e vilos, permitindo que as trocas fisiológicas aconteçam em toda a superfície (difusa) (Senger 2003).
A parte corioalantoide da placenta é a camada externa que envolve o feto (saco placentário) (Fig.29 e 30). O córion é a superfície vilosa em contato com o útero. O alantoide é a superfície lisa em contato com o âmnion. A maior parte do córion consiste em uma zona central grande com uma superfície aveludada composta por numerosas saliências que interdigitam com o endométrio, dobras transversais e numerosas aréolas (semelhantes a taças rasas) opostas à abertura das glândulas do endométrio uterino. As aréolas (inset Fig.28) são estruturas morfológicas normais importantes para a transferência de nutrientes para o feto, incluindo o ferro, que é necessário para a hematopoese fetal. A zona central é limitada em cada lado por zonas paraplacentárias caracterizadas por uma superfície lisa e brilhante, vasos sanguíneos longitudinais distintos e quase total ausência de aréolas. As extremidades do saco placentário (pontas necróticas) são bem demarcadas das zonas paracentrais por constrições. Estas extremidades são zonas isquêmicas, que muitas vezes são secas, enrugadas, endurecidas, marrom escuras e com aspecto pegajoso (Fig.30). As pontas necróticas apresentam normalmente 3-8cm de largura na região avascular entre um concepto e outro. Especula-se que estas zonas de isquemia nas pontas impedem a fusão de placentas adjacentes entre embriões nos dias 29 e 50 de gestação, período crítico para a prevenção do desenvolvimento de freemartin, que parece ser raro em suínos (Yaeger 2012).
A maioria das causas infecciosas de abortamento em suínos é de origem viral e quando há lesões, estas ocorrem no feto. Embora a placenta seja considerada essencial para o diagnóstico de abortamentos de etiologia bacteriana e/ou fúngica em várias espécies domésticas, essas causas em suínos são infrequentes. A submissão do saco placentário juntamente com os fetos tem valia diagnóstica em casos de abortamento por Brucella spp., Leptospira spp., clamídias, Nocardia spp. e outras bactérias que causam septicemia (Erysipelothrix rhusiopathiae, Salmonella enterica) (Yaeger 2012). Variações morfológicas normais na placenta de suínos não devem ser confundidas com lesões. Placas esbranquiçadas (Fig.31) macias podem ser observadas próximas à junção das membranas coriônicas e alantoides. Essas placas são depósitos de material mineralizado finamente granular, situados no estroma da placenta de fetos suínos normais nascidos a termo e não devem ser confundidas com lesões de abortamento de origem micótica. Pequenos cistos epiteliais (Fig.32) de 1 a 4mm são não lesões frequentemente observadas no interior ou logo abaixo da membrana coriônica (Long 1986).
Em abortos de origem infecciosa, o agente etiológico pode afetar apenas um leitão, mais de um leitão ou todos os leitões da leitegada (Yaeger 2012). Então, para ter sucesso no diagnóstico é recomendável necropsiar ou enviar ao laboratório quatro a seis fetos não mumificados e todos os mumificados da leitegada refrigerados. Durante a necropsia de fetos é possível observar as seguintes não lesões: apêndice decidual, fímbrias linguais (Fig.1) e espessura semelhante da parede dos ventrículos do coração. Apêndices deciduais (Fig.33) estão presentes nos membros torácicos e pélvicos com a finalidade de recobrir os cascos, protegendo o útero gravídico. A presença dos apêndices deciduais em leitões natimortos indica que estes tiveram morte pré e/ou intraparto. Adicionalmente, diferenciar macroscopicamente um natimorto de um neonato que morreu logo após o parto, requer o exame dos pulmões. Pulmões vermelhos escuros e que não flutuam quando imergidos em meio líquido correspondem à atelectasia congênita (Fig.34), o que é normal em um feto e esperado em um natimorto. Já o leitão que nasceu vivo e morreu logo após o parto tem os pulmões inflados por ar no momento do nascimento, e portanto, flutuam em meio líquido. Quando o pulmão e os outros tecidos flutuam em formol, indica que há putrefação post mortem de todos os tecidos, e a diferenciação entre natimorto e neonato que morreu logo após o parto fica prejudicada. Quando inspecionamos o coração de fetos e recém-nascidos, a parede do ventrículo esquerdo não apresenta diferença significativa quanto à espessura quando comparada à do ventrículo direito (Fig.35), já que a resistência vascular da circulação fetal sistêmica não é maior que a da pulmonar devido à existência do forame oval (comunicação interatrial).
Sistema respiratório
O conhecimento da divisão dos lobos pulmonares em suínos é importante para a descrição correta da localização e extensão das lesões. Com isso, o médico veterinário pode suspeitar da possível etiologia da lesão, bem como auxiliar o patologista na determinação da patogenia.
A literatura veterinária clínica de suínos (Sims & Glastonbury 1996, Van Alstine 2012, Sobestiansky & Barcellos 2012) considera que o pulmão é dividido em sete lobos: quatro no lado direito (cranial, médio, caudal e intermediário) e três no lado esquerdo (cranial, médio, caudal) (Fig.36). Os lobos cranial, médio, caudal e intermediário também são denominados apical, cardíaco, diafragmático e acessório, respectivamente (Getty 1981). Os anatomistas puristas descrevem os lobos cranial e médio esquerdos como sendo um único lobo, subdividido em duas porções: cranial e caudal (Getty 1981, Caswell & Williams 2007). Dessa forma, para os anatomistas, o lado esquerdo do pulmão tem apenas dois lobos (cranial e caudal) (Getty 1981).
Para a identificação de parasitas pulmonares (Metastrongylus spp.), especialmente em animais de vida livre como o javali, é necessário examinar os brônquios em toda a sua extensão, pois os parasitas geralmente estão localizados nas suas porções finais. Uma particularidade do pulmão dos suínos (e ruminantes) é que a ventilação do lobo cranial direito é suprida pelo ramo broncotraqueal (Fig.36). Em virtude disso, esse lobo está predisposto a lesões de origem aerógena (Caswell & Williams 2007).
Cada lobo pulmonar é dividido em múltiplos lóbulos bem demarcados por tecido conjuntivo, prontamente vistos na superfície pulmonar (Fig.37). Nos suínos, cada lóbulo é considerado uma unidade funcional completa e a comunicação entre lóbulos vizinhos é limitada (Caswell & Williams 2007). Essa característica anatômica é responsável pelo padrão macroscópico de tabuleiro de xadrez observado em pneumonia broncointersticial, particularmente as causadas por vírus influenza A e infecção aguda por Mycoplasma hyopneumoniae. Nesse tipo de padrão macroscópico, os lóbulos afetados são intercalados por lóbulos normais.
Uma não lesão raramente observada em suínos é a melanose congênita, desordem em que ocorre acúmulo excessivo do pigmento melanina. Esses acúmulos geralmente se apresentam como manchas pretas multifocais na superfície de órgãos como pulmão e fígado e penetram pouco no parênquima. Além disso, melanina pode ser encontrada nos linfonodos e glândula mamária (Herenda 1994). Melanose adquirida foi descrita em linfonodos de suínos Nero Siciliano que ingeriram frutos de árvores da família do carvalho (Lanteri et al. 2009). Melanose deve ser diferenciada de hemorragia (especialmente hematomas) e pseudomelanose (alteração post mortem). Quando a melanose estiver presente nos linfonodos, deve ser diferenciada de pigmento férrico e hemorragia.
Sistema tegumentar
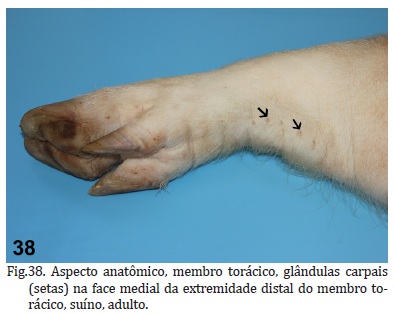
As glândulas carpais (Fig.38) são estruturas circulares, em número de cinco a sete, localizadas na região medial do carpo e presentes em suínos machos e fêmeas (Heise-Pavlov et al. 2005). Os orifícios observados macroscopicamente são recobertos por pelos e correspondem às aberturas de glândulas écrinas (Heise-Pavlov et al. 2005). Os orifícios dessas glândulas já foram confundidos com picada de cobra. As glândulas carpais secretam substâncias odoríferas (Heise-Pavlov et al. 2005) e antimicrobianas (Fukui et al. 2012). Em suínos de vida livre os orifícios dessas glândulas podem estar recobertos por acúmulo de secreção leitosa e transferi-la para a vegetação enquanto o animal se movimenta ou marcar o solo enquanto está em decúbito esternal (Heise-Pavlov et al. 2005). Por isso, acredita-se que as glândulas carpais estejam envolvidas no reconhecimento entre filhotes e mães e na comunicação intra e intergrupal (Heise-Pavlov et al. 2005).
Sistema urinário
Neonatos têm os tufos glomerulares congestos e dilatados, que macroscopicamente podem ser erroneamente interpretados como petéquias (Drolet 2012). Em neonatos também pode se observar persistência da lobulação fetal. Já em suínos adultos, a urina residual muitas vezes é branca e opaca (Sims & Glastonbury 1996).
ARTEFATOS
Os principais artefatos observados durante a necropsia de suínos são decorrentes de métodos de eutanásia. A eutanásia em suínos é geralmente realizada por concussão cerebral (em leitões jovens) ou eletrocussão (animais mais velhos) seguida de sangria (AVMA 2013, National Pork Board 2009). Em javalis, utiliza-se geralmente arma de fogo e como alvo, os grandes vasos da cavidade torácica, com esfacelamento de áreas focalmente extensas do pulmão e/ou coração e com hemorragia adjacente. Quando se realiza a concussão cerebral como método de eutanásia, observa-se múltiplas fraturas dos ossos do crânio, hemorragia subdural nos hemisférios cerebrais e esmagamento da massa encefálica, por vezes com fragmentos de ossos dentro do encéfalo. Petéquias multifocais podem aparecer na superfície do pulmão (Fig.39) e rins após a eutanásia por choque elétrico e devem ser diferenciadas de petéquias observadas em doenças importantes como a peste suína clássica (Fernández & White 2010). No momento da descarga elétrica, as contrações musculares podem ser tão fortes e seguidas de queda brusca do suíno, que em alguns casos pode ocorrer fratura da coluna vertebral (Alberton et al. 2012) (Fig.39) e fratura do colo do fêmur. Raramente, fraturas de vértebras lombossacrais são vistas em casos de descarga elétrica por raios (Van Alstine & Widmer 2003) e devem ser diferenciadas das causadas durante a eutanásia.
Para realizar a sangria geralmente secciona-se a artéria carótida e a veia jugular na altura da entrada do tórax (Herenda 1994). Ao cortar estes vasos, a traqueia pode ser acidentalmente seccionada e o sangue pode ser aspirado para o pulmão (Fig.40). Durante o processo de sangria pode haver distribuição irregular de sangue no baço, podendo as áreas com acúmulo de sangue dar a falsa impressão de infartos (Fig.41). Após a eutanásia e sangria, as vísceras adquirem aspecto pálido (Fig.42) e isso deve ser considerado durante a avaliação macroscópica quanto à cor. Se a necropsia é realizada logo após a eutanásia do suíno, como preconizado, o intestino delgado pode ainda exibir contrações musculares involuntárias e adquirir aspecto cerebriforme quando observado pela serosa (Fig.43), mimetizando a lesão de enterite proliferativa causada por Lawsonia intracellularis. Para diferenciar dessa lesão verdadeira, deve-se esticar o intestino delgado para ver se as dobras da mucosa se desfazem. Essas contrações involuntárias do intestino delgado podem também formar intussuscepção intestinal post mortem, especialmente em leitões (King et al. 2005). Ao contrário da intussuscepção ante mortem em que a área afetada apresenta hemorragia, edema e fibrina, não há reação tecidual na intussuscepção post mortem (Fig.44).
LESÕES SEM SIGNIFICADO CLÍNICO
Lesões sem significado são aquelas não importantes para a causa da morte, mas que algumas vezes podem ser confundidas com lesões importantes.
Uma das lesões sem significado clínico mais comuns em suínos são os cistos renais congênitos, observados em suínos jovens e adultos (Fig.45). Também existem alguns tipos de cistos na proximidade do ovário e oviduto que, ao contrário dos cistos luteínicos ou luteinizados ou dos cistos foliculares do ovário que possuem grande interferência na atividade ovariana, não interferem na sua atividade. Esses cistos incluem os cistos paraováricos, cistos da rete ovarii, cistos bursa-ováricos, cistos remanescentes do ducto mesonéfrico, cistos paratubáricos (Fig.46), entre outros (Nascimento & Santos 2008). Hematomas valvulares ou hematocistos (cistos contendo sangue) (Fig.47) e linfocistos (cistos contendo linfa) são raramente observados nas válvulas atrioventriculares do coração. Na maioria das vezes, esses cistos não interferem com o fechamento adequado da válvula (Muller et al. 2011). Apesar de raros em outros órgãos, os cistos congênitos devem ser diferenciados de cistos parasitários, especialmente quando se realiza a necropsia em javalis, que são animais de vida livre. Um exemplo são os cistos hepáticos congênitos que não devem ser confundidos com cistos parasitários de Cysticercus spp. Nos cistos parasitários é possível observar o escólex de cerca de 1mm (Guillamón & Jalón 2010).
Hemorragias subendocárdicas (Fig.47) são geralmente encontradas no ventrículo esquerdo e consideradas lesões de pouco significado clínico se não houver evidência de toxemia/septicemia. Ocorre em função de contrações cardíacas forçadas contra a resistência periférica aumentada (King et al. 2005). É uma alteração comum encontrada em javalis abatidos com arma de fogo.
Na pele, a lesão de pitiríase rósea (dermatite psoriasiforme juvenil dos suínos), que é de pouco significado clínico já que os animais se recuperam espontaneamente, pode ser confundida com lesões de dermatofitose (Trichophyton spp.), varíola (poxvírus suíno), epidermite exsudativa (Staphylococcus hyicus) (Doster 1995) e a forma cutânea da síndrome da dermatite e nefropatia suína (CReSA 2013). Na pitiríase rósea, as lesões iniciais são em forma de anel, vermelhas e elevadas, localizadas geralmente na porção ventral do abdômen e parte interna dos membros pélvicos (Fig.48). À medida que as lesões progridem, o anel aumenta e o centro fica recoberto por crostas que se desprendem quando a pele está completamente regenerada. Nos estágios mais avançados, as lesões coalescem e apresentam aspecto serpiginoso (Doster 1995). O quadro clínico permite o diagnóstico imediato, mas a confirmação pode ser realizada por biópsia de pele (Sobestiansky & Barcellos 2012).
Os linfonodos da carcaça, especialmente em suínos jovens, ficam inicialmente marrom-escuros e depois de algum tempo alaranjados, após a administração subcutânea ou intramuscular de ferro dextrano (Fig.11, 13 e 49). Esse pigmento deve ser distinguido de hemorragia ou melanose. Em javalis, múltiplos pelos podem ser observados nas criptas da tonsila. Nesses casos, os linfonodos retrofaríngeos e submandibulares podem estar aumentados de volume devido à hiperplasia linfoide secundária aos pelos, que agem como reação por corpo estranho.
Múltiplos papilomas (Fig.50) (Sobestiansky & Barcellos 2012) e hemangiomas (Teankum et al. 2008) podem ser observados no escroto de cachaços velhos. O aspecto macroscópico desses dois tumores benignos pode ser indistinguível, sendo necessário enviar o material para exame histológico para o diagnóstico final. Hemangioma é o tumor de ovário mais comum em porcas (Schlafer & Miller 2007), embora de ocorrência menos frequente que vista no escroto. Outro achado sem significado clínico observado em reprodutores velhos é a esclerodermia da região da paleta, conhecida como "escudo do cachaço". Esclerodermia é o espessamento e endurecimento da pele, que nos cachaços geralmente ocorre na região da escápula e é considerada uma característica sexual secundária, pois se desenvolve durante os conflitos laterais com outros machos, que é uma atitude comum entre reprodutores (Sobestiansky & Barcellos 2012).
Múltiplos ossículos próximos à borda mesentérica do intestino delgado (Fig.51) também podem ser vistos em suínos mais velhos (Sims & Glastonbury 1996, King et al. 2005). Embora um trabalho tenha associado a presença desses ossículos com torção de mesentério (Sanford & Rehmtulla 1994), é pouco provável que ocorra essa associação.
Em suínos é muito comum encontrar a mucosa glandular da porção fúndica do estômago avermelhada (Fig.52), considerado um achado fisiológico, especialmente quando há ingesta. Esse avermelhamento é mais intenso do que em outras espécies domésticas porque a porção fúndica do estômago é normalmente parda em suínos adultos (Fig.3a) (Getty 1981). A falta de hemorragia, exsudato, úlceras ou edema nessas áreas são evidências adicionais que não se trata de gastrite, como é frequentemente denominada (King et al. 2005). Avermelhamento da mucosa gástrica associada a múltiplos trombos de fibrina microscópicos e gastrite aguda com hemorragia é vista em casos de infecção por Salmonella Choleraesuis (Carlson et al. 2012) em suínos domésticos e em infecção experimental pelo vírus da peste suína africana em javalis (Gabriel et al. 2011), respectivamente.
Poucos filetes branco-amarelados semelhantes ao aspecto macroscópico de fibrina podem ser vistos sobre as vísceras abdominais em leitões normais e não devem ser confundidos com peritonite (Sims & Glastonbury 1996).
ALTERAÇÕES POST MORTEM
As alterações post mortem ou autolíticas são aquelas que ocorrem após a morte espontânea ou eutanásia do animal. Os suínos domésticos adultos demoram a dissipar o calor interno após a morte, devido à camada de tecido adiposo subcutânea. Embora em javalis essa camada de gordura seja menos espessa, há maior quantidade de pelos recobrindo a pele, o que também impede a dissipação do calor. Por isso, para evitar que as alterações post mortem mascarem as lesões, o ideal é que a necropsia seja realizada imediatamente ou nas primeiras horas após a morte do animal, principalmente em períodos de tempo quente.
Ao exame externo, a principal alteração post mortem que pode ser vista em suínos de pele branca é o livor mortis ou congestão hipostática. A porção inferior do cadáver fica extensamente vermelha (Fig.53) por causa da deposição de sangue nas partes mais baixas. Dependendo do local onde o cadáver permaneceu, observam-se padrões bem demarcados, reproduzindo o relevo da superfície sobre a qual o suíno permaneceu após a morte (Fig.54). Esses padrões bem demarcados podem ser geométricos e devem ser diferenciados de lesões causadas por Erysipelothrix rhusiopathiae e das observadas na síndrome da dermatite e nefropatia suína. Os grandes músculos da porção inferior da carcaça ficam pressionados pelo peso do suíno, expulsando o sangue dessas áreas. Ao corte, essas massas musculares ficam pálidas. À medida que o intervalo post mortem aumenta, todos os músculos da carcaça ficam pálidos, conferindo-lhes aspecto de carne cozida (Fig.55). Essa alteração deve ser diferenciada de carne PSE (pálida, macia e exsudativa, do inglês Pale, Soft, Exudative). A lesão de PSE geralmente afeta os músculos lombares, os quais ficam pálidos, moles e suculentos.
Distensão abdominal leve a moderada ocorre em suínos adultos após fermentação e formação de gás por bactérias dentro do intestino. Se a distensão for acentuada e ocorrer logo após a morte em suínos da fase de terminação e adultos, a morte provavelmente ocorreu por torção de mesentério, que é uma causa comum de morte súbita em suínos dessa idade (Thomson & Friendship 2012). Cerca de 24 horas após a morte, outra alteração que pode ser observada ao exame externo em suínos brancos é o esverdeamento da pele do abdômen (Fig.56). Isso ocorre devido à pseudomelanose. A pseudomelanose se caracteriza por áreas focalmente extensas cinzas, esverdeadas ou azuladas, causadas pela decomposição do sangue por ação de bactérias, com formação de sulfeto de hidrogênio. Além de ser observada na parede do abdômen, também é vista na superfície de órgãos internos em contato com o intestino como o fígado, rins (Fig.57) e baço.
Focos post mortem pálidos multifocais a coalescentes podem ser encontrados na cápsula do fígado (Fig.58), podem se estender superficialmente pelo parênquima hepático e podem ser confundidos com áreas de necrose. Em comparação, as áreas de necrose são levemente deprimidas, podendo estar associadas com hemorragia, e se estendem para o interior do parênquima. À medida que o intervalo entre a morte do animal e a realização da necropsia aumenta, o fígado pode ficar difusamente pálido a amarronzado e com inúmeras bolhas de putrefação (Fig.59), que são causadas por bactérias que migram do intestino para o fígado após a morte e aí produzem bolhas de gás. A embebição biliar é uma alteração post mortem comumente vista na cápsula do fígado e na serosa do intestino delgado em contato com a vesícula biliar. Após a morte, há o relaxamento do esfíncter do duodeno e a perda de adesão entre as células, acarretando o extravasamento de bile para o lúmen do duodeno, estômago e tecidos adjacentes. A embebição biliar tinge os tecidos de verde ou verde-amarelado e deve ser diferenciada de icterícia, que é sempre difusa. Em fetos, uma alteração post mortem comum é a presença de quantidade variável de líquido sanguinolento na cavidade torácica e abdominal (Fig.60), que não deve ser interpretada como hidrotórax ou ascite. Edema no tecido subcutâneo de fetos e natimortos também é uma alteração post mortem comum (Fig.60) e não deve ser interpretado como lesão, uma vez que reflete o extravasamento de fluido do músculo para o tecido subcutâneo, especialmente em fetos que ficam retidos por um ou dois dias no útero. Áreas pálidas focalmente extensas podem ser observadas no coração de fetos devido à distribuição irregular de sangue (inset Fig.60). Essa palidez deve ser diferenciada de miocardite causada por circovírus suíno tipo 2 (Pescador et al. 2010, Segalés 2012).
DISCUSSÃO E CONCLUSÕES
O conhecimento de estruturas anatômicas, não lesões, artefatos e alterações pouco significativas e post mortem permite o médico veterinário focar na interpretação dos achados macroscópicos das lesões importantes para o diagnóstico definitivo. Isso otimiza o uso racional dos laboratórios de diagnóstico, pois muitas vezes o envio de amostras sem lesões importantes gera custos e pode atrasar o resultado do diagnóstico. Além disso, o conhecimento anatômico de estruturas pouco enviadas para a rotina de diagnóstico laboratorial, como a colheita do gânglio do nervo trigêmeo para a doença de Aujeszky, pode ser útil para médicos veterinários do serviço oficial que trabalham em programas sanitários.
É também importante saber se os suínos foram eutanasiados e qual foi o método de eutanásia, ou se foram encontrados mortos. Essa informação pode ajudar na interpretação das alterações observadas durante a necropsia. Recomenda-se realizar a necropsia logo após a morte ou eutanásia para obtenção de amostras de boa qualidade para o diagnóstico laboratorial. Contudo, a necropsia realizada 12 a 24 horas após a morte do animal não deve ser desencorajada, pois há condições patológicas que podem ser diagnosticadas macroscopicamente, mesmo com a carcaça apresentando algum grau de decomposição, como úlcera gástrica, torções e fraturas.
Apesar do procedimento de necropsia variar entre laboratórios, aconselha-se que cada médico veterinário escolha e siga constantemente apenas uma técnica de necropsia para se familiarizar com a posição, cor, consistência normais das vísceras etc. Uma técnica de necropsia sistemática permite a visualização de todos os órgãos e também facilita a descrição das lesões macroscópicas, que é fundamental para o sucesso do diagnóstico final.
Recebido em 18 de julho de 2013.
Aceito para publicação em 25 de outubro de 2013.
- Alberton G.C., Moreira L.M., Belo C.P. & Dornbush P.T. 2012. Fraturas vertebrais em suínos no abate: Avaliação macroscópica. Anais VII Sinsui, Porto Alegre, RS, p.263-267. (Apresentação de casos clínicos)
- AVMA 2013. Guidelines for the euthanasia of animals. Disponível em <https://www.avma.org/KB/Policies/Documents/euthanasia.pdf> Acesso em 8 jul. 2013.
- Bal H.S. & Ghoshal N.G. 1972. Histomorphology of the torus pyloricus of the domestic pig (Sus scrofa domestica). Zentralbl. Veterinärmed. C 1:289-298.
- Cardenas H. & Pope W.F. 2001. Control of ovulation rate in swine. J. Anim. Sci. 80:E36-E46.
- Carlson S.A., Barnhill A.E. & Griffith R.W. 2012. Salmonellosis, p.821-840. In: Zimmerman J.J., Karriker L.A., Ramirez A., Schwartz K.J. & Stevenson G.W. (Eds), Diseases of Swine. 10th ed. Iowa State University Press, Ames, Iowa.
- Casteignau A., Fontan A., Morillo A., Oliveros J.A. & Segalés J. 2006. Clinical, pathological and toxicological findings of an iatrogenic selenium toxicosis case in feeder pigs. J. Vet. Med. A, Physiol. Pathol. Clin. Med. 53:323-326.
- Casteleyn C., Breugelmans S., Simoens P. & den Broeck W.V. 2011. The tonsils revisited: Review of the anatomical localization and histological characteristics of the tonsils of domestic and laboratory animals. Clinic. Dev. Immunol. 14 p. doi:10.1155/2011/472460
- Caswell J.L. & Williams K.J. 2007. Respiratory system, p.523-653. In: Maxie M.G. (Ed.), Jubb, Kennedy and Palmer's Pathology of Domestic Animals. Vol.2. 5th ed. Saunders Elsevier, Philadelphia.
- Clark S.G., Schaeffer B.D.J. & Althouse G.C. 2003. B-Mode ultrasonographic evaluation of paired testicular diameter of mature boars in relation to average total sperm numbers. Theriogenology 60:1011-1023.
- Corrêa A.M.R., Pescador C.A., Schmitz M., Zlotowski P., Rozza D.B., Oliveira E.C., Barcellos D.E. & Driemeier D. 2006. Aspectos clínico-patológicos associados à circovirose suína no Rio Grande do Sul. Pesq. Vet. Bras. 26:9-13.
- CReSA 2013. Case archive. Slaughterhouse support network. Disponível em http://www.cresa.cat/blogs/sesc/quin-es-el-teu-diagnostic-6/?lang=en
- Doige C. & Horowitz A. 1975. A study of articular surfaces and synovial fossae of the pectoral limb of swine. Can. J. Comp. Med. 39:7-16.
- Doster A.R. 1995. Skin diseases of swine. Swine Health Prod. 3:256-261.
- Drolet R. 2012. Urinary system, p.363-379. In: Zimmerman J.J., Karriker L.A., Ramirez A., Schwartz K.J. & Stevenson G.W. (Eds), Diseases of Swine. 10th ed. Iowa State University Press, Ames, Iowa.
- Fernández P.J. & White W.R. 2010. Atlas of Transboundary Animal Diseases. World Organisation for Animal Health, Paris. 277p.
- Frappier B.L. 2006. Digestive system, p.170-211. In: Eurell J.A. & Frappier B.L. (Eds), Dellmann's Textbook of Veterinary Histology. 6th ed. Blackwell, Iowa.
- Fukui K., Yasui T., Gomi H., Sugiya H., Fujimori O., Meyer W. & Tsukise A. 2012. Histochemical distribution of sialic acids and antimicrobial substances in porcine carpal glands. Arch. Dermatol. Res. 304:599-607. Doi: 10.1007/s00403-012-1226-4
- Gabriel C., Blome S., Malogolovkin A., Parilov S., Kolbasov D., Teifke J.P. & Beer M. 2011. Characterization of African swine fever virus Caucasus isolate in European wild boars. Emerging Infec. Dis. 17:2342-2345.
- Getty R. 1981. Anatomia dos Animais Domésticos (Suínos). Vol.2. 5ª ed. Interamericana, Rio de Janeiro, p.1139-1332.
- Guillamón M.H. & Jalón J.A.G. 2010. Guía de Diagnóstico de Necropsia en Patología Porcina. 3ª ed. Servet, Navarra. 183p.
- Heise-Pavlov S., Heise-Pavlov P. & Bradley A. 2005. Carpal glands in feral pigs (Sus domesticus) in tropical lowland rainforest in northeast Queensland, Australia. J. Zoo. 266:73-80. Doi: 10.1017/S0952836905006655
- Herenda D. 1994. FAO Manual on meat inspection for developing countries. Disponível em <http://www.fao.org/docrep/003/t0756e/t0756e02.htm> Acesso em 6 jul. 2013.
- King J.M., Roth-Johnson L., Dodd D.C. & Newson M.E. 2005. The necropsy book. Cornell University, Ithaca. 242p.
- Knox R.V. 2005. Recruitment and selection of ovarian follicles for determination of ovulation rate in the pig. Dom. Animal Endocrinol. 29:385-397.
- Langohr I.M., Stevenson G.W., Nelson E.A., Lenz D.S., HogenEsch H., Wei H. & Pogranichniy R.M. 2010. Vascular Lesions in Pigs Experimentally Infected With Porcine Circovirus Type 2 Serogroup B. Vet Pathol. 47:140-147.
- Lanteri G., Marino F., Lagana G., Bellocco E., Barreca D., Liotta L., Sfacteria A. & Macri B. 2009. Acquired melanosis caused by acorn ingestion in the Nero Siciliano pig. Vet. Pathol. 46:329-333.
- Long G.G. 1986. Examination of the porcine fetus. Vet. Clin. North Am., Food Anim. Pract. 2:147-159.
- Maldonado J., Segalés J., Martinez-Puig D., Calsamiglia M., Riera P., Domingo M. & Artigas C. 2005. Identification of viral pathogens in aborted fetuses and stillborn piglets from cases of swine reproductive failure in Spain. Vet. J. 169:454-456.
- Muller M., Van Vleet J.F. & Gal A. 2011. Cardiovascular system and lymphatic vessels, p.539-588. In: Zachary J.F. & McGavin M.D. (Eds), Pathologic Basis of Veterinary Disease. 5th ed. Elsevier Mosby, St Louis.
- Nascimento E.F. & Santos R.L. 2008. Patologia da Reprodução dos Animais Domésticos. Guanabara Koogan, Rio de Janeiro, p.15-37.
- National Pork Board 2009. Eutanasia em la Granja: recomendaciones para el produtor. Disponível em <http://www.aasv.org/aasv/documents/SwineEuthanasiaSP.pdf> Acesso em 5 jul. 2012.
- Oliveira F.N., Rech R.R., Rissi D.R., Barros R.R. & Barros C.S.L. 2005. Intoxicação em suínos pela ingestão de sementes de Aeschynomene indica (Leg. Papilionoideae) Pesq. Vet. Bras. 25:135-142.
- Pescador C.A., Bandarra P.M., Antoniassi N.A.B., Santos A.S., Oliveira E.C., Barcellos D.E.S.N. & Driemeier D. 2010. Metodologia aplicada na avaliação de fetos suínos abortados e natimortos. Pesq. Vet. Bras. 30:1058-1063.
- Romero C.H., Meade P.N., Homer B.L., Shultz J.E. & Lollis G. 2003. Potential sites of virus latency associated with indigenous pseudorabies viruses in feral swine. J. Wildl. Dis. 39:567-575.
- Rothköter H.J., Zimmermann H.J. & Pabst R. 1990. Size of jejune Peyer's patches and migration of lymphocyte subsets in pigs after resection or transposition of the continuous ileal Peyer's patch. Scand. J. Immunol. 31:191-197.
- Salles M.W., Scholes S.F., Dauber M., Strebelow G., Wojnarowicz C., Hassard L., Acton A.C. & Bollinger T.K. 2011. Porcine teschovirus polioencephalomyelitis in western Canada. J. Vet. Diagn. Invest. 23:367-73.
- Sanford S.E. & Rehmtulla A.J. 1994. Heterotopic mesenteric bone: an unexpected cause of mesenteric torsion in a sow. Swine Health Prod. 2:17-18.
- Schlafer D.H. & Miller R.B. 2007. Female genital system, p. 329-564. In: Maxie M.G. (Ed.), Jubb, Kennedy and Palmer's Pathology of Domestic Animals. Vol.3. 5th ed. Saunders Elsevier, Philadelphia.
- Schneider C., Kressin M. & Schnorr B. 1996. Morphology of the marginal lingual papillae in newborn piglets. Anat. Histol. Embryol. 25:95-100.
- Segalés J. 2012. Porcine circovirus type 2 (PCV2) infections: clinical signs, pathology and laboratory diagnosis. Virus Res. 164:10-19.
- Senger P.L. 2003. Placentation, the endocrinology of gestation and parturition, p.304-325. In: Ibid. (Ed.), Pathways to Pregnancy and Parturition. Current Conceptions, Pullman. 373p.
- Sims L.D. & Glastonbury J.R.W. 1996. Pathology of the Pig: a diagnostic guide. The Pig Research and Development Corporation, Australia. 456p.
- Sobestiansky J. & Barcellos D. 2012. Doenças dos Suínos. 2ª ed. Cânone, Goiânia. 959p.
- Soede N.M., Langendijk P. & Kempa B. 2011. Reproductive cycles in pigs. Anim. Reprod. Sci. 124:251-258.
- Summers B.A., Cummings J.F. & De Lahunta A. 1995. Veterinary Neuropathology. Mosby, St Louis, p.156-157.
- Teankum K., Hauser B., Grest P., Pospischil A., Janett F., Burgi E. & Borel N. 2008. Capillary haemangiomas of the scrotum and testicle in boars. J. Comp. Pathol. 139:177-186.
- Thomson J.R. & Friendship R.M. 2012. Digestive system, p.199-226. In: Zimmerman J.J., Karriker L.A., Ramirez A., Schwartz K.J. & Stevenson G.W. (Eds), Diseases of Swine. 10th ed. Iowa State University Press, Ames.
- Tokarnia C.H., Peixoto P.V., Dobereiner J., Barros S.S. & Riet-Correa F. 2004. O surto de peste suína africana ocorrido em 1978 no município de Paracambi, Rio de Janeiro. Pesq. Vet. Bras. 24:223-238.
- Van Alstine 2012. Respiratory system, p.348-362. In: Zimmerman J.J., Karriker L.A., Ramirez A., Schwartz K.J. & Stevenson G.W. (Eds), Diseases of Swine. 10th ed. Iowa State University Press, Ames.
- Van Alstine W.G. & Widmer W.R. 2003. Lightning injury in an outdoor swine herd. J. Vet. Diagn. Invest. 15:289-291.
- Yaeger M.J. 2012. Disorders of pig, p.89-146. In: Njaa B.L. (Ed.), Kirkbride´s Diagnosis of Abortion and Neonatal Loss in Animals. 4th ed, Wiley-Blackwell, Ames, Iowa.
- Youngquest R.S. & Threlfall W.R. 2007. Porcine theriogenology, p.717-841. In: Ibid. (Eds) Current Therapy in Large Animal Theriogenology. Saunders Elsevier, USA. 1088p.
Datas de Publicação
-
Publicação nesta coleção
20 Dez 2013 -
Data do Fascículo
Out 2013
Histórico
-
Recebido
18 Jul 2013 -
Aceito
25 Out 2013