Resumos
Este estudo avaliou a participação de Neospora caninum em casos de abortos em bovinos provenientes de propriedades rurais da região sul de Minas Gerais por meio de análises histopatológicas, imuno-histoquímicas (IHQ) e pela reação em Cadeia de Polimerase (PCR). O material utilizado foi obtido de um estudo retrospectivo de casos de aborto recebidos pelo Setor de Patologia Veterinária da Universidade Federal de Lavras e de fetos necropsiados durante os anos de 2011 a 2013. De 60 fetos estudados, 30 (50%) tinham lesões microscópicas. Destes, 19 (63%) apresentaram lesões compatíveis com aborto por N. caninum, caracterizadas principalmente por encefalite não supurativa multifocal, necrose e gliose multifocal, assim como, miocardite e miosite não supurativa. Em 14 fetos chegou-se ao diagnóstico definitivo. Destes, cinco tiveram sua confirmação somente pela marcação IHQ e cinco foram positivos somente na PCR. Quatro fetos foram positivos tanto na IHQ quanto na PCR. Cinco fetos, provenientes do estudo retrospectivo apresentaram lesões compatíveis com N. caninum, mas a presença do protozoário não foi confirmada pela marcação IHQ. Os achados demonstram que o N. caninum é um importante agente associado ao aborto em bovinos na região sul de Minas Gerais. Para tanto, além das lesões microscópicas a associação entre a IHQ e a técnica de PCR foi essencial para a confirmação do diagnóstico.
Aborto; Neospora caninum; neosporose; doenças da reprodução; protozoário; bovinos; PCR; IHQ
The present study evaluates the participation of Neospora caninum in bovine abortions from farms in the southern region of Minas Gerais state, Brazil, through histopathological, immunohistochemical (IHQ) analysis and DNA detection by polymerase chain reaction (PCR). The material used in this study was obtained through retrospective study of bovine abortion cases received by the Setor de Patologia Veterinária da Universidade Federal de Lavras and by necropsies performed in fetuses from 2011 to 2013. From 60 fetuses studied, 30 (50%) had microscopic lesions; 19 (63%) of them had histologic lesions compatible with N. caninum abortion, characterized by multifocal non-suppurative encephalitis, necrosis and gliosis in the central nervous system and multifocal nonsuppurative myocarditis and myositis. From the 19 fetuses with protozoa lesions in 14 the final diagnosis was performed; five were confirmated only by IHQ staining and five were positive only by PCR. Four fetuses were positive in IHC and in PCR. In five fetuses from the retrospective study lesions compatible with N. caninum were seen, but the presence of the protozoan was not confirmed by IHQ labeling. The findings demonstrate that N. caninum is an important agent associated with abortion in cattle from Minas Gerais. Therefore, beyond the microscopic lesions association between IHC and PCR was essential to confirm the diagnosis.
Abortion; Neospora caninum; neosporosis; diseases of reproduction; protozoan; cattle; PCR; IHQ
ANIMAIS DE PRODUÇÃO
Abortos por Neosporacaninum em bovinos do sul de Minas Gerais
Neosporacaninum abortions in cattle in southern Minas Gerais, Brazil
Débora R. Orlando; Rafael C. Costa; Bruno A. Soares; Natália S.C. Oliveira; Lismara C. Nascimento; Ana P. Peconick; Djeison L. Raymundo; Mary S. Varaschin* * Autor para correspondência: msvaraschin@dmv.ufla.br
Setor de Patologia Veterinária, Departamento de Medicina Veterinária, Universidade Federal de Lavras (UFLA), Cx. Postal 3037, Lavras, MG 37200-000, Brasil
RESUMO
Este estudo avaliou a participação de Neospora caninum em casos de abortos em bovinos provenientes de propriedades rurais da região sul de Minas Gerais por meio de análises histopatológicas, imuno-histoquímicas (IHQ) e pela reação em Cadeia de Polimerase (PCR). O material utilizado foi obtido de um estudo retrospectivo de casos de aborto recebidos pelo Setor de Patologia Veterinária da Universidade Federal de Lavras e de fetos necropsiados durante os anos de 2011 a 2013. De 60 fetos estudados, 30 (50%) tinham lesões microscópicas. Destes, 19 (63%) apresentaram lesões compatíveis com aborto por N. caninum, caracterizadas principalmente por encefalite não supurativa multifocal, necrose e gliose multifocal, assim como, miocardite e miosite não supurativa. Em 14 fetos chegou-se ao diagnóstico definitivo. Destes, cinco tiveram sua confirmação somente pela marcação IHQ e cinco foram positivos somente na PCR. Quatro fetos foram positivos tanto na IHQ quanto na PCR. Cinco fetos, provenientes do estudo retrospectivo apresentaram lesões compatíveis com N. caninum, mas a presença do protozoário não foi confirmada pela marcação IHQ. Os achados demonstram que o N. caninum é um importante agente associado ao aborto em bovinos na região sul de Minas Gerais. Para tanto, além das lesões microscópicas a associação entre a IHQ e a técnica de PCR foi essencial para a confirmação do diagnóstico.
Termo de indexação: Aborto, Neospora caninum, neosporose, doenças da reprodução, protozoário, bovinos, PCR, IHQ.
ABSTRACT
The present study evaluates the participation of Neospora caninum in bovine abortions from farms in the southern region of Minas Gerais state, Brazil, through histopathological, immunohistochemical (IHQ) analysis and DNA detection by polymerase chain reaction (PCR). The material used in this study was obtained through retrospective study of bovine abortion cases received by the Setor de Patologia Veterinária da Universidade Federal de Lavras and by necropsies performed in fetuses from 2011 to 2013. From 60 fetuses studied, 30 (50%) had microscopic lesions; 19 (63%) of them had histologic lesions compatible with N. caninum abortion, characterized by multifocal non-suppurative encephalitis, necrosis and gliosis in the central nervous system and multifocal nonsuppurative myocarditis and myositis. From the 19 fetuses with protozoa lesions in 14 the final diagnosis was performed; five were confirmated only by IHQ staining and five were positive only by PCR. Four fetuses were positive in IHC and in PCR. In five fetuses from the retrospective study lesions compatible with N. caninum were seen, but the presence of the protozoan was not confirmed by IHQ labeling. The findings demonstrate that N. caninum is an important agent associated with abortion in cattle from Minas Gerais. Therefore, beyond the microscopic lesions association between IHC and PCR was essential to confirm the diagnosis.
Index terms: Abortion, Neospora caninum, neosporosis, diseases of reproduction, protozoan, cattle, PCR, IHQ.
INTRODUÇÃO
Neospora caninum é um protozoário coccídeo, intracelular obrigatório que pode infectar várias espécies animais, dentre elas canídeos domésticos e selvagens, bovinos, equídeos (Adreotti 2010) e caprinos (Dubey 2003, Varaschin et al. 2012, Mesquita et al. 2013). Este parasito possui uma eficiente capacidade de transmissão dentro do rebanho, podendo infectar até 90% dos animais (Dubey et al. 2006).
A principal manifestação clínica de bovinos infectados por N. caninum é o aborto entre o terceiro e o oitavo mês de gestação. Porém, a morte fetal, em uma fase inicial da gestação, com consequente reabsorção do feto e repetição de cio, também pode ocorrer (Barr 1991). Desta forma, os prejuízos financeiros vão além da perda com o aborto, pois pode ocorrer uma queda na produção de leite e um descarte precoce dos animais afetados (Collantes-Fernández et al. 2006). Estudos demonstram que o Brasil perde, anualmente, devido a neosporose, 51,3 milhões de dólares na pecuária leiteira e 101,0 milhões de dólares no setor de corte (Reichel et al. 2013).
A patogenia do aborto é muito complexa e parcialmente compreendida. Sabe-se que para sua ocorrência, é necessário um contato primário da vaca prenhe com N. caninum ou a reativação do protozoário que se encontra encistado nos tecidos, os quais são provenientes de um contato prévio do bovino com este agente. Consequentemente, ocorre a parasitemia, a infecção da placenta e posteriormente do feto (Dubey et al. 2006).
A morte do feto pode ser devido a lesões na placenta, lesões no feto ou ambos. As lesões provocadas pela multiplicação do parasito na placenta podem prejudicar a oxigenação do feto e provocar a liberação de prostaglandinas e/ou citocinas inflamatórias comprometendo a sobrevivência fetal. Há ainda a liberação de hormônio adrenocorticotrófico fetal com posterior estimulo a expulsão do mesmo (Dubey et al. 2006). Mais frequentemente são observadas áreas de necrose em vários tecidos fetais, além de encefalite e gliose no sistema nervoso central, e miosite e miocardite mononuclear (Dubey & Lindsay 1996, Wouda et al. 1997, Corbellini et al. 2002, Santos et al. 2011, Varaschin et al. 2012).
O diagnóstico de neosporose, deve ser realizado mediante a associação das lesões encontradas na histopatologia com a imuno-histoquímica (IHQ) (Dubey & Lindsay 1996) e/ou a reação em cadeia de polimerase (PCR) (Payne & Ellis 1996, Santos et al. 2011). Apesar das lesões microscópicas presentes nos tecidos, os protozoários não são facilmente visualizados pelas colorações de rotina, ou podem não estar presentes nos tecidos analisados. A IHQ auxilia na visualização do agente etiológico quando há poucos taquizoítos ou cistos nos tecidos e quando o material encontra-se em adiantado estado de autólise (Dubey 2003). Já a PCR, por se basear na detecção de porções do genoma, oferece, entre outros benefícios, uma sensibilidade maior quando comparada com de algumas técnicas de diagnóstico (Payne & Ellis 1996, Medina et al. 2006).
O estado de Minas Gerais é considerado o maior produtor de leite do Brasil, com aproximadamente 25,6% da produção nacional (IBGE, 2012). A frequencia de N. caninum como agente causador de abortos em bovinos de Minas Gerais é desconhecida e consequentemente não se sabe a importância desta doença na ocorrência de abortos no rebanho leiteiro, uma vez que, muitos dos estudos realizados são de soroprevalência (Dubey & Schares, 2011). A região estudada pertence a uma grande bacia leiteira do Sul de Minas Gerais, que contribui juntamente com a região sudeste com aproximadamente 18% da produção do estado (IBGE, 2012) e consequentemente a neosporose pode impactar significativamente na economia da região.
O objetivo do presente trabalho foi estudar a participação de N. caninum como agente causador de aborto em bovinos na região sul de Minas Gerais. Assim como caracterizar as principais lesões encontradas, determinar quais são os tecidos mais afetados e comparar a eficiência da técnica de IHQ em relação a PCR no diagnóstico da neosporose.
MATERIAL E MÉTODOS
Origem e característica das amostras
O material de estudo foi proveniente de fetos bovinos necropsiados entre os anos de 2011 e 2013 (estudo prospectivo) e de uma análise retrospectiva de 10 anos de casos de aborto bovino recebidos pelo Setor de Patologia Veterinária (SPV) da Universidade Federal de Lavras (UFLA), Minas Gerais, Brasil.
Para a obtenção do histórico dos fetos, recebidos entre os anos de 2011 e 2013, era realizada uma anamnese com os proprietários e/ou veterinários, para coleta de dados sobre manejo e profilaxias. A idade fetal foi determinada por meio de registros de cobertura dos animais, fornecidos pelos proprietários, associado à mensuração do feto durante a necropsia conforme recomendado por Barr et al. (1990).
Durante a necropsia, amostras de sistema nervoso central (córtex dos hemisférios cerebrais e do cerebelo, tálamo, colículo rostral e caudal, pedúnculos cerebelares, óbex e medula cervical, torácica e lombar), músculos esqueléticos (occipital, semitendinoso, semimembranoso, infraespinhal, diafragma e língua), coração, esôfago, pulmão, fígado, rim, baço, linfonodos mesentéricos, intestinos, timo, válvula íleo-cecal, ovário/testículo, útero, pele, rúmen, retículo, omaso, abomaso e glânglio trigeminal, foram coletados em formalina a 10% tamponada e processados rotineiramente para histopatologia. Cortes de 5µm de espessura foram corados pela Hematoxilina e Eosina (HE) e avaliados mediante microscopia ótica.
Os tecidos dos fetos que apresentassem lesões compatíveis com neosporose eram submetidos à marcação imuno-histoquimica e a técnica de Reação em Cadeia de Polimerase. Para a realização da PCR, amostras de córtex cerebral e ápice do coração foram coletados em tubos de Eppendorf autoclavados, identificadas, congeladas a -20ºC e armazenadas até a realização da mesma.
Técnica de Imuno-histoquímica
Para realização da imuno-histoquimica, os cortes histológicos em lâminas silanizadas, após desparafinados e rehidratados, foram submetidos ao bloqueio da peroxidase endógena por meio de peróxido de hidrogênio a 3% por 30 minutos. A recuperação antigênica foi feita por digestão enzimática com tripsina 0,1% (pH 7,8) por 10 minutos a 37ºC, seguida pela recuperação pelo calor por 2 minutos no tampão citrato (pH 6,0). Para o bloqueio de reações inespecíficas, os cortes histopatológicos foram submergidos em solução de leite desnatado (Molico®, Nestlé) diluído em PBS a 5% por uma hora. As lâminas foram incubadas por 45 minutos a 37ºC com anticorpo primário policlonal anti-Neospora caninum e anti-Toxoplasma gondii na diluição de 1:2000 (VMRD, Pullman, USA), seguido pela incubação com o anticorpos secundários biotinilados conjulgados a streptavidina (Dako, Carpinteria, CA) por 20 minutos na temperatura ambiente. Na revelação utilizou-se o cromógeno Vector Red (Vector NovaRed®) no tempo de 1 a 5 minutos, e as lâminas foram contra coradas com hematoxilina. Amostras de tecido placentário e de sistema nervoso central de caprinos contendo cistos de N. caninum (Varaschin et al., 2012) foram utilizadas como controles positivos e como controle negativo o anticorpo foi substituído por água destilada.
Reação em Cadeia de Polimerase (PCR)
As amostras de DNA foram extraídas de 40 mg de tecido, a partir das amostras de córtex cerebral e ápice do coração. A extração foi realizada utilizando-se o kit comercial Wizard SV Genomic Purification System (Promega, Madison, USA), por meio da técnica de lise por proteinase K, segundo as recomendações do fabricante. As concentrações (ng/µl) e qualidade do DNA extraído foram determinadas no espectrofotômetro NanoVueTM plus e eletroforese em gel de agarose a 0,8%.
Para a detecção de Neosporacaninum, foram desenhados (utilizando sowftare Primer-BLAST do NCBI) e sintetizados (Sigma-Aldrich) iniciadores para a amplificação de sequências genéticas do protozoário em questão, tendo como molde seu cromossomo XII. Desta forma, os primers forwards CTGTTAGAAGGTGCGGCGAA e reverse TCTCTTGCTGCGGTGGAAAT amplificam um fragmento de 168pb.
Cada reação de cadeia de polimerase foi constituída de 4X de tampão de PCR (100 Mm Tris-HCl ph 8,4; 500mM KCl); 75mM de MgCl2; 5mM de dNTPs; 50 ng da amostra de DNA; 1,6 U da Taq DNA Polimerase Go Taq® Flexi DNA Polymerase (Promega), 5mM dos iniciadores forward e reverse; água deionizada autoclavada para completar um volume final de 25µl. Como controle positivo, foi utilizada amostra de placenta de cabra naturalmente infectada por N. caninum (Varaschin et al. 2012), um controle negativo (um feto sem lesões de neosporose e com diagnóstico negativo em diferentes técnicas para a presença do protozoário) e um controle branco.
As reações foram realizadas em termociclador (Applied Biosystems Veriti 96 Well Thermal Cycler) conforme o seguinte protocolo: desnaturação a 95ºC por 2 min, seguido de 40 ciclos de 95 ºC por 1 minuto, anelamento de 57ºC por 1 min, extensão a 72ºC por dois minutos e trinta segundos e extensão final a 72ºC por 7 min. As amostras foram aplicadas em gel de agarose de alta resolução 1,5%, corado com Gel RedTM 1X, na voltagem de 120 volts em cuba de eletroforese horizontal, contendo TBE (Tris-borato 0,09 M e EDTA 0,002 M) como tampão de corrida. Com o auxílio de padrão de peso molecular (Ladder da Ludwig 100PB 250 microlitros) as bandas foram identificadas.
Sequenciamento do material
Os fragmentos dos genes amplificados na PCR e visualizados na eletroforese em gel de agarose com o tamanho esperado foram purificados utilizando o kit Wizard® SV Gel and PCR Clean-Up System (Promega®), de acordo com as especificações do fabricante. Posteriormente, esses fragmentos foram submetidos ao sequenciamento genético no sequenciador automático capilar ABI310 (Applied Biosystems) pelo método enzimático descrito por Sanger et al. (1977).
Para análise in silico e subsequente confirmação da especificidade, utilizou-se o programa BlastN (Altschul et al. 1990) para comparar com as sequências dos fragmentos dos genes disponíveis no banco de dados do NCBI.
RESULTADOS
Distribuição amostral: estudo retrospectivo e fetos necropsiados
De 60 fetos estudados em 51 deles a origem da região sul de Minas Gerais foi confirmado. Destes, 30 fetos, todos provenientes do sul de Minas Gerias (50%), apresentaram lesões microscópicas e em 19 (63%) lesões compatíveis com aborto por Neospora caninum foram observadas. Em 14 fetos chegou-se ao diagnóstico definitivo. Destes, nove tiveram sua confirmação pela marcação IHQ e cinco foram positivos na PCR. Quatro fetos foram positivos tanto na IHQ quanto na PCR. Cinco fetos, provenientes do estudo retrospectivo apresentaram lesões compatíveis com N. caninum, mas a presença do protozoário não foi confirmada pela marcação IHQ e não havia material disponível para realização da PCR.
Em trinta fetos não foi possível diagnósticar a etiologia do aborto, sendo que, sete estavam em adiantado estado de autólise e vinte e três não apresentaram lesões. Muitos foram provenientes do estudo retrospectivo onde os tecidos coletados foram insuficientes para o diagnóstico, não podendo também, ser descartada a possibilidade de que a origem destes abortos não fosse infecciosa.
A idade gestacional predominante dos 19 fetos foi entre o quinto e sexto mês de gestação (Fig.1).
Achados macroscópicos e microscópicos dos abortos por Neospora caninum
Não foram observadas lesões macroscópicas nos 19 fetos. As lesões microscópicas compativeis com neosporose ocorreram mais frequentes no coração, seguido de músculatura esquelética, encéfalo e fígado.
As lesões encontradas nos músculos cardíacos e esqueléticos eram constituídas por áreas focais ou multifocais de infiltrado inflamatório entre os feixes musculares de linfócitos, plasmócitos e macrófagos, sendo que, a miocardite mononuclear moderada a acentuada (Fig.2) foi observada em 16 fetos (84,21%) e a miosite mononuclear moderada a acentuada (Fig.3) foi observada em 15 fetos (78,94%). No material proveniente do estudo retrospectivo não havia identificação de quais músculos foram coletados, porém em um feto foi possível identificar a miosite na musculatura da lingua. Já nos fetos do estudo prospectivo, cinco apresentaram miosite no músculo semitendinoso, três no músculo infraespinhoso, quatro no músculo semimembranoso, três no diafragma e apenas um no músculo occipital.
No SNC as lesões observadas foram áreas de gliose em regiões do córtex cerebral (52,63%), colículos (21,05%), córtex cerebelar (21,05%), tálamo (10,52%), bulbo ao nível do óbex (5,26%) e pedúnculo cerebelar (5,26%). Áreas multifocais de necrose caracterizadas por acidofilia do tecido e núcleos picnóticos, circundadas por células da glia e/ou infiltrado inflamatório mononuclear (Fig. 4) foram observadas em 36,84% dos fetos com lesões de neosporose. Sendo que dos 19 fetos, 36,84% apresentaram essa lesão em córtex, 15,78% no colículo, 10,52% no cerebelo e em 5,26 % dos fetos no tálamo.
As lesões no fígado consistiram de infiltrado inflamatório mononuclear no espaço porta e, por vezes, áreas multifocais de necrose. Este tipo de lesão estava presente em 31,57% dos fetos com lesões de neosporose.
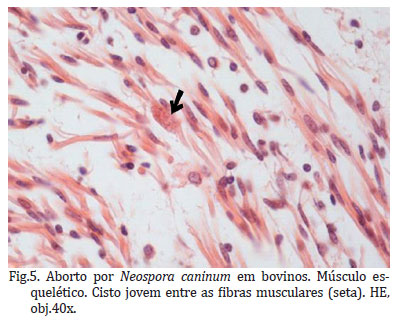
Estruturas compatíveis com o protozoário, sempre próximas ao infiltrado inflamatório, foram observadas em quatro fetos (21,05%) pela coloração de Hematoxilina-Eosina (H.E). Em dois fetos do estudo retrospectivo foi visualizado cisto contendo bradizoítos, no córtex cerebral (feto 1) e em musculatura esquelética (cisto jovem, de parede fina) (feto 7) (Fig.5). No feto 14, do estudo prospectivo, um cisto jovem (parede fina), foi observada no cerebelo. Já, estruturas parasitárias semelhantes a taquizoítos foram observados na musculatura esquelética (feto 2).
Achados imuno-histoquímicos
A imunomarcação ocorreu somente com o anticorpo policlonal anti-N. caninum em 9 fetos (47,36%) dos 19 fetos que apresentaram lesões sugestivas de aborto por protozoário. A marcação mais frequente ocorreu no sistema nervoso central (66,66%), seguido de musculatura esquelética (22,22%) e cardíaca (11,11%). O local da imunomarcação esta detalhado no Quadro 1 assim como o mês em que ocorreu o aborto. As Figuras 6 e 7 ilustram a imunomarcação para Neospora caninum dos fetos 11 e 12.
Análises moleculares
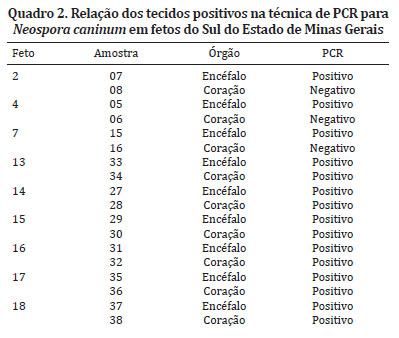
Dos 19 fetos que possuíam lesões compatíveis com neosporose, nove foram positivos na PCR, totalizando 47,36% dos fetos. No Quadro 2 são destacadas quais amostras coletadas foram detectadas a presença do DNA de N.caninum pela técnica de PCR. O sequenciamento confirmou o diagnóstico de N. caninum nestes tecidos.
DISCUSSÃO
No presente estudo observou-se que a grande maioria dos fetos suspeitos e com o diagnóstico confirmado de neosporose (63%) foram abortados entre o quinto e sexto mês de gestação. Estes achados são compatíveis com os descritos por Sager et al (2001) que descreve uma maior frequência entre o quinto ao sétimo mês de gestação, e Antoniassi et al (2013) o qual relata em seu estudo que 62% dos fetos abortados encontravam-se no segundo trimestre da gestação.
As lesões mais frequentemente descritas em fetos bovinos com neosporose são a necrose focal circundada por infiltrado inflamatório mononuclear discreto, encontradas principalmente no sistema nervoso central (Sager et al. 2001, Maley et al. 2003, Benavides et al. 2012). No presente estudo, apesar destas lesões estarem presentes, o achado mais comum foi o infiltrado inflamatório mononuclear, na musculatura cardíaca e esquelética. Achados estes, semelhantes aos de Pescador et al. (2007) que observou que a musculatura esquelética foi a mais afetada. Dos fetos necropsiados no estudo prospectivo foi possível a coleta e a identificação da musculatura esquelética, onde os músculos mais frequentemente acometidos em ordem decrescente foram: o músculo semitendinoso, infraespinhoso, semimembranoso, diafragma e occipital. Estes achados podem indicar um padrão de coleta da musculatura esquelética para o diagnóstico da neosporose em fetos. A necrose hepática e hepatite ocorerram menos frequentemente neste estudo. Estes achados são semelhantes aos descritos por Maley et al. (2003) e Benavides et al. (2012).
Dos 14 abortos comprovadamente positivos, quatro (28,57%) foram confirmados em ambos os testes, cinco (35,71%) apenas pela PCR e cinco apenas (35,71%) pela imuno-histoquímica. Porém é pertinente observar que dos cinco fetos confirmados pela IHQ, em três fetos, a PCR não foi realizada por se tratar de material do estudo restrospectivo, onde os tecidos estavam disponíveis somente em blocos de parafina. Desta forma, nos fetos que passaram pelas duas técnicas a PCR apresentou uma maior sensibilidade (55,55%) quando comparada a imuno-histoquímica (22,22%). Esses resultados, em que a PCR supera em sensibilidade a imuno-histoquímica, tem sido descrito por vários autores (Payne & Ellis 1996, Santos et al. 2011). Seguindo este mesmo raciocínio, observa-se que os fetos classificados como suspeitos (5 fetos) provenientes principalmente do estudo retrospectivo (4 fetos) foram aqueles em que as lesões eram compatíveis com as causadas por protozoários, mas que não houve imunomarcação, provavelmente por não haver estruturas parasitárias nos tecidos coletados. Nestes fetos também não haviam tecidos congelados disponíveis para a realização da PCR, comprometendo assim, o diagnóstico definitivo. Porém ressalta-se que muitos fetos podem apresentar adiantado estado de autólise, dificultando o isolamento e identificação do agente sendo a imuno-histoquímica um método viável e importante para o diagnóstico (Santos et al. 2011).
O diagnóstico de aborto por Neospora caninum foi baseado na presença de lesões microscópicas como miosite, miocardite e gliose (com ou sem necrose), as quais sinalizam para a presença deste protozoário, associado com a marcação imuno-histoquímica positiva somente para N. caninum e os resultados do sequenciamento genético. Os resultados encontrados neste estudo permitem concluir que N. caninum, é um importante agente associado ao aborto em bovinos no sul de Minas Gerais e que para o diagnóstico definitivo é extremamente importante a associação de mais de uma técnica de diagnóstico.
Agradecimentos.- À FAPEMIG pela bolsa de mestrado e auxílio financeiro. Ao CNPq pela bolsa de Iniciação Cientifica.
Recebido em 10 de setembro de 2013.
Aceito para publicação em 22 de outubro de 2013.
- Adreotti R., Barros J.C., Pereira A.R., Oshiro L.M., Cunha R.C. & Figueiredo Neto L.F. 2010. Association between seropositivy for Neospora caninum and reproductive performance of beef heifers in the Pantanal of Mato Grosso do Sul, Brazil. Revta Bras. Parasitol. Vet. 19:119-123.
- Altschul S.F., Gish W., Miller W., Myers E.W. & Lipmas D.J. 1990. Basic local alignment search tool. J. Molec. Biology 215(3):403-410.
- Antoniassi N.A.B., Juffo G.D., Santos A.S., Pescador C.A., Corbellini L.G. & Driemeier D. 2013. Causas de aborto bovino diagnosticadas no Setor de Patologia Veterinária da UFRGS de 2003 a 2011. Pesq. Vet. Bras. 33:155-160.
- Barr C.B., Anderson M.L., Dubey J.P. & Conrad P.A. 1991. Neospora-like protozol infections with bovine abortion. Vet. Pathol. 28:110-116.
- Barr C.B., Anderson M.L., Blanchard P.C., Daft B.M., Kinde H. & Conrad P.A. 1990. Bovine fetal encephalitis and myocarditis associated with protozoal infections. Vet. Pathol. 27:354-361.
- Baszler T.V., Gay L.J.C., Long M.T. & Mathison B.A. 1999. Detection by PCR of Neospora caninum in fetal tissues from spontaneous bovine abortions. J. Clin. Microbiol. 37:4059-4064.
- Benavides J., Katzer F., Maley S.W., Bartley P.M., Cantón G., Palarea-Albaladejo J., Purslow C.A., Pang Y., Rocchi M.S., Chianini F., Buxton D. & Innes E.A. 2012. High rate of transplacental infection and transmission of Neospora caninum following experimental challenge of cattle at day 210 of gestation. Vet. Res. 43:1-13.
- Buxton D., Maley S.W., Wright S., Thomson K.M., Rae A.G. & Innes E.A. 1998. The pathogenesis of experimental neosporosis in pregnant sheep. J. Comp. Pathol. 118:267-279.
- Collantes-Fernández E., Arnáiz-Seco I., Burgos B.M., Rodriguez-Bertos A., Aduriz G., Fernández-García A. & Ortega-Mora L.M. 2006. Comparison of Neospora caninum distribution, parasite loads and lesions between epidemic and endemic bovine abortion cases. Vet. Parasitol. 142:187-191.
- Corbellini L.G., Driemeier D., Cruz C.F.E., Gondim L.F.P. & Wald V. 2002. Neosporosis as a cause of abortion in dairy cattle in Rio Grande do Sul, southern Brazil. Vet. Parasitol. 103:195-202.
- Dubey J.P. 2003. Review of Neospora caninum and neosporosis in animals. Korean J. Parasitol. 41:116.
- Dubey J.P. & Lindsay D.S. 1996. A review of Neospora caninum and neosporosis. Vet. Parasitol. 67:1-59.
- Dubey J.P. & Schares G. 2011. Neosporosis in animals: the last five years. Vet. Parasitol. 180:90-108.
- Dubey J.P., Buxon D. & Wouda W. 2006. Pathogenesis of bovine neosporosis. J. Comp. Pathol. 134:267-289.
- Goggin C.L. 1994. Variation in the two internal transcribed spacers and 5.8 s ribossomal RNA from five isolates of the marine parasite Perkinsus (Protista, Apicomplexa). Mol. Biochem. Parasitol. 65:179-182.
- IBGE 2012. Intitutuo Brasileiro de Geografia e Estatística. <http://www.ibge.gov/br/home/estatistica/economia> Acesso em 20 ago. 2013.
- Maley S.W., Buxton D., Rae A.G., Wright S.E., Shock A., Bartley P.M., Esteban-Redondo I., Swales C., Hamilton C.M., Sales J. & Innes E.A. 2003. The pathognesis of neosporosis in pregnant cattle: innoculation at mid-gestation. J. Comp. Pathol. 129:186-195.
- Medina L., Cruz-Várquez C., Quezada T., Morales E. & García-Várquez Z. 2006. Survey of Neospora caninum infection by nested PCR in aborted fetus from dairy farms in Aguascalientes, México. Vet. Parasitol. 136: 187-191.
- Mesquita L.P., Nogueira C.I., Costa R.C., Orlando D.R., Bruhn F.R.P., Lopes P.F.R., Nakagaki K.R.Y., Peconick A.P., Seixas J.N., Bezerra Júnior P.S., Raymundo D.L. & Varaschin M.S. 2013. Antibody kinetics in goats and conceptuses naturally infected with Neosporacaninum Vet. Parasitol. 196:327-332.
- Moore D.P., Regidor-Cerrillo J., Morrell E., Poso M.A., Cano D.B., Leunda M.R., Linschinky L., Odeón A.C., Odriozola E., Ortega-Mora L.M. & Cam- pero C.M. 2008. The role of Neospora caninum and Toxoplasma gondii in spontaneous bovine abortion in Argentina. Vet. Parasitol. 156:163-167.
- Payne S. & Ellis J. 1996. Direction of Neosporacaninum DNA by the Polymerase chain position. Int. J. Parasitol. 26:347-351.
- Pescador C.A., Corbellini L.G., Oliveira E.C., Raymundo D.L. & Driemeier D. 2007. Histopathological and immunohistochemical aspects of Neosporacaninum diagnosis in bovine aborted fetuses. Vet. Parasitol. 150: 159-163.
- Reichel M.P., Ayanegui-Alcérreca M.A., Gondim L.F.P. & Ellis J.T. 2013. What is the global economic impact of Neospora caninum in cattle: the billion dollar question. Int. J. Parasitol. 43:133-142.
- Sáchez G.F.D., Banda R.V.M., Sahagun R.A., Ledesma M.N. & Morales S.E. 2009. Comparison between immunohistochemistry and two PCR methods for detection of Neospora caninum in formalin-fixed and paraffin-embedded brain tissue of bovine fetuses. Vet. Parasitol. 164:328-332.
- Sager H., Fischer I., Furrer K., Strasser M., Waldvogel A., Boerlin P., Audigé L. & Gottstein B. 2001. A Swiss case-control study to assess Neospora caninum-associated bovine abortions by PCR, histopathology and sero- logy. Vet. Parasitol. 102:1-15.
- Sanger F., Nicklen S. & Coulson A.R. 1977. DNA sequencing with chain-terminating inhibitors. Biotechnology 24:104-108.
- Santos D.S., Andrade M.P., Varaschin M.S., Guimarães A.M. & Hirsch C. 2011. Neospora caninum in bovine fetuses of Minas Gerais, Brazil: genetic characteristics of RDNA. Revta Bras. Parasitol. Vet. 20:281-288.
- Stuart P., Zintl A., WAAL T.D., Mulcahy G., Hawkins C. & Lawton C. 2013. Investigating the role of wild carnivores in the epidemiology of bovine neosporosis. Parasitology 140:296-302.
- Varaschin M.S., Hirsch C., Wouters F., Nakagaki K.R.Y., Guimarães A.M., Santos D.S., Bezerra Júnior P.S., Costa R.C., Peconick A.P. & Langohr I.M. 2012. Congenital Neosporosis in Goats from the State of Minas Gerais, Brazil. Korean J. Parasitol. 50:63-67.
- Wouda W., Dubey J.P. & Jenkins M.C. 1997. Serological diagnosis of bovine fetal neosporosis. J. Parasitol. 83:545-547.
Datas de Publicação
-
Publicação nesta coleção
21 Jan 2014 -
Data do Fascículo
Nov 2013
Histórico
-
Recebido
10 Set 2013 -
Aceito
22 Out 2013