Resumo:
A citologia é um importante exame complementar utilizado para a detecção de alterações no perfil celular do trato respiratório e auxílio no diagnóstico de doenças. No entanto, como os primeiros meses de vida compõem o período de adaptação à vida extrauterina resultando em possíveis alterações das populações celulares, é essencial a padronização das características comuns aos animais sadios, possibilitando a identificação e análise de qualquer mudança no quadro esperado. O objetivo desta pesquisa foi caracterizar o perfil celular por citologia do lavado broncoalveolar obtido semanalmente por broncoscopia de dez bezerros durante os três primeiros meses de vida. A análise estatística foi realizada utilizando-se o software Minitab® 15.0, empregando-se o teste T pareado para as amostras paramétricas e Mann-Whitney para as amostras não paramétricas, considerando nivel de significância P≤0,05. Os resultados obtidos apontaram que o perfil celular do lavado broncoalveolar de bezerros hígidos durante os primeiros 90 dias de vida apresentou predomínio de macrófagos, com média geral de 63,17%, seguido de 33,69% de neutrófilos. Porém observou-se diminuição significativa na porcentagem de macrófagos (P=0,04) e aumento de neutrófilos (P=0,05) ao longo dos momentos, comprovada pela forte correlação negativa entre as porcentagens de macrófagos e neutrófilos ao longo dos momentos. Não houve diferença entre as porcentagens de células gigantes, células epiteliais, linfócitos, eosinófilos e basófilos durante o experimento. Apesar dos resultados serem influenciados por fatores ambientais e de manejo, os resultados dessa pesquisa fornecem subsídios para a identificação de alterações críticas que descaracterizem o perfil celular de bezerros acometidos por doenças respiratórias.
Termos de Indexação:
Bovino; calf; doenças respiratórias; lavado broncoalveolar; broncoscopia
Abstract:
Cytology is an important supplementary test used for the detection of changes in the mobile profile of the respiratory tract and aid in the diagnosis of diseases. However, as the first few months of life make up the period of adjustment to extrauterine life resulting in possible changes in cellular populations, it is essential to the standardization of the characteristics common to healthy animals, enabling the identification and analysis of any change in the expected frame. The objective of this research was to characterize the cellular profile by cytology of bronchoalveolar lavage obtained weekly for bronchoscopy of ten calves during the first three months of life. Statistical analysis was performed using the Minitab® 15.0 software, using the paired T test for parametric samples, and Mann-Whitney for nonparametric samples, considering significance level as P≤0,05. The results obtained showed that the profile of bronchoalveolar lavage of healthy calves during the first 90 days of life showed a predominance of macrophages, with medium average of 63.17%, followed by 33.69% neutrophils. However it was observed significant decrease in percentage of macrophages (P=0.04) and increased neutrophils (P=0,05) over the times, proven by the strong negative correlation between percentages of macrophages and neutrophils along the times. There was no difference between the percentages of giant cells, epithelial cells, lymphocytes, eosinophils and basophils during the experiment. Although the results are influenced by environmental factors and management, the results of this research provide subsidies for the identification of critical changes in cell profile of calves affected by respiratory diseases.
Index Terms:
Cattle; calf; respiratory disease; bronchoalveolar lavage; bronchoscopy
Introdução
Os primeiros meses de vida compõem o período mais crítico para o bezerro, pois é quando ocorre a adaptação à vida extrauterina e há a necessidade de atender exigências vitais como homeotermia, nutrição e função cardiorrespiratória, além de corresponder ao período de grande estresse natural tornando-o mais susceptível a determinadas enfermidades (Allen et al. 1992Allen J.W., Viel L., Bateman K.G., Rosendal S. & Shewen P.E. 1992. Cytological findings in bronchoalveolar lavage fluid from feedlot calves: associations with pulmonary microbial flora. Can. J. Vet. Res. 56(2): 122-126.). Somado a isso, o êxito da transferência de imunidade passiva provida pelo colostro e o desenvolvimento da imunidade adquirida (Benesi, 1993Benesi F.J. 1993. Síndrome asfixia neonatal dos bezerros. Importância e avaliação crítica. Arq. Esc. Med. Vet. UFBA 16:38-48.) refletem na efetividade imunológica do trato respiratório (Yeo et al. 1993Yeo S.P., Stokes C.R., Taylor F.G. & Bourne F.J. 1993. Maturation of cellular defence in the respiratory tract of young calves. Res. Vet. Sci. 55(3):292-297.).
A etiologia e os sintomas de enfermidades respiratórias de bezerros são muito variados, e a realização de um completo exame clínico é fundamental para o diagnóstico (Gonçalves & Feitosa 2008Gonçalves R.C. & Feitosa F.L.F. 2008. Semiologia do sistema respiratório de grandes animais, p.275-306. In: Feitosa F.L.F. (Ed.),. Semiologia Veterinária: a arte do diagnóstico. Roca, São Paulo ). No entanto, técnicas de inspeção indireta como a broncoscopia, enriquecidas pela avaliação citológica, são complementares e auxiliam no delineamento do perfil de resposta inflamatória e, no grau da lesão do local acometido, facilitando a escolha do tratamento e a obtenção de um prognóstico mais preciso (Fernandes et al. 2000Fernandes W.R., Mori E. & Sanches A. 2000. Avaliação citológica de lavados traqueobrônquico e broncoalveolar em cavalos clinicamente sadios pelo método de coloração de Rosenfeld. Arq. Bras. Med. Vet. Zootec. 52(6):604-609., Franz 2008Franz S. 2008. Importance of endoscopic techniques for diagnosis and therapy in ruminants. Hungarian Vet. J. 130(1):33-36.).
A endoscopia respiratória, ou broncoscopia é um exame que permite, por meio de instrumento óptico, a inspeção indireta do sistema respiratório, desde a cavidade nasal até a árvore brônquica (Franz 2008Franz S. 2008. Importance of endoscopic techniques for diagnosis and therapy in ruminants. Hungarian Vet. J. 130(1):33-36.). Em associação, a análise citológica das amostras de lavados broncoalveolares coletados por endoscopia, representa método adequado para gerar informação sobre o perfil imunológico celular das vias respiratórias (Fogarty et al. 1983Fogarty U., Quinn P.J. & Hannan J. 1983. Bronchopulmonary lavage in the calf: a new technique. Irish Vet. J. 37(2):35-38., Gonçalves 1997Gonçalves R.C. 1997. Estudo clínico e citológico em bezerros clinicamente sadios e portadores de broncopneumonia moderada e grave - o lavado traqueobrônquico como complemento diagnóstico. Tese de Doutorado, Universidade Estadual Paulista Júlio Mesquita Filho, São Paulo, SP.) em animais sadios ou acometidos por infecções (Gonçalves et al. 2004Gonçalves R.C., Mattos M.C.F.I., Kuchembuck M.R.G., Lopes R.S. & Borges A.S. 2004. Lavagem traqueobrônquica por sondagem nasotraqueal em bezerros. Arq. Bras. Med. Vet. Zootec. 56(3):307-311.) virais ou bacterianas (Kimman et al. 1986Kimman T.G., Zimmer G.M., Straver P.J. & De Leeuw P.W. 1986. Diagnosis of bovine respiratory syncytial virus infections improved by virus detection in lung lavage samples. Am. J. Vet. Res. 47(1):143-147., Brown & Ananaba et al. 1988Brown T.T. & Ananaba G. 1988. Effect of respiratory infections caused by bovine herpesvirus-1 or parainfluenza-3 virus on bovine alveolar macrophage functions. Am. J. Vet. Res. 49(9):1447-1451.).
Por representar uma técnica de diagnóstico rápida, simples e econômica, além de causar risco mínimo ao paciente, a citologia também fornece informações úteis para definir se testes adicionais mais adequados podem ser realizados para se chegar ao diagnóstico definitivo (Rakich & Latimer 2003Rakich P.M. & Latimer K.S. 2003. Citology, p.304-330. In: Mahaffey E.A. & Prasse K.W. (Eds), Duncan and Prasse's Veterinary Laboratory Medicine: Clinical Pathology. 4th ed. Iowa State Press, Ames.).
Para tal, a realização da citologia do lavado broncoalveolar (LBA), utilizando a técnica de citocentrifugação facilita a visualização e o reconhecimento dos tipos celulares, pois promove a concentração de células por campo de visão do microscópio preservando a morfologia adequada (Fernandes et al. 2000Fernandes W.R., Mori E. & Sanches A. 2000. Avaliação citológica de lavados traqueobrônquico e broncoalveolar em cavalos clinicamente sadios pelo método de coloração de Rosenfeld. Arq. Bras. Med. Vet. Zootec. 52(6):604-609., Biava et al. 2005Biava J.S., Gonçalves R.C., Zanotto G.M., Tonin V.R., Caron P.E., Biondo A.W. & Telles J.E. 2005. Uso da citocentrífuga e coloração especiais no exame citológico do lavado broncoalveolar em cavalo. Ciênc. Anim. 3(4):47-50.). Na espécie bovina, equina, canina, suína e felina a alteração na proporção dos tipos celulares coincide com um aumento do número de bactérias, e está diretamente relacionada com o diagnóstico de animais acometidos por doenças respiratórias (Fogarty 1990Fogarty U. 1990. Evaluation of a bronchoalveolar lavage technique. Equine Vet. J. 22(3):174-176., Padrid et al. 1991Padrid P.A., Feldman B.F., Funk K., Samitz E.M., Reil D. & Cross C.E. 1991. Cytologic, microbiologic, and biochemical analysis of bronchoalveolar lavage fluid obtained from 24 healthy cats. Am. J. Vet. Res. 52(8):1300-1307., Yeo et al. 1993Yeo S.P., Stokes C.R., Taylor F.G. & Bourne F.J. 1993. Maturation of cellular defence in the respiratory tract of young calves. Res. Vet. Sci. 55(3):292-297., Ganter & Hensel 1997Ganter M. & Hensel A. 1997. Cellular variables in bronchoalveolar lavage fluids (BALF) in selected healthy pigs. Res. Vet. Sci. 63(3):215-217., Fernandes et al. 2000Fernandes W.R., Mori E. & Sanches A. 2000. Avaliação citológica de lavados traqueobrônquico e broncoalveolar em cavalos clinicamente sadios pelo método de coloração de Rosenfeld. Arq. Bras. Med. Vet. Zootec. 52(6):604-609., Hirt et al. 2010Hirt R.A., Wiederstein I., Denner E.B.M., Mosing M., Arespacochaga A.G., Spergser J. & Van den Hoven R. 2010. Influence of the collection and oxygenation method on quantitative bacterial composition in bronchoalveolar lavage fluid samples from healthy dogs. Vet. J. 184(1):77-82.).
Em suma, o esclarecimento das condições impostas pelo sistema respiratório durante os primeiros meses de vida até o estabelecimento completo de sua imunidade é fundamental para o diagnóstico e para o tratamento das doenças infecciosas. Esta importância é crescente, pois quanto maior é o valor comercial atribuído aos animais especializados, maior é a necessidade do conhecimento do sistema respiratório do bezerro para a prevenção destas doenças, além de existirem poucos valores de referência na citologia de LBA em bezerros jovens (Gonçalves et al. 2011Gonçalves R.C., Rocha A.E.A., Silva A.A., Takahira R.K. & Chiacchio S.B. 2011. Influência da suplementação de vitamina E na profilaxia e tratamento da broncopneumonia moderada e grave em bezerros. Pesq. Vet. Bras. 31(2):127-135.) tornando o emprego da técnica necessário ao banco de dados da pesquisa. Este trabalho teve por objetivo caracterizar o perfil celular do LBA de dez bezerros sadios durante os três primeiros meses de vida.
Material e Métodos
Animais empregados e delineamento experimental. Foram avaliados durante os primeiros três meses de vida 10 bezerros selecionados da raça Holandesa, provenientes de propriedades leiteiras localizadas no Estado de São Paulo. Todos os bezerros receberam quantidade de colostro correspondente a 10 % do peso vivo, cuja eficiência de transferência de imunidade passiva foi avaliada por meio da mensuração de proteína total. Uma vez incluídos na pesquisa esses animais foram pesados, examinados clinicamente e monitorados semanalmente durante o experimento.
Coleta do Lavado Broncoalveolar. As coletas foram realizadas em oito momentos distintos, sendo: (A) na primeira semana de vida, (B) do 8º ao 14º dia de vida, (C) do 15º ao 22º dia de vida, (D) do 23º ao 30º dia de vida, (E) do 31º ao 40º dia de vida, (F) do 41º ao 50º dia de vida, (G) do 51º ao 60º dia de vida, e (H) no 90º dia de vida. As amostras de LBA foram obtidas por meio de broncoscopia utilizando-se o aparelho gastroscópio EG-250PE5, Fujinon®, com 8,2 mm de diâmetro e comprimento de trabalho de 1,100mm compatível com o tamanho dos bezerros e para sua realização os animais foram submetidos a jejum alimentar de, no mínimo, 12 horas, e sedados com xilazina 2% na dose de 0,02mg/kg por via intramuscular.
Previamente ao exame e após a sedação, instilou-se lidocaína spray 10% na narina do animal e o aparelho foi lubrificado com lidocaína geléia 2%. Os animais foram contidos em decúbito esternal e introduziu-se o gastroscópio na cavidade nasal, até os brônquios finais, onde foi instilado através do canal de trabalho do aparelho 20mL de solução fisiológica aspirando-se o LBA logo em seguida. Este processo foi repetido por três vezes, totalizando 60mL de solução fisiológica. O material foi acondicionado em tubos cônicos de 50mL (tipo Falcon), e em seguida colocados em isopor com gelo.
Obtenção das células. Para a recuperação das células, o LBA foi primeiramente dividido em dois tubos do tipo falcon de 50mL. Em seguida, completou-se o volume com tampão fosfato salina (PBS - Phosphate Buffered Saline) refrigerado até atingir 50mL e estes foram centrifugados por 15 minutos em centrífuga (Eppendorf® Centrifuge 5810R) refrigerada a 4o °C e velocidade de 1000 x g.
Após a centrifugação, o sobrenadante foi descartado e o botão de células foi ressuspendido em PBS refrigerado, num volume de 10mL. Repetiu-se o processo de centrifugação na velocidade de 400xg por 10 minutos, a 4°C. Após essa segunda lavagem, foi desprezado o sobrenadante e o botão ressuspendido, dependendo do tamanho do botão celular, em 1 a 5mL de RPMI estéril (Roswell Park Memorial Institute - RPMI 1640 Sigma® R7638) enriquecido com 10% de soro fetal bovino.
Montagem das lâminas. Identificou-se as lâminas em duplicata com número do animal e da coleta. As lâminas foram encaixadas juntamente com o filtro, a base e a caçapa, que compõem o suporte da citocentrífuga (Cytospin 3 Shandon®). Após a lâmina ser montada no suporte, foram pipetados 200μL da amostra no local adequado da lâmina para em seguida serem centrifugadas a 28xg por 6 minutos.
Coloração das Lâminas. Os botões celulares formados nas lâminas foram fixados em metanol P.A. por 5 minutos e após estarem secas as mesmas foram coradas de acordo com a coloração de Rosenfeld.
Contagem Diferencial das células. Utilizou-se microscópio Nikon® ECLIPSE E200, e contador automático Leucotron® T-P. Foram contadas 400 células, em um aumento de 1000x com óleo de imersão, diferenciando-se as células em macrófagos, neutrófilos, linfócitos, basófilos, eosinófilos, células gigantes, células ciliadas, bactérias (cocos, bacilos, cocobacilos, espiroquetas) e fungos.
Análise estatística. Nas amostras paramétricas utilizou-se o teste T pareado, com significância P≤0,05 e nas amostras não paramétricas utilizou-se o teste de Mann-Whitney, com significância P≤0,05, por meio do software Minitab® 15.0.
Resultados e Discussão
Durante todo o experimento, os dez animais mantiveram seus parâmetros gerais e específicos do sistema respiratório dentro dos limites de normalidade para a espécie, segundo Feitosa (2008)Feitosa F.L.F. 2008. Semiologia Veterinária: a arte do diagnóstico. Roca, São Paulo..
Foram confeccionadas um total de 160 lâminas citológicas de LBA, em duplicata, das quais foi selecionada a melhor de cada lâmina duplicada para, então, realizar-se a leitura de 80 lâminas dos dez bezerros. A citologia do LBA foi considerada uma técnica rápida e de simples aplicação, sendo sua metodologia e capacitação facilmente explicáveis, além de possuir boa correlação com o estado de saúde dos bezerros.
O perfil celular observado nas amostras de LBA apresentou predomínio de macrófagos alveolares, nestes inclusos os macrófagos espumosos, durante os três primeiros meses de vida (Quadro 1 e Quadro 2), sendo o restante da população de células composta principalmente de neutrófilos. Do 41º ao 50º dia de vida (F) observou-se queda na proporção de macrófagos e aumento acentuado da população de neutrófilos. Também foram recuperadas células epiteliais, linfócitos, eosinófilos, células epiteliais ciliadas, células degeneradas e um baixo número de basófilos. Todas as lâminas de LBA apresentaram quantidades semelhantes de muco e bactérias cocos, cocobacilos e bacilos gram positivos (Fig.1A-F).
Contagem diferencial de células do lavado broncoalveolar expressados em média ± desvio padrão da porcentagem de macrófagos (MO) e neutrófilos (NEU). São Paulo 2010
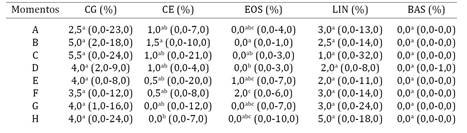
Contagem diferencial de células do lavado broncoalveolar expressados em mediana (mínimos-máximos) do número de células gigantes (CG), células epiteliais (CE), eosinófilos (EOS), linfócitos (LIN) e basófilos (BAS). São Paulo 2010
Células de lavado broncoalveolar de bezerros (Bos taurus taurus) hígidos, identificadas morfologicamente empregando microscopia óptica de imersão. (A) Macrófago espumoso (a) e neutrófilo bastonete (b). (B) Macrófago espumoso (a - seta para esquerda), macrófago (a - seta para cima) e célula gigante (b). (C) Célula epitelial ciliada obtida no lavado. (D) Eosinófilo (a) envolto por macrófagos, broncoalveolar. (E) Macrófago espumoso (a) e linfócitos (b). (F) Macrófago espumoso (a) e neutrófilos segmentados. Obj.100x.
Ao longo do período experimental, foi recuperada maior proporção de macrófagos espumosos do que macrófagos, que somados totalizaram em média 63,17%, semelhante ao encontrado por Allen et al. (1992)Allen J.W., Viel L., Bateman K.G., Rosendal S. & Shewen P.E. 1992. Cytological findings in bronchoalveolar lavage fluid from feedlot calves: associations with pulmonary microbial flora. Can. J. Vet. Res. 56(2): 122-126. e Yeo et al. (1993)Yeo S.P., Stokes C.R., Taylor F.G. & Bourne F.J. 1993. Maturation of cellular defence in the respiratory tract of young calves. Res. Vet. Sci. 55(3):292-297., que observaram respectivamente 64,1% e 54,5%, porém diferente do encontrado por Pringle et al. (1988)Pringle J.K., Viel L., Shewen P.E., Willoughby R.A., Martin S.W. & Valli V.E. 1988. Bronchoalveolar lavage of cranial and caudal lung regions in selected normal calves: cellular, microbiological, immunoglobulin, serological and histological variables. Can. J. Vet. Res. 52(2):239-248. e Brown & Ananaba (1988)Brown T.T. & Ananaba G. 1988. Effect of respiratory infections caused by bovine herpesvirus-1 or parainfluenza-3 virus on bovine alveolar macrophage functions. Am. J. Vet. Res. 49(9):1447-1451., que descreveram respectivamente 91,5% e 98,2 %.
Notou-se a diminuição progressiva na porcentagem de macrófagos desde o momento A (68,75%) até o momento final H (55,47%) apresentando diferença estatística entre esses tempos (P=0,04). Além disso, houve diferença entre os momentos C e G (P=0,02) e C e H (P=0,03), demonstrando que a partir do 51º dia de vida há uma diminuição significativa da porcentagem de macrófagos no LBA de bezerros chegando a 55% aos 90 dias de idade.
De forma semelhante, porém inversa, a porcentagem de neutrófilos aumentou ao longo dos momentos, alcançando valor máximo no momento H (40,38%) e este diferindo do momento A (28,05%) com P=0,05. Houve diferença também entre os momentos C e H (P=0,03). A correlação negativa entre macrófagos e neutrófilos ao longo dos momentos foi comprovada por meio da correlação de Pearson (-0, 863 e R²=0, 745), como mostra a Figura 2.
Correlação da Proporção de Macrófagos x Neutrófilos ao dos três primeiros meses de vida dos bezerros.
Os achados descritos acima são semelhantes ao encontrado por outros autores (Brown & Ananaba 1988Brown T.T. & Ananaba G. 1988. Effect of respiratory infections caused by bovine herpesvirus-1 or parainfluenza-3 virus on bovine alveolar macrophage functions. Am. J. Vet. Res. 49(9):1447-1451., Pringle et al. 1988Pringle J.K., Viel L., Shewen P.E., Willoughby R.A., Martin S.W. & Valli V.E. 1988. Bronchoalveolar lavage of cranial and caudal lung regions in selected normal calves: cellular, microbiological, immunoglobulin, serological and histological variables. Can. J. Vet. Res. 52(2):239-248., Allen et al. 1992Allen J.W., Viel L., Bateman K.G., Rosendal S. & Shewen P.E. 1992. Cytological findings in bronchoalveolar lavage fluid from feedlot calves: associations with pulmonary microbial flora. Can. J. Vet. Res. 56(2): 122-126., Yeo et al. 1993Yeo S.P., Stokes C.R., Taylor F.G. & Bourne F.J. 1993. Maturation of cellular defence in the respiratory tract of young calves. Res. Vet. Sci. 55(3):292-297., Fernandes et al. 2000Fernandes W.R., Mori E. & Sanches A. 2000. Avaliação citológica de lavados traqueobrônquico e broncoalveolar em cavalos clinicamente sadios pelo método de coloração de Rosenfeld. Arq. Bras. Med. Vet. Zootec. 52(6):604-609.), e apresentam o mesmo padrão observado nas espécies bovina (Batista et al. 2012Batista C.F., Blagitz M.G., Santos B.P., Bertagnon H.G., Parra A.C., Vianna R.S. & Della Libera A.M.M.P. 2012. Maturation of mononuclear phagocytes in the lungs of young calves--in vitro study. J. Dairy Sci. 95(10):5909-5915.) equina (Fogarty 1990Fogarty U. 1990. Evaluation of a bronchoalveolar lavage technique. Equine Vet. J. 22(3):174-176., Fernandes et al. 2000Fernandes W.R., Mori E. & Sanches A. 2000. Avaliação citológica de lavados traqueobrônquico e broncoalveolar em cavalos clinicamente sadios pelo método de coloração de Rosenfeld. Arq. Bras. Med. Vet. Zootec. 52(6):604-609.), canina (Hirt et al. 2010Hirt R.A., Wiederstein I., Denner E.B.M., Mosing M., Arespacochaga A.G., Spergser J. & Van den Hoven R. 2010. Influence of the collection and oxygenation method on quantitative bacterial composition in bronchoalveolar lavage fluid samples from healthy dogs. Vet. J. 184(1):77-82.), suína (Hennig-Pauka et al. 2007Hennig-Pauka I., Bremerich S., Nienhoff H., Schröder C., Ganter M., Blecha F. & Gerlach G.F. 2007. Comparison of three common methods of lung lavage in healthy pigs. J. Vet. Med. A, Physiol. Pathol. Clin. Med. 54(8):428-433.), felina (Padrid et al. 1991Padrid P.A., Feldman B.F., Funk K., Samitz E.M., Reil D. & Cross C.E. 1991. Cytologic, microbiologic, and biochemical analysis of bronchoalveolar lavage fluid obtained from 24 healthy cats. Am. J. Vet. Res. 52(8):1300-1307.) e em coelhos (Hawkins et al. 2008Hawkins M.G., Vernau W., Drazenovich T.L., Griffey S.M. & Johnson L.R. 2008. Results of cytologic and microbiologic analysis of bronchoalveolar lavage fluid in New Zealand White rabbits. Am. J. Vet. Res. 69(5):572-578.).
Em condições de normalidade, o tipo celular predominante é o macrófago, um fagócito mononuclear mediador das defesas pulmonares, porém linfócitos, neutrófilos e células endoteliais também são encontrados no LBA e contribuem para essa defesa (Khadom et al. 1985Khadom N.J., Dedieu J.F. & Viso M. 1985. Bovine alveolar macrophage: a review. Ann. Rech. Vét. 16(3):175-183.).
Dessa forma, macrófagos alveolares representam as células mais frequentes no LBA de bezerros saudáveis (Lohmeyer et al. 1994Lohmeyer J., Friedrich J., Rosseau S., Pralle H. & Seeger W. 1994. Multiparameter flow cytometric analysis of inflammatory cells contained in bronchoalveolar lavage fluid. J. Immunol. Methods 172(1):59-70., Garn 2006Garn H. 2006. Specific aspects of flow cytometric analysis of cells from the lung. Exp. Toxicol. Pathol. 57(Suppl.2):21-24.) e desempenham papel importante na depuração pulmonar e resistência do hospedeiro à infecções bacterianas e virais (Myrvik et al. 1961Myrvik Q.N., Leake E.S. & Fariss B. 1961. Lysozyme content of alveolar and peritoneal macrophages from the rabbit. J. Immunol. 86:133-136., Hearst et al. 1980Hearst J.E., Warr J.A. & Jakab G.J. 1980. Characterization of murine lung and peritoneal macrophages. J. Reticuloendothel Soc. 27:631-637.).
As porcentagens de macrófagos encontrados diferem em alguns dos momentos dos encontrados por Batista et al. (2012)Batista C.F., Blagitz M.G., Santos B.P., Bertagnon H.G., Parra A.C., Vianna R.S. & Della Libera A.M.M.P. 2012. Maturation of mononuclear phagocytes in the lungs of young calves--in vitro study. J. Dairy Sci. 95(10):5909-5915. já que este autor utilizou a técnica de citometria de fluxo para identificação de macrófagos por meio de marcadores de superfície (CD14). Segundo Raidal et al. (1998)Raidal S.L., Bailey G.D. & Love D.N. 1998. Flow cytometric determination of oxidative burst activity of equine peripheral blood and bronchoalveolar lavage-derived leucocytes. Vet. J. 156(2):117-126. as populações celulares encontradas no LBA são constituídas por macrófagos, células não macrofágicas e outras subpopulações de macrófagos que realizam diferentes funções além da fagocitose e não expressam o CD14. Essa informação corrobora com a porcentagem encontrada por Batista et al. (2012)Batista C.F., Blagitz M.G., Santos B.P., Bertagnon H.G., Parra A.C., Vianna R.S. & Della Libera A.M.M.P. 2012. Maturation of mononuclear phagocytes in the lungs of young calves--in vitro study. J. Dairy Sci. 95(10):5909-5915., principalmente ao compararmos os resultados do 31° ao 40° dia de vida (momento E) no qual obteve-se 64,00 % na citologia e 49,25 % na citometria, assim como nas coletas do 41º a 50º (momento F) e 51º a 60º dias de vida (momento G), nos quais foram encontrados valores de 56,71% para citologia e 38,01% para citometria e 57,84% para citologia e 73,61% para citometria, respectivamente. Apesar das diferenças numéricas, durante os oito momentos a variação nos valores encontrados pelas duas técnicas seguiu a mesma tendência em aumentar ou diminuir.
Por outro lado, Benesi et al. (2012)Benesi F.J., Wachholz L., Bertagnon H.G., Leal M.L.R., Mori E. & Fernandes W.R. 2012. Citologia dos lavados traqueobrônquico (LTB) e broncoalveolar (LBA) de bezerros holandeses sadios durante o primeiro mês de vida. Pesq. Vet. Bras. 32(3):267-270. encontraram padrão citológico de forma diversa com predomínio neutrofílico em bezerros com idade inferior a um mês, provavelmente em decorrência da diferente resposta celular da região traqueobrônquica escolhida pelos autores.
Apesar do aumento observado na porcentagem de neutrófilos, a magnitude de aumento neutrofílico no trato respiratório pode não ser representativa de broncopneumonia, assim como concluído por Gonçalves et al. (2011)Gonçalves R.C., Rocha A.E.A., Silva A.A., Takahira R.K. & Chiacchio S.B. 2011. Influência da suplementação de vitamina E na profilaxia e tratamento da broncopneumonia moderada e grave em bezerros. Pesq. Vet. Bras. 31(2):127-135., já que devido a imaturidade imune, neonatos bovinos montam resposta inflamatória com grande influxo celular, menos severa e com pouca sintomatologia, em decorrência da menor eficiência celular.
Em contrapartida, os animais mais velhos recrutam menor número de neutrófilos, que são mais eficientes na eliminação dos patógenos, porém mais danosa ao tecido hospedeiro (Grell et al. 2005Grell S.N., Riber U., Tjørnehøj K., Larsen L.E. & Heegaard P.M.H. 2005. Age-dependent differences in cytokine and antibody responses after experimental RSV infection in a bovine model. Vaccine 23(26):3412-3423., Batista et al. 2012Batista C.F., Blagitz M.G., Santos B.P., Bertagnon H.G., Parra A.C., Vianna R.S. & Della Libera A.M.M.P. 2012. Maturation of mononuclear phagocytes in the lungs of young calves--in vitro study. J. Dairy Sci. 95(10):5909-5915.), corroborando com os dados de citologia broncoalveolar em bovinos estudados a partir dos 90 dias de idade encontrados por Bertagnon (2015)Bertagnon H.G. 2015. Avaliação da resposta imune inata respiratória em bezerros sadios durante o segundo trimestre de vida. Tese de Doutorado, Universidade de São Paulo, São Paulo., nos quais a média até os 180 dias de vida dos animais foi de 67% para macrófagos e 23% para neutrófilos, não apresentando diferença entre os momentos experimentais.
Ao se levar em consideração que os neutrófilos são as células mais rapidamente recrutadas e que podem gerar um grande número de produtos inflamatórios, incluindo oxidantes e enzimas proteolíticas (Donnelly & Haslett 1992Donnelly S.C. & Haslett C. 1992. Cellular mechanisms of acute lung injury: implications for future treatment in the adult respiratory distress syndrome. Thorax 47(4):260-263.), as quais podem exacerbar a inflamação pulmonar bem como as manifestações clínicas (Faden & Ogra 1986Faden H. & Ogra P. 1986. Neutrophils and antiviral defense. Pediatr. Infect. Dis. 5(1):6-92., Donnelly & Haslett 1992Donnelly S.C. & Haslett C. 1992. Cellular mechanisms of acute lung injury: implications for future treatment in the adult respiratory distress syndrome. Thorax 47(4):260-263.), julga-se que bezerros saudáveis com idade inferior a três meses apresentem aumento na porcentagem de neutrófilos a fim de suprir a imaturidade funcional de macrófagos alveolares.
Como os dez animais apresentaram os parâmetros físicos específicos do sistema respiratório dentro do considerado saudável, o aumento de neutrófilos com consequente redução na proporção de macrófagos pode ter ocorrido devido às sucessivas coletas, pois se acredita que com a passagem do broncoscópio desde a cavidade nasal até os brônquios terminais, o aparelho possa levar certa quantidade de microrganismos para dentro do pulmão elevando a pressão de infecção local, o que resulta em defesa do organismo sem caracterizar o animal como doente.
Outra sugestão para essa alteração foi que a partir do 41º ao 50º dia de vida (momento F) o centro experimental onde se alocou os bezerros estava com sua capacidade máxima, compondo um total de nove bezerros de diferentes idades (de 40 a 90 dias), enquanto que nos momentos anteriores este número não excedeu a quatro. A maior concentração de animais com idades e níveis imunológicos diferentes no mesmo lote pode favorecer a instalação e disseminação de agentes patogênicos entre os animais, como descrito por Callan & Garry (2002)Callan R.J. & Garry F.B. 2002. Biosecurity and bovine respiratory disease. Vet. Clin. North Am., Food Anim. Pract. 18(1):57-77., Svensson & Liberg (2006)Svensson C. & Liberg P. 2006. The effect of group size on health and growth rate of Swedish dairy calves housed in pens with automatic milk-feeders. Prev. Vet. Med. 73(1):43-53. ou proporcionar uma condição de risco para broncopneumonia como descrito por Gonçalves et al. (2011)Gonçalves R.C., Rocha A.E.A., Silva A.A., Takahira R.K. & Chiacchio S.B. 2011. Influência da suplementação de vitamina E na profilaxia e tratamento da broncopneumonia moderada e grave em bezerros. Pesq. Vet. Bras. 31(2):127-135., resultando em maior resposta imunológica, sem caracterizar uma doença respiratória, quando analisado juntamente aos parâmetros do exame físico geral, que se encontraram dentro dos limites fisiológicos.
Apesar da proporção observada de células epiteliais e eosinófilos ter apresentado diferença estatística (P<0,05) acredita-se isto resultou principalmente por causa dos desvios padrão, pois como o número absoluto estava dentro da normalidade, esta diferença não tem significado clínico. As porcentagens de células gigantes, linfócitos e basófilos não demonstraram significância estatística durante o experimento, assim como foi observado por Brown & Ananaba (1988)Brown T.T. & Ananaba G. 1988. Effect of respiratory infections caused by bovine herpesvirus-1 or parainfluenza-3 virus on bovine alveolar macrophage functions. Am. J. Vet. Res. 49(9):1447-1451., Pringle et al. (1988)Pringle J.K., Viel L., Shewen P.E., Willoughby R.A., Martin S.W. & Valli V.E. 1988. Bronchoalveolar lavage of cranial and caudal lung regions in selected normal calves: cellular, microbiological, immunoglobulin, serological and histological variables. Can. J. Vet. Res. 52(2):239-248., Allen et al. (1992)Allen J.W., Viel L., Bateman K.G., Rosendal S. & Shewen P.E. 1992. Cytological findings in bronchoalveolar lavage fluid from feedlot calves: associations with pulmonary microbial flora. Can. J. Vet. Res. 56(2): 122-126., Yeo et al. (1993)Yeo S.P., Stokes C.R., Taylor F.G. & Bourne F.J. 1993. Maturation of cellular defence in the respiratory tract of young calves. Res. Vet. Sci. 55(3):292-297., Fernandes et al. (2000Fernandes W.R., Mori E. & Sanches A. 2000. Avaliação citológica de lavados traqueobrônquico e broncoalveolar em cavalos clinicamente sadios pelo método de coloração de Rosenfeld. Arq. Bras. Med. Vet. Zootec. 52(6):604-609.) e Mori (2000)Mori E. 2000. Avaliação da função dos macrófagos alveolares após infecção experimental em cavalos (Equus cabalus Linnaeus, 1758) por herpesvírus equino tipo 1 (HVE-1). Tese de Doutorado, Universidade de São Paulo, São Paulo, SP.. Todas as lâminas de LBA apresentaram quantidades pequenas e semelhantes de muco e bactérias cocos, cocobacilos e bacilos gram positivos.
Conclusão
O perfil celular do LBA de bezerros hígidos durante os primeiros 90 dias de vida apresenta maior proporção de macrófagos, porém este perfil pode ser influenciado por fatores ambientais e de manejo, acarretando em diminuição da proporção de macrófagos e aumento da proporção de neutrófilos encontrados na leitura das lâminas de LBA, coletados pelo método de broncoscopia. Assim, como proposto, resultados desta pesquisa contribuem para a caracterização do perfil celular do LBA de bezerros sadios durante os três primeiros meses de vida, viabilizando a identificação precoce de alterações críticas que podem preceder doenças respiratórias.
Agradecimentos
Os autores agradecem o financiamento da bolsa de iniciação científica (FMVZ-USP-PIBIC)
Referências
- Allen J.W., Viel L., Bateman K.G., Rosendal S. & Shewen P.E. 1992. Cytological findings in bronchoalveolar lavage fluid from feedlot calves: associations with pulmonary microbial flora. Can. J. Vet. Res. 56(2): 122-126.
- Batista C.F., Blagitz M.G., Santos B.P., Bertagnon H.G., Parra A.C., Vianna R.S. & Della Libera A.M.M.P. 2012. Maturation of mononuclear phagocytes in the lungs of young calves--in vitro study. J. Dairy Sci. 95(10):5909-5915.
- Benesi F.J. 1993. Síndrome asfixia neonatal dos bezerros. Importância e avaliação crítica. Arq. Esc. Med. Vet. UFBA 16:38-48.
- Benesi F.J., Wachholz L., Bertagnon H.G., Leal M.L.R., Mori E. & Fernandes W.R. 2012. Citologia dos lavados traqueobrônquico (LTB) e broncoalveolar (LBA) de bezerros holandeses sadios durante o primeiro mês de vida. Pesq. Vet. Bras. 32(3):267-270.
- Bertagnon H.G. 2015. Avaliação da resposta imune inata respiratória em bezerros sadios durante o segundo trimestre de vida. Tese de Doutorado, Universidade de São Paulo, São Paulo.
- Biava J.S., Gonçalves R.C., Zanotto G.M., Tonin V.R., Caron P.E., Biondo A.W. & Telles J.E. 2005. Uso da citocentrífuga e coloração especiais no exame citológico do lavado broncoalveolar em cavalo. Ciênc. Anim. 3(4):47-50.
- Brown T.T. & Ananaba G. 1988. Effect of respiratory infections caused by bovine herpesvirus-1 or parainfluenza-3 virus on bovine alveolar macrophage functions. Am. J. Vet. Res. 49(9):1447-1451.
- Callan R.J. & Garry F.B. 2002. Biosecurity and bovine respiratory disease. Vet. Clin. North Am., Food Anim. Pract. 18(1):57-77.
- Donnelly S.C. & Haslett C. 1992. Cellular mechanisms of acute lung injury: implications for future treatment in the adult respiratory distress syndrome. Thorax 47(4):260-263.
- Faden H. & Ogra P. 1986. Neutrophils and antiviral defense. Pediatr. Infect. Dis. 5(1):6-92.
- Feitosa F.L.F. 2008. Semiologia Veterinária: a arte do diagnóstico. Roca, São Paulo.
- Fernandes W.R., Mori E. & Sanches A. 2000. Avaliação citológica de lavados traqueobrônquico e broncoalveolar em cavalos clinicamente sadios pelo método de coloração de Rosenfeld. Arq. Bras. Med. Vet. Zootec. 52(6):604-609.
- Fogarty U. 1990. Evaluation of a bronchoalveolar lavage technique. Equine Vet. J. 22(3):174-176.
- Fogarty U., Quinn P.J. & Hannan J. 1983. Bronchopulmonary lavage in the calf: a new technique. Irish Vet. J. 37(2):35-38.
- Franz S. 2008. Importance of endoscopic techniques for diagnosis and therapy in ruminants. Hungarian Vet. J. 130(1):33-36.
- Ganter M. & Hensel A. 1997. Cellular variables in bronchoalveolar lavage fluids (BALF) in selected healthy pigs. Res. Vet. Sci. 63(3):215-217.
- Garn H. 2006. Specific aspects of flow cytometric analysis of cells from the lung. Exp. Toxicol. Pathol. 57(Suppl.2):21-24.
- Gonçalves R.C. 1997. Estudo clínico e citológico em bezerros clinicamente sadios e portadores de broncopneumonia moderada e grave - o lavado traqueobrônquico como complemento diagnóstico. Tese de Doutorado, Universidade Estadual Paulista Júlio Mesquita Filho, São Paulo, SP.
- Gonçalves R.C. & Feitosa F.L.F. 2008. Semiologia do sistema respiratório de grandes animais, p.275-306. In: Feitosa F.L.F. (Ed.),. Semiologia Veterinária: a arte do diagnóstico. Roca, São Paulo
- Gonçalves R.C., Mattos M.C.F.I., Kuchembuck M.R.G., Lopes R.S. & Borges A.S. 2004. Lavagem traqueobrônquica por sondagem nasotraqueal em bezerros. Arq. Bras. Med. Vet. Zootec. 56(3):307-311.
- Gonçalves R.C., Rocha A.E.A., Silva A.A., Takahira R.K. & Chiacchio S.B. 2011. Influência da suplementação de vitamina E na profilaxia e tratamento da broncopneumonia moderada e grave em bezerros. Pesq. Vet. Bras. 31(2):127-135.
- Grell S.N., Riber U., Tjørnehøj K., Larsen L.E. & Heegaard P.M.H. 2005. Age-dependent differences in cytokine and antibody responses after experimental RSV infection in a bovine model. Vaccine 23(26):3412-3423.
- Hawkins M.G., Vernau W., Drazenovich T.L., Griffey S.M. & Johnson L.R. 2008. Results of cytologic and microbiologic analysis of bronchoalveolar lavage fluid in New Zealand White rabbits. Am. J. Vet. Res. 69(5):572-578.
- Hearst J.E., Warr J.A. & Jakab G.J. 1980. Characterization of murine lung and peritoneal macrophages. J. Reticuloendothel Soc. 27:631-637.
- Hennig-Pauka I., Bremerich S., Nienhoff H., Schröder C., Ganter M., Blecha F. & Gerlach G.F. 2007. Comparison of three common methods of lung lavage in healthy pigs. J. Vet. Med. A, Physiol. Pathol. Clin. Med. 54(8):428-433.
- Hirt R.A., Wiederstein I., Denner E.B.M., Mosing M., Arespacochaga A.G., Spergser J. & Van den Hoven R. 2010. Influence of the collection and oxygenation method on quantitative bacterial composition in bronchoalveolar lavage fluid samples from healthy dogs. Vet. J. 184(1):77-82.
- Khadom N.J., Dedieu J.F. & Viso M. 1985. Bovine alveolar macrophage: a review. Ann. Rech. Vét. 16(3):175-183.
- Kimman T.G., Zimmer G.M., Straver P.J. & De Leeuw P.W. 1986. Diagnosis of bovine respiratory syncytial virus infections improved by virus detection in lung lavage samples. Am. J. Vet. Res. 47(1):143-147.
- Lohmeyer J., Friedrich J., Rosseau S., Pralle H. & Seeger W. 1994. Multiparameter flow cytometric analysis of inflammatory cells contained in bronchoalveolar lavage fluid. J. Immunol. Methods 172(1):59-70.
- Mori E. 2000. Avaliação da função dos macrófagos alveolares após infecção experimental em cavalos (Equus cabalus Linnaeus, 1758) por herpesvírus equino tipo 1 (HVE-1). Tese de Doutorado, Universidade de São Paulo, São Paulo, SP.
- Myrvik Q.N., Leake E.S. & Fariss B. 1961. Lysozyme content of alveolar and peritoneal macrophages from the rabbit. J. Immunol. 86:133-136.
- Padrid P.A., Feldman B.F., Funk K., Samitz E.M., Reil D. & Cross C.E. 1991. Cytologic, microbiologic, and biochemical analysis of bronchoalveolar lavage fluid obtained from 24 healthy cats. Am. J. Vet. Res. 52(8):1300-1307.
- Pringle J.K., Viel L., Shewen P.E., Willoughby R.A., Martin S.W. & Valli V.E. 1988. Bronchoalveolar lavage of cranial and caudal lung regions in selected normal calves: cellular, microbiological, immunoglobulin, serological and histological variables. Can. J. Vet. Res. 52(2):239-248.
- Raidal S.L., Bailey G.D. & Love D.N. 1998. Flow cytometric determination of oxidative burst activity of equine peripheral blood and bronchoalveolar lavage-derived leucocytes. Vet. J. 156(2):117-126.
- Rakich P.M. & Latimer K.S. 2003. Citology, p.304-330. In: Mahaffey E.A. & Prasse K.W. (Eds), Duncan and Prasse's Veterinary Laboratory Medicine: Clinical Pathology. 4th ed. Iowa State Press, Ames.
- Svensson C. & Liberg P. 2006. The effect of group size on health and growth rate of Swedish dairy calves housed in pens with automatic milk-feeders. Prev. Vet. Med. 73(1):43-53.
- Yeo S.P., Stokes C.R., Taylor F.G. & Bourne F.J. 1993. Maturation of cellular defence in the respiratory tract of young calves. Res. Vet. Sci. 55(3):292-297.
Datas de Publicação
-
Publicação nesta coleção
Maio 2016
Histórico
-
Recebido
04 Nov 2015 -
Aceito
01 Mar 2016