RESUMO:
A infestação de pastagens por Pteridium arachnoideum é um problema que afeta a pecuária em diversas partes do mundo, ocasionando perdas produtivas e mortalidades nos rebanhos, bem como a redução das áreas de pastagens. Devido aos prejuízos na bovinocultura, foi proposto o acompanhamento de uma propriedade no Rio Grande do Sul com perdas por Pteridium arachnoideum. Realizou-se um levantamento das mortes associadas à intoxicação por samambaia na propriedade durante o período de janeiro de 2007 a janeiro de 2015. Adicionalmente, testou-se a viabilidade de ovinos como ferramenta de controle biológico de samambaia e se acompanhou as tentativas de controle da planta através do uso dos herbicidas metilsulfuron-metil e picloram, os quais eram associados ou não à roçada prévia. Das mortes por intoxicação natural acompanhadas na propriedade, observou-se 22 casos de quadro agudo de diátese hemorrágica e seis de quadro crônico de carcinomas do trato digestório superior. Em cinco bovinos jovens com diátese hemorrágica, além de hemorragias disseminadas e infartos, observou-se acentuado edema laríngeo, que cursava, clinicamente, com dispneia e estertores respiratórios característicos. Os carcinomas do trato digestório superior, apesar de menos frequentes, causaram perdas expressivas, devido à mortalidade anual de reprodutoras. Notou-se que a introdução de bovinos jovens em áreas recentemente roçadas pode resultar no consumo de grandes quantidades de samambaia e na ocorrência de surtos da enfermidade aguda. O controle das populações de samambaia pelo pastejo por ovinos não foi eficiente, devido ao baixo consumo observado com a lotação de quatro ovinos por hectare, embora mortalidade de ovinos por consumo da planta não tenha sido registrada. Após a retirada do potreiro infestado por samambaia, ao final do experimento, oito dos ovinos foram acompanhados, clinicamente, por três anos e não apresentaram nenhuma alteração. A utilização dos herbicidas resultou em uma redução da cobertura de P. arachnoideum. No entanto, essa prática necessita de estudos adicionais, já que algumas áreas não tiveram recuperação satisfatória da pastagem e o seu uso pode causar impactos ambientais e aquisição de resistência de P. arachnoideum aos herbicidas.
TERMOS DE INDEXAÇÃO:
Plantas tóxicas; Pteridium (aquilinum) arachnoideum; samambaia; intoxicação por plantas; controle; bovinos; toxicoses.
ABSTRACT:
The infestation of pastures by populations of Pteridium arachnoideum has been a considerable and global problem to the livestock production, due to animal mortality and pasture coverage reduction. Given the impact of P. arachnoideum on cattle production, it has been proposed to monitor a beef cattle farm in Rio Grande do Sul, to assess some of the losses associated with the plant consumption and the methods employed for the plant control. A survey of cattle deaths associated with fern poisoning on the farm was carried out from January 2007 to January 2015. In addition, the viability of sheep as a biological control tool was tested. Attempts to control the plant through the use of the herbicides methylsulfuron-methyl and picloram associated or not with previous mowing were monitored. Cases of natural poisoning observed in the farm included the acute form (22), known as hemorrhagic diathesis as well as the chronic form, consisting in digestive carcinomas (6). Five cases of hemorrhagic diathesis in young cattle went along with marked laryngeal edema, which was clinically manifested as dyspnea and roaring, in addition to the classic pathological changes of widespread hemorrhages and infarcts. Even though less frequent, upper digestive tract carcinomas caused significant losses, due to annual mortality of mature cows. In occasions, when cattle were moved to newly mowed infested areas, outbreaks of acute poisoning were observed. The attempted control by sheep introduction showed to be unpractical, due to the little consumption seen at a stocking rate of four sheep per hectare. However, sheep mortality due to P. arachnoideum consumption was not recorded. The plant control method applied at the farm is based on both, the mowing of densely populated areas and the use of herbicides, namely metylsulfuron-methyl and picloram, in all paddocks. The reduction of P. arachnoideum coverage showed to be varied in different paddocks, however allowed the recovery of some grazing areas. This practice needs further studies, as some areas have not had satisfactory pasture recovery, and its indiscriminate use could lead to environmental impacts and resistance of P. arachnoideum to herbicides.
INDEX TERMS:
Poisonous plants; Pteridium (aquilinum) arachnoideum; bracken fern; diseases; cattle; plant poisoning; control; toxicoses.
Introdução
Espécies do gênero Pteridium estão distribuídas em todo mundo, exceto na Antártida e são conhecidas no Brasil pelos nomes populares de samambaia, samambaia-do-campo, feto, entre outros. Recentemente, a planta foi reclassificada conforme caracteres genéticos e morfométricos, o que alterou o nível taxonômico de subespécies para espécies. Assim, são reconhecidas duas espécies com ocorrência no Brasil, Pteridium arachnoideum e P. caudatum (Thomson et al. 2008Thomson J.A., Mickel J.T. & Mehltreter K. 2008. Taxonomic status and relationships of bracken ferns (Pteridium: Dennstaedtiaceae) of Laurasian affinity in Central and North America. Botanical Journal of the Linnean Society 157(1):1-17. <http://dx.doi.org/10.1111/j.1095-8339.2008.00791.x>
https://doi.org/10.1111/j.1095-8339.2008...
, Tokarnia et al. 2012aTokarnia C.H., Brito M.F., Barbosa J.D., Peixoto P.V. & Döbereiner J. 2012a. Plantas de ação radiomimética, p.349-364. In: Ibid. (Eds), Plantas Tóxicas do Brasil para Animais de Produção. 2ª ed. Helianthus, Rio de Janeiro.). A samambaia contém dois princípios tóxicos conhecidos, um ptaquilosídeo de ação radiomimética e a tiaminase tipo I. O ptaquilosídeo é responsável pelo efeito anti-hematopoético e carcinogênico em ruminantes, enquanto a tiaminase tipo I, enzima que inativa a tiamina (vitamina B1), ocasiona quadro clínico neurológico, neuromuscular, além de arritmias cardíacas, principalmente, em equinos (Hirono et al. 1984Hirono I., Kono Y., Takahashi K., Yamada K., Niwa H., Ojika M., Kigoshi H., Niiyama K. & Uosaki Y. 1984. Reproduction of acute bracken poisoning in a calf with ptaquiloside, a bracken constituent. Vet. Rec. 115(15):375-378. <http://dx.doi.org/10.1136/vr.115.15.375> <PMid:6506412>
https://doi.org/10.1136/vr.115.15.375...
, Tokarnia et al. 2012aTokarnia C.H., Brito M.F., Barbosa J.D., Peixoto P.V. & Döbereiner J. 2012a. Plantas de ação radiomimética, p.349-364. In: Ibid. (Eds), Plantas Tóxicas do Brasil para Animais de Produção. 2ª ed. Helianthus, Rio de Janeiro.).
A intoxicação por samambaia, no entanto, tem maior impacto econômico na bovinocultura, devido à mortalidade, frequentemente, observada nessa espécie. O consumo da planta está associado a três apresentações clínicas em bovinos, uma aguda (diátese hemorrágica) e duas crônicas (hematúria enzoótica e os carcinomas de trato digestório superior) (França et al. 2002França T.N., Tokarnia C.H. & Peixoto P.V. 2002. Enfermidades determinadas pelo princípio radiomimético de Pteridium aquilinum (Polypodiaceae). Pesq. Vet. Bras. 22(3):85-96. <http://dx.doi.org/10.1590/S0100-736X2002000300001>
https://doi.org/10.1590/S0100-736X200200...
). No Brasil, as intoxicações por plantas figuram entre as maiores causas de perdas econômicas para a bovinocultura, equiparando-se a enfermidades como botulismo e raiva (Tokarnia et al. 2012bTokarnia C.H., Brito M.F., Barbosa J.D., Peixoto P.V. & Döbereiner J. 2012b. Parte Geral, p.5-26. In: Ibid. (Eds), Plantas Tóxicas do Brasil para Animais de Produção. 2ª ed. Helianthus, Rio de Janeiro .). Levantamentos realizados no sul do Brasil demonstram que a intoxicação por plantas é uma das principais causas de mortes em bovinos nessa região (Pedroso et al. 2007Pedroso P.M.O., Pescador C.A., Oliveira E.C., Sonne L., Bandarra P.M., Raymundo D.L. & Driemeier D. 2007. Intoxicações naturais por plantas em ruminantes diagnosticadas no Setor de Patologia Veterinária da UFRGS no período de 1996-2005. Acta Scient. Vet. 35(2):213-218., Rissi et al. 2007Rissi D.R., Rech R.R., Pierezan F., Gabriel A.L., Trost M.E., Brum J.S., Kommers G.D. & Barros C.S.L. 2007. Intoxicações por plantas e micotoxinas associadas a plantas em bovinos no Rio Grande do Sul: 461 casos. Pesq. Vet. Bras. 27(7):261-268. <http://dx.doi.org/10.1590/S0100-736X2007000700002>
https://doi.org/10.1590/S0100-736X200700...
, Casagrande et al. 2008Casagrande R.A., Mazzocco M.B., Frizon R., Lentz D., Traverso S.D. & Gava A. 2008. Doenças de bovinos diagnosticadas pelo laboratório de Patologia Animal CAV/UDESC de janeiro de 2000 a abril de 2008. Anais do 3º Encontro Nacional de Diagnóstico Veterinário, Campo Grande, MS, p.55-56. (Resumo), Lucena et al. 2010Lucena R.B., Pierezan F., Kommers G.D., Irigoyen L.F., Fighera R.A. & Barros C.S.L. 2010. Doenças de bovinos no Sul do Brasil: 6.706 casos. Pesq. Vet. Bras. 30(5):428-434. <http://dx.doi.org/10.1590/S0100-736X2010000500010>
https://doi.org/10.1590/S0100-736X201000...
, Lucena et al. 2011Lucena R.B., Rissi D.R., Kommers G.D., Pierezan F., Oliveira-Filho J.C., Macêdo J.T., Flores M.M. & Barros C.S.L. 2011. A retrospective study of 586 tumours in brazilian cattle. J. Comp. Pathol. 145(1):20-24. <http://dx.doi.org/10.1016/j.jcpa.2010.11.002> <PMid:21247583>
https://doi.org/10.1016/j.jcpa.2010.11.0...
, Tokarnia et al. 2012bTokarnia C.H., Brito M.F., Barbosa J.D., Peixoto P.V. & Döbereiner J. 2012b. Parte Geral, p.5-26. In: Ibid. (Eds), Plantas Tóxicas do Brasil para Animais de Produção. 2ª ed. Helianthus, Rio de Janeiro .). Dentre as enfermidades tóxicas de bovinos registradas no Rio Grande do Sul, a intoxicação por samambaia (P. arachnoideum) é registrada como a segunda mais importante, apenas superada pela intoxicação por plantas do gênero Senecio (Rissi et al. 2007Rissi D.R., Rech R.R., Pierezan F., Gabriel A.L., Trost M.E., Brum J.S., Kommers G.D. & Barros C.S.L. 2007. Intoxicações por plantas e micotoxinas associadas a plantas em bovinos no Rio Grande do Sul: 461 casos. Pesq. Vet. Bras. 27(7):261-268. <http://dx.doi.org/10.1590/S0100-736X2007000700002>
https://doi.org/10.1590/S0100-736X200700...
, Lucena et al. 2010Lucena R.B., Pierezan F., Kommers G.D., Irigoyen L.F., Fighera R.A. & Barros C.S.L. 2010. Doenças de bovinos no Sul do Brasil: 6.706 casos. Pesq. Vet. Bras. 30(5):428-434. <http://dx.doi.org/10.1590/S0100-736X2010000500010>
https://doi.org/10.1590/S0100-736X201000...
). Adicionalmente, o risco do consumo do princípio ativo por humanos em produtos de origem animal, assim como os prejuízos ecológicos ocasionados pelo comportamento invasivo da planta em matas e florestas têm sido discutidos (Hojo-Souza et al. 2010Hojo-Souza N.S., Carneiro C.M. & Santos R.C. 2010. Pteridium aquilinum: o que sabemos e o que ainda falta saber. Biosci. J. 26(5):798-808., Gil da Costa et al. 2012Costa R.M.G., Bastos M.M., Oliveira P.A. & Lopes C. 2012. Bracken-associated human and animal health hazards: chemical, biological and pathological evidence. J. Hazard. Mater. 203-204:1-12. <http://dx.doi.org/10.1016/j.jhazmat.2011.12.046> <PMid:22226718>
https://doi.org/10.1016/j.jhazmat.2011.1...
).
Em ovinos, a intoxicação natural por Pteridium spp. tem sido descrita no Reino Unido, Nova Zelândia e Austrália, como causa de diátese hemorrágica, hematúria enzoótica, tumores intestinais e degeneração progressiva da retina (Harbutt & Leaver 1969Harbutt P.R. & Leaver D.D. 1969. Carcinoma of the bladder of sheep. Aust. Vet. J. 45(10):473-475. <http://dx.doi.org/10.1111/j.1751-0813.1969.tb06593.x> <PMid:5408647>
https://doi.org/10.1111/j.1751-0813.1969...
, McCrea & Head 1978McCrea C.T. & Head K.W. 1978. Sheep tumours in North East Yorkshire. I. Prevalence on seven moorland farms. Brit. Vet. J. 134(5):454-461. <http://dx.doi.org/10.1016/S0007-1935(17)33387-0> <PMid:698772>
https://doi.org/10.1016/S0007-1935(17)33...
, Sunderman 1987Sunderman F.M. 1987. Bracken poisoning in sheep. Aust. Vet. J. 64(1):25-26. <http://dx.doi.org/10.1111/j.1751-0813.1987.tb06053.x> <PMid:3593134>
https://doi.org/10.1111/j.1751-0813.1987...
, Hirono et al. 1993Hirono I., Ito M., Yagyu S., Haga M., Wakamatsu K., Kishikawa T., Nishikawa O., Yamada K., Ojika M. & Kigoshi H. 1993. Reproduction off progressive retinal degeneration (Bright Blindness) in sheep by administration of ptaquiloside contained in bracken. J. Vet. Med. Sci. 55(6):979-983. <http://dx.doi.org/10.1292/jvms.55.979> <PMid:8117827>
https://doi.org/10.1292/jvms.55.979...
, França et al. 2002França T.N., Tokarnia C.H. & Peixoto P.V. 2002. Enfermidades determinadas pelo princípio radiomimético de Pteridium aquilinum (Polypodiaceae). Pesq. Vet. Bras. 22(3):85-96. <http://dx.doi.org/10.1590/S0100-736X2002000300001>
https://doi.org/10.1590/S0100-736X200200...
). Entretanto, a intoxicação parece ser menos frequente nessa espécie, possivelmente, em decorrência de uma resistência maior à síndrome hemorrágica aguda, ou devido ao hábito de pastejo mais seletivo que determina um consumo menor de samambaia (Parker & McCrea 1965Parker W.H. & McCrea C.T. 1965. Bracken (Pteris aquilina) poisoning of sheep in the North York Moors. Vet. Rec. 77(30):861-865. <PMid:14331487>, Sunderman 1987Sunderman F.M. 1987. Bracken poisoning in sheep. Aust. Vet. J. 64(1):25-26. <http://dx.doi.org/10.1111/j.1751-0813.1987.tb06053.x> <PMid:3593134>
https://doi.org/10.1111/j.1751-0813.1987...
). Conforme observado em outros estudos, os ovinos podem ser utilizados como controle biológico de plantas tóxicas em determinadas situações, inclusive se especula que essa maior resistência esteja associada ao tipo de pastejo ou particularidades do metabolismo desses animais (Parker & McCrea 1965Parker W.H. & McCrea C.T. 1965. Bracken (Pteris aquilina) poisoning of sheep in the North York Moors. Vet. Rec. 77(30):861-865. <PMid:14331487>, Sunderman 1987Sunderman F.M. 1987. Bracken poisoning in sheep. Aust. Vet. J. 64(1):25-26. <http://dx.doi.org/10.1111/j.1751-0813.1987.tb06053.x> <PMid:3593134>
https://doi.org/10.1111/j.1751-0813.1987...
, Kellerman et al. 2005Kellerman T.S., Coetzer J.A.W., Naude T.W. & Botha C.J. 2005. Plant Poisonings and Mycotoxicoses of Livestock in Southern Africa. 2nd ed. Oxford University Press, Oxford. 310p., Bandarra et al. 2012Bandarra P.M., Oliveira L.G.S., Dalto A.C., Boabaid F.M., Juffo G., Riet-Correa F., Driemeier D. & Cruz C.E.F. 2012. Sheep production as a Senecio spp. control tool. Pesq. Vet. Bras. 32(10):1017-1022. <http://dx.doi.org/10.1590/S0100-736X2012001000013>
https://doi.org/10.1590/S0100-736X201200...
).
O grande apelo econômico associado à irreversibilidade da doença em bovinos tem motivado estudos sobre o controle de Pteridium sp. através de práticas mecânicas, agentes químicos, ou biológicos. Tratamentos com herbicidas são, atualmente, os métodos mais empregados no controle, porém requerem aplicação intensiva por longos períodos e apresentam resultados variáveis. Dessa forma, justifica-se a intensificação da pesquisa voltada ao desenvolvimento de métodos alternativos de controle da planta (Robinson 1999Robinson R.C. 1999. The means to large-scale, effective bracken clearance in the UK, p.156-162. In: Smith R.T. & Taylor J.A. (Eds), Bracken Fern: toxicity, biology and control. International Bracken Group Conference, Manchester., Papavlasopoulos 2003Papavlasopoulos A.K. 2003. Biological control of Pteridium aquilinum (L.) Kuhn as a realistic prospect. Agro Thesis 1:13-18.). Este trabalho tem como objetivos descrever a ocorrência da intoxicação por P. arachnoideum em uma propriedade dedicada à bovinocultura de corte, no estado do Rio Grande do Sul, além de relatar a tentativa de desenvolvimento de métodos de controle biológico e químico de populações de P. arachnoideum empregados nesta propriedade.
Material e Métodos
Escolha do local de estudo. Uma propriedade com casos recorrentes de intoxicação por P. arachnoideum, identificada através da solicitação de diagnóstico post mortem ao Setor de Patologia Veterinária da Universidade Federal do Rio Grande do Sul (SPV-UFRGS), foi convidada, em janeiro de 2012, a fazer parte deste estudo. Após acordado, registraram-se as informações relativas às necropsias realizadas no local, a invasão de pastagens pela planta, tentativas e métodos utilizados para controle da planta, práticas agrícolas utilizadas na propriedade e avaliação visual da cobertura vegetal.
Identificação botânica. Amostras de samambaia encontradas na propriedade, compostas por folhas com esporos (folhas férteis), folhas sem esporos e caule, foram prensadas e, após secagem, encaminhadas para classificação taxonômica no Instituto de Ciências Naturais (ICN) da UFRGS. Depois de classificadas, realizou-se a confecção da exsicata para armazenamento permanente no herbário do mesmo instituto, onde recebeu a identificação de registro ICN191717.
Necropsia e análises histológicas. Os bovinos, naturalmente, intoxicados na propriedade morreram de forma espontânea, ou foram submetidos à eutanásia devido ao prognóstico desfavorável. Durante a necropsia, os achados macroscópicos foram identificados e avaliados. Para os exames histológicos, coletaram-se fragmentos de diversos órgãos, os quais foram fixados em formalina a 10%, processados por técnicas histológicas de rotina e avaliados em microscopia óptica.
Controle de Pteridium arachnoideum por pastejo de ovinos. Para o estudo da utilização de ovinos, como ferramenta de controle de samambaia, foi identificada uma área com infestação abundante pela planta, com gramíneas nativas disponíveis e árvores, em distribuição esparsa, para sombreamento. Conforme no restante da propriedade, o substrato do piquete era composto de turfa. A área com sete hectares (ha) foi delimitada por uma cerca de sete fios de arame liso. Foram construídos, também, um curral e um brete para manejo dos ovinos, além de uma represa de, aproximadamente, oito metros quadrados, para fornecimento de água. Ovinos, mestiços e da raça Texel, com idade entre 1-6 anos, foram adquiridos em um criatório no Rio Grande do Sul em que não havia samambaia.
Antes da entrada dos animais, o piquete foi roçado a, aproximadamente, 20 cm de altura do solo, em maio de 2012. No mesmo mês, foi introduzido um lote de 28 ovinos na área, contabilizando uma lotação de quatro ovinos/ha. Os ovinos recebiam blocos de suplemento mineral próprio para a espécie e manejo sanitário semanal. Além disso, era realizada uma observação diária dos animais. Antes da realização das práticas sanitárias semanais, os animais eram observados quanto ao seu comportamento de pastejo. A prenhez das ovelhas foi monitorada até o nascimento dos cordeiros (meses de setembro, outubro e início de novembro de 2012). No mês de julho e novembro de 2012, foram realizadas novas roçadas no local, para manter a altura da pastagem e da planta ideal para o consumo por ovinos. A determinação do nível de infestação por P. arachnoideum e da eficácia de controle foi realizada através da observação semanal e de fotografias em áreas determinadas do piquete em estudo.
No mês de novembro, adicionalmente, dois ovinos, foram levados para instalações do SPV-UFRGS. Essa medida teve o objetivo de induzir dois ovinos (Ovino 1 e Ovino 2) ao consumo da planta para que, por meio do princípio de facilitação social (Wilson 2000Wilson E.O. 2000. Sociobiology: the new synthesis. Belknap, Cambridge. 697p.), estimulassem os demais ovinos mantidos na propriedade a consumirem a planta. Ambos os ovinos selecionados eram machos, não castrados, de cerca de dois anos de idade, em bom estado corporal (Ovino 1: 42,0 kg e Ovino 2: 48,9 kg). Para a indução ao consumo, coletaram-se, semanalmente, folhas e caules de samambaia no piquete da fazenda em que se mantinham os ovinos. Subsequentemente, as amostras de plantas coletadas eram secas à sombra por um período aproximado de sete dias. Em seguida, o feno de samambaia era mantido em sacos em ambiente seco e limpo.
Os dois ovinos foram mantidos estabulados, recebendo água à vontade, alfafa e ração comercial para ovinos, em quantidades adequadas ao peso corporal dos animais, no período da manhã. Ao final do dia, os dois ovinos eram examinados e avaliados quanto à temperatura corporal, frequências cardíaca e respiratória, movimentos ruminais, coloração das mucosas, aspecto das fezes e urina, além do comportamento. Coletou-se ainda, sangue dos ovinos em tubos vacutainer® de 5 mL com EDTA para contagem de plaquetas no Laboratório de Análises Clínicas Veterinárias da UFRGS, para monitoramento de um parâmetro sensível ao consumo de samambaia. Após a avaliação, os ovinos recebiam, conjuntamente, 800g do feno de samambaia. No outro dia, pela manhã, as sobras eram recolhidas e pesadas. Os ovinos foram pesados no início e no final do experimento de adequação. O experimento de indução ao consumo foi mantido durante 22 dias.
Controle de Pteridium arachnoideum por uso de herbicidas. O controle químico empregado na propriedade foi realizado sob a orientação de engenheiros agrônomos, e foi acompanhado de janeiro de 2012 a janeiro de 2015. Foram utilizados dois herbicidas comerciais consorciados, o picloram (Padron®), do grupo químico do ácido piridinocarboxílico, de ação sistêmica e classificação toxicológica III (medianamente tóxico) e o metsulfurom-metílico (Ally®), do grupo químico das sulfonilureias, também de ação sistêmica e de classificação toxicológica I (extremamente tóxico). Esses produtos químicos foram escolhidos devido ao insucesso no tratamento com outros compostos, em anos anteriores.
Para aplicação foram utilizados 500mL de Padron® e 10g de Ally® por hectare, através de pulverizador hidráulico, sobretudo entre novembro e março. Nas áreas pouco invadidas, realizou-se uma aplicação por ano através de jato dirigido, enquanto que as áreas intensamente invadidas eram roçadas em setembro, com realização de controle químico dois a três meses após. Dessa forma, o grau de infestação também determinou o número de aplicações ao longo do ano, sendo as áreas pouco invadidas submetidas a uma aplicação anual e as áreas intensamente invadidas submetidas a duas aplicações anuais no período de rebrota.
Resultados
Descrição do local do estudo e das perdas de bovinos na propriedade
A fazenda localizada no distrito de Itapuã, município de Viamão, Rio Grande do Sul (S 30° 16.177’ e W 50° 54.355’), dedicada ao plantio de arroz e à criação de bovinos de corte da raça Angus, apresentava problemas frequentes decorrentes da intoxicação por Pteridium arachnoideum. A propriedade possui uma área total de 1.900 hectares, dos quais 1.250 hectares são destinados à pecuária de corte, com um rebanho total médio de aproximadamente 1.300 bovinos. Desde o ano de 2007, realizam-se necropsias de bovinos do rebanho da propriedade com quadros clínico-patológicos de diátese hemorrágica e carcinomas do trato digestório superior.
A mortalidade de bovinos registrada na propriedade foi de 9,34% (96/1028) em 2012, 12,01% (159/1324) em 2013 e 13,02% (181/1390) em 2014. Nesses anos, a intoxicação por samambaia foi a causa mais importante de mortes na espécie e correspondeu a 18,53% dos diagnósticos clínicos, seguida pela tristeza parasitária bovina, que representou 17,94% dos casos. Em 2012 foram observadas 29 mortes de bovinos com sinais clínicos sugestivos de diátese hemorrágica e seis de carcinoma de trato digestório superior, dentre as 96 mortes registradas naquele ano.
A maioria dos piquetes destinados à criação de bovinos apresentava infestação por samambaia em quantidades que variavam de touceiras isoladas até extensos aglomerados. Em alguns locais, a planta se encontrava escassamente dispersa nos piquetes, ou em pequenas quantidades que marginavam as valas de condução de água (construídas para a lavoura de arroz). Por outro lado, havia áreas na propriedade onde a samambaia formava extensas áreas de cobertura regular monoespecífica, inutilizáveis para a produção de gado de corte. O solo da propriedade era composto por turfa e o pH médio estava em torno de 4,8.
Identificação botânica
As amostras de samambaia obtidas nos campos da fazenda foram classificadas como Pteridium arachnoideum (Kaulf.) Maxon, Dennstaedtiaceae.
Quadro clínico-patológico dos bovinos com diátese hemorrágica
Durante o período de janeiro de 2007 a janeiro de 2015, foram realizadas 22 necropsias de bovinos da propriedade com diagnóstico de diátese hemorrágica por consumo de samambaia. Dos bovinos submetidos à necropsia, 11 eram fêmeas e 11 eram machos e pertenciam às categorias: até 12 meses (12/22); entre 13 e 24 meses (6/22); entre 25 e 36 meses (1/22); com mais de 36 meses (2/22), e um caso sem registro de idade. Entre os bovinos acometidos, a idade mínima foi de quatro meses e a máxima de seis anos. As mortes de bovinos da propriedade por intoxicação aguda por P. arachnoideum ocorreram de forma esporádica, ou em pequenos surtos em diferentes períodos do ano, mas a maioria dos casos (19/22) foi registrada entre os meses de abril e setembro, época de maior escassez de forragens na propriedade. Seis bovinos submetidos à necropsia apresentaram histórico de morte sem sinais clínicos prévios. Os demais apresentaram curso clínico agudo ou subagudo, caracterizado por hipertermia (40-41oC), apatia, sangramento nasal, fezes fétidas e enegrecidas, ou com coágulos de sangue (Fig.1A), mucosas genitais e oculares pálidas e/ou com hemorragias petequeais, além de sangramento prolongado constatado após a aplicação de medicamentos, picada de insetos ou à punção venosa (Fig.1B). Durante o ano de 2012, entre os bovinos examinados à necropsia com quadro de diátese hemorrágica, seis pertenciam a um lote de 114 bezerros recém-desmamados, de 5-6 meses de idade, no qual houve um surto que resultou na morte de 17 bezerros (14,9% do lote). Esses bezerros haviam sido alocados em um piquete recém-roçado, no qual havia grande quantidade de samambaia em brotação, homogeneamente, distribuída. Após cerca de 30 dias de permanência nesse local, os bezerros começaram a apresentar sinais clínicos semelhantes aos descritos anteriormente, porém, em quatro casos, observou-se, adicionalmente, edema discreto a moderado da região submandibular e cervical ventral, além de intensa dispneia associada a estertor respiratório (“ronqueira”). Posteriormente, em janeiro de 2015, em um outro lote de 216 bovinos com um ano de idade, dois bovinos morreram com sinais clínicos respiratórios semelhantes aos observados nos bezerros, um dos quais foi encaminhado para a necropsia no SPV-UFRGS.
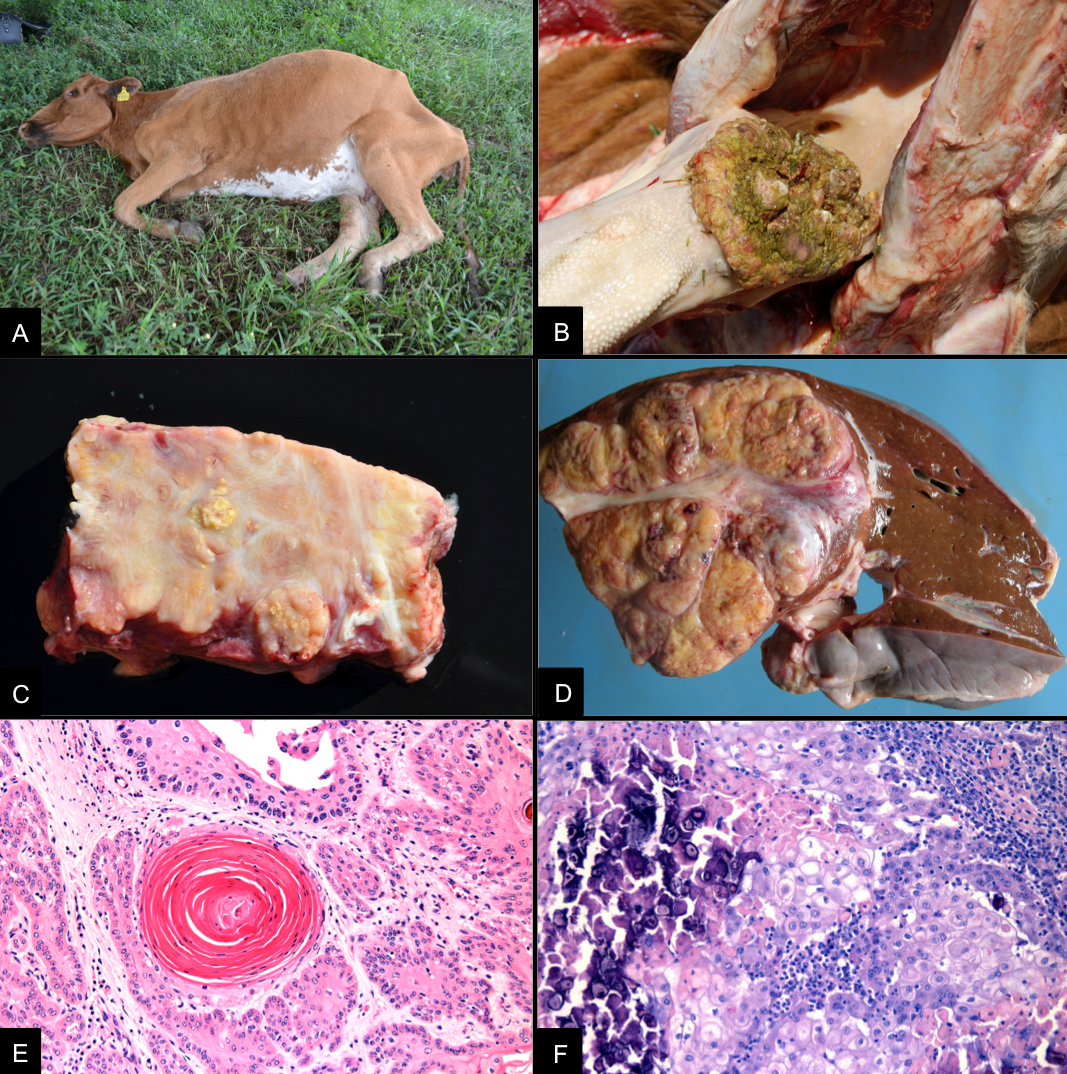
Bovinos da propriedade com síndrome hemorrágica aguda. (A) Fezes diarreicas com coágulos de sangue. (B) Intoxicação aguda em um lote de bezerros após a introdução em um piquete, recentemente, roçado com grande quantidade de brotos de samambaia. Bezerro com apatia e sangramento contínuo após a punção da veia jugular. (C) Duodeno com áreas multifocais de hemorragia na parede e lúmen preenchido por sangue coagulado. (D) Artéria pulmonar, epicárdio e pulmão com área multifocais de hemorragia. (E) Áreas multifocais a coalescentes de infarto na superfície de corte do fígado. (F) Extensa área de infarto com hemorragia na porção dorsal do lobo diafragmático esquerdo do pulmão.
À necropsia dos bovinos com quadro de diátese hemorrágica foram observadas mucosas pálidas e/ou com hemorragias petequiais, sangue com aspecto aquoso, hemorragias petequiais a sufusivas e hematomas no tecido subcutâneo, evidentes principalmente nas áreas de aplicação de medicamentos, ou de coleta de sangue. Ocasionalmente, havia quantidades variáveis de sangue e coágulos no interior da cavidade abdominal, torácica e do saco pericárdico. Foram observadas ainda hemorragias na pleura e peritônio parietal e, em diversos órgãos da cavidade abdominal e torácica. Também havia hemorragia nos intestinos, mesentério, omento, pró-ventrículos, abomaso, vesícula biliar, baço, coração, diafragma, músculo esquelético e pulmões. No intestino delgado e grosso eram frequentes as hemorragias na serosa e mucosa, ou ocasionalmente trasmurais, associadas a conteúdo enegrecido ou com grandes coágulos de sangue (Fig.1C). O abomaso, ocasionalmente, apresentava hemorragias e úlceras na mucosa também com conteúdo enegrecido e/ou com coágulos de sangue. Em um caso havia, na porção pilórica do abomaso, uma úlcera extensa, associada a grande quantidade de sangue coagulado que ocluía totalmente o lúmen do órgão. Hemorragias extensas da serosa e mucosa também eram, frequentemente, visualizadas na vesícula biliar. No coração havia hemorragias em diversos graus, principalmente no epicárdio e endocárdio, as quais, ocasionalmente, envolviam o miocárdio adjacente, além de hemorragias nos grandes vasos da base do coração (Fig.1D). No fígado observaram-se focos de hemorragias discretas e áreas multifocais esbranquiçadas bem delimitadas, com extensão variável de puntiforme a massiva, de contorno geométrico e com os bordos hemorrágicos (infartos), na superfície e no parênquima do órgão (Fig.1E). Foram observadas hemorragias no tecido perirrenal e ocasionais infartos no parênquima renal. A bexiga, por vezes, apresentava hemorragias petequiais a equimóticas na mucosa; entretanto, não foram registrados casos de hematúria. Nos bovinos submetidos à necropsia, visualizou-se, por vezes, grande quantidade de espuma na traqueia e nos brônquios principais, edema de septos lobulares, áreas multifocais de hemorragias no parênquima e áreas bem delimitadas de coloração vermelha e consistência firme (infartos), as quais estavam, ocasionalmente, recobertas por uma membrana de fibrina sobre a superfície pleural (Fig.1F). Em cinco bovinos foram observados edema difuso moderado a acentuado e áreas multifocais de hemorragia acentuada da laringe, faringe e/ou tecidos moles adjacentes, os quais causavam estreitamento da rima da glote (Fig.2). Os linfonodos retrofaríngeos e mandibulares desses bovinos se apresentavam, eventualmente, hemorrágicos e suculentos ao corte. Um bovino apresentou inúmeros papilomas com menos de 1cm de diâmetro, na mucosa do esôfago e na entrada do rúmen. Outros órgãos que apresentaram lesões hemorrágicas incluíram traqueia, timo, adrenal, útero, testículo e sistema nervoso central.
Quadro de diátese hemorrágica em bovinos. (A) Edema e hemorragia acentuada na região retrofaríngea. (B) Edema da região perifaríngea. (C) Espessamento da parede da laringe por edema. (D) Sufusões multifocais na mucosa da laringe e edema com amplas áreas de hemorragia na faringe e tecidos periféricos.
Na histologia, o principal achado foi observado na medula óssea, caracterizado por marcada redução ou ausência de trilinhagem hematopoiética (aplasia da medula óssea), em todos os casos (Fig.3A). Os focos de hemorragia e ulcerações vistos durante a necropsia foram confirmados na análise microscópica e estavam, frequentemente, associados a edema e deposição de fibrina (Fig.3B). As áreas esbranquiçadas visualizadas, macroscopicamente, no fígado correspondiam a focos bem delimitados de necrose de coagulação, frequentemente, associados a trombos e miríades de estruturas bacterianas, compatíveis com infartos por embolismo séptico (Fig.3C). Os infartos renais, esplênicos e pulmonares, apesar de serem vistos com menor frequência, possuíam as mesmas características que as vistas nos fígados. No parênquima pulmonar, observou-se ainda, com frequência, edema, deposição de fibrina e infiltrado inflamatório variável de neutrófilos, macrófagos, linfócitos e plasmócitos. Na parede da laringe e nos tecidos adjacentes havia edema difuso acentuado com grande quantidade de fibrina, trombose, áreas extensas de necrose, ocasionalmente, associadas a infiltrado inflamatório discreto a moderado, principalmente, de neutrófilos e macrófagos, além de miríades de bactérias no interior de vasos e em meio ao tecido (Fig.3D).
Quadro de diátese hemorrágica em bovinos. (A) Medula óssea com depleção completa das células precursoras hematopoiéticas em bovino com diátese hemorrágica. HE, obj.10x. No detalhe, medula óssea de um bovino sem alterações. HE, obj.10x. (B) Hemorragia, focalmente, extensa da mucosa do intestino grosso. HE, obj.10x. (C) Fígado com áreas multifocais a coalescentes de infarto com numerosas bactérias ao centro. HE, obj.10x. (D) Edema difuso acentuado da laringe, com trombose e numerosas bactérias. HE, obj.10x.
Quadro clínico-patológico dos bovinos com carcinoma do trato digestório superior
No período de estudo, seis bovinos submetidos à necropsia na propriedade apresentaram quadro crônico de intoxicação por Pteridium arachnoideum associado ao desenvolvimento de carcinoma de células escamosas no trato digestório superior. Os bovinos eram fêmeas adultas, com idade entre três e 12 anos e os sinais clínicos observados incluíam emagrecimento, dificuldade de deglutição, tosse, respiração ruidosa, halitose e timpanismo ruminal gasoso crônico recorrente. À necropsia, os bovinos apresentavam retração dos globos oculares e perda de elasticidade da pele, condição corporal ruim e, ocasionalmente, distensão abdominal (Fig.4A). À abertura das cavidades, o principal achado consistia em massas infiltrativas, localizadas no trato digestório superior, incluindo a base da língua (Fig.4B), a orofaringe, a epiglote, o esôfago (cranial, médio e distal), o esfíncter cárdico e o rúmen, associado a obliteração ou estenose da porção acometida. Essas massas apresentavam superfície irregular, frequentemente ulcerada, com crescimento exofítico, formando massas exuberantes, ou crescimento endofítico, ocasionando o espessamento da parede do órgão. Ao corte, as massas apresentavam consistência firme e coloração branca com áreas amareladas (Fig.4C). Em todos os bovinos foram notados, concomitantemente, inúmeros papilomas sésseis ou pedunculadas de 0,1 a 1,0 cm de diâmetro na mucosa da faringe, esôfago e/ou rúmen. Em quatro casos foram vistas metástases em linfonodos regionais, os quais se apresentavam aumentados e ocupados por massas brancacentas e firmes, ocasionando a perda da distinção corticomedular. Massas semelhantes foram vistas em um caso, ocupando aproximadamente metade do parênquima hepático (Fig.4D) e ocluindo a veia porta e suas tributárias. Em um caso adicional, constatou-se a perfuração da parede do rúmen associado a uma massa tumoral transmural, com peritonite fibrinosa secundária.
Carcinomas do trato digestório superior. (A) Bovino com seis anos, fêmea, em péssimo estado corporal e com aprofundamento dos globos oculares, além de timpanismo ruminal. (B) Massa tumoral invasiva e exofítica na superfície da língua. (C) Massas tumorais invasivas em superfície de corte da língua, de coloração brancacenta e áreas amareladas (correspondente às concreções de queratina). (D) Fígado, na superfície de corte, há uma massa tumoral branco amarelada dividida por septos de tecido conjuntivo fibroso, em múltiplos lóbulos comprimindo o parênquima hepático adjacente. (E) Rúmen, proliferação neoplásica invasiva de ceratinócitos, com formação de pérolas de queratina. HE, obj.20x. (F) Observa-se infiltrado de linfócitos e plasmócitos na periferia da neoplasia, além de áreas multifocais de mineralização, em meio à massa tumoral. HE, obj.20x.
Na histologia, as massas tumorais correspondiam a carcinomas de células escamosas, caracterizados pela proliferação de queratinócitos, moderadamente, diferenciados, não encapsulados e com comportamento invasivo. As células se arranjavam em ilhas ou trabéculas, formando concreções lamelares concêntricas eosinofílicas (pérolas de queratina), sustentadas por moderado a abundante estroma fibrovascular (Fig.4E). Observou-se também, desmoplasia acentuada, áreas de necrose, mineralização (Fig.4F), hemorragia e displasia do epitélio adjacente ao sítio tumoral. Havia ainda, em áreas adjacentes, infiltrado multifocal de linfócitos, plasmócitos, macrófagos e, em áreas com mineralização acentuada, células gigantes multinucleadas. Os papilomas, por sua vez, consistiam em proliferações exofíticas papilomatosas de queratinócitos bem diferenciados, suportados por discreto tecido fibrovascular.
As metástases de carcinoma de células escamosas nos linfonodos preenchiam os seios medulares e subcapsulares e obliteravam a arquitetura nodal. Eventualmente, havia áreas de mineralização associada a macrófagos, eosinófilos e células gigantes multinucleadas. No caso com metástase hepática, o neoplasma substituía o parênquima do órgão e a luz de grandes vasos. No caso do bovino com perfuração do rúmen, havia uma área, focalmente, extensa de necrose transmural ruminal, com hemorragia e intensa deposição de fibrina, associada ao carcinoma de células escamosas. Na serosa dos órgãos da cavidade abdominal, havia peritonite fibrinosupurativa acentuada, com miríades de bactérias cocoides.
Controle de Pteridium arachnoideum através do uso de herbicidas
Tentativas de controle, baseadas no uso de agentes químicos haviam sido realizadas em anos anteriores, porém, aparentemente, a interrupção precoce dos tratamentos e a aplicação localizada dos produtos, conforme relatado pelo encarregado local, comprometeram o sucesso dessas tentativas. O controle químico de toda a área da propriedade destinada à bovinocultura, através da consorciação picloram e metsulfurom-metílico resultou na redução de 50% a 90% de cobertura da planta, ao longo dos três anos de estudo. No entanto, observou-se a permanência de alguns bolsões da planta em áreas de difícil acesso para o maquinário, como no interior e no entorno das valas de condução da água, anteriormente, utilizadas no cultivo de arroz.
Controle de Pteridium arachnoideum por pastejo de ovinos
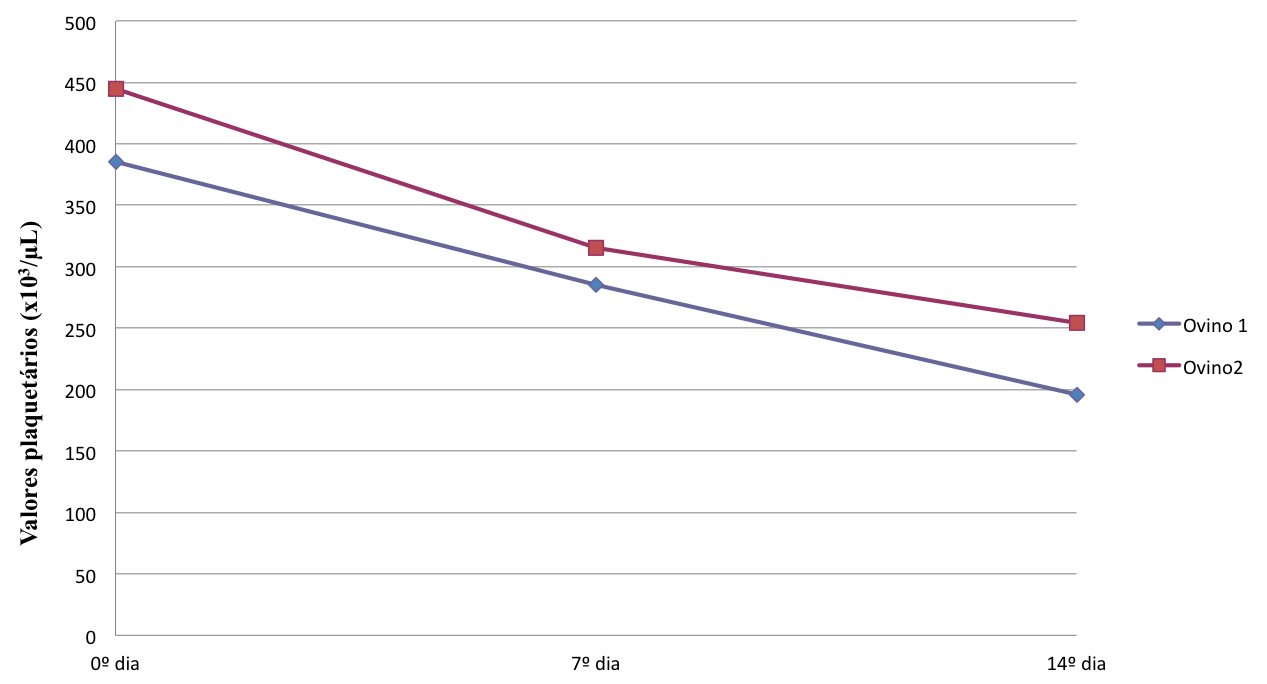
Durante as visitas semanais à propriedade, antes do manejo sanitário, observava-se que os ovinos demonstravam predileção às gramíneas nativas e excluíam a samambaia da dieta. Apenas, raramente, constataram-se ovinos ingerindo pequenas porções de brotos de samambaia. A inspeção visual da planta no piquete também revelou raros sinais de consumo das partes aéreas. Durante o período de maio de 2012 a março de 2013, os ovinos não apresentaram quaisquer sinais clínicos compatíveis com intoxicação por samambaia, assim como não houve animais com escore corporal baixo ou mesmo com perda fetal. Oito cordeiros nasceram no período de outubro e novembro de 2012. Dos 36 ovinos que constituíam o rebanho após a parição, três ovinos morreram por parasitose e dois foram subtraídos por furto. Os dois ovinos (1 e 2) transferidos ao SPV-UFRGS para a realização da indução ao consumo de samambaia, apresentaram consumo voluntário da planta durante todo o período da indução. Não foram observadas alterações clínicas, mas durante o período de adaptação, o ovino 2 perdeu 6,1kg de peso corporal; enquanto, o ovino 1 manteve o peso. Ao final da indução, a quantidade total de samambaia consumida, pelos dois ovinos, foi de 13,952kg, e os parâmetros clínicos diários dos ovinos se mantiveram dentro dos padrões. A contagem de plaquetas apresentou queda nos valores ao longo do experimento, demonstrando o efeito trombocitopênico decorrente do consumo da planta. Os valores da contagem de plaquetas estão apresentados na Figura 5. No 22º dia de indução, encerrou-se o fornecimento de samambaia e, no 24º, os ovinos foram recolocados no potreiro infestado . Mesmo após a reintrodução dos ovinos induzidos ao consumo, não se observou qualquer diferença no consumo de P. arachnoideum pelo rebanho, tampouco foi observado consumo pelos ovino 1 e 2 (Fig.6). Na metade de março de 2013, encerrou-se a tentativa de controle com ovinos. Adicionalmente, após o pastejo no potreiro infestado pela planta, oito ovinos do rebanho permaneceram sendo observados no aprisco do SPV-UFRGS, sem receber a planta por um período de três anos, em que não manifestaram qualquer sinal clínico compatível com intoxicação por samambaia.
Valores plaquetários dos dois ovinos ao longa da indução ao consumo de Pteridium arachnoideum. Valor de referência para espécie ovina = 250-750x103/μL (Fonte: Kaneko et al. 1997Kaneko J.J., Harvey J.W. & Bruss M.L. 1997. Clinical Biochemistry of Domestic Animals. 5th ed. Academic Press, San Diego. 932p.).
Aspecto visual da cobertura vegetal da área experimental. (A) Severa infestação por samambaia, em abril de 2012, antes da introdução dos ovinos. (B) Vegetação baixa após roçada, em julho de 2012, ovinos introduzidos há, aproximadamente, dois meses. (C) Experimento de indução de consumo por ingestão voluntária de samambaia por ovinos. (D) Severa infestação por samambaia e supressão da vegetação restante do campo, em janeiro de 2013, ovinos introduzidos há oito meses.
Discussão e Conclusões
Os diagnósticos dos quadros de diátese hemorrágica e de carcinomas do trato digestório superior por consumo de Pteridium arachnoideum foram baseados nos achados clínicos e patológicos semelhantes aos descritos por diversos autores em bovinos intoxicados tanto natural quanto experimentalmente (Tokarnia et al. 1967Tokarnia C.H., Döbereiner J. & Canella C.F. 1967. Ocorrência da intoxicação aguda pela “samambaia” (Pteridium aquilinum (L.) Kuhn) em bovinos no Brasil. Pesq. Agropec. Bras., Seção Veterinária 2:329-336., Hirono et al. 1984Hirono I., Kono Y., Takahashi K., Yamada K., Niwa H., Ojika M., Kigoshi H., Niiyama K. & Uosaki Y. 1984. Reproduction of acute bracken poisoning in a calf with ptaquiloside, a bracken constituent. Vet. Rec. 115(15):375-378. <http://dx.doi.org/10.1136/vr.115.15.375> <PMid:6506412>
https://doi.org/10.1136/vr.115.15.375...
, Barros et al. 1987Barros C.S.L., Graça D.L., Santos M.N. & Barros S.S. 1987. Intoxicação aguda por samambaia (Pteridium aquilinum) em bovinos no Rio Grande do Sul. Hora Vet. 7:333-339., Gava et al. 2002Gava A., Neves D.S., Gava D., Moura S.T., Schild A.L. & Riet-Correa F. 2002. Bracken fern (Pteridium aquilinum) poisoning in cattle in southern Brazil. Vet. Hum. Toxicol. 44(6):362-365. <PMid:12458643>, Souto et al. 2006Souto M.A.M., Kommers G.D., Barros C.S.L., Piazer J.V.M., Rech R.R., Riet-Correa F. & Schild A.L. 2006. Neoplasias do trato alimentar superior de bovinos associadas ao consumo espontâneo de samambaia (Pteridium aquilinum). Pesq. Vet. Bras. 26(2):112-122. <http://dx.doi.org/10.1590/S0100-736X2006000200009>
https://doi.org/10.1590/S0100-736X200600...
, Anjos et al. 2008Anjos B.L., Irigoyen L.F., Fighera R.A., Gomes A.D., Kommers G.D. & Barros C.S.L. 2008. Intoxicação aguda por samambaia (Pteridium aquilinum) em bovinos na Região Central do Rio Grande do Sul. Pesq. Vet. Bras. 28(10):501-507. <http://dx.doi.org/10.1590/S0100-736X2008001000010>
https://doi.org/10.1590/S0100-736X200800...
, Anjos et al. 2009Anjos B.L., Irigoyen L.F., Piazer J.V., Brum J.S., Fighera R.A. & Barros C.S.L. 2009. Intoxicação experimental aguda por samambaia (Pteridium aquilinum) em bovinos. Pesq. Vet. Bras. 29(9):753-766. <http://dx.doi.org/10.1590/S0100-736X2009000900013>
https://doi.org/10.1590/S0100-736X200900...
, Furlan et al. 2014aFurlan F.H., Mendes E.R.S., Ducatti K.R., Marcon G.C., Dombrosky T., Amorim T.M. & Riet-Correa F. 2014a. Intoxicação aguda por Pteridium arachnoideum e Pteridium caudatum em bovinos e distribuição das plantas em Mato Grosso. Pesq. Vet. Bras. 34(4):343-348. <http://dx.doi.org/10.1590/S0100-736X2014000400008>
https://doi.org/10.1590/S0100-736X201400...
).
Na propriedade estudada, a intoxicação por Pteridium arachnoideum tem sido um problema constante na produção de bovinos, devido não somente à mortalidade anual, mas também decorrente dos custos associados ao tratamento e ao controle químico e mecânico das populações de samambaia. Levantamentos realizados em laboratórios de diagnóstico no Rio Grande do Sul têm demonstrado que a intoxicação por Pteridium arachnoideum está entre as principais causas de morte em bovinos por plantas tóxicas nesse estado (Riet-Correa & Medeiros 2001Riet-Correa F. & Medeiros R.M.T. 2001. Intoxicações por plantas em ruminantes no Brasil e no Uruguai: importância econômica, controle e riscos para saúde pública. Pesq. Vet. Bras. 21(1):38-42. <http://dx.doi.org/10.1590/S0100-736X2001000100008>
https://doi.org/10.1590/S0100-736X200100...
, Rissi et al. 2007Rissi D.R., Rech R.R., Pierezan F., Gabriel A.L., Trost M.E., Brum J.S., Kommers G.D. & Barros C.S.L. 2007. Intoxicações por plantas e micotoxinas associadas a plantas em bovinos no Rio Grande do Sul: 461 casos. Pesq. Vet. Bras. 27(7):261-268. <http://dx.doi.org/10.1590/S0100-736X2007000700002>
https://doi.org/10.1590/S0100-736X200700...
, Antoniassi et al. 2011Antoniassi N.A.B., Raymundo D.L., Boabaid F.M., Juffo G.D., Bandarra P.M., Pedroso P.M.O., Cruz C.E.F. & Driemeier D. 2011. Poisonous plants affecting ruminants in southern Brazil, p.87-90. In: Riet-Correa F., Pfister J., Schild A.L. & Wierenga T. (Eds), Poisoning by Plants, Mycotoxins and Related Toxins. CABI International, Oxford, Oxfordshire. <http://dx.doi.org/10.1079/9781845938338.0087>.
https://doi.org/10.1079/9781845938338.00...
, Lucena et al. 2011Lucena R.B., Rissi D.R., Kommers G.D., Pierezan F., Oliveira-Filho J.C., Macêdo J.T., Flores M.M. & Barros C.S.L. 2011. A retrospective study of 586 tumours in brazilian cattle. J. Comp. Pathol. 145(1):20-24. <http://dx.doi.org/10.1016/j.jcpa.2010.11.002> <PMid:21247583>
https://doi.org/10.1016/j.jcpa.2010.11.0...
). Dessa forma, conclui-se que as perdas registradas nessa propriedade não são um evento isolado, mas reproduzem condição comum em propriedades no Rio Grande do Sul, bem como em outras partes do Brasil e do mundo, haja vista a distribuição cosmopolita desta planta (Roos et al. 2010Roos K., Rödel H.G. & Beck E. 2010. Short- and long-term effects of weed control in pastures infested with Pteridium arachnoideum and an attempt to regenerate abandoned pastures in South Ecuador. Weed Res. 51(2):165-176. <http://dx.doi.org/10.1111/j.1365-3180.2010.00833.x>
https://doi.org/10.1111/j.1365-3180.2010...
, Tokarnia et al. 2012aTokarnia C.H., Brito M.F., Barbosa J.D., Peixoto P.V. & Döbereiner J. 2012a. Plantas de ação radiomimética, p.349-364. In: Ibid. (Eds), Plantas Tóxicas do Brasil para Animais de Produção. 2ª ed. Helianthus, Rio de Janeiro., Furlan et al. 2014aFurlan F.H., Mendes E.R.S., Ducatti K.R., Marcon G.C., Dombrosky T., Amorim T.M. & Riet-Correa F. 2014a. Intoxicação aguda por Pteridium arachnoideum e Pteridium caudatum em bovinos e distribuição das plantas em Mato Grosso. Pesq. Vet. Bras. 34(4):343-348. <http://dx.doi.org/10.1590/S0100-736X2014000400008>
https://doi.org/10.1590/S0100-736X201400...
, 2014bFurlan F.H., Costa F.L., Torres Junior S.C.S., Kerber F.L., Damasceno E.S., Salino A. & Riet-Correa F. 2014b. Perfil de propriedades rurais com pastos invadidos por Pteridium arachnoideum na região norte de Mato Grosso e prevalência de hematúria enzoótica bovina. Pesq. Vet. Bras. 34(8):753-759. <http://dx.doi.org/10.1590/S0100-736X2014000800008>
https://doi.org/10.1590/S0100-736X201400...
). Acredita-se, entretanto, que, principalmente as mortes associadas à forma aguda da intoxicação possam ainda estar sendo subestimadas devido à semelhança na apresentação clínica com outras enfermidades que cursam com hipertermia, como a tristeza parasitária bovina, muito mais conhecida no meio rural do Sul do Brasil (Sippel 1952Sippel W.L. 1952. Bracken fern poisoning. J. Am. Vet. Med. Assoc. 121(904):9-13. <PMid:14927519>, Tokarnia et al. 1967Tokarnia C.H., Döbereiner J. & Canella C.F. 1967. Ocorrência da intoxicação aguda pela “samambaia” (Pteridium aquilinum (L.) Kuhn) em bovinos no Brasil. Pesq. Agropec. Bras., Seção Veterinária 2:329-336.).
As causas conhecidas que estimulam o consumo de P. arachnoideum por bovinos incluem a baixa disponibilidade de pastagens, a contaminação do feno pela planta, a carência de fibras na alimentação, a roçada ou queimada dos campos infestados, com subsequente rebrota, além da introdução de animais provindos de áreas livres da planta (Barros et al. 1987Barros C.S.L., Graça D.L., Santos M.N. & Barros S.S. 1987. Intoxicação aguda por samambaia (Pteridium aquilinum) em bovinos no Rio Grande do Sul. Hora Vet. 7:333-339., Tokarnia et al. 2012aTokarnia C.H., Brito M.F., Barbosa J.D., Peixoto P.V. & Döbereiner J. 2012a. Plantas de ação radiomimética, p.349-364. In: Ibid. (Eds), Plantas Tóxicas do Brasil para Animais de Produção. 2ª ed. Helianthus, Rio de Janeiro.). No nosso estudo, a maior parte dos casos agudos ocorreu entre os meses de abril e setembro, período em que o pasto nativo se torna mais escasso. Além disso, a roçada de campos invadidos por P. arachnoideum, aparentemente, predispõe à ocorrência de casos de intoxicação aguda pela planta, como no surto de mortalidade de bezerros, no ano de 2012. O fato se deve, provavelmente, ao consumo de grandes quantidades de brotos, dotados de altas doses do princípio ativo. É válido lembrar ainda que, segundo alguns autores, após experimentar a planta, provavelmente o bovino adquira o vício em consumi-la (Sippel 1952Sippel W.L. 1952. Bracken fern poisoning. J. Am. Vet. Med. Assoc. 121(904):9-13. <PMid:14927519>, Tokarnia et al. 2007Tokarnia C.H., Döbereiner J., Peixoto P.V., Barbosa J.D., Brito M.F. & Silva M.F. 2007. Plantas Tóxicas da Amazônia a Bovinos e outros Herbívoros. 2ª ed. INPA, Manaus. 97p.). Embora não haja confirmação da importância para o consumo de samambaia por ruminantes, talvez possa ocorrer facilitação social, em que um animal passa a ingerir uma planta e acaba induzindo os demais ao consumo, semelhante ao que é visto em outras plantas tóxicas, como Ipomoea carnea subsp. fistulosa ou Turbina cordata (Pessoa et al. 2013Pessoa C.R.M., Medeiros R.M.T. & Riet-Correa F. 2013. Importância econômica, epidemiologia e controle das intoxicações por plantas no Brasil. Pesq. Vet. Bras. 33(6):752-758. <http://dx.doi.org/10.1590/S0100-736X2013000600011>
https://doi.org/10.1590/S0100-736X201300...
).
Outra constatação importante diz respeito à mortalidade total na propriedade, que apresentou uma média aproximada de 11,46% no período de janeiro de 2012 a janeiro de 2015. Segundo o veterinário responsável, esse índice vem diminuindo e está estabilizando em cerca de 5% nos últimos anos. Essa condição está associada ao incremento das técnicas de manejo utilizadas, especialmente o controle integrado da intoxicação por P. arachnoideum que inclui a diminuição da infestação das pastagens através do controle químico e prevenção dos principais fatores de risco associados com o consumo da samambaia através do fornecimento de pré-secado durante o vazio forrageiro, transferência da temporada de parição para agosto, desmame no verão e o fim do desmame precoce. Todas essas medidas visaram evitar escassez alimentar, principalmente, de alimento fibroso, para os bezerros ao desmame, pois tratam-se de importantes fatores predisponentes para ocorrência de intoxicação pela planta (Barros et al. 1987Barros C.S.L., Graça D.L., Santos M.N. & Barros S.S. 1987. Intoxicação aguda por samambaia (Pteridium aquilinum) em bovinos no Rio Grande do Sul. Hora Vet. 7:333-339., Tokarnia et al. 2012aTokarnia C.H., Brito M.F., Barbosa J.D., Peixoto P.V. & Döbereiner J. 2012a. Plantas de ação radiomimética, p.349-364. In: Ibid. (Eds), Plantas Tóxicas do Brasil para Animais de Produção. 2ª ed. Helianthus, Rio de Janeiro.).
Os sinais clínicos e achados patológicos característicos da forma aguda incluem hipertermia, hemorragias em diversos órgãos e rarefação acentuada das células da medula óssea (Hirono et al. 1984Hirono I., Kono Y., Takahashi K., Yamada K., Niwa H., Ojika M., Kigoshi H., Niiyama K. & Uosaki Y. 1984. Reproduction of acute bracken poisoning in a calf with ptaquiloside, a bracken constituent. Vet. Rec. 115(15):375-378. <http://dx.doi.org/10.1136/vr.115.15.375> <PMid:6506412>
https://doi.org/10.1136/vr.115.15.375...
, Anjos et al. 2008Anjos B.L., Irigoyen L.F., Fighera R.A., Gomes A.D., Kommers G.D. & Barros C.S.L. 2008. Intoxicação aguda por samambaia (Pteridium aquilinum) em bovinos na Região Central do Rio Grande do Sul. Pesq. Vet. Bras. 28(10):501-507. <http://dx.doi.org/10.1590/S0100-736X2008001000010>
https://doi.org/10.1590/S0100-736X200800...
), os quais foram, constantemente, observados nos casos registrados na propriedade. Neste estudo foram constatados, adicionalmente, quadros de dispneia e estertores respiratórios, que estavam associados a edema e hemorragias na laringe, faringe e nos tecidos moles adjacentes. De forma semelhante ao que foi descrito por outros autores, esses quadros ocorreram, principalmente, em bovinos jovens (Sippel 1952Sippel W.L. 1952. Bracken fern poisoning. J. Am. Vet. Med. Assoc. 121(904):9-13. <PMid:14927519>, Radostits et al. 2002Radostits O.M., Gay C.C., Blood D.C. & Hinchcliff K.W. 2002. Principais fitotoxinas causadoras de doenças: Intoxicação por ptaquilosídeo, p.1498-1501. In: Ibid. (Eds), Clínica Veterinária: um tratado de doenças dos bovinos, ovinos, suínos, caprinos e equinos. 9ª ed. Guanabara Koogan, Rio de Janeiro.). Especula-se que essa manifestação esteja relacionada a danos infligidos aos mastócitos teciduais, com liberação de histamina e consequentes aumento do diâmetro e da permeabilidade vascular, culminando em edema (Radostits et al. 2002Radostits O.M., Gay C.C., Blood D.C. & Hinchcliff K.W. 2002. Principais fitotoxinas causadoras de doenças: Intoxicação por ptaquilosídeo, p.1498-1501. In: Ibid. (Eds), Clínica Veterinária: um tratado de doenças dos bovinos, ovinos, suínos, caprinos e equinos. 9ª ed. Guanabara Koogan, Rio de Janeiro.), embora a diminuição das proteínas plasmáticas, observada na intoxicação aguda, também tenha sido cogitada (Sippel 1952Sippel W.L. 1952. Bracken fern poisoning. J. Am. Vet. Med. Assoc. 121(904):9-13. <PMid:14927519>). Quadros semelhantes a esses foram, escassamente, descritos no Brasil (Gonçalves et al. 2009Gonçalves R.C., Pereira E.C., Toma H.S., Delfiol D.J.Z., Shiacchio S.B., Borges A.S. & Amorim R.M. 2009. Intoxicação aguda por Pteridium aquilinum em dois bovinos. Anais VIII Congresso Brasileiro de Buiatria, Belo Horizonte. Ciênc. Anim. Bras. 10(Supl.1):302-307., Anjos et al. 2009Anjos B.L., Irigoyen L.F., Piazer J.V., Brum J.S., Fighera R.A. & Barros C.S.L. 2009. Intoxicação experimental aguda por samambaia (Pteridium aquilinum) em bovinos. Pesq. Vet. Bras. 29(9):753-766. <http://dx.doi.org/10.1590/S0100-736X2009000900013>
https://doi.org/10.1590/S0100-736X200900...
).
Alguns autores subdividem o quadro clínico-patológico da intoxicação aguda por Pteridium spp. em bovinos em dois tipos, o primeiro chamado “entérico”, caracterizado por apatia, inapetência, hipertermia, pulso fraco, palidez e sangramento nas mucosas, além de enterite com coágulos de sangue nas fezes, enquanto que o segundo tipo, chamado “laríngeo”, cursa com hipertermia, estertor, dificuldade respiratória, associado a hemorragias e edema de laringe (Fletcher 1944Fletcher J.M. 1944. Bracken poisoning in cattle. Vet Rec. 56(49):478., Sippel 1952Sippel W.L. 1952. Bracken fern poisoning. J. Am. Vet. Med. Assoc. 121(904):9-13. <PMid:14927519>). No entanto, diante dos diversos casos naturais acompanhados na propriedade em que se observou edema laríngeo, juntamente com achados característicos da forma entérica, podemos concluir, conforme também proposto por Anjos et al. (2009)Anjos B.L., Irigoyen L.F., Piazer J.V., Brum J.S., Fighera R.A. & Barros C.S.L. 2009. Intoxicação experimental aguda por samambaia (Pteridium aquilinum) em bovinos. Pesq. Vet. Bras. 29(9):753-766. <http://dx.doi.org/10.1590/S0100-736X2009000900013>
https://doi.org/10.1590/S0100-736X200900...
, que essas apresentações podem se sobrepor.
O ptaquilosídeo, princípio ativo presente na planta, possui ação radiomimética e é responsável pela redução progressiva das células hematopoiéticas da medula óssea, observada nos quadros de intoxicação aguda (Hirono et al. 1984Hirono I., Kono Y., Takahashi K., Yamada K., Niwa H., Ojika M., Kigoshi H., Niiyama K. & Uosaki Y. 1984. Reproduction of acute bracken poisoning in a calf with ptaquiloside, a bracken constituent. Vet. Rec. 115(15):375-378. <http://dx.doi.org/10.1136/vr.115.15.375> <PMid:6506412>
https://doi.org/10.1136/vr.115.15.375...
). A perda acentuada dessas populações celulares culmina em diátese hemorrágica trombocitopênica, por afetar a formação do tampão plaquetário (hemostasia primária), agravada pela septicemia, decorrente da neutropenia (Valli 2007Valli V.E.O. 2007. Hematopoietic system, p.107-324. In: Jubb K.V.F., Kennedy P.C. & Palmer N. (Eds). Pathology of Domestic Animals. Vol.3. 5th ed. Saunders Elsevier, Edinburgh.). Adicionalmente, a bacteremia pode levar a trombose e, portanto, originar infartos (Radostits et al. 2002Radostits O.M., Gay C.C., Blood D.C. & Hinchcliff K.W. 2002. Principais fitotoxinas causadoras de doenças: Intoxicação por ptaquilosídeo, p.1498-1501. In: Ibid. (Eds), Clínica Veterinária: um tratado de doenças dos bovinos, ovinos, suínos, caprinos e equinos. 9ª ed. Guanabara Koogan, Rio de Janeiro.), como aqueles vistos no fígado, baço, pulmões e rins de alguns dos casos acompanhados.
Neste estudo, os carcinomas do trato digestório superior foram registrados com menor frequência do que a forma aguda da intoxicação, possivelmente devido à ocorrência de surtos de mortalidade na forma aguda. A forma crônica da intoxicação com desenvolvimento de carcinomas teve importância, por ocasionar a mortalidade de vacas em idade reprodutiva. Além disso, para o desenvolvimento da forma crônica, os bovinos precisam consumir pequenas quantidades da planta ao longo de vários meses ou anos (Tokarnia et al. 2012aTokarnia C.H., Brito M.F., Barbosa J.D., Peixoto P.V. & Döbereiner J. 2012a. Plantas de ação radiomimética, p.349-364. In: Ibid. (Eds), Plantas Tóxicas do Brasil para Animais de Produção. 2ª ed. Helianthus, Rio de Janeiro.), consequentemente, essas mortes ocorrem de forma esporádica na propriedade.
O caráter irreversível da intoxicação pelo Pteridium archnoideum, a prevalência elevada no Brasil, a alta letalidade e os consequentes prejuízos econômicos qualificam a intoxicação por P. arachnoideum como doença de controle prioritário para a pecuária nacional (Riet-Correa & Medeiros 2001Riet-Correa F. & Medeiros R.M.T. 2001. Intoxicações por plantas em ruminantes no Brasil e no Uruguai: importância econômica, controle e riscos para saúde pública. Pesq. Vet. Bras. 21(1):38-42. <http://dx.doi.org/10.1590/S0100-736X2001000100008>
https://doi.org/10.1590/S0100-736X200100...
, Souto et al. 2006Souto M.A.M., Kommers G.D., Barros C.S.L., Piazer J.V.M., Rech R.R., Riet-Correa F. & Schild A.L. 2006. Neoplasias do trato alimentar superior de bovinos associadas ao consumo espontâneo de samambaia (Pteridium aquilinum). Pesq. Vet. Bras. 26(2):112-122. <http://dx.doi.org/10.1590/S0100-736X2006000200009>
https://doi.org/10.1590/S0100-736X200600...
, Anjos et al. 2008Anjos B.L., Irigoyen L.F., Fighera R.A., Gomes A.D., Kommers G.D. & Barros C.S.L. 2008. Intoxicação aguda por samambaia (Pteridium aquilinum) em bovinos na Região Central do Rio Grande do Sul. Pesq. Vet. Bras. 28(10):501-507. <http://dx.doi.org/10.1590/S0100-736X2008001000010>
https://doi.org/10.1590/S0100-736X200800...
, Tokarnia et al. 2012aTokarnia C.H., Brito M.F., Barbosa J.D., Peixoto P.V. & Döbereiner J. 2012a. Plantas de ação radiomimética, p.349-364. In: Ibid. (Eds), Plantas Tóxicas do Brasil para Animais de Produção. 2ª ed. Helianthus, Rio de Janeiro.). Os métodos de controle das perdas devem ser direcionados à prevenção da ingestão da planta pelos bovinos, visto que não há tratamento efetivo para a intoxicação. Neste sentido, o uso de ovinos como controle biológico de populações de P. arachnoideum surgiu como uma alternativa a ser testada, dado o potencial da espécie como método de controle de diferentes plantas daninhas e tóxicas (Holloway 1968Holloway J.K. 1968. Proyectos en el control biologico de las malas hierbas, p.761-785. In: DeBach P. (Ed.), Control Biologico de Las Plagas de Insectos y Malas Hierbas. Compañia Editorial Continental, Buenos Aires., Bandarra et al. 2012Bandarra P.M., Oliveira L.G.S., Dalto A.C., Boabaid F.M., Juffo G., Riet-Correa F., Driemeier D. & Cruz C.E.F. 2012. Sheep production as a Senecio spp. control tool. Pesq. Vet. Bras. 32(10):1017-1022. <http://dx.doi.org/10.1590/S0100-736X2012001000013>
https://doi.org/10.1590/S0100-736X201200...
).
Segundo alguns autores, os ovinos parecem ser menos suscetíveis à intoxicação pela planta, o que pode ser devido a mecanismos particulares de detoxificação hepática ou adaptação de flora ruminal, ou talvez, devido ao seu hábito de pastejo, por serem relutantes em consumir a planta em quantidades suficientes para ocasionar a apresentação clínica (Parker & McCrea 1965Parker W.H. & McCrea C.T. 1965. Bracken (Pteris aquilina) poisoning of sheep in the North York Moors. Vet. Rec. 77(30):861-865. <PMid:14331487>, Sunderman 1987Sunderman F.M. 1987. Bracken poisoning in sheep. Aust. Vet. J. 64(1):25-26. <http://dx.doi.org/10.1111/j.1751-0813.1987.tb06053.x> <PMid:3593134>
https://doi.org/10.1111/j.1751-0813.1987...
, Kellerman et al. 2005Kellerman T.S., Coetzer J.A.W., Naude T.W. & Botha C.J. 2005. Plant Poisonings and Mycotoxicoses of Livestock in Southern Africa. 2nd ed. Oxford University Press, Oxford. 310p.). Além disso, notamos que, apesar das consideráveis perdas de bovinos intoxicados por Pteridium sp. em nossa região e a observação de infestação de samambaia também em propriedades de criação de ovinos, a intoxicação nesta espécie não tem sido relatada. A carência de informações referentes à metodologia aplicável para tanto (lotação, período, uso de espécies herbívoras associadas, época de introdução, etc.) e ao desempenho produtivo de rebanhos ovinos mantidos em pastejo de áreas invadidas pela planta motivou a realização desse trabalho.
A utilização de ovinos para controlar as populações de P. arachnoideum, do mesmo modo que controlam Senecio spp. (Bandarra et al. 2012Bandarra P.M., Oliveira L.G.S., Dalto A.C., Boabaid F.M., Juffo G., Riet-Correa F., Driemeier D. & Cruz C.E.F. 2012. Sheep production as a Senecio spp. control tool. Pesq. Vet. Bras. 32(10):1017-1022. <http://dx.doi.org/10.1590/S0100-736X2012001000013>
https://doi.org/10.1590/S0100-736X201200...
) se mostrou ineficiente em uma lotação de quatro ovinos por hectare. A opção de não exceder a lotação do piquete foi para que não se prejudicasse o desempenho produtivo e reprodutivo do rebanho, já que esses são fatores essenciais na criação de qualquer espécie de valor zootécnico. Além disso, a indução ao consumo também não apresentou resultados satisfatórios, pois ao serem reintroduzidos, os dois ovinos não mantiveram o hábito de consumir a planta em condições de campo e, consequentemente, não estimularam os demais ao consumo. Finalmente, apesar do reduzido potencial da espécie como controle biológico da planta, não se observou alteração compatível com intoxicação por P. arachnoideum em qualquer dos ovinos introduzidos ou nascidos na área experimental, mesmo com os altos níveis de infestação presentes nesse campo, o que sugere potencial aplicabilidade da ovinocultura em áreas, severamente, infestadas por P. arachnoideum.
O controle químico da samambaia tem se mostrado um método relativamente efetivo no controle da planta (Le Duc 2000Le Duc M.G. 2000. The variable responses of bracken fronds to control treatments in Great Britain. Annals of Botany. 85:17-29. <http://dx.doi.org/10.1006/anbo.1999.1052>
https://doi.org/10.1006/anbo.1999.1052...
). Em um experimento realizado no Equador, os mesmos herbicidas empregados na propriedade estudada (picloram e metsulfurom-metílico), demonstraram ser mais eficazes que outros princípios, embora, não tenham conseguido erradicar a planta após seis aplicações em um período de 23 meses (Roos et al. 2010Roos K., Rödel H.G. & Beck E. 2010. Short- and long-term effects of weed control in pastures infested with Pteridium arachnoideum and an attempt to regenerate abandoned pastures in South Ecuador. Weed Res. 51(2):165-176. <http://dx.doi.org/10.1111/j.1365-3180.2010.00833.x>
https://doi.org/10.1111/j.1365-3180.2010...
). Apesar dessa combinação de compostos possibilitar a redução das populações de Pteridium sp., ainda há muitas controvérsias quanto à sua aplicação, pois é sabido que, quando herbicidas com o mesmo modo de ação são aplicados, repetidamente, por vários anos para controlar a mesma espécie de planta invasora, biótipos resistentes da planta podem sobreviver ao tratamento, propagar e passar a dominar a área (Rodrigues & Almeida 2005Rodrigues B.N. & Almeida F.S. 2005. Guia de Herbicidas. 5ª ed. Grafmarke, Londrina. 592p).
Além disso, outro fator negativo da utilização de controle químico, principalmente se aplicado sem orientação profissional, é o efeito ambiental decorrente da baixa especificidade de ação sobre o organismo alvo. Dessa forma, é preciso levar em conta quais as outras espécies vegetais, ou mesmo animais que serão afetadas com seu uso sistemático. Nesse contexto, há produtos com efeito em um amplo grupo de organismos, desde vegetais até animais vertebrados, envolvendo os animais de interesse pecuário e mesmo o ser humano. Outros compostos podem afetar vegetais cultivados, inclusive forrageiras, ou ainda, o campo nativo e sua intrincada rede de interações ecológicas, o que poderia resultar em declínio de produtividade de forma indireta (Freemark & Boutin 1995Freemark K. & Boutin C. 1995. Impacts of agricultural herbicide use on terrestrial wildlife in temperate landscapes: a review with special reference to North America. Agricult. Ecosyst. Environ. 52(2-3):67-91. <http://dx.doi.org/10.1016/0167-8809(94)00534-L>
https://doi.org/10.1016/0167-8809(94)005...
).
A solução da questão reside, portanto, na escolha do agente químico com melhor ação sobre a planta alvo, neste caso Pteridium arachnoideum, considerando-se o menor impacto sobre os outros elementos do ambiente. Entretanto, tais qualidades são dificilmente encontradas juntas em um mesmo princípio ativo (Roos et al. 2010Roos K., Rödel H.G. & Beck E. 2010. Short- and long-term effects of weed control in pastures infested with Pteridium arachnoideum and an attempt to regenerate abandoned pastures in South Ecuador. Weed Res. 51(2):165-176. <http://dx.doi.org/10.1111/j.1365-3180.2010.00833.x>
https://doi.org/10.1111/j.1365-3180.2010...
) e, depende-se de aplicação racional e seletiva, de forma que os produtos não causem prejuízos na pastagem, desequilíbrio ao ambiente, ou contaminem os produtos de origem animal e fontes de água.
Referências
- Anjos B.L., Irigoyen L.F., Fighera R.A., Gomes A.D., Kommers G.D. & Barros C.S.L. 2008. Intoxicação aguda por samambaia (Pteridium aquilinum) em bovinos na Região Central do Rio Grande do Sul. Pesq. Vet. Bras. 28(10):501-507. <http://dx.doi.org/10.1590/S0100-736X2008001000010>
» https://doi.org/10.1590/S0100-736X2008001000010 - Anjos B.L., Irigoyen L.F., Piazer J.V., Brum J.S., Fighera R.A. & Barros C.S.L. 2009. Intoxicação experimental aguda por samambaia (Pteridium aquilinum) em bovinos. Pesq. Vet. Bras. 29(9):753-766. <http://dx.doi.org/10.1590/S0100-736X2009000900013>
» https://doi.org/10.1590/S0100-736X2009000900013 - Antoniassi N.A.B., Raymundo D.L., Boabaid F.M., Juffo G.D., Bandarra P.M., Pedroso P.M.O., Cruz C.E.F. & Driemeier D. 2011. Poisonous plants affecting ruminants in southern Brazil, p.87-90. In: Riet-Correa F., Pfister J., Schild A.L. & Wierenga T. (Eds), Poisoning by Plants, Mycotoxins and Related Toxins. CABI International, Oxford, Oxfordshire. <http://dx.doi.org/10.1079/9781845938338.0087>.
» https://doi.org/10.1079/9781845938338.0087 - Bandarra P.M., Oliveira L.G.S., Dalto A.C., Boabaid F.M., Juffo G., Riet-Correa F., Driemeier D. & Cruz C.E.F. 2012. Sheep production as a Senecio spp. control tool. Pesq. Vet. Bras. 32(10):1017-1022. <http://dx.doi.org/10.1590/S0100-736X2012001000013>
» https://doi.org/10.1590/S0100-736X2012001000013 - Barros C.S.L., Graça D.L., Santos M.N. & Barros S.S. 1987. Intoxicação aguda por samambaia (Pteridium aquilinum) em bovinos no Rio Grande do Sul. Hora Vet. 7:333-339.
- Casagrande R.A., Mazzocco M.B., Frizon R., Lentz D., Traverso S.D. & Gava A. 2008. Doenças de bovinos diagnosticadas pelo laboratório de Patologia Animal CAV/UDESC de janeiro de 2000 a abril de 2008. Anais do 3º Encontro Nacional de Diagnóstico Veterinário, Campo Grande, MS, p.55-56. (Resumo)
- Costa R.M.G., Bastos M.M., Oliveira P.A. & Lopes C. 2012. Bracken-associated human and animal health hazards: chemical, biological and pathological evidence. J. Hazard. Mater. 203-204:1-12. <http://dx.doi.org/10.1016/j.jhazmat.2011.12.046> <PMid:22226718>
» https://doi.org/10.1016/j.jhazmat.2011.12.046 - Fletcher J.M. 1944. Bracken poisoning in cattle. Vet Rec. 56(49):478.
- França T.N., Tokarnia C.H. & Peixoto P.V. 2002. Enfermidades determinadas pelo princípio radiomimético de Pteridium aquilinum (Polypodiaceae). Pesq. Vet. Bras. 22(3):85-96. <http://dx.doi.org/10.1590/S0100-736X2002000300001>
» https://doi.org/10.1590/S0100-736X2002000300001 - Freemark K. & Boutin C. 1995. Impacts of agricultural herbicide use on terrestrial wildlife in temperate landscapes: a review with special reference to North America. Agricult. Ecosyst. Environ. 52(2-3):67-91. <http://dx.doi.org/10.1016/0167-8809(94)00534-L>
» https://doi.org/10.1016/0167-8809(94)00534-L - Furlan F.H., Mendes E.R.S., Ducatti K.R., Marcon G.C., Dombrosky T., Amorim T.M. & Riet-Correa F. 2014a. Intoxicação aguda por Pteridium arachnoideum e Pteridium caudatum em bovinos e distribuição das plantas em Mato Grosso. Pesq. Vet. Bras. 34(4):343-348. <http://dx.doi.org/10.1590/S0100-736X2014000400008>
» https://doi.org/10.1590/S0100-736X2014000400008 - Furlan F.H., Costa F.L., Torres Junior S.C.S., Kerber F.L., Damasceno E.S., Salino A. & Riet-Correa F. 2014b. Perfil de propriedades rurais com pastos invadidos por Pteridium arachnoideum na região norte de Mato Grosso e prevalência de hematúria enzoótica bovina. Pesq. Vet. Bras. 34(8):753-759. <http://dx.doi.org/10.1590/S0100-736X2014000800008>
» https://doi.org/10.1590/S0100-736X2014000800008 - Gava A., Neves D.S., Gava D., Moura S.T., Schild A.L. & Riet-Correa F. 2002. Bracken fern (Pteridium aquilinum) poisoning in cattle in southern Brazil. Vet. Hum. Toxicol. 44(6):362-365. <PMid:12458643>
- Gonçalves R.C., Pereira E.C., Toma H.S., Delfiol D.J.Z., Shiacchio S.B., Borges A.S. & Amorim R.M. 2009. Intoxicação aguda por Pteridium aquilinum em dois bovinos. Anais VIII Congresso Brasileiro de Buiatria, Belo Horizonte. Ciênc. Anim. Bras. 10(Supl.1):302-307.
- Harbutt P.R. & Leaver D.D. 1969. Carcinoma of the bladder of sheep. Aust. Vet. J. 45(10):473-475. <http://dx.doi.org/10.1111/j.1751-0813.1969.tb06593.x> <PMid:5408647>
» https://doi.org/10.1111/j.1751-0813.1969.tb06593.x - Hirono I., Kono Y., Takahashi K., Yamada K., Niwa H., Ojika M., Kigoshi H., Niiyama K. & Uosaki Y. 1984. Reproduction of acute bracken poisoning in a calf with ptaquiloside, a bracken constituent. Vet. Rec. 115(15):375-378. <http://dx.doi.org/10.1136/vr.115.15.375> <PMid:6506412>
» https://doi.org/10.1136/vr.115.15.375 - Hirono I., Ito M., Yagyu S., Haga M., Wakamatsu K., Kishikawa T., Nishikawa O., Yamada K., Ojika M. & Kigoshi H. 1993. Reproduction off progressive retinal degeneration (Bright Blindness) in sheep by administration of ptaquiloside contained in bracken. J. Vet. Med. Sci. 55(6):979-983. <http://dx.doi.org/10.1292/jvms.55.979> <PMid:8117827>
» https://doi.org/10.1292/jvms.55.979 - Hojo-Souza N.S., Carneiro C.M. & Santos R.C. 2010. Pteridium aquilinum: o que sabemos e o que ainda falta saber. Biosci. J. 26(5):798-808.
- Holloway J.K. 1968. Proyectos en el control biologico de las malas hierbas, p.761-785. In: DeBach P. (Ed.), Control Biologico de Las Plagas de Insectos y Malas Hierbas. Compañia Editorial Continental, Buenos Aires.
- Kaneko J.J., Harvey J.W. & Bruss M.L. 1997. Clinical Biochemistry of Domestic Animals. 5th ed. Academic Press, San Diego. 932p.
- Kellerman T.S., Coetzer J.A.W., Naude T.W. & Botha C.J. 2005. Plant Poisonings and Mycotoxicoses of Livestock in Southern Africa. 2nd ed. Oxford University Press, Oxford. 310p.
- Le Duc M.G. 2000. The variable responses of bracken fronds to control treatments in Great Britain. Annals of Botany. 85:17-29. <http://dx.doi.org/10.1006/anbo.1999.1052>
» https://doi.org/10.1006/anbo.1999.1052 - Lucena R.B., Pierezan F., Kommers G.D., Irigoyen L.F., Fighera R.A. & Barros C.S.L. 2010. Doenças de bovinos no Sul do Brasil: 6.706 casos. Pesq. Vet. Bras. 30(5):428-434. <http://dx.doi.org/10.1590/S0100-736X2010000500010>
» https://doi.org/10.1590/S0100-736X2010000500010 - Lucena R.B., Rissi D.R., Kommers G.D., Pierezan F., Oliveira-Filho J.C., Macêdo J.T., Flores M.M. & Barros C.S.L. 2011. A retrospective study of 586 tumours in brazilian cattle. J. Comp. Pathol. 145(1):20-24. <http://dx.doi.org/10.1016/j.jcpa.2010.11.002> <PMid:21247583>
» https://doi.org/10.1016/j.jcpa.2010.11.002 - McCrea C.T. & Head K.W. 1978. Sheep tumours in North East Yorkshire. I. Prevalence on seven moorland farms. Brit. Vet. J. 134(5):454-461. <http://dx.doi.org/10.1016/S0007-1935(17)33387-0> <PMid:698772>
» https://doi.org/10.1016/S0007-1935(17)33387-0 - Papavlasopoulos A.K. 2003. Biological control of Pteridium aquilinum (L.) Kuhn as a realistic prospect. Agro Thesis 1:13-18.
- Parker W.H. & McCrea C.T. 1965. Bracken (Pteris aquilina) poisoning of sheep in the North York Moors. Vet. Rec. 77(30):861-865. <PMid:14331487>
- Pedroso P.M.O., Pescador C.A., Oliveira E.C., Sonne L., Bandarra P.M., Raymundo D.L. & Driemeier D. 2007. Intoxicações naturais por plantas em ruminantes diagnosticadas no Setor de Patologia Veterinária da UFRGS no período de 1996-2005. Acta Scient. Vet. 35(2):213-218.
- Pessoa C.R.M., Medeiros R.M.T. & Riet-Correa F. 2013. Importância econômica, epidemiologia e controle das intoxicações por plantas no Brasil. Pesq. Vet. Bras. 33(6):752-758. <http://dx.doi.org/10.1590/S0100-736X2013000600011>
» https://doi.org/10.1590/S0100-736X2013000600011 - Radostits O.M., Gay C.C., Blood D.C. & Hinchcliff K.W. 2002. Principais fitotoxinas causadoras de doenças: Intoxicação por ptaquilosídeo, p.1498-1501. In: Ibid. (Eds), Clínica Veterinária: um tratado de doenças dos bovinos, ovinos, suínos, caprinos e equinos. 9ª ed. Guanabara Koogan, Rio de Janeiro.
- Riet-Correa F. & Medeiros R.M.T. 2001. Intoxicações por plantas em ruminantes no Brasil e no Uruguai: importância econômica, controle e riscos para saúde pública. Pesq. Vet. Bras. 21(1):38-42. <http://dx.doi.org/10.1590/S0100-736X2001000100008>
» https://doi.org/10.1590/S0100-736X2001000100008 - Rissi D.R., Rech R.R., Pierezan F., Gabriel A.L., Trost M.E., Brum J.S., Kommers G.D. & Barros C.S.L. 2007. Intoxicações por plantas e micotoxinas associadas a plantas em bovinos no Rio Grande do Sul: 461 casos. Pesq. Vet. Bras. 27(7):261-268. <http://dx.doi.org/10.1590/S0100-736X2007000700002>
» https://doi.org/10.1590/S0100-736X2007000700002 - Robinson R.C. 1999. The means to large-scale, effective bracken clearance in the UK, p.156-162. In: Smith R.T. & Taylor J.A. (Eds), Bracken Fern: toxicity, biology and control. International Bracken Group Conference, Manchester.
- Rodrigues B.N. & Almeida F.S. 2005. Guia de Herbicidas. 5ª ed. Grafmarke, Londrina. 592p
- Roos K., Rödel H.G. & Beck E. 2010. Short- and long-term effects of weed control in pastures infested with Pteridium arachnoideum and an attempt to regenerate abandoned pastures in South Ecuador. Weed Res. 51(2):165-176. <http://dx.doi.org/10.1111/j.1365-3180.2010.00833.x>
» https://doi.org/10.1111/j.1365-3180.2010.00833.x - Sippel W.L. 1952. Bracken fern poisoning. J. Am. Vet. Med. Assoc. 121(904):9-13. <PMid:14927519>
- Souto M.A.M., Kommers G.D., Barros C.S.L., Piazer J.V.M., Rech R.R., Riet-Correa F. & Schild A.L. 2006. Neoplasias do trato alimentar superior de bovinos associadas ao consumo espontâneo de samambaia (Pteridium aquilinum). Pesq. Vet. Bras. 26(2):112-122. <http://dx.doi.org/10.1590/S0100-736X2006000200009>
» https://doi.org/10.1590/S0100-736X2006000200009 - Sunderman F.M. 1987. Bracken poisoning in sheep. Aust. Vet. J. 64(1):25-26. <http://dx.doi.org/10.1111/j.1751-0813.1987.tb06053.x> <PMid:3593134>
» https://doi.org/10.1111/j.1751-0813.1987.tb06053.x - Thomson J.A., Mickel J.T. & Mehltreter K. 2008. Taxonomic status and relationships of bracken ferns (Pteridium: Dennstaedtiaceae) of Laurasian affinity in Central and North America. Botanical Journal of the Linnean Society 157(1):1-17. <http://dx.doi.org/10.1111/j.1095-8339.2008.00791.x>
» https://doi.org/10.1111/j.1095-8339.2008.00791.x - Tokarnia C.H., Döbereiner J. & Canella C.F. 1967. Ocorrência da intoxicação aguda pela “samambaia” (Pteridium aquilinum (L.) Kuhn) em bovinos no Brasil. Pesq. Agropec. Bras., Seção Veterinária 2:329-336.
- Tokarnia C.H., Brito M.F., Barbosa J.D., Peixoto P.V. & Döbereiner J. 2012a. Plantas de ação radiomimética, p.349-364. In: Ibid. (Eds), Plantas Tóxicas do Brasil para Animais de Produção. 2ª ed. Helianthus, Rio de Janeiro.
- Tokarnia C.H., Brito M.F., Barbosa J.D., Peixoto P.V. & Döbereiner J. 2012b. Parte Geral, p.5-26. In: Ibid. (Eds), Plantas Tóxicas do Brasil para Animais de Produção. 2ª ed. Helianthus, Rio de Janeiro .
- Tokarnia C.H., Döbereiner J., Peixoto P.V., Barbosa J.D., Brito M.F. & Silva M.F. 2007. Plantas Tóxicas da Amazônia a Bovinos e outros Herbívoros. 2ª ed. INPA, Manaus. 97p.
- Valli V.E.O. 2007. Hematopoietic system, p.107-324. In: Jubb K.V.F., Kennedy P.C. & Palmer N. (Eds). Pathology of Domestic Animals. Vol.3. 5th ed. Saunders Elsevier, Edinburgh.
- Wilson E.O. 2000. Sociobiology: the new synthesis. Belknap, Cambridge. 697p.
Datas de Publicação
-
Publicação nesta coleção
Ago 2018
Histórico
-
Recebido
16 Jan 2018 -
Aceito
29 Jan 2018