Resumos
Três esteroides (espinasterol, espinasterona e glicopiranosil espinasterol) foram isolados do caule de Moutabea guianensis, planta de origem amazônica. Suas estruturas foram determinadas a partir das análises de RMN e por comparação com dados espectroscópicos da literatura. Foram avaliadas as atividades alelopáticas das três substâncias em duas plantas invasoras de pastagens comuns da região amazônica: Mimosa pudica (malícia) e Senna obtusifolia (mata-pasto). A substância glicopiranosil espinasterol foi mais ativa no ensaio de desenvolvimento da radícula, inibindo a espécie Senna obtusifolia em 75%; o espinasterol inibiu em 22% o desenvolvimento do hipocótilo de Senna obtusifolia; e no bioensaio de germinação de sementes as substâncias espinasterol e espinasterona proporcionaram 10% de inibição em Mimosa pudica. A partir desses resultados, observou-se que a diferença de substituintes observada na posição-3 dos esteroides é capaz de alterar a atividade alelopática. O grupo glicosil na posição-3 elevou a atividade alelopática de forma mais expressiva no bioensaio de desenvolvimento de radícula da espécie malícia, quando comparado aos esteroides hidroxilado e carbonilado. Este é o primeiro estudo químico e alelopático do gênero Moutabea.
Moutabea guianensis; Polygalaceae; alelopatia; Senna obtusifolia; Mimosa pudica
Three steroids (spinasterol, spinasterone, and spinasterol glucopyranosyl) were isolated from the stem of the Amazonian plant Moutabea guianensis. Their structures were determined on the basis of NMR analysis and by comparison with spectroscopic data found in the literature. The allelopathic activities of the three substances were evaluated against two common weeds of the Amazon region, Mimosa pudica ('malicia') and Senna obtusifolia ('mata-pasto'). The substance spinasterol glucopyranosyl was the most active in the radicle growth bioassay, inhibiting Senna obtusifolia in 75%; spinasterol inhibited the development of hypocotyl of Senna obtusifolia in 22%, and spinasterone and spinasterol inhibited 10% of the seed germination of the species Mimosa pudica. These results showed that the difference of substitutes at the C-3 position of the steroids can influence allelopathic activity: the glicosyl group at the C-3 position enhanced the inhibition of hypocotyl growth of the species Mimosa pudica, compared to the hydroxilated and carbonylated steroid. This is the first chemical and allelopathic study with Moutabea guianensis.
Moutabea guianensis; Polygalaceae; allelopathy; Senna obtusifolia; Mimosa pudica
ARTIGOS
Bioensaios de atividade alelopática dos esteroides espinasterol, espinasterona e glicopiranosil espinasterol
Bioassays of allelopathic activity of the steroids spinasterol, spinasterone, and spinasterol glicopyranosyl
Ripardo Filho, H.S.I; Pacheco, L.C.II; Souza Filho, A.P.S.III; Guilhon, G.M.S.P.IV; Arruda, M.S.P.IV; Santos, L.S.IV
IDoutorando em Química, Programa de Pós-Graduação em Química, Universidade Federal do Pará - UFPA, Rua Augusto Corrêa, S/N, 66075-900 Belém-PA
IIBolsista de Iniciação Científica - CNPq, UFPA
IIIEngo-Agro., Doutor, Embrapa Amazônia Oriental, Trav. Dr. Enéas Pinheiro, S/N, 66095-100 Belém-PA
IVProf. Dr., Programa de Pós-Graduação em Química, UFPA
RESUMO
Três esteroides (espinasterol, espinasterona e glicopiranosil espinasterol) foram isolados do caule de Moutabea guianensis, planta de origem amazônica. Suas estruturas foram determinadas a partir das análises de RMN e por comparação com dados espectroscópicos da literatura. Foram avaliadas as atividades alelopáticas das três substâncias em duas plantas invasoras de pastagens comuns da região amazônica: Mimosa pudica (malícia) e Senna obtusifolia (mata-pasto). A substância glicopiranosil espinasterol foi mais ativa no ensaio de desenvolvimento da radícula, inibindo a espécie Senna obtusifolia em 75%; o espinasterol inibiu em 22% o desenvolvimento do hipocótilo de Senna obtusifolia; e no bioensaio de germinação de sementes as substâncias espinasterol e espinasterona proporcionaram 10% de inibição em Mimosa pudica. A partir desses resultados, observou-se que a diferença de substituintes observada na posição-3 dos esteroides é capaz de alterar a atividade alelopática. O grupo glicosil na posição-3 elevou a atividade alelopática de forma mais expressiva no bioensaio de desenvolvimento de radícula da espécie malícia, quando comparado aos esteroides hidroxilado e carbonilado. Este é o primeiro estudo químico e alelopático do gênero Moutabea.
Palavras-chave:Moutabea guianensis, Polygalaceae, alelopatia, Senna obtusifolia, Mimosa pudica.
ABSTRACT
Three steroids (spinasterol, spinasterone, and spinasterol glucopyranosyl) were isolated from the stem of the Amazonian plant Moutabea guianensis. Their structures were determined on the basis of NMR analysis and by comparison with spectroscopic data found in the literature. The allelopathic activities of the three substances were evaluated against two common weeds of the Amazon region, Mimosa pudica ('malicia') and Senna obtusifolia ('mata-pasto'). The substance spinasterol glucopyranosyl was the most active in the radicle growth bioassay, inhibiting Senna obtusifolia in 75%; spinasterol inhibited the development of hypocotyl of Senna obtusifolia in 22%, and spinasterone and spinasterol inhibited 10% of the seed germination of the species Mimosa pudica. These results showed that the difference of substitutes at the C-3 position of the steroids can influence allelopathic activity: the glicosyl group at the C-3 position enhanced the inhibition of hypocotyl growth of the species Mimosa pudica, compared to the hydroxilated and carbonylated steroid. This is the first chemical and allelopathic study with Moutabea guianensis.
Keywords:Moutabea guianensis, Polygalaceae, allelopathy, Senna obtusifolia, Mimosa pudica.
INTRODUÇÃO
As formas atuais de controle de plantas daninhas, como roçagem (Chiovato et al., 2007; Tipping, 2008), queimadas (Durigan et al., 2007) e utilização de herbicidas sintéticos (Duke et al., 2007), não estão atendendo às atuais necessidades da sociedade, devido às agressões aos recursos naturais (água e solo), à vida silvestre e aos alimentos dos animais e das pessoas, além de favorecer o aumento sistemático no número de espécies de plantas daninhas resistentes aos atuais produtos no mundo (Owen et al., 2007; Powles & Yu, 2010; Gressel, 2011; Riar et al., 2011). Somada a esses fatores ainda existe a busca dos produtores por herbicidas que possam proporcionar maior produtividade, lucratividade e redução nos gastos com estes produtos. Esses fatores estão forçando os agricultores a buscar novas fontes de herbicidas que atendam às novas exigências.
Aliado a esses aspectos, a percepção de que plantas e microrganismos podem fornecer novas perspectivas de exploração agrícola vem se somar às inúmeras possibilidades de uso da biodiversidade. Especificamente na região amazônica, pela rica e diversificada biodiversidade, as espécies que compõem a floresta tropical podem representar fonte ímpar para a descoberta de inovadoras e importantes fontes químicas a fo, de para fazer frente ao desafio de se desenvolver a atividade agrícola compatível com as atuais e futuras exigências da sociedade e de mercado (Mourão Junior & Souza Filho, 2010).
Estudos envolvendo alelopatia, uma subárea da ecologia química, vêm sendo desenvolvidos na tentativa de encontrar possíveis substâncias que possam ser utilizadas pela indústria agroquímica como potentes bioerbicidas.
Entende-se por alelopatia efeitos diretos ou indiretos de uma planta sobre outra, por meio da liberação de substâncias. Esses efeitos podem estimular ou prejudicar o desenvolvimento de espécies sensíveis a essas substâncias - também denominadas de aleloquímicos. Os aleloquímicos podem ser liberados para o meio ambiente de diferentes formas: lixiviação de tecidos vivos e mortos da planta, exsudação radicular, decomposição de tecidos e volatilização (Rice, 1984).
Um dos maiores esforços realizados em estudos envolvendo alelopatia é encontrar maneiras de potencializar os efeitos alelopáticos apresentados por algumas substâncias, a fim de produzir aleloquímicos mais potentes. Uma das formas é inserir modificações estruturais através de semissíntese na molécula de interesse e, posteriormente, testar a atividade da molécula modificada. Dentro dessa perspectiva, este trabalho teve como objetivo comparar a atividade alelopática de três esteroides, que possuem o esqueleto estigmasta-7,22-dien, diferenciando-se um do outro apenas por apresentarem diferentes substituintes na posição-3. Assim, foram analisados de que forma esses substituintes são capazes de interferir na atividade alelopática dos esteroides. As três substâncias foram isoladas da espécie amazônica Moutabea guianensis, que pertence à família Polygalaceae - uma família quase cosmopolita que possui cerca de 22 gêneros e 1.000 espécies (Furness & Sttaford, 1995; Coelho et al., 2008). A espécie M.guianensis é conhecida popularmente como cipó-gogó-de-guariba, e o seu fruto, como olho-de-abutre ou fruto-de-macaco (Pastore, 2006). Este é o primeiro estudo dessa espécie sob o ponto de vista químico e alelopático. Foram utilizadas como plantas-alvo duas plantas invasoras de pastagens típicas da região amazônica: Mimosa pudica (malícia) e Senna obtusifolia (mata-pasto).
MATERIAL E MÉTODOS
Coleta e preparo do material botânico
O material botânico utilizado (caule de Moutabea guianensis) foi coletado por parataxônomos, e a identificação botânica, feita por botânico do Museu Paraense Emílio Goeldi, onde uma exsicata encontra-se catalogada sob o registro MG 195862.
Isolamento e identificação das substâncias
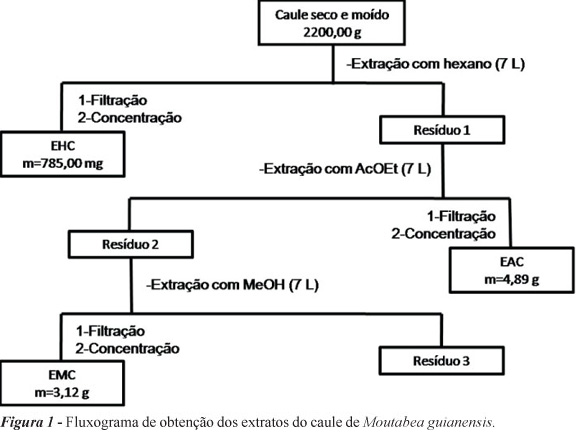
O caule seco e moído de Moutabea guianensis foi extraído sucessivamente com hexano, acetato de etila e metanol durante cinco dias, fornecendo os extratos hexânico (EHC; 785,00 mg), acetato de etila (EAC; 4,89 g) e metanólico (EMC; 3,12 g). O extrato hexânico foi fracionado em CC em gel de sílica eluída com misturas de hexano e acetato de etila. Após monitoramento em CCD, as frações de 7-10 eluídas em Hex/AcOEt 10% foram reunidas e recristalizadas em metanol, de onde foi obtida a substância S1 (espinasterol). O extrato acetato de etila foi fracionado também em CC, tendo como adsorvente gel de sílica e, como eluentes, hexano, acetato de etila e metanol. Após o fracionamento, as frações foram monitoradas por CCD e aquelas com perfis cromatográficos semelhantes foram reunidas. Da fração 3 eluída em Hex/AcOEt 10% foi identificada a substância S2 (espinasterona), e da fração 24 eluída em AcOEt/MeOH 50% foi identificada a substância S3 (glicopiranosil espinasterol). A elucidação estrutural das substâncias isoladas foi realizada pela análise de seus espectros de ressonância magnética nuclear (RMN de 1H, RMN de 13C, DEPT) e comparação com dados da literatura (Figura 1).
Análise da atividade alelopática
Bioensaio de germinação de sementes: A germinação foi monitorada em um período de cinco dias, com contagens diárias e eliminação das sementes germinadas. Foram consideradas sementes germinadas aquelas que apresentavam extensão radicular maior ou igual a 2,00 mm (Juntila, 1976; Duram & Tortosa, 1985). Os bioensaios foram realizados em câmara de germinação em temperatura constante de 25 ºC e fotoperíodo de 12 horas. No bioensaio de germinação de sementes, cada placa de Petri de 9,0 cm de diâmetro, forrada com um disco de papel-filtro qualitativo, recebeu 15 sementes previamente tratadas com ácido sulfúrico, para a quebra de dormência (Souza Filho et al., 1998).
Bioensaio de desenvolvimento de radícula e hipocótilo: Os bioensaios de desenvolvimento da radícula e do hipocótilo foram realizados em um período de 10 dias. Ao final desse período, mediu-se o comprimento da radícula e do hipocótilo. Os bioensaios de desenvolvimento foram realizados em câmara de germinação em temperatura constante de 25 ºC e fotoperíodo de 24 horas. Nos bioensaios de desenvolvimento da radícula e do hipocótilo, cada placa de Petri de 9 cm de diâmetro, forrada com papel-filtro qualitativo, recebeu duas semente pré-germinadas.
Procedimentos comuns: Em todos os bioensaios, as substâncias S1, S2 e S3 foram testadas separadamente. Cada placa de Petri de 9 cm de diâmetro recebeu 3 mL de solução das substâncias-teste, na concentração de 20 mg L-1; as soluções foram adicionadas apenas uma vez, no início dos bioensaios, sendo então adicionada apenas água destilada quando necessário, para manter a concentração inicial.
Delineamento experimental e análise estatística
O delineamento experimental foi inteiramente casualizado, e as três substâncias foram avaliadas em uma única concentração de 20 mg L-1, com três repetições. Para o experimento, utilizou-se como tratamento testemunha água destilada. Os dados foram analisados pelo teste F, e as médias, comparadas pelo teste de Tukey (p>0,05). Na análise dos dados utilizou-se o programa SAS (1989).
RESULTADOS E DISCUSSÃO
Identificação das substâncias
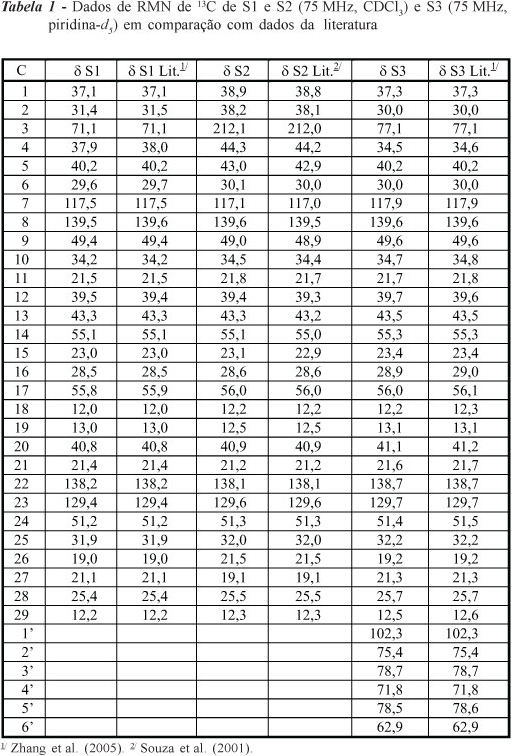
A substância S1 (Figura 2) foi isolada da fração 12 do extrato hexânico do caule de M.guianensis como um sólido branco solúvel em diclorometano e apresentou perfil típico de esteroide no espectro de RMN de 1H, onde é possível observar, entre outros sinais, um multipleto em δH 3,60 característico de hidrogênio oximetínico da posição-3 do esqueleto dos esteroides, dois sinais na região de hidrogênios olefínicos, δH 5,02 (1H, dd, J=15,2 Hz, J=8,5 Hz) e uma sobreposição de sinais em δH 5,15 (2H, m). Nos espectros de RMN de 13C e DEPT são observados 29 sinais de carbono, dos quais seis são referentes a carbonos metílicos, nove, a metilênicos, dez, a metínicos, e quatro, a quaternários. Desses sinais, podem-se destacar δC 71,1 característico de carbono oximetínico em C3 de esteroides e em δC 117,5, δC 129,4, δC 138,2 e δC 139,5 os sinais de carbonos olefínicos de duas insaturações. Com base nos dados dos espectros de RMN de 1H, de 13C e DEPT e comparação com dados da literatura (Zhang et al., 2005), a substância S1 foi identificada como espinasterol - um esteroide muito encontrado em espécies da família Polygalaceae. Na Tabela 1 é mostrada a comparação dos dados de RMN de 13C obtidos com os dados encontrados na literatura para o espinasterol.
A substância S2 (Figura 2) foi obtida da fração ACC3 do extrato acetato de etila do caule de M.guianensis. A substância apresentou-se como um sólido branco solúvel em diclorometano. Em seu espectro de RMN de 1H foram observadas algumas semelhanças com o espectro de RMN de 1H da substância S1, com a diferença de que neste espectro não foi possível observar o multipleto referente ao hidrogênio H-3. No espectro de RMN de 13C foram observados 29 sinais majoritários, dos quais podem-se destacar os sinais de carbonos metínicos δC 117,1, δC 129,6 e δC 138,1 e o de carbono totalmente substituído δC 139,6, que indicam tratar-se de carbonos olefínicos. Pode-se destacar também o sinal em δC 212,1, indicativo de carbonila de cetona. A partir das informações acumuladas pelas análises dos espectros de RMN de 1H, de 13C e DEPT da substância S1 analisada anteriormente e comparação com dados da literatura (Souza et al., 2001) (Tabela 1), a substância S2 foi identificada como a espinasterona.
A substância S3 (Figura 2) foi isolada da fração AC24 do extrato acetato de etila do caule de M.guianensis como um sólido cristalino solúvel em piridina. O seu espectro de RMN de 1H apresentou-se muito semelhante ao espectro de RMN de 1H da substância S1, com a diferença de que o multipleto em torno de δH 3,60 encontra-se deslocado para δH 4,00 e pela presença de sinais de hidrogênio na região de açúcar, sugerindo a presença de uma unidade de açúcar na posição-3. Também podem ser destacados, no espectro de RMN de 1H, dois multipletos em δH 5,02 e δH 5,20 na região de hidrogênios olefínicos. No espectro de RMN de 13C e no espectro de DEPT, foi observada a presença de 35 sinais. Dos 35 sinais, seis são referentes a carbonos metílicos e dez a metilênicos, entre eles δC 62,9, característico da posição-6 de unidade de glicose, além de 15 metínicos, dos quais podem-se destacar os sinais de RMN de 13C indicativos de unidade glicosídica (δC 71,8, δC 75,4, δC 78,6, δC 78,7 e δC 102,3), o sinal de carbono oximetínico (δC 77,1) e os sinais presentes na região de carbonos olefínicos (δC 117,9, δC 129,7 e δC 138,7); ainda estão presentes quatro sinais de carbonos quaternários, entre eles aquele localizado na região de carbonos olefínicos: δC 139,9. Com as informações obtidas dos espectros de RMN de 1H, de 13C e DEPT e comparação com dados da literatura (Zhang et al., 2005), a substância S3 foi identificada como glicopiranosil espinasterol (Tabela 1).
Análise da atividade alelopática das substâncias
No bioensaio de atividade alelopática sobre a germinação de sementes, foi observado que a espécie Mimosa pudica (malícia) foi a mais sensível e apresentou maiores inibições diante das substâncias espinasterol (S1) e espinasterona (S2), ambas com 10% de inibição, enquanto o glicopiranosil espinasterol (S3) inibiu 7%. Esses resultados são indicativos de que a diferença existente na posição-3 dos esteroides testados (S1-hidroxila, S2-carbonila e S3-glicose) não provocou diferenças significativas nos potenciais de inibição de germinação dessas substâncias na invasora Mimosa pudica (malícia). A espécie Senna obtusifolia (mata-pasto) não se mostrou sensível ao ensaio de germinação de sementes. Na Figura 3 é apresentado o gráfico com os resultados de inibição de germinação das substâncias S1, S2 e S3.
A espécie que sofreu maiores inibições no bioensaio de desenvolvimento da radícula (Figura 4) foi Senna obtusifolia (mata-pasto), e a substância que proporcionou maior atividade alelopática para essa invasora foi a glicopiranosil espinasterol (S3), com potencial de inibição de 75%, seguida de espinasterona (S2), com 46%, e espinasterol (S1), com 37% de inibição, mostrando que o esteroide substituído na posição-3 pela unidade de açúcar é o mais ativo. A espécie daninha Mimosa pudica (malícia) sofreu maior redução no desenvolvimento da radícula (13%) diante da substância espinasterol (S1).
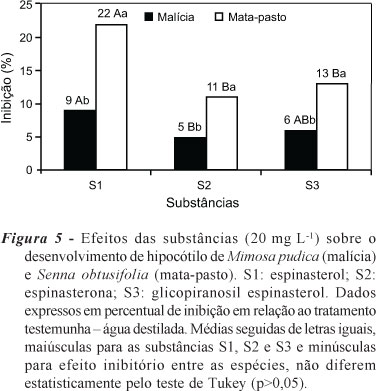
No ensaio de desenvolvimento do hipocótilo (Figura 5), a espécie mata-pasto se mostrou mais afetada diante das substâncias espinasterol (S1) e glicopiranosil espinasterol (S3), com potenciais de inibição de 22 e 13%, respectivamente, mostrando que a presença da hidroxila na posição-3 tem maior influência nessa atividade. A espécie invasora Mimosa pudica (malícia) mostrou-se mais sensível ao efeito inibitório da substância espinasterol (S1), 9%.
Trabalhos envolvendo atividade alelopática de esteroides não são frequentes na literatura. Estudos recentes têm demonstrado que substâncias naturais presentes no arroz (Oryzasativa) possuem atividades herbicidas, entre as quais esteroides livres e glicosilados (Chung & Ahmad, 2010). Os esteroides estigmasterol e β-sitosterol apresentaram efeitos alelopáticos sobre o crescimento do feijão-caupi (Vigna unguiculata), mostrando efeito inibitório sobre a taxa de germinação, o comprimento da parte aérea e o peso fresco (Kpoviessi et al., 2006). Macias et al. (1997) demonstraram as atividades alelopáticas de diversos esteroides isolados de Melilotus messanensis sobre a germinação e o crescimento das monocotiledôneas Hordeum vulgare e Allium cepa, bem como das dicotiledôneas Lactuca sativa (var. Nigra e var. Romana) e Lycopersicon esculentum. Santos et al. (2008a) relataram a atividade alelopática dos esteroides esgosterol e peróxido de ergosterol isolados do fungo endofítico Pestalotiopsis guepinii, cujos resultados se assemelham aos potenciais observados no presente estudo. Em estudo recente (Santos et al., 2008b), foi demonstrado que substâncias que guardam estreitas semelhanças com os esteroides, como os triterpenos, potencializam os efeitos alelopáticos em diferentes pH, e esse é um caminho a ser explorado.
Nos bioensaios de atividade alelopática sobre a germinação de sementes, os esteroides testados não proporcionaram inibições significativas, tendo Mimosa pudica (malícia) e Senna obtusifolia (mata-pasto) como espécies receptoras. Resultados expressivos foram obtidos nos bioensaios de desenvolvimento da radícula, em que a substância glicosilada S3 foi a mais ativa, evidenciando que a substituição na posição-3 dos esteroides pode influenciar no potencial alelopático avaliado. De maneira geral, as atividades alelopáticas foram doses- dependentes e variaram de acordo com a espécie testada e o parâmetro analisado. O fato de triterpenos exibirem atividade alelopática potencializada em diferentes pH e de a atividade alelopática dos esteroides avaliados no presente estudo variar com a substituição na posição-3 abre expectativa para estudos de correlação estrutura química versus atividade biológica, variando os substituintes dessa posição.
AGRADECIMENTOS
À CAPES e ao CNPq, pelo apoio financeiro.
LITERATURA CITADA
Recebido para publicação em 19.11.2011 e aprovado em 21.3.2012.
Parte da dissertação de mestrado do primeiro autor.
- COELHO, V. P. M.; AGRA, M. F.; BARACHO, G. S. Flora da Paraíba, Brasil: Polygala L. (Polygalaceae). Acta Bot. Bras., v. 22, n. 1, p. 225-239, 2008.
- CHIOVATO, M. G. et al. Diferentes densidades de plantas daninhas e métodos de controle nos componentes de produção do milho orgânico. Planta Daninha, v. 25, n. 2, p. 277-283, 2007.
- CHUNG, I. M.; AHMAD, A. Herbicidal activities of allelopathic and other compounds from Oryza sativa Allelopathy J., v. 26, n. 2, p. 139-156, 2010.
- DUKE, S. O. et al. Interactions of synthetic herbicides with plant disease and microbial herbicides. In: VURRO, M.; GRESSEL, J. (Eds.). Novel biotechnologies for biocontrol agent enhancement and management Dordrecht: Springer, 2007. p. 277-296.
- DURAM, R. D.; TORTOSA, M. E. The effect of mechanical and chemical scarification on germination of charlock (Sinapis arvensis L.) seeds. Seed Sci. Technol., v. 13, n.1, p. 155-163, 1985.
- DURIGAN, G. et al. Threats to the Cerrado remnants of the state of São Paulo, Brazil. Sci. Agric., v. 64, n. 4, p. 355-363, 2007.
- FURNESS, S. H.; STAFFORD, P.J. Polygalaceae. Rev. Paleobot. Palynol., v. 88, n. 1, p. 61-82, 1995.
- GRESSEL, J. Low pesticide rates may hasten the evolution of resistance by increasing mutation frequencies. Pest Manag. Sci., v. 67, n. 3, p. 253-257, 2011.
- JUNTILA, O. Seed and embryo germination in S. vulgaris and S. reflexa as affected by temperature during seed development. Physiol. Plant, v. 29, n. 2, p. 264-268, 1976.
- KPOVIESSI, D. S. S. et al. Allelopathic effects on cowpea (Vigna unguiculata (L.) Walp) plant and cytotoxic activities of sterols and triterpene isolated from Justicia anselliana (NEES) T. Anders. Electron. J. Nat. Subs., v. 1, n. 1, p. 12-19, 2006.
- MACIAS, F. A.; SIMONET, A. M.; GALINDO, J. C. G. Bioactive steroids and triterpenes from Melilotus messanensis and their allelopathic potential. J. Chem. Ecol., v. 23, n. 7, p. 1781-1803, 1997.
- MOURÃO JUNIOR, M.; SOUZA FILHO, A. P. S. Diferenças da atividade alelopática em espécies da família Leguminosae. Planta Daninha, v. 28, p. 939-951, 2010. Edição Especial.
- OWEN, M. J. Widespread occurrence of multiple herbicide resistance in Western Australian annual ryegrass (Lolium rigidum) populations. Austr. J. Agric. Res., v. 58, n. 7, p. 711-718, 2007.
- PASTORE, J. F. B. Polygalaceae Hoffmannsegg e Link no Distrito Federal, Brasil. 2006 216 f. Dissertação (Mestrado em Botânica) - Instituto de Ciências Biológicas, Universidade de Brasília, Brasília, 2006.
- POWLES, S. B.; YU, Q. Evolution in action: plants resistant to herbicides. Ann. Rev. Plant Biol., v. 61, n. 1, p. 317-347, 2010.
- RIAR, D. S. et al. Glyphosate resistance in a johnson grass (Sorghum halepense) biotype from Arkansas. Weed Sci., v. 59, n. 3, p. 299-304, 2011.
- RICE, E. L. Allelopathy New York: Academic Press, 1984. 422 p.
- SANTOS, L. S. et al. Potencial herbicida da biomassa e de substâncias químicas produzidas pelo fungo endofítico Pestalotiopsis guepinii Planta Daninha, v. 26, n. 3, p. 539-548, 2008a.
- SANTOS, L. S. et al. Atividade alelopática de substâncias químicas isoladas do capim-marandu e suas variações em função do pH. Planta Daninha, v. 26, n. 3, p. 531-538, 2008b.
- STATITISTICAL ANALYSIS SYSTEM - SAS. User's guide Version 6.4. Cary: 1989. 846 p.
- SOUZA, A. D. L. et al. Constituintes químicos de Gustavia augusta L. (LECYTHIDACEAE). Química Nova, v. 24, n. 4, p. 439-442, 2001.
- SOUZA FILHO, A. P. S.; DUTRA, S.; SILVA, M. A. M. M. Métodos de superação de dormência de sementes de plantas daninhas de pastagens cultivadas da Amazônia. Planta Daninha, v. 16, n. 1, p. 3-11, 1998.
- TIPPING, P. W. Mowing-induced changes in soil seed banks and populations of plumeless thistle (Carduus acanthoides) and musk thistle (Carduus nutans). Weed Technol., v. 22, n. 1, p. 49-55, 2008.
- ZHANG, L. et al. A new sterol from Securidaca inappendiculata J. Asian Nat. Produc. Res., v. 7, n. 4, p. 649-653, 2005.
Datas de Publicação
-
Publicação nesta coleção
09 Out 2012 -
Data do Fascículo
Dez 2012
Histórico
-
Recebido
19 Nov 2011 -
Aceito
21 Mar 2012