Resumos
Linhagens de estafilococos coagulase negativos e pauciprodutores de enterotoxina de A a E, com capacidade de síntese variando de 1,4 a 16ng/mL oriundas de sítios anatômicos de cabras sadias, procedentes da Espanha, foram estudadas com o intuito de se avaliar a capacidade de desenvolvimento e produção de enterotoxina estafilocócica ("SE"), em alimentos experimentalmente inoculados. Para tal, leite integral "tipo longa vida" e presunto cozido foram, de maneira isolada e em duplicata, inoculados com 14 linhagens teste, S.caprae, duas amostras; S.chromogenes; S.cohnii; S.epidermidis; S.haemolyticus, duas amostras; S.hyicus; S.lentus; S.sciuri; S.xylosus, duas amostras; e S.warneri, duas amostras; previamente caracterizadas bioquimicamente. Estes substratos alimentícios, uma vez inoculados, foram mantidos em estufa a 30°C, durante 24 e 48h de incubação e, neste período, submetidos à contagem de células estafilocócicas em ágar Baird Parker e à avaliação de presença de "SE", através do ensaio de "ELISA-SET-EIA, Enzyme Linked-Immunosorbent Assay," e "RPLA, Reversed Passive Latex Agglutination Assay". Os resultados obtidos evidenciaram, tanto em leite integral "tipo longa vida" como em presunto cozido, desenvolvimento mínimo estipulado em 10(6) e máximo de 10(9)UFC/g ou mL do alimento, decorridas 48h de incubação.De acordo com as condições aplicadas neste experimento não apresentaram, contudo, em nenhuma ocasião produção de "SE" que pudesse ter sido detectada .
Staphylococcus-coagulase negativos; enterotoxinas
Fourteen coagulase-negative low-enterotoxin-producing staphylococcal strains -- S.caprae; S.chromogenes; S.cohnii; S.epidermidis; S.haemolyticus, two strains; S.hyicus; S.lentus; S.sciuri; S.xylosus, two strains; e S.warneri, two strains -- with capacity of synthesis ranging from 1.4 to 16.8ng of staphylococal enterotoxin/mL were obtained from anatomic sites of healthy goats in Spain. Those staphylococcal strains were used with the aim of evaluating their growth and enterotoxigenic capacity in experimentally inoculated foods. Samples of whole milk and cooked ham were inoculated with 10(4)UFC Staphylococci/g ormL. These substrates were kept at 30°C, during 24 and 48 hours and submitted to the enumeration of staphylococcal cells on Baird Parker agar. The enterotoxin detection was made by ELISA and RPLA. The results revealed, concerning to staphylococcal behaviour in whole milk and cooked ham, that all strains showed development range of 10(6) to 10(9)CFU/g ormL after 48 hours incubation and no SE production was observed in the inolculated substrates that could be detected by ELISA, SET-EIA and RPLA.
coagulase-negative low-staphylococcal; enterotoxins
11 Recebido para publicação em21/07/00. Aceito para publicação em 02/08/01.
Maria Lúcia PEREIRA21 Recebido para publicação em21/07/00. Aceito para publicação em 02/08/01. ,*1 Recebido para publicação em21/07/00. Aceito para publicação em 02/08/01. , Luiz Simeão CARMO21 Recebido para publicação em21/07/00. Aceito para publicação em 02/08/01. , José Luiz PEREIRA31 Recebido para publicação em21/07/00. Aceito para publicação em 02/08/01.
RESUMO
Linhagens de estafilococos coagulase negativos e pauciprodutores de enterotoxina de A a E, com capacidade de síntese variando de 1,4 a 16ng/mL oriundas de sítios anatômicos de cabras sadias, procedentes da Espanha, foram estudadas com o intuito de se avaliar a capacidade de desenvolvimento e produção de enterotoxina estafilocócica ("SE"), em alimentos experimentalmente inoculados. Para tal, leite integral "tipo longa vida" e presunto cozido foram, de maneira isolada e em duplicata, inoculados com 14 linhagens teste, S.caprae, duas amostras; S.chromogenes; S.cohnii; S.epidermidis; S.haemolyticus, duas amostras; S.hyicus; S.lentus; S.sciuri; S.xylosus, duas amostras; e S.warneri, duas amostras; previamente caracterizadas bioquimicamente. Estes substratos alimentícios, uma vez inoculados, foram mantidos em estufa a 30°C, durante 24 e 48h de incubação e, neste período, submetidos à contagem de células estafilocócicas em ágar Baird Parker e à avaliação de presença de "SE", através do ensaio de "ELISA-SET-EIA, Enzyme Linked-Immunosorbent Assay," e "RPLA, Reversed Passive Latex Agglutination Assay". Os resultados obtidos evidenciaram, tanto em leite integral "tipo longa vida" como em presunto cozido, desenvolvimento mínimo estipulado em 106 e máximo de 109UFC/g ou mL do alimento, decorridas 48h de incubação.De acordo com as condições aplicadas neste experimento não apresentaram, contudo, em nenhuma ocasião produção de "SE" que pudesse ter sido detectada .
Palavras-chave: Staphylococcus-coagulase negativos; enterotoxinas.
SUMMARY
EVALUATION OF GROWTH AND ENTEROTOXIGENIC CAPACITY OF COAGULASE-NEGATIVE LOW-ENTEROTOXIN-PRODUCING STAPHYLOCOCCAL STRAINS IN EXPERIMENTALLY INOCULATED FOOD. Fourteen coagulase-negative low-enterotoxin-producing staphylococcal strains ¾ S.caprae; S.chromogenes; S.cohnii; S.epidermidis; S.haemolyticus, two strains; S.hyicus; S.lentus; S.sciuri; S.xylosus, two strains; e S.warneri, two strains ¾ with capacity of synthesis ranging from 1.4 to 16.8ng of staphylococal enterotoxin/mL were obtained from anatomic sites of healthy goats in Spain. Those staphylococcal strains were used with the aim of evaluating their growth and enterotoxigenic capacity in experimentally inoculated foods. Samples of whole milk and cooked ham were inoculated with 104UFC Staphylococci/g ormL. These substrates were kept at 30°C, during 24 and 48 hours and submitted to the enumeration of staphylococcal cells on Baird Parker agar. The enterotoxin detection was made by ELISA and RPLA. The results revealed, concerning to staphylococcal behaviour in whole milk and cooked ham, that all strains showed development range of 106 to 109CFU/g ormL after 48 hours incubation and no SE production was observed in the inolculated substrates that could be detected by ELISA, SET-EIA and RPLA.
Keywords: coagulase-negative low-staphylococcal; enterotoxins.
1 ¾ INTRODUÇÃO
Vários tipos de alimentos já foram epidemiologicamente incriminados e são freqüentemente relatados como capazes de suportar o desenvolvimento natural e artificial de Staphylococcus aureus, bem como a produção de suas enterotoxinas. Dentre os substratos alimentícios podem ser destacados produtos lácteos (queijos, leite cru, pasteurizado e em pó, manteiga e sorvetes), produtos de confeitaria (tortas, bolos recheados e doces cremosos), carnes frescas e curadas, ovos e massas alimentícias.
A detecção de enterotoxinas estafilocócicas, "SE", até o presente momento designadas como "SEA", "SEB", "SEC", "SED", "SEE", "SEG", "SEH", foi realizada através de métodos biológicos, que consistem na administração da toxina por via intragástrica em macacos. A partir de sua purificação, as técnicas de detecção fundamentaram-se no uso de anticorpos preparados contra as mesmas. Reações específicas de precipitação em agarose foram utilizadas e desenvolvidas, destacando-se o ensaio de imunodifusão em microlâmina e, ainda, o ensaio da "Sensibilidade Ótima em Placa, OSP", este último atingindo níveis de detecção da ordem de 0,5µg/g de enterotoxina, em líquido sobrenadante de cultura.
Contudo, questionamentos a respeito da eficácia e sensibilidade desses métodos começaram a existir quando isolados de S.aureus, procedentes de alimentos implicados em surtos de intoxicação alimentar apresentaram-se negativos para a produção de enterotoxinas quando testados por esses métodos, embora positivos nos testes de reação emética em macacos. Este fato tornou-se evidente através da informação de que 100 a 200ng/g de "SEA" constituiu dose suficiente para resultar numa intoxicação estafilocócica, em escola nos Estados Unidos, onde crianças ingeriram leite achocolatado que continha de 0,4 a 0,7ng/g da enterotoxina detectada pelo método de "ELISA" e não puderam ser detectadas pelos métodos tradicionais de imunodifusão como "OSP" [7].
Pesquisas conduzidas a partir de leite e sítios anatômicos de animais demonstraram haver espécies coagulase negativas, como S.xylosus, S.haemolyticus, S.epidermidis, S.cohnii, S.chromogenes, S.warneri, S.sciuri e S.lentus, que produziam enterotoxinas em meios de cultivo laboratorial [15].
Desta maneira, a primazia da capacidade enterotoxigênica, que pertencia quase com exclusividade a S.aureus, foi estendida, embora este fato já houvesse sido, também, relatado para outras espécies coagulase positivas como S.hyicus e S.intermedius [5, 9].
Apesar da crença de que, usualmente, espécies coagulase negativas não constituíssem objeto de importância na epidemiologia das intoxicações estafilocócicas, as pesquisas ora referidas conclamam a explorações no sentido da averiguação de espécies outras que as produtoras de coagulase.
Com base nas considerações então delineadas, a presente pesquisa objetivou a averiguação de desenvolvimento e capacidade enterotoxigênica de estafilococos pauciprodutores de enterotoxinas, oriundos de sítios anatômicos de cabras sadias, através de inoculação experimental em leite integral "tipo longa vida" e presunto cozido.
2 ¾ MATERIAL E MÉTODOS
2.1 ¾ Linhagens teste
Foram utilizadas 14 linhagens teste de estafilococos coagulase negativos e pauciprodutores de enterotoxina de A a E, com capacidade de síntese variando de 1,4 a 16,8ng/mL para uma ou até três enterotoxinas, conforme informações de VALLE et al [15], da Universidade de Cáceres, Extremadura, Espanha, de onde procederam. Estas linhagens, coletadas a partir de sítios anatômicos de cabras sadias, encontram-se listadas na Tabela 1, em conformidade com o tipo e quantidade de "SE" produzida.
2.2 ¾ Procedimentos para avaliação de desenvolvimento e produção de "SE" pelas linhagens teste, em alimentos
2.2.1 ¾ Inoculação experimental
Quatorze unidades de leite integral tipo "longa vida" (500mL) e 14 unidades de presunto cozido foram, de forma individualizada e em duplicata, experimentalmente inoculados com as 14 linhagens teste. A densidade populacional foi estabelecida a partir de leitura de absorbância a 550nm e contagem de células em ágar padrão para contagem, "PCA" (Difco) de forma a se obter inóculo inicial (tempo zero) aproximado de 104UFC/mL ou g de alimento. Antes da inoculação das linhagens, estes substratos foram submetidos a análise microbiológica e determinação de pH [4, 16].
2.2.2 ¾ Contagem bacteriana após 24 e 48h de incubação dos alimentos inoculados
No período de 24 e 48h, ambos substratos foram submetidos a leitura de pH e analisados quanto à contagem de células viáveis das linhagens teste inoculadas, utilizando-se ágar Baird Parker, BP (Biobrás) incubado a 37°C até 72h, semeando-se por espalhamento 0,1mL das diluições seriadas a partir de homogeneizado de 25mL de leite e 25g de presunto em Água Peptonada Tamponada, APT [16].
2.2.3 ¾ Detecção de enterotoxinas
Para a detecção de enterotoxinas foi utilizado o teste de "ELISA-SET-EIA", constituído por esferas de poliestireno sensibilizadas com antitoxinas específicas, empregando-se 20mL do leite e 25g do presunto, este último obtido a partir de prévia homogeneização de 125g da amostra em 150mL de tampão salina-fosfato centrifugados a 7400g, durante 20min. As alíquotas foram tomadas após incubação de 24 e 48h [8].
Para os extratos de presunto efetuou-se, devido à ausência de turbidez destes, também pesquisas de "SE" pelo método de "RPLA", segundo IGARASHI et al [10], adotando-se a adição de 5% de IgG normal de coelho em concentração igual a 0,74µg/mL, para se evitar a presença de reações inespecíficas [14].
Tendo em vista a necessidade de obtenção de extratos límpidos, concentrou-se leite integral tipo "longa vida" que, após quelagem a cobre, foi submetido a cromatografia de imunoafinidade em coluna de "Sepharose 6-B" [6]. Os extratos, assim obtidos, puderam então ser analisados por "RPLA". Esta metodologia foi previamente validada através de ensaio piloto utilizando duas alíquotas do mesmo queijo "tipo Minas", reconhecidamente não enterotoxigênico, as quais foram, de maneira isolada, experimentalmente inoculadas com 10ng e 1ng de "SEA" padrão.
A Figura 1 apresenta o fluxograma adotado no decorrer de toda metodologia experimental.
3 ¾ RESULTADOS E DISCUSSÃO
A prévia análise microbiológica de leite integral tipo "longa vida" e presunto cozido demonstrou tratarem-se de substratos de qualidade compatível aos preceitos legais vigentes, apresentando estes, entre outros, desenvolvimento nulo de bactérias mesófilas e, principalmente, de estafilococos (dado não constante em Tabela).
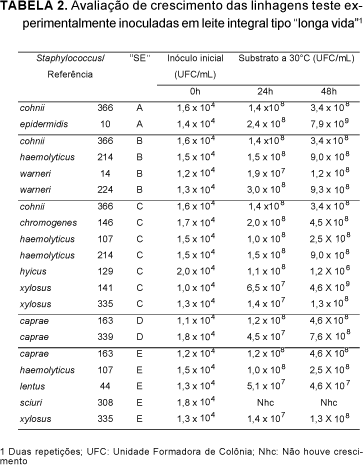
Os resultados concernentes ao desenvolvimento das linhagens teste em ambos alimentos, leite integral tipo "longa vida" e presunto cozido, e aqueles relativos às tomadas de pH no substrato lácteo encontram-se dispostos na Tabela 2, Tabela 3 e Tabela 4, respectivamente.
O inóculo inicial para as linhagens teste variou de 1,0 x 104 a 2,0 x 104UFC/mL ou g para ambos alimentos (Tabela 2 e Tabela 3). Estes valores podem ser considerados uniformes e foram estipulados com intuito de se atingir, após 24 e/ou 48h de incubação, densidade populacional compatível com aquela de 106-107UFC/mL ou g, dose estimada como sendo a necessária para produção de "SE", em surtos relacionados com S.aureus [1].
Avaliando-se primeiramente o leite integral tipo "longa vida" (Tabela 2), pode-se perceber que tal substrato apresentou, de maneira geral, condições adequadas ao desenvolvimento das linhagens testadas. Isto pode ser exemplificado em se considerando que a partir do inóculo inicial de 104UFC/mL, sete linhagens (S. cohnii, S. epidermidis, S. haemolyticus, S. warneri, S. chromogenes, S. haemolyticus e S.caprae, ref. 366, 10, 224, 146, 107, 214, 163) tiveram população elevada para 108; cinco (S.warneri, S.xylosus, S.xylosus, S.caprae e S.lentus, ref. 14, 141, 335, 339 e 44) para 107 e uma (S.hyicus, ref. 129) para 106UFC/mL, no período de 24h de incubação, tendo cerca de 70% das linhagens atingido, em 48h, população igual a 108UFC/mL. Exceção se fez, para S.sciuri, ref. 308, que apresentou ausência de desenvolvimento, após inoculação nos dois períodos de tempo estudados. Por sua vez, S.hyicus, ref. 129, limitou-se ao desenvolvimento de 106UFC/mL e o máximo desenvolvimento, 109UFC/mL, foi alcançado por S.xylosus, ref.141.
De acordo com os resultados apresentados na Tabela 3, foi observado no presunto cozido, para o período de 24h, leitura um pouco inferior àquela obtida em leite integral tipo "longa vida". Neste alimento, cinco linhagens (S.cohnii, S.warneri, S.warneri, S.chromogenes e S.haemolyticus, ref. 366, 14, 224, 146 e 107) tiveram sua densidade populacional elevada para 108; quatro (S.xylosus, S.xylosus, S.caprae e S.lentus, ref. 141, 335, 163 e 44) para 107 e quatro (S.epidermidis, S.haemolyticus, S.hyicus e S.caprae, ref. 10, 214, 129 e 339) para 106UFC/g. Entretanto, decorrido o tempo de 48h de incubação, aproximadamente, 20%, 66% e 13% destas linhagens atingiram densidade populacional de 106, 108 e 109UFC/g, respectivamente. Estes valores foram superiores àqueles reportados para o leite integral tipo "longa vida", neste mesmo período de incubação. Já S.sciuri, ref. 308, desenvolveu-se, o que não ocorreu em leite integral tipo "longa vida", como se confirma na Tabela 2, atingindo 106UFC/g, índice este, novamente, não ultrapassado por S.hyicus, ref. 129 (Tabela 3).
Quanto à produção de enterotoxinas (dados não constantes em Tabelas), estas se fizeram ausentes em ambos substratos pesquisados, até o período de 48h, para todas as 14 linhagens teste, sem exceção.
Buscando-se uma explicação para a não ocorrência de produção de "SE" nestas condições, a alteração de pH no substrato pesquisado poderia ser indicativa de que, somente para S.hyicus, ref. 129, este fator pudesse ter vindo a funcionar como inibitório ao crescimento celular, uma vez que o potencial hidrogeniônico, com valor médio aproximado de 6,8, para o leite integral tipo "longa vida", no momento da inoculação, decresceu para 5,0, após 48h de permanência a 30°C (Tabela 4). Todavia, o valor de pH próximo a este, 5,31, foi relatado para o mesmo substrato inoculado, nas mesmas condições, com S.warneri, ref. 14, mas que apresentou desenvolvimento situado na faixa de 108UFC/mL.
Fez-se oportuno comentar que o procedimento piloto no qual se avaliou o ensaio de cromatografia de imunoafinidade usando cobre quelado à amostra mostrou-se plenamente eficaz para o substrato teste ¾ queijo tipo "Minas", sabidamente não enterotoxigênico ¾ recuperando-se as quantidades de 10ng e 1ng de "SEA" experimentalmente adicionadas (dado não constante em Tabelas). Este procedimento, além do efeito de concentração da amostra em até 20 vezes, conseguiu viabilizar a conduta de detecção de "SE" através do método de "RPLA", pela clareza e limpidez dos extratos fornecidos, no caso leite integral "tipo longa vida", reforçando o resultado de ausência de produção de "SE" no alimento e método de detecção considerados.
A realidade de que espécies não produtoras de coagulase conseguem, potencialmente, alcançar alimentos e nestes virem a se desenvolver pode ser entendida pelo fato de que tanto o homem como os animais são portadores usuais destas estirpes [2].
No que concerne à produção de enterotoxinas e envolvimento destas em surtos, dados de literatura relatam, de maneira exígua, mas consistente, dois episódios de intoxicação alimentar nos quais estafilococos não produtores de coagulase foram evidenciados. O primeiro teve lugar no Japão com a participação de 40 estudantes, onde o agente causal foi igualmente detectado nas fezes e em superfícies de pratos utilizados no lanche do hotel [13]. O segundo, no qual 145 comensais manifestaram a doença, S.epidermidis produtor de "SEA" foi detectado na carne consumida e também em lesões secas de impetigo presentes nas mãos de um manipulador, caracterizando o primeiro registro de detecção de enterotoxina sintetizada a partir de espécie não produtora de coagulase [3].
Até o presente momento, a produção de "SE" por espécies não produtoras de coagulase foi relatada por OLIVEIRA [12], onde as estirpes de origem bovina, S.warneri e S.chromogenes, experimentalmente inoculadas em presunto cozido e creme de confeitaria, produziram "SEC" e "SED". E ainda por LI E CHENG [11] que já haviam descrito a produção das enterotoxinas anteriormente descritas para S.warneri CCRC 12929 e S.haemolyticus CCRC 12923. Todavia, os dados relatados nessas duas pesquisas não informam se a quantidade de enterotoxinas produzidas identificavam linhagens baixo produtoras, o que, contrariamente, se assegurou no experimento ora realizado, onde todas as 14 linhagens teste responsabilizavam-se por ínfima produção, situada entre 1,4 a 16,8ng/mL de fluido sobrenadante de cultura.
4 ¾ CONCLUSÕES
Os dados obtidos neste experimento demonstraram que, com exceção de S.sciuri, ref. 308 que não se desenvolveu apenas em leite integral tipo "longa vida" embora o fazendo em presunto cozido, todas as linhagens teste apresentaram desenvolvimento nestes alimentos quando incubados a 30°C, nos períodos de 24 e 48h. Por sua vez, não se detectou produção de enterotoxina nos dois substratos considerados inoculados com as linhagens teste, empregando os ensaios de "ELISA-SET-EIA" e "RPLA".
5 ¾ REFERÊNCIAS BIBLIOGRÁFICAS
6 ¾ AGRADECIMENTOS
À FAPEMIG, Fundação de Amparo à Pesquisa do Estado de Minas Gerais, através do Projeto CBS-1129/93 e aos Professores Dr. Merlin Scott Bergdoll e Dr. António de Melo Serrano (in memorian).
2 FUNED, IOM, Divisão de Bromatologia, Toxicologia e Medicamentos. CEP 30510-010 MG malu@funed.mg.gov.br
3 UNICAMP, FEA, Caixa Postal 6121 CEP 13081-970 Campinas SP
* A quem a correspondência deve ser enviada.
- [1] BERGDOLL, M.S. Staphylococcus aureus In: Doyle,M.P. (ed). Foodborne bacterial pathogens INC, New York, p.463-523, 1989.
- [2] BERGDOLL, M. S. Importance of staphylococci that produce nanogram quantities of enterotoxin. Zbl. Bakt, v.282, p.1-6, 1995.
- [3] BRECKINRINDGE, J.C. & BERGDOLL, M. S. Outbreak of food-borne gastroenteritis due to a coagulase-negative enterotoxin producing Staphylococcus Medical Intelligence, v.284, n.10, p.541-543, 1971.
- [4] BRASIL. Ministério da Saúde. Secretaria Nacional de Vigilância Sanitária. Portaria n° 01, de 28 de janeiro de 1987 Seção 1. Brasília, DF., p.2197-2200, 1987.
- [5] DEVRIESE, L.A. Isolation and identification of Staphylococcus hyicus Am. J. Vet. Res, v.38, n.6, p.787-797, 1977.
- [6] DICKIE, N. & AKHTAR, M. Concentration of staphylococcal enterotoxin from food extract using copper chelate sepharose. J. Food Protect, v.52, n.12, p.903-905, 1989.
- [7] EVENSON, M. L., HINDS, M. W., BERNSTEIN, R. S. et al Estimation of human dose of staphylococcal enterotoxin A from a large outbreak involving chocolat milk. Int. J. Food Microbiol, v.7, p.311-316, 1988.
- [8] FEY, H. & PFISTER, H. A diagnostic kit for the detection of staphylococcal enterotoxins (SET) A,B,C and D (SEA,SEB,SEC,SED). In: AVRAMEAS, S. et al (eds.) Immunoenzymatic Techniques. Elsevier, Amsterdam, p.345-348, 1983.
- [9] HIROOKA, E.Y.; MULLER, E. E.; FREITAS, J.C. et al Enterotoxigenicity of Staphylococcus intermedius of canine origin. Int. J. Food Microbiol; v.7, p.185-191, 1988.
- [10] IGARASHI, H., FUJIKAWA, H., SHINGAKI, M. et al Latex agglutination test fos staphylococcal toxic shock syndrome toxin-1. J. Clin. Microbiol, v.23, n.2, p.509-512, 1986.
- [11] LI, F.C.& CHENG, C.C. Growth and enterotoxins production by coagulase-negative Staphylococcus strains. Staphylococcus warneri CCRC 12929 and S.haemolyticus CCRC 12923 in cow milk and goat milk. Food-Science, v.24, n.1, p.120-128,1997.
- [12] OLIVEIRA, A.M. Investigação do comportamento de estafilococos enterotoxigênicos coagulase negativos, em alimentos. (Tese de Doutorado) 1999. 102p. Faculdade de Engenharia de Alimentos ž Universidade Estadual de Campinas (UNICAMP).
- [13] OMORI, G. & KATO, Y. A staphylococcal food-poisoning caused by a coagulase negative strain. Bilken's J, v.2, p.92, 1959.
- [14] PEREIRA, M.L.; HENEINE, L.G.; SANTOS, E.J. et al Prevention of nonspecific.reactions on reversed passive latex agglutination assay for.detecting staphylococcal enterotoxins low amounts. Rev. Lat-. Amer. Microbiol, v.39, n.1-2, p. 57-63, 1999.
- [15] VALLE, J., GOMEZ-LUCIA, E., PIRIZ, S. et al Enterotoxin production by staphylococci isolated from healthy goats. Appl. Environ. Microbiol., v.56, n.5, p.1323-1326, 1990.
- [16] VANDERZANT, C. & SPLITTSTOESSER, D.F. Compendium for the microbiological examination of foods American Public Health Association. 3.ed. Washington, DC., p.1291, 1992.
Datas de Publicação
-
Publicação nesta coleção
25 Abr 2002 -
Data do Fascículo
Ago 2001
Histórico
-
Aceito
02 Ago 2001 -
Recebido
21 Jul 2000