Resumo
A hipertensão (pressão arterial > 140/90 mmHg) é muito comum em pacientes submetidos à diálise regular, com uma prevalência de 70-80%, e apenas a minoria tem controle adequado da pressão arterial (PA). Em contraste com a associação incerta entre de PA pré-dialítica com mortalidade cardiovascular, estudos prospectivos mostraram que a PA interdialítica, registrada como PA domiciliar ou pela monitorização ambulatorial da pressão arterial em pacientes em hemodiálise, está mais relacionada à mortalidade e eventos cardiovasculares. Embora a PA seja medida com frequência no ambiente de tratamento de diálise, aspectos relacionados à técnica de medição tradicionalmente empregada podem ser insatisfatórios. Várias outras ferramentas estão agora disponíveis, e estão sendo usadas em ensaios clínicos e na prática clínica para avaliar e tratar a PA elevada em pacientes com doença renal crônica (DRC). Enquanto esperamos pela revisão das diretrizes do KIDGO para a pressão sanguíneana DRC, não há nenhuma diretriz para a população em diálise abordando essa importante questão. Assim, o objetivo desta revisão é fornecer uma análise crítica das informações disponíveis sobre a epidemiologia, os mecanismos patogênicos e os principais pilares sustentadores do manejo da pressão arterial no estágio 5-D da DRC, com base no conhecimento atual.
Palavras-chave:
Hipertensão; Diálise Renal; Diálise Peritoneal
Abstract
Hypertension (blood pressure > 140/90 mm Hg) is very common in patients undergoing regular dialysis, with a prevalence of 70-80%, and only the minority has adequate blood pressure (BP) control. In contrast to the unclear association of predialytic BP recordings with cardiovascular mortality, prospective studies showed that interdialytic BP, recorded as home BP or by ambulatory blood pressure monitoring in hemodialysis patients, associates more closely with mortality and cardiovascular events. Although BP is measured frequently in the dialysis treatment environment, aspects related to the measurement technique traditionally employed may be unsatisfactory. Several other tools are now available and being used in clinical trials and in clinical practice to evaluate and treat elevated BP in chronic kidney disease (CKD) patients. While we wait for the ongoing review of the CKD Blood Pressure KIDGO guidelines, there is no guideline for the dialysis population addressing this important issue. Thus, the objective of this review is to provide a critical analysis of the information available on the epidemiology, pathogenic mechanisms, and the main pillars involved in the management of blood pressure in stage 5-D CKD, based on current knowledge.
Keywords:
Hypertension; Renal Dialysis; Peritoneal Dialysis
Introdução
Entender os mecanismos, avaliar e definir o melhor manejo da pressão arterial (PA) em pacientes que recebem terapias de substituição renal por meio de hemodiálise (HD) ou diálise peritoneal (DP) é um desafio significativo para os profissionais de saúde. Embora a PA seja medida com freqüência no ambiente de tratamento de diálise, aspectos relacionados à técnica de medição empregada podem ser insatisfatórios. Várias outras ferramentas estão agora disponíveis e sendo usadas em ensaios clínicos e na prática clínica para avaliar e tratar a PA elevada em pacientes com doença renal crônica (DRC)11 Parati G, Ochoa JE, Bilo G, Agarwal R, Covic A, Dekker FW, et al.; European Renal and Cardiovascular Medicine (EURECA-m) working group of the European Renal Association-European Dialysis Transplantation Association (ERA-EDTA). Hypertension in Chronic Kidney Disease Part 2: Role of Ambulatory and Home Blood Pressure Monitoring for Assessing Alterations in Blood Pressure Variability and Blood Pressure Profiles. Hypertension 2016;67:1102-10.,22 Parati G, Ochoa JE, Bilo G, Agarwal R, Covic A, Dekker FW, et al.; European Renal and Cardiovascular Medicine (EURECA-m) working group of the European Renal Association-European Dialysis Transplantation Association (ERA-EDTA). Hypertension in Chronic Kidney Disease Part 1: Out-of-Office Blood Pressure Monitoring: Methods, Thresholds, and Patterns. Hypertension 2016;67:1093-101.. Diferentes níveis de PA podem ser observados no mesmo paciente em situações distintas, que incluem avaliações antes, durante ou após a sessão de diálise, e em casa, utilizando medidas ambulatoriais (MAPA), sendo frequente e substancialmente menores do que durante a diálise33 Alborzi P, Patel N, Agarwal R. Home blood pressures are of greater prognostic value than hemodialysis unit recordings. Clin J Am Soc Nephrol 2007;2:1228-34..
Em pacientes com doença renal terminal (DRT) recebendo diálise, a pressão arterial elevada é comum e geralmente mal controlada44 Agarwal R, Nissenson AR, Batlle D, Coyne DW, Trout JR, Warnock DG. Prevalence, treatment, and control of hypertension in chronic hemodialysis patients in the United States. Am J Med 2003;115:291-7.. Embora a sobrecarga de volume e a retenção de sódio pareçam ser os principais mecanismos patogênicos da hipertensão nessa população, outros fatores como aumento da rigidez arterial, ativação do sistema renina-angiotensina-aldosterona, apnéia do sono, ativação do sistema nervoso simpático e uso de eritropoetina recombinante também podem estar envolvidos55 Sarafidis PA, Persu A, Agarwal R, Burnier M, de Leeuw P, Ferro CJ, et al. Hypertension in dialysis patients: a consensus document by the European Renal and Cardiovascular Medicine (EURECA-m) working group of the European Renal Association-European Dialysis and Transplant Association (ERA-EDTA) and the Hypertension and the Kidney working group of the European Society of Hypertension (ESH). Nephrol Dial Transplant 2017;32:620-40..
A associação entre hipertensão e risco de doença cardiovascular tem sido bem documentada na população geral, mas em pacientes em diálise o risco associado é pouco compreendido e ainda apresenta relatos paradoxais e inesperados66 Levin NW, Kotanko P, Eckardt KU, Kasiske BL, Chazot C, Cheung AK, et al. Blood pressure in chronic kidney disease stage 5D-report from a Kidney Disease: Improving Global Outcomes controversies conference. Kidney Int 2010;77:273-84.. A presença de DRC no estágio 5-D está associada a um risco várias vezes aumentado de mortalidade cardiovascular, em comparação com controles pareados por idade e sexo sem DRC77 Foley RN, Collins AJ. End-stage renal disease in the United States: an update from the United States Renal Data System. J Am Soc Nephrol 2007;18:2644-8.. Estudos epidemiológicos mostraram que a pressão arterial sistólica (PAS), a pressão arterial diastólica (PAD) e os fatores de risco tradicionais para doenças cardiovasculares estão associados a danos em órgãos-alvo, incluindo rigidez vascular e resultados ruins em pacientes em diálise. De fato, o aumento e a diminuição da PAS estão associados a doenças cardiovasculares (DCV) e a diminuição da PAS após hipertensão prévia também está associada a resultados adversos88 Li Z, Lacson E Jr, Lowrie EG, Ofsthun NJ, Kuhlmann MK, Lazarus JM, et al. The epidemiology of systolic blood pressure and death risk in hemodialysis patients. Am J Kidney Dis 2006;48:606-15.. Enquanto esperamos pela revisão das diretrizes do KIDGO para pressão sanguínea DRC, até o momento não há nenhuma diretriz para a população em diálise abordando essa importante questão. Assim, o objetivo desta revisão é fornecer uma análise crítica das informações disponíveis sobre a epidemiologia, os mecanismos patogênicos e os principais pilares sustentadores do manejo da pressão arterial no estágio 5-D da DRC, com base no conhecimento atual.
Epidemiologia da hipertensão no estágio 5 de pacientes em diálise com DRC
Hipertensão arterial (pressão arterial > 140/90 mmHg) é comum em pacientes submetidos à diálise regular, com prevalência de 70-80% entre os pacientes em hemodiálise regular99 Cheigh JS, Milite C, Sullivan JF, Rubin AL, Stenzel KH. Hypertension is not adequately controlled in hemodialysis patients. Am J Kidney Dis 1992;19:453-9. e apenas a minoria tem controle adequado da pressão arterial. A situação para pacientes em diálise peritoneal (DP) não é diferente, e a variabilidade relatada para a prevalência de hipertensão é ainda maior, variando de aproximadamente 30 a mais de 90%1010 Ortega LM, Materson BJ. Hypertension in peritoneal dialysis patients: epidemiology, pathogenesis, and treatment. J Am Soc Hypertens 2011;5:128-36.. Essa variabilidade está relacionada principalmente a diferenças nas definições utilizadas para diagnosticar a hipertensão e as ferramentas aplicadas em vários estudos55 Sarafidis PA, Persu A, Agarwal R, Burnier M, de Leeuw P, Ferro CJ, et al. Hypertension in dialysis patients: a consensus document by the European Renal and Cardiovascular Medicine (EURECA-m) working group of the European Renal Association-European Dialysis and Transplant Association (ERA-EDTA) and the Hypertension and the Kidney working group of the European Society of Hypertension (ESH). Nephrol Dial Transplant 2017;32:620-40.. Estudos epidemiológicos em pacientes em hemodiálise nos EUA, usando diferentes formas de definir a hipertensão, revelaram que 72 a 88% de todos os pacientes estudados apresentavam PA elevada44 Agarwal R, Nissenson AR, Batlle D, Coyne DW, Trout JR, Warnock DG. Prevalence, treatment, and control of hypertension in chronic hemodialysis patients in the United States. Am J Med 2003;115:291-7.,1111 Salem MM. Hypertension in the hemodialysis population: a survey of 649 patients. Am J Kidney Dis 1995;26(3):461-8.,1212 Agarwal R. Supervised atenolol therapy in the management of hemodialysis hypertension. Kidney Int 1999;55:1528-35.. No entanto, nesses estudos, uma alta proporção de pacientes com pressão arterial elevada estava tomando agentes anti-hipertensivos e o número de pacientes com pressão controlada era baixo, entre 30% e 50%44 Agarwal R, Nissenson AR, Batlle D, Coyne DW, Trout JR, Warnock DG. Prevalence, treatment, and control of hypertension in chronic hemodialysis patients in the United States. Am J Med 2003;115:291-7.,1111 Salem MM. Hypertension in the hemodialysis population: a survey of 649 patients. Am J Kidney Dis 1995;26(3):461-8..
Em contraste com a associação incerta entre os registros de PA pré-dialítica e a mortalidade cardiovascular, estudos prospectivos mostraram que a PA interdialítica, registrada como PA domiciliar ou pela monitorização ambulatorial da pressão arterial em pacientes em hemodiálise, tem uma associação mais clara com mortalidade e eventos cardiovasculares1313 Amar J, Vernier I, Rossignol E, Bongard V, Arnaud C, Conte JJ, et al. Nocturnal blood pressure and 24-hour pulse pressure are potent indicators of mortality in hemodialysis patients. Kidney Int 2000;57:2485-91.), (1414 Tripepi G, Fagugli RM, Dattolo P, Parlongo G, Mallamaci F, Buoncristiani U, et al. Prognostic value of 24-hour ambulatory blood pressure monitoring and of night/day ratio in nondiabetic, cardiovascular events-free hemodialysis patients. Kidney Int 2005;68:1294-302.. Em um estudo transversal conduzido na Itália com pacientes em diálise peritoneal usando a definição da OMS/ISH, a prevalência de PA elevada foi de 88% 1515 Cocchi R, Degli Esposti E, Fabbri A, Lucatello A, Sturani A, Quarello F, et al. Prevalence of hypertension in patients on peritoneal dialysis: results of an Italian multicentre study. Nephrol Dial Transplant 1999;14:1536-40.. Em outros estudos, a média de PA de 24 horas não foi diferente entre pacientes em diálise peritoneal automatizada e diálise peritoneal ambulatorial contínua1212 Agarwal R. Supervised atenolol therapy in the management of hemodialysis hypertension. Kidney Int 1999;55:1528-35.,1616 Atas N, Erten Y, Okyay GU, Inal S, Topal S, Öneç K, et al. Left ventricular hypertrophy and blood pressure control in automated and continuous ambulatory peritoneal dialysis patients. Ther Apher Dial 2014;18:297-304., e houve correlações positivas do índice de massa ventricular esquerda com as medidas de PA e carga pressórica1616 Atas N, Erten Y, Okyay GU, Inal S, Topal S, Öneç K, et al. Left ventricular hypertrophy and blood pressure control in automated and continuous ambulatory peritoneal dialysis patients. Ther Apher Dial 2014;18:297-304.. A pressão arterial elevada diagnosticada fora da unidade de diálise com monitorização domiciliar ou ambulatorial da PA está intimamente relacionada à mortalidade33 Alborzi P, Patel N, Agarwal R. Home blood pressures are of greater prognostic value than hemodialysis unit recordings. Clin J Am Soc Nephrol 2007;2:1228-34.,1313 Amar J, Vernier I, Rossignol E, Bongard V, Arnaud C, Conte JJ, et al. Nocturnal blood pressure and 24-hour pulse pressure are potent indicators of mortality in hemodialysis patients. Kidney Int 2000;57:2485-91.. Além disso, os pacientes em diálise muitas vezes não apresentam a diminuição normal da PA à noite,1717 Baumgart P, Walger P, Gemen S, von Eiff M, Raidt H, Rahn KH. Blood pressure elevation during the night in chronic renal failure, hemodialysis and after renal transplantation. Nephron 1991;57:293-8. aumentando seu risco para o desenvolvimento de hipertrofia ventricular esquerda e mortalidade cardiovascular.1818 Foley RN, Parfrey PS, Harnett JD, Kent GM, Martin CJ, Murray DC, et al. Clinical and echocardiographic disease in patients starting end-stage renal disease therapy. Kidney Int 1995;47:186-92. De fato, Foley et al.1919 Foley RN, Parfrey PS, Harnett JD, Kent GM, Murray DC, Barre PE. Impact of hypertension on cardiomyopathy, morbidity and mortality in end-stage renal disease. Kidney Int 1996;49:1379-85. observaram que cada aumento de 10 mmHg na PA média estava independentemente associado a um aumento progressivo da prevalência de hipertrofia ventricular esquerda concêntrica, desenvolvimento de insuficiência cardíaca recorrente e doença cardíaca isquêmica de novo. Adicionalmente, o grau de atrofia cerebral e a pressão pré-dialítica, bem como a atrofia cerebral e a duração da hipertensão, apresentam uma correlação muito alta2020 Savazzi GM, Cusmano F, Bergamaschi E, Vinci S, Allegri L, Garini G. Hypertension as an etiopathological factor in the development of cerebral atrophy in hemodialyzed patients. Nephron 1999;81:17-24.. Esses dados sugerem que a hipertensão de longo prazo é frequentemente não bem controlada, e representa um fator de risco significativo para eventos cardiovasculares em pacientes com DRC em hemodiálise.
Diagnóstico de hipertensão em pacientes em diálise
O diagnóstico da hipertensão na população geral baseia-se em diferentes diretrizes disponíveis, como as diretrizes americana, brasileira e europeia, aumentando a complexidade e a controvérsia do problema2121 Whelton PK, Carey RM, Aronow WS, Casey DE Jr, Collins KJ, Dennison Himmelfarb C, et al. 2017 ACC/AHA/AAPA/ABC/ACPM/AGS/APhA/ASH/ASPC/NMA/PCNA Guideline for the Prevention, Detection, Evaluation, and Management of High Blood Pressure in Adults: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. J Am Coll Cardiol 2018;71:e127-248.
22 Mancia G, Fagard R, Narkiewicz K, Redón J, Zanchetti A, Böhm M, et al. 2013 ESH/ESC Guidelines for the management of arterial hypertension: the Task Force for the management of arterial hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC). J Hypertens 2013;31:1281-357.-2323 Malachias MVB, Gomes MAM, Nobre F, Alessi A, Feitosa AD, Coelho EB. 7th Brazilian Guideline of Arterial Hypertension: Chapter 2 - Diagnosis and Classification. Arq Bras Cardiol 2016;107:7-13.. A diretriz da National Kidney Foundation - Kidney Diseases Outcomes Quality Initiative estabeleceu que a hipertensão em pacientes em hemodiálise é diagnosticada quando a PA pré-diálise é > 140/90 mmHg ou quando a PA pós-diálise é > 130/80 mmHg,2424 Kidney Disease Outcomes Quality Initiative (K/DOQI). K/DOQI clinical practice guidelines on hypertension and antihypertensive agents in chronic kidney disease. Am J Kidney Dis 2004;43:S1-290. mas o exame peridialítico convencional pode não ser preciso. As medidas de PA pré e pós-diálise são obtidas pela equipe da unidade de diálise, muitas vezes sem a atenção necessária para com a técnica correta de mensuração.11 Parati G, Ochoa JE, Bilo G, Agarwal R, Covic A, Dekker FW, et al.; European Renal and Cardiovascular Medicine (EURECA-m) working group of the European Renal Association-European Dialysis Transplantation Association (ERA-EDTA). Hypertension in Chronic Kidney Disease Part 2: Role of Ambulatory and Home Blood Pressure Monitoring for Assessing Alterations in Blood Pressure Variability and Blood Pressure Profiles. Hypertension 2016;67:1102-10.,22 Parati G, Ochoa JE, Bilo G, Agarwal R, Covic A, Dekker FW, et al.; European Renal and Cardiovascular Medicine (EURECA-m) working group of the European Renal Association-European Dialysis Transplantation Association (ERA-EDTA). Hypertension in Chronic Kidney Disease Part 1: Out-of-Office Blood Pressure Monitoring: Methods, Thresholds, and Patterns. Hypertension 2016;67:1093-101. Além disso, outros fatores podem determinar uma leitura imprecisa da PA pré e pós-diálise, como o efeito do jaleco branco, medo de agulhagem incorreta na fístula arteriovenosa, flutuações no volume e tempo limitado para relaxamento (o paciente está ansioso para iniciar a diálise).2525 Rohrscheib MR, Myers OB, Servilla KS, Adams CD, Miskulin D, Bedrick EJ, et al. Age-related blood pressure patterns and blood pressure variability among hemodialysis patients. Clin J Am Soc Nephrol 2008;3:1407-14. Além disso, a baixa acurácia diagnóstica dos registros de PA peri-dialítica foi bem estabelecida por uma metanálise, mostrando que as leituras de pressão arterial pré e pós-diálise fornecem estimativas imprecisas da PA interdialítica média registrada pelo monitoramento ambulatorial da PA de 44 horas.2626 Agarwal R, Peixoto AJ, Santos SF, Zoccali C. Pre- and postdialysis blood pressures are imprecise estimates of interdialytic ambulatory blood pressure. Clin J Am Soc Nephrol 2006;1:389-98. Assim, uma alternativa poderia ser a utilização da média da medida da PA intradialítica, que pode proporcionar maior sensibilidade e especificidade na detecção da hipertensão interdialítica, quando comparada às avaliações da PA pré e pós-diálise.2727 Agarwal R, Metiku T, Tegegne GG, Light RP, Bunaye Z, Bekele DM, et al. Diagnosing hypertension by intradialytic blood pressure recordings. Clin J Am Soc Nephrol 2008;3:1364-72.
No entanto, as medidas da PA obtidas fora das unidades de diálise são frequentemente necessárias para diagnosticar a hipertensão em pacientes em diálise. O monitoramento domiciliar da PA é amplamente aplicado e fortemente recomendado para diagnóstico e tratamento da hipertensão na população geral 2828 Parati G, Stergiou GS, Asmar R, Bilo G, de Leeuw P, Imai Y, et al.; ESH Working Group on Blood Pressure Monitoring. European Society of Hypertension guidelines for blood pressure monitoring at home: a summary report of the Second International Consensus Conference on Home Blood Pressure Monitoring. J Hypertens 2008;26:1505-26.. Além disso, a PA medida em casa demonstrou alta reprodutibilidade a curto prazo de uma semana para outra e está fortemente associada a índices de lesão de órgãos-alvo, como rigidez aórtica e hipertrofia ventricular esquerda (HVE)2929 Moriya H, Ohtake T, Kobayashi S. Aortic stiffness, left ventricular hypertrophy and weekly averaged blood pressure (WAB) in patients on haemodialysis. Nephrol Dial Transplant 2007;22:1198-204.. Atualmente, muitos autores sugerem que a monitorização ambulatorial da pressão arterial (MAPA) pode ser o método padrão-ouro para o diagnóstico da hipertensão em pacientes em diálise22 Parati G, Ochoa JE, Bilo G, Agarwal R, Covic A, Dekker FW, et al.; European Renal and Cardiovascular Medicine (EURECA-m) working group of the European Renal Association-European Dialysis Transplantation Association (ERA-EDTA). Hypertension in Chronic Kidney Disease Part 1: Out-of-Office Blood Pressure Monitoring: Methods, Thresholds, and Patterns. Hypertension 2016;67:1093-101.,1212 Agarwal R. Supervised atenolol therapy in the management of hemodialysis hypertension. Kidney Int 1999;55:1528-35.. Estudos observacionais sugerem claramente que a MAPA prediz mortalidade por todas as causas e cardiovascular melhor do que a PA peri-dialítica1313 Amar J, Vernier I, Rossignol E, Bongard V, Arnaud C, Conte JJ, et al. Nocturnal blood pressure and 24-hour pulse pressure are potent indicators of mortality in hemodialysis patients. Kidney Int 2000;57:2485-91.. A MAPA tem a vantagem de registrar a PA à noite, pois muitos pacientes em diálise apresentam um padrão noturno de PA sem queda, associado à HVE e à mortalidade cardiovascular3030 Zoccali C, Benedetto FA, Tripepi G, Cambareri F, Panuccio V, Candela V, et al. Nocturnal hypoxemia, night-day arterial pressure changes and left ventricular geometry in dialysis patients. Kidney Int 1998;53:1078-84.. Entretanto, a MAPA é inconveniente para muitos pacientes em diálise com alta carga de tratamento, alta prevalência de distúrbios do sono e, eventualmente, comprometimento de membros superiores bilaterais com fístula arteriovenosa. Portanto, a monitorização domiciliar da PA parece ser uma abordagem simples e eficaz para avaliar a PA e tomar decisões terapêuticas em pacientes em diálise3131 Zoccali C, Tripepi R, Torino C, Tripepi G, Mallamaci F. Moderator's view: Ambulatory blood pressure monitoring and home blood pressure for the prognosis, diagnosis and treatment of hypertension in dialysis patients. Nephrol Dial Transplant 2015;30:1443-8.. A Tabela 1 apresenta informações para o diagnóstico de hipertensão em pacientes em diálise. Em contraste com o declínio típico da PA durante a sessão de hemodiálise, 10 a 15% dos pacientes em hemodiálise exibem uma elevação paradoxal da pressão intradialítica3232 Georgianos PI, Sarafidis PA, Zoccali C. Intradialysis Hypertension in End-Stage Renal Disease Patients: Clinical Epidemiology, Pathogenesis, and Treatment. Hypertension 2015;66:456-63., e embora essa resposta anormal tenha sido reconhecida há muito tempo, a razão exata ainda não é bem conhecida. A hipertensão intradialítica pode ser definida como um aumento de pelo menos 15 mmHg na PA média durante a diálise ou um aumento de pelo menos 10 mmHg na PA sistólica durante ou imediatamente após a diálise em um certo número de sessões de diálise (as últimas três ou quatro sessões de diálise)3333 Inrig JK. Intradialytic hypertension: a less-recognized cardiovascular complication of hemodialysis. Am J Kidney Dis 2010;55:580-9..
Mecanismos envolvidos nas alterações da pressão arterial no estágio 5 da DRC
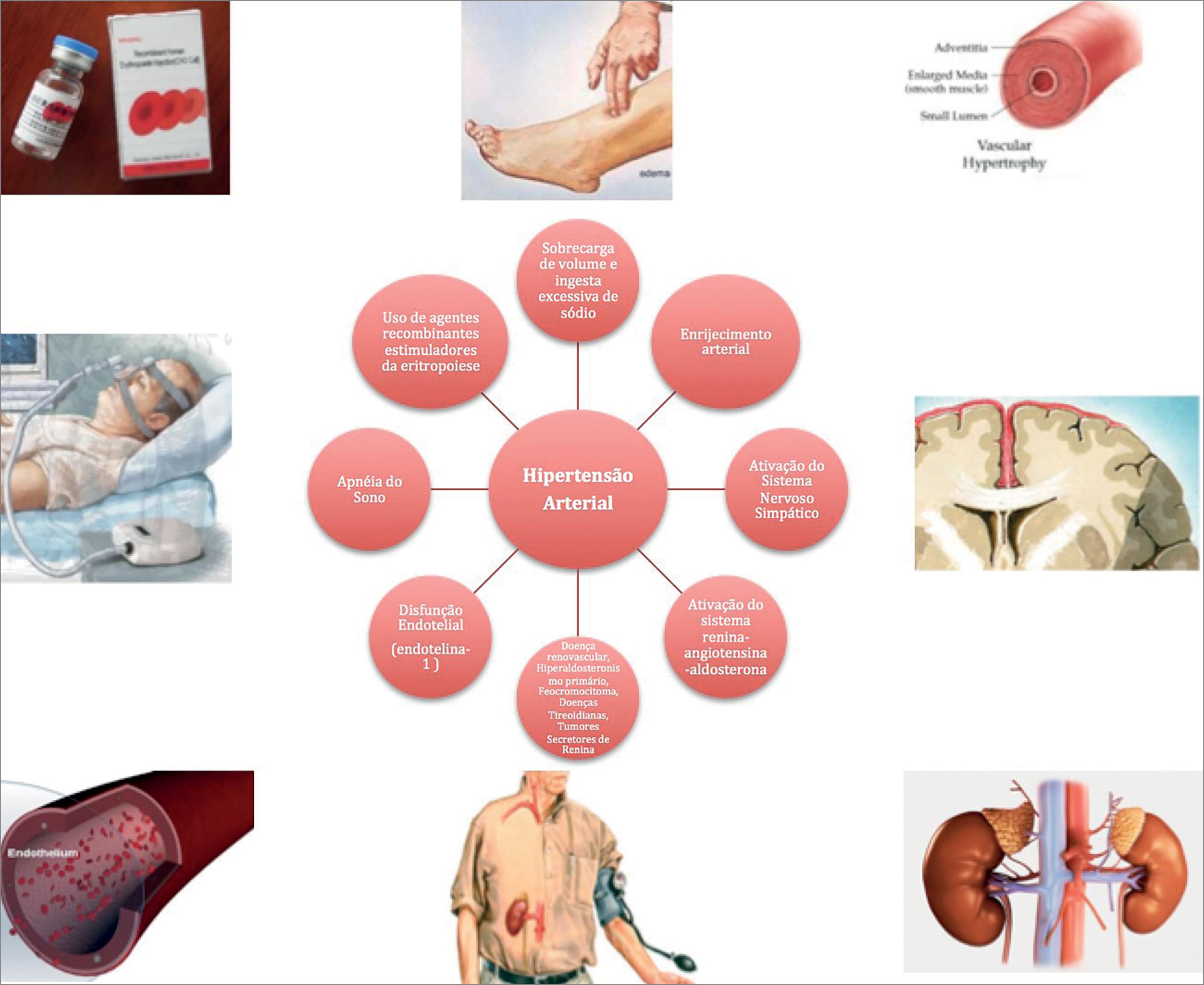
A fisiopatologia da hipertensão em pacientes em diálise é complexa e multifatorial66 Levin NW, Kotanko P, Eckardt KU, Kasiske BL, Chazot C, Cheung AK, et al. Blood pressure in chronic kidney disease stage 5D-report from a Kidney Disease: Improving Global Outcomes controversies conference. Kidney Int 2010;77:273-84.,1212 Agarwal R. Supervised atenolol therapy in the management of hemodialysis hypertension. Kidney Int 1999;55:1528-35.. Uma seleção de fatores de risco potencialmente envolvidos no desenvolvimento da hipertensão em pacientes em diálise está listada na Figura 1. O aumento do débito cardíaco, resistência vascular periférica ou ambos resultam em elevação da pressão arterial em pacientes em diálise. Em primeiro lugar, o volume intravascular excessivo é o principal fator patogênico da hipertensão em pacientes em diálise, e essa expansão do volume extracelular é mais provável de ser observada em pacientes com doença renal terminal em estágio avançado (DRT)55 Sarafidis PA, Persu A, Agarwal R, Burnier M, de Leeuw P, Ferro CJ, et al. Hypertension in dialysis patients: a consensus document by the European Renal and Cardiovascular Medicine (EURECA-m) working group of the European Renal Association-European Dialysis and Transplant Association (ERA-EDTA) and the Hypertension and the Kidney working group of the European Society of Hypertension (ESH). Nephrol Dial Transplant 2017;32:620-40.. Há mais água corporal total em pacientes hipertensos em hemodiálise quando comparados a normotensos3434 Anderstam B, Katzarski K, Bergström J. Serum levels of NG, NG-dimethyl-L-arginine, a potential endogenous nitric oxide inhibitor in dialysis patients. J Am Soc Nephrol 1997;8:1437-42., e quando fluidos corporais excessivos são removidos e o peso seco é atingido com diálise lenta e mais freqüente, a PA pode ser melhorada em aproximadamente 90% dos pacientes3535 Chazot C, Charra B, Laurent G, Didier C, Vo Van C, Terrat JC, et al. Interdialysis blood pressure control by long haemodialysis sessions. Nephrol Dial Transplant 1995;10:831-7.. De fato, perturbações na auto-regulação vascular podem ocorrer em pacientes com DRT hipervolêmicos, a saber, o aumento inadequado da angiotensina II em relação ao volume, aumento da reatividade vascular a pressores endógenos e aumento do débito cardíaco na presença de alta resistência vascular periférica3636 Mailloux LU. Hypertension in chronic renal failure and ESRD: prevalence, pathophysiology, and outcomes. Semin Nephrol 2001;21:146-56.. Em muitos casos, a hipertensão está relacionada ao ganho de peso durante o intervalo entre duas sessões de diálise e a PA pode ser melhorada pela correção do volume extracelular, embora os resultados obtidos em diferentes estudos sejam contraditórios. De fato, alguns estudos observaram que o estado do volume afeta a PA interdialítica3737 Rahman M, Dixit A, Donley V, Gupta S, Hanslik T, Lacson E, et al. Factors associated with inadequate blood pressure control in hypertensive hemodialysis patients. Am J Kidney Dis 1999;33:498-506., enquanto outras séries não confirmaram essa relação3838 Savage T, Fabbian F, Giles M, Tomson CR, Raine AE. Interdialytic weight gain and 48-h blood pressure in haemodialysis patients. Nephrol Dial Transplant 1997;12:2308-11.. Além disso, existe uma correlação entre a perda de peso durante a hemodiálise e a redução da PAS3939 Mittal SK, Kowalski E, Trenkle J, McDonough B, Halinski D, Devlin K, et al. Prevalence of hypertension in a hemodialysis population. Clin Nephrol 1999;51:77-82.; e a sensibilidade ao volume é maior em pacientes hipertensos do que em pacientes normotensos em diálise4040 Grekas D, Bamichas G, Bacharaki D, Goutzaridis N, Kasimatis E, Tourkantonis A. Hypertension in chronic hemodialysis patients: current view on pathophysiology and treatment. Clin Nephrol 2000;53:164-8..
Também já foi relatado que a normalização do volume extracelular do paciente ajuda a melhorar o ritmo circadiano da PA, que pode ser anormal na presença de expansão de volume4141 Zucchelli P, Santoro A. Dry weight in hemodialysis: volemic control. Semin Nephrol 2001;21:286-90.. Em pacientes que permanecem hipertensos apesar da ultrafiltração intensiva, o excesso de sódio e volume pode desempenhar apenas um papel secundário. Além disso, a falta de correlação entre o volume extracelular e a PA nesses pacientes já foi descrita anteriormente4242 Schultze G, Piefke S, Molzahn M. Blood pressure in terminal renal failure. Fluid spaces and the renin-angiotensin-system. Nephron 1980;25:15-24.. Curiosamente, Titze et al.4343 Titze J, Ritz E. Salt and its effect on blood pressure and target organ damage: new pieces in an old puzzle. J Nephrol 2009;22:177-89. recentemente descreveram um sistema desconhecido de armazenamento de sódio, particularmente ligado a glicosaminoglicanos na pele, que não promove atividade osmótica. Este novo compartimento, com concentrações de sódio de 180-190 meq/L, age como um tampão para o sódio exógeno. De maneira inadequada, esse estoque de sódio pode ser liberado no sangue, resultando em hipervolemia e estresse oxidativo, ou induzindo a ativação de mecanismos celulares envolvidos na fibrose tecidual. De fato, em pacientes em hemodiálise, sódio e água na pele e músculos estão aumentados e o fator de crescimento endotelial vascular (VEGF) está reduzido quando comparado a indivíduos saudáveis pareados por idade, e esse fenômeno pode contribuir para a hipertensão4444 Dahlmann A, Dörfelt K, Eicher F, Linz P, Kopp C, Mössinger I, et al. Magnetic resonance-determined sodium removal from tissue stores in hemodialysis patients. Kidney Int 2015;87:434-41..
O papel da secreção excessiva de renina em relação ao volume e ao sódio tem sido reconhecido como um fator importante na patogênese da hipertensão em pacientes em diálise. É bem conhecido que a ativação do sistema renina-angiotensina-aldosterona ocorre mesmo em pacientes com DRT em tratamento dialítico,4545 Kornerup HJ, Schmitz O, Danielsen H, Pedersen EB, Giese J. Significance of the renin-angiotensin system for blood pressure regulation in end-stage renal disease. Contrib Nephrol 1984;41:123-7. resultando em hipertensão dependente de renina refratária à diálise. Além disso, o hiperaldosteronismo secundário contribui para a hipertensão e recentemente ficou claro que, além da hipertensão, a aldosterona pode ter inúmeras ações independentes da pressão arterial que, sob condições de alta concentração salina, é prejudicial ao rim, coração e vasculatura.4646 Ritz E, Koleganova N. Aldosterone in uremia - beyond blood pressure. Blood Purif 2010;29:111-3.
O aumento da rigidez arterial ocorre com frequência em pacientes em diálise, principalmente relacionado ao metabolismo de distúrbios de cálcio e fosfato, resultando em calcificação vascular.4747 Georgianos PI, Sarafidis PA, Lasaridis AN. Arterial stiffness: a novel cardiovascular risk factor in kidney disease patients. Curr Vasc Pharmacol 2015;13:229-38. Envelhecimento vascular prematuro e enrijecimento arterial são observados com a progressão da DRC e na DRT. Esse envelhecimento acelerado está associado à remodelação externa de grandes vasos, caracterizada por aumento do raio arterial que não é totalmente compensado pela hipertrofia da parede arterial. O enrijecimento arterial em pacientes com DRC e DRT é de origem multifatorial, com extensas calcificações arteriais representando uma co-variável maior.4848 Briet M, Boutouyrie P, Laurent S, London GM. Arterial stiffness and pulse pressure in CKD and ESRD. Kidney Int 2012;82:388-400. Em pacientes em diálise, a rigidez arterial avaliada pela velocidade da onda de pulso aórtica (VOP) está intimamente relacionada à PA interdialítica elevada, e o aumento da VOP enfraquece a amplitude circadiana da PA sistólica e da pressão de pulso.4949 Agarwal R, Light RP. Arterial stiffness and interdialytic weight gain influence ambulatory blood pressure patterns in hemodialysis patients. Am J Physiol Renal Physiol 2008;294:F303-8.
O aumento da atividade do sistema nervoso simpático pode contribuir para a hipertensão em pacientes com doença renal terminal.5050 Campese VM, Romoff MS, Levitan D, Lane K, Massry SG. Mechanisms of autonomic nervous system dysfunction in uremia. Kidney Int 1981;20:246-53. A descarga simpática foi 2,5 vezes maior em pacientes em diálise do que em indivíduos normais e esta alta não foi correlacionada com a concentração plasmática de noradrenalina ou com a atividade da renina plasmática.5151 Converse RL Jr, Jacobsen TN, Toto RD, Jost CM, Cosentino F, Fouad-Tarazi F, et al. Sympathetic overactivity in patients with chronic renal failure. N Engl J Med 1992;327:1912-8. A sobrecarga hídrica de mais de 6% do peso corporal resulta na ativação do sistema nervoso simpático5252 Odar-Cederlöf I, Ericsson F, Theodorsson E, Kjellstrand CM. Is neuropeptide Y a contributor to volume-induced hypertension? Am J Kidney Dis 1998;31:803-8. e a inibição da enzima conversora de angiotensina (ECA) pode resultar em redução dessa hiperatividade simpática.5353 Ligtenberg G, Blankestijn PJ, Oey PL, Klein IH, Dijkhorst-Oei LT, Boomsma F, et al. Reduction of sympathetic hyperactivity by enalapril in patients with chronic renal failure. N Engl J Med 1999;340:1321-8. A vasodilatação dependente do endotélio é prejudicada na uremia, e a deficiência de óxido nítrico (NO) ocorre em pacientes com insuficiência renal terminal, contribuindo para a hipertensão em pacientes em hemodiálise e diálise peritoneal.5454 Schmidt RJ, Domico J, Samsell LS, Yokota S, Tracy TS, Sorkin MI, et al. Indices of activity of the nitric oxide system in hemodialysis patients. Am J Kidney Dis 1999;34:228-34. A produção de NO pelo endotélio vascular é inibida pela dimetil-arginina assimétrica (ADMA), que se acumula em pacientes com DRC, particularmente naqueles com complicações ateroscleróticas.5555 Kielstein JT, Böger RH, Bode-Böger SM, Schäffer J, Barbey M, Koch KM, et al. Asymmetric dimethylarginine plasma concentrations differ in patients with end-stage renal disease: relationship to treatment method and atherosclerotic disease. J Am Soc Nephrol 1999;10:594-600. No entanto, nenhuma correlação significativa foi observada entre as concentrações de ADMA e BP em pacientes em diálise.3434 Anderstam B, Katzarski K, Bergström J. Serum levels of NG, NG-dimethyl-L-arginine, a potential endogenous nitric oxide inhibitor in dialysis patients. J Am Soc Nephrol 1997;8:1437-42. Além disso, a deficiência de renalase, uma enzima produzida pelo rim que metaboliza catecolaminas e substâncias semelhantes a catecolaminas, pode contribuir para o aumento da atividade do sistema nervoso simpático na DRC.5656 Desir GV. Regulation of blood pressure and cardiovascular function by renalase. Kidney Int 2009;76:366-70.
A disfunção endotelial pode contribuir para a hipertensão em pacientes em diálise por meio de vários mecanismos. Pacientes com DRC apresentam disponibilidade reduzida de NO medida em vasodilatação dependente de NO, e esse fenômeno pode estar relacionado à redução da produção de NO.5757 Wever R, Boer P, Hijmering M, Stroes E, Verhaar M, Kastelein J, et al. Nitric oxide production is reduced in patients with chronic renal failure. Arterioscler Thromb Vasc Biol 1999;19:1168-72. De fato, altos níveis circulantes de dimetil-arginina assimétrica (ADMA), um inibidor da NO sintase endógena, são observados em pacientes com DRC,5858 Vallance P, Leone A, Calver A, Collier J, Moncada S. Accumulation of an endogenous inhibitor of nitric oxide synthesis in chronic renal failure. Lancet 1992;339:572-5. e em pacientes em hemodiálise por DRT, a ADMA está associada com doença cardiovascular e mortalidade5959 Boger RH, Zoccali C. ADMA: a novel risk factor that explains excess cardiovascular event rate in patients with end-stage renal disease. Atheroscler Suppl 2003;4:23-8.. Além disso, a endotelina-1 pode ter um papel importante no desenvolvimento da hipertensão intradialítica,6060 Gutiérrez-Adrianzén OA, Moraes ME, Almeida AP, Lima JW, Marinho MF, Marques AL, et al. Pathophysiological, cardiovascular and neuroendocrine changes in hypertensive patients during the hemodialysis session. J Hum Hypertens 2015;29:366-72. que ocorre regularmente em 10 a 15% dos pacientes em hemodiálise6161 Van Buren PN. Pathophysiology and implications of intradialytic hypertension. Curr Opin Nephrol Hypertens 2017;26:303-10..
Em 20 a 30% dos pacientes com DRC, a administração regular de eritropoietina recombinante humana (rHuEPO) é acompanhada por hipertensão "de novo" ou agravamento da hipertensão preexistente e o aumento da PA ocorre dentro de algumas semanas a meses após o início da rHuEPO.6262 Abraham PA, Macres MG. Blood pressure in hemodialysis patients during amelioration of anemia with erythropoietin. J Am Soc Nephrol 1991;2:927-36. Grekas et al. (40) observaram hipertensão em 62% dos pacientes em hemodiálise tratados com rHuEPO, mas apenas em 38% daqueles que não receberam rHuEPO. Um aumento na massa de hemácias durante ou após a correção da anemia leva a aumentar a viscosidade sanguínea e pós-carga cardíaca6363 Mayer G, Hörl WH. Cardiovascular effects of increasing hemoglobin in chronic renal failure. Am J Nephrol 1996;16:263-7. e pode contribuir para a hipertensão nesses pacientes, mas o aumento da PA pode ocorrer mesmo antes do aumento do hematócrito6464 Lebel M, Kingma I, Grose JH, Langlois S. Hemodynamic and hormonal changes during erythropoietin therapy in hemodialysis patients. J Am Soc Nephrol 1998;9:97-104.. Outros fatores relacionados à hipertensão induzida pela rHuEPO em pacientes com DRC incluem liberação de endotelina, disfunção endotelial vascular, hipertensão preexistente, elevação do cálcio livre no citosol nas células musculares lisas vasculares, inibição da síntese de NO, e rápida correção da anemia6565 Hörl MP, Hörl WH. Hemodialysis-associated hypertension: pathophysiology and therapy. Am J Kidney Dis 2002;39:227-44.. Além disso, doses mais altas de rHuEPO, níveis mais altos de hemoglobina alvo6666 Phrommintikul A, Haas SJ, Elsik M, Krum H. Mortality and target haemoglobin concentrations in anaemic patients with chronic kidney disease treated with erythropoietin: a meta-analysis. Lancet 2007;369:381-8. e, possivelmente, a modalidade de diálise6767 Krapf R, Hulter HN. Arterial hypertension induced by erythropoietin and erythropoiesis-stimulating agents (ESA). Clin J Am Soc Nephrol 2009;4:470-80. foram associados a uma maior resposta da PA.
A apnéia do sono é altamente prevalente e pode estar relacionada à sobrecarga de volume6868 Tada T, Kusano KF, Ogawa A, Iwasaki J, Sakuragi S, Kusano I, et al. The predictors of central and obstructive sleep apnoea in haemodialysis patients. Nephrol Dial Transplant 2007;22:1190-7. em pacientes em diálise. A hipoxemia noturna na apnéia do sono tem sido associada a maior PAS noturna e maior espessura relativa da parede ventricular esquerda3030 Zoccali C, Benedetto FA, Tripepi G, Cambareri F, Panuccio V, Candela V, et al. Nocturnal hypoxemia, night-day arterial pressure changes and left ventricular geometry in dialysis patients. Kidney Int 1998;53:1078-84. e hipertensão resistente,1212 Agarwal R. Supervised atenolol therapy in the management of hemodialysis hypertension. Kidney Int 1999;55:1528-35.,6969 Abdel-Kader K, Dohar S, Shah N, Jhamb M, Reis SE, Strollo P, et al. Resistant hypertension and obstructive sleep apnea in the setting of kidney disease. J Hypertens 2012;30:960-6. enquanto o índice de apnéia-hipopnéia obstrutiva é significativamente reduzido após hemodiálise com redução da sobrecarga de líquidos.7070 Ogna A, Forni Ogna V, Mihalache A, Pruijm M, Halabi G, Phan O, et al. Obstructive Sleep Apnea Severity and Overnight Body Fluid Shift before and after Hemodialysis. Clin J Am Soc Nephrol 2015;10:1002-10.
O hiperparatireoidismo secundário também pode resultar em hipertensão na população com doença renal terminal por mecanismos que incluem a entrada de cálcio nas células musculares lisas da parede do vaso. No entanto, a paratireoidectomia não conseguiu corrigir a hipertensão em pacientes em hemodiálise crônica.7171 Ifudu O, Matthew JJ, Macey LJ, Hong JS, Sumrani N, Sommer BG, et al. Parathyroidectomy does not correct hypertension in patients on maintenance hemodialysis. Am J Nephrol 1998;18:28-34. Em contraste, a terapia com vitamina D ativada para o hiperparatireoidismo secundário resultou em reduções significativas na pressão média.7272 Raine AE, Bedford L, Simpson AW, Ashley CC, Brown R, Woodhead JS, et al. Hyperparathyroidism, platelet intracellular free calcium and hypertension in chronic renal failure. Kidney Int 1993;43:700-5.
Em pacientes em diálise, os níveis plasmáticos do peptídeo natriurético atrial α-humano (α-ANP) estão elevados, refletindo a expansão do volume extracelular. Os valores de α-ANP diminuem após a diálise, mas permanecem elevados em pacientes com alteração hemodinâmica do átrio esquerdo.6565 Hörl MP, Hörl WH. Hemodialysis-associated hypertension: pathophysiology and therapy. Am J Kidney Dis 2002;39:227-44. Semelhante ao α-ANP, a concentração de peptídeo natriurético cerebral (BNP) é maior em pacientes em hemodiálise do que em voluntários saudáveis, e o BNP é diminuído de forma menos eficiente pelo procedimento de diálise.7373 Kohse KP, Feifel K, Mayer-Wehrstein R. Differential regulation of brain and atrial natriuretic peptides in hemodialysis patients. Clin Nephrol 1993;40:83-90. Franz et al.7474 Franz M, Woloszczuk W, Hörl WH. N-terminal fragments of the proatrial natriuretic peptide in patients before and after hemodialysis treatment. Kidney Int 2000;58:374-83. observaram que, em pacientes em hemodiálise com hipertensão moderada ou grave, os níveis de fragmentos pró-ANP e α-ANP foram maiores do que em pacientes com hipertensão leve. De fato, os peptídeos natriuréticos cardíacos estão relacionados à massa ventricular esquerda e predizem mortalidade cardiovascular em pacientes em diálise.66 Levin NW, Kotanko P, Eckardt KU, Kasiske BL, Chazot C, Cheung AK, et al. Blood pressure in chronic kidney disease stage 5D-report from a Kidney Disease: Improving Global Outcomes controversies conference. Kidney Int 2010;77:273-84.
Embora tenha sido estabelecido que a restrição de sal interdialítico ou a remoção intradialítica de sal e fluidos é eficaz na redução da PA, o sucesso ao longo do tempo é muito raro.7575 Luik AJ, v d Sande FM, Weideman P, Cheriex E, Kooman JP, Leunissen KM. The influence of increasing dialysis treatment time and reducing dry weight on blood pressure control in hemodialysis patients: a prospective study. Am J Nephrol 2001;21:471-8. Outros estudos foram realizados na população em diálise para investigar o impacto da restrição de sal nos níveis pressóricos. Ozkahya et al.,7676 Ozkahya M, Ok E, Cirit M, Aydin S, Akçiçek F, Basçi A, et al. Regression of left ventricular hypertrophy in haemodialysis patients by ultrafiltration and reduced salt intake without antihypertensive drugs. Nephrol Dial Transplant 1998;13:1489-93. enfatizaram a restrição de sódio, interrompendo todos os fármacos anti-hipertensivos e intensificando a ultrafiltração, observaram não apenas redução significativa nos níveis de PA, mas também na espessura da parede do ventrículo esquerdo. O mesmo grupo observou, em outro estudo, que a restrição de cloreto de sódio a < 6 g/dia determinou a normalização dos níveis de PA após 36 meses.7777 Ozkahya M, Töz H, Unsal A, Ozerkan F, Asci G, Gürgün C, et al. Treatment of hypertension in dialysis patients by ultrafiltration: role of cardiac dilatation and time factor. Am J Kidney Dis 1999;34:218-21.
Como o concentrado de sódio do dialisato é geralmente maior que o do soro do paciente, ele pode influenciar a sede pós-diálise, o ganho de peso interdialítico e a PA. Além disso, o balanço salino é positivo com a ingestão habitual de sódio e o uso de soluções salinas para manter o volume plasmático durante a UF e para tratar episódios de hipotensão durante o tratamento dialítico. Baixo nível de sódio no dialisato resultou em menor sódio plasmático intra e inter-dialítico quando comparado com alto dialisato de sódio,7878 De Nicola L, Bellizzi V, Minutolo R, Cioffi M, Giannattasio P, Terracciano V, et al. Effect of dialysate sodium concentration on interdialytic increase of potassium. J Am Soc Nephrol 2000;11:2337-43. e uma diálise com programação variável de sódio de 155 meq/L a 135mEq/L resultou em redução do uso de drogas anti-hipertensivas, sem alterações na PA pré-sistêmica quando comparada à concentração de sódio no dialisato de 140 meq/L.7979 Flanigan MJ, Khairullah QT, Lim VS. Dialysate sodium delivery can alter chronic blood pressure management. Am J Kidney Dis 1997;29:383-91.
Manejo da hipertensão no estágio 5 da DRC
Dados atuais de vários estudos observacionais1212 Agarwal R. Supervised atenolol therapy in the management of hemodialysis hypertension. Kidney Int 1999;55:1528-35.,8080 Carney EF. Dialysis: U-shaped associations between changes in blood pressure during dialysis and patient survival. Nat Rev Nephrol 2013;9:431. e de um estudo prospectivo de coorte8181 Robinson BM, Tong L, Zhang J, Wolfe RA, Goodkin DA, Greenwood RN, et al. Blood pressure levels and mortality risk among hemodialysis patients in the Dialysis Outcomes and Practice Patterns Study. Kidney Int 2012;82:570-80. sugerem uma associação em "U" entre a PA pré-HD e a mortalidade. Isso significa que a pressão arterial abaixo de certos níveis pode ser mais prejudicial do que níveis elevados, especialmente quando os pacientes apresentam cardiomiopatia grave, que frequentemente modifica a relação entre PA e mortalidade, determinando uma sobrevida muito baixa em pacientes com insuficiência renal terminal e PAS < 115 mmHg.8282 Klassen PS, Lowrie EG, Reddan DN, DeLong ER, Coladonato JA, Szczech LA, et al. Association between pulse pressure and mortality in patients undergoing maintenance hemodialysis. JAMA 2002;287:1548-55. Por outro lado, PAS pós-diálise > 180 e PAD > 90 mmHg estiveram associadas ao aumento da mortalidade cardiovascular e devem ser tratadas de forma agressiva.8383 Zager PG, Nikolic J, Brown RH, Campbell MA, Hunt WC, Peterson D, et al. »," ®,(r) §,§ ­, ¹,¹ ²,² ³,³ ß,ß Þ,Þ þ,þ ×,× Ú,Ú ú,ú Û,Û û,û Ù,Ù ù,ù ¨,¨ Ü,Ü ü,ü Ý,Ý ý,ý ¥,¥ ÿ,ÿ ¶,¶ U »," ®,(r) §,§ ­, ¹,¹ ²,² ³,³ ß,ß Þ,Þ þ,þ ×,× Ú,Ú ú,ú Û,Û û,û Ù,Ù ù,ù ¨,¨ Ü,Ü ü,ü Ý,Ý ý,ý ¥,¥ ÿ,ÿ ¶,¶ curve association of blood pressure and mortality in hemodialysis patients. Medical Directors of Dialysis Clinic, Inc. Kidney Int 1998;54:561-9. Essa epidemiologia reversa da PA e a mortalidade cardiovascular dificultam o estabelecimento de um alvo real e confiável para os níveis de PA em pacientes em diálise. No entanto, diretrizes internacionais para doença cardiovascular recomendam nível de PA menor que 140/90 mmHg no início da semana. Contudo, essa recomendação não deve ser aplicada uniformemente em situações de diálise,1212 Agarwal R. Supervised atenolol therapy in the management of hemodialysis hypertension. Kidney Int 1999;55:1528-35.,8484 Hirakata H, Nitta K, Inaba M, Shoji T, Fujii H, Kobayashi S, et al.; Japanese Society for Dialysis Therapy. Japanese Society for Dialysis Therapy guidelines for management of cardiovascular diseases in patients on chronic hemodialysis. Ther Apher Dial 2012;16:387-435. pois a abordagem agressiva para o controle da PA pode aumentar o risco de hipotensão intra-dialítica sintomática e suas conseqüências.
Terapia não farmacológica
A maioria dos pacientes no estágio 5 da DRC desenvolve um balanço de sódio positivo e um aumento no volume extracelular (VEC), com sobrecarga de sal e água desempenhando um papel central no desenvolvimento da hipertensão. O alto consumo de sal mostrou-se associado a uma alta PAS pré-diálise e doença cardiovascular.8585 Mc Causland FR, Waikar SS, Brunelli SM. Increased dietary sodium is independently associated with greater mortality among prevalent hemodialysis patients. Kidney Int 2012;82:204-11. A normalização do equilíbrio de sódio e fluidos é fundamental para controlar a PA e reduzir os eventos cardiovasculares, conforme indicado pela diretriz mais recente;66 Levin NW, Kotanko P, Eckardt KU, Kasiske BL, Chazot C, Cheung AK, et al. Blood pressure in chronic kidney disease stage 5D-report from a Kidney Disease: Improving Global Outcomes controversies conference. Kidney Int 2010;77:273-84. a restrição dietética de sal deve estar abaixo de 5-6 g/dia e o ganho de peso interdialítico não deve exceder 0,8 kg/dia. De fato, em pacientes em diálise peritoneal, o excesso de sal e água são os determinantes mais importantes da PA elevada,1212 Agarwal R. Supervised atenolol therapy in the management of hemodialysis hypertension. Kidney Int 1999;55:1528-35.,8686 Chen W, Cheng LT, Wang T. Salt and fluid intake in the development of hypertension in peritoneal dialysis patients. Ren Fail 2007;29:427-32. e muitos autores recomendam restrição de sal (< 5g/dia) para todos os pacientes em diálise peritoneal, a menos que haja evidência de contração de volume.8787 Wang AY, Brimble KS, Brunier G, Holt SG, Jha V, Johnson DW, et al. ISPD Cardiovascular and Metabolic Guidelines in Adult Peritoneal Dialysis Patients Part I - Assessment and Management of Various Cardiovascular Risk Factors. Perit Dial Int 2015;35:379-87. Tais metas dietéticas são particularmente importantes na perda da função renal residual e quando o paciente tem um elevado transporte de membrana que interfere negativamente na ultrafiltração.
Outra maneira de regular o volume de líquidos dos pacientes em diálise, particularmente em hemodiálise, é definir um peso seco adequado (PS). Na prática clínica, o PS é geralmente estabelecido por um declínio progressivo no peso corporal pós-diálise durante um período de 4-8 semanas após o início da hemodiálise de manutenção.8888 Chazot C, Charra B, Vo Van C, Jean G, Vanel T, Calemard E, et al. The Janus-faced aspect of 'dry weight'. Nephrol Dial Transplant 1999;14:121-4. Este PS pós-diálise pode ser definido como o peso corporal pós-diálise em que o VEC está dentro da faixa normal ou o valor da PA alvo sem a necessidade de medicação anti-hipertensiva.66 Levin NW, Kotanko P, Eckardt KU, Kasiske BL, Chazot C, Cheung AK, et al. Blood pressure in chronic kidney disease stage 5D-report from a Kidney Disease: Improving Global Outcomes controversies conference. Kidney Int 2010;77:273-84. Essas definições, obviamente, não podem ser aplicadas àqueles pacientes que são hipotensos devido à cardiomiopatia. Em contraste, estabelecer um PS para pacientes em DP é muito complicado, e motivo de debates frequentes. Existem algumas tentativas de monitorar o estado volêmico dos pacientes em DP com bioimpedância multifreqüencial e os resultados são aceitáveis.1212 Agarwal R. Supervised atenolol therapy in the management of hemodialysis hypertension. Kidney Int 1999;55:1528-35.,8989 Davies SJ, Davenport A. The role of bioimpedance and biomarkers in helping to aid clinical decision-making of volume assessments in dialysis patients. Kidney Int 2014;86:489-96.
A história clínica e o exame físico podem ajudar a detectar aumentos mais óbvios do VEC, mas, em geral, a avaliação do PS utilizando parâmetros clínicos apresenta baixa sensibilidade.9090 Wizemann V, Schilling M. Dilemma of assessing volume state--the use and the limitations of a clinical score. Nephrol Dial Transplant 1995;10:2114-7. Tentativas foram feitas para determinar o PS pelo dispositivo de bioimpedância (BIA),9191 Zhu F, Kuhlmann MK, Kotanko P, Seibert E, Leonard EF, Levin NW. A method for the estimation of hydration state during hemodialysis using a calf bioimpedance technique. Physiol Meas 2008;29:S503-16. monitorando a resistência regional e a resistividade na panturrilha, mostrando que o peso alvo prescrito pode diminuir com o tempo, melhorando o controle da PA. Outros dispositivos de BIA que avaliam a composição corporal completa, fornecem leituras do estado da PA e do VEC que podem ser úteis no acompanhamento do equilíbrio de fluidos e informações sobre o aumento do risco de mortalidade quando há super-hidratação.9292 Wizemann V, Wabel P, Chamney P, Zaluska W, Moissl U, Rode C, et al. The mortality risk of overhydration in haemodialysis patients. Nephrol Dial Transplant 2009;24:1574-9. Estudos randomizados controlados demonstraram que a otimização do PS por métodos de bioimpedância é segura e capaz de melhorar o controle da PA em pacientes em diálise1212 Agarwal R. Supervised atenolol therapy in the management of hemodialysis hypertension. Kidney Int 1999;55:1528-35.,9393 Moissl U, Arias-Guillén M, Wabel P, Fontseré N, Carrera M, Campistol JM, et al. Bioimpedance-guided fluid management in hemodialysis patients. Clin J Am Soc Nephrol 2013;8:1575-82..
Outros métodos para avaliar o VEC incluem a medição do diâmetro da veia cava, que requer tempo para o equilíbrio pós-diálise e é dependente do operador9494 Brennan JM, Ronan A, Goonewardena S, Blair JE, Hammes M, Shah D, et al. Handcarried ultrasound measurement of the inferior vena cava for assessment of intravascular volume status in the outpatient hemodialysis clinic. Clin J Am Soc Nephrol 2006;1:749-53.. A ultrassonografia pulmonar pode detectar congestão pulmonar assintomática em pacientes em hemodiálise, e o escore BL-US (ultrassonografia de linhas B) resultante é um preditor forte e independente de morte e eventos cardíacos nessa população9595 Zoccali C, Torino C, Tripepi R, Tripepi G, D'Arrigo G, Postorino M, et al.; Lung US in CKD Working Group. Pulmonary congestion predicts cardiac events and mortality in ESRD. J Am Soc Nephrol 2013;24:639-46..
Aumentar a concentração de sódio no dialisante acima dos valores pré-diálise pode ajudar a reduzir os episódios de hipotensão intradialítica, mas pode levar ao aumento do ganho de peso pela sede aumentada66 Levin NW, Kotanko P, Eckardt KU, Kasiske BL, Chazot C, Cheung AK, et al. Blood pressure in chronic kidney disease stage 5D-report from a Kidney Disease: Improving Global Outcomes controversies conference. Kidney Int 2010;77:273-84.. Pode ser melhor ajustar a concentração de dialisato de sódio para corresponder ao sódio plasmático pré-diálise do paciente e não usar o dialisato de sódio mais alto. O uso de dextrose hipertônica em vez de solução salina no manejo da hipotensão intradialítica e cãibras também aumenta o potencial para um balanço de sódio neutro. A restrição de sal na dieta é útil para a otimização da DP e o controle da pressão arterial em pacientes em diálise. Vários estudos têm relatado consistentemente uma diminuição no ganho de peso interdialítico, redução associada nos níveis de PA e redução mais significativa na massa ventricular esquerda1212 Agarwal R. Supervised atenolol therapy in the management of hemodialysis hypertension. Kidney Int 1999;55:1528-35.,9696 Kayikcioglu M, Tumuklu M, Ozkahya M, Ozdogan O, Asci G, Duman S, et al. The benefit of salt restriction in the treatment of end-stage renal disease by haemodialysis. Nephrol Dial Transplant 2009;24:956-62..
Sessões mais frequentes de diálise
A hemodiálise convencional é freqüentemente associada a altas taxas de ultrafiltração (UF), o que aumenta o risco de cãibras musculares e episódios hipotensivos. Os sintomas são tratados por infusão intravenosa de solução salina, o que favorece a expansão do VCE, a hipertensão e o risco de desenvolver HVE. A prescrição de sessões de diálise mais longas ou mais frequentes permite a diminuição das taxas de UF e reduz o risco de complicações intradialíticas9797 Okada K, Abe M, Hagi C, Maruyama T, Maruyama N, Ito K, et al. Prolonged protective effect of short daily hemodialysis against dialysis-induced hypotension. Kidney Blood Press Res 2005;28:68-76., melhorando a HVE9898 Ayus JC, Mizani MR, Achinger SG, Thadhani R, Go AS, Lee S. Effects of short daily versus conventional hemodialysis on left ventricular hypertrophy and inflammatory markers: a prospective, controlled study. J Am Soc Nephrol 2005;16:2778-88. e a função cardíaca9999 Chan C, Floras JS, Miller JA, Pierratos A. Improvement in ejection fraction by nocturnal haemodialysis in end-stage renal failure patients with coexisting heart failure. Nephrol Dial Transplant 2002;17:1518-21.. As sessões de hemodiálise mais freqüentes do que o esquema convencional, de três vezes por semana, reduzem a PA de maneira mais consistente e requerem menos medicações anti-hipertensivas para atingir o mesmo controle da PA1212 Agarwal R. Supervised atenolol therapy in the management of hemodialysis hypertension. Kidney Int 1999;55:1528-35.,100100 Zimmerman DL, Ruzicka M, Hebert P, Fergusson D, Touyz RM, Burns KD. Short daily versus conventional hemodialysis for hypertensive patients: a randomized cross-over study. PLoS One 2014;9:e97135.. As diretrizes da European Best Practices recomendam que a duração da sessão de hemodiálise não seja determinada apenas por um resultado ótimo de KT/V, mas pelo estabelecimento de pelo menos três sessões de diálise de 4 horas cada para garantir o status ideal do volume101101 Tattersall J, Martin-Malo A, Pedrini L, Basci A, Canaud B, Fouque D, et al. EBPG guideline on dialysis strategies. Nephrol Dial Transplant 2007;22:ii5-21..
Além disso, no estudo FREEDOM (102), um estudo de coorte prospectivo de HD diária curta, o número médio de agentes anti-hipertensivos prescritos diminuiu de 1,7 para 1,0 em 1 ano, enquanto o percentual de pacientes que não receberam anti-hipertensivos aumentou de 21 para 47%. Kotanko et al. (103) analisaram os efeitos de sessões de hemodiálise mais freqüentes sobre o controle da PA em um estudo controlado randomizado, incluindo pacientes em tratamento diurno e noturno, diariamente em HD, versus três sessões semanais de HD, e observaram após doze meses uma redução sustentada e significativa em ambos os sistemas diastólico e sistólico da PA, bem como no número de prescrições de medicamentos anti-hipertensivos. A HD noturna parece reduzir acentuadamente a resistência periférica total e a noradrenalina plasmática e restaurar a vasodilatação dependente do endotélio. Em conclusão, as informações acima indicam que a HD intensiva, em geral, reduz a PA e a necessidade de medicamentos anti-hipertensivos.
Terapia farmacológica
Ao prescrever medicamentos anti-hipertensivos para pacientes no estágio 5 de DRC submetidos à diálise, é preciso estar ciente de que a farmacocinética pode estar alterada pela excreção renal prejudicada e pela capacidade de absorção do medicamento. Além disso, a adesão reduzida, os efeitos colaterais e os custos financeiros podem ter um impacto na eficácia do tratamento. Outros problemas relacionados a essa população especial são a ocorrência de hipotensão intradialítica e trombose de acesso vascular.104104 Sulowicz W, Radziszewski A. Dialysis induced hypotension--a serious clinical problem in renal replacement therapy. Med Pregl 2007;60:14-20. Adicionalmente, alguns medicamentos anti-hipertensivos também são cardioprotetores, diminuindo o risco de morte por doença cardiovascular. Exemplos de drogas nessa categoria são os inibidores do sistema renina-angiotensina-aldosterona (SRAA), os bloqueadores beta-adrenérgicos, os bloqueadores dos canais de cálcio (BCCs) e os inibidores da aldosterona (para pacientes que não fazem diálise). A angiotensina II tem sido implicada na disfunção endotelial, na proliferação do músculo liso, na ruptura da placa aterosclerótica e na HVE, esta última ocorrendo mesmo quando a PA é controlada66 Levin NW, Kotanko P, Eckardt KU, Kasiske BL, Chazot C, Cheung AK, et al. Blood pressure in chronic kidney disease stage 5D-report from a Kidney Disease: Improving Global Outcomes controversies conference. Kidney Int 2010;77:273-84.. Na população geral, o uso de bloqueadores do SRAA diminui eventos cardiovasculares105105 Chrysant SG, Chrysant GS. The pleiotropic effects of angiotensin receptor blockers. J Clin Hypertens (Greenwich) 2006;8:261-8. em pacientes com disfunção ventricular esquerda e com doença arterial coronariana estável. Da mesma forma, na população sem DRT, o uso clínico de β-bloqueadores confere proteção cardiovascular106106 Furgeson SB, Chonchol M. Beta-blockade in chronic dialysis patients. Semin Dial 2008;21:43-8. e os BCC diminuem os níveis de cálcio intracelular produzidos pelo hiperparatireoidismo secundário e alteram o perfil lipídico, o que pode reduzir o risco cardiovascular107107 Gadallah MF, el-Shahawy M, Andrews G, Ibrahim M, Ramdeen G, Hanna D, et al. Factors modulating cytosolic calcium. Role in lipid metabolism and cardiovascular morbidity and mortality in peritoneal dialysis patients. Adv Perit Dial 2001;17:29-36..
Estudos com drogas anti-hipertensivas em pacientes em diálise com DRC mostraram resultados limitados, e duas metanálises de ensaios randomizados concluíram que o verdadeiro mérito desses medicamentos (SRAA, BCCs, bloqueadores β-adrenérgicos) não está bem estabelecido108108 Agarwal R, Sinha AD. Cardiovascular protection with antihypertensive drugs in dialysis patients: systematic review and meta-analysis. Hypertension 2009;53:860-6.,109109 Heerspink HJ, Ninomiya T, Zoungas S, de Zeeuw D, Grobbee DE, Jardine MJ, et al. Effect of lowering blood pressure on cardiovascular events and mortality in patients on dialysis: a systematic review and meta-analysis of randomised controlled trials. Lancet 2009;373:1009-15.. As duas meta-análises confirmaram que o tratamento com agentes anti-hipertensivos esteve associado à redução de eventos cardiovasculares, mas quando pacientes normotensos foram incluídos na análise, os efeitos benéficos das drogas ficaram marcadamente diminuídos, tornando-se não significativos. Mais importante ainda, nenhum dos ensaios incluídos nestas meta-análises visou especificamente os níveis de PA. De acordo com esses dados, o controle da PA por medicamentos anti-hipertensivos leva a melhores desfechos cardiovasculares, no entanto, um esquema preferencial para controle da PA e redução da mortalidade ainda não foi estabelecido.
Quanto à hemodiálise, faltam estudos para definir o alvo ideal da pressão arterial para reduzir os eventos cardiovasculares. No entanto, um estudo recente merece alguns comentários. Um estudo controlado randomizado descreveu um benefício significativo na função cardíaca de pacientes em diálise peritoneal com o uso de espironolactona, além de um inibidor do SRAA, sem qualquer risco adicional de hipercalemia110110 Ito Y, Mizuno M, Suzuki Y, Tamai H, Hiramatsu T, Ohashi H, et al.; Nagoya Spiro Study Group. Long-term effects of spironolactone in peritoneal dialysis patients. J Am Soc Nephrol 2014;25:1094-102.. Finalmente, não há estudos suficientes comparando os benefícios de uma classe de anti-hipertensivos em relação a outro para pacientes em DP. No entanto, o impacto positivo dos inibidores do SRAA na função renal residual e na preservação da membrana peritoneal encontrados em alguns estudos deu alguma popularidade a essas classes de drogas anti-hipertensivas111111 Li PK, Chow KM, Wong TY, Leung CB, Szeto CC. Effects of an angiotensin-converting enzyme inhibitor on residual renal function in patients receiving peritoneal dialysis. A randomized, controlled study. Ann Intern Med 2003;139:105-12.,112112 Suzuki H, Kanno Y, Sugahara S, Okada H, Nakamoto H. Effects of an angiotensin II receptor blocker, valsartan, on residual renal function in patients on CAPD. Am J Kidney Dis 2004;43:1056-64..
As recomendações sobre drogas anti-hipertensivas em pacientes em diálise com DRC baseiam-se em seus efeitos na redução da PA, efeitos colaterais e efeitos cardiovasculares protetores. O uso de inibidores do SRAA, bloqueadores β-adrenérgicos e BCCs é desejável em pacientes em diálise, devido a seus efeitos na atividade da renina plasmática, na redução da atividade simpática e na diminuição dos níveis de cálcio intracelular, respectivamente66 Levin NW, Kotanko P, Eckardt KU, Kasiske BL, Chazot C, Cheung AK, et al. Blood pressure in chronic kidney disease stage 5D-report from a Kidney Disease: Improving Global Outcomes controversies conference. Kidney Int 2010;77:273-84.. Além de qualquer preferência individual, não há evidências fortes que recomendem uma classe específica de medicamento anti-hipertensivo em relação à outra na população em diálise com DRC, e apenas poucos estudos clínicos demonstraram alguns efeitos cardiovasculares benéficos da inibição do SRAA e bloqueadores β-adrenérgicos nesses pacientes113113 Suzuki H, Kanno Y, Sugahara S, Ikeda N, Shoda J, Takenaka T, et al. Effect of angiotensin receptor blockers on cardiovascular events in patients undergoing hemodialysis: an open-label randomized controlled trial. Am J Kidney Dis 2008;52:501-6.,114114 Cice G, Ferrara L, D'Andrea A, D'Isa S, Di Benedetto A, Cittadini A, et al. Carvedilol increases two-year survivalin dialysis patients with dilated cardiomyopathy: a prospective, placebo-controlled trial. J Am Coll Cardiol 2003;41:1438-44.. Os inibidores do SRAA devem ser usados em pacientes com DRC-VD porque esses agentes são particularmente benéficos para doenças cardíacas frequentemente observadas em pacientes em diálise, e são eficazes na redução da massa ventricular esquerda e na mortalidade115115 Matsumoto N, Ishimitsu T, Okamura A, Seta H, Takahashi M, Matsuoka H. Effects of imidapril on left ventricular mass in chronic hemodialysis patients. Hypertens Res 2006;29:253-60.,116116 Takahashi A, Takase H, Toriyama T, Sugiura T, Kurita Y, Ueda R, et al. Candesartan, an angiotensin II type-1 receptor blocker, reduces cardiovascular events in patients on chronic haemodialysis--a randomized study. Nephrol Dial Transplant 2006;21:2507-12.. Especificamente relacionado a esse tópico de interesse, há um estudo de fase 3 em andamento avaliando a espironolactona 25 mg (bloqueio da aldosterona para Avaliação da Melhoria na Saúde na Doença Renal Crônica Terminal (ACHIEVE) - https://clinicaltrials.gov/ct2/show/NCT03020303), e sua finalidade é determinar se a espironolactona reduz a morte ou hospitalização por insuficiência cardíaca, e se a droga é bem tolerada em pacientes que necessitam de diálise.
Hipertensão e insuficiência cardíaca (IC) são condições frequentemente observadas na população com DRC e a hiperatividade simpática desempenha um papel importante nesse cenário, tornando os β-bloqueadores adequados para o tratamento de ambas as condições117117 Bakris GL, Hart P, Ritz E. Beta blockers in the management of chronic kidney disease. Kidney Int 2006;70:1905-13.. Uma metanálise concluiu que o tratamento com betabloqueadores melhorou a mortalidade por todas as causas em pacientes com DRC e insuficiência cardíaca118118 Badve SV, Roberts MA, Hawley CM, Cass A, Garg AX, Krum H, et al. Effects of beta-adrenergic antagonists in patients with chronic kidney disease: a systematic review and meta-analysis. J Am Coll Cardiol 2011;58:1152-61.. Além disso, alguns estudos prospectivos demonstraram que o uso de β-bloqueadores está associado à redução do risco de mortalidade em pacientes em hemodiálise114114 Cice G, Ferrara L, D'Andrea A, D'Isa S, Di Benedetto A, Cittadini A, et al. Carvedilol increases two-year survivalin dialysis patients with dilated cardiomyopathy: a prospective, placebo-controlled trial. J Am Coll Cardiol 2003;41:1438-44.,119119 Nakao K, Makino H, Morita S, Takahashi Y, Akizawa T, Saito A, et al.; J-DOPPS Investigators Group. Beta-blocker prescription and outcomes in hemodialysis patients from the Japan Dialysis Outcomes and Practice Patterns Study. Nephron Clin Pract 2009;113:c132-9.. Mais recentemente, outro agente terapêutico, o sacubitril-valsartan, foi aprovado para uso em pacientes com IC e esse agente de dupla ação potencializa as funções dos peptídeos natriuréticos e inibe o sistema renina-angiotensina 120120 Gervasini G, Robles NR. Potential beneficial effects of sacubitril-valsartan in renal disease: a new field for a new drug. Expert Opin Investig Drugs 2017;26:651-9., com potencial benefício para pacientes com DRC.
Finalmente, a remoção de um fármaco anti-hipertensivo durante as sessões de diálise (por exemplo, β-bloqueadores) pode predispor os pacientes a um descontrole da PA121121 Weir MA, Dixon SN, Fleet JL, Roberts MA, Hackam DG, Oliver MJ, et al. ß-Blocker dialyzability and mortality in older patients receiving hemodialysis. J Am Soc Nephrol 2015;26:987-96. e a farmacocinética dos inibidores da ECA é bastante diferente, determinando a suplementação pós-diálise de medicamentos em alguns casos. Alguns medicamentos com efeitos anti-hipertensivos de longa duração (Atenolol e Lisinopril) podem ser administrados três vezes por semana, aumentando assim a farmaco-aderência1212 Agarwal R. Supervised atenolol therapy in the management of hemodialysis hypertension. Kidney Int 1999;55:1528-35.,122122 Agarwal R, Lewis R, Davis JL, Becker B. Lisinopril therapy for hemodialysis hypertension: hemodynamic and endocrine responses. Am J Kidney Dis 2001;38:1245-50..
Conclusões
A hipertensão é freqüentemente diagnosticada na população em diálise, é de difícil manejo e associada a um risco aumentado de doença cardiovascular. A complexa fisiopatologia dessa condição explica a grande dificuldade de seu tratamento. Atualmente, a superioridade da pressão arterial auto-mensurada no domicílio na pré-hemodiálise é convincente e outras ferramentas de investigação, como a monitorização ambulatorial da pressão arterial, estão se tornando mais aplicadas em populações com DRC. Em geral, todos os medicamentos anti-hipertensivos podem ser usados na população em diálise, com o ajuste adequado da dose determinado pela depuração durante as sessões de diálise. O uso combinado de terapias não farmacológicas, particularmente dietética de sódio, ajuste de sódio no dialisato e uso de drogas anti-hipertensivas (preferencialmente cardioprotetoras) pode ser a melhor prática para otimizar o controle da pressão arterial. Ensaios clínicos randomizados com drogas anti-hipertensivas visando reduzir a mortalidade ainda são necessários, bem como uma diretriz definitiva do controle da PA na população em diálise. Além disso, intervenções não farmacológicas com diferentes modalidades ou esquemas de diálise e restrição de sódio devem ser adequadamente testadas nesta população de alto risco.
References
-
1Parati G, Ochoa JE, Bilo G, Agarwal R, Covic A, Dekker FW, et al.; European Renal and Cardiovascular Medicine (EURECA-m) working group of the European Renal Association-European Dialysis Transplantation Association (ERA-EDTA). Hypertension in Chronic Kidney Disease Part 2: Role of Ambulatory and Home Blood Pressure Monitoring for Assessing Alterations in Blood Pressure Variability and Blood Pressure Profiles. Hypertension 2016;67:1102-10.
-
2Parati G, Ochoa JE, Bilo G, Agarwal R, Covic A, Dekker FW, et al.; European Renal and Cardiovascular Medicine (EURECA-m) working group of the European Renal Association-European Dialysis Transplantation Association (ERA-EDTA). Hypertension in Chronic Kidney Disease Part 1: Out-of-Office Blood Pressure Monitoring: Methods, Thresholds, and Patterns. Hypertension 2016;67:1093-101.
-
3Alborzi P, Patel N, Agarwal R. Home blood pressures are of greater prognostic value than hemodialysis unit recordings. Clin J Am Soc Nephrol 2007;2:1228-34.
-
4Agarwal R, Nissenson AR, Batlle D, Coyne DW, Trout JR, Warnock DG. Prevalence, treatment, and control of hypertension in chronic hemodialysis patients in the United States. Am J Med 2003;115:291-7.
-
5Sarafidis PA, Persu A, Agarwal R, Burnier M, de Leeuw P, Ferro CJ, et al. Hypertension in dialysis patients: a consensus document by the European Renal and Cardiovascular Medicine (EURECA-m) working group of the European Renal Association-European Dialysis and Transplant Association (ERA-EDTA) and the Hypertension and the Kidney working group of the European Society of Hypertension (ESH). Nephrol Dial Transplant 2017;32:620-40.
-
6Levin NW, Kotanko P, Eckardt KU, Kasiske BL, Chazot C, Cheung AK, et al. Blood pressure in chronic kidney disease stage 5D-report from a Kidney Disease: Improving Global Outcomes controversies conference. Kidney Int 2010;77:273-84.
-
7Foley RN, Collins AJ. End-stage renal disease in the United States: an update from the United States Renal Data System. J Am Soc Nephrol 2007;18:2644-8.
-
8Li Z, Lacson E Jr, Lowrie EG, Ofsthun NJ, Kuhlmann MK, Lazarus JM, et al. The epidemiology of systolic blood pressure and death risk in hemodialysis patients. Am J Kidney Dis 2006;48:606-15.
-
9Cheigh JS, Milite C, Sullivan JF, Rubin AL, Stenzel KH. Hypertension is not adequately controlled in hemodialysis patients. Am J Kidney Dis 1992;19:453-9.
-
10Ortega LM, Materson BJ. Hypertension in peritoneal dialysis patients: epidemiology, pathogenesis, and treatment. J Am Soc Hypertens 2011;5:128-36.
-
11Salem MM. Hypertension in the hemodialysis population: a survey of 649 patients. Am J Kidney Dis 1995;26(3):461-8.
-
12Agarwal R. Supervised atenolol therapy in the management of hemodialysis hypertension. Kidney Int 1999;55:1528-35.
-
13Amar J, Vernier I, Rossignol E, Bongard V, Arnaud C, Conte JJ, et al. Nocturnal blood pressure and 24-hour pulse pressure are potent indicators of mortality in hemodialysis patients. Kidney Int 2000;57:2485-91.
-
14Tripepi G, Fagugli RM, Dattolo P, Parlongo G, Mallamaci F, Buoncristiani U, et al. Prognostic value of 24-hour ambulatory blood pressure monitoring and of night/day ratio in nondiabetic, cardiovascular events-free hemodialysis patients. Kidney Int 2005;68:1294-302.
-
15Cocchi R, Degli Esposti E, Fabbri A, Lucatello A, Sturani A, Quarello F, et al. Prevalence of hypertension in patients on peritoneal dialysis: results of an Italian multicentre study. Nephrol Dial Transplant 1999;14:1536-40.
-
16Atas N, Erten Y, Okyay GU, Inal S, Topal S, Öneç K, et al. Left ventricular hypertrophy and blood pressure control in automated and continuous ambulatory peritoneal dialysis patients. Ther Apher Dial 2014;18:297-304.
-
17Baumgart P, Walger P, Gemen S, von Eiff M, Raidt H, Rahn KH. Blood pressure elevation during the night in chronic renal failure, hemodialysis and after renal transplantation. Nephron 1991;57:293-8.
-
18Foley RN, Parfrey PS, Harnett JD, Kent GM, Martin CJ, Murray DC, et al. Clinical and echocardiographic disease in patients starting end-stage renal disease therapy. Kidney Int 1995;47:186-92.
-
19Foley RN, Parfrey PS, Harnett JD, Kent GM, Murray DC, Barre PE. Impact of hypertension on cardiomyopathy, morbidity and mortality in end-stage renal disease. Kidney Int 1996;49:1379-85.
-
20Savazzi GM, Cusmano F, Bergamaschi E, Vinci S, Allegri L, Garini G. Hypertension as an etiopathological factor in the development of cerebral atrophy in hemodialyzed patients. Nephron 1999;81:17-24.
-
21Whelton PK, Carey RM, Aronow WS, Casey DE Jr, Collins KJ, Dennison Himmelfarb C, et al. 2017 ACC/AHA/AAPA/ABC/ACPM/AGS/APhA/ASH/ASPC/NMA/PCNA Guideline for the Prevention, Detection, Evaluation, and Management of High Blood Pressure in Adults: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. J Am Coll Cardiol 2018;71:e127-248.
-
22Mancia G, Fagard R, Narkiewicz K, Redón J, Zanchetti A, Böhm M, et al. 2013 ESH/ESC Guidelines for the management of arterial hypertension: the Task Force for the management of arterial hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC). J Hypertens 2013;31:1281-357.
-
23Malachias MVB, Gomes MAM, Nobre F, Alessi A, Feitosa AD, Coelho EB. 7th Brazilian Guideline of Arterial Hypertension: Chapter 2 - Diagnosis and Classification. Arq Bras Cardiol 2016;107:7-13.
-
24Kidney Disease Outcomes Quality Initiative (K/DOQI). K/DOQI clinical practice guidelines on hypertension and antihypertensive agents in chronic kidney disease. Am J Kidney Dis 2004;43:S1-290.
-
25Rohrscheib MR, Myers OB, Servilla KS, Adams CD, Miskulin D, Bedrick EJ, et al. Age-related blood pressure patterns and blood pressure variability among hemodialysis patients. Clin J Am Soc Nephrol 2008;3:1407-14.
-
26Agarwal R, Peixoto AJ, Santos SF, Zoccali C. Pre- and postdialysis blood pressures are imprecise estimates of interdialytic ambulatory blood pressure. Clin J Am Soc Nephrol 2006;1:389-98.
-
27Agarwal R, Metiku T, Tegegne GG, Light RP, Bunaye Z, Bekele DM, et al. Diagnosing hypertension by intradialytic blood pressure recordings. Clin J Am Soc Nephrol 2008;3:1364-72.
-
28Parati G, Stergiou GS, Asmar R, Bilo G, de Leeuw P, Imai Y, et al.; ESH Working Group on Blood Pressure Monitoring. European Society of Hypertension guidelines for blood pressure monitoring at home: a summary report of the Second International Consensus Conference on Home Blood Pressure Monitoring. J Hypertens 2008;26:1505-26.
-
29Moriya H, Ohtake T, Kobayashi S. Aortic stiffness, left ventricular hypertrophy and weekly averaged blood pressure (WAB) in patients on haemodialysis. Nephrol Dial Transplant 2007;22:1198-204.
-
30Zoccali C, Benedetto FA, Tripepi G, Cambareri F, Panuccio V, Candela V, et al. Nocturnal hypoxemia, night-day arterial pressure changes and left ventricular geometry in dialysis patients. Kidney Int 1998;53:1078-84.
-
31Zoccali C, Tripepi R, Torino C, Tripepi G, Mallamaci F. Moderator's view: Ambulatory blood pressure monitoring and home blood pressure for the prognosis, diagnosis and treatment of hypertension in dialysis patients. Nephrol Dial Transplant 2015;30:1443-8.
-
32Georgianos PI, Sarafidis PA, Zoccali C. Intradialysis Hypertension in End-Stage Renal Disease Patients: Clinical Epidemiology, Pathogenesis, and Treatment. Hypertension 2015;66:456-63.
-
33Inrig JK. Intradialytic hypertension: a less-recognized cardiovascular complication of hemodialysis. Am J Kidney Dis 2010;55:580-9.
-
34Anderstam B, Katzarski K, Bergström J. Serum levels of NG, NG-dimethyl-L-arginine, a potential endogenous nitric oxide inhibitor in dialysis patients. J Am Soc Nephrol 1997;8:1437-42.
-
35Chazot C, Charra B, Laurent G, Didier C, Vo Van C, Terrat JC, et al. Interdialysis blood pressure control by long haemodialysis sessions. Nephrol Dial Transplant 1995;10:831-7.
-
36Mailloux LU. Hypertension in chronic renal failure and ESRD: prevalence, pathophysiology, and outcomes. Semin Nephrol 2001;21:146-56.
-
37Rahman M, Dixit A, Donley V, Gupta S, Hanslik T, Lacson E, et al. Factors associated with inadequate blood pressure control in hypertensive hemodialysis patients. Am J Kidney Dis 1999;33:498-506.
-
38Savage T, Fabbian F, Giles M, Tomson CR, Raine AE. Interdialytic weight gain and 48-h blood pressure in haemodialysis patients. Nephrol Dial Transplant 1997;12:2308-11.
-
39Mittal SK, Kowalski E, Trenkle J, McDonough B, Halinski D, Devlin K, et al. Prevalence of hypertension in a hemodialysis population. Clin Nephrol 1999;51:77-82.
-
40Grekas D, Bamichas G, Bacharaki D, Goutzaridis N, Kasimatis E, Tourkantonis A. Hypertension in chronic hemodialysis patients: current view on pathophysiology and treatment. Clin Nephrol 2000;53:164-8.
-
41Zucchelli P, Santoro A. Dry weight in hemodialysis: volemic control. Semin Nephrol 2001;21:286-90.
-
42Schultze G, Piefke S, Molzahn M. Blood pressure in terminal renal failure. Fluid spaces and the renin-angiotensin-system. Nephron 1980;25:15-24.
-
43Titze J, Ritz E. Salt and its effect on blood pressure and target organ damage: new pieces in an old puzzle. J Nephrol 2009;22:177-89.
-
44Dahlmann A, Dörfelt K, Eicher F, Linz P, Kopp C, Mössinger I, et al. Magnetic resonance-determined sodium removal from tissue stores in hemodialysis patients. Kidney Int 2015;87:434-41.
-
45Kornerup HJ, Schmitz O, Danielsen H, Pedersen EB, Giese J. Significance of the renin-angiotensin system for blood pressure regulation in end-stage renal disease. Contrib Nephrol 1984;41:123-7.
-
46Ritz E, Koleganova N. Aldosterone in uremia - beyond blood pressure. Blood Purif 2010;29:111-3.
-
47Georgianos PI, Sarafidis PA, Lasaridis AN. Arterial stiffness: a novel cardiovascular risk factor in kidney disease patients. Curr Vasc Pharmacol 2015;13:229-38.
-
48Briet M, Boutouyrie P, Laurent S, London GM. Arterial stiffness and pulse pressure in CKD and ESRD. Kidney Int 2012;82:388-400.
-
49Agarwal R, Light RP. Arterial stiffness and interdialytic weight gain influence ambulatory blood pressure patterns in hemodialysis patients. Am J Physiol Renal Physiol 2008;294:F303-8.
-
50Campese VM, Romoff MS, Levitan D, Lane K, Massry SG. Mechanisms of autonomic nervous system dysfunction in uremia. Kidney Int 1981;20:246-53.
-
51Converse RL Jr, Jacobsen TN, Toto RD, Jost CM, Cosentino F, Fouad-Tarazi F, et al. Sympathetic overactivity in patients with chronic renal failure. N Engl J Med 1992;327:1912-8.
-
52Odar-Cederlöf I, Ericsson F, Theodorsson E, Kjellstrand CM. Is neuropeptide Y a contributor to volume-induced hypertension? Am J Kidney Dis 1998;31:803-8.
-
53Ligtenberg G, Blankestijn PJ, Oey PL, Klein IH, Dijkhorst-Oei LT, Boomsma F, et al. Reduction of sympathetic hyperactivity by enalapril in patients with chronic renal failure. N Engl J Med 1999;340:1321-8.
-
54Schmidt RJ, Domico J, Samsell LS, Yokota S, Tracy TS, Sorkin MI, et al. Indices of activity of the nitric oxide system in hemodialysis patients. Am J Kidney Dis 1999;34:228-34.
-
55Kielstein JT, Böger RH, Bode-Böger SM, Schäffer J, Barbey M, Koch KM, et al. Asymmetric dimethylarginine plasma concentrations differ in patients with end-stage renal disease: relationship to treatment method and atherosclerotic disease. J Am Soc Nephrol 1999;10:594-600.
-
56Desir GV. Regulation of blood pressure and cardiovascular function by renalase. Kidney Int 2009;76:366-70.
-
57Wever R, Boer P, Hijmering M, Stroes E, Verhaar M, Kastelein J, et al. Nitric oxide production is reduced in patients with chronic renal failure. Arterioscler Thromb Vasc Biol 1999;19:1168-72.
-
58Vallance P, Leone A, Calver A, Collier J, Moncada S. Accumulation of an endogenous inhibitor of nitric oxide synthesis in chronic renal failure. Lancet 1992;339:572-5.
-
59Boger RH, Zoccali C. ADMA: a novel risk factor that explains excess cardiovascular event rate in patients with end-stage renal disease. Atheroscler Suppl 2003;4:23-8.
-
60Gutiérrez-Adrianzén OA, Moraes ME, Almeida AP, Lima JW, Marinho MF, Marques AL, et al. Pathophysiological, cardiovascular and neuroendocrine changes in hypertensive patients during the hemodialysis session. J Hum Hypertens 2015;29:366-72.
-
61Van Buren PN. Pathophysiology and implications of intradialytic hypertension. Curr Opin Nephrol Hypertens 2017;26:303-10.
-
62Abraham PA, Macres MG. Blood pressure in hemodialysis patients during amelioration of anemia with erythropoietin. J Am Soc Nephrol 1991;2:927-36.
-
63Mayer G, Hörl WH. Cardiovascular effects of increasing hemoglobin in chronic renal failure. Am J Nephrol 1996;16:263-7.
-
64Lebel M, Kingma I, Grose JH, Langlois S. Hemodynamic and hormonal changes during erythropoietin therapy in hemodialysis patients. J Am Soc Nephrol 1998;9:97-104.
-
65Hörl MP, Hörl WH. Hemodialysis-associated hypertension: pathophysiology and therapy. Am J Kidney Dis 2002;39:227-44.
-
66Phrommintikul A, Haas SJ, Elsik M, Krum H. Mortality and target haemoglobin concentrations in anaemic patients with chronic kidney disease treated with erythropoietin: a meta-analysis. Lancet 2007;369:381-8.
-
67Krapf R, Hulter HN. Arterial hypertension induced by erythropoietin and erythropoiesis-stimulating agents (ESA). Clin J Am Soc Nephrol 2009;4:470-80.
-
68Tada T, Kusano KF, Ogawa A, Iwasaki J, Sakuragi S, Kusano I, et al. The predictors of central and obstructive sleep apnoea in haemodialysis patients. Nephrol Dial Transplant 2007;22:1190-7.
-
69Abdel-Kader K, Dohar S, Shah N, Jhamb M, Reis SE, Strollo P, et al. Resistant hypertension and obstructive sleep apnea in the setting of kidney disease. J Hypertens 2012;30:960-6.
-
70Ogna A, Forni Ogna V, Mihalache A, Pruijm M, Halabi G, Phan O, et al. Obstructive Sleep Apnea Severity and Overnight Body Fluid Shift before and after Hemodialysis. Clin J Am Soc Nephrol 2015;10:1002-10.
-
71Ifudu O, Matthew JJ, Macey LJ, Hong JS, Sumrani N, Sommer BG, et al. Parathyroidectomy does not correct hypertension in patients on maintenance hemodialysis. Am J Nephrol 1998;18:28-34.
-
72Raine AE, Bedford L, Simpson AW, Ashley CC, Brown R, Woodhead JS, et al. Hyperparathyroidism, platelet intracellular free calcium and hypertension in chronic renal failure. Kidney Int 1993;43:700-5.
-
73Kohse KP, Feifel K, Mayer-Wehrstein R. Differential regulation of brain and atrial natriuretic peptides in hemodialysis patients. Clin Nephrol 1993;40:83-90.
-
74Franz M, Woloszczuk W, Hörl WH. N-terminal fragments of the proatrial natriuretic peptide in patients before and after hemodialysis treatment. Kidney Int 2000;58:374-83.
-
75Luik AJ, v d Sande FM, Weideman P, Cheriex E, Kooman JP, Leunissen KM. The influence of increasing dialysis treatment time and reducing dry weight on blood pressure control in hemodialysis patients: a prospective study. Am J Nephrol 2001;21:471-8.
-
76Ozkahya M, Ok E, Cirit M, Aydin S, Akçiçek F, Basçi A, et al. Regression of left ventricular hypertrophy in haemodialysis patients by ultrafiltration and reduced salt intake without antihypertensive drugs. Nephrol Dial Transplant 1998;13:1489-93.
-
77Ozkahya M, Töz H, Unsal A, Ozerkan F, Asci G, Gürgün C, et al. Treatment of hypertension in dialysis patients by ultrafiltration: role of cardiac dilatation and time factor. Am J Kidney Dis 1999;34:218-21.
-
78De Nicola L, Bellizzi V, Minutolo R, Cioffi M, Giannattasio P, Terracciano V, et al. Effect of dialysate sodium concentration on interdialytic increase of potassium. J Am Soc Nephrol 2000;11:2337-43.
-
79Flanigan MJ, Khairullah QT, Lim VS. Dialysate sodium delivery can alter chronic blood pressure management. Am J Kidney Dis 1997;29:383-91.
-
80Carney EF. Dialysis: U-shaped associations between changes in blood pressure during dialysis and patient survival. Nat Rev Nephrol 2013;9:431.
-
81Robinson BM, Tong L, Zhang J, Wolfe RA, Goodkin DA, Greenwood RN, et al. Blood pressure levels and mortality risk among hemodialysis patients in the Dialysis Outcomes and Practice Patterns Study. Kidney Int 2012;82:570-80.
-
82Klassen PS, Lowrie EG, Reddan DN, DeLong ER, Coladonato JA, Szczech LA, et al. Association between pulse pressure and mortality in patients undergoing maintenance hemodialysis. JAMA 2002;287:1548-55.
-
83Zager PG, Nikolic J, Brown RH, Campbell MA, Hunt WC, Peterson D, et al. »," ®,(r) §,§ ­, ¹,¹ ²,² ³,³ ß,ß Þ,Þ þ,þ ×,× Ú,Ú ú,ú Û,Û û,û Ù,Ù ù,ù ¨,¨ Ü,Ü ü,ü Ý,Ý ý,ý ¥,¥ ÿ,ÿ ¶,¶ U »," ®,(r) §,§ ­, ¹,¹ ²,² ³,³ ß,ß Þ,Þ þ,þ ×,× Ú,Ú ú,ú Û,Û û,û Ù,Ù ù,ù ¨,¨ Ü,Ü ü,ü Ý,Ý ý,ý ¥,¥ ÿ,ÿ ¶,¶ curve association of blood pressure and mortality in hemodialysis patients. Medical Directors of Dialysis Clinic, Inc. Kidney Int 1998;54:561-9.
-
84Hirakata H, Nitta K, Inaba M, Shoji T, Fujii H, Kobayashi S, et al.; Japanese Society for Dialysis Therapy. Japanese Society for Dialysis Therapy guidelines for management of cardiovascular diseases in patients on chronic hemodialysis. Ther Apher Dial 2012;16:387-435.
-
85Mc Causland FR, Waikar SS, Brunelli SM. Increased dietary sodium is independently associated with greater mortality among prevalent hemodialysis patients. Kidney Int 2012;82:204-11.
-
86Chen W, Cheng LT, Wang T. Salt and fluid intake in the development of hypertension in peritoneal dialysis patients. Ren Fail 2007;29:427-32.
-
87Wang AY, Brimble KS, Brunier G, Holt SG, Jha V, Johnson DW, et al. ISPD Cardiovascular and Metabolic Guidelines in Adult Peritoneal Dialysis Patients Part I - Assessment and Management of Various Cardiovascular Risk Factors. Perit Dial Int 2015;35:379-87.
-
88Chazot C, Charra B, Vo Van C, Jean G, Vanel T, Calemard E, et al. The Janus-faced aspect of 'dry weight'. Nephrol Dial Transplant 1999;14:121-4.
-
89Davies SJ, Davenport A. The role of bioimpedance and biomarkers in helping to aid clinical decision-making of volume assessments in dialysis patients. Kidney Int 2014;86:489-96.
-
90Wizemann V, Schilling M. Dilemma of assessing volume state--the use and the limitations of a clinical score. Nephrol Dial Transplant 1995;10:2114-7.
-
91Zhu F, Kuhlmann MK, Kotanko P, Seibert E, Leonard EF, Levin NW. A method for the estimation of hydration state during hemodialysis using a calf bioimpedance technique. Physiol Meas 2008;29:S503-16.
-
92Wizemann V, Wabel P, Chamney P, Zaluska W, Moissl U, Rode C, et al. The mortality risk of overhydration in haemodialysis patients. Nephrol Dial Transplant 2009;24:1574-9.
-
93Moissl U, Arias-Guillén M, Wabel P, Fontseré N, Carrera M, Campistol JM, et al. Bioimpedance-guided fluid management in hemodialysis patients. Clin J Am Soc Nephrol 2013;8:1575-82.
-
94Brennan JM, Ronan A, Goonewardena S, Blair JE, Hammes M, Shah D, et al. Handcarried ultrasound measurement of the inferior vena cava for assessment of intravascular volume status in the outpatient hemodialysis clinic. Clin J Am Soc Nephrol 2006;1:749-53.
-
95Zoccali C, Torino C, Tripepi R, Tripepi G, D'Arrigo G, Postorino M, et al.; Lung US in CKD Working Group. Pulmonary congestion predicts cardiac events and mortality in ESRD. J Am Soc Nephrol 2013;24:639-46.
-
96Kayikcioglu M, Tumuklu M, Ozkahya M, Ozdogan O, Asci G, Duman S, et al. The benefit of salt restriction in the treatment of end-stage renal disease by haemodialysis. Nephrol Dial Transplant 2009;24:956-62.
-
97Okada K, Abe M, Hagi C, Maruyama T, Maruyama N, Ito K, et al. Prolonged protective effect of short daily hemodialysis against dialysis-induced hypotension. Kidney Blood Press Res 2005;28:68-76.
-
98Ayus JC, Mizani MR, Achinger SG, Thadhani R, Go AS, Lee S. Effects of short daily versus conventional hemodialysis on left ventricular hypertrophy and inflammatory markers: a prospective, controlled study. J Am Soc Nephrol 2005;16:2778-88.
-
99Chan C, Floras JS, Miller JA, Pierratos A. Improvement in ejection fraction by nocturnal haemodialysis in end-stage renal failure patients with coexisting heart failure. Nephrol Dial Transplant 2002;17:1518-21.
-
100Zimmerman DL, Ruzicka M, Hebert P, Fergusson D, Touyz RM, Burns KD. Short daily versus conventional hemodialysis for hypertensive patients: a randomized cross-over study. PLoS One 2014;9:e97135.
-
101Tattersall J, Martin-Malo A, Pedrini L, Basci A, Canaud B, Fouque D, et al. EBPG guideline on dialysis strategies. Nephrol Dial Transplant 2007;22:ii5-21.
-
102Jaber BL, Lee Y, Collins AJ, Hull AR, Kraus MA, McCarthy J, et al. Effect of daily hemodialysis on depressive symptoms and postdialysis recovery time: interim report from the FREEDOM (Following Rehabilitation, Economics and Everyday-Dialysis Outcome Measurements) Study. Am J Kidney Dis 2010;56:531-9.
-
103Kotanko P, Garg AX, Depner T, Pierratos A, Chan CT, Levin NW, et al.; FHN Trial Group. Effects of frequent hemodialysis on blood pressure: Results from the randomized frequent hemodialysis network trials. Hemodial Int 2015;19:386-401.
-
104Sulowicz W, Radziszewski A. Dialysis induced hypotension--a serious clinical problem in renal replacement therapy. Med Pregl 2007;60:14-20.
-
105Chrysant SG, Chrysant GS. The pleiotropic effects of angiotensin receptor blockers. J Clin Hypertens (Greenwich) 2006;8:261-8.
-
106Furgeson SB, Chonchol M. Beta-blockade in chronic dialysis patients. Semin Dial 2008;21:43-8.
-
107Gadallah MF, el-Shahawy M, Andrews G, Ibrahim M, Ramdeen G, Hanna D, et al. Factors modulating cytosolic calcium. Role in lipid metabolism and cardiovascular morbidity and mortality in peritoneal dialysis patients. Adv Perit Dial 2001;17:29-36.
-
108Agarwal R, Sinha AD. Cardiovascular protection with antihypertensive drugs in dialysis patients: systematic review and meta-analysis. Hypertension 2009;53:860-6.
-
109Heerspink HJ, Ninomiya T, Zoungas S, de Zeeuw D, Grobbee DE, Jardine MJ, et al. Effect of lowering blood pressure on cardiovascular events and mortality in patients on dialysis: a systematic review and meta-analysis of randomised controlled trials. Lancet 2009;373:1009-15.
-
110Ito Y, Mizuno M, Suzuki Y, Tamai H, Hiramatsu T, Ohashi H, et al.; Nagoya Spiro Study Group. Long-term effects of spironolactone in peritoneal dialysis patients. J Am Soc Nephrol 2014;25:1094-102.
-
111Li PK, Chow KM, Wong TY, Leung CB, Szeto CC. Effects of an angiotensin-converting enzyme inhibitor on residual renal function in patients receiving peritoneal dialysis. A randomized, controlled study. Ann Intern Med 2003;139:105-12.
-
112Suzuki H, Kanno Y, Sugahara S, Okada H, Nakamoto H. Effects of an angiotensin II receptor blocker, valsartan, on residual renal function in patients on CAPD. Am J Kidney Dis 2004;43:1056-64.
-
113Suzuki H, Kanno Y, Sugahara S, Ikeda N, Shoda J, Takenaka T, et al. Effect of angiotensin receptor blockers on cardiovascular events in patients undergoing hemodialysis: an open-label randomized controlled trial. Am J Kidney Dis 2008;52:501-6.
-
114Cice G, Ferrara L, D'Andrea A, D'Isa S, Di Benedetto A, Cittadini A, et al. Carvedilol increases two-year survivalin dialysis patients with dilated cardiomyopathy: a prospective, placebo-controlled trial. J Am Coll Cardiol 2003;41:1438-44.
-
115Matsumoto N, Ishimitsu T, Okamura A, Seta H, Takahashi M, Matsuoka H. Effects of imidapril on left ventricular mass in chronic hemodialysis patients. Hypertens Res 2006;29:253-60.
-
116Takahashi A, Takase H, Toriyama T, Sugiura T, Kurita Y, Ueda R, et al. Candesartan, an angiotensin II type-1 receptor blocker, reduces cardiovascular events in patients on chronic haemodialysis--a randomized study. Nephrol Dial Transplant 2006;21:2507-12.
-
117Bakris GL, Hart P, Ritz E. Beta blockers in the management of chronic kidney disease. Kidney Int 2006;70:1905-13.
-
118Badve SV, Roberts MA, Hawley CM, Cass A, Garg AX, Krum H, et al. Effects of beta-adrenergic antagonists in patients with chronic kidney disease: a systematic review and meta-analysis. J Am Coll Cardiol 2011;58:1152-61.
-
119Nakao K, Makino H, Morita S, Takahashi Y, Akizawa T, Saito A, et al.; J-DOPPS Investigators Group. Beta-blocker prescription and outcomes in hemodialysis patients from the Japan Dialysis Outcomes and Practice Patterns Study. Nephron Clin Pract 2009;113:c132-9.
-
120Gervasini G, Robles NR. Potential beneficial effects of sacubitril-valsartan in renal disease: a new field for a new drug. Expert Opin Investig Drugs 2017;26:651-9.
-
121Weir MA, Dixon SN, Fleet JL, Roberts MA, Hackam DG, Oliver MJ, et al. ß-Blocker dialyzability and mortality in older patients receiving hemodialysis. J Am Soc Nephrol 2015;26:987-96.
-
122Agarwal R, Lewis R, Davis JL, Becker B. Lisinopril therapy for hemodialysis hypertension: hemodynamic and endocrine responses. Am J Kidney Dis 2001;38:1245-50.
Datas de Publicação
-
Publicação nesta coleção
08 Nov 2018 -
Data do Fascículo
Jul-Sep 2019
Histórico
-
Recebido
16 Jul 2018 -
Aceito
05 Set 2018