Resumos
Phenakospermum guyannense é popularmente conhecida na Amazônia como sororoca, geralmente encontrada próxima a cursos d´água, em ambientes ombrófilos. Objetivou-se com este estudo descrever a morfoanatomia e histoquímica da semente madura de P. guyannense, como contribuição a estudos taxonômicos, fisiológicos e ecológicos. Sementes maduras foram coletadas nas margens da Cachoeira do Urubuí, no Município de Presidente Figueiredo, Amazonas. O estudo anatômico foi realizado conforme técnicas usuais para análise em microscopia óptica e eletrônica de varredura. Foram aplicados testes histoquímicos para a detecção de compostos fenólicos, amido, proteína e lipídios. A semente madura de P. guyannense é estenospérmica, com envoltório de cor negra, formado por vários estratos de diferentes tipos celulares, sendo a maioria impregnada de compostos fenólicos. O hilo é punctiforme, circundado por células que constituem o arilo. O endosperma é sólido, constituído por células tetraédricas de conteúdo amiláceo e proteico. O embrião é basal capitado, apresentando células de conteúdo lipídico e proteico, composto por eixo hipocótilo-radícula levemente dilatado de forma cilíndrica e localiza-se na região proximal. O haustório apresenta formato aplanado e situa-se na região distal.
anatomia vegetal; sementes florestais; Zingiberales
Phenakospermum guyannense, popularly known in the Amazon as sororoca, is usually found along rivers and in ombrophilous environments. The objective of this study was to describe the morpho-anatomy and histochemistry of mature seeds of P. guyannense collected at the Urubuí Waterfall, Presidente Figueiredo, Amazonas state, Brazil. Seed anatomy was studied using a light and a scanning electron microscopes (SEM). Histochemical tests were performed to identify phenolic compounds, starch, protein and lipids. The mature seed of P. guyannense is stenospermic, with a black seed coat composed of several layers of different cell types, with most containing phenolic compounds. The hilum is punctiform, surrounded by cells, which form the aryl. The endosperm is solid, formed by tetrahedral cells containing starch and protein. The embryo, which is cylindrical and located in the proximal region, is basal capitate, with cells containing lipids and proteins and is composed of a slightly dilated hypocotyl-radicle axis. The haustorium is flattened and located in the distal region.
plant anatomy; forest seeds; Zingiberales
Morfoanatomia e histoquímica da semente de sororoca (Phenakospermum guyannense (Rich.) Endl. - Strelitziaceae)
Morpho-anatomy and histochemistry of the seed of sororoca (Phenakospermum Guyannense Rich.) Endl. - Strelitziaceae)
Andréia Barroncas de OliveiraI,* * Autor para correspondência < andreiabo@hotmail.com> ; Mariana Franco CassinoI; Ely Simone Cajueiro GurgelII; Maria Anália Duarte de SouzaI; Sandra Maria Carmello-GuerreiroIII; Renata Maria Strozi Alves MeiraIV; Maria Silvia de MendonçaV
IInstituto Nacional de Pesquisas da Amazônia (INPA), Universidade Federal do Amazonas (UFAM), 69045-070 - Manaus, AM, Brasil
IIMuseu Paraense Emílio Goeldi, Ministério da Ciência e Tecnologia, Caixa Postal 399, 66040-170 - Belém, PA, Brasil
IIIDepartamento de Biologia Vegetal, Universidade Estadual de Campinas (UNICAMP), Caixa Postal 6109, 13083-970 - Campinas, SP, Brasil
IVDepartamento de Biologia Vegetal, Universidade Federal de Viçosa (UFV), 36570-000 - Viçosa, MG, Brasil
VUniversidade Federal do Amazonas (UFAM), 69077-000 - Manaus, AM, Brasil
RESUMO
Phenakospermum guyannense é popularmente conhecida na Amazônia como sororoca, geralmente encontrada próxima a cursos d´água, em ambientes ombrófilos. Objetivou-se com este estudo descrever a morfoanatomia e histoquímica da semente madura de P. guyannense, como contribuição a estudos taxonômicos, fisiológicos e ecológicos. Sementes maduras foram coletadas nas margens da Cachoeira do Urubuí, no Município de Presidente Figueiredo, Amazonas. O estudo anatômico foi realizado conforme técnicas usuais para análise em microscopia óptica e eletrônica de varredura. Foram aplicados testes histoquímicos para a detecção de compostos fenólicos, amido, proteína e lipídios. A semente madura de P. guyannense é estenospérmica, com envoltório de cor negra, formado por vários estratos de diferentes tipos celulares, sendo a maioria impregnada de compostos fenólicos. O hilo é punctiforme, circundado por células que constituem o arilo. O endosperma é sólido, constituído por células tetraédricas de conteúdo amiláceo e proteico. O embrião é basal capitado, apresentando células de conteúdo lipídico e proteico, composto por eixo hipocótilo-radícula levemente dilatado de forma cilíndrica e localiza-se na região proximal. O haustório apresenta formato aplanado e situa-se na região distal.
Termos para indexação: anatomia vegetal, sementes florestais, Zingiberales.
ABSTRACT
Phenakospermum guyannense, popularly known in the Amazon as sororoca, is usually found along rivers and in ombrophilous environments. The objective of this study was to describe the morpho-anatomy and histochemistry of mature seeds of P. guyannense collected at the Urubuí Waterfall, Presidente Figueiredo, Amazonas state, Brazil. Seed anatomy was studied using a light and a scanning electron microscopes (SEM). Histochemical tests were performed to identify phenolic compounds, starch, protein and lipids. The mature seed of P. guyannense is stenospermic, with a black seed coat composed of several layers of different cell types, with most containing phenolic compounds. The hilum is punctiform, surrounded by cells, which form the aryl. The endosperm is solid, formed by tetrahedral cells containing starch and protein. The embryo, which is cylindrical and located in the proximal region, is basal capitate, with cells containing lipids and proteins and is composed of a slightly dilated hypocotyl-radicle axis. The haustorium is flattened and located in the distal region.
Index terms: plant anatomy, forest seeds, Zingiberales.
Introdução
As monocotiledôneas compõem um grupo monofilético, cuja característica-chave é o cotilédone único, que pode ou não estar bem desenvolvido na semente madura (Judd et al., 2002). Dentro desse grupo, a ordem Zingiberales apresenta-se como um clado naturalmente delimitado (Tomlinson, 1962; Cronquist, 1981; Dahlgren et al., 1985; Judd et al., 2002), que inclui 89 gêneros e cerca de 1.800 espécies, ocorrentes predominantemente nos trópicos. A família Strelitziaceae compreende três gêneros: Strelitzia (5 espécies), Ravenala (1 espécie) e Phenakospermum (1 espécie), restritos, respectivamente, ao sul da África, Madagascar e América tropical (Heywood, 1993).
Phenakospermum guyannense (Rich.) Endl., conhecida popularmente como sororoca na região amazônica, ocorre em ambientes ombrófilos, em florestas inundáveis, ao longo dos rios e igapós, florestas de terra firme, savanas amazônicas e campinas de areia branca (Black et al., 1950 apud Schnell, 1987). A espécie possui caule do tipo rizoma, e apresenta pseudocaule, folhas largas e uma grande inflorescência terminal (Dahlgren et al., 1985). Apresenta potencial ornamental, apesar de ser ainda pouco usada na composição de jardins. Na região amazônica, a semente tostada é utilizada para fins alimentares, e as folhas são usadas para cobrir taperas e envolver peixes durante o cozimento sobre brasas.
Encontraram-se poucos registros sobre a anatomia de sementes de espécies da ordem Zingiberales, dentre os quais se destacam os trabalhos de Grootjen e Bouman (1981), Graven et al. (1996) e Liao e Wu (2000). Da mesma forma, estudos sobre aspectos histoquímicos das sementes de monocotiledôneas também são poucos e enfocam geralmente os componentes de reserva das sementes (cf. DeMason, 1986; DeMason, 1988; Panza et al., 2004, Panza et al., 2009). Assim, este estudo teve por objetivo realizar a caracterização morfoanatômica e histoquímica da semente de sororoca (Phenakospermum guyannense (Rich.) Endl., a fim de contribuir para o conhecimento das monocotiledôneas amazônicas, fornecendo subsídios para estudos voltados à taxonomia, fisiologia e ecologia da espécie, que poderão contribuir com programas de conservação e manutenção dos recursos genéticos da Amazônia.
Material e Métodos
Sementes maduras de Phenakospermum guyannense foram coletadas de plantas ocorrentes nas margens da Cachoeira do Urubuí, no Município de Presidente Figueiredo (2º14'26"S; 60º01'44''W), no estado do Amazonas, Brasil. As análises experimentais foram realizadas na Universidade Federal do Amazonas, em Manaus (AM) e no Museu Paraense Emílio Goeldi, em Belém (PA), Brasil.
Para a caracterização morfológica, foram utilizadas 100 sementes, retiradas de três indivíduos, das quais foram descritos o formato da semente, a coloração e a textura do tegumento. As sementes tiveram o seu comprimento e diâmetro medidos com auxílio de um paquímetro digital. Foi aferido o peso da matéria fresca e seca em balança eletrônica. Para obtenção da matéria seca, as sementes foram colocadas em estufa regulada a 105 ºC até obtenção de peso constante. O grau de umidade das sementes foi obtido pela equação: P1 - P2/P1*(100) = U, onde: P1 (peso da matéria fresca); P2 (peso da matéria seca); U (umidade), de acordo com Lara et al. (1976). Dez sementes foram abertas para descrição da morfologia interna e para retirada dos embriões, os quais foram avaliados quanto à forma, coloração e posição.
Para o estudo anatômico, amostras de sementes e embriões foram fixadas em FAA (formol, ácido acético glacial e etanol 50, 1:1:18, v/v) por 48h (Kraus e Arduin, 1997), posteriormente desidratadas em série etílica, incluídas em 2-hidroxietil-metacrilato (Historesin® Leica) e seccionadas em micrótomo rotativo. Para a caracterização estrutural, os cortes foram corados com azul de toluidina pH 4,4 (O'Brien e McCully, 1981) e as lâminas foram montadas com resina sintética (Permount, Fisher).
Testes histoquímicos foram aplicados em cortes transversais e longitudinais obtidos em micrótomo de mesa de amostras frescas da semente e do embrião, os quais foram submetidos aos seguintes reagentes: dicromato de potássio para detecção de compostos fenólicos (Gabe, 1968); floroglucina para detecção de lignina (Johansen, 1940); sudan III e sudan black B para detecção de lipídios (Pearse, 1980); vermelho de rutênio para caracterização de pectinas e mucilagens (Johansen, 1940). Foram montadas lâminas temporárias em glicerina + água (1:1). Cortes de amostras incluídas em metacrilato foram submetidos ao reagente xilidine Ponceau para detecção de proteínas (O'Brien e McCully, 1981). Cortes histológicos de material fresco e de amostras incluídas em metacrilato foram submetidos ao azul de toluidina pH 4,4, contra-corados com Lugol para detecção de amido (Jensen, 1962, com modificações; O'Brien e McCully, 1981).
O material histológico estudado foi fotografado em estereoscópio ZEISS acoplado a câmera MC-80 DX e câmera digital Power Shot A-620 CANON.
Para caracterização micromorfológica, amostras de 0,25 cm2 foram fixadas em FAA por 48 horas e estocadas em etanol 70%. As amostras foram desidratadas em série etílica e levadas à secagem em ponto crítico de CO2, utilizando equipamento modelo CPD 020, Bal-Tec, Balzers, Liechtenstein (Bozzola e Russel, 1992). Após a fixação das amostras nos suportes com fita dupla-face, foi realizada deposição metálica com ouro (equipamento Sputter Coater, modelo FDU 010, Bal-Tec, Balzers, Liechtenstein). A observação e a captura de imagens foram realizadas em microscópio eletrônico de varredura (modelo Zeiss, LEO 1430 VP, Cambridge, Inglaterra) do Museu Paraense Emílio Goeldi.
Resultados e Discussão
A semente de Phenakospermum guyannense é arilada, estenospérmica, pois apresenta pouca variabilidade de forma entre as sementes. Possui formato ovalado com ápice arredondado e mais largo que a base (Figura 1.A; 1.B), apresentando peso médio de 0,31 g. As sementes sem o arilo medem em média 9,74 mm de comprimento, 6,42 mm de largura, 5,86 mm de espessura e apresentam 0,25 g de matéria fresca e 0,22 g de matéria seca, o que representa um teor de água de 12%.
A semente é monocrômica, negra, pétrea quando desidratada, apresenta superfície rugosa e, quando vista sob estereomicroscópio, observam-se estrias longitudinais (Figura 1.A). A micrópila e a rafe são imperceptíveis a vista desarmada.
A região hilar da semente de Phenakospermum guyannense é basal, afunilada e rugosa; o hilo é punctiforme (Figura 1.B; 1.C). Circundando o hilo, é encontrado um arilo seco e oleoso, formado por células de paredes celulósicas espessadas (Figura 2.A), com conteúdo lipídico e proteico (Figura 2.B; 2.C; Tabela 1), de cor alaranjada (Figura 1.A), facilmente removível na semente embebida.
O arilo de P. guyannense pode estar relacionado à dispersão das sementes por aves, uma vez que, segundo Pijl (1982), a cor alaranjada corresponde à síndrome da ornitocoria. Ademais, de acordo com Stiles (1993), sementes ariladas estão entre as mais nutritivas devido ao alto teor de lipídios geralmente encontrado neste acessório, o que é condizente com a alta demanda energética das aves.
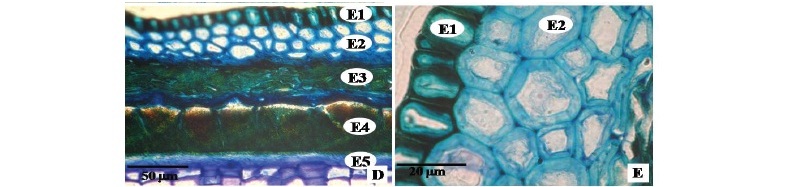
O envoltório da semente madura pode ser dividido em vários estratos. O primeiro estrato (E1) é formado pela camada mais externa, uniestratificada, composta por células tetraédricas (Figura 1.D), de paredes espessadas (Figura 2.D; 2.E), impregnadas de compostos fenólicos (Figura 2.F; Tabela 1). Internamente a esta camada celular, o segundo estrato (E2) é constituído de várias camadas de células parenquimáticas, volumosas, de paredes celulósicas, espessadas (Figura 2.D; 2.E; 2.F), não lignificadas, onde se observam com nitidez as lamelas medianas e os campos de pontoações primárias em seção longitudinal. O número de camadas de células deste estrato varia de acordo com a região da semente, podendo chegar a dezenas nas regiões apicais (sub-hilar e micropilar) e a uma única camada na região equatorial da semente. Internamente a esse estrato, ocorrem camadas de células parenquimáticas colapsadas (Figura 2.D) com conteúdo fenólico (Figura 2.F; 2.G; Tabela 1), formando o terceiro estrato (E3). A distribuição das células neste estrato segue a mesma das células do estrato E2, constituída por numerosas camadas nas regiões apicais da semente e camadas escassas na região equatorial. O quarto estrato (E4) é formado por células cuboides, muito volumosas (Figura 2.D; 2.H), com conteúdo fenólico (Tabela 1) e paredes anticlinais e periclinais internas espessadas, caracterizando um típico espessamento em U (Figura 2.D). Adjacente a este estrato, ocorre o estrato mais interno (E5), com células colapsadas em contato com o endosperma (Figura 2.D; 2.H) e recobertas por uma cutícula voltada para o estrato E4 (Figura 2.H).
Segundo Liao e Wu (2000), as sementes de Zingiberales se apresentam geralmente, adjacente ao envoltório, um perisperma, originado a partir do tecido nucelar, e uma região micropilar incluindo um colar micropilar (região diferenciada na região da micrópila). De acordo com Graven et al. (1996), o perisperma em Musaceae é composto por camadas de células completamente comprimidas das quais apenas as paredes celulares permanecem, de forma muito semelhante à camada de células colapsadas encontradas no estrato mais interno do envoltório (E5) da semente de P. guyannense. Graven et al. (1996) também encontraram um colar micropilar bem definido nas sementes de Musaceae. Nas sementes de P. guyannense, não foi encontrada tal estrutura, o que corrobora a observação de Grootjen e Bouman (1981) e Takhtajan (1985), segundo os quais esta é ausente nas famílias basais de Zingiberales, como Strelitziaceae e Heliconiaceae. Liao e Wu (2000) sugeriram que essa ausência pode ser um caráter primitivo na ordem, mas este aspecto requer investigações complementares.
A cutícula encontrada na região mais interna do envoltório da semente de P. guyannense também foi descrita por Graven et al. (1996) para sementes de Musaceae. Segundo esses autores, tal estrutura pode funcionar como a última barreira à difusão de água em combinação com as camadas mais externas. Além da cutícula presente na camada interna do envoltório da semente de P. guyannense (estrato E5), a grande quantidade de compostos fenólicos nas diversas camadas do envoltório também contribui potencialmente para a impermeabilidade da semente à água. De fato, Graven et al. (1996) discutem que as células justapostas de paredes espessas presentes nos envoltórios de sementes de Musaceae devem provavelmente sua impermeabilidade à água à presença de substâncias hidrofóbicas, como os compostos fenólicos depositados em redes poliméricas nas paredes celulares. Ceballos et al. (1998) enfatizam a importância dos fenólicos presentes no envoltório de sementes na proteção contra patógenos do embrião dormente e da radícula, na imposição de dormência mecânica e na liberação de aleloquímicos durante a embebição. Diante disso, alguns autores, como Kuiters (1990) indicam que os compostos fenólicos são capazes de afetar a taxa de germinação. No entanto, segundo Graven et al. (1996), no envoltório de sementes de Musa, tais compostos parecem ser componentes estruturais genuínos das paredes celulares, não afetando a germinação.
Graven et al. (1996), ao estudarem sementes da família Musaceae, discutem a demanda conflitante entre proteção e germinação, enfatizando que os envoltórios oferecem eficiente proteção durante a maturação, dispersão e dormência. No entanto, dificultam a germinação, já que o embrião necessita romper o envoltório da semente.
O endosperma é sólido, homogêneo, esbranquiçado, ocupando grande proporção da semente (Figura 1.B). A camada mais externa do endosperma é formada por um único estrato de células, que se diferem das demais por serem tetraédricas alongadas e apresentarem conteúdo lipídico (Figura 2.H; Tabela 1). Estas células, uma vez que contêm lipídeos, funcionalmente podem estar atuando como uma barreira hidrofóbica, da mesma maneira que as camadas celulares que compõem o envoltório da semente. Neste caso, a presença de lipídeos provavelmente não está relacionada à reserva de nutrientes.
As demais camadas do endosperma são compostas por células isodiamétricas (Figura 3.A), volumosas, de paredes finas, contendo amido (Fig 3.C; Tabela 1), que ocupa a quase totalidade do citoplasma, e proteína (Figura 3.B; Tabela 1), que ocupa a periferia celular. Dentre estas camadas, as mais externas possuem maior quantidade de conteúdo proteico (Figura 3.A) que, neste caso, pode ocupar grande proporção do lúmen celular.
Em outras famílias de monocotiledôneas, especificamente Arecaceae, a reserva de carboidratos do endosperma encontra-se na forma de paredes celulares espessadas (Panza et al., 2009). Tais dados contrastam com o encontrado em P. guyannense, uma vez que o endosperma desta apresenta células com paredes finas e grande quantidade de amido.
O embrião de P. guyannense é basal capitado (Martin, 1946), crasso, encaixado no endosperma (Figura 1.B). O eixo embrionário é levemente dilatado, apresenta forma cilíndrica e localiza-se na região proximal (em relação ao funículo) (Figura 3.D). A região distal do cotilédone tem formato aplanado (Figura 3.G). Durante a germinação, tal região se desenvolverá em um haustório, funcionando como uma estrutura de sucção que fornece metabólitos necessários ao processo germinativo e crescimento inicial da plântula (Sugimura e Murakami, 1990).
O embrião é revestido por uma protoderme uniestratificada formada por células de formato quadrado a retangular, com citoplasma denso, núcleo evidente (Figura 3.D; 3.F), conteúdo lipídico e proteico (Figura 3.H; 3.I; Tabela 1).
A plúmula é distinta e os primórdios foliares são delimitados por uma protoderme, onde ocorrem células indiferenciadas em intensa atividade meristemática (Figura 3.D; 3.E) organizadas no interior da cavidade cotiledonar (Figura 3.E). Opostamente à plúmula, localiza-se o pólo radicular. O procâmbio está organizado em nove cordões, que percorrem longitudinalmente o limbo cotiledonar (Figura 3.F; 3.G), composto, na sua maioria, por parênquima, com células volumosas de conteúdo lipídico e proteico (Figura 3.H; 3.I; Tabela 1) e ausência de amido (Tabela 1). A presença de lipídeos e proteínas como compostos de reserva no embrião de monocotiledôneas já foi registrada em palmeiras por Demason (1988), Panza et al. (2004) e Panza et al. (2009). Já o amido pode estar presente ou não nesta estrutura, tendo sido registrada a sua ocorrência no embrião de Euterpe edulis Mart. por Panza et al. (2004) e a sua ausência em Washingtonia filifera (Linden ex André) H. Wendl. ex de Bary por Demason (1988).
O formato do embrião, sua localização e as características do eixo hipocótilo-radícula da semente de P. guyannense são típicos das monocotiledôneas (Demason e Thomson, 1981; Demason, 1988; Mendonça et al., 2008; Oliveira et al., 2010).
A grande quantidade de amido no endosperma, de lipídio no embrião e de proteína em ambas as estruturas constitui a fonte de reserva nutricional para o embrião em desenvolvimento. Estudos em sementes de monocotiledôneas indicam que embora tanto o embrião quanto o endosperma apresentem compostos de reserva, a proporção destes compostos no endosperma é bem maior. Em Washingtonia filifera, por exemplo, o endosperma é formado por 93% de compostos de reserva enquanto o cotilédone, por apenas 41% (Demason, 1988). Tais dados indicam que provavelmente, em P. guyannense, o endosperma também se apresenta como a principal estrutura de armazenamento de nutrientes. Além disso, o fato do endosperma da semente estudada ser bem mais volumoso que o embrião corrobora esta proposição.
Segundo Marcos Filho (2005), as sementes com grande quantidade de amido, como registrado na espécie estudada, possuem alto potencial de armazenamento. Entretanto, a presença abundante de proteínas e a ocorrência de lipídeos no embrião de P. guyannense podem contribuir para a redução do potencial do tempo de armazenamento, devido à menor estabilidade química dos lipídios em relação ao amido e à elevada afinidade das proteínas com a água.
Conclusões
Os caracteres morfoanatômicos descritos neste trabalho apresentam informações relevantes para a taxonomia e fisiologia da espécie estudada. A presença de amido e proteína no endosperma, e lipídio e proteína no embrião constituem as reservas nutritivas da semente de sororoca. Os compostos fenólicos presentes no revestimento da semente, assim como os lipídeos presentes tanto no envoltório da semente quanto na camada externa do endosperma possivelmente atuam como barreiras à passagem de água, suprindo as necessidades eco-fisiológicas da planta. Recomenda-se a realização de investigações ontogenéticas para melhor compreensão da origem de cada estrato que compõe o envoltório da semente, e de estudos fisiológicos, a fim de verificar a relação entre estrutura e função.
Agradecimentos
À Universidade Federal do Amazonas (UFAM), em especial ao Laboratório de Botânica Agroflorestal (LABAF) e ao Museu Paraense Emílio Goeldi (MPEG), pelo apoio logístico. À Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (CAPES), através do Programa Nacional de Cooperação Acadêmica (PROCAD UFAM/UFV).
Submetido em 08/02/2011.
Aceito para publicação em 27/09/2011.
- BOZZOLA, J.J.; RUSSEL, L.D . Electron microscopy Boston: Jones and Bartlett Publishers, 1992. 542p.
- CEBALLOS, L.; MCKEY, M.H.; MCKEY, D.; ANDARY, C. Rapid deployment of allelochemicals in exudates of germinating seeds of Sesbania (Fabaceae): roles of seed anatomy and histolocalization of polyphenolic compounds in anti-pathogen defense of seedlings. Chemoecology, v.8, p.141-151, 1998.
- CRONQUIST, A.J. An integrated system of classification of flowering plants New York: Columbia University Press, 1981. 1262p.
- DAHLGREN, R.M.T.; CLIFFORD, H.T.; YEO, P.F. The families of the monocotyledons Berlin: Springer-Verlag, 1985. 520p.
- DEMASON, D.; THOMSON, W.W. Structure and ultrastructure of the cotyledon of date palm (Phoenix dactylifera L.). Botanical Gazette, v.142, n.3, p.320-328, 1981.
- DEMASON, D. Endosperm structure and storage reserve histochemistry in the palm Washingtonia filifera. American Journal of Botany, v.73, p.1332-1340, 1986. http://www.jstor.org/discover/10.2307/2444067?uid=3737664&uid=2129&uid=2&uid=70&uid=4&sid=21100675622001
- DEMASON, D. Embryo structure and storage reserve histochemistry in the palm Washingtonia filifera. American Journal of Botany, v.75, p.330-337, 1988. http://www.jstor.org/discover/10.2307/2443980?uid=3737664&uid=2129&uid=2&uid=70&uid=4&sid=21100675622001
- GABE, M. Techniques histologiques. Paris: Masson & Cie, 1968. 1113p.
- GRAVEN, P.; KOSTER, C.G.; BOON, J.J.; BOUMAN, F. Structure and macromolecular composition of the seed coat of the Musaceae. Annals of Botany, v.77, p.105-122, 1996.
- GROOTJEN, C.J.; BOUMAN,F. Seed structure in Cannaceae: taxonomic and ecological implications. Annals of Botany, v.61, p.363-371, 1981.
- HEYWOOD, V.H. Flowering plants of the world London: BT Batsford Ltd, 1993. 335p.
- JENSEN, W.A. Botanical histochemistry: Principles and Practice. San Francisco: W.H. Freeman & Co., 1962. 408p.
- JOHANSEN, D.A. Plant microtechnique New York: McGraw-Hill, 1940. 523p.
- JUDD, W.S.; CAMPBELL, C.S.; KELLOGG, E.A.; STEVENS, P.F.; DONOGHUE M.J. Plant systematics: a phylogenetic approach. 2.ed. Sunderland: Sinauer Associates, 2002. 576p.
- KRAUS, J.E.; Arduin, M. Manual básico de métodos em morfologia vegetal. Rio de Janeiro: EDUR, 1997. 198p.
- KUITERS, A.T. Role of the phenolic substances from decomposing forest litter in plant soil interactions. Acta Botanica Neerlandica, v.39, p.329-348, 1990.
- LARA, A.B.W.H.; NAZÁRIO, G.; ALMEIDA, M.E.W.; PREGNOLATO, W. Normas analíticas do Instituto Adolfo Lutz. Métodos químicos e físicos para análise de alimentos. v.1. 2.ed. São Paulo: Instituto Adolfo Lutz, 1976. 371p.
- LIAO, J.P.; WU, Q. A preliminary study of the seed anatomy of Zingiberaceae. Botanical Journal of Linnean Society, v.134, p.287-300, 2000.
- MARCOS-FILHO, J. Fisiologia de sementes de plantas cultivadas Piracicaba: Fealq, 2005. 495p.
- MARTIN, A.C. The comparative internal mophology of seeds The American Midland Naturalist, Indiana, v.36, n.3, p.513-660, 1946.
- MENDONÇA, M.S.; OLIVEIRA, A.B.; ARAÚJO, M.G.P.; ARAÚJO, L.M. Morfo-anatomia do fruto e da semente de Oenocarpus minor Mart. (Arecaceae). Revista Brasileira de Sementes, v.30, n.1, p.90-95, 2008. http://www.scielo.br/pdf/rbs/v30n1/a12v30n1.pdf
- O'BRIEN, T.P.; MCCULLY, M.E. The study of structure principles and selected methods Melbourn: Termarcarphi Pty. LTD, 1981. 280p.
- OLIVEIRA, A.B.; MENDONÇA, M. S.; ARAÚJO, M.G.P. Aspectos anatômicos do embrião e desenvolvimento inicial de Oenocarpus minor Mart.: uma palmeira da Amazônia. Acta Botanica Brasilica, v. 24, p. 20-24, 2010. http://www.scielo.br/pdf/abb/v24n1/03.pdf
- PANZA, V.; LÁINEZ, V.; MALDONADO, S. Seed structure and histochemistry in the palm Euterpe edulis Botanical Journal of the Linnean Society, v. 145, p. 445-453, 2004.
- PANZA, V.; PIGHIN, D.; LÁINEZ, V.; POLLERO, R.J.; MALDONADO, S. Storage lipids and proteins of Euterpe edulis seeds. Biocell, v.33, n.2, p.99-106, 2009. http://www.scielo.org.ar/pdf/biocell/v33n2/v33n2a04.pdf
- PEARSE, A.G.E. Histochemistry theoretical and applied v.2. 4.ed. Baltimore: Longman Group Limited, 1980. 1518p.
- PIJL, L. Principles of dispersal in higher plants. Berlin: Springer-Verlag, 1982. 214p.
- SCHNELL, R. La Forêt et la Végétation de l´Amérique Tropicale. Généralités, les flores, les formations forestières et les formations mésophiles. Tome 1. Paris: Masson, 1987. 480p.
- STILES, E.W. The influence of pulp lipids on preference by birds. Vegetatio, v.107/108, n.1, p.227-235, 1993.
- SUGIMURA, Y.; MURAKAMI, T . Structure and function of the haustorium in germinating coconut palm seed. Japan Agricultural Research Quarterly, v.24, p.1-14, 1990. http://www.jircas.affrc.go.jp/english/publication/jarq/24-1/24-1-001-014.pdf
- TAKHTAJAN, A. Anatomia seminum comparativa. v.1 Liliopsida seu monocotyledones Leninpoli: Nauka, 1985.
- TOMLINSON, P.B. Commelinales-Zingiberales. In: Metcalfe, C.R. (Ed.) Anatomy of the monocotiledons Oxford: Clarendon Press, 1962.
Datas de Publicação
-
Publicação nesta coleção
27 Jun 2012 -
Data do Fascículo
Jun 2012
Histórico
-
Recebido
08 Fev 2011 -
Aceito
27 Set 2011