Resumos
A biologia reprodutiva de Hylocryptus rectirostris (Wied, 1831) é descrita pela primeira vez. As coletas de dados foram realizadas no período de abril de 2004 a novembro de 2005, no Parque Nacional da Serra do Cipó, Minas Gerais. Os indivíduos foram marcados com anilhas coloridas e acompanhados ao longo de duas estações reprodutivas. Ovos, ninhegos e jovens foram descritos. O sucesso reprodutivo foi avaliado em cinco categorias: construção de ninhos, ovos, ninhegos, casais e ninhos. Casos de competição por cavidades e predação também foram registrados. A atividade reprodutiva é altamente sincrônica tanto entre os casais quanto entre as estações. Foram encontrados 20 ninhos, todos construídos em barrancos localizados nas margens de rios. O período de incubação é de 17 dias e o período de ninhego varia entre 21 a 25 dias. O casal se reveza na construção do ninho, incubação e alimentação da prole, sendo que a fêmea apresenta maior desenvolvimento da placa incubatória. A porcentagem de ninhos que produziram um ou mais filhotes foi de 33% (n = 9) na estação de 2004 e 18% (n = 11) na estação de 2005. As causas dos fracassos ocorridos ao longo da atividade reprodutiva foram principalmente destruição do ninho por desabamento ou enchente do rio. Este estudo fornece conhecimentos a respeito da biologia básica de H. rectirostris e pode contribuir para futuras medidas de conservação e manejo desta espécie.
Estação reprodutiva; incubação; ninho; sucesso reprodutivo
Here, we provide the first description of the breeding biology of the Henna-browed Foliage-gleaner, Hylocryptus rectirostris (Wied, 1831). The foliage-gleaner was studied at the Serra do Cipó Nationa Park (Parque Nacional da Serra do Cipó), in the state of Minas Gerais, southeastern Brazil. Birds were marked with color bands and monitored through two reproductive seasons from April 2004 to November 2005. Eggs, nestlings and young are described. Breeding success was calculated for five categories: nest construction, eggs, fledglings, pairs and nests. Nest predation and competition for cavities were also observed. Breeding activity is very synchronous for breeding pairs and in the two reproductive seasons. Twenty nests were found in cavities excavated in steep river banks. Incubation lasts 17 days and nestlings remain in the nest another 21-25 days. Both adults build the nest, incubate the eggs and feed the nestlings, but females develop a larger brood patch. In 2004, nesting success (one or more offspring that fledged) was 33% (n = 9) and in 2005 was 18% (n = 11). Landslides or flooding caused the most nest failures. This study can contribute to future measures for the conservation of this species.
Incubation; nest; reproductive period; reproductive success
BIOLOGY
Biologia reprodutiva do fura-barreira Hylocryptus rectirostris (Aves: Furnariidae)
Breeding biology of the Henna-capped Foliage-gleaner Hylocryptus rectirostris(Aves: Furnariidae)
Luciene C. P. FariaI; Lucas A. CarraraI; Marcos RodriguesII
IAves Gerais Monitoramento Ambiental. Avenida Portugal 2020, 31555-000 Belo Horizonte, Minas Gerais, Brasil. E-mail: avesgerais@avesgerais.com.br
IILaboratório de Ornitologia, Departamento de Zoologia, Universidade Federal de Minas Gerais. Caixa Postal 486, 31270-901 Belo Horizonte, Minas Gerais, Brasil. E-mail: ornito@mono.icb.ufmg.br
RESUMO
A biologia reprodutiva de Hylocryptus rectirostris (Wied, 1831) é descrita pela primeira vez. As coletas de dados foram realizadas no período de abril de 2004 a novembro de 2005, no Parque Nacional da Serra do Cipó, Minas Gerais. Os indivíduos foram marcados com anilhas coloridas e acompanhados ao longo de duas estações reprodutivas. Ovos, ninhegos e jovens foram descritos. O sucesso reprodutivo foi avaliado em cinco categorias: construção de ninhos, ovos, ninhegos, casais e ninhos. Casos de competição por cavidades e predação também foram registrados. A atividade reprodutiva é altamente sincrônica tanto entre os casais quanto entre as estações. Foram encontrados 20 ninhos, todos construídos em barrancos localizados nas margens de rios. O período de incubação é de 17 dias e o período de ninhego varia entre 21 a 25 dias. O casal se reveza na construção do ninho, incubação e alimentação da prole, sendo que a fêmea apresenta maior desenvolvimento da placa incubatória. A porcentagem de ninhos que produziram um ou mais filhotes foi de 33% (n = 9) na estação de 2004 e 18% (n = 11) na estação de 2005. As causas dos fracassos ocorridos ao longo da atividade reprodutiva foram principalmente destruição do ninho por desabamento ou enchente do rio. Este estudo fornece conhecimentos a respeito da biologia básica de H. rectirostris e pode contribuir para futuras medidas de conservação e manejo desta espécie.
Palavras-Chave: Estação reprodutiva; incubação; ninho; sucesso reprodutivo.
ABSTRACT
Here, we provide the first description of the breeding biology of the Henna-browed Foliage-gleaner, Hylocryptus rectirostris (Wied, 1831). The foliage-gleaner was studied at the Serra do Cipó Nationa Park (Parque Nacional da Serra do Cipó), in the state of Minas Gerais, southeastern Brazil. Birds were marked with color bands and monitored through two reproductive seasons from April 2004 to November 2005. Eggs, nestlings and young are described. Breeding success was calculated for five categories: nest construction, eggs, fledglings, pairs and nests. Nest predation and competition for cavities were also observed. Breeding activity is very synchronous for breeding pairs and in the two reproductive seasons. Twenty nests were found in cavities excavated in steep river banks. Incubation lasts 17 days and nestlings remain in the nest another 21-25 days. Both adults build the nest, incubate the eggs and feed the nestlings, but females develop a larger brood patch. In 2004, nesting success (one or more offspring that fledged) was 33% (n = 9) and in 2005 was 18% (n = 11). Landslides or flooding caused the most nest failures. This study can contribute to future measures for the conservation of this species.
Key Words: Incubation; nest; reproductive period; reproductive success.
Furnariidae é composta por 236 espécies exclusivas da Região Neotropical (REMSEN 2003), sendo caracterizada pela diversidade e complexidade de ninhos (NAROSKY et al. 1983, DE LA PEÑA 1987). Os ninhos são, em geral, grandes e conspícuos, justificando a profusão de publicações abordando o tema que contemplam ao menos 170 espécies da família (REMSEN 2003). A arquitetura dos ninhos vem sendo utilizada em classificações taxonômicas e análises filogenéticas dentro da família (VAURIE 1980, ZYSKOWSKI & PRUM 1999), sendo, portanto, uma importante caracterização para o grupo.
Apesar da notabilidade dos ninhos dos furnarídeos, informações detalhadas sobre a biologia reprodutiva são bastante escassas. Dados a respeito do período de incubação são relatados para apenas 20 espécies da família, período de ninhegos para 14 espécies e cuidado parental para 11 espécies de furnarídeos (REMSEN 2003).
Dentre as pouco estudadas espécies de Furnariidae podem ser citadas as duas únicas representantes de Hylocryptus Chapman, 1919: H. erythrocephalus Chapman, 1919 e H. rectirostris (Wied, 1831). A primeira é uma espécie com distribuição restrita e classificada como ameaçada (BIRDLIFE INTERNATIONAL 2000), sendo escassas as informações envolvendo sua biologia reprodutiva (REMSEN 2003). A segunda é uma espécie exclusiva de matas ciliares da região do Cerrado (SILVA 1995, VIELLIARD & SILVA 2001), cuja distribuição inclui a região centro-sul do Brasil, chegando ao extremo leste do Paraguai (RIDGELY & TUDOR 1994, SICK 1997, REMSEN 2003). Apesar da ampla área de ocorrência, a destruição de seu habitat vem acelerando seu declínio populacional em algumas regiões, constando, por exemplo, na lista de espécies ameaçadas do estado de São Paulo (SÃO PAULO 1998). Além de ser considerada rara a incomum, pouco se sabe sobre sua biologia, sendo, portanto, uma espécie prioritária para pesquisa (RIDGELY & TUDOR 1994, STOTZ et al. 1996).
sendo demonstrada a existência de dimorfismo sexual morfométrico (FARIA et al. 2007a), de forte territorialidade e de especificidade alimentar (FARIA et al. 2007b). Através destes estudos, foi possível comprovar a estabilidade dos territórios ao longo de todo ano e sua íntima relação com as matas ciliares. A defesa dos territórios é executada com maior intensidade pelos machos, o que parece explicar a diferença de tamanho de asa e cauda observada entre os sexos, parâmetros intimamente relacionados à capacidade de vôo. Machos solitários mantêm territórios estáveis por longos períodos, mesmo na ausência de fêmeas (veja FARIA et al. 2007a, b para maiores detalhes).
O presente estudo busca incrementar as informações a respeito de H. rectirostris, investigando os aspectos de sua biologia reprodutiva. O esclarecimento destes aspectos poderá contribuir em futuras medidas de conservação e manejo da espécie. O principal objetivo é descrever a biologia reprodutiva do fura-barreira H. rectirostris quanto à descrição de seu ninho, determinação da estação reprodutiva, descrição de ovos, ninhego e jovem e avaliação do sucesso reprodutivo da população estudada.
MATERIAL E MÉTODOS
Área de Estudo
O estudo foi conduzido no Parque Nacional da Serra do Cipó, localizado na porção sul da Cadeia do Espinhaço (19°13S, 43°29W e 19°31S, 43°32W), ao longo da Serra do Cipó, estado de Minas Gerais. O Parque possui uma área total de 33.800 ha e caracteriza-se por apresentar altitudes entre 800 e 1400 m, em uma serra onde na vertente leste destaca-se a vegetação de Mata Atlântica e na oeste, o Cerrado. Possui na sua porção alta, como substrato rochoso mais comum, o quartzito, onde se desenvolve o campo rupestre (RIBEIRO & WALTER 1998). Na sua região de baixada, vertente oeste, o Cerrado está representado por várias fitofisionomias, desde o campo limpo até o cerradão, apresentando também áreas de mata semi-decídua e matas ciliares, todas elas em diversos estágios de conservação (RODRIGUES et al. 2005). O estudo foi conduzido na porção baixa do Parque, nas matas ciliares do vale do rio Cipó, formado por dois principais afluentes, os rios Mascates e Bocaina.
O clima da região é do tipo mesotérmico (Cwb de Köpen) com estações seca e chuvosa bem definidas e precipitação anual em torno de 1400 mm. A temperatura da região tem pouca variação anual e mensal, mas a precipitação mostra-se com larga variação ao longo do ano. De acordo com MADEIRA & FERNANDES (1999), quatro períodos estacionais podem ser definidos: estação seca de maio a setembro; estação chuvosa de novembro a janeiro; estação pós-chuvosa de fevereiro a abril; e estação pósseca em outubro (Fig. 1).
Marcação e monitoramento dos indivíduos
O estudo foi desenvolvido entre abril de 2004 e novembro de 2005, abrangendo duas estações reprodutivas e o período não reprodutivo. Foram capturados e marcados 22 indivíduos adultos e 11 jovens. Na estação reprodutiva de 2004 foram monitorados cinco casais e três adultos solitários, enquanto na estação de 2005 foram acompanhados seis casais e quatro adultos solitários. Destes, três casais e um adulto solitário foram monitorados continuamente nas duas estações.
Os adultos foram capturados por meio de redes de neblina de malha 36 mm, enquanto os ninhegos foram apanhados diretamente dos ninhos. Cada ave capturada foi marcada com uma anilha de alumínio fornecida pelo CEMAVE/IBAMA e duas anilhas coloridas, com combinação de cores única para cada indivíduo, sendo uma delas referente a seu território e a outra individual.
De cada indivíduo capturado foram obtidas medidas morfológicas (peso, asa, cauda, cúlmen e tarso) e foi coletada uma amostra de sangue para sexagem molecular (veja FARIA et al. 2007a para maiores detalhes). A presença de mudas de penas e de placa de incubação foi determinada seguindo o método proposto pelo IBAMA (1994).
Dados foram coletados em visitas alternadas em cada um dos territórios determinados e mensurados por FARIA et al. (2007b). Após a localização e identificação, os indivíduos foram observados durante uma hora. O esforço amostral foi de 137 dias de trabalho em campo e 760 horas ao longo de todo o estudo, sendo 129 horas de observações de comportamento reprodutivo.
Localização e medidas dos ninhos
A partir do acompanhamento dos indivíduos foi possível localizar os ninhos e detectar o início do comportamento reprodutivo. A posição dos ninhos foi registrada a partir de um aparelho equipado com sistema de posicionamento global (GPS, marca Garmin, modelo e-Trex Legend). Foram obtidas as seguintes dimensões dos ninhos encontrados: altura e largura da entrada do túnel, profundidade do túnel, distância da entrada do ninho até o topo e até a base do barranco, distância da entrada do ninho à margem mais próxima do rio e altura da entrada do ninho em relação à lâmina d'água do rio. Todas as medidas foram obtidas em centímetros utilizando-se trena de cinco metros. Foi efetuada a medida da inclinação do túnel em relação à horizontal por meio de transferidor de graus. Utilizou-se um frasco transparente com líquido como referência horizontal, sendo medido, em graus, o menor arco entre a lâmina d'água do recipiente e o prolongamento de uma régua posicionada no túnel do ninho.
Observações e monitoramento dos ninhos
Para o exame interno do ninho foi desenvolvido um aparelho constituído de haste rígida metálica com 60 cm de comprimento, lanterna pequena e estreita (duas pilhas AAA), espelho com dobradiça e cordão. Ao ser introduzido na cavidade, o equipamento iluminava a câmara e refletia a imagem do interior do ninho no espelho. O cordão permitia o movimento do espelho e a localização do centro da tigela. Este aparelho foi indispensável à verificação da presença de ovos e/ou filhotes nos ninhos, permitindo definir os períodos de incubação, ninhego e estação reprodutiva.
Uma vez localizados, os ninhos foram examinados com intervalo máximo de sete dias, sendo a maioria das vistorias diárias ou a cada dois dias. Cada ninho foi observado à distância mínima de 10 m durante uma hora. Ao longo dessas observações foi possível acompanhar adultos em comportamento de construção dos ninhos e cuidado parental (GREEN 2004).
A estação reprodutiva foi definida como o período entre a data de postura do primeiro ovo e a data do último filhote a deixar o ninho (PERRINS & BIRKHEAD 1983). O período de incubação foi considerado como o tempo compreendido entre a postura do último ovo e a eclosão do primeiro ovo, enquanto o período de ninhego foi definido como o tempo entre a eclosão do primeiro ovo até o último filhote deixar o ninho.
Os ovos foram descritos quanto ao seu formato e coloração. O comprimento e a largura dos ovos foram medidos com paquímetro (±0,05 mm). Os filhotes foram examinados no ninho, sendo anotadas características da plumagem e a data da abertura dos olhos e ouvidos ao longo de seu desenvolvimento.
O sucesso reprodutivo foi avaliado comparando-se as estações reprodutivas de 2004 e 2005 em cinco categorias: construção de ninhos, ovos, ninhegos, casais e ninhos. Foram considerados ninhos construídos com sucesso aqueles em que houve postura, enquanto o sucesso dos ovos foi considerado quando houve eclosão. O sucesso dos ninhegos foi considerado quando pelo menos um filhote saiu do ninho. O sucesso dos casais e dos ninhos foi avaliado quando houve produção de pelo menos um jovem. Todas as análises foram feitas em porcentagens. Eventos reprodutivos de um mesmo casal em estações diferentes foram considerados independentes.
Para verificar a influência das enchentes sobre o sucesso reprodutivo foi instalada uma régua graduada de madeira no rio Cipó (19º20'37"S, 43º36'51"W) para monitorar a flutuação do nível da lâmina d'água ao longo do ano. A medida da altura do ninho em relação ao nível do rio foi analisada junto à leitura da régua na data de medição, proporcionando a obtenção da altura do ninho independente do nível da lâmina d'água do rio.
Em um ninho ocupado por um pequeno mamífero foi necessário efetuar sua captura para identificação. Para isto foi afixada uma armadilha do tipo tomahawk na entrada do ninho. O indivíduo capturado foi medido, fotografado e identificado.
RESULTADOS
Construção e descrição do ninho
Ao longo do período de estudo, foram encontrados 20 ninhos, sendo nove na estação reprodutiva de 2004 e 11 na temporada de 2005. Todos foram construídos em barrancos e apenas um ninho não estava localizado na margem do rio, mas sim em barranco situado a 55 m da margem mais próxima.
Machos e fêmeas participam da construção do ninho, sendo o bico a ferramenta para a escavação. No início da construção, quando a entrada da cavidade ainda não está formada o suficiente para que o indivíduo consiga se apoiar, o bico é utilizado apenas uma ou duas vezes, seguido de pouso no solo do barranco ou em galhos próximos. À medida que o túnel se forma, cada indivíduo dispensa períodos mais longos para escavação. Na maioria das vezes, os parceiros se alternam durante o processo. Com incessantes escavações, vai se formando um túnel reto e inclinado para cima entre 30 e 50 graus em relação à horizontal (média = 37,9 ± 7,8 graus, n = 12), cuja profundidade varia entre 48 e 150 cm (média = 82,1 ± 30,4 cm, n = 16) (Tab. I). O fim do túnel se alarga, formando uma câmara com formato esférico de cerca de 25 cm de diâmetro. O material retirado cai naturalmente durante a escavação através do túnel e, principalmente, durante a saída dos adultos, favorecido pela cauda das aves.
Após a escavação do túnel e da câmara, é confeccionada uma tigela rasa de gravetos finos e uniformes bastante rígida, que permanece intacta mesmo se retirada da cavidade. Cascas de galhos finos são utilizadas para forrar a tigela (Fig. 2). Foram medidos 20 ninhos, sendo 16 completamente construídos e com a tigela formada e quatro inacabados. As medidas dos ninhos estão expostas na tabela I.
Em geral, os ninhos começaram a ser construídos um mês antes do início da estação reprodutiva, fato observado em cinco casais. No entanto, os ninhos podem ser construídos em poucos dias, como observado em dois casais que tiveram seu primeiro ninho perdido. Um segundo ninho foi finalizado em apenas três dias.
O exame interno do ninho utilizando o equipamento criado para essa função foi possível em 69% (n = 12) dos ninhos com tigela, ou seja, ninhos finalizados. Ninhos com túneis com profundidade maior que 92 cm (n = 5) não puderam ser examinados.
Cuidado parental e aspectos sociais
Durante a atividade reprodutiva foi observado que machos e fêmeas participam de todas as etapas da reprodução: construção do ninho, incubação dos ovos, alimentação dos ninhegos e da prole durante a permanência dos filhotes no território.
No entanto, fêmeas parecem contribuir mais durante a incubação. A captura de um casal durante a incubação revelou aspectos diversos de desenvolvimento de placa de incubação entre os sexos. A placa incubatória da fêmea estava intensamente vascularizada e sem penas, enquanto a do macho apresentava menor vascularização e algumas penas, características que diminuem a eficiência de transferência de calor aos ovos. O período máximo de permanência contínua de um indivíduo adulto no ninho durante a incubação foi de 52 minutos.
A permanência de pareamento de três casais ao longo de duas estações reprodutivas revelou que H. rectirostris apresenta comportamento monogâmico ao longo dos anos. Alteração na composição dos casais ocorreu apenas em decorrência do desaparecimento de fêmeas, não tendo sido observada nenhuma troca entre casais. Todos indivíduos solitários acompanhados ao longo do estudo foram sexados como machos (veja FARIA et al. 2007b para mais detalhes).
Machos solitários defendem territórios ao longo de todo ano. Um macho reproduziu em 2004 e na estação de 2005 permaneceu no mesmo território, porém solitário. No território de outro macho, houve o desaparecimento de sua parceira antes da estação reprodutiva de 2004, o que impossibilitou tentativas de reprodução nesta temporada. Em 2005, a chegada de outra fêmea em seu território possibilitou sua reprodução.
Estação reprodutiva
O início da reprodução foi altamente sincrônico, tanto entre os casais quanto entre as estações de 2004 e 2005. Os primeiros ninhos em construção foram encontrados na primeira semana de agosto e as posturas iniciaram-se exatamente no mesmo dia nas duas estações reprodutivas: 3 de setembro. No entanto, após o início da estação reprodutiva os eventos tornaram-se assincrônicos devido aos fracassos e múltiplas tentativas reprodutivas. A estação reprodutiva limitou-se a setembro, outubro e novembro, ao longo de 82 dias em 2004 e 85 dias em 2005 (Fig. 3).
A principal limitação à reprodução de H. rectirostris a partir de dezembro na área de estudo foi a elevação do nível do rio, responsável pela destruição dos ninhos e desabamento dos barrancos. O monitoramento da oscilação do nível do rio demonstrou picos de cheia nos períodos de novembro a janeiro e março a abril. Oito dos nove ninhos construídos no final de 2004 e nos primeiros meses de 2005 foram atingidos e destruídos pela cheia do rio (Fig. 4).
A postura dos ovos ocorreu em intervalos de 24 horas e a incubação iniciou-se somente após o término da postura de todos os ovos, fato observado em três ninhos. Nos dias de posturas dos primeiros ovos da ninhada, o ninho permaneceu desprotegido a maior parte do dia. Foram observadas posturas de um, dois ou três ovos em onze ninhos, sendo a média de 2,3 ± 0,5 ovos em quatro ninhos (2004), 2,6 ± 0,6 ovos em sete ninhos (2005) e 2,5 ± 0,4 (ambas temporadas).
O período de incubação foi observado com precisão em dois ninhos, sendo de 17 dias. Em alguns casos, o comportamento de incubação foi observado em 24 dias consecutivos. Tal fato sugere a ocorrência de fracasso dos primeiros ovos e posturas subseqüentes no mesmo ninho. Já o período de ninhego teve duração de 21, 23 e 25 dias, observado com precisão em três ninhos. Assim como o início da incubação, o nascimento dos filhotes parece ser altamente sincrônico. Em um ninho foi possível registrar a eclosão dos ovos em intervalos inferiores à 90 minutos. O tamanho semelhante dos ninhegos observados em vários estágios reforça a sincronia de eclosão entre os filhotes.
Descrição de ovos e filhotes
Os ovos examinados apresentaram formato elíptico, de acordo com classificação proposta por de la Peña (1987), com coloração branca pura, fosca e translúcida. Na superfície dos ovos foram encontradas estrias brancas longitudinais. O comprimento médio foi de 28,0 ± 0,7 mm (n = 10) e a largura média foi de 19,3 ± 0,8 mm (n = 10). O peso médio dos ovos foi de 5,6 ± 0,5 g (n = 10).
Os filhotes nascem com olhos e ouvidos fechados, sem penas e pesando em média 6,2 ± 0,6 g (n = 3). Com uma semana de vida os ninhegos possuem plumas e canhões de penas nas asas, cauda e algumas regiões do dorso e ventre. Os olhos se encontram semi-abertos e os ouvidos totalmente abertos, pesando em média 15,0 ± 1,8 g (n = 6). Com 12 dias de vida o ninhego apresenta o corpo coberto por penas, atingindo em média o peso de 32,5 ± 2,7 g (n = 6). Faltando um dia para deixar o ninho, o filhote pesa em média 46,0 ± 3,2 g (n = 3), já quase atingindo o peso de um adulto (média 48,5 ± 3,2 g, n = 38) (FARIA et al. 2007a). Porém, a plumagem dos filhotes ao abandonar o ninho é bastante diferente dos pais.
O jovem permanece no território dos pais por 90 dias após deixar o ninho, fato observado em dois territórios distintos. Ao abandonar o território dos pais, os jovens ainda possuem plumagem juvenil, caracterizada pela face castanha, penas da fronte e píleo amplamente marginadas de negro, mento, garganta, bigode, pescoço e peito castanhos com a borda das penas negras, dorso marrom escuro, asas e cauda ruivas como o adulto, íris marrom escuro, bico, tarso e dedos negro-acinzentados. A plumagem definitiva de adulto é adquirida em menos de um ano, já na estação reprodutiva seguinte.
Sucesso reprodutivo
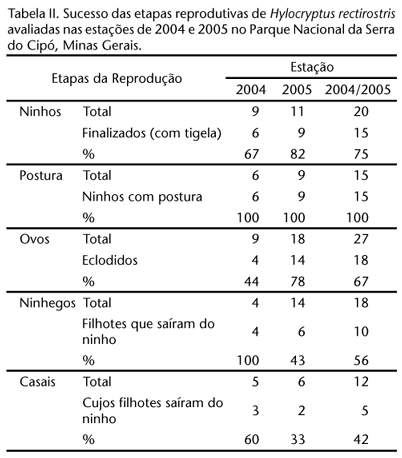
Alguns casais construíram mais de um ninho por estação reprodutiva. Dentre as construções finalizadas, 67% (n = 6) e 82% (n = 9) dos ninhos tiveram postura de ovos, respectivamente, em 2004 e 2005. Na estação reprodutiva de 2004, 44% (n = 4) dos ovos eclodiram, enquanto em 2005 houve eclosão de 78% (n = 14) dos ovos. Todos os ninhegos nascidos em 2004 tiveram sucesso. Já em 2005 apenas 43% (n = 6) dos ninhegos conseguiram voar dos ninhos. Em 2004, 60% (n = 3) dos casais obtiveram êxito reprodutivo, produzindo quatro filhotes, sendo três machos e uma fêmea. Em 2005, 33% (n = 2) dos casais produziram cinco filhotes machos e uma fêmea (Tab. II). Um terço dos nove ninhos (33%) finalizados produziram pelo menos um filhote em 2004 e apenas dois dos onze ninhos (18%) obtiveram sucesso reprodutivo em 2005.
Causas do fracasso reprodutivo
O fracasso reprodutivo ocorreu nas três etapas reprodutivas: construção do ninho, incubação e ninhego. Os motivos de fracasso que puderam ser observados foram (1) destruição do ninho causada pela enchente do rio ou pelo desabamento do teto, (2) predação, e (3) competição com outra espécie. A destruição de ninhos na fase de construção representou a causa de fracasso mais freqüente (Tab. III).
Após a estação reprodutiva de 2004, em março de 2005, três casais estavam em fase de construção e a enchente do rio destruiu os ninhos. Outra ocorrência de fracasso por enchente ocorreu no fim da estação reprodutiva de 2005, na quarta tentativa de reprodução de um casal, quando a enchente do rio alcançou um ninho com filhote.
O desabamento do teto atingiu dois ninhos construídos consecutivamente em 2005 por um mesmo casal, ambos com a tigela formada e um deles com dois ovos. Nas duas ocasiões, quando foi certificado o abandono dos ninhos, o material foi coletado e depositado na Coleção Ornitológica do Departamento de Zoologia da Universidade Federal de Minas Gerais.
Houve duas ocorrências de predação, ambas na fase de ninhego. Em um deles, um predador indeterminado cavou o teto do ninho alcançando os filhotes. No segundo caso, o casal estava em fase de alimentação dos ninhegos quando todos indivíduos da família sumiram repentinamente.
Em três ninhos foi registrada competição com outra espécie. Em uma ocasião um indivíduo de Furnarius figulus (Lichtenstein, 1823) (Furnariidae) ocupou um ninho em que H. rectirostris estava incubando. Em outra ocasião, quando H. rectirostris estava em fase de alimentação de ninhego, um casal de Tersina viridis (Illiger, 1811) (Emberizidae) ameaçava entrar no ninho insistentemente. Perseguições foram observadas repetidas vezes e dois dias depois, o ninho foi encontrado abandonado e os ninhegos ausentes. A ameaça de T. viridis parece ter sido a causa do fracasso deste ninho. No último caso, o ninho já estava finalizado quando um roedor, rato-de-árvore Rhipidomys mastacalis (Lund, 1840) (Muridae), ocupou o ninho para se reproduzir.
Interações agonísticas
Foram registrados outros conflitos interespecíficos ao longo da estação reprodutiva nos quais H. rectirostris se defendeu com sucesso de F. figulus, Stelgidopteryx ruficollis (Vieillot, 1817) (Hirundinidae) e T. viridis. Embora a defesa consistisse principalmente na vocalização do casal, houve também contacto físico.
Um casal de H. rectirostris permaneceu duas horas defendendo seu ninho diante da presença e vocalização de F. figulus. Durante a briga, os indivíduos chegaram a cair no rio. Outro confronto aconteceu quando um indivíduo de H. rectirostris estava incubando os ovos e S. ruficollis pousou na entrada da cavidade. Porém, os conflitos mais agressivos foram registrados com T. viridis. Em uma ocasião, um casal de T. viridis insistia em rondar o ninho de H. rectirostris, sendo perseguidos em vôo por H. rectirostris. Em outra situação, uma fêmea de T. viridis foi encontrada morta a 50 cm de um ninho com filhotes de H. rectirostris.
DISCUSSÃO
Assim como ocorre para vários membros de Furnariidae, o ninho de H. rectirostris apresenta características exclusivas que permitem sua identificação, independente da presença de indivíduos. A inclinação ascendente do túnel de acesso à câmara incubatória entre 30 e 50 graus em relação ao horizonte parece representar uma característica ainda não relatada para nenhuma espécie da família que confecciona ninhos em barrancos (NAROSKY et al. 1983, DE LA PEÑA et. al 1987, SICK 1997, REMSEN 2003), incluindo seu congênere H. erytrocephalus (REMSEN 2003). Este caractere pode auxiliar em pesquisas abordando as relações filogenéticas dos furnarídeos, ainda mal resolvidas para o grupo de espécies que nidificam em barrancos (ZYSKOWSKI & PRUM 1999).
A inclinação dos túneis de H. rectirostris também permite a diferenciação dos demais ninhos escavados em barrancos na Serra do Cipó por aves de outras famílias: Galbula ruficauda Cuvier, 1816 (Galbulidae), Chloroceryle americana (Gmelin, 1788) e C. amazona (Latham, 1790) (Alcedinidae), todos predominantemente horizontais. Ao contrário destas espécies, H. rectirostris não utiliza as patas para retirada dos sedimentos extraídos (SICK 1997), que escoam naturalmente em decorrência da declividade da rampa do túnel.
A originalidade do ninho de H. rectirostris aliado à especificidade de hábitat, representam características que facilitam a detecção e monitoramento das populações. O comportamento pouco arisco da espécie próximo ao ninho, também favorece seu monitoramento.
Cabe ressaltar que a nidificação de H. rectirostris em barrancos de rio, relatada anteriormente por G.T. Matos (SICK 1997) e propagada na literatura (REMSEN 2003), menciona a construção de uma galeria horizontal com tigela confeccionada de folhas secas e capim. Estas características não foram registradas em nenhum ninho encontrado durante este estudo no Parque Nacional da Serra do Cipó.
Instrumentos que permitem exames internos dos ninhos de cavidade são fundamentais para estudos a respeito da biologia reprodutiva das espécies. Entretanto, os aparelhos disponíveis para este fim apresentam alto custo (BOLAND & PHILLIPS 2005). O aparelho desenvolvido para este estudo revelou eficácia e baixo preço, podendo ser utilizado em ninhos de cavidades de outras espécies.
Além de representar uma característica que permite a diferenciação de ninhos de H. rectirostris, a inclinação do túnel representou a medida mais uniforme entre os ninhos avaliados. A seguir, apareceram a altura e largura da entrada do túnel e altura do ninho em relação à lâmina d'água do rio. Por outro lado, as medidas que mais variaram foram distância do ninho ao rio, distância da entrada do ninho ao topo do barranco e à sua base.
A combinação da medida de três parâmetros avaliados é fundamental para o sucesso da construção do ninho: distância do topo do barranco até a abertura do ninho, profundidade do túnel e ângulo de inclinação do túnel. Conforme a combinação entre eles o desabamento do teto da câmara torna-se inevitável. A vegetação do barranco também parece influenciar no desabamento do teto do ninho. Barrancos expostos parecem mais susceptíveis ao desmoronamento do que aqueles cobertos por vegetação.
A altura da entrada do ninho em relação ao rio, associado à inclinação e profundidade do túnel também representam uma combinação importante ao sucesso reprodutivo, pois está relacionada com o nível máximo que o rio pode atingir durante as enchentes repentinas, sem alcançar a câmara incubatória. Um filhote foi salvo graças à combinação dos valores destas variáveis durante uma primeira enchente que desabou parte do túnel de acesso à câmara incubatória. No entanto, a persistência da chuva acabou alcançando o filhote alguns dias depois. A altura da câmara em relação ao nível normal do rio pode determinar o sucesso ou fracasso do ninho em caso de enchentes passageiras.
O início da estação reprodutiva de H. rectirostris coincide com o registrado para Passeriformes da região central do Brasil (Marini & Durães 2001) e do vale do Rio Cipó. Porém, a estação reprodutiva da maior parte dos Passeriformes se prolonga até março/abril, período muito mais longo do que o encontrado para H. rectirostris. A estação reprodutiva de uma população de Phacellodomus rufifrons (Wied, 1821) (Furnariidae) estudada na mesma área prolongou-se durante 202 dias, mais que o dobro em relação ao encontrado para H. rectirorstris. O período reprodutivo de H. rectirostris é limitado pelas chuvas intensas do verão que provocam a subida do nível do rio e o desabamento dos ninhos. A reprodução em barrancos de rios torna-se inviável durante o verão, ao menos que uma estiagem incomum ocorra. É provável que o encurtamento do período reprodutivo seja responsável pela elevada sincronia observada durante o início da atividade reprodutiva entre os casais.
Machos e fêmeas de H. rectirostris participam de todas atividades reprodutivas, fato comprovado para pelo menos outros onze furnarídeos (REMSEN 2003). A igualdade de esforço reprodutivo entre os sexos observado em membros de Furnariidae concorda com a ausência de dimorfismo sexual aparente neste grupo.
O maior desenvolvimento da placa incubatória em fêmeas de H. rectirostris concorda com o observado no joãograveto P. rufifrons. Neste furnarídeo, as fêmeas desenvolvem maior irrigação no ventre e permanecem mais tempo incubando os ovos do que os machos. Em Furnarius rufus (Gmelin, 1788) e Pseudoseisura lophotes (Spix, 1824) (Furnariidae) foi constatado que apenas um indivíduo, provavelmente a fêmea segundo os autores, incuba os ovos durante a noite, enquanto o macho pernoita nas proximidades (FRAGA 1980, NORES & NORES 1994). Estudos mostram que a permanência de adultos no ninho aumenta a probabilidade de eventos predatórios (KOFORD et al. 1990), sugerindo que as fêmeas de H. rectirostris podem ser mais susceptíveis à predação, caso permaneçam no ninho durante a noite. Este comportamento poderia explicar seu baixo número na população. Contudo, estudos mais detalhados são necessários para comprovar essa hipótese.
Em geral, ovos de espécies que nidificam em ninhos fechados apresentam cor branca, pois não necessitam de camuflagem (ONIKI 1985). Hylocryptus rectirostris se enquadra neste padrão assim como a maioria dos membros de sua família (NAROSKY et al. 1983, DE LA PEÑA 1987, SICK 1997, REMSEN 2003).
O número de ovos encontrado em ninhos de furnarídeos é relatado para 99 espécies, sendo que 63% incubam dois ou três ovos (REMSEN 2003). Dados sobre o período de incubação de furnarídeos são muito limitados, com observações para apenas 20 espécies. A incubação pode ocorrer em 13 dias, no caso de Cranioleuca pyrrhophia (Vieillot, 1818) (peso do adulto: 10/16g) até 21 dias em Automolus ochrolaemus (Tschudi, 1844) (peso do adulto: 30/46 g), havendo uma tendência de espécies maiores incubarem por períodos mais longos (REMSEN 2003, SKUTCH 1945).
A duração do período de ninhego é conhecida para 15 espécies de furnarídeos sendo o menor com duração de 13 dias em Xenops minutus (Sparrman, 1788) (peso do adulto: 9/13 g) e o maior com duração de 29 dias em Pseudocolaptes lawrencii Ridgway, 1878 (peso do adulto: 45/58 g) (SKUTCH 1945). Hylocryptus rectirostris (peso do adulto: 45-55 g) apresenta período intermediário em relação a essas espécies com período de ninhego de 21 a 25 dias. O menor período de ninhego de H. rectirostris em relação a um furnarídeo de porte semelhante pode ter sido evolutivamente selecionado pela pressão imposta pelas freqüentes enchentes de verão, eventos que restringem a temporada reprodutiva de uma espécie que nidifica em barrancos de rio. Períodos de ninhego de outras espécies de furnarídeos de porte semelhante devem ser conhecidos para permitir conclusões mais seguras a respeito deste tema.
Assim como observado para H. rectirostris, jovens de outras espécies de furnarídeos permanecem no território dos pais por longos períodos (REMSEN 2003): quatro a nove meses para F. rufus (FRAGA 1980) e até mesmo 13 meses para P. lophotes (NORES & NORES 1994) e mais de 24 meses para P. rufifrons (RODRIGUES & CARRARA 2004), sedo esta última, uma espécie com reprodução cooperativa.
CORY & HELLMAYR (1925) apresentam rápida descrição do jovem de H. rectirostris sem, contudo, mencionar a cor da íris, característica bem evidente e diferenciada do adulto. SICK (1997) e RIDGELY & TUDOR (1994) não mencionam nada a respeito da diferença de plumagem entre jovens e adultos de H. rectirostris, enquanto REMSEN (2003) afirma não haver descrição. WILLIS & ONIKI 2003 apresentam uma prancha com jovem e adulto, destacando a coloração da íris e as barras escuras presentes na coroa e peito dos juvenis, como observado neste estudo.
Em geral, os jovens de furnarídeos são caracterizados pela coloração desbotada nas partes inferiores e borda escura nas penas da garganta e peito. Diferenças de plumagem entre jovens e adultos foram relatadas para 166 espécies de furnarídeos (REMSEN 2003). A plumagem pode ser bem parecida com os adultos ou bastante diferente como relatado neste estudo e para o acrobata Acrobatornis fonsecai Pacheco, Whitney & Gonzaga, 1996 (PACHECO et al. 1996). A plumagem discreta e a cor escura da íris dos jovens de H. rectirostris parecem favorecer sua camuflagem, característica essencial à proteção contra predadores. Aliado a isto, a plumagem nitidamente distinta dos jovens de H. rectirostris parece representar uma característica capaz de evitar a agressão por parte dos adultos territorialistas que não reconhecem nos jovens potenciais competidores (SICK 1997).
Estudos a respeito do sucesso reprodutivo em furnarídeos são escassos (REMSEN 2003). SKUTCH (1985) calculou o percentual de sucesso reprodutivo de ninhos que produziram ao menos um filhote para diversas espécies tropicais equivalente a 35%, valor aproximado daquele encontrado para H. rectirostris na estação de 2004 e bem acima do encontrado em 2005, respectivamente 33% e 18%. Em P. rufifrons, 44% dos grupos produziram pelo menos um filhote, taxa semelhante aos 42% encontradas para os casais de H. rectirostris nas duas estações em conjunto. Em F. rufus, 72% dos ovos postos produziram filhotes que deixaram o ninho (FRAGA 1980), enquanto em P. lophotes a taxa foi de 59% (NORES & NORES 1994), ambos bastante superiores aos 37% constatados para H. rectirostris nas duas estações.
Confrontando as estações reprodutivas de 2004 e 2005 percebe-se uma diferença nítida da etapa responsável pelo maior fracasso. Em 2004, mais da metade dos ovos foram perdidos enquanto em 2005 o fracasso maior ocorreu na fase de ninhego. Agrupando as estações, as diferenças são suavizadas, apesar de inclinada a uma maior perda de ovos em relação a ninhegos. Dentre as causas determinadas, as principais responsáveis pelo fracasso reprodutivo nestas fases foram: predação e competição.
A predação tem sido uma das principais causas de fracasso reprodutivo relatadas em estudos conduzidos em regiões tropicais (SKUTCH 1985, NORES & NORES 1994, STUTCHBURY & MORTON 2001). Roedores podem representar predadores potenciais de ninhos de cavidade (BRADLEY & MARZLUFF 2003). Espécies de roedores de Thomasomys, Proechimys e Oryzomys foram encontrados em ninhos de furnarídeos, mas não foi confirmado se a ocupação foi apenas em ninhos abandonados ou se houve ocorrência por expulsão (REMSEN 2003), como observado neste estudo.
Não foi possível certificar se a ocupação de um ninho pelo roedor R. mastacalis foi acompanhada por predação de ovos recém postos. No entanto, a presença de um grande número de penas de adultos de H. rectirostris na entrada do ninho sugeriu algum tipo de confronto. A captura do casal que construiu o ninho uma semana após a invasão pelo roedor revelou indício de agressão. O lado ventral direito do macho apresentava uma lesão recente, sugerindo que roedores podem potencialmente provocar a morte de ninhegos e até mesmo de adultos de H. rectirostris.
No caso de H. rectirostris, ovos e ninhegos recém-nascidos podem ter sido retirados dos ninhos pelos competidores de ninhos. A competição com espécies incapazes de produzir seus próprios ninhos representa uma ameaça ao sucesso reprodutivo de aves que nidificam em cavidades (Pizo 1996).
Além de ninhos ativos, ninhos abandonados de H. rectirostris também foram utilizados por outras espécies. Foi registrada a nidificação de F. figulus em três ninhos abandonados e de T. viridis em outro ninho. Assim, H. rectirostris, juntamente com outras aves que escavam galerias em barrancos, produzem sítios que permitem a reprodução de animais incapazes de construir seus próprios ninhos, sejam aves ou pequenos mamíferos, favorecendo, desta forma, a diversidade de espécies.
O estudo da biologia reprodutiva de H. rectirostris revelou vários aspectos, até então, desconhecidos para espécies de Furnariidae. As peculiaridades de seu ninho associadas ao sedentarismo, monogamia e territorialidade favorecem o monitoramento de suas populações. Sua íntima dependência das matas ciliares do Cerrado gabarita a espécie como bio-indicadora de qualidade ambiental desta fisionomia, que apesar de protegida por lei, foi e continua sendo descaracterizada em várias regiões do bioma. Projetos de preservação e revitalização das matas ciliares do Cerrado podem, portanto, utilizar as populações de H. rectirostris como parâmetro de qualidade ambiental.
AGRADECIMENTOS
Agradecemos ao Laboratório de Biodiversidade e Evolução Molecular (UFMG); ao desenhista Marcus Ferreira (UFMG); aos funcionários do IBAMA do PARNA da Serra do Cipó pelo apoio; ao Centro Nacional de Pesquisas para Conservação das Aves Silvestres pela concessão das anilhas e licença para anilhamento; ao Programa de Pós-graduação em Ecologia, Conservação e Manejo de Vida Silvestre (UFMG); ao USFish and Wildlife Service pelo apoio financeiro; à CAPES, pela bolsa de mestrado à L.F. M.R. agradece ao CNPq (processos 473428/2004-0 e 300731/2006-0) e à Fundação O Boticário de Proteção à Natureza pelo apoio.
LITERATURA CITADA
BIRDLIFE INTERNATIONAL. 2000. Threatened birds of the world. Barcelona, Lynx Editions, BirdLife International, 852p.
BOLAND, C.R.J. & R.M. PHILLIPS. 2005. A small, lightweight, and inexpensive "burrowscope" for viewing nest contents of tunnel-nesting birds. Journal of Field Ornithology 76 (1): 21-26.
BRADLEY, J.E. & J.M. MARZLUFF. 2003. Rodents as nest predators: influences on predatory behavior and consequences to nesting birds. Auk 120 (4): 1180-1187.
CORY, C.B. & C.E. HELLMAYR. 1925. Catalogue of birds of the Americas. Field Museum of Natural History Publication, Zoological Series, 13 (4): 1-390.
DE LA PEÑA, M.R. 1987. Nidos y huevos de las aves argentinas. Santa Fé, M.R. de La Peña, 263p.
FARIA, L.; L.A. CARRARA & M. RODRIGUES. 2007a. Dimorfismo sexual de tamanho no fura-barreira Hylocryptus rectirostris (Wied) (Aves Furnariidae). Revista Brasileira de Zoologia 24 (1): 207-212.
FARIA, L.; L.A. CARRARA & M. RODRIGUES. 2007b. Sistema territorial e forrageamento do fura-barreira Hylocryptus rectirostris (Aves: Furnariidae). Revista Brasileira de Ornitologia 15 (3): 395402.
FRAGA, R.M. 1980. The breeding of rufous horneros (Furnarius rufus). Condor 82: 58-68.
GREEN, R.E. 2004. Breeding biology, p. 57-83. In: W.J. SUTHERLAND; I. NEWTON & R.E. GREEN (Eds). Bird ecology and conservation, a handbook of techniques. Oxford, Oxford Univerity Press, 386p.
IBAMA. 1994. Manual de anilhamento de aves silvestres. Brasília, Instituto Brasileiro do Meio Ambiente e dos Recursos Naturais Renováveis, 146p.
KOFORD, R.R.; B.S. BOWEN & S.L. VEHRENCAMP. 1990. Grooved-billed Anis: joint-nesting in a tropical cuckoo, p. 335-355. In: P.B. STACEY & W.D. KOENIG (Eds). Cooperative breeding in birds: long-term studies of ecology and behavior. Cambridge, Cambridge University Press, 615p.
MADEIRA, A.J. & W.G. FERNANDES. 1999. Reprodutive phenology of sympatric taxa of Chamaecrista (Leguminosae) in Serra do Cipó, Brazil. Jornal of Tropical Ecology 15 (2): 463-479.
MARINI, M.Â. & R.D. DURÃES. 2001. Annual pattern of molt and reproductive activity of passerines in south-central Brazil. Condor 115: 767-775.
NAROSKY, T.; R. FRAGA & M. DE LA PEÑA. 1983. Nidificacion de las aves argentinas (Dendrocolaptidae y Furnariidae). Buenos Aires, Asociacion Ornitologica del Plata, 98p.
NORES, A.I. & M. NORES. 1994. Nest building and nesting behavior of the brown cacholote. Wilson Bulletin 106 (1): 106-120.
ONIKI, Y. 1985. Why robin eggs are blue and birds build nests: statistical tests for Amazonian birds, p. 536-545. In: P.A. BUCKLEY; M.S. FOSTER; E.S. MORTON; R.S. RIDGELY & F.G. BUCKLEY (Ed.). Neotropical ornithology. Washington, American Ornitho-logists Union, Ornithological Monographs 36, 1041p.
PACHECO, J.F.; B.M. WHITNEY & L.P. GONZAGA. 1996. A new genus and species of furnariid (Aves: Furnariidae) from the cocoagrowing region of southeastern Bahia, Brazil. Wilson Bulletin 108 (3): 397-433.
PERRINS, C.M. & T.R. BIRKHEAD. 1983. Avian ecology. Glasgow, Blackie, 221p.
PIZO, M.A. 1996. Interspecific aggression in the hole-nesting long-tailed tyrant, Colonia colonus (Aves, Tyrannidae). Ciência e Cultura 48 (4): 278-281.
REMSEN, J.V. 2003. Family Furnariidae (ovenbirds), p. 162-357. In: J. DEL HOYO; A. ELLIOTT & D.A. CHRISTIE (Eds). Handbook of the birds of the world. Broadbills to Tapaculos. Barcelona, Lynx Edicions, vol. 8, 845p.
RIBEIRO, J.F. & B.M.T. WALTER. 1998. Fitofisionomias do bioma cerrado, p. 89-166. In: SANO, S.M. & S.P. ALMEIDA (Eds) Cerrado: Ambiente e Flora. Planaltina, Embrapa, 556p.
RIDGELY, R.S. & G. TUDOR. 1994. The birds of South America. Oxford, Oxford University Press, vol. 2, 814p.
RODRIGUES, M. & L. CARRARA. 2004. Co-operative breeding in the rufous-fronted thornbird Phacellodomus rufifrons: a Neotropical ovenbird. Ibis 146: 351-354.
RODRIGUES, M.; L. CARRARA; L. FARIA & H. GOMES. 2005. Aves do Parque Nacional da Serra do Cipó: o Vale do Rio Cipó. Revista Brasileira de Zoologia 22 (2): 326-338.
SÃO PAULO. 1998. Fauna ameaçada no estado de São Paulo. São Paulo, Secretaria do Meio Ambiente, Documentos Ambientais, Série Probio, 56p.
SICK, H. 1997.Ornitologia brasileira. Rio de Janeiro, Editora Nova, 862p.
SILVA, J.M.C. 1995. Birds of the Cerrado Region, South America. Steenstrupia 21 (2): 69-92.
SKUTCH, A.F. 1945. Incubation and nestling periods of Central American birds. Auk 62: 8-3.
SKUTCH, A.F. 1985. Clutch size, nesting success, and predation on nests of Neotropicalbirds, reviewed, p. 575-594. In: P.A. BUCKLEY; M.S. FOSTER; E.S. MORTON; R.S. RIDGELY & F.G. BUCKLEY (Ed.). Neotropical ornithology. Washington, American Ornithologists Union, Ornithological Monographs 36, 1041p.
STOTZ, D.F.; J.W. FITZPATRICK; T.A. PARKER III & D.K. MOSKOVITS. 1996. Neotropical birds: ecology and conservation. Chicago, The University of Chicago Press, 478p.
STUTCHBURY, B.J.M. & E.S. MORTON. 2001. Behavioral ecology of tropical birds. San Diego, Academic press, 165p.
VAURIE, C. 1980. Taxonomy and geographical distribution of the Furnariidae (Aves, Passeriformes). Bulletin of the American Museum of Natural History 166 (1): 1-357.
VIELLIARD, J. & W.R. SILVA. 2001. Avifauna de mata ciliar, p. 169185. In: R.R. RODRIGUES & H.F. FILHO (Eds). Matas Ciliares: conservação e recuperação. São Paulo, Editora da Universidade de São Paulo, Fapesp, 320p.
WILLIS, E.O. & Y. ONIKI. 2003. Aves do estado de São Paulo. Rio Claro, Divisa, 398p.
ZYSKOWSKI, K. & R.O. PRUM. 1999. Phylogenetic analysis of the nest architecture of neotropical ovenbirds (Furnariidae). Auk 116 (4): 891-911.
Submitted: 03.V.2007; Accepted: 26.V.2008.
Editorial responsibility: Lena Geise
- BIRDLIFE INTERNATIONAL. 2000. Threatened birds of the world. Barcelona, Lynx Editions, BirdLife International, 852p.
- BOLAND, C.R.J. & R.M. PHILLIPS. 2005. A small, lightweight, and inexpensive "burrowscope" for viewing nest contents of tunnel-nesting birds. Journal of Field Ornithology 76 (1): 21-26.
- BRADLEY, J.E. & J.M. MARZLUFF. 2003. Rodents as nest predators: influences on predatory behavior and consequences to nesting birds. Auk 120 (4): 1180-1187.
- CORY, C.B. & C.E. HELLMAYR. 1925. Catalogue of birds of the Americas. Field Museum of Natural History Publication, Zoological Series, 13 (4): 1-390.
- DE LA PEÑA, M.R. 1987. Nidos y huevos de las aves argentinas. Santa Fé, M.R. de La Peña, 263p.
- FARIA, L.; L.A. CARRARA & M. RODRIGUES. 2007a. Dimorfismo sexual de tamanho no fura-barreira Hylocryptus rectirostris (Wied) (Aves – Furnariidae). Revista Brasileira de Zoologia 24 (1): 207-212.
- FARIA, L.; L.A. CARRARA & M. RODRIGUES. 2007b. Sistema territorial e forrageamento do fura-barreira Hylocryptus rectirostris (Aves: Furnariidae). Revista Brasileira de Ornitologia 15 (3): 395402.
- FRAGA, R.M. 1980. The breeding of rufous horneros (Furnarius rufus). Condor 82: 58-68.
- GREEN, R.E. 2004. Breeding biology, p. 57-83. In: W.J. SUTHERLAND; I. NEWTON & R.E. GREEN (Eds). Bird ecology and conservation, a handbook of techniques. Oxford, Oxford Univerity Press, 386p.
- IBAMA. 1994. Manual de anilhamento de aves silvestres Brasília, Instituto Brasileiro do Meio Ambiente e dos Recursos Naturais Renováveis, 146p.
- KOFORD, R.R.; B.S. BOWEN & S.L. VEHRENCAMP. 1990. Grooved-billed Anis: joint-nesting in a tropical cuckoo, p. 335-355. In: P.B. STACEY & W.D. KOENIG (Eds). Cooperative breeding in birds: long-term studies of ecology and behavior. Cambridge, Cambridge University Press, 615p.
- MADEIRA, A.J. & W.G. FERNANDES. 1999. Reprodutive phenology of sympatric taxa of Chamaecrista (Leguminosae) in Serra do Cipó, Brazil. Jornal of Tropical Ecology 15 (2): 463-479.
- MARINI, M.Â. & R.D. DURÃES. 2001. Annual pattern of molt and reproductive activity of passerines in south-central Brazil. Condor 115: 767-775.
- NAROSKY, T.; R. FRAGA & M. DE LA PEÑA. 1983. Nidificacion de las aves argentinas (Dendrocolaptidae y Furnariidae). Buenos Aires, Asociacion Ornitologica del Plata, 98p.
- NORES, A.I. & M. NORES. 1994. Nest building and nesting behavior of the brown cacholote. Wilson Bulletin 106 (1): 106-120.
- ONIKI, Y. 1985. Why robin eggs are blue and birds build nests: statistical tests for Amazonian birds, p. 536-545. In: P.A. BUCKLEY; M.S. FOSTER; E.S. MORTON; R.S. RIDGELY & F.G. BUCKLEY (Ed.). Neotropical ornithology. Washington, American Ornitho-logists Union, Ornithological Monographs 36, 1041p.
- PACHECO, J.F.; B.M. WHITNEY & L.P. GONZAGA. 1996. A new genus and species of furnariid (Aves: Furnariidae) from the cocoagrowing region of southeastern Bahia, Brazil. Wilson Bulletin 108 (3): 397-433.
- PERRINS, C.M. & T.R. BIRKHEAD. 1983. Avian ecology. Glasgow, Blackie, 221p.
- PIZO, M.A. 1996. Interspecific aggression in the hole-nesting long-tailed tyrant, Colonia colonus (Aves, Tyrannidae). Ciência e Cultura 48 (4): 278-281.
- REMSEN, J.V. 2003. Family Furnariidae (ovenbirds), p. 162-357. In: J. DEL HOYO; A. ELLIOTT & D.A. CHRISTIE (Eds). Handbook of the birds of the world. Broadbills to Tapaculos. Barcelona, Lynx Edicions, vol. 8, 845p.
- RIBEIRO, J.F. & B.M.T. WALTER. 1998. Fitofisionomias do bioma cerrado, p. 89-166. In: SANO, S.M. & S.P. ALMEIDA (Eds) Cerrado: Ambiente e Flora. Planaltina, Embrapa, 556p.
- RIDGELY, R.S. & G. TUDOR. 1994. The birds of South America. Oxford, Oxford University Press, vol. 2, 814p.
- RODRIGUES, M. & L. CARRARA. 2004. Co-operative breeding in the rufous-fronted thornbird Phacellodomus rufifrons: a Neotropical ovenbird. Ibis 146: 351-354.
- RODRIGUES, M.; L. CARRARA; L. FARIA & H. GOMES. 2005. Aves do Parque Nacional da Serra do Cipó: o Vale do Rio Cipó. Revista Brasileira de Zoologia 22 (2): 326-338.
- SÃO PAULO. 1998. Fauna ameaçada no estado de São Paulo. São Paulo, Secretaria do Meio Ambiente, Documentos Ambientais, Série Probio, 56p.
- SICK, H. 1997.Ornitologia brasileira. Rio de Janeiro, Editora Nova, 862p.
- SILVA, J.M.C. 1995. Birds of the Cerrado Region, South America. Steenstrupia 21 (2): 69-92.
- SKUTCH, A.F. 1945. Incubation and nestling periods of Central American birds. Auk 62: 8-3.
- SKUTCH, A.F. 1985. Clutch size, nesting success, and predation on nests of Neotropicalbirds, reviewed, p. 575-594. In: P.A. BUCKLEY; M.S. FOSTER; E.S. MORTON; R.S. RIDGELY & F.G. BUCKLEY (Ed.). Neotropical ornithology. Washington, American Ornithologists Union, Ornithological Monographs 36, 1041p.
- STOTZ, D.F.; J.W. FITZPATRICK; T.A. PARKER III & D.K. MOSKOVITS. 1996. Neotropical birds: ecology and conservation. Chicago, The University of Chicago Press, 478p.
- STUTCHBURY, B.J.M. & E.S. MORTON. 2001. Behavioral ecology of tropical birds. San Diego, Academic press, 165p.
- VAURIE, C. 1980. Taxonomy and geographical distribution of the Furnariidae (Aves, Passeriformes). Bulletin of the American Museum of Natural History 166 (1): 1-357.
- VIELLIARD, J. & W.R. SILVA. 2001. Avifauna de mata ciliar, p. 169185. In: R.R. RODRIGUES & H.F. FILHO (Eds). Matas Ciliares: conservação e recuperação. São Paulo, Editora da Universidade de São Paulo, Fapesp, 320p.
- WILLIS, E.O. & Y. ONIKI. 2003. Aves do estado de São Paulo. Rio Claro, Divisa, 398p.
- ZYSKOWSKI, K. & R.O. PRUM. 1999. Phylogenetic analysis of the nest architecture of neotropical ovenbirds (Furnariidae). Auk 116 (4): 891-911.
Datas de Publicação
-
Publicação nesta coleção
01 Ago 2008 -
Data do Fascículo
Jun 2008
Histórico
-
Aceito
26 Maio 2008 -
Recebido
03 Maio 2007