Resumos
Estudou-se, pela histomorfometria da bolsa de Fabrício, o envolvimento da apoptose como mecanismo de depleção linfocitária em frangos de corte, após ingestão de toxina T-2 de Fusarium sporotrichioides veiculada pela ração. Foram utilizados 42 pintos de um dia de idade, distribuídos ao acaso em três grupos. O grupo tratado (n = 15) recebeu diariamente ração contaminada com 2,64 mg/kg da toxina T-2; o grupo residual (n = 12) recebeu ração contaminada por 7 ou 14 dias, passando a receber ração limpa (não contaminada) na semana antecedente ao sacrifício. Um grupo controle (n = 15) recebeu ração não contaminada. Aos 7, 14 e 21 dias de experimento cinco animais de cada um dos grupos controle e tratado e aos 14 e 21dias seis do grupo residual foram sacrificados, colhendo-se as bolsas de Fabrício (BF) para análise histomorfométrica e determinação do índice apoptótico. As características da apoptose foram confirmadas pela técnica de marcação in situ da fragmentação do genoma (TUNEL) e pela eletroforese do DNA, em gel de agarose. As BF nos grupos tratado e residual, aos 14 e 21 dias, apresentaram depleção linfocitária de moderada a intensa e elevado índice apoptótico, significativamente maior do que do grupo controle (P<0,05). Os resultados permitem concluir que a apoptose está envolvida no mecanismo da depleção linfocitária provocada pela toxina T-2, em frangos de corte.
Frango de corte; bolsa de Fabricius; apoptose; toxina T-2
It was studied by the histomorphometry of the bursa of Fabricius the involvement of apoptosis as a mechanism of lymphoid depletion in broiler chicks, after the intake of feed containing T-2 toxin of Fusarium sporotrichioides. Forty-two one-day-old chicks were distributed randomly in three groups. The treated group (n=15) received contaminated feed with 2.64 mg/kg of the T-2 toxin. The residual group (n=12) received contaminated feed up to 7 and 14 days and noncontaminated feed during the last week. One control group (n=15) received noncontaminated feed. Five animals from each control and treated groups were killed at 7, 14 and 21 days, and six from the residual group at 14 and 21 days, and their bursa of Fabricius (BF) were collected for histomorphometric analysis and determination of apoptotic index. The apoptosis was confirmed by in situ labeling of the fragmentation of the genome (TUNEL) and by electrophoresis of DNA in agarose gel. BF of treated and residual groups showed moderate to intense depletion of the lymphoid follicles and higher apoptotic index than the control group (P< 0.05). These results allowed to conclude that apoptosis is involved in the mechanism of lymphoid depletion caused by T-2 toxin in broiler chicks.
Broiler chick; bursa of Fabricius; apoptosis, T-2 toxin
Apoptose na depleção linfocitária induzida pela toxina T-2 em frangos de corte. Histomorfometria da bolsa de Fabricius
[Apoptosis in the lymphoid depletion induced by T-2 toxin in broiler chicks. Histomorphometry of the bursa of Fabricius]
M.A. Rachid1, A.C. Vasconcelos2* * Autor para correspondência E-mail anilton@icb.ufmg.br , V.A. Nunes1
1Escola de Veterinária da UFMG
2Instituto de Ciências Biológicas da UFMG
Caixa Postal 486
31270-010 Belo Horizonte, MG
Recebido para publicação, após modificações, em 21 de setembro de 2000.
Apoio financeiro: FAPEMIG, CNPq. Trabalho do Núcleo de Estudo em Patologia da Nutrição (NEPAN).
RESUMO
Estudou-se, pela histomorfometria da bolsa de Fabrício, o envolvimento da apoptose como mecanismo de depleção linfocitária em frangos de corte, após ingestão de toxina T-2 de Fusarium sporotrichioides veiculada pela ração. Foram utilizados 42 pintos de um dia de idade, distribuídos ao acaso em três grupos. O grupo tratado (n = 15) recebeu diariamente ração contaminada com 2,64 mg/kg da toxina T-2; o grupo residual (n = 12) recebeu ração contaminada por 7 ou 14 dias, passando a receber ração limpa (não contaminada) na semana antecedente ao sacrifício. Um grupo controle (n = 15) recebeu ração não contaminada. Aos 7, 14 e 21 dias de experimento cinco animais de cada um dos grupos controle e tratado e aos 14 e 21dias seis do grupo residual foram sacrificados, colhendo-se as bolsas de Fabrício (BF) para análise histomorfométrica e determinação do índice apoptótico. As características da apoptose foram confirmadas pela técnica de marcação in situ da fragmentação do genoma (TUNEL) e pela eletroforese do DNA, em gel de agarose. As BF nos grupos tratado e residual, aos 14 e 21 dias, apresentaram depleção linfocitária de moderada a intensa e elevado índice apoptótico, significativamente maior do que do grupo controle (P<0,05). Os resultados permitem concluir que a apoptose está envolvida no mecanismo da depleção linfocitária provocada pela toxina T-2, em frangos de corte.
Palavras-Chave: Frango de corte, bolsa de Fabricius, apoptose, toxina T-2
ABSTRACT
It was studied by the histomorphometry of the bursa of Fabricius the involvement of apoptosis as a mechanism of lymphoid depletion in broiler chicks, after the intake of feed containing T-2 toxin of Fusarium sporotrichioides. Forty-two one-day-old chicks were distributed randomly in three groups. The treated group (n=15) received contaminated feed with 2.64 mg/kg of the T-2 toxin. The residual group (n=12) received contaminated feed up to 7 and 14 days and noncontaminated feed during the last week. One control group (n=15) received noncontaminated feed. Five animals from each control and treated groups were killed at 7, 14 and 21 days, and six from the residual group at 14 and 21 days, and their bursa of Fabricius (BF) were collected for histomorphometric analysis and determination of apoptotic index. The apoptosis was confirmed by in situ labeling of the fragmentation of the genome (TUNEL) and by electrophoresis of DNA in agarose gel. BF of treated and residual groups showed moderate to intense depletion of the lymphoid follicles and higher apoptotic index than the control group (P< 0.05). These results allowed to conclude that apoptosis is involved in the mechanism of lymphoid depletion caused by T-2 toxin in broiler chicks.
Keywords: Broiler chick, bursa of Fabricius, apoptosis, T-2 toxin.
INTRODUÇÃO
A apoptose é um processo de morte celular individual e ativo, caracterizado pela fragmentação nuclear e pela formação de corpos apoptóticos (Cohen, 1991). Ao contrário da necrose, não ocorre liberação do conteúdo celular para o interstício e, conseqüentemente, não incita inflamação ao redor das células mortas (Wyllie et al., 1980). Esse tipo de autodestruição celular pode ser iniciada por estímulos fisiológicos ou patológicos, como por algumas toxinas (Anilkumar et al., 1992; Gruber et al., 1994; Arai et al., 1996; Li & Shimizu, 1996; Hickman & Boyle, 1997).
A toxina T-2 pertence ao grupo dos tricotecenos produzidos por fungos do gênero Fusarium (Baldissera et al., 1992; Osweiler, 1998). Os tricotecenos são toxinas veiculadas principalmente pelo milho contaminado por fungos e são considerados potentes agentes cáusticos e radiomiméticos (Hoerr et al., 1982; Sharma, 1993).
Como agente radiomimético pode causar imunossupressão em aves, dependendo da dose e do período de exposição (Chi et al., 1977; Hoerr et al., 1982; Sharma, 1991), mas seu mecanismo imunossupressor não é totalmente conhecido. Postula-se que a toxina T-2 exerça sua atividade imunossupressora diretamente sobre as células de defesa, levando-as à apoptose. No entanto, existem evidências de que ela causa necrose dos tecidos linfóides e de linfócitos circulantes (Holt & DeLoarch, 1988).
O objetivo deste trabalho foi estudar o envolvimento da apoptose de células linfóides da bolsa de Fabrício no mecanismo da depleção linfocitária provocada pela toxina T-2 em frangos de corte.
MATERIAL E MÉTODOS
Foram utilizados 42 pintos de um dia de idade, da linhagem Hubbard, todos machos, distribuídos ao acaso em três grupos: controle (n = 15), tratado (n = 15) e residual (n = 12). As aves foram submetidas ao esquema usual de vacinação e alojados, por sorteio, nas gaiolas centrais de oito baterias, providas de comedouro linear, bebedouros de pressão e fonte de aquecimento, numa lotação de cinco a seis aves por gaiola.
A ração básica, à base de milho e soja, formulada para atender às exigências de frangos de corte até 21 dias de idade (Rostagno et al., 1996) foi fornecida ad libitum. A matéria-prima usada era isenta de contaminantes biológicos e de micotoxinas. Para o grupo tratado, todo o milho da formulação foi substituído por milho contaminado, contendo apenas toxina T-2 de Fusarium sporotrichioides, na concentração de 2,6mg/kg. O grupo residual foi dividido em dois subgrupos. O primeiro recebeu ração contaminada durante sete dias, passando a receber ração não contaminada por mais sete dias. O segundo recebeu a mesma ração por 14 dias, passando a receber ração não contaminada até o final do experimento, que teve a duração de 21 dias.
Cinco animais de cada um dos grupos controle e tratado foram sacrificados e necropsiados aos 7, 14 e 21 dias. Do grupo residual foram sacrificados seis animais aos 14 dias e outros seis aos 21. À necropsia, foram colhidos dois fragmentos da bolsa de Fabrício de cada animal. Um dos fragmentos foi imerso em formalina neutra e tamponada a 10%, processado pela técnica rotineira de inclusão em parafina e corado pelas técnicas de hematoxilina-eosina (HE) (Luna, 1968) e methyl green pyronin (MGP) (Prophet et al., 1992). Para identificação in situ da fragmentação do DNA, foi utilizada a técnica de inserção de nucleotídeos biotinilados na extremidade do fragmento do genoma terminal deoxynucleotidil transferase uracil nick end labeling (TUNEL) (Apoptag Kit - Catálogo S7101-Kit; Oncor - 209 Perrry Parkway, Gaithersburg, MD, 20877) (Gavrieli et al., 1992). O outro foi acondicionado em tubos de 1,5ml (tipo Eppendorf) e estocado a 80° C, para posterior extração e eletroforese do DNA.
As lâminas obtidas foram examinadas ao microscópio óptico para identificação e caracterização das lesões e posteriormente submetidas à análise morfométrica por intermédio de sistema analisador de imagens Kontron Elektronic GMBH e programa KS 300 V2.0.
Foi determinada a razão parênquima:estroma em três campos microscópicos por secção histológica. Em cada campo, com área total de 5,65862´ 106, mediram-se as áreas folicular (folículos linfóides) e de espaços vazios. Subtraindo-se essas áreas da área total do campo obteve-se a área do estroma. A razão parênquima:estroma foi obtida pela divisão da área folicular (parênquima) pela área do estroma. Foi estabelecida a proporção percentual do parênquima e de todos os dados obtiveram-se a média e o desvio-padrão.
As secções coradas pela técnica de MGP foram submetidas à morfometria pelo programa KS 400 V2.0 para quantificação do índice apoptótico (número total de linfócitos em apoptose/número total de linfócitos). Foram quantificadas como apoptóticas as células com morfologia típica, isto é, com condensação nuclear e citoplasmática ou resíduos citoplasmáticos contendo densos fragmentos de cromatina.
O número mínimo de campos significativos a serem avaliados foi estabelecido em 150 campos de uma só secção. Dos 150 campos contados, foram obtidos 10 valores médios, considerados como unidades experimentais, para 10 amostras de 5, 6, 7, 8, 9, 10 e 11 campos. Pelo teste de instabilidade (desvio-padrão) das unidades experimentais (Sampaio, 1998) ficou comprovado que a contagem de oito campos por secção seria suficiente (Fig. 1). Assim, neste estudo, o índice apoptótico foi estabelecido em oito campos/secção.
Para o teste de TUNEL foi seguido o protocolo especificado pelo fabricante, sendo o tempo de proteinase K adaptado para o tecido da bursa. As proteínas foram removidas do núcleo pela incubação com 25mg/ml de proteinase K (Sigma), durante 15 minutos, a 37oC. Foram consideradas características de apoptose a marcação específica de grumos amarronzados, revelados pela diaminobenzidina (DAB).
Para extração do DNA, os fragmentos da bolsa de Fabrício foram macerados e lavados em 0,5ml de tampão lítico hipotônico TTE (10mM Tris, 0,25% Triton x 100, 1mM EDTA) por 0,125cm3 de tecido. As proteínas foram removidas por extração pelo álcool isoamílico-fenol-clorofórmio (1:25:24). Em seguida, foi feita a sedimentação do DNA com acetato de sódio 3M, pH 5,2, no volume de 1:20, e etanol a 96o, a 20oC, durante a noite, no volume de 1:2. O sedimento de DNA foi lavado duas vezes em etanol a 70%, seco à temperatura ambiente e ressuspenso em TE [Tris-HCl a 10 mM (pH 7,4) e EDTA a 1mM] e submetido à eletroforese em gel de agarose a 1,5%, durante 100 minutos, a 60V. O gel foi corado com brometo de etídio e fotografado sob transiluminação ultravioleta.
O delineamento experimental foi o inteiramente ao acaso. As variáveis razão parênquima:estroma e índice apoptótico foram analisadas pelo teste não paramétrico de Kruskal-Wallis (Sampaio, 1998). Os dados de proporção percentual do parênquima foram submetidos à análise de variância pelo Sistema de Análise Estatística (SAS) e as médias comparadas pelo teste de Duncan.
RESULTADOS E DISCUSSÃO
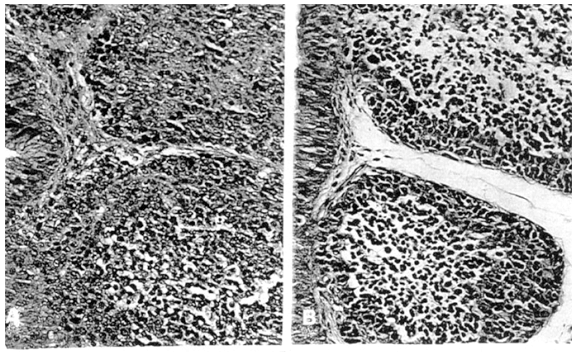
No grupo controle, independentemente do período experimental, a morfologia da bolsa de Fabrício não apresentou alterações dignas de nota. Os folículos linfóides estavam bem celularizados, totalmente preenchidos por linfócitos, com definição clara das regiões cortical e medular e mostrando raras células com cromatina condensada (apoptose). As pregas bursais estavam revestidas por epitélio simples colunar com algumas células caliciformes (Fig. 2A, C ).
No grupo tratado, as alterações histológicas foram moderadas aos 7 e 14 dias e mais evidentes aos 21 dias. Observaram-se folículos linfóides diminuídos de volume, com rarefação difusa de linfócitos tanto da região cortical quanto medular (Fig. 2B), com formação de inúmeros espaços vazios (Fig. 2D ). Notou-se ainda presença de corpos apoptóticos (Fig. 2D ) esparsos no interior dos espaços vazios e de vários linfócitos com cromatina condensada (apoptose). O estroma de sustentação estava mais evidente e o epitélio de revestimento era irregular, com aumento do número de células caliciformes. Arai et al. (1996) observaram a indução de apoptose por irradiação de linfócitos da BF. A morfologia típica de células em apoptose foi visualizada por microscopia óptica e confirmada pela microscopia eletrônica. Foram consideradas como características morfológicas típicas a retração celular, a condensação periférica da cromatina e a fragmentação nuclear e celular, com a formação de corpos apoptóticos. Foram estas características, descritas por Arai et al. (1996), as consideradas no presente estudo, quando se faz referência aos linfócitos em apoptose.
No grupo residual as lesões histológicas eram mais acentuadas e constantes em todos os períodos de observação, quando comparadas àquelas do grupo tratado. As bolsas de Fabrício apresentavam supremacia de folículos com depleção linfocitária, com sensível redução do número de linfócitos, em algumas bolsas atingindo tanto a região medular quanto a cortical. Os cortes histológicos mostravam espaços vazios multifocais difusamente distribuídos pelo órgão, dando uma aparência de "peneira" e com muitas células em apoptose. Além disso, o estroma era mais evidente, observando-se enrugamento irregular do epitélio de revestimento.
Assim, pela avaliação morfológica qualitativa, as BF dos grupos tratado e residual evidenciaram menor celularidade do que no grupo controle, caracterizando graus variados de depleção linfóide.
As lesões microscópicas descritas neste trabalho assemelham-se às descritas na literatura para a depleção linfóide provocada pela toxina T-2 (Hoerr et al., 1981; Hoerr et al., 1982; Neiger et al., 1994). Terao et al. (1978) salientam que os linfócitos da porção central dos folículos são os mais severamente acometidos. Esses pesquisadores observaram, por microscopia eletrônica de transmissão, que os linfócitos necróticos apresentavam mudanças seqüenciais, tais como marginalização da cromatina, condensação do núcleo e fagocitose por macrófagos, que contêm os remanescentes celulares. Esses achados são característicos da apoptose em outros tecidos (Kerr, 1993) e em bursa de aves sujeitas a várias condições patológicas (Vasconcelos et al., 1996).
As porcentagens médias de parênquima das BF das aves dos grupos tratado e residual foram ligeiramente menores que as do grupo controle, embora sem diferenças significativas (P>0,05) (Tab.1). Como no presente estudo foi utilizada uma dose subletal (2,64 mg/kg) da toxina T-2 e por curto período experimental, presume-se que não houve tempo suficiente para o desencadeamento de lesões mais intensas que pudessem alterar significativamente a proporção de parênquima. Pode-se considerar ainda que, com o número de unidades experimentais utilizado nas obtenção dos valores médios de porcentagem de parênquima, não se tenha logrado dados tão expressivos que permitissem distinguir, com sucesso, as diferenças estatísticas entre os grupos.
As porcentagens médias de parênquima, tanto do grupo controle quanto do tratado, só foram significativamente menores aos 7 dias, quando comparadas com os demais períodos (Tab.1). Isso não chega a surpreender, pois naquele período o parênquima (tecido linfóide) está iniciando sua fase de crescimento rápido. As células da BF de pintos de um dia de idade são ainda relativamente imaturas (Rodak et al., 1969), atingindo sua maturidade e crescimento a partir da primeira semana (Glick, 1956).
Os valores médios da razão parênquima:estroma (P:E), avaliados pelo teste de Kruskal-Wallis, confirmam as assertivas feitas acima. Aos 7 dias a P:E era menor (P<0,05), tanto no grupo controle como no tratado, do que aos 14 e 21 dias, demostrando que nesse período existe menor quantidade de tecido linfóide (Tab.2). Aos 14 dias foi observada redução significativa da P:E dos grupos tratado e residual, quando comparados com o controle, já demonstrando o efeito da toxina T-2 sobre a BF.
Fato surpreendente é que aos 21 dias só o grupo residual apresentou P:E significativamente menor do que o grupo controle (Tab.2). Essa observação sugere que a hipotrofia linfóide foi mais acentuada nesse grupo e mais evidente nesse período. Coincidentemente, as lesões histológicas também mostraram-se mais pronunciadas nas BF do grupo residual. Entretanto, Haynes et al.(1980) relatam que a toxina T-2 administrada continuamente a camundongos causa depleção medular menos intensa à sexta semana do que à terceira. Isso, provavelmente, é devido à diminuição da susceptibilidade dos camundongos aos efeitos tóxicos sobre a medula óssea ou a uma resposta regenerativa ou adaptativa da medula. Assim, especula-se se os efeitos mais acentuados da T-2 no grupo residual não seriam por falha de regeneração da BF.
Como pode ser observado na Tab.3, os índices apoptóticos dos grupos avaliados aos 7 dias não diferiram entre si. Aos 14 dias, os índices apoptóticos das BF dos grupos tratado e residual foram estatisticamente maiores do que os do grupo controle (P<0,05). Já aos 21 dias, embora as médias do índice apoptótico tenham sido discretamente maiores nos grupos tratado e residual, não foi observada diferença estatística entre os grupos (P<0,05).
É interessante salientar que aos 14 dias a menor relação parênquima:estroma nos grupos tratado e residual quando comparados com o grupo controle ocorre concomitantemente com um índice apoptótico significativamente maior, sugerindo o envolvimento da apoptose no mecanismo da depleção linfóide provocada pela toxina T-2.
A técnica de TUNEL confirmou a ocorrência de apoptose pela marcação positiva de células com morfologia sugestiva nos campos analisados. A maioria das marcações positivas localizava-se esparsamente no parênquima ou em lacunas correspondentes aos espaços vazios descritos nos cortes corados por HE e MGP.
A fragmentação internucleossômica do DNA é considerada característica de apoptose (McConkey et al., 1990). A eletroforese em gel de agarose do DNA extraído da bolsa de Fabrício das aves dos grupos tratado e residual mostrou o clássico padrão em "escada", indicando a fragmentação internucleossômica do genoma. No grupo controle tal fragmentação do genoma não ficou evidente. Fragmentos de DNA, correspondentes a um até cinco nucleossomas, foram identificados como bandas pela eletroforese em gel, tanto no grupo residual como no tratado. As bandas presentes no grupo residual mostraram-se mais intensas, indicando maior fragmentação. Sabe-se que quanto mais intensa é a apoptose, maior será o número de bandas formadas, isso pelo baixo peso molecular do DNA fragmentado. Tudo confirma o envolvimento da apoptose na depleção linfóide provocada pela T-2. Por outro lado, as bandas evidenciadas no grupo tratado, apesar de intensas, mostravam "rastros" de DNA entre elas, indicando alguma fragmentação aleatória do genoma, devido provavelmente à ocorrência de necrose.
No presente estudo, ficou demonstrado que a toxina T-2, na dose de 2,64 mg/kg, causa depleção linfóide e redução da porcentagem de parênquima e da razão parênquima:estroma na BF, associadas ao aumento do índice apoptótico aos 14 dias. Bioquimicamente foi constatada fragmentação internucleossômica do DNA e, pela imuno-histoquímica, apoptose característica.
CONCLUSÃO
A toxina T-2, na dose de 2,64mg/kg, provoca depleção linfocitária na bolsa de Fabricius de frangos de corte, como conseqüência do aumento da apoptose das células linfóides.
- ANILKUMAR, T.V., SARRAF, C.E., ALISON, M.R. The biology and pathology of programmed cell death. Vet. Hum. Toxicol., v.34, p.251-254, 1992.
- ARAI, S., KOWADA, T., TAKEHANA, K. et al. Apoptosis in the chicken bursa of Fabricius induced by X-irradiation. J. Vet. Med. Sci., v.58, p.1001-1006, 1996.
- BALDISSERA, M.A., SANTURIO, J.M., SILVA, J.B. et al. Aflatoxinas, ocratoxina A e zearalenona em grăos e raçőes para consumo animal no Sul do Brasil. Cięnc. Tecnol. Alim, v.12, p.72-82, 1992.
- CHI, M.S., MIROCHA, C.J., KURTZ, H.J. Subacute toxicity of T-2 toxin in broiler chicks. Poult. Sci., v.56, p.306-313, 1977.
- COHEN, J.J. Programmed cell death in the immune system. Adv. Immunol., v.50, p.55-85, 1991.
- GAVRIELI, Y., SHERMAN, Y., BEM-SASSON, S. Identification of programmed cell death in situ via specific labeling of nuclear DNA fragmentation. J. Cell. Biol., v.119, p.493-501, 1992.
- GLICK, B. Normal growth of the bursa of Fabricius in chickens. Poult. Sci., v.35, p.843-851, 1956.
- GRUBER, J., SGONC, R., HU, Y.H. et al. Thymocyte apoptosis induced by elevated endogenous corticosterone levels. Eur. J. Immunol, v.24, p.1115-1121, 1994.
- HAYNES, M.A., BELLAMY, J.E.C., SCHIEFER, H.B. Subacute toxicity of dietary T-2 toxin in mice: morphological and hematological effects. Can. J. Comp. Med., v.44, p.203-218, 1980.
- HIKCMAN, J.A., BOYLE, C.C. Apoptosis and cytotoxins. Br. Med Bull, v.52, p.632-643, 1997.
- HOERR, F.J., CARLTON, W.W., YAGEN, B. Mycotoxicosis caused by a single dose of T-2 toxin or diacetoxyscirpenol in broiler chickens. Vet. Pathol., v.18, p.652-664, 1981.
- HOERR, F.J., CARLTON, W.W., YAGEN, B. et al. Mycotoxicosis produced in broiler chickens by multiple doses of either T-2 toxin or diacetoxyscirpenol. Avian Pathol., v.11, p.369-383, 1982.
- HOLT, S., DELOARCH, R. In vitro effect of T-2 mycotoxin on the immune response of mice. Am. J. Vet. Res., v.49, p.1480-1484, 1988.
- KERR, J.F.R. Definition of apoptosis and overview of its incidence. Immunol. Rev., v.142, p.1-15, 1993.
- LI, J., SHIMIZU, T. Course of apoptotic changes in the rat gastric mucosa caused by oral administration of fusarenon-X. J. Vet. Med. Sci., v.59, p.191-199, 1996.
- LUNA, L.G. Manual of histology staining methods of the Armed Forces Institute of Pathology. 3 ed. New York: McGraw Hill, 1968. 258p.
- McCONKEY, D.J., HARTZELL, P., ORRENIUS, S. Rapid turnover of endogenous endonuclease activity in thymocytes: effects of inhibitors of macromolecular synthesis. Arch. Bioch. Bioph., v.278, p.284-287, 1990.
- NEIGER, R.D., JOHNSON, T.J., HURLEY, D.J. et al. The short-term effect of low concentrations of dietary aflatoxin and T-2 toxin on Mallard ducklings. Avian Dis., v.38, p.738-743, 1994.
- OSWEILER, G.D.p. Toxicologia veterinária. Porto Alegre: Artes Médicas, 1998.
- PROPHET, E.B., MELLS, B., ARRINGTON, J.B. et al. Laboratory method in histotechnology. Washington: American Registry of Pathology, 1992. 275p.
- RODAK, L., PROCHÁZKA, Z., KREJCÍ. Postembrional histological and histochemical changes in the bursa of Fabricius and spleen of chickens and their relationship to development of immunological competence. Br.Vet. J, v.125, p.183-194, 1969.
- ROSTAGNO, H.S., BARBARINO Jr., P., BARBOSA, W.A. Exigęncias nutricionais das aves determinadas no Brasil. In: SIMPÓSIO INTERNACIONAL SOBRE EXIGĘNCIAS NUTRICIONAIS DE AVES E SUÍNOS, 1996, Viçosa. Anais...Viçosa: UFV, 1996, p.361-388.
- SHARMA, J.M. Overview of the avian immune system. Vet. Immunol. Immunopathol, v.30, p.31-44, 1991.
- SHARMA, R. P. Immunotoxicity of mycotoxins. J. Dairy Sci., v.76, p.892-897, 1993.
- TERAO, K., KERA, K., YAZIMA, T. The effects of trichothecene toxins on the bursa of Fabricius in day-old chicks. Virchows Arch. B. Cell. Path., v.27, p.359-370, 1978.
- VASCONCELOS, A.C., MORO, L., DA SILVA, P.M. Apoptose ou morte celular programada e sua importância em patologia veterinária. Rev. Port. Cięnc. Vet., v.91, p.182-193, 1996.
- WYLLIE, A.H., KERR, J.F.R., CURRIE, A.R. Cell death: The significance of apoptosis. Int. Rev. Cytol., v.68, p.251-305, 1980.
Datas de Publicação
-
Publicação nesta coleção
08 Fev 2001 -
Data do Fascículo
Dez 2000
Histórico
-
Recebido
21 Set 2000