Resumos
Utilizaram-se 140 coelhos das raças Nova Zelândia Branco e Califórnia, com 60 dias de idade, de ambos os sexos, distribuídos em 14 tratamentos experimentais, com o objetivo de determinar a biodisponibilidade de zinco (Zn) de três fontes inorgânicas, óxido de zinco (OZ), sulfato de zinco (SZ) e carbonato de zinco (CZ) e uma orgânica, quelato de zinco (QZ) usados nas concentrações de 0, 50, 100, 150 e 200 ppm para determinação da curva padrão. O maior consumo de ração ocorreu nos tratamentos 50OZ e 100OZ e o menor nos tratamentos 200OZ, 100SZ, 200SZ e 200QZ (R²= 0,18). Para ganho de peso os melhores resultados foram para os tratamentos 50OZ, 100CZ, 200CZ, 100SZ, 200SZ, 100QZ e 200QZ; os tratamentos 0OZ e 100OZ apresentaram os menores resultados (R²=0,23). Para conversão alimentar os tratamentos 0OZ, 100OZ, 150OZ e 150SZ apresentaram os maiores valores e os menores foram para os tratamentos 200SZ, 200QZ, 200CZ, 100QZ e 100SZ, respectivamente (R²= 0,26). Para concentração de zinco no fígado os tratamentos 100OZ, 150OZ e 150SZ apresentaram os maiores valores, e 100CZ e 200CZ os menores. Não houve diferença com relação ao sexo, mas os animais Nova Zelândia Branco apresentaram maior deposição de zinco. Pelosresultados chegou-se à equação de regressão: Y Zn= 1,11 + 0,66 x1 + 0,55 x2 + 0,57 x3 + 0,56 x4 + 0,56 x5 (R² = 0,59).
Coelho; biodisponibilidade; zinco; fonte orgânica; fonte inorgânica
One hundred and forty 60-day-old New Zealand White and California rabbits of both sexes were used to determine bioavailability of different inorganic zinc sources, zinc oxide (ZO), zinc sulfate (ZS), and zinc carbonate (ZC), and an inorganic zinc source, zinc quelate (ZQ) in the concentrations of 0, 50, 100, 150 and 200 ppm. The standard curve was also determined. Consumption was higher for 50ZO and 100ZO diets, and lower for 200ZO, 100ZS, 200ZS and 200ZQ (R²= 0.18). Higher weight gains were observed for animals fed on 50ZO, 100ZC, 200ZC, 100ZS, 200ZS, 100ZQ and 200ZQ diets and lower for animals fed on 0ZO and 100ZO diets (R²= 0.23) Higher feed: weight gain ratios were observed for animals fed on 0ZO, 100ZO, 150ZO and 150ZS, and lower for rabbits fed on 200ZS, 200ZQ, 200ZC, 100ZQ and 100ZS diets (R²= 0.26). Rabbits fed on 100ZO, 150ZO and 150ZS diets showed the highest zinc concentrations, and 100ZC and 200ZC diets the lowest concentrations. No differences between sexes were observed but New Zealand White rabbits presented the highest zinc deposition. The equation to predict zinc concentration in the liver (<IMG SRC="/img/fbpe/abmvz/v54n6/a13img01.gif">) based on basal diet zinc consumption (x1), and zinc oxide (x2), zinc sulfate (x3) zinc carbonate (x4) and zinc quelate consumptions (x5) was estimated as <IMG SRC="/img/fbpe/abmvz/v54n6/a13img01.gif" > or = 1.11 + 0.66 x1 + 0.55 x2 0.57 x3 + 0.56 x4 + 0.56 x5 (R²= 0.59).
Rabbit; bioavailability; zinc; organic sources; inorganic source
Biodisponibilidade de diferentes fontes de zinco para coelhos
[Bioavailability of different Zinc sources for rabbits]
W.M. FerreiraI; S.G. CavalcanteI; A.P. NaranjoI; G.S. Santiago II
IEscola de Veterinária da UFMG
IIFaculdade de Veterinária da Universidade Estadual do Ceará
Endereço para correspondência Endereço para correspondência W.M. Ferreira S.G. Cavalcante A.P. Naranjo Caixa Postal 567 30123-970 Belo Horizonte, MG E-mail: waltermf@vet.ufmg.br
RESUMO
Utilizaram-se 140 coelhos das raças Nova Zelândia Branco e Califórnia, com 60 dias de idade, de ambos os sexos, distribuídos em 14 tratamentos experimentais, com o objetivo de determinar a biodisponibilidade de zinco (Zn) de três fontes inorgânicas, óxido de zinco (OZ), sulfato de zinco (SZ) e carbonato de zinco (CZ) e uma orgânica, quelato de zinco (QZ) usados nas concentrações de 0, 50, 100, 150 e 200 ppm para determinação da curva padrão. O maior consumo de ração ocorreu nos tratamentos 50OZ e 100OZ e o menor nos tratamentos 200OZ, 100SZ, 200SZ e 200QZ (R2= 0,18). Para ganho de peso os melhores resultados foram para os tratamentos 50OZ, 100CZ, 200CZ, 100SZ, 200SZ, 100QZ e 200QZ; os tratamentos 0OZ e 100OZ apresentaram os menores resultados (R2=0,23). Para conversão alimentar os tratamentos 0OZ, 100OZ, 150OZ e 150SZ apresentaram os maiores valores e os menores foram para os tratamentos 200SZ, 200QZ, 200CZ, 100QZ e 100SZ, respectivamente (R2= 0,26). Para concentração de zinco no fígado os tratamentos 100OZ, 150OZ e 150SZ apresentaram os maiores valores, e 100CZ e 200CZ os menores. Não houve diferença com relação ao sexo, mas os animais Nova Zelândia Branco apresentaram maior deposição de zinco. Pelosresultados chegou-se à equação de regressão: YZn= 1,11 + 0,66 x1 + 0,55 x2 + 0,57 x3 + 0,56 x4 + 0,56 x5 (R2 = 0,59).
Palavras-chave: Coelho, biodisponibilidade, zinco, fonte orgânica, fonte inorgânica
ABSTRACT
One hundred and forty 60-day-old New Zealand White and California rabbits of both sexes were used to determine bioavailability of different inorganic zinc sources, zinc oxide (ZO), zinc sulfate (ZS), and zinc carbonate (ZC), and an inorganic zinc source, zinc quelate (ZQ) in the concentrations of 0, 50, 100, 150 and 200 ppm. The standard curve was also determined. Consumption was higher for 50ZO and 100ZO diets, and lower for 200ZO, 100ZS, 200ZS and 200ZQ (R2= 0.18). Higher weight gains were observed for animals fed on 50ZO, 100ZC, 200ZC, 100ZS, 200ZS, 100ZQ and 200ZQ diets and lower for animals fed on 0ZO and 100ZO diets (R2= 0.23) Higher feed: weight gain ratios were observed for animals fed on 0ZO, 100ZO, 150ZO and 150ZS, and lower for rabbits fed on 200ZS, 200ZQ, 200ZC, 100ZQ and 100ZS diets (R2= 0.26). Rabbits fed on 100ZO, 150ZO and 150ZS diets showed the highest zinc concentrations, and 100ZC and 200ZC diets the lowest concentrations. No differences between sexes were observed but New Zealand White rabbits presented the highest zinc deposition. The equation to predict zinc concentration in the liver ( ) based on basal diet zinc consumption (x1), and zinc oxide (x2), zinc sulfate (x3) zinc carbonate (x4) and zinc quelate consumptions (x5) was estimated as
) based on basal diet zinc consumption (x1), and zinc oxide (x2), zinc sulfate (x3) zinc carbonate (x4) and zinc quelate consumptions (x5) was estimated as  = 1.11 + 0.66 x1 + 0.55 x2 0.57 x3 + 0.56 x4 + 0.56 x5 (R2= 0.59).
= 1.11 + 0.66 x1 + 0.55 x2 0.57 x3 + 0.56 x4 + 0.56 x5 (R2= 0.59).
Keywords: Rabbit, bioavailability, zinc, organic sources, inorganic source
INTRODUÇÃO
Dentre os microminerais reconhecidos nutricionalmente como importantes para os animais domésticos inclui-se o zinco (Zn). Sabe-se que vários fatores químicos, incluindo o potencial redox, o pH e a forma inicial dos microelementos, influenciam o curso da digestão e subseqüentemente a solubilidade e disponibilidade desses elementos (Madsen & Johnson, 1989).
Pesquisadores, ao usarem proteinados ou quelatos de diferentes minerais, têm demonstrado que a digestibilidade desses minerais orgânicos é superior à de seus semelhantes inorgânicos, sendo que um aminoácido (aa) específico, ao qual o mineral está quelatado, determina o tecido ou sistema enzimático para o qual se destina.
A característica de um mineral quelatado é a ligação entre um mineral da primeira série de transição da tabela periódica com um aa, por meio de uma ligação covalente coordenada, formando uma estrutura cíclica, que é estável e eletricamente neutra (Vandergrift, 1993), guardando proporção molar (metal:aa) de 1:1 até 1:3, preferencialmente 1:2 (Brown & Zeringue, 1994).
A essencialidade biológica do Zn refere-se a mecanismos homeostáticos que regulam sua absorção, captação celular, distribuição através dos compartimentos intracelulares e macromoléculas, bem como sua excreção. De 30 a 40% do Zn celular total está no núcleo, cerca de 50% está no citoplasma e suas organelas, e a quantidade remanescente na membrana e/ou parede celular (Vallee & Falchuk, 1993).
Em sistemas biológicos há muito pouco, se houver, Zn livre em solução. Ele é um cátion divalente que sob condições fisiológicas não sofre redução ou oxidação sendo, portanto, estável no meio biológico (Vallee & Falchuk, 1993). Está presente em muitos tecidos moles como músculos, cérebro, pulmões e coração. Nesses órgãos, a concentração de Zn é relativamente estável, ou não responde a quantidades de Zn dietético. Outros tecidos como ossos, testículos, sangue e pêlos tendem a refletir o grau de ingestão. As maiores concentrações no corpo são encontradas nos ossos, próstata e coróide do olho. O músculo esquelético, apesar de sua concentração moderada, possui a maior proporção de Zn do corpo (60%), em função de sua extensão. Juntamente com os ossos (tecido calcificado e medula), respondem por aproximadamente 90% de todo o metal do corpo. Fígado e medula possuem os maiores "pools" metabolicamente ativos (Cousins & Hempe, 1990).
O Zn distribui-se amplamente no corpo, porém os animais têm limitada capacidade de estocá-lo numa forma que seja rapidamente mobilizada para prevenir deficiências (Underwood, 1977). Em geral estoques prontamente disponíveis são muitos pequenos, como aparece nos casos de depressão dos valores séricos de Zn, quando ocorre deficiência por 24 horas, depois de ter sido trocada a dieta por uma de baixa concentração em Zn. A metalotioneína age como forma de estoque do metal no fígado, o que é confirmado quando de sua mobilização durante as necessidades metabólicas.
Tecidos com maiores taxas de absorção presumivelmente têm altas taxas correspondentes de renovação de Zn e talvez grande importância funcional. As taxas iniciais de absorção de uma dose ingerida são maiores no fígado, na medula, no osso, na pele, nos rins e no timo (McDowell, 1992).
Este trabalho foi realizado com o objetivo de determinar a biodisponibilidade de quatro fontes (três inorgânicas e uma orgânica) de zinco e estabelecer o nível mais adequado desse mineral para coelhos.
MATERIAL E MÉTODOS
Em cada tratamento experimental foram alocados 10 coelhos de raça Nova Zelândia Branco ou Califórnia, com 60 dias de idade, de ambos os sexos, com média de peso inicial de 1992,3± 213,3g, alojados e identificados individualmente em gaiolas de aço inoxidável.
Os animais receberam dieta basal (Tab. 1) de acordo com suas necessidades segundo De Blas (1989), constituída de milho, feno de alfafa, farelo de trigo e farelo de soja, sal, mistura vitamínico-mineral (livre de Zn) e um complemento constituído de uma das fontes de Zn e quantidade de sulfato de cobre (CuSO4) adequada para suprir as necessidades dos animais de acordo com Smith et al. (1997). O complemento foi diluído em caolim, que funcionou como inerte.
As fontes de Zn estudadas foram: óxido de zinco (ZnO) considerado como 100% disponível, sulfato de zinco (ZnSO4), carbonato de zinco (ZnCO3) e quelato de zinco (ZnQ), produto comercial com 10% de zinco (Bioplex de zinco (Alltech Agroindustrial do Brasil Ltda.)).
Os tratamentos experimentais consistiram na adição das fontes de zinco de forma a suprir os níveis a serem estudados, como se segue: 0OZ - 0 ppm de zinco, 50OZ - 50 ppm de zinco proveniente do ZnO, 100OZ - 100 ppm de zinco proveniente do ZnO, 150OZ - 150 ppm de zinco proveniente do ZnO, 200OZ - 200 ppm de zinco proveniente do ZnO, 100CZ - 100 ppm de zinco proveniente do ZnCO3, 150CZ - 150 ppm de zinco proveniente do ZnCO3, 200CZ - 200 ppm de zinco proveniente do ZnCO3, 100SZ - 100 ppm de zinco proveniente do ZnSO4, 150SZ - 150 ppm de zinco proveniente do ZnSO4, 200SZ - 200 ppm de zinco proveniente do ZnSO4, 100QZ- 100 ppm de zinco proveniente do ZnQ a 10%, 150QZ - 150 ppm de zinco proveniente do ZnQ a 10%, 200QZ - 200 ppm de zinco proveniente do ZnQ a 10%.
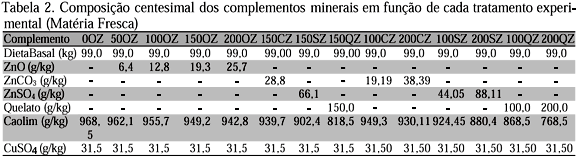
A composição centesimal dos complementos é apresentada na Tab. 2.
As dietas foram peletizadas e oferecidas aos animais na base de 100g de ração/cabeça/dia e a água desmineralizada foi fornecida à vontade. Na condução do experimento adotou-se um período de adaptação de sete dias, e o período experimental teve a duração de 30 dias.
Ao final dos experimentos, determinaram-se ganho de peso (GP), consumo de ração (CR) e conversão alimentar (CA). Todos os animais foram sacrificados por sangramento na jugular para se obterem amostras de fígado total. O material foi acondicionado em sacos plásticos devidamente identificados e congelados para posterior processamento e análises.
As amostras de fígado foram trituradas utilizando-se gral e pistilo para aumentar sua superfície de contato. Desse material pesaram-se aproximadamente 5g em cadinho de porcelana, utilizados apenas para análises de microminerais, seguindo-se o procedimento recomendado pelo Laboratório Nacional de Referência Animal, que consiste em se adicionar à amostra 2,5ml de nitrato de magnésio [Mg(NO3)2.6 H2O] a 66,6% (com o objetivo de homogeinizá-la com relação à concentração, já que ela não necessariamente está distribuída de maneira igual pelo tecido, antes de se proceder a digestão ácida). Após esse preparo, a amostra foi seca em capela aquecedora, provida de exaustor, a 100oC e em seguida incineradas a 500oC por 16 horas. Depois de resfriadas foram adicionados 2ml de ácido nítrico (HNO3) a 50% (com a finalidade de clarear as cinzas resultantes), posteriormente levada à chapa aquecedora para evaporação dessa solução, retornando à mufla por mais duas horas, a 550oC. As cinzas finais foram dissolvidas com 10ml de ácido clorídrico (HCl) 1N, e em seguida lidas no espectrofotômetro de absorção atômica Perkin Elmer 403 a 324,7nm.
As análises estatísticas foram realizadas utilizando-se o delineamento inteiramente ao acaso, usando-se o pacote estatístico Statistical... (1985). O teste Duncan a 5% de probabilidade foi usado para comparação de médias.
Mediante regressão linear múltipla, usando-se a concentração do mineral no fígado como variável dependente (Y) e o consumo de mineral da ração basal proveniente dos sais-teste como variáveis independentes (X), foi obtida uma equação do tipo Y= a + b1x1 + b2x2 + b3x3 + b4x4 + b5x5, sendo x1= consumo de mineral da ração basal; x2= consumo de Zn do ZnO; x3= consumo de Zn do ZnSO4 ; x4= consumo de Zn do ZnCO3 e x5= consumo de Zn do quelato.
A biodisponibilidade foi calculada pela relação dos coeficientes de regressão (slope ratio technique), considerando-se o Zn do ZnO como 100% disponível. Ex.: b4 (ZnO) / b2 (ZnSO4) x 100 = % Zn-DIS.
RESULTADOS E DISCUSSÃO
Os dados de consumo de ração, ganho de peso e conversão alimentar são apresentados na Tab. 3.
Os tratamentos com melhor consumo da ração (CR) foram 0OZ, 50OZ e 100OZ, enquanto que o menor consumo foi observado nos tratamentos 200OZ, 200SZ e 200QZ. Para essa variável, a análise estatística apontou R2 igual a 0,18.
Para ganho de peso (GP) observou-se que sete tratamentos mostraram melhores resultados, isto é, 50OZ, 100CZ, 200CZ, 100SZ, 200SZ, 100QZ e 200QZ. Os tratamentos 0OZ e 100OZ foram os de menor ganho de peso. O R2 foi de 0,23. Pimentel et al. (1991), em experimento com aves, observaram que a adição do mineral não teve efeito marcante sobre o GP, pois a dieta já provia um mínimo suficiente do mineral para atender suas necessidades, diferente do resultado encontrado neste trabalho.
O índice de conversão alimentar (CA) foi melhor para o grupo 200SZ e os maiores valores foram os dos tratamentos 0OZ e 100OZ; valores médios ocorreram nos outros grupos. O R2 foi de 0,26. Comparando-se estes resultados com os obtidos por Hossain & Bertechini (1993), este índice apresentou valores bem mais elevados apesar de a idade dos animais ser semelhante.
Hossain et al. (1992), utilizando ZnO com várias concentrações de Zn (0, 10, 20, 90 e 270ppm), não encontraram diferenças significativas para GP, mas CR e CA foram afetados. No trabalho de Hossain & Bertechini (1993) o maior GP e a melhor CA foram encontrados com a dieta contendo 90ppm de Zn
Os resultados das análises de concentração de Zn (ppm) nas amostras de fígado encontram-se na Tab. 4. Eles estão expressos na base de matéria seca.
Observa-se que a maior deposição hepática de Zn ocorreu nos tratamentos 100OZ, 150OZ e 150SZ mas estatisticamente semelhantes a dos grupos 200OZ e 150CZ. A menor deposição de Zn foi observada nos tratamentos 100CZ e 200CZ que não diferiram dos tratamentos 100SZ, 200SZ, 100QZ e 200QZ. Os resultados dos demais tratamentos são valores intermediários entre estes. Não se observou efeito linear da concentração do Zn sobre a deposição no fígado.
Wedekin et al. (1992) trabalharam com concentrações de 0, 250, 500 e 750ppm de ZnSO4, ZnO e Zn-Metionina e não encontraram respostas lineares para nenhuma das fontes pesquisadas.
Quanto à fonte de Zn utilizada, pode-se dizer que ZnO apresentou maior deposição no fígado, independente do nível utilizado, comparado com as outras fontes que mostraram resultados variáveis.
Hossain et al. (1992), ao utilizarem ZnO em diversas concentrações, notaram diferenças na deposição do mineral nos distintos tecidos estudados, inclusive no fígado, determinando que as exigências de Zn situavam-se em 106ppm.
Quando as reservas hepáticas de Zn foram relacionadas à raça dos animais (Tab. 5), os animais Nova Zelândia Branco apresentaram maior quantidade de Zn do que os da raça Califórnia.
O efeito das fontes de Zn e dos diferentes níveis desse elemento sobre a concentração de Zn no fígado encontra-se na Tab. 6.
No nível de 150ppm houve maior depósito de Zn no fígado para as fontes sulfato, carbonato e quelato. Para a fonte ZnO, a concentração de Zn no fígado não foi afetada pelos níveis utilizados.
Ao comparar as fontes dentro de um mesmo nível, observa-se maior concentração com óxido de zinco para os níveis de 100 e 200ppm e para o nível de 150ppm não houve diferença entre as fontes testadas para a concentração do mineral no fígado.
A equação de regressão múltipla obtida por meio dos dados de consumo de Zn nas dietas teste é a seguinte:
YZn = 1,11 + 0,66 x1 + 0,55 x2 + 0,57 x3 + 0,56 x4 + 0,56 x5, R2 = 0,59.
A partir dessa equação pode-se dizer que a biodisponibilidade das fontes de Zn foram: sulfato 103,6%, óxido 100%, carbonato 102,7% e do quelato 102,4%.
CONCLUSÕES
Com base nos dados obtidos pode-se concluir que a fonte de Zn na forma de óxido (ZnO), apesar de ser melhor depositada no fígado em todos níveis estudados e ser considerada como fonte padrão na literatura, não mostrou efeito quanto à biodisponibilidade. Considerando a concentração do Zn no fígado pode-se dizer que o nível de 150ppm foi mais bem utilizado, independente da fonte analisada. Como a biodisponibilidade de Zn das fontes avaliadas foi semelhante, pode-se escolher aquela que ao atingir o objetivo nutricional satisfaça também o aspecto econômico na exploração cunícola.
REFERÊNCIAS BIBLIOGRAFICAS
Recebido para publicação em 4 de junho de 2001
Recebido para publicação, após modificações, em 13 de janeiro de 2002
- BROWN, T.F.; ZERINGUE, L.K. Laboratory evaluations of solubility and structural integrity of complexed and chelated trace mineral supplements. J. Dairy Sci., v.77, p.181-189,1994.
- COUSINS, R.J.; HEMPE, J.M. Zinc. In: BROWN, M.L. (Ed.) Present knowledge in nutrition 6.ed. Washington: International Life Science Institute, 1990. 532p.
- DeBLAS, C. Alimentación del conejo 2.ed. Madrid: Ediciones Mundi-Prensa, 1989. 175p.
- HOSSAIN, S.M.; BERTECHINI, A.G. Requirement of zinc for growing rabbits. Arq. Bras. Med. Vet. Zootec., v.45, p.323-329, 1993.
- HOSSAIN, S.M.; FERREIRA, R.G.; VALE, A.R. et al. Efeitos de vários níveis de zinco no desempenho e composição dos tecidos de coelhos na fase de crescimento. In: REUNIÃO ANUAL DA SOCIEDADE BRASILEIRA DE ZOOTECNIA, 29, Lavras. Anais.. Lavras, SBZ, 1992. p.301.
- MADSEN, F.C.; JOHNSON, B. Chemistry of essential trace elements studied during diet preparation, digestion. Feedstuffs, p13-16, 1989.
- MCDOWELL, L.R. Minerals in animal and human nutrition San Diego: Academic, 1992. 544p.
- PIMENTEL, J.L.; COOK, M. E.; GREGER, J. L. Research note: bioavailability of zinc-methionine for chicks. Poult. Sci., v.70, p.1637-1639, 1991.
- SMITH, J.W; TOKACH, M.D.; GOODBAND, R.D. et al. Effects of the interrelationship between zinc oxide and copper sulfate on growth performance of early-weaned pigs. J. Anim. Sci., v.75, p.1861-1866, 1997.
- STATISTICAL analysis system users guide: statistics. 5.ed. Cary: SAS Institute Inc., 1985.
- UNDERWOOD, E.J. Trace elements in animal and human nutrition 4.ed. London: Academic, 1977. 545p.
- VALLEE, B.L.; FALCHUK, K.H. The biochemical basis of zinc physiology. Physiol. Rev., v.73, p.79-118, 1993.
- VANDERGRIFT, B. The role of mineral proteinates in immunity and reproduction. What do we really know about them? Biotechnology in the Feed Industry, 9. Proceedings 1993. 419p.
- WEDEKIND, K.J.; HORTIN, A.E.; BAKER, D.H. Methodology for assessing zinc bioavailability: efficacy estimates for zinc-methionine, zinc sulfate and zinc oxide. J. Anim. Sci., v.70, p.178-187, 1992.
Datas de Publicação
-
Publicação nesta coleção
25 Mar 2003 -
Data do Fascículo
Dez 2002
Histórico
-
Recebido
04 Jun 2001 -
Revisado
13 Jan 2002