Resumos
Verificou-se a influência da proteína quinase C (PK-C) no reinício e na progressão da meiose em oócitos bovinos, determinando se as células do cumulus são mediadoras da PK-C na regulação da maturação dos oócitos. Complexos cumulus-oócitos (CCO) e oócitos desnudos (OD), distribuídos aleatoriamente em seis tratamentos (T) com base na presença de um ativador da PK-C (PMA) (T1 e T2), de um forbol éster incapaz de ativar a PK-C (4alfa-PDD-controle) (T3 e T4) ou de apenas o meio básico (TCM-199-controle) (T5 e T6), foram cultivados por 7, 9, 12, 18 e 22 horas. A percentagem de rompimento da vesícula germinativa no grupo cultivado com PMA foi maior do que nos dois grupos controle, com e sem células do cumulus. O cultivo de CCO e OD por 12 e 18 horas demonstrou que a PK-C influencia a progressão para os estádios de metáfase I (MI) e metáfase II (MII) de maneira dependente das células do cumulus. Nos períodos de 9 e 22 horas, não foi possível observar diferença entre os grupos quanto aos diferentes estádios de maturação. A ativação da PK-C acelera o reinício da meiose independentemente das células somáticas e acelera a progressão até os estádios de MI e MII na dependência das células do cumulus.
bovino; maturação nuclear de oócitos; PK-C
The aim of this study was to evaluate the effect of protein kinase C (PK-C) on the meiotic resumption and progression in bovine oocyte, and to determine if the cumulus cells mediate the PK-C action in the regulation of bovine oocyte nuclear maturation. Cumulus-oocyte complexes (COC) and denuded oocytes (DO), randomly allotted to 6 treatments (T) based on the presence of an activator of PK-C (PMA) (T1 and T2), or a phorbol ester unable to activate PK-C (4alphaPDD-control) (T3 and T4) or a basic culture medium (T5 and T6), were cultivated for 7, 9, 12, 18 and 22 hours. The percentage of germinal vesicle breakdown (GVBD) was higher when the oocytes were cultured with PMA than in the control groups with and without cumulus cells. However, PK-C was dependent of cumulus cells to affect the progression to the stages of metaphase I (MI) and metaphase II (MII) at 12 and 18 hours of culture. At 9 and 22 hours, no difference among groups was detected. PK-C accelerates the meiotic resumption independently of the somatic cells but depends on cumulus cells for the progression to the stages of MI and MII.
bovine; oocyte nuclear maturation; PK-C
MEDICINA VETERINÁRIA
Interação entre células do cumulus e atividade da proteína quinase C em diferentes fases da maturação nuclear de oócitos bovinos
Interaction between cumulus cells and the activity of protein kinase C at different stages of bovine oocyte nuclear maturation
A.C. Bertagnolli; P.B.D. Gonçalves* * Autor para correspondência E-mail: bayard@biorep.ufsm.br ; I.C. Giometti; L.F.S. Costa; J.F.C. Oliveira; I.D.V. Gonçalves; K.P. Barreto; I.P. Emanuelli; L.F.K. Borges
Laboratório de Biotecnologia e Reprodução Animal BioRep Departamento de Clínica de Grandes Animais Universidade Federal de Santa Maria Faixa de Camobi, km 9 97105-900 - Santa Maria, RS
RESUMO
Verificou-se a influência da proteína quinase C (PK-C) no reinício e na progressão da meiose em oócitos bovinos, determinando se as células do cumulus são mediadoras da PK-C na regulação da maturação dos oócitos. Complexos cumulus-oócitos (CCO) e oócitos desnudos (OD), distribuídos aleatoriamente em seis tratamentos (T) com base na presença de um ativador da PK-C (PMA) (T1 e T2), de um forbol éster incapaz de ativar a PK-C (4a-PDD-controle) (T3 e T4) ou de apenas o meio básico (TCM-199-controle) (T5 e T6), foram cultivados por 7, 9, 12, 18 e 22 horas. A percentagem de rompimento da vesícula germinativa no grupo cultivado com PMA foi maior do que nos dois grupos controle, com e sem células do cumulus. O cultivo de CCO e OD por 12 e 18 horas demonstrou que a PK-C influencia a progressão para os estádios de metáfase I (MI) e metáfase II (MII) de maneira dependente das células do cumulus. Nos períodos de 9 e 22 horas, não foi possível observar diferença entre os grupos quanto aos diferentes estádios de maturação. A ativação da PK-C acelera o reinício da meiose independentemente das células somáticas e acelera a progressão até os estádios de MI e MII na dependência das células do cumulus.
Palavras-chave: bovino, maturação nuclear de oócitos, PK-C
ABSTRACT
The aim of this study was to evaluate the effect of protein kinase C (PK-C) on the meiotic resumption and progression in bovine oocyte, and to determine if the cumulus cells mediate the PK-C action in the regulation of bovine oocyte nuclear maturation. Cumulus-oocyte complexes (COC) and denuded oocytes (DO), randomly allotted to 6 treatments (T) based on the presence of an activator of PK-C (PMA) (T1 and T2), or a phorbol ester unable to activate PK-C (4aPDD-control) (T3 and T4) or a basic culture medium (T5 and T6), were cultivated for 7, 9, 12, 18 and 22 hours. The percentage of germinal vesicle breakdown (GVBD) was higher when the oocytes were cultured with PMA than in the control groups with and without cumulus cells. However, PK-C was dependent of cumulus cells to affect the progression to the stages of metaphase I (MI) and metaphase II (MII) at 12 and 18 hours of culture. At 9 and 22 hours, no difference among groups was detected. PK-C accelerates the meiotic resumption independently of the somatic cells but depends on cumulus cells for the progression to the stages of MI and MII.
Keywords: bovine, oocyte nuclear maturation, PK-C
INTRODUÇÃO
Oócitos de folículos antrais removidos do ambiente folicular e cultivados in vitro em meio adequado reiniciam espontaneamente a divisão meiótica (Milovanov e Sirard, 1994). Durante o processo de crescimento até a aquisição de competência para o reinício da meiose, o oócito sofre diversas mudanças bioquímicas, estruturais e citoesqueléticas importantes à maturação, fecundação e sustentação do desenvolvimento embrionário. No entanto, o percentual de embriões que se desenvolve a partir de oócitos maturados e fecundados in vitro é inferior àquele obtido in vivo, isso em decorrência de problemas no processo de maturação citoplasmática, também denominada capacitação oocitária.
O tempo necessário para a conclusão da primeira divisão meiótica in vitro de oócitos bovinos varia de 18 a 24 horas (Süss et al., 1988; Hytel et al., 1989). O primeiro evento da maturação nuclear é o processo de rompimento da vesícula germinativa (RVG) que ocorre, in vitro, entre sete e 12 horas após o início do cultivo, enquanto a metáfase I (MI) ocorre entre 12 e 15 horas. A anáfase I (AI) e a telófase I (TI) ocorrem entre 15 e 18 horas e a metáfase II (MII), a partir de 18 horas. Mais de 95% dos oócitos apresentam bloqueio em MII entre 22 e 24 horas de cultivo (Hytel et al., 1989; Vignola et al., 1994).
Essas mudanças são reguladas por fosforilação e desfosforilação de proteínas, envolvendo diferentes quinases e fosfatases (Milanov e Sirard, 1994; Levesque e Sirard, 1995). O reinício do processo meiótico ocorre com o incremento na atividade do fator promotor de maturação (MPF) e da proteína quinase mitogênica ativada (MAPK). Para que o oócito avance do estádio de metáfase e entre em interfase, deve ocorrer redução dos níveis de MPF e MAPK (Yang, 1997). Após a fase de maturação os oócitos são mantidos em MII, provavelmente por ação de fatores citostáticos (CSF), até ocorrer a fecundação ou ativação partenogenética (Colledge et al., 1994).
A proteína quinase C (PK-C) é uma serina-treonina proteína quinase que participa de vários processos celulares, incluindo a regulação do ciclo de transição celular da maturação de oócitos (Gonçalves et al., 1994; Vignola, 1995; Rose-Hellekant e Bavister, 1996) e a transição de oócito maduro a zigoto (Colonna et al., 1997). A implicação da PK-C na maturação do oócito tem sido demonstrada em diversas espécies animais. Tem sido sugerido que ela inibe a divisão meiótica em oócitos de camundongo (Bornslaeger et al., 1986; Gonçalves e Graves, 1992; Lu et al., 2001) e de Xenopus (Stith et al., 1992), porém, deve ser ativada para que o oócito de camundongo passe a MII (Colonna et al., 1997). A PK-C estimula a maturação nuclear de oócitos em ratos (Aberdam e Dekel, 1985), rã (Rana dybowskii) (Kwon e Lee, 1991), peixes (killifish) (Cerdá et al., 1998), bovinos (Vignola, 1995; Montagner et al., 1999; Rose-Hellekant e Bavister, 1996) e suínos (Su et al., 1999), mas não está envolvida no reinício da meiose de oócitos de corvina (Patiño et al., 2003).
Estudos utilizando neomicina e estaurosporina (inibidores da hidrólise de compostos fosfatados) não revelaram influência significativa da PK-C na maturação de oócitos bovinos (Homa, 1991). No entanto, substâncias que ativam a PK-C, como PMA (4a -phorbol 12-myristate 13-acetate) e o ativador natural DiC8 (diacilglicerol sintético, permeável à membrana celular), estimulam de maneira dose-dependente a retomada da meiose (Hernandez et al., 1995; Mondadori et al., 1999). A ativação da PK-C com PMA ou DIC8 por 24 horas acelera a maturação, caracterizada pelo RVG e pela formação dos pró-núcleos em presença de PMA (Vignola, 1995). Segundo Vignola (1995), a ativação da PK-C estimula o RVG, que alcança índices de 93,9% às sete horas de maturação, enquanto que sem PMA esse índice é de 59,6%. Além disso, Vignola (1995) demonstrou que a ativação da PK-C durante 18 horas aumenta proporção de oócitos que atingem o estádio de MII. Rose-Hellekant e Bavister (1996), utilizando um sistema que mimetiza as condições in vivo, determinaram que a ativação da PK-C participa do mecanismo hormonal relacionado com o reinício da meiose em oócitos bovinos.
As células do complexo cumulus-oócito (CCO) exercem importante papel na regulação da maturação do oócito e a retirada dessas células reduz significativamente o desenvolvimento embrionário subseqüente (Zhang et al., 1995; Shioya et al., 1998). Há evidência suficiente da importância da PK-C no processo de maturação de oócitos. No entanto, ainda não foi determinado se a ação da PK-C é mediada por essas células e se ela tem função nos diferentes estádios do processo de maturação do oócito bovino. Assim, este trabalho foi realizado com o objetivo de verificar a influência da proteína quinase C (PK-C) no reinício e progressão da meiose em oócitos bovinos e determinar se as células do cumulus são mediadoras de sua ação.
MATERIAL E MÉTODOS
Ovários obtidos em abatedouro localizado a 22km do laboratório foram transportados em garrafas térmicas com solução de cloreto de sódio a 0,9% e à temperatura de 30ºC. No laboratório, os ovários foram lavados com solução de cloreto de sódio (0,9%) e os folículos de 2 a 8mm de diâmetro aspirados a vácuo (3mm Hg) com agulha 20G, e transferidos para tubo de ensaio. Os oócitos coletados foram mantidos em liquido folicular até o momento da seleção. Foram selecionados com estereomicroscópio os oócitos completamente rodeados por, no mínimo, três camadas de células do cumulus e com ooplasma de coloração marrom clara e homogênea. A seleção e maturação dos oócitos foi realizada no meio livre de proteína TCM-199, com sais de Earle e contendo 0,685mM de L-glutamina, 25mM de HEPES, 2,2g/l de bicarbonato de sódio, 0,22mM de piruvato de sódio, 100UI de penicilina, 50µg/ml de estreptomicina e 1mg/ml de álcool polivinílico (PVA). A maturação foi feita em estufa a 39ºC, com atmosfera de 5% de CO2 e 98% de umidade. O período decorrido desde a retirada dos ovários até o cultivo foi de aproximadamente três horas.
Um total de 1899 oócitos foi aleatoriamente distribuído nos seguintes grupos: 1) PMA-C: PMA1 1 PMA = forbol éster ativador da PK-C + complexo cumulus-oócito; 2) PMA-D: PMA + oócito desnudo; 3) 4a -PDD-C: 4a -PDD + complexo cumulus-oócito; 4) 4a -PDD-D: 4a -PDD2 2 4a -PDD = 4-forbol 12-13 didecanoetate incapaz de ativar a PK-C + oócito desnudo; 5) TCM-C: TCM3 3 TCM = meio de cultivo + complexo cumulus-oócito e 6) TCM-D: TCM + oócito desnudo. Nos grupos com oócitos desnudos (OD), as células do cumulus foram retiradas pelo processo de agitação mecânica (em vórtex) durante três minutos antes da maturação; nos demais grupos o mesmo processo foi realizado após o cultivo. Os oócitos foram cultivados por períodos de 7, 9, 12, 18 e 22 horas. Ao final de cada período de cultivo, todos os oócitos foram fixados em solução de ácido acético: metanol (1:3). Após 12 horas de fixação, os oócitos foram corados com 1% de lacmóide com 45% de ácido acético em PBS (phosphate bufered saline). A observação do estádio de maturação nuclear foi realizada ao microscópio óptico de contraste de fase com aumento de 1000x, segundo as características descritas por Vignola et al. (1994).
O delineamento experimental utilizado foi o de blocos inteiramente ao acaso. Os diferentes tratamentos foram realizados simultaneamente, sendo cada repetição considerada um bloco. Os resultados em percentagem foram transformados pelo PROC RANK (Conover e Iman, 1981) com o programa estatístico SAS, para a aplicação de testes paramétricos na análise dos resultados. O modelo estatístico utilizado foi: gij=µ+ai+bj+eii, em que: gij é a variável dependente,µ é a constante comum para todas as observações, ai é o efeito dos tratamentos, bj é o efeito dos blocos, e eii é o efeito do resíduo.
RESULTADOS E DISCUSSÃO
O cultivo de 564 oócitos por um período de sete horas em seis repetições mostrou que o PMA acelerou o reinício da meiose independente da presença das células do cumulus. A percentagem de oócitos que atingiu o estádio de RVG no grupo cultivado com PMA foi significativamente maior do que seu antagônico 4a -PDD, com (P= 0,0032) ou sem (P= 0,0044) células do cumulus, e do que o grupo-controle negativo só com TCM, com (P= 0,0008) ou sem células do cumulus (P= 0,0002). Isso demonstra que realmente as células do cumulus não são necessárias para mediar a ação da PK-C (Fig. 1). Apesar da presença das células do cumulus ser importante para o processo de maturação e competência no desenvolvimento embrionário (Zhang et al., 1995) e sua ausência acelerar o RVG em oócitos bovinos (Fissore et al., 1996), elas não foram essenciais para a ação da PK-C, na mudança da cinética da meiose durante o início do processo de maturação do oócito.
A percentagem média de oócitos que estavam em RVG, após sete horas de cultivo, ficou entre 1,7% e 28,6% nos vários tratamentos (Fig. 1). Essa baixa percentagem em oócitos de bovinos foi atribuída ao curto período de maturação, tendo em vista que esse estádio da divisão meiótica inicia-se às sete horas de cultivo in vitro (Hytel et al., 1989; Vignola et al., 1994). Se os oócitos tivessem sido cultivados por mais tempo, provavelmente não seria observada diferença entre os grupos, já que com nove horas 51,4% a 69,7% (n=403) dos oócitos atingiram o estádio de RVG, independente do tratamento (Fig. 2).
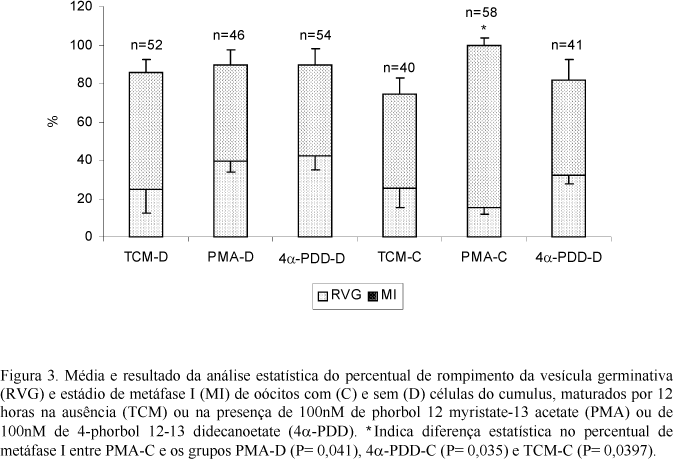
Às 12 horas (n=291), quando o estádio de MI começa a ser observado em oócito bovino cultivado in vitro, a ativação da PK-C resultou em uma percentagem de 84,8% de oócitos em MI, comparado com apenas 49,6% no grupo sem ativação (P= 0,035) e 49,2% no grupo-controle (P= 0,0397), com células do cumulus. No entanto, essa diferença não foi notada nos oócitos desnudos (Fig. 3). Estes resultados evidenciam que a ação da PK-C no início da MI é mediada pelas células do cumulus, diferentemente do estádio de RVG.
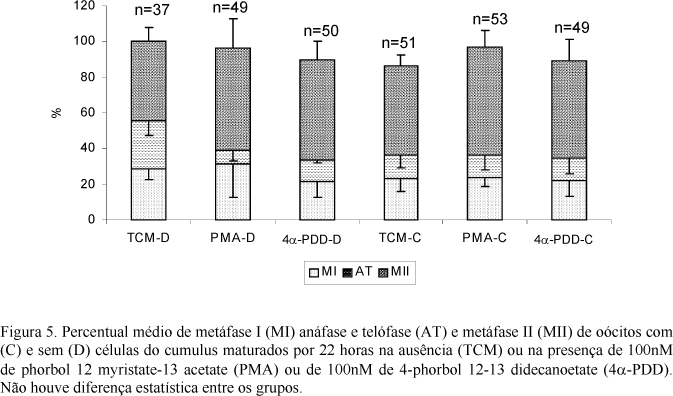
De maneira similar, às 12 horas de cultivo (n=352), a ativação da PK-C por 18 horas (Fig. 4) proporcionou incremento significativo na percentagem de oócitos no estádio de MII, quando as células do cumulus estavam presentes, em comparação ao 4a-PDD-C (P= 0,0052) e ao TCM-C (P= 0,05). Essa diferença não foi observada às 22 horas (n=289) após ativação da PK-C (Fig. 5).
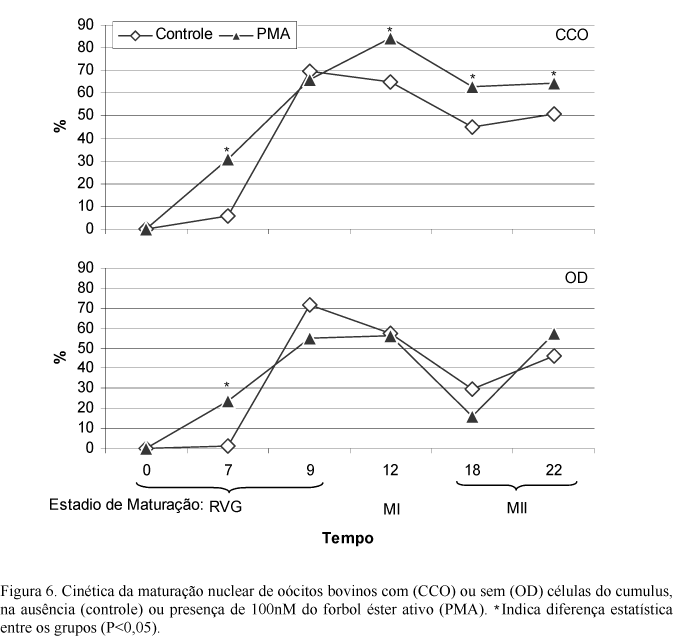
A PK-C é capaz de alterar a cinética da maturação de oócitos (Fig. 6) nos mesmos períodos em que foi demonstrado, em outros estudos, o incremento das concentrações de MPF (Wehrend e Meinecke, 2001). A atividade do MPF em oócitos bovinos está diminuída no estádio de vesícula germinativa, subseqüentemente atinge seu pico no estádio de MI, sofrendo um decréscimo nos estádios de anáfase I e telófase I e torna a aumentar em MII (Wehrend e Meinecke, 2001). Nos períodos em que o estádio de maturação já está definido, não é possível detectar diferença entre os grupos (Fig. 6). Isso demonstra que: (1) o desenho experimental foi adequado para detectar alteração da cinética da maturação nuclear e (2) a PK-C regula a maturação de oócitos, coincidentemente com os períodos descritos de ativação do MPF (Wehrend e Meinecke, 2001), mas uma vez estabelecido o estádio de maturação, perde sua ação. O MPF é composto por uma subunidade catalítica p34cdc2 e uma subunidade regulatória cyclin B (Gonçalves et al., 2001). A hipótese é que a PK-C ativa a cdc25 fosfatase, necessária para desfosforilar a treonina-14 e a tirosina-15 e para ativar a p34cdc2 no processo de ativação do MPF. Pela primeira vez foi determinada a importância das células do cumulus na ação da PK-C.
CONCLUSÕES
A PK-C atua na fase de RVG independente das células do cumulus. No entanto, nos estádios de MI e MII, a ativação da PK-C participa da regulação da maturação de oócitos e é mediada pelas células do cumulus.
AGRADECIMENTOS
Os autores agradecem ao CNPq-PRONEX e FAPERGSF pelo suporte financeiro e ao frigorífico Silva e Frigorífico Pelegrini pela doação dos ovários.
Recebido para publicação em 22 de agosto de 2002
Recebido para publicação, após modificações, em 12 de fevereiro de 2004
Trabalho realizado com suporte financeiro do CNPq-PRONEX e FAPERGS.
- ABERDAM, E.; DEKEL, N. Activators of protein kinase C stimulate meiotic maturation of rat oocytes. Biochem. Biophys. Res. Commun., v.132, p.570-574, 1985.
- BORNSLAEGER, E.A.; POEYMIROU, W.T.; MATTEI, P. et al. Effects of protein kinase C activators on germinal vesicle breakdown and polar body emission of mouse oocytes. Exp. Cell. Res., v.165, p.507-517, 1986.
- CERDÁ, J.; REICH, G.; WALLACE, R.A.; SELMAN, K. Serotonin inhibition of steroid-induced meiotic maturation in the teleost Fundulus heteroclitus: role of cyclic AMP and protein kinases. Mol. Reprod. Dev., v.49, p.333-341, 1998.
- COLLEDGE, W.H.; CARLTON, M.B.L.; UDY, G.B. et al. Disruption of c-mos causes parthenogenetic development of unfertilized mouse eggs. Nature, v.370, p.65-68, 1994.
- COLONNA, R.; TATONE, C.; FRANCIONE, A. et al. Protein quinase C is required for dissappearence of MPF upon artificial activation in mouse eggs. Mol. Rep. Dev., v.48, p.292-299, 1997.
- CONOVER, W.J.; IMAN, R.L. Rank transformation as bridge between parametric and nonparametric statistics. Am. Statistician, v.35, p.124-129, 1981.
- DOWNS, S.M.; COTTOM, J.; HUNZICKER-DUNN, M. Protein kinase C and meiotic regulation in isolated mouse oocytes. Mol. Reprod. Dev., v.58, p.101-115, 2001
- FISSORE, R.A.; HE, C.L.; VANDE, W.G.F. Potential role of mitogen-activated protein kinase during meiosis resumption in bovine oocytes. Biol. Reprod, v.55, p.1261-1270, 1996.
- GONÇALVES, P.B.D.; GRAVES, C.N. Interaction between cAMP, Diacylglycerol and Ca-Calmodulin pathways in the regulation of cumulus expansion. Biol. Reprod, v.46, (Suppl.), p.66, 1992.
- GONÇALVES, P.B.D.; HERNANDEZ, A.G.; RUBIN, M.I.B. et al. Função da proteína quinase C na maturação nuclear em oócitos bovinos. Zootecnia, v.32, p.42, 1994.
- GONÇALVES, P.B.D.; NEVES, J.P.; CARÁMBULA, S.F. Regulatory aspects of oocyte maturation in mammals. In: SILVA, A.A.M.R. (Ed.). Br monographs of reproduction & catalog group. São Paulo, 2001. p.149-160.
- HERNÁNDEZ, A.G.; GONÇALVES, P.B.D.; RUBIN, M.I.B. Efeito de diferentes concentrações de forbol éster no reinício da meiose em oócitos bovinos. In: SEMIN INTERN TRANSF EMBR BIOTEC TECNOL AVANZ, 1995, Montevideo, Uruguai. Anais.. Montevideo, 1995. P.122 (Abstract).
- HOMA, S.T. Neomycin, a inhibitor of phosphoinositide hydrolysis, inhibits the resumptiom of bovine oocyte spontaneous meiotic maturation. J. Exp. Zool, v.258, p.95-103, 1991.
- HYTEL, P.; GREVE, T.; CALLESEN, H. Ultraestructural aspects of oocyte maturation and fertilization in cattle. J. Reprod. Fertil, v.38, p.35-47, 1989.
- KWON, H.B.; LEE, W.K. Involvement of protein kinase C in the regulation of oocyte maturation in amphibians (Rana dybowskii). J. Exp. Zool, v.257, p.115-123, 1991.
- LEVESQUE, J.T.; SIRARD, M. Effects of different kinases and phosfatases on nuclear cytoplasmic maturation of bovine oocytes. Mol. Reprod. Devel, v.42, p.114-121, 1995.
- LU, Z.; XIA, G.; ZHANG, J. Protein kinase C, rather than protein kinase A is involved in follicle-stimulating hormone-mediated meiotic resumption of mouse cumulus cell-enclosed oocytes in hypoxanthine-supplemented medium. Mol. Cell. Endoc, v.182, p.225-232, 2001.
- MILOVANOV, C.; SIRARD, M.A. Manipulation of chromossome condensation by protein synthesis inhibitors and cyclic AMP during maturation of bovine oocytes. Theriogenology, v.41, p.819-827, 1994.
- MONDADORI, R.G.; GONÇALVES, P.B.D.; NEVES, J.P.D. et al. Fecundação e clivagem após a ativação da Proteína Quinase C durante a maturação de oócitos bovinos. Ciên. Rural, v.29, p.105-110, 1999.
- MONTAGNER, M.M.; CARÁMBULA, S.F.; BORTOLOTTO, E.B. Fecundação e clivagem após a ativação da proteína quinase C durante a maturação de oócitos bovinos. Ciên. Rural, v.29, p.105-110, 1999.
- NOLAND, T.A.; DIMINO, M.J. Caracterization and distribuition of protein Kinase C in ovarian tissue. Biol. Reprod, v.35, p.863-872, 1986.
- PATIÑO, R.; YOSHIZAKI, G.; BOLAMBA, D.; THOMAS, P. Role of arachidonic acid and protein kinase C during maturation-inducing hormone-dependent meiotic resumption and ovulation in ovarian follicles of atlantic croaker. Biol. Reprod, v.68, p.516-523, 2003.
- ROSE-HELLEKANT, T.A.; BAVISTER, B.D. Roles of protein kinase A and C in spontaneous maturation and forskolin or 3-isibutyl-1-methylxantine, maintained meiotic arrest of bovine oocytes. Mol. Reprod. Devel, v.44, p.241-249, 1996.
- SHIOYA, Y.; KUWAYAMA, M.; FUKUSHIMA, M. et al. In vitro fertilization and cleavage capability of follicular oocytes classified by cumulus cells and matured in vitro. Theriogenology, v.30, p.489-489, 1998.
- STITH, B.J.; GOALSTONE, M.L.; KIRKWOOD, A.J. Protein kinase C initially inhibits the induction of meiotic cell division in Xenopus oocytes. Cell Signal, v.4, p.393-403, 1992.
- SU, Y.Q.; XIA, G.L.; BYSKOV, A.G. et al. Protein kinase C and intracellular calcium are involved in follicle-stimulating hormone-mediated meiotic resumption of cumulus cell-enclosed porcine oocytes in hypoxanthine-supplemented medium. Mol. Reprod. Dev, v.53, p.51-58, 1999.
- SÜSS, U.; WÜTHRICH, K.; STRANZINGER, G. Chromossome configurations and time sequence of the first meiotic division in bovine oocytes maturation in vitro. Biol. Reprod, v.38, p.871-880, 1988.
- VIGNOLA, A.G.H. Regulação da maturação nuclear e expansão das células do cumulus pelas proteínas quinase A e C em oócitos bovinos. 1995. 84f. Dissertação (Mestrado em Medicina Veterinária) Universidade Federal Santa Maria, Santa Maria, RS.
- VIGNOLA, A.H.; PRADO, A.; VALENTE, A. et al. Técnicas de coloração cromossômica para estádios específicos da maturação nuclear de oócitos bovinos. Ciên. Rural, v.24, p.583-589, 1994.
- WEHREND, A.; MEINECKE, B. Kinetics of meiotic progression, M-phase promoting factor (MPF) and mitogen-activated protein kinase (MAP KINASE) activities during in vitro maturation of porcine and bovine oocytes: species specific differences in the length of the meiotic stages. Anim. Reprod. Sci, v.66, p.174-184, 2001.
- YANG, X. Cellular and molecular regulation of oocyte maturation, activation and fertilization in cattle. Arq. Fac. Vet UFRGS, v.25, p.84-92, 1997 (Supl.).
- ZHANG, L.; JIANG, S.; WOZNIAK, P.J. et al. Cumulus cell function during bovine oocyte maturation, fertilization, and embryo development in vitro. Mol. Reprod. Devel, v.40, p.338-344, 1995.
Datas de Publicação
-
Publicação nesta coleção
29 Out 2004 -
Data do Fascículo
Ago 2004
Histórico
-
Aceito
12 Fev 2004 -
Recebido
22 Ago 2002