Resumos
Avaliou-se a patogenicidade do circovírus suíno tipo 2 (PCV2) isolado no estado de Santa Catarina mediante coinfecção experimental com parvovírus suíno (PPV). Foram utilizados 24 leitões specific pathogen free (SPF) com cinco dias de idade, distribuídos em quatro grupos (G), alojados em salas independentes e inoculados por via intranasal: G1 - controle (n=4); G2 - inoculados com PCV2 (n=7); G3 - inoculados com PPV (n=6); G4 - inoculados com PCV2 e PPV (n=7). Os animais foram monitorados diariamente para avaliação clínica e necropsiados 48 dias após a infecção. As principais lesões anatomopatológicas observadas nos suínos do G2 e G4 foram: aumento do volume dos linfonodos, depleção linfocitária com redução dos folículos linfóides nos órgãos linfocitários e presença de infiltrado eosinofílico nos linfonodos. A técnica de nested-PCR para PCV2 foi utilizada detectando DNA viral em órgãos de todos os animais do G2 e G4. O PCV2 infectou suínos SPF por via intranasal e foi detectado em outros órgãos, com mais lesões histopatológicas e em maior proporção nos animais coinfectados com PPV (G4), quando comparados aos infectados somente com PCV2 (G2).
suíno; circovírus suíno tipo 2; parvovírus suíno; síndrome multisistêmica do definhamento dos suínos
The virulence of porcine circovirus type 2 (PCV2) isolated in Santa Catarina State by coinfection with porcine parvovirus (PPV) was investigated. Twenty-four, 5-day-old SPF pigs were distributed into four groups, housed in separate rooms and inoculated by intranasal route: G1 - control (n=4); G2 - inoculated with PCV2 (n=7); G3 - inoculated with PPV (n=6); G4 - inoculated with PCV2 and PPV (n=7). The animals were monitored daily for clinical evaluation and were necropsied 48 days after the infection. The pathological lesions seen in G2 and G4 pigs were: enlargement of lymph nodes, mild to moderate lymphoid cell depletion, affecting lymphoid follicles in lymphoid organs and presence of infiltration by eosinophils in lymph nodes. PCV2 DNA was detected by a nested-PCR in all pigs of G2 and G4. These findings confirmed that pigs were successfully infected intranasally with PCV2. The presence of PCV2 DNA in tissue samples and the pathological lesions were more evident in pigs infected with both PCV2 and PPV than in pigs infected with PCV2 alone.
swine; porcine circovirus type 2; porcine parvovirus; post-weaning wasting syndrome
MEDICINA VETERINÁRIA
Coinfecção experimental de circovírus suíno tipo 2 isolado no Brasil e parvovírus suíno em suínos SPF
Experimental coinfection of SPF pigs with porcine circovirus type 2 isolated in Brazil and porcine parvovirus
L.T. FernandesI; J.R. Ciacci-ZanellaII; J. SobestianskyI; M.F. SchiochetII; C. TrombettaIII
IEscola de Veterinária - UFG Campus Samambaia - Caixa Postal 131 74001-970 Goiânia, GO
IIEmbrapa Suínos e Aves - Concórdia, SC
IIIUniversidade do Contestado - Concórdia, SC
RESUMO
Avaliou-se a patogenicidade do circovírus suíno tipo 2 (PCV2) isolado no estado de Santa Catarina mediante coinfecção experimental com parvovírus suíno (PPV). Foram utilizados 24 leitões specific pathogen free (SPF) com cinco dias de idade, distribuídos em quatro grupos (G), alojados em salas independentes e inoculados por via intranasal: G1 controle (n=4); G2 - inoculados com PCV2 (n=7); G3 - inoculados com PPV (n=6); G4 - inoculados com PCV2 e PPV (n=7). Os animais foram monitorados diariamente para avaliação clínica e necropsiados 48 dias após a infecção. As principais lesões anatomopatológicas observadas nos suínos do G2 e G4 foram: aumento do volume dos linfonodos, depleção linfocitária com redução dos folículos linfóides nos órgãos linfocitários e presença de infiltrado eosinofílico nos linfonodos. A técnica de nested-PCR para PCV2 foi utilizada detectando DNA viral em órgãos de todos os animais do G2 e G4. O PCV2 infectou suínos SPF por via intranasal e foi detectado em outros órgãos, com mais lesões histopatológicas e em maior proporção nos animais coinfectados com PPV (G4), quando comparados aos infectados somente com PCV2 (G2).
Palavras-chave: suíno, circovírus suíno tipo 2, parvovírus suíno, síndrome multisistêmica do definhamento dos suínos
ABSTRACT
The virulence of porcine circovirus type 2 (PCV2) isolated in Santa Catarina State by coinfection with porcine parvovirus (PPV) was investigated. Twenty-four, 5-day-old SPF pigs were distributed into four groups, housed in separate rooms and inoculated by intranasal route: G1 - control (n=4); G2 - inoculated with PCV2 (n=7); G3 - inoculated with PPV (n=6); G4 - inoculated with PCV2 and PPV (n=7). The animals were monitored daily for clinical evaluation and were necropsied 48 days after the infection. The pathological lesions seen in G2 and G4 pigs were: enlargement of lymph nodes, mild to moderate lymphoid cell depletion, affecting lymphoid follicles in lymphoid organs and presence of infiltration by eosinophils in lymph nodes. PCV2 DNA was detected by a nested-PCR in all pigs of G2 and G4. These findings confirmed that pigs were successfully infected intranasally with PCV2. The presence of PCV2 DNA in tissue samples and the pathological lesions were more evident in pigs infected with both PCV2 and PPV than in pigs infected with PCV2 alone.
Keywords: swine, porcine circovirus type 2, porcine parvovirus, post-weaning wasting syndrome
INTRODUÇÃO
O circovírus suíno (PCV) foi descoberto em 1974 como contaminante de linhagens contínuas de células renais de suínos (PK15) (Tischer et al., 1974). Estudos subseqüentes demonstraram, pela caracterização de seus ácidos nucléicos, que estes vírus possuíam um filamento único de DNA, circular e fechado covalentemente. Por ser o primeiro vírus animal a apresentar genoma circular de DNA, o nome de circovírus suíno foi proposto, passando a fazer parte da família Circoviridae (Tischer et al., 1982). Até o momento já foram identificados dois tipos de PCV: o circovírus suíno tipo 1 (PCV1), contaminante de células PK15 e apatogênico para suínos e o circovírus suíno tipo 2 (PCV2) associado à síndrome multisistêmica do definhamento dos suínos (SMD). Os circovírus suínos são vírus pequenos, com 17nm de diâmetro, icosaédricos, não-envelopados e possuem um dos menores genomas entre os vírus que infectam vertebrados, com aproximadamente 1.760 nucleotídeos (Todd, 2000).
A SMD é uma doença emergente causada pelo PCV2 e está associada com importantes taxas de mortalidade de suínos nas fases de creche e engorda (Allan et al., 1998). A enfermidade foi reconhecida pela primeira vez no Canadá em 1991 e, desde então, tem sido descrita em vários países, sendo considerada, atualmente, como uma doença de distribuição mundial (Clark, 1997; Allan e Ellis, 2000). Clinicamente, é caracterizada por emagrecimento progressivo, dispnéia, anemia, aumento do volume dos linfonodos superficiais inguinais, pneumonia, diarréia, icterícia e morte (Clark, 1997; Rosell et al., 1999). As lesões histopatológicas atribuídas à SMD são observadas em diversos órgãos, mas predominantemente em órgãos linfóides. Essas lesões consistem em depleção linfocitária com infiltração no tecido linfóide de células gigantes multinucleadas e histiócitos que podem apresentar corpúsculos de inclusão viral localizados no citoplasma dessas células. Também se observam lesões com ocorrência e freqüência variável no fígado, rins e pulmões dos animais infectados (Ellis et al., 1998; Rosell et al., 1999).
No Brasil, o PCV2 associado à SMD foi diagnosticado em 2000 (Zanella e Mores, 2000), mas ainda não se conhece sua prevalência no país. Também não se conhecem as características patogênicas das amostras de PCV2 isoladas no Brasil, mas sabe-se que a coinfecção desse vírus com outros patógenos, como o parvovírus suíno (PPV), pode ser importante fator na patogênese da SMD (Allan et al., 1999; Kim et al., 2003). O objetivo deste trabalho foi avaliar a patogenicidade do PCV2 isolado no Brasil em leitões SPF (Specific Pathogen Free), experimentalmente coinfectados com PPV através de critérios clínicos, anatomopatológicos e virológicos.
MATERIAL E MÉTODOS
Foram utilizados 24 leitões SPF, mestiços (raças Landrace e Large White) com cinco dias de idade no início do experimento (D0), pesos entre 1,4 e 3,1kg e provenientes de três leitegadas diferentes. Os animais foram identificados e alojados em salas de isolamento. Foi realizada colheita de sangue (2ml/leitão) e administrado antibiótico à base de cloridrato de ceftiofur1 1 Excenel ® RTU, Pfizer Inc., USA. na concentração de 3mg/kg de peso vivo, repetindo-se o tratamento em intervalo de 24 horas durante dois dias.
O inóculo de PCV2 foi produzido a partir de células de testículo suíno (ST) livres de PCV1, inoculadas com suspensão de órgãos (linfonodos, pulmões e tonsilas) de um suíno com SMD proveniente de um rebanho localizado no Estado de Santa Catarina (amostra pertencente à Embrapa Suínos e Aves). Para aumentar o título viral no inóculo, as células primariamente inoculadas foram subcultivadas a cada 24 horas, totalizando 14 passagens. Ao final da 14ª passagem, as culturas foram congeladas e descongeladas três vezes, e a suspensão resultante deste processo foi estocada a 80°C. O título foi calculado em 105 TCID50/ml (tissue culture fifty percent infectious dose). Alíquotas da suspensão foram testadas por nested-PCR (reação em cadeia da polimerase) e análise com enzimas de restrição (Hamel et al., 2000) para confirmar a presença de PCV2 no inóculo e pela reação de hemaglutinação (HA) para excluir a presença de contaminação cruzada com patógenos hemaglutinantes.
Para produção de inóculo de PPV, foram utilizadas células de rins de suíno (SK6) inoculadas com 2,5ml de amostra pura do vírus cedida pelo Laboratório de Virologia do Centro de Diagnóstico em Saúde Animal (CEDISA/Concórdia, SC). As células foram passadas uma vez e incubadas a 37°C por cinco dias. Após o período de incubação, as culturas foram congeladas e descongeladas três vezes, a suspensão resultante foi centrifugada a 500x g por 10 minutos, desprezado o pellet e o sobrenadante estocado a 80°C. O título foi calculado em 105 TCID50/ml (tissue culture fifty percent infectious dose).
As suspensões contendo PCV2 e PPV foram tratadas com clorofórmio (50µl/ml), incubadas a temperatura ambiente por 10 minutos, centrifugadas a 500x g por cinco minutos, e a fase superior foi descartada (Allan et al., 1999).
Os animais, de ambos os sexos, foram distribuídos aleatoriamente em quatro grupos distintos e alojados separadamente em salas de isolamento. O grupo 1 (G1) foi formado por quatro suínos controle inoculados com suspensão de células ST não-infectadas. O grupo 2 (G2) foi constituído por sete leitões inoculados com PCV2, o grupo 3 (G3) com seis animais inoculados com PPV e o grupo 4 (G4) formado por sete suínos inoculados com PCV2 e PPV. Todos os animais foram inoculados aos seis dias de idade (D1) com 0,5ml de inóculo por via intranasal. Durante todo o período experimental, os animais foram monitorados diariamente para avaliação do estado clínico geral e observação de sinais clínicos compatíveis com a SMD.
Os animais foram necropsiados com 53 dias de idade (D48), sendo realizados colheita de 50ml de sangue/suíno, exame macroscópico das carcaças e colheita dos seguintes órgãos para exame histopatológico e virológico: linfonodos parotidianos, mesentéricos e inguinais, tonsilas, timo, traquéia, coração, pulmões, fígado, pâncreas, baço, rins e testículos.
Para o exame histopatológico, fragmentos dos órgãos foram fixados em formalina a 10%, tamponada a pH 7,0 e incluídos em parafina histológica. As amostras foram seccionadas em cortes de 4µm e coradas por hematoxilina e eosina (Luna, 1968).
A detecção de PCV2 nos órgãos dos suínos foi realizada por meio da técnica de nested-PCR descrita por Kim et al. (2001). Fragmentos dos órgãos coletados à necropsia, previamente estocados a 80°C, pesando aproximadamente um grama, foram submetidos à digestão a 56°C por quatro horas em tampão de lise (200mM NaCl, 100 mM Trizma Base pH 7,5, 20mM EDTA 0,5M pH 8,0 e 1% SDS) e 20mg/ml de proteinase K2 2 Sigma Chemical Co., St. louis, USA. . O DNA foi extraído com fenol: clorofórmio: álcool isoamílico (25:24:1), precipitado com etanol absoluto (dois volumes) e 10M de acetato de sódio, mantido por 20 horas a -20°C. O DNA foi lavado em 75% de etanol que foi centrifugado a 5000x g por cinco minutos, retirado o sobrenadante e o pellet ressuspenso em 100µl de tampão TE (10mM Trizma Base pH 7,5 e 1mM EDTA 0,5M pH 8,0) (Sambrook et al., 1989).
Os primers utilizados para a realização da técnica de PCR foram designados por serem específicos para PCV2, contendo uma seqüência de nucleotídeos para a região da ORF2 (open reading frame 2) que codifica proteínas para formação do capsídeo viral. Foram realizadas duas reações: uma PCR externa (outer-PCR) e outra interna (nested-PCR) como descrita por Kim et al. (2001). Como controle positivo, foi utilizada a amostra de PCV2 utilizada na inoculação dos animais. Água ultrapura estéril foi utilizada como controle negativo das reações. Após a amplificação por nested-PCR, os produtos amplificados foram submetidos à eletroforese em gel de agarose a 1,5%.
As amostras de sangue de todos os animais, colhidas antes das inoculações e no momento da necropsia, foram centrifugadas por 500× g durante 10 minutos, sendo o soro estocado a 80°C. Alíquotas destes soros foram testadas por meio da reação de inibição da hemaglutinação (HI) para avaliar a soroconversão contra PPV.
RESULTADOS
Na avaliação clínica, dois animais do grupo 4 (G4) apresentaram inapetência e incoordenação motora no 10º dia após inoculação. No 28º dia, foram observadas, em dois animais do G4 e em um do G2, lesões multifocais na pele, circunscritas, levemente elevadas, vermelho-escuras e distribuídas sobre os membros posteriores e a região inguinal. Essas lesões de pele evoluíram para cicatrização após 10 dias. Entre o 30º e o 33º dia, observou-se diarréia em todos os suínos do G2. Os animais do G1 e do G3 não manifestaram sinais clínicos evidentes.
Durante a necropsia, o aumento do volume de linfonodos inguinais superficiais e mesentéricos foi observado em três dos sete suínos do G2 (42,8%) e em seis dos sete animais do G4 (85,7%). Dois animais do G2 e do G4 (28,6%) apresentaram redução do volume do timo e um animal do G4 apresentou ausência de colabamento pulmonar (14,3%) com pequenas áreas de consolidação pulmonar localizadas na região cranioventral. Os animais do G1 e G3 não apresentaram alterações macroscópicas.
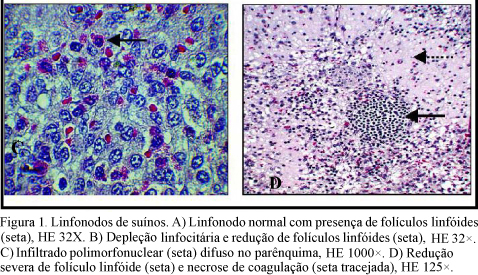
O exame histopatológico dos fragmentos de órgãos dos suínos revelou alterações restritas aos órgãos linfóides, com exceção de dois animais do G4 (28,6%) que apresentaram aumento de celularidade da parede alveolar, mas com ausência de infiltrado inflamatório; 57,1% dos animais do G2 apresentaram discreta depleção linfocitária com redução dos folículos linfóides nos linfonodos (Fig. 1B). No G4, essa lesão foi observada em grau moderado nos linfonodos de todos os animais (100%), nas tonsilas (14,3%), timo e baço (28,6%). Nos linfonodos de todos os animais que apresentaram depleção linfocitária e redução de folículos linfóides, foi observada presença de infiltrado polimorfonuclear, predominantemente do tipo eosinofílico, difuso em todo o parênquima e mais intensamente nas trabéculas (Fig. 1C), além de alguns neutrófilos e mastócitos. Um animal do G4 (14,3%) apresentou áreas de necrose de coagulação no parênquima dos linfonodos (Fig. 1D). Os animais do G1 e G3 não apresentaram alterações histopatológicas (Fig. 1A).
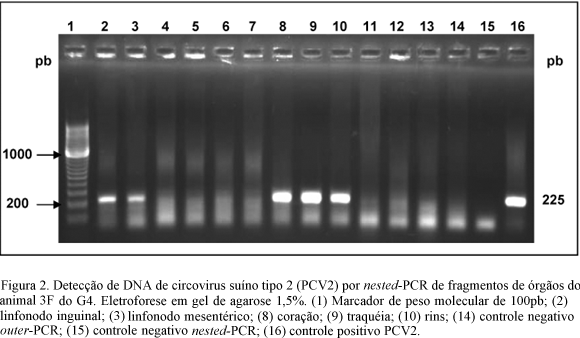
O DNA de PCV2 nos órgãos dos suínos inoculados foi detectado pela técnica de nested-PCR, que amplificou um produto de 225pb (Fig. 2). Todos os animais dos grupos G2 e G4 resultaram positivos para PCV2, encontrando-se o DNA viral em linfonodos parotidianos, inguinais e mesentéricos; em tonsilas, timo, baço, coração, traquéia, rins, fígado, pulmões e testículos (Tab. 1). O PCV2 não foi detectado em nenhum animal do G1 e G3. As Tab. 2 e 3 apresentam os resultados individualizados dos exames anatomopatológicos, histopatológicos e virológicos dos suínos pertencentes ao G2 e ao G4.
A soroconversão contra PPV foi observada pela reação de inibição da hemaglutinação (HI), realizada a partir do soro colhido dos animais no início e no final do experimento, obtendo-se títulos entre 1:256 e 1:1024 para animais do G3 e G4 e títulos negativos para animais do G1 e G2.
DISCUSSÃO
O trabalho demonstrou que leitões SPF com seis dias de idade foram infectados por via intranasal com PCV2 associado ou não com PPV. Foram observadas lesões multifocais na pele de dois animais do G2 e um do G4, 28 dias após inoculação, que evoluíram para cicatrização. Essa alteração não foi observada em estudos que utilizaram leitões infectados experimentalmente somente com PCV2 ou em associação com o PPV (Allan et al., 1999; Ellis et al., 1999; Balasch et al., 1999; Krakowka et al., 2000). Lesões multifocais na pele de suínos têm sido observadas em animais acometidos pela síndrome da dermatite e nefropatia suína (SDNS), doença também associada ao PCV2. As lesões foram multifocais, circulares, vermelho-escuras, que se distribuíram sobre os membros posteriores, região ventral do abdômen e tórax. Em curso grave dessa enfermidade, a maioria dos suínos acometidos morre nos três primeiros dias após o início dos sinais por falha renal aguda. Na forma mais leve, os animais podem apresentar lesões de pele que regridem até cicatrização, sem necessidade de tratamento (Rosell et al., 2000).
Todos os suínos inoculados com PCV2 foram infectados, resultado confirmado na prova de nested-PCR. Como em outros trabalhos de inoculação experimental, suínos inoculados apenas com este vírus foram infectados, mas não desenvolveram sinais clínicos graves da SMD (Balasch et al., 1999; Ellis et al., 1999). Entretanto, outros autores demonstraram a reprodução da SMD em suínos inoculados com PCV2 apenas (Allan et al., 1999). Essas diferenças podem estar relacionadas com utilização de diferentes amostras de PCV2, tipo de inóculo (suspensão de órgãos ou vírus isolado de cultura de células), via de inoculação, dose viral, número de passagens de vírus na cultura celular, tipo de suíno (convencionais, gnobióticos, que não mamaram colostro) e idade dos animais inoculados (Balasch et al., 1999; Ellis et al., 1999; Kennedy et al., 2000).
Os animais inoculados com PCV2 e PPV expressaram de forma leve a doença clínica e lesões microscópicas de grau leve a moderado, apesar de todos os suínos terem sido infectados pelo PCV2. Em todos os estudos em que se observaram sinais clínicos e lesões severas compatíveis com a SMD, pela infecção experimental por PCV2 e PPV, foram utilizados leitões gnobióticos que não mamaram colostro (Allan et al., 1999; Kennedy et al., 2000; Krakowka et al., 2000; Kim et al., 2003). Neste trabalho foram utilizados leitões com cinco dias de idade que mamaram colostro e, dessa forma, a menor severidade das alterações verificadas pode ser explicada pela utilização de leitões não imunodeprimidos.
A diferença entre a infecção induzida experimentalmente e a infecção natural faz supor que nas infecções naturais outros fatores podem influenciar na manifestação clínica da doença. Madec e Waddilove (2002) associaram fatores de risco como densidade elevada, baixa qualidade do ar, água e ração, mistura de lotes de idades e procedências diferentes com o desenvolvimento da infecção por PCV2. Neste experimento, os animais foram mantidos em ambiente controlado e não foram submetidos a fatores que provocassem estresse como os relacionados ao manejo, alimentação ou presença de outros agentes patogênicos concomitantes.
Na obtenção de informações sobre o tropismo do PCV2, foi utilizada uma prova de nested-PCR específica para PCV2 que detectou DNA viral em diversos órgãos dos suínos do G2 e G4. Nos animais do G2, a detecção de PCV2 resultou positiva no coração, linfonodos inguinais e mesentéricos, timo, traquéia, rins e pulmões, e negativa nos linfonodos parotidianos, tonsilas, baço, fígado e testículos. Nos do G4, foi detectado DNA viral em todos os órgãos citados e em maior proporção quando comparado ao G2.
O PCV2 e o PPV são vírus notavelmente dependentes da síntese de DNA da célula hospedeira para eficiente replicação viral. A hipótese de a infecção por PCV2 ser exacerbada pela coinfecção por PPV pode ser justificada pela característica que o PCV2 possui de infectar células linfóides e sua replicação ser estimulada por agentes que promovam esse fenômeno. Kim et al. (2003) relataram que a infecção de macrófagos pelo PPV pode promover altos níveis de replicação de PCV2 durante a fase pré-clínica da infecção.
A detecção de PCV2 nos testículos dos dois machos do G2 resultou negativa, mas em testículos de cinco (83,3%) dos seis machos do G4 foi detectado DNA viral. Estes resultados confirmam os de Larochelle et al. (2000) e Kim et al. (2001) que detectaram DNA de PCV2 no sêmen de suínos após inoculação experimental ou infecção natural. Nos dois estudos não foi demonstrado em quais células do sistema reprodutivo do macho o vírus estaria presente. Estes dados reforçam a hipótese de que o macho suíno pode representar papel importante na disseminação do PCV2, principalmente através de sêmen infectado.
Em resumo, a manifestação de sinais clínicos e lesões associadas com a SMD ocorreram de forma leve em leitões SPF infectados com PCV2 e PPV. No entanto, o PCV2 foi detectado em mais órgãos, com mais lesões histopatológicas e em maior proporção dos suínos coinfectados com PPV (G4) quando comparados aos infectados somente com PCV2 (G2), reforçando a hipótese de que a infecção por PCV2 seja acentuada pela coinfecção por PPV.
Recebido em 18 de maio de 2004
Aceito em 13 de outubro de 2005
E-mail: janice@cnpsa.embrapa.br
- ALLAN, G.M.; ELLIS, J. Porcine circovirus: A review. J. Vet. Diagn. Investig., v. 12, p.3-14, 2000.
- ALLAN, G.M.; KENNEDY, S.; MCNEILLY, F. et al. Experimental reproduction of severe wasting disease by co-infection of pigs with porcine circovirus and porcine parvovirus. J. Comp. Pathol., v.121, p.1-11, 1999.
- ALLAN, G.M.; MCNEILLY, F.; KENNEDY, B. et al. Isolation of porcine circovirus-like viruses from pigs with a wasting disease in the USA and Europe. J. Vet. Diagn. Investig., v.10, p.3-10,1998.
- BALASCH, M.; SEGALÉS, J.; ROSELL, C. et al. Experimental inoculation of conventional pigs with tissue homogenates from pigs with post-weaning multisystemic wasting syndrome. J. Comp. Pathol., v.121, p.139-148, 1999.
- CLARK, E. G. Post weaning multisystemic wasting syndrome. Proc. Am. Assoc. Swine Pract., v.28, p.499-501, 1997.
- ELLIS, J.; HASSARD, L.; CLARK, E. et al. Isolation of circovirus from lesions of pigs with postweaning multisystemic wasting syndrome. Can. Vet. J., v.39, p 44-51, 1998.
- ELLIS, J.; KRAKOWKA, S.; LAIRMORE, M. et al. Reproduction of lesions of postweaning multisystemic wasting syndrome in gnobiotic piglets. J. Vet. Diagn. Investig., v. 11, p. 3-14, 1999.
- HAMEL, AL.; LIN, L.L.; SACHVIE, C. et al. PCR detection and characterization of type-2 porcine circovirus. Can. J. Vet. Res., v.64, p.44-52, 2000.
- KENNEDY, S.; MOFFETT, D.; MCNEILLY, F. et al. Reproduction of lesions of post weaning multisystemic wasting syndrome by infection of conventional pigs with porcine circovirus type 2 alone or in combination with porcine parvovirus. J. Comp. Pathol., v.122, p.9-24, 2000.
- KIM, J.; CHOI, C.; CHAE, C. Pathogenesis of postweaning multisystemic wasting syndrome reproduced by co-infection with korean isolates of porcine circovirus 2 and porcine parvovirus. J. Comp. Pathol., v.128, p. 52-59, 2003.
- KIM, J.; HAN DU; CHOI, C.; CHAE, C. Differentiation of porcine circovirus (PCV)-1 and PCV2 in boar semen using a multiplex nested polymerase chain reaction. J. Virol. Meth., v.98, p.25-31, 2001.
- KRAKOWKA, S.; ELLIS, J.A.; MEEHAN, B. et al. Viral wasting syndrome of swine: Experimental reproduction of PMWS in gnotobiotic swine by co-infection with porcine circovirus-2 (PCV2) and porcine parvovirus (PPV). Vet. Pathol., v.37, p.254-263, 2000.
- LAROCHELLE, R.; BIELANSKI, A.; MULLER, P. et al. Evidence of shedding of porcine circovirus type 2 (PCV2) in boars semen following experimental infection. In: International Pig Veterinary Society Congress, 16., 2000, Melbourne. Proceedings..., Melbourne Austrália: IPVS, 2000. p.580.
- LUNA. L.G. Manual of Histologic Staining of Armed Forces Institute of Pathology 3.ed. New York: McGraw-Hill Book, 1968. 258p.
- MADEC, F.; WADDILOVE, J. Control PCV2 or control other factors? Several approaches to a complex problem. In: PMWS and PCV2 diseases. In: International Pig Veterinary Society Congress, 17, 2002, Ames. Proceedings Ames, EUA: IPVS, 2002. p.79.
- ROSELL, C.; SEGALÉS, J.; PLANA-DURAN, J. et al. Pathological, immunohistochemical, and in situ hybridization studies of natural cases of post-weaning multisystemic wasting syndrome (PMWS) in pigs. J. Comp. Pathol., v.120, p.59-68, 1999.
- ROSELL, C.; SEGALES, J.; RAMOS-VARA, J. A. et al. Identification of porcine circovirus in tissues of pigs with porcine dermatitis and nephropathy syndrome. Vet. Rec., v.146, p.40-43, 2000.
- SAMBROOK, J.; FRITSCH, E.F.; MANIATIS, T. Molecular cloning, a laboratory manual 2.ed. New York: Cold Spring Harbor Laboratory, 1989.
- TISCHER, I.; GELDERBLOM, H.; VETTERMAN, W. et al. A very small porcine virus with circular single-stranded DNA. Nature, v.295, p.64-66, 1982.
- TISCHER, I.; RASCH, R.; TOCHTERMANN, G. Characterization of papovavirus and picornavirus like particles in permanent pig kidney cell lines. Zentralbl. Bakteriol. Parasitenkd. Infektionskr. Hyg. Abt. 1 Orig., v.26, p.153-167, 1974.
- TODD, D. Circoviruses: immunosuppressive threats to avian species: a review. Avian Pathol., v.29, p.373-394, 2000.
- ZANELLA, J.R.C.; MORES, N. Síndrome multisistêmica do definhamento do leitão desmamado (SMDLD) causada por circovírus suíno. In: CONGRESO MERCOSUR DE PRODUCCIÓN PORCINA, Buenos Aires, 2000.
Datas de Publicação
-
Publicação nesta coleção
19 Abr 2006 -
Data do Fascículo
Fev 2006
Histórico
-
Recebido
18 Maio 2004 -
Aceito
13 Out 2005