Resumos
Empregou-se a técnica de reação em cadeia pela polimerase precedida de transcrição reversa para detecção do vírus da cinomose canina (CC). Para a padronização da técnica foram selecionados quatro pares de oligonucleotídeos (P1, P2, N1, H1), baseados em seqüências dos genes da fosfoproteína, neuraminidase e hemaglutinina, sendo utilizadas três cepas vacinais de vírus da CC como controles positivos. Foram analisadas três amostras isoladas de cães com cinomose e quatro amostras provenientes de cães com suspeita clínica de cinomose. Não houve amplificação nas amostras com suspeita clínica da doença. Os resultados obtidos com os oligonucleotídeos P1 e N1 foram superiores aos de H1. Os oligonucleotídeos P2 foram considerados inapropriados para a detecção do vírus da CC. Os amplicons obtidos com os oligonucleotídeos P1, N1 e H1 foram clivados com endonucleases de restrição, sendo os perfis das amostras virais comparados aos da amostra vacinal Lederle, utilizada como referência. Um padrão similar de restrição foi observado em todas as amostras analisadas.
cão; cinomose; RT-PCR; polimorfismo
The reverse transcription-polymerase chain reaction was used to detect canine distemper virus (CDV). Four oligonucleotide pairs were selected (P1, P2, N1, H1), based on the sequences of the phosphoprotein, hemagglutinin and nuraminidase genes for assay standardization, and three CDV vaccine strains were used as positive controls. Three viral isolates from dogs with canine distemper and four samples from animals clinically suspected of distemper were analysed. No amplification was detected in suspected samples. Results obtained by using P1 and N1 oligonucleotides were superior to those with H1 ones. P2 oligonucleotides were considered inadequate for CDV detection. Amplicons resulting from amplification of P1, N1 and H1 oligonucleotides were submitted to cleavage by restriction endonucleases and restriction patterns of viral samples were compared to that of Lederle strain used as reference. A similar restriction pattern was observed in all analysed samples.
dog; canine distemper virus; RT-PCR; polymorphism
MEDICINA VETERINÁRIA
Detecção do vírus da cinomose canina por RT-PCR utilizando-se oligonucleotídeos para os genes da fosfoproteína, hemaglutinina e neuraminidase
Detection of canine distemper virus by RT-PCR using oligonucleotides targeted to the phosphoprotein, hemagglutinin and neuraminidase genes
M. PozzaI; A.B. SimonettiII,* * Autor para correspondência ( corresponding author) E-mail: amauri@ufrgs.br ; P.A. EstevesII; F.A.M. RijsewijkIII; P.M. RoeheII, III
IAluno de pós-graduação - FA-UFRGS Porto Alegre, RS
IIInstituto de Ciências Básicas da Saúde - UFRGS Rua Sarmento Leite, 500 90050-170 Porto Alegre, RS
IIIInstituto de Pesquisas Veterinárias Desidério Finamor Eldorado do Sul, RS
RESUMO
Empregou-se a técnica de reação em cadeia pela polimerase precedida de transcrição reversa para detecção do vírus da cinomose canina (CC). Para a padronização da técnica foram selecionados quatro pares de oligonucleotídeos (P1, P2, N1, H1), baseados em seqüências dos genes da fosfoproteína, neuraminidase e hemaglutinina, sendo utilizadas três cepas vacinais de vírus da CC como controles positivos. Foram analisadas três amostras isoladas de cães com cinomose e quatro amostras provenientes de cães com suspeita clínica de cinomose. Não houve amplificação nas amostras com suspeita clínica da doença. Os resultados obtidos com os oligonucleotídeos P1 e N1 foram superiores aos de H1. Os oligonucleotídeos P2 foram considerados inapropriados para a detecção do vírus da CC. Os amplicons obtidos com os oligonucleotídeos P1, N1 e H1 foram clivados com endonucleases de restrição, sendo os perfis das amostras virais comparados aos da amostra vacinal Lederle, utilizada como referência. Um padrão similar de restrição foi observado em todas as amostras analisadas.
Palavras-chave: cão, cinomose, RT-PCR, polimorfismo
ABSTRACT
The reverse transcription-polymerase chain reaction was used to detect canine distemper virus (CDV). Four oligonucleotide pairs were selected (P1, P2, N1, H1), based on the sequences of the phosphoprotein, hemagglutinin and nuraminidase genes for assay standardization, and three CDV vaccine strains were used as positive controls. Three viral isolates from dogs with canine distemper and four samples from animals clinically suspected of distemper were analysed. No amplification was detected in suspected samples. Results obtained by using P1 and N1 oligonucleotides were superior to those with H1 ones. P2 oligonucleotides were considered inadequate for CDV detection. Amplicons resulting from amplification of P1, N1 and H1 oligonucleotides were submitted to cleavage by restriction endonucleases and restriction patterns of viral samples were compared to that of Lederle strain used as reference. A similar restriction pattern was observed in all analysed samples.
Keywords: dog, canine distemper virus, RT-PCR, polymorphism
INTRODUÇÃO
O vírus da cinomose canina (CC), membro do gênero Morbillivirus, é altamente contagioso e causa infecção multissistêmica principalmente em filhotes com menos de três meses de idade, com altos índices de mortalidade (Murphy et al., 1999; Biazonno et al., 2001). Além de cães domésticos, outros membros da família Canidae e alguns das famílias Mustelidae, Procyonidae, Hyaenidae, Ailuridae, Viverridae e Tuyussuidae, grandes felinos e primatas Cercopithecidae são suscetíveis à infecção natural pelo vírus da CC (Deem et al., 2000).
As primeiras vacinas de vírus vivos atenuados que reduziram drasticamente o impacto da infecção na população canina pelo vírus da CC surgiram há mais de 50 anos (Harder e Osterhaus, 1997). Desde então, utiliza-se a mesma vacina na proteção de cães em todo o mundo. Vários relatos, porém, e estudos epidemiológicos revelaram aumento na incidência da infecção por este agente tanto em cães vacinados como em não vacinados (Jozwik e Frymus, 2002). Vários estudos evidenciaram diferenças antigênicas entre amostras vacinais e selvagens (Ohashi et al., 1998; Haas et al., 1999; Hashimoto et al., 2001; Negrão et al., 2006).
No Brasil, a epidemiologia do vírus da CC é muito pouco estudada. Um estudo epidemiológico realizado no Rio Grande do Sul revelou que 11,7% dos animais submetidos à necropsia tiveram sua morte relacionada à infecção pelo vírus da CC (Headley e Graça, 2000). Os sintomas clínicos da cinomose canina (CC) são semelhantes aos de várias outras doenças caninas como hepatite, parvovirose, leptospirose, toxoplasmose e raiva, dificultando seu diagnóstico clínico. Faz-se, então, necessário um teste confirmatório eficaz para o diagnóstico laboratorial dessa doença.
Tradicionalmente, a CC vem sendo diagnosticada por técnicas de isolamento viral, imunofluorescência e soroneutralização. Essas técnicas, entretanto, demandam demasiado tempo para análise e amostras com grande quantidade de partículas virais. O isolamento viral necessita de partículas viáveis para o sucesso do isolamento. As técnicas moleculares podem fornecer resultados confiáveis e rápidos na detecção do vírus da CC devido às suas altas sensibilidade e especificidade, não necessitando a presença de partículas viáveis nas amostras. Diversos estudos com o uso da RT-PCR foram relatados, onde foram utilizados oligonucleotídeos direcionados para diferentes genes do vírus da CC, principalmente da fosfoproteína, da hemaglutinina e da neuraminidase (Frisk et al., 1999; Rzezutka e Mizak, 2002; Shin et al., 2004). No Brasil, estudos sobre a utilização de RT-PCR para o diagnóstico de infecção pelo vírus da cinomose canina, com o emprego de oligonucleotídeos desenhados a partir da seqüência do gene que codifica a nucleoproteína do vírus da CC, foram realizados por Gebara et al., 2004; Negrão et al., 2006; Negrão et al., 2007.
O objetivo deste trabalho foi testar uma técnica de RT-PCR para a detecção de CDV com oligonucleotídeos direcionados para seqüências dos genes P, H e N do vírus, pelo uso de amostras vacinais para sua padronização com subseqüente análise por endonucleases de restrição para confirmar sua especificidade.
MATERIAL E MÉTODOS
Foram utilizadas três amostras vacinais de vírus da CC: Lederle1 1 Biovet S.A. - Vargem Grande Paulista, Brasil. , Snyder Hill (ATCC VR-526) e Rockborn2 2 ID-Lelystad - Lelystad, Holanda. (gentilmente cedida pelo Dr. Franz Rijsewijk); três amostras virais (chamadas de SNC 1, SNC 2 e SNC 3) de cães infectados por vírus da CC provenientes da região urbana de Londrina, PR, diagnosticados por análise histológica de material de cérebro, cerebelo e bexiga e pela técnica de RT-PCR (amostras gentilmente cedidas pelo Dr. Amauri Alfieri, do Laboratório de Virologia Animal-Centro de Ciências Agrárias da Universidade Estadual de Londrina, Paraná). Essas amostras foram cultivadas e mantidas em células de linhagem de rim canino (MDCK) (ATCC CCI-34), suplementadas com meio essencial mínimo3 3 Gibco-BRL - São Paulo, Brasil. (MEM) e 7% de soro fetal bovino4 4 Nutricell - Campinas, Brasil (SFB), com enrofloxacina5 5 Schering-Plough Veterinária - Rio de Janeiro, Brasil (10U/ml); um isolado de vírus Parainfluenza bovino tipo 3 (SF-4) (gentilmente cedido pela Dra. Sílvia Sardi da Universidade Federal da Bahia) e quatro amostras virais isoladas no Instituto de Pesquisas Veterinárias Desidério Finamor (IPVDF) a partir de cérebros de cães com sintomatologia sugestiva de CC (amostras L1, L2, L3 e L4), cultivadas e mantidas em células MDCK suplementadas com MEM e SFB, com enrofloxacina (10U/ml). Além dessas amostras, para se testar a especificidade da técnica de RT-PCR, foram utilizadas cinco amostras virais: Herpesvirus bovino tipo 1 (BHV-1), (gentilmente cedida pelo Instituto Nacional de Tecnologia Agropecuária, Balcarce, Argentina); vírus influenza A eqüino (FLU, A/Equine/miami/1/73-H7N7) (gentilmente cedida pela Dra. Marilda M. Siqueira do Laboratório de Vírus Respiratório e Sarampo da Fundação Oswaldo Cruz, Rio de Janeiro); amostras com vírus do sarampo, caxumba e rubéola6 6 Glaxo Smith Kline Biologicals S/A, Rio de Janeiro, RJ, Brasil (vacina tríplice SCR) e amostra de Parvovirus (PAR) (ATCC VR-2209). Para multiplicação viral foram utilizadas MDCK cultivadas em MEM e suplementadas com SFB6 6 Glaxo Smith Kline Biologicals S/A, Rio de Janeiro, RJ, Brasil , com enrofloxacina7 7 Ultrospec® II - LKB Biochrom, Cambridge, Inglaterra (10U/ml). O cálculo da DICC50/ml (dose infectante para 50% dos cultivos celulares) foi efetuado pelo método de Reed e Müench (1938). Os estoques de vírus foram produzidos pela inoculação dos cultivos com uma multiplicidade de infecção entre 0,1 e 1,0 e coletados quando o efeito citopatogênico (ECP) atingiu aproximadamente 90% da monocamada celular. Após esse período, os cultivos foram congelados a -70ºC, clarificados por centrifugação a baixa velocidade e o sobrenadante dividido em alíquotas e estocado a -70ºC até o momento de uso.
Com o auxílio do software Vector NTI 4.0 (InforMax, Inc.) foram desenhados quatro pares de oligonucleotídeos iniciadores: dois para o gene da fosfoproteína (P1 e P2), um para a nucleoproteína (N1) e um para a hemaglutinina (H1). Além desses, foram selecionados dois pares de oligonucleotídeos (EXT e INT) que amplificam uma região homóloga do gene P dos Morbillivirus (Barret, 1987; Rzezutka e Mizak, 2002). Na Tab. 1 encontram-se as seqüências dos oligonucleotídeos utilizados para amplificar os genes de P, N e H.
Todo o material utilizado na extração de RNA total foi tratado com dietilpirocarbonato 0,1% (DEPC) por 12 horas e autoclavado. Para extração de RNA total utilizou-se Trizol® LS5 5 Schering-Plough Veterinária - Rio de Janeiro, Brasil , cujo protocolo de extração foi realizado conforme as instruções do fabricante. A concentração e a pureza do RNA total foram estimadas por espectrofotometria7 7 Ultrospec® II - LKB Biochrom, Cambridge, Inglaterra , de acordo com metodologia descrita por Sambrook et al. (1989).
Para a síntese do cDNA foram utilizados a enzima transcriptase reversa M-MLV8 8 Invitrogen Life Technology, Carlsbad, CA, EUA e inibidor de RNAse8 8 Invitrogen Life Technology, Carlsbad, CA, EUA , segundo as instruções do fabricante. Foi utilizado como branco, nessa etapa, RNA de CDV submetido às mesmas condições de transcrição reversa, com exceção da enzima M-MLV. As reações de amplificação foram realizadas em tubo com um volume final de 25µl com a seguinte composição: 2,5µl de cDNA, 14,7µl de água autoclavada (MILLI-Q), 1µl de albumina sérica bovina (0.8µg/µl), 1 mM de cada dNTP8 8 Invitrogen Life Technology, Carlsbad, CA, EUA (dATP, dTTP, dCTP, dGTP), MgCl2 2mM, tampão Taq 1x (200mM Tris-HCl pH 8,4, 500 mM KCl), 40nM de cada oligonucleotídeo senso e reverso e 1U da enzima Taq DNA Polimerase8 8 Invitrogen Life Technology, Carlsbad, CA, EUA . As reações foram efetuadas em termociclador Mastercycler Personal9 9 Eppendorf Scientific Inc. - Westbury, EUA com um total de 35 ciclos, sendo um minuto por etapa. Como controles positivos foram utilizadas as cepas vacinais e como controles negativos, tubo com cDNA de células MDCK não infectadas e tubo com todos os reagentes com exceção de cDNA.
Para visualização dos fragmentos de DNA foi realizada eletroforese em gel de agarose a 1% em tampão TBE pH 8.4 (TRIS 50 mM, ácido bórico 67mM, EDTA 1mM) corado com brometo de etídio (0,5µg/ml) e posterior visualização sob luz ultravioleta10 10 FGTI-88 Fisher Scientific - Atlanta, EUA . Utilizou-se marcador molecular de DNA ladder 1Kb8 8 Invitrogen Life Technology, Carlsbad, CA, EUA .
As condições ótimas de temperatura de pareamento, concentração de reagentes e de DNA para a RT-PCR foram testadas utilizando-se a amostra vacinal Lederle como controle. O teste de sensibilidade foi efetuado pelo emprego da amostra vacinal Lederle mediante quantificação do cDNA por espectrofotometria (Sambrook et al., 1989) e diluições posteriores (1:10) em água MILLI-Q. Para se testar a especificidade, além da amostra Lederle, foram incluídas amostras de outros vírus (SF-4, BHV-1, FLU, PAR) e da vacina tríplice SCR. As reações de amplificação foram efetuadas nas mesmas condições previamente descritas. Como controles negativos, foram incluídos tubo com cDNA de células MDCK não infectadas e tubo com todos os reagentes com exceção de cDNA. Para testar a reprodutibilidade da técnica foram feitas cinco reações de amplificação com o oligonucleotídeo P1, efetuadas pela mesma pessoa e no mesmo dia, pelo uso da amostra de cDNA (100ng/µl) obtida a partir da amostra Lederle.
Pela análise de seqüências do vírus da CC de canídeos, obtidas no GENE BANK (número de acesso AY386316), foi observado um mapa de restrição para cada um dos três pares de oligonucleotídeos e selecionadas as seguintes enzimas: para H1 foram utilizadas as enzimas EcoRI11 11 Promega-Madison, Wisconsin, EUA e EcoRV12 12 Pharmacia Biotech, Uppsala, Suécia ; para P1 as enzimas AvaI8 8 Invitrogen Life Technology, Carlsbad, CA, EUA e PvuII12 12 Pharmacia Biotech, Uppsala, Suécia e para o oligonucleotídeo N1 a enzima AvaI8 8 Invitrogen Life Technology, Carlsbad, CA, EUA e NcoI13 13 (New England Biolabs-Ipswich, MA, EUA) .
Após otimização da PCR, os amplicons dos oligonucleotídeos P1, N1 e H1 foram quantificados por espectofotometria e submetidos à clivagem pelas endonucleases de restrição, de acordo com as instruções dos fabricantes. O material foi incubado por uma hora a 37º C e os produtos clivados foram analisados por eletroforese em gel de agarose a 1%, em tampão TBE pH 8.4 (TRIS 50 mM, ácido bórico 67 mM, EDTA 1 mM), corado com brometo de etídeo (0,5µl/ml) e visualizado sob luz ultravioleta. Foram comparadas a amostra vacinal Lederle e as amostras SNC1, SNC2 e SNC3.
RESULTADOS E DISCUSSÃO
Inicialmente, todos os oligonuclotídeos H1, P1, P2 e N1 foram testados em temperaturas de pareamento que oscilaram de 46 a 58°C, com concentrações de MgCl2 variando de 1 a 3mM. Após os testes iniciais foram estabelecidas as temperaturas ótimas para cada par de oligonucleotídeos, como indicado na Tab. 1.
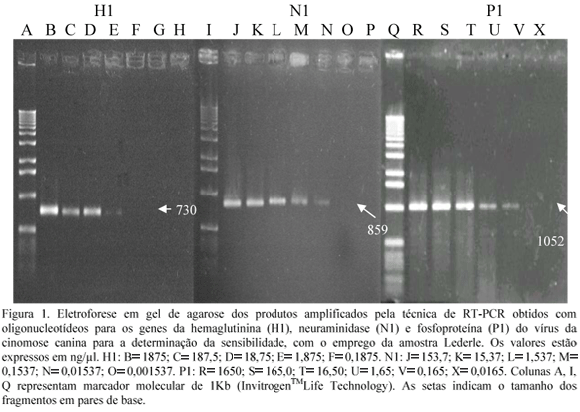
Utilizando-se a amostra vacinal Lederle como amostra padrão para RT-PCR, com os oligonucleotídeos P1, N1 e H1 visualizaram-se fragmentos de 1052, 859 e 730pb, respectivamente (Fig. 1). Resultados semelhantes foram obtidos quando foram testadas as amostras vacinais ROCK e SH (resultados não mostrados). Amplicons específicos para o gene NP do vírus da CC foram obtidos anteriormente (Shin et al., 1995; Frisk et al., 1999; Rzezutka e Mizak, 2002; Scagliarini et al., 2003). A PCR efetuada com o oligonucleotídeo P2 não apresentou fragmento amplificado de 771pb esperado, mesmo quando testado em diferentes temperaturas de pareamento sendo, por isso, descartado.
Em relação à sensibilidade da técnica de RT-PCR, os resultados foram melhores quando foram utilizados os oligonucleotídeos P1 e N1, que amplificaram fragmentos específicos até as concentrações de 16,5 e 15,3pg/µl de cDNA, respectivamente. Com o oligonucleotídeo H1 se obteve amplificação até 1,88ng/µl (Fig. 1). Utilizando um par de oligonucleotídeos para o gene P, Rzezutka e Mizak (2002) avaliaram a sensibilidade da RT-PCR com a cepa Onderstepoort e obtiveram um título de 1 DICT50. Experimentos que avaliaram a sensibilidade da técnica de RT-PCR para o vírus da CC revelaram que uma célula Vero infectada ou 200 cópias de cDNA são suficientes para obter produtos de amplificação (Shin et al., 1995). Estudo de Frisk et al. (1999) com oligonucleotídeos para o gene NP demonstrou a presença de amplicons específicos na RT-PCR em 86% de amostras séricas e 88% de amostras de fluido cefalorraquidiano coletados de cães com cinomose, salientando que a sensibilidade da reação era dependente dos oligonucleotídeos usados, além da possibilidade da influência de RNases endógenas e quantidade insuficiente de RNA viral utilizada. A menor sensibilidade do olignonucleotídeo H1 poderia ser explicada pelo fato de que, aparentemente, durante a infecção por Morbillivirus, ocorre um gradiente de produção de RNAm com concentrações descrescentes no sentido do gene N ao gene H (Harder e Osterhaus, 1997).
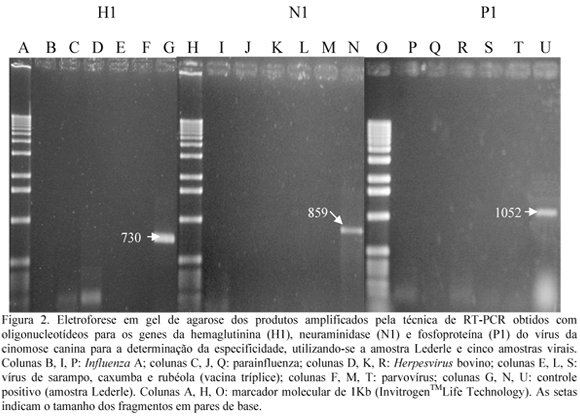
Na Fig. 2 são mostrados os resultados dos testes de especificidade da PCR com a utilização dos oligonucleotídeos P1, N1 e H1 diante da amostra vacinal Lederle, usada como controle positivo, e cinco amostras de outros vírus. Pode-se verificar a presença dos fragmentos específicos amplificados com os três oligonucleotídeos para a amostra Lederle, não havendo amplificação de fragmentos específicos para outros vírus testados, apesar de ter ocorrido amplificação inespecífica de um fragmento de aproximadamente 150pb com o oligonucleotídeo H1 em relação à cepa BHV-1. Nas condições utilizadas no presente trabalho, estes resultados evidenciam a especificidade dos oligonucleotídeos selecionados mesmo que dois pares (EXT e INT) amplifiquem uma região do gene P, homóloga entre os membros do grupo Morbillivirus. Estes resultados foram confirmados pela análise dos fragmentos de restrição obtidos após clivagem com endonucleases (Fig. 3 e 4). Gebara et al. (2004) utilizaram oligonucleotídeos desenhados a partir de seqüência do gene que codifica a nucleoproteína do CDV e avaliaram a especificidade da técnica após clivagem do fragmento amplificado de 287pb com a enzima Hinf I, que produziu dois fragmentos esperados de 227 e 60pb. Outros autores confirmaram a especificidade da técnica de RT-PCR para o gene NP (Frisk et al., 1999) e gene P (Rzezutka e Mizak, 2002) do CDV por Southern blot.
Nas condições testadas neste estudo, utilizando-se cDNA da amostra Lederle e oligonucleotídeos P1, a técnica de RT-PCR se mostrou reprodutível, sendo possível a visualização dos fragmentos com intensidade similar nos cinco testes realizados (resultados não mostrados).
Na Fig. 3 são mostrados os padrões de clivagem da amostra vacinal Lederle, obtidos com os oligonucleotídeos P1, N1 e H1 e as enzimas Eco RI, Eco RV, Ava I, Pvu II e Nco I. Verificou-se clivagem dos amplificados de DNA obtidos com os oligonucleotídeos P1 e N1, que originaram produtos com tamanho esperado, com exceção do segundo fragmento obtido com a enzima PvuII no amplicon P1, que foi maior do que o tamanho esperado de 480pb. No amplicon de H1 pode-se observar a clivagem com a enzima EcoRI, com obtenção dos fragmentos esperados de 550 e 180pb, respectivamente, sem ocorrer clivagem em relação à enzima EcoRV.
Com o padrão de restrição da amostra vacinal Lederle estabelecido, foram realizados experimentos similares com os isolados SNC1, SNC2, e SNC3. Na Fig. 4 são apresentados os resultados das análises de restrição dos amplicons P1, N1 e H1 do isolado SNC1 com diferentes enzimas. Houve similaridade entre os padrões dos três isolados analisados e o da amostra Lederle, com algumas diferenças no tamanho de alguns fragmentos que podem ser devidas a pequenas variações ocorridas durante a execução das técnicas.
Pequenas diferenças no tamanho dos fragmentos que foram observadas em relação ao amplicon H1 poderiam ser devidas à variabilidade do gene H que é responsável pelas características antigênicas do vírus; essa variabilidade tem sido utilizada na diferenciação de cepas de CDV (Carpenter et al., 1998; Mochizuki et al., 1999; Iwatsuki et al., 2000; Negrão et al., 2006). Por estar submetido à pressão do sistema imune do hospedeiro, o gene da hemaglutinina é o menos conservado dentre todos os genes do CDV (Hashimoto et al., 2001).
Em relação à enzima Eco RV, sua utilização em análises do gene da hemaglutinina é baseada no trabalho de Ohashi et al. (1998) que propõem o uso dessa enzima para diferenciar as amostras vacinais (mais antigas) das selvagens recentes. Nas vacinais não ocorre a clivagem enzimática. Amostras recentes, entretanto, isoladas do ambiente, possuem sítios de clivagem para essa enzima. Os autores propõem seu uso para rápida identificação molecular de amostras isoladas do ambiente. De acordo com esse critério, as amostras analisadas neste estudo seriam selvagens antigas, uma vez que para o amplicon H1 houve clivagem somente com a enzima Eco RI e não com Eco RV. A enzima Ssp I foi utilizada para diferenciar infecções causadas por amostras selvagens do vírus de CC das vacinais (Uema et al., 2005). Seria interessante realizar um estudo com maior número de amostras colhidas de animais de diferentes regiões do Brasil para se avaliar a utilidade dessas técnicas de RFLP na diferenciação das amostras do vírus da CC no País.
Após otimização da RT-PCR com a amostra vacinal Lederle, foram analisadas as amostras SNC1, SNC2 e SNC3, utilizando-se os oligonucleotídeos P1, N1 e H1. Foram observados fragmentos amplificados de 1052, 859 e 730pb, respectivamente, similares aos verificados com a amostra Lederle (resultados não mostrados), indicando que estas amostras são vírus da CC. Tais amostras já haviam sido identificadas por Gebara et al. (2004) como sendo vírus da CC, embora os autores tenham utilizado na RT-PCR oligonucleotídeos para a nucleoproteína do vírus da CC, cujo resultado foi um produto amplificado de 287pb.
As amostras provenientes de cães com sintomatologia sugestiva de CC (L1, L2, L3 e L4), após cultivo e produção de efeito citopatogênico em células MDCK, não apresentaram amplificação com os oligonucleotídeos P1, N1 e H1 ou mesmo com os oligonucleotídeos universais (EXT e INT) para Morbillivirus. Isto sugere que o quadro clínico apresentado pelos cães não foi causado por infecção com vírus da CC.
Embora a sensibilidade e a especificidade da RT-PCR sejam influenciadas pelo tipo de oligonucleotídeo selecionado, dentro das condições utilizadas neste estudo, os resultados mostraram que esta é uma técnica confiável para a detecção do vírus da CC.
Concluindo, a técnica de RT-PCR mostrou-se eficiente para a detecção do vírus da CC em amostras virais cultivadas em células MDCK. Apesar do pequeno número de amostras analisadas, a técnica de RFLP poderia ser útil na caracterização de amostras do vírus da CC.
AGRADECIMENTOS
Os autores agradecem ao CNPq e à CAPES pelo suporte financeiro e ao Dr. Amauri Alfieri, do Laboratório de virologia animal - Centro de Ciências Agrárias da Universidade Estadual de Londrina, Paraná) pelas amostras gentilmente cedidas. À Dra. Ana Paula Guedes Fração pela revisão do artigo.
Recebido em 9 de fevereiro de 2006
Aceito em 12 de setembro de 2007
- BARRET, T. The molecular biology of the Morbillivirus (measles) group. Biochem. Soc. Symp., v.53, p.25-37, 1987.
- BIAZONNO, L.; HAGIWARA, M.K.; CORRÊA, A.R. Avaliação da resposta imune humoral em cães jovens imunizados contra a cinomose com vacina de vírus atenuado. Braz. J. Vet. Res. Anim. Sci., v. 38, p. 245-250, 2001.
- CARPENTER, M.A.; APPEL, M.J.; ROELKE-PARKER, M.E. et al. Genetic characterization of canine distemper virus in Serengeti carnivores. Vet. Immunol. Immunopathol., v.65, p.259-266. 1998.
- DEEM, S.L.; SPELMAN, L.H.; YATES, R.A. et al. Canine distemper in terrestrial carnivores: a review. J. Zoo Wild. Med., v.31, p. 441-451, 2000.
- ELNIFRO, E.M.; ASHASHI, A.M.; COOPER, R.J. et al. Multiplex PCR: optimization and application in diagnostic virology. Clin. Microbiol. Rev, v.13, p.559-570, 2000.
- FRISK, A.L.; KÖNIG, M.; MORITZ, A. et al. Detection of canine distemper virus nucleoprotein RNA by reverse transcription-PCR using serum, whole blood and cerebrospinal fluid from dogs with distemper. J. Clin. Microbiol, v.7, p.3634-3643, 1999.
- GEBARA, C.M.S.; WOSIACKI, S.R.; NEGRÃO, F.J. et al. Lesões histológicas no sistema nervoso central de cães com encefalite e diagnóstico molecular da infecção pelo vírus da cinomose canina. Arq. Bras. Med. Vet. Zootec., v.56, p.168-174, 2004.
- HAAS, L.; LIERMANN, H.; HARDER, T.C. et al. Analysis of the H gene, the central untranslated region and the proximal coding part of the F gene of wild-type and vaccine canine distemper virus. Vet. Microbiol, v.69, p.15-18,1999.
- HARDER, T.C.; OSTERHAUS, A.D.M.E. Canine distemper virus a morbillivirus in search of new hosts? Trends Microbiol, v.5, p.120-124, 1997.
- HASHIMOTO, M.; UNE, Y.; MOCHIZUKI, H. Hemagglutinin genotype profiles of canine distemper virus from domestic dogs in Japan. Arch. Virol, v.146, p.149-155, 2001.
- HEADLEY, S.A.; GRAÇA, D.L. Canine distemper: epidemiological findings of 250 cases. Braz. J. Vet. Res. Anim. Sci, v.37, p.1413-1423, 2000.
- IWATSUKI, K.; TOKIYOSHI, S.; HIRAYAMA, N. et al. Antigenic differences in the H proteins of canine distemper virus. Vet. Microbiol., v.71, p.281-286, 2000.
- JOZWIK, A.; FRYMUS T. Natural distemper in vaccinated and unvaccinated dogs in Warsaw. J. Vet. Med., v.49, p.413-414, 2002.
- MOCHIZUKI, M.; HASHIMOTO, M.; HAGIWARA, S. et al. Genotypes of canine distemper virus determined by analysis of the hemagglutinin genes of recent isolates from dogs in Japan. J. Clin. Microbiol., v.37, p.2936-2942, 1999.
- MURPHY F.A.; GIBBS, E.P.; HORZINEK, M.C. et al. (Eds). Veterinary virology 3 ed. New York: Academic, 1999. 629p.
- NEGRÃO, F.J.; ALFIERI, A.A.; ALFIERI, A.F. Avaliação da urina e de leucócitos como amostras biológicas para a detecção ante mortem do vírus da cinomose canina por RT-PCR em cães naturalmente infectados. Arq. Bras. Med. Vet. Zootec., v.59, p. 253-257, 2007.
- NEGRÃO, F.J.; WOSIACKI, S.H.; ALFIERI, A.A. et al. Perfil de restrição de um fragmento do gene da hemaglutinina amplificado pela PCR-RT a partir de estirpes vacinais e selvagens do vírus da cinomose canina. Arq. Bras. Med. Vet. Zootec., v. 58, p. 1099-1106, 2006.
- OHASHI, K.; IWATSUKI, K.; NAKAMURA, K. et al. Molecular identification of a recent type of canine distemper virus in Japan by restriction fragment length polymorphism. J. Vet. Med. Sci., v.60, p.1209-1212, 1998.
- REED, L.J.; MÜENCH, H. A simple method of estimating fifty per cent end-points. Am. J. Hyg., v.27, p.493-7, 1938.
- RZEZUTKA, A.; MIZAK, B. Application of N-PCR for diagnosis of distemper in dogs and fur animals. Vet. Microbiol., v.88, p.95-103, 2002.
- SAMBROOK, J.; FRITSCH, E.F.; MANIATIS, T. (Eds). Molecular cloning: a laboratory manual. 2.ed. New York: Cold Spring Harbor Laboratory, 1989.
- SCAGLIARINI, A.; BATTILANI, M.; CIULLI, S. et al. Molecular analysis of the NP gene of Italian CDV isolates. Vet. Res. Commun., v.27, suppl. 1, p.355-357, 2003.
- SHIN, Y.J.; MORI, T.; OKITA, M. et al. Detection of canine distemper virus nucleocapsid protein gene in canine peripheral blood mononuclear cells by RT-PCR. J. Vet. Med. Sci., v.57, p.439-445, 1995.
- SHIN, Y.J.; CHO, K.O.; CHO, H.S. et al. Comparison of one-step RT-PCR and a nested PCR for the detection of canine distemper virus in clinical samples. Aust. Vet. J, v.82, p.83-86, 2004.
- UEMA, M.; OHASHI, K.; WAKASA, C. et al. Phylogenetic and restriction fragment length polymorphism analyses of hemagglutinin (H) protein of canine distemper virus isolates from domestic dogs in Japan. Vir. Res, v.109, p.59-63, 2005.
Datas de Publicação
-
Publicação nesta coleção
19 Dez 2007 -
Data do Fascículo
Out 2007
Histórico
-
Recebido
09 Fev 2006 -
Aceito
12 Nov 2007