Resumos
Dezessete bezerros foram utilizados para avaliar o efeito de ácidos graxos voláteis (AGV) sobre a morfologia ruminal, a epiderme do plano nasolabial, a epicera e o perioplum, e para validar a execução de biópsias tegumentares como indicadores de alterações da mucosa ruminal. Os animais receberam infusões intra-ruminal de butirato, propionato, lactato ou salina (controle) durante 37 dias. A insulina sorológica foi dosada no 22º dia experimental nos tempos de 0, 90, 180 e 360 minutos em relação à infusão diária da manhã. No 89º dia de vida, após o abate, foram coletados fragmentos ruminais e epidérmicos. Todos os AGV induziram aumento proporcionalmente maior no peso do ruminorretículo que no peso do omaso, sendo o butirato aparentemente mais estimulador da massa do estômago aglandular. Embora o butirato tenha sido mais estimulador da secreção de insulina, os AGV foram incapazes de induzir ganho nas dimensões papilares. Os AGV aumentaram a proliferação celular nos epitélios do rúmen e do perioplum traseiro, contrariamente ao efeito sobre o plano nasolabial e a epicera. Os efeitos dos AGV sobre a morfologia da mucosa ruminal e de outros tecidos queratinizados sugerem que danos morfológicos no rúmen e cascos podem ter causa comum. Biópsias tegumentares podem ter utilidade como indicadores de alterações morfológicas da mucosa ruminal.
bezerro; ácidos graxos voláteis; plano nasolabial; epicera; perioplum
The effect of butyrate, propionate, and lactate on ruminal wall, epidermis of nasolabial surface, perioplum, and epicera of 17 neonatal calves was evaluated. The experiment also aimed to validate the procedure and interpretation of tegument biopsies as indicators of ruminal mucosa alterations. Serum insulin was sampled on the 22nd day from the beginning of treatments, at 0, 90, 180, and 360 minutes after the morning infusion. After slaughtering, samples were collected from ruminal wall, nasolabial surface, epicera, and perioplum from face and hindquarters. All volatile fatty acids (VFA) induced greater increase in ruminal-reticulum proportionate weight than in omasum. Butyrate was a greater stimulator of non-glandular stomach growth. Although butyrate stimulated more insulin secretion, this VFA was not capable to induced gain on papillae area or height. The effect of nasolabial surface VFA infusion was the opposite to that observed in the rumen. VFA increased hind perioplum mitotic index, contrary to its effect on the nasolabial surface and epicera. VFA effects on ruminal mucosa morphology and on other keratinized tissues suggest that morphological damage on hoof and ruminal epithelium may have a common cause. Tegumentary biopsies may be useful as indicators of morphological alterations of ruminal mucosa.
calf; volatile fatty acids; nasolabial surface; epicera; perioplum
MEDICINA VETERINÁRIA
Alterações morfológicas induzidas por butirato, propionato e lactato sobre a mucosa ruminal e a epiderme de bezerros I Aspectos histológicos
Lactate, propionate and, butyrate induced morphological alterations on calf ruminal mucosa and epidermis - I Histologycals aspects
S.F. Costa; M.N. Pereira; L.Q. Melo; J.C. Resende Júnior; M.L. Chaves
Universidade Federal de Lavras, Caixa Postal 3037, 37200-000 - Lavras, MG
RESUMO
Dezessete bezerros foram utilizados para avaliar o efeito de ácidos graxos voláteis (AGV) sobre a morfologia ruminal, a epiderme do plano nasolabial, a epicera e o perioplum, e para validar a execução de biópsias tegumentares como indicadores de alterações da mucosa ruminal. Os animais receberam infusões intra-ruminal de butirato, propionato, lactato ou salina (controle) durante 37 dias. A insulina sorológica foi dosada no 22º dia experimental nos tempos de 0, 90, 180 e 360 minutos em relação à infusão diária da manhã. No 89º dia de vida, após o abate, foram coletados fragmentos ruminais e epidérmicos. Todos os AGV induziram aumento proporcionalmente maior no peso do ruminorretículo que no peso do omaso, sendo o butirato aparentemente mais estimulador da massa do estômago aglandular. Embora o butirato tenha sido mais estimulador da secreção de insulina, os AGV foram incapazes de induzir ganho nas dimensões papilares. Os AGV aumentaram a proliferação celular nos epitélios do rúmen e do perioplum traseiro, contrariamente ao efeito sobre o plano nasolabial e a epicera. Os efeitos dos AGV sobre a morfologia da mucosa ruminal e de outros tecidos queratinizados sugerem que danos morfológicos no rúmen e cascos podem ter causa comum. Biópsias tegumentares podem ter utilidade como indicadores de alterações morfológicas da mucosa ruminal.
Palavras-chave: bezerro, ácidos graxos voláteis, plano nasolabial, epicera, perioplum
ABSTRACT
The effect of butyrate, propionate, and lactate on ruminal wall, epidermis of nasolabial surface, perioplum, and epicera of 17 neonatal calves was evaluated. The experiment also aimed to validate the procedure and interpretation of tegument biopsies as indicators of ruminal mucosa alterations. Serum insulin was sampled on the 22nd day from the beginning of treatments, at 0, 90, 180, and 360 minutes after the morning infusion. After slaughtering, samples were collected from ruminal wall, nasolabial surface, epicera, and perioplum from face and hindquarters. All volatile fatty acids (VFA) induced greater increase in ruminal-reticulum proportionate weight than in omasum. Butyrate was a greater stimulator of non-glandular stomach growth. Although butyrate stimulated more insulin secretion, this VFA was not capable to induced gain on papillae area or height. The effect of nasolabial surface VFA infusion was the opposite to that observed in the rumen. VFA increased hind perioplum mitotic index, contrary to its effect on the nasolabial surface and epicera. VFA effects on ruminal mucosa morphology and on other keratinized tissues suggest that morphological damage on hoof and ruminal epithelium may have a common cause. Tegumentary biopsies may be useful as indicators of morphological alterations of ruminal mucosa.
Keywords: calf, volatile fatty acids, nasolabial surface, epicera, perioplum
INTRODUÇÃO
A fermentação microbiana e a produção de ácidos graxos voláteis (AGV) no rúmen são eventos nutricionalmente importantes em ruminantes, uma vez que aproximadamente 70% das exigências energéticas nesses animais podem ser atendidas por acetato, propionato e butirato (Bergman, 1990). A ingestão de dietas ricas em carboidratos rapidamente fermentáveis no rúmen pode resultar em acúmulo excessivo de AGV no fluido ruminal, desencadeando um quadro de acidose (Barker et al., 1995; Bernardes et al., 2007). O estímulo da capacidade de clearance de AGV pela parede do rúmen por manipulação dietética da morfologia papilar (Gaebel et al., 1987) pode ser uma estratégia alimentar plausível em vacas leiteiras, propiciando alta absorção de energia sem induzir acúmulo excessivo de AGV no fluido ruminal.
O tipo de AGV presente no conteúdo ruminal pode afetar a resposta em crescimento das células do epitélio. O propionato e o butirato parecem ser mais estimuladores do crescimento papilar que o acetato (Vair et al., 1960). A alta produção ruminal de butirato, no entanto, parece ser indesejável do ponto de vista de integridade e atividade metabólica da parede ruminal em razão dos efeitos diretos indesejáveis desse ácido sobre a proliferação e a queratinização das células epiteliais (Gálfi et al., 1993). O papel dos AGV na etiopatogenia da acidose em vacas leiteiras precisa ser mais bem esclarecido para que medidas de controle tecnicamente fundamentadas sejam adotadas.
Alterações microscópicas no processo de queratinização observadas em bovinos com distúrbios nos membros locomotores (Andersson e Bergman, 1980; Singh et al., 1992) podem atuar como fator predisponente ao aparecimento de afecções de casco (Hendry et al., 1999). Danos morfológicos no tecido epitelial do rúmen e dos cascos podem ter os AGV como causa comum, possivelmente explicando a ocorrência simultânea de anomalias no rúmen e nos cascos de bovinos sujeitos à acidose ruminal.
O objetivo deste trabalho foi avaliar o efeito de AGV sobre a morfologia da mucosa ruminal, da epiderme no plano nasolabial, da epicera e do perioplum de bezerros, visando fornecer subsídios para melhor compreensão da etiopatogenia da acidose em bovinos e validar a execução e a interpretação de biópsias tegumentares como indicadores de alterações morfológicas da mucosa ruminal.
MATERIAL E MÉTODOS
Foram utilizados 17 bezerros da raça Holandesa, alimentados diariamente com quatro litros de leite integral fornecidos em duas alimentações às 7 e 19 horas, com acesso contínuo à água. Os animais não tiveram acesso a alimento sólido, visando inibir o desenvolvimento mecanicamente estimulável do estômago aglandular. Assumiu-se que qualquer alteração morfológica observada no rúmen foi decorrente dos tratamentos.
Aos 45 dias de vida, todos os animais foram submetidos à implantação cirúrgica de sonda de gastrostomia1 1 Ross Flexiflo 20 French, Abbot Laboratórios do Brasil Ltda. - São Paulo, Brasil. humana no rúmen. Aos 52 dias de idade, os animais foram aleatoriamente alocados em um dos quatro tratamentos, por 37 dias: infusões intra-ruminal de butirato (B), lactato (L), propionato (P) ou salina (S), este último usado como controle.
Uma hora após o aleitamento da manhã, os animais receberam diariamente infusões intra-ruminal com 500ml de salina (cloreto de sódio 0,9%) ou o mesmo volume de soluções contendo propionato (ácido propiônico 99%)2 2 Farmalabor Comercial Ltda. - São Paulo, Brasil. , lactato (ácido lático 85%)2 2 Farmalabor Comercial Ltda. - São Paulo, Brasil. ou butirato (ácido butírico 99%). Uma hora após o aleitamento da tarde, o mesmo volume de solução foi novamente infundido em todos os animais. O pH das soluções foi ajustado para 6,1 com hidróxido de sódio3 3 Hidróxido de Sódio PA Chemo, Alquimia Comércio de Materiais para Laboratórios Ltda. Campinas, Brasil. . A quantidade diária infundida de propionato e butirato foi 0,0744 moles/kg de peso metabólico (peso vivo0,75), e a quantidade de lactato foi 0,0639 moles/kg de peso metabólico. A cada três dias, os animais foram pesados, e a quantidade infundida foi ajustada para a variação no peso vivo.
Para a dosagem de insulina sorológica, amostras sangüíneas da veia jugular externa foram obtidas no 22º dia de aplicação dos tratamentos nos tempos 0, 90, 180 e 360 minutos relativamente à infusão diária da manhã. Utilizou-se a técnica de radioimunoensaio em fase sólida pelo procedimento do kit para análise de insulina Coat-A Count4 4 DPC Medlab Produtos Médico-Hospitalares Ltda. - São Paulo, Brasil. modificado (Vaughn et al., 1993). As mensurações foram feitas em um contador de raios gama5 5 Gamma Cord Brand-AMES - São Paulo, Brasil. .
Aos 89 dias de vida, uma hora após a primeira infusão, os animais foram pesados, sacrificados in extremis, eviscerados, e os compartimentos do estômago isolados. Após limpeza e remoção do excesso de tecido conjuntivo circundante, os órgãos foram abertos, esvaziados, lavados em água corrente e pesados em balança de precisão.
Avaliaram-se: pesos do ruminorretículo, do omaso e do abomaso; peso da mucosa e do restante da parede ruminal; número de papilas por cm2 de mucosa ruminal; altura e área das papilas ruminais; índice mitótico (IM) das células da camada basal nos epitélios queratinizados do rúmen, do plano nasolabial, da epicera e do perioplum e características histológicas.
Amostras de aproximadamente 3cm2 foram obtidas da parede do recesso e do saco cranial do rúmen e mantidas em solução de tampão fosfato 0,1M, pH 7,4. O número de papilas por cm2 de mucosa ruminal foi avaliado em três áreas aleatórias delimitadas por um marcador de metal com área de 1cm2, com lupa estereoscópica em aumento de 6X. O peso da mucosa e dos demais tecidos da parede ruminal foi determinado em fragmentos circulares com 1cm de diâmetro.
Para a avaliação histológica das papilas, foram coletados fragmentos da parede do saco cranial, do recesso e do saco cego caudo-ventral do rúmen e fixados por 12 horas em líquido de Bouin (Luna, 1968). Foram também obtidos fragmentos da epiderme do plano nasolabial, da epicera direita, do perioplum do terceiro dedo do membro dianteiro direito e do quarto dedo do membro traseiro direito, que foram fixados em formalina por 24 horas e mantidos em álcool etílico a 70ºGL até serem processados. Todo o material fixado foi processado rotineiramente e incluído em parafina histológica. Os blocos de parafina foram seccionados em micrótomo manual6 6 Micrótomo Rotativo 781, Ancap Equipamentos Eletro-Eletrônicos Ltda. - São Paulo - Brasil. , obtendo-se secções de sete micrômetros de espessura.
Para a análise morfométrica das papilas ruminais e a determinação do IM das células da camada basal dos epitélios do rúmen, do plano nasolabial, da epicera e do perioplum, as lâminas foram coradas com Hematoxilina-Eosina (HE), segundo Luna (1968). A altura e a área das papilas ruminais foram mensuradas com o software KS300 contido em um analisador de imagens7 7 Kontron Elektronic/Carl Zeiss, Carl Zeiss do Brasil - São Paulo, Brasil. de acordo com Caliari (1997).
Para a determinação do IM, utilizou-se microscópio de luz8 8 Jenamed-Carl Zeiss Jena, Carl Zeiss do Brasil - São Paulo - Brasil. , em aumento de 400X. Foram contados todos os núcleos das células da camada basal do epitélio e todas as células com núcleo apresentando figuras mitóticas. O IM foi calculado dividindo-se o número de núcleos com figuras mitóticas pelo total de núcleos contados. O exame histológico constou de uma avaliação de todo corte histológico presente na lâmina de cada animal por tratamento nas diferentes regiões do rúmen.
Os dados morfológicos foram analisados pelo procedimento GLM do pacote estatístico SAS (Users..., 1985), e a concentração de insulina sorológica ao longo do tempo, analisada pelo procedimento MIXED do pacote estatístico SAS (Littell et al., 1996). Em todas as análises, foram testados três contrastes ortogonais com um grau de liberdade: butirato versus salina, lactato versus salina e propionato versus salina.
RESULTADOS E DISCUSSÃO
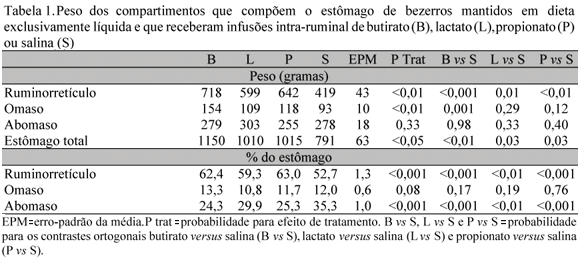
Todos os AGV induziram aumento proporcionalmente maior no peso do ruminorretículo que no peso do omaso, sendo butirato aparentemente mais estimulador da massa do estômago aglandular que propionato e lactato (Tab. 1). Nesses animais, as infusões de AGV induziram uma relação intermediária entre os pesos do ruminorretículo e os pesos do omaso e do abomaso, comparativamente à observada para bezerros abatidos com 30 ou 60 dias de idade e que tiveram acesso contínuo e irrestrito a alimentos concentrados do nascimento à desmama aos 30 dias (Coelho, 1999). O aumento no peso do estômago aglandular não foi dependente do trabalho mecânico de digestão, desde que os animais foram mantidos em dieta líquida durante todo o período experimental. O efeito positivo da ingestão de alimentos sólidos sobre o crescimento ruminal de bezerros (Warner, 1991) pode ser mais dependente dos produtos finais da fermentação e de outros fatores humorais que do estímulo à motilidade do órgão.
Propionato e butirato induziram aumento na massa do omaso em relação ao tratamento-controle (Tab. 1). O fato de muito pouco AGV chegar ao abomaso (Barcroft et al., 1944) e de não ter sido observado efeito de tratamento sobre a massa do estômago glandular possivelmente indica que a resposta em peso estomacal ocorreu apenas em compartimentos do órgão onde houve absorção de AGV. Pode ser que a absorção e a metabolização de AGV pela parede do omaso tenham sido tão participativa no metabolismo dos AGV produzidos no rúmen quanto o metabolismo pelo epitélio ruminal, desde que cerca de 50% do clearance dos AGV produzidos no ruminorretículo de ruminantes adultos ocorre por passagem com a fase fluida ruminal (Resende Júnior, 2006).
Embora os AGV tenham aumentado a massa de mucosa ruminal (Tab. 2), eles reduziram o número de papilas por cm2 de parede ruminal (Tab. 3). O crescimento papilar induzido por propionato foi semelhante ao observado para bezerros com acesso irrestrito a alimentos sólidos por 30 dias após a desmama (Coelho, 1999). O manejo alimentar e a freqüência de infusões adotados neste experimento podem ter determinado o pequeno tamanho papilar proporcionalmente à idade dos animais.
A infusão de butirato teve efeito significativo sobre a mucosa do saco cranial, enquanto os outros AGV aumentaram apenas numericamente a massa de mucosa ruminal. Considerando que a média na proporção de mucosa nos dois fragmentos ruminais seja representativa da porcentagem de mucosa na parede do rúmen, foi estimado que a massa da mucosa ruminal, calculada por multiplicação da porcentagem de mucosa (Tab. 2) pelo peso do rúmen (Tab. 1), foi três vezes maior que a do controle no tratamento B e duas vezes maior nos tratamentos L e P. Assumindo que a massa da mucosa ruminal reflita, em parte, a área total da parede, desde que a porcentagem da mucosa na parede ruminal tenha sido pouco diferente entre tratamentos (Tab. 2), o número total de papilas ruminais seria maior nos animais que receberam infusões de AGV que nos animais que receberam salina. O número de papilas por cm2 foi cerca de 1,5 vez maior no tratamento S que nos tratamentos com AGV; no entanto, a massa da mucosa ruminal foi de duas a três vezes menor nesse tratamento. O maior número de papilas por cm2 no tratamento S pode ter sido resultado da concentração de papilas em uma menor área da parede ruminal. Julgando por esse parâmetro, os AGV foram estimuladores do desenvolvimento papilar.
A infusão de butirato, apesar de ter resultado em aumento no número calculado de papilas ruminais, foi incapaz de induzir ganho em área ou altura das papilas (Tab. 3). O propionato, além de ter sido menos inibidor do número de papilas por cm2 que butirato e lactato, também tendeu a aumentar o tamanho papilar no saco cranial do rúmen. Os efeitos inibitórios de butirato e estimulatórios de propionato sobre o desenvolvimento papilar são semelhantes a observações in vitro (Gálfi et al., 1993), sugerindo que a ação direta dos AGV sobre as células epiteliais pode ter predominado sobre mecanismos humorais. O fato de maiores concentrações plasmáticas de insulina no tratamento com butirato terem sido acompanhadas por menor tamanho papilar, o oposto do observado para propionato (Fig. 1), também suporta tal suposição. A insulina é sabidamente estimuladora do desenvolvimento papilar (Sakata et al., 1980; Gálfi et al., 1993).
Todos os AGV induziram aumento na proliferação das células da camada basal do epitélio do rúmen (Fig. 2 e Tab. 4). Entretanto, maior proliferação celular não se refletiu em maior tamanho papilar (Tab. 3). A freqüência de lesões histológicas foi acentuada nos tratamentos L e B. A resposta em mitose celular à infusão de lactato e butirato pode ter ocorrido devido a uma ruminite induzida por AGV, conforme observado por Hamada (1975). As lesões histológicas causadas por propionato foram moderadas. A resposta em tamanho papilar foi inversamente proporcional à freqüência de lesões no epitélio e não foi correlacionada ao IM.
O efeito dos AGV sobre o IM na epicera foi semelhante ao efeito observado no plano nasolabial (Fig. 2 e Tab. 4). Butirato e lactato foram inibidores de mitose. Contrariamente, os AGV aumentaram o IM no perioplum traseiro dos cascos (Tab. 4). O efeito dos AGV sobre o perioplum dianteiro foi não significativo (Tab. 4). Esse achado merece consideração, pois a incidência de problemas nos locomotores de bovinos é prevalente nos membros posteriores (Weaver et al., 1981; Tranter e Morris, 1991), mais responsivos, neste trabalho, à infusão intra-ruminal de AGV. Distúrbios de queratinização podem atuar como fator predisponente de problemas de casco por atuar sobre a morfologia e a dureza dos cascos bovinos (Budras et al., 1996; Hendry et al., 1999).
Sugere-se que a biópsia tegumentar pode ser utilizada para detectar efeitos de AGV sobre o epitélio estratificado do rúmen. Essas técnicas são menos invasivas que o acesso cirúrgico ao rúmen de animais canulados. Julgando-se pela similaridade na resposta, aparentemente o perioplum traseiro tem potencial como representante da resposta ruminal em IM. No entanto, como indicador de integridade do epitélio ruminal, biópsias na epicera podem ser interessantes, julgando-se pela similaridade em IM entre os tratamentos P e S e o menor IM nos tratamentos B e L, estes últimos também causadores de danos histopatológicos na parede ruminal. Apesar de não ter sido detectado efeito significativo de tratamento sobre o IM no plano nasolabial, a similaridade numérica entre a resposta nesse tecido e a resposta na epicera torna biópsias no focinho promissoras tanto pela facilidade de execução, quanto pelo fato de biópsias na epicera não serem executáveis em bovinos leiteiros descornados. A interpretação de tais biópsias como representante de eventos ruminais requer validações futuras.
Suter et al. (1997) citam que baixas concentrações de ácido retinóico (10-7 a 10-10 M) podem ser estimulatórias da proliferação celular em células epiteliais humanas, enquanto altas concentrações (10-6 M) podem ser inibitórias em camundongos, mostrando que a resposta de epitélios estratificados a moduladores de divisão celular pode ser inversa e dependente da espécie e da concentração sorológica. A infusão de uma mistura de AGV no cólon proximal de ratos anestesiados estimulou o IM nesse local e em locais proximais do trato digestivo sem contato direto com a solução de AGV infundida. Entretanto, não foi detectado efeito dos AGV sobre o IM nas regiões do duodeno, ceco, cólon distal e epiderme da orelha desses animais (Sakata e Engelhardt, 1983), sugerindo que a estimulação mitótica dos AGV pode estar restrita a certos tecidos.
Nos quatro animais infundidos com salina, a mucosa ruminal estava íntegra e com papilas de contorno regular. Nenhuma área avaliada dos epitélios do rúmen de animais que receberam infusões de AGV foi considerada normal, devido à presença de lesões celulares, as quais sugeriram processos degenerativos. O epitélio nas diferentes regiões do rúmen dos animais que receberam propionato apresentou lesões leves ou moderadas. Em todos os animais que receberam infusões intra-ruminais de lactato, foram observadas papilas bem ramificadas e com desproporção entre as camadas celulares, comparado ao tratamento S. Em dois dos quatro animais infundidos com butirato, o epitélio no recesso e no saco cego caudo-ventral do rúmen apresentou desproporção entre as camadas celulares, grandes vacúolos intracitoplasmáticos, infiltrado inflamatório polimorfonuclear e áreas de erosão. Observaram-se grandes áreas preenchidas por material amorfoeosinofílico com desarranjo na arquitetura epitelial.
CONCLUSÕES
O crescimento anatômico do estômago aglandular foi induzido pela presença de AGV, sem a necessidade de trabalho mecânico de digestão. O propionato foi o AGV, responsável pelo crescimento fisiológico de papilas metabolicamente ativas. Os efeitos direto e indireto dos AGV sobre a morfologia da mucosa ruminal e de outros tecidos queratinizados sugerem que danos morfológicos no epitélio do rúmen e de cascos podem ter causa comum, explicando a ocorrência simultânea de anomalias nessas estruturas em bovinos sujeitos à acidose ruminal. Biópsias tegumentares podem ter utilidade como indicadores morfológicos da mucosa do rúmen.
AGRADECIMENTOS
Os autores agradecem àFAPEMIG (CAG 1269-97) e ao CNPq pelo apoio financeiro.
Recebido em 3 de maio de 2007
Aceito em 28 de dezembro de 2007
E-mail: sfcosta@ufla.br
- ANDERSSON, L.; BERGMAN, A. Pathology of bovine laminitis especially as regards vascular lesions. Acta Vet. Scand., v.21, p.559-566, 1980.
- BARCROFT, J.; MCNALLY, R.A.; PHILLIPSON, A.T. Absorption of volatile acids from the alimentary tract of the sheep and others animals. J. Exp. Biol., v.20, p.120-129, 1944.
- BARKER, I.K.; VAN DREUMEL, A.A.; PALMER, N. The alimentary system. In: JUBB, K.V.F.; KENNEDY, P.C.; PALMER, N. (Eds). Pathology of Domestic Animals 4. ed. San Diego: Academic, 1995. v.2.
- BERGMAN, E.N. Energy contribution of volatile fatty acids from the gastrointestinal tract in various species. Physiol. Rev., v.70, p.567-590, 1990.
- BERNARDES, E.B.; COELHO, S.G.; CARVALHO, A.V. et al. Efeito da substituição do feno de Tifton 85 pelo caroço de algodão como fonte de fibra na dieta de bezerros. Arq. Bras. Med. Vet. Zootec., v.59, p.955-964, 2007.
- BUDRAS, K.D.; MÜLLING, C.H.; HOROWITZ, A. Rate of keratinization of the wall segment of the hoof and its relation to width and structure of the zone alba (white line) with respect to claw disease in cattle. Am. J. Vet. Res., v.57, p.444-455, 1996.
- CALIARI, M.V. (Ed). Princípios de morfometria digital: KS300 para iniciantes Belo Horizonte: UFMG, 1997. 149p.
- COELHO, S.G. Ganho de peso e desenvolvimento do estômago de bezerros desaleitados aos trinta dias de idade e alimentados com concentrado e com ou sem feno. 1999. 123f. Tese (Doutorado) Escola de Veterinária, Universidade Federal de Minas Gerais, Belo Horizonte, MG.
- GAEBEL, G.; MARTENS, H.; SUENDERMANN, M. et al. The effects of diet intra-ruminal pH and osmolarity on sodium, chloride and magnesium absorption from the temporarily isolated and washed reticule-rumen of sheep. Q. J. L. Exp. Physiol., v.72, p.501-511, 1987.
- GÁLFI, P.; GABEL, G.; MARTENS, H. Influence of intracellular matriz components on the growth and differentiation of ruminal epithelial cells in primary culture. Res. Vet. Sci., v.54, p.102-109, 1993.
- HENDRY, K.A.K.; MacCALLUM, A.J.; KNIGHT, C.H. et al. Effect of endocrine and paracrine factors on protein synthesis and cell proliferation in bovine hoof tissue culture. J. Dairy Sci., v.66, p.23-33, 1999.
- LITTELL, R. C.; MILLIKEN, G. A.; STROUP, W.W. et al. SAS system for mixed models Cary, NC: SAS Institute, 1996. 633p.
- LUNA, L.G. (Ed). Manual of histology staining methods of the Armed Forces Institute Pathology. 3.ed. New York: McGraw Hill, 1968. 258p.
- RESENDE JÚNIOR, J.C.; PEREIRA, M.N.; BOHER, H. et al. Comparison of techniques to determine the clearance of ruminal volatile fatty acids. J. Dairy Sci., v.89, p.3096-3106, 2006.
- SAKATA, T.; ENGELHARDT, W. V. Stimulatory effect of short chain fatty acids on the epithelial cell proliferation in rat large intestine. Comp. Biochem. Physiol., v.74, p.459-462, 1983.
- SAKATA, T.; HIKOSAKA, K.; SHIOMURA, Y. et al. Stimulatory effect of insulin on ruminal epithelium cell mitosis in adult sheep. Br. J. Nutr., v.44, p.325, 1980.
- SINGH, S.S.; MURRAY, R.D.; WARD, W.D. Histopathological and morphometric studies on the hooves of dairy and beef cattle in relation to overgrown sole and laminitis. J. Comp. Pathol., v.107, p.319-328, 1992.
- SUTER, M.M.; CRAMERI, F.M.; OLIVRY, T. et al. Review article. Keratinocyte biology and pathology. Vet. Dermatol., v.8, p.67-100, 1997.
- TRANTER, W.P.; MORRIS, R.S. A case study of lameness in three dairy herds. N. Z. Vet. J., v.39, p.88-96, 1991.
- USERS guide: statistics 5.ed. Cary. SAS Institute, 1985. 1290p.
- VAIR, C.; WARD, G.M.; FRANDSON, R.D. et al. Influence of sodium salts of volatile fatty acids on rumen development in the young calf. J. Dairy Sci., v.43, p.890, 1960.
- VAUGHN, A.S.; GRUMMER, R.R.; BERTICS, S.J. Effect of prepartum propylene glycol administration on periparturient fatty liver in dairy cows J. Dairy Sci., v.76, p.2931-2932, 1993.
- WARNER, R. G. Nutritional factors affecting the development of a functional ruminant - A historical perspective. In: CORNELL CONFERENCE FOR FEED MANUFACTURERS, 1991, Rochester. Proceedings.. Ithaca: Cornell University, 1991. p.1-13.
- WEAVER, A.D.; ANDERSSON, L.; DE LAISTRE BANTING, A. et al. Review of disorders of the ruminant digit with proposals for anatomical and pathological terminology and recording. Vet. Rec., v.108, p.1-17, 1981.
Datas de Publicação
-
Publicação nesta coleção
05 Maio 2008 -
Data do Fascículo
Fev 2008
Histórico
-
Aceito
28 Dez 2007 -
Recebido
03 Maio 2007